一种双pH敏感美沙拉嗪结肠靶向缓释固体分散体及其制备方法与流程
本发明属于药物制剂领域,具体涉及美沙拉嗪结肠靶向缓释固体分散体及其制备方法。
背景技术:
溃疡性结肠炎(uc)是一种慢性肠道疾病,发病于结肠黏膜,以腹泻、腹痛、黏液脓血便为主要症状,病程易于反复、迁延不愈。uc的病因尚不明确,目前认为其为环境、遗传、免疫系统、吸烟、精神等因素综合作用的结果。uc患者发生结直肠癌风险高出正常人2-5倍。
5-氨基水杨酸(5-asa)也称美沙拉嗪,是目前缓解轻、中度uc的一线药物,应用广泛。其通过抑制引起炎症的前列腺素合成和炎症介质白三烯的形成,从而达到对肠壁炎症有显著的消炎作用。5-asa最常见的给药途径为灌肠,但大部分患者无法接受,因此口服制剂的研发非常有必要。但5-asa口服存在小肠上段吸收迅速、结肠浓度低、释药过早导致不良反应等问题。
结肠靶向给药系统(ocdds)指药物经口服后,避免在上消化道释放,而将药剂运送到人体回盲肠区才开始崩解和释放出药物,且在一定时间内黏附于结肠黏膜表面,以一定速度释放药物,从而达到提高药物局部浓度和生物效性的目的。
多糖是由单糖或低聚糖聚合而成的大分子聚合物,来源广泛、稳定无毒、生物相容性好,并在结肠中被大量微生物产生的酶特异性降解,而在胃和小肠中不降解,这一原理使其作为ocdds载体成为可能,然而天然多糖疏水性差,水中易溶胀腐蚀,导致药物提前释放,故常与其他材料配合使用或通过化学修饰降低亲水性后再被应用,以达到更好的结肠定位效果。
壳聚糖是由甲壳素去乙酰化后得到的一种聚阳离子多糖,具有无毒、生物相容性和黏附性好、易被结肠菌群降解的优点。然而壳聚糖易溶于酸,会降低剂型在胃内的完整性,制约了其在ocdds中的应用。
海藻酸盐是一种聚阴离子多糖,由β-d-甘露糖酸和α-l-古罗糖醛酸按一定比例通过1,4-糖苷键连接而成,其自身不能形成凝胶,但分子骨架上的古罗糖醛酸可进行修饰形成网状结构,从而作为载体递送材料。
ph敏感性材料主要有三种,聚阳离子型、聚阴离子型和两性离子型水凝胶。其中聚阳离子型在酸性溶液中,溶胀效率增强。聚阴离子型在溶液为碱性时,溶胀率增加。两性离子水凝胶主要含有酸碱基团,当ph改变时,这两种基团会产生不同的离子化作用。当溶液为碱性时-cooh会离子化,氨基会质子化,当溶液为酸性时。-cooh会质子化,氨基会离子化,而在溶液接近中性的时候,其溶胀率就会降低,从而达到双ph敏感的目的。
目前主要的美沙拉嗪制剂是通过聚乙二醇等粘合剂且在乙醇-水混合溶液中进行对美沙拉嗪的包合(专利号:cn108159012a),存在粘合剂毒性较大、制剂工艺复杂(专利号:cn109310642a)、重现性差等缺点。
技术实现要素:
本发明要解决的技术问题之一是提供了一种双ph敏感美沙拉嗪结肠靶向缓释固体分散体。本发明要解决的技术问题之二是提供了一种双ph敏感美沙拉嗪结肠靶向缓释固体分散体的机械化学制备方法。为了解决上述技术问题,本发明采用如下技术方案:
在本发明的第一方面,提供了一种双ph敏感美沙拉嗪结肠靶向缓释固体分散体,以壳聚糖或聚赖氨酸为聚阳离子型辅料,以海藻酸钠、海藻酸或聚谷氨酸为聚阴离子型辅料,以5-氨基水杨酸为活性成分,所述的聚阳离子型辅料、聚阴离子型辅料及活性成分的质量比为1~2:1~2:1~2。
作为本发明的优选技术方案,所述的聚阳离子型辅料、聚阴离子型辅料及活性成分的质量比为1:1:1。
作为本发明的优选技术方案,采用固相下借助阴阳离子氢键结合作用,避免了交联剂/粘合剂的使用。
作为本发明的优选技术方案,所述的美沙拉嗪固体分散体在模拟胃液中1小时释放3.07%~12.28%,2小时释放12.28%~18.94%,溶出采用中国药典装置2桨法75r进行。
作为本发明的优选技术方案,所述的美沙拉嗪固体分散体在模拟肠液中1小时释放5.42%~21.54%,2小时释放21.54%~28.85%,4小时释放28.85%~49.23%,6小时释放大于62.72%,溶出采用中国药典装置2桨法75r进行。
此外,本发明还提供了一种双ph敏感美沙拉嗪结肠靶向缓释固体分散体的制备方法,包括如下步骤:
(1)将聚阳离子型辅料和聚阳离子型辅料按质量比球磨混合,备用;
(2)将球磨后的辅料与5-氨基水杨酸按质量比混合,得到双ph敏感美沙拉嗪结肠靶向缓释固体分散体。
进一步,步骤(1)中,所述的球磨转速优选为30r/min,球磨时间为2h。
进一步,步骤(2)中,所述的球磨转速优选为30r/min,球磨时间优选为4h。
与现有技术相比,本发明的有益效果在于:本发明所制备的双ph敏感美沙拉嗪结肠靶向缓释制剂有固相交联,它具有胃肠道吸收少,保持病变结肠段有效药物浓度的特点,药物释放持续/稳定且安全的特点。本发明采用的机械化学制备方法,制备工艺简单,便于操作,重现性好,并有效降低了制造成本。
附图说明
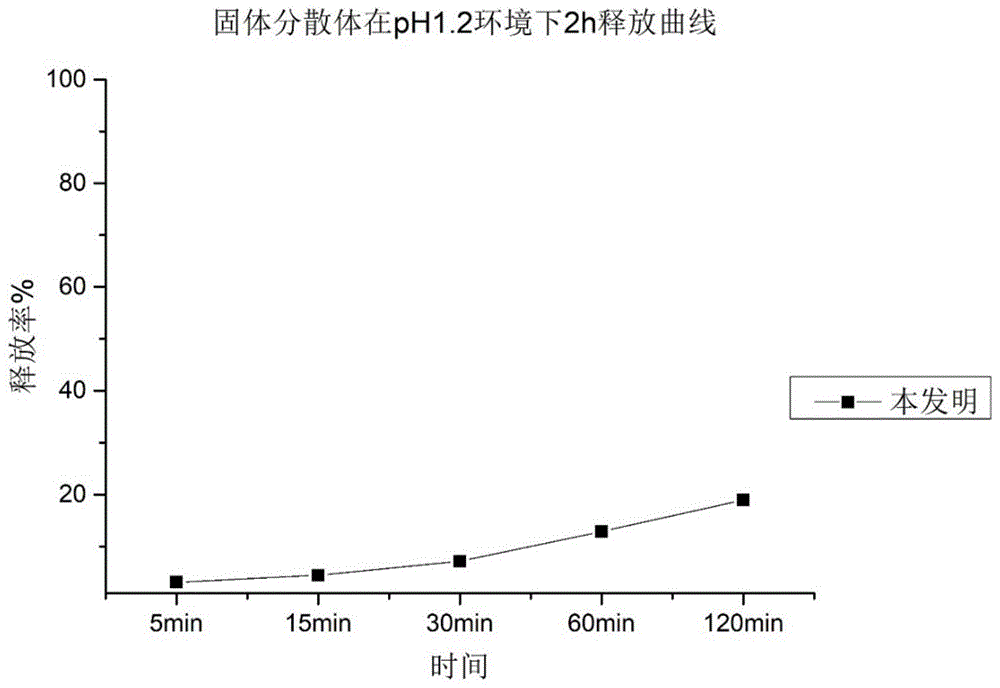
图1是本发明实施例7中固体分散体在模拟的胃ph1.2条件下体外释放曲线图。
图2是本发明实施例7中固体分散体在模拟的肠道ph6.8条件下体外释放曲线图。
具体实施方式
以下结合实施例进一步阐明本发明的内容,但并不限制本发明:
所有实施例中含药固体分散体的收率均≥98%。
本发明的美沙拉嗪固体分散体体外释放度研究方法如下:
药物体外模拟胃部环境释放度测定方法:将制得的固体分散体置于溶出杯中,照中国药典释放度测定方法中第二法装置,以ph1.2溶液为溶剂,转速为每分钟75转,依法操作,分别于5min,15min,30min,1h,2h溶出时间取样3ml,并迅速补充37℃溶剂3ml,滤过,hplc分析,计算不同时间的药物释放量。
药物体外模拟肠道环境释放度测定方法:将制得的固体分散体置于溶出杯中,照中国药典释放度测定方法中第二法装置,以ph6.8溶液为溶剂,转速为每分钟75转,依法操作,分别于5min,15min,30min,1h,2h,4h,6h溶出时间取样3ml,并迅速补充37℃溶剂3ml,滤过,hplc分析,计算不同时间的药物释放量。
实施例1
包合辅料处方:
1壳聚糖10g
2海藻酸10g
包合辅料制备方法:将壳聚糖和海藻酸以质量比1:1,转速30r,球磨2h混合制得。
包衣工艺:将壳聚糖-海藻酸固体分散体与5-氨基水杨酸以质量比1:1,转速30r/min,球磨混合2h即得。
实施例2
包合辅料处方:
1壳聚糖10g
2海藻酸钠10g
包合辅料制备方法:将壳聚糖和海藻酸钠以质量比1:1,转速30r,球磨2h混合制得。
包衣工艺:将壳聚糖-海藻酸钠固体分散体与5-氨基水杨酸以质量比1:1,转速30r/min,球磨混合2h即得。
实施例3
包合辅料处方:
1壳聚糖10g
2聚谷氨酸10g
包合辅料制备方法:将壳聚糖和聚谷氨酸以质量比1:1,转速30r,球磨2h混合制得。
包衣工艺:将壳聚糖-聚谷氨酸固体分散体与5-氨基水杨酸以质量比1:1,转速30r/min,球磨混合2h即得。
实施例4
包合辅料处方:
1聚赖氨酸10g
2聚谷氨酸10g
包合辅料制备方法:将聚赖氨酸和聚谷氨酸以质量比1:1,转速30r,球磨2h混合制得。
包衣工艺:将聚赖氨酸-聚谷氨酸固体分散体与5-氨基水杨酸以质量比1:1,转速30r/min,球磨混合2h即得。
实施例5
包合辅料处方:
1壳聚糖10g
2海藻酸钠10g
包合辅料制备方法:将壳聚糖和海藻酸钠以质量比1:1,转速30r,球磨2h混合制得。
包衣工艺:将壳聚糖-海藻酸钠固体分散体与5-氨基水杨酸以质量比2:1,转速30r/min,球磨混合2h即得。
实施例6
包合辅料处方:
1壳聚糖10g
2海藻酸钠10g
包合辅料制备方法:将壳聚糖和海藻酸钠以质量比1:1,转速30r,球磨2h混合制得。
包衣工艺:将壳聚糖-海藻酸钠固体分散体与5-氨基水杨酸以质量比3:1,转速30r/min,球磨混合2h即得。
实施例7
包合辅料处方:
1壳聚糖10g
2海藻酸钠10g
包合辅料制备方法:将壳聚糖和海藻酸钠以质量比1:1,转速30r,球磨2h混合制得。
包衣工艺:将壳聚糖-海藻酸钠固体分散体与5-氨基水杨酸以质量比2:1,转速30r/min,球磨混合4h即得。
实施例8
取实施例1~7固体分散体样品,按上述药物体外释放度测定方法考察制备样品的药物体外释放度,结果见表1,表2。
表1固体分散体体外模拟胃部环境释放度结果
表2固体分散体体外模拟肠道环境释放度结果
- 还没有人留言评论。精彩留言会获得点赞!