一种基于造影技术的脑血管疾病成像方法及应用的造影剂与流程
本发明属于医学图像处理及医学制剂制备技术领域,尤其涉及一种基于造影技术的脑血管疾病成像方法及应用的造影剂。
背景技术:
脑血管疾病泛指脑部血管的各种疾病,包括脑动脉粥样硬化、血栓形成、狭窄、闭塞、脑动脉炎、脑动脉损伤、脑动脉瘤、颅内血管畸形、脑动静脉瘘等,其共同特点是引起脑组织的缺血或出血性意外,导致患者的残废或死亡。因此,需要通过提前检测和诊断脑血管中的危险因素,来预防心脑血管疾病的发生或者复发,从而达到降低死亡率的目的。
脑血管造影是观察脑部血管最直接的方法,能了解血管的形态、分布、粗细、移位、闭塞、狭窄等,尚可观察血管本身的病变(如脑动脉瘤和脑动静脉畸形(avm)等)。电子计算机断层扫描(computedtomography,ct)是利用x射线束对人体组织器官进行一定厚度的层面进行扫描,具有扫描时间快,图像清晰等优点,广泛用于医学诊断中。由于ct的成像特点,其对实体组织如骨骼、肝脏等具有较好的成像功能,但对血管等组织的成像能力较差,为了增强ct对血管等组织的成像效果,ct造影剂开始被开发和应用。传统ct造影剂主要利用了碘溶液吸收x射线的特性,一定程度增强了ct造影效果,但大多存在生物毒性较大、造影效果不佳、制作工艺复杂等缺点。近年来,随着纳米材料技术的飞速发展,各种性能优越(如吸收能力强、散射截面大、表面等离子体共振效应明显等)的纳米材料不断被研制出来。因此,以新型的纳米材料作为造影剂进行辅助增强成像的相关研究受到了科学家们的广泛关注。
申请号为200910113084.9的中国发明专利公开了一种ct成像造影剂及其制备方法,该造影剂由纳米金颗粒为核心,外围包裹碘海醇,虽然增强了对x射线的吸收系数,但仍然存在注射剂量大、血液半衰期短的问题。而且,采用ct采集注射造影剂后的脑血管图像时,随着采集时间的延长,造影剂不可避免的会渗出至血管周围的软组织中,导致血管与周围软组织的界限变模糊,从而影响血管分割的精度。
技术实现要素:
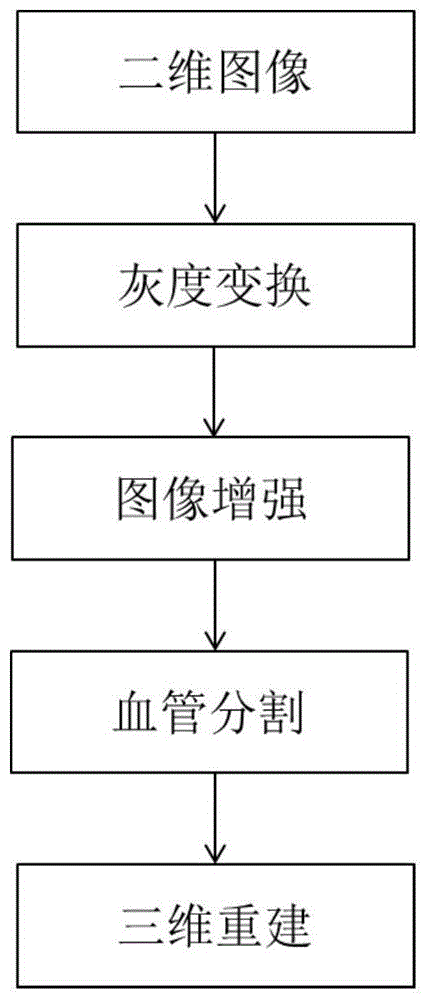
针对上述现有技术存在的缺陷,本发明的目的在于提供一种基于造影技术的脑血管疾病成像方法。采用x射线断层扫描采集注射造影剂后的脑血管横截面二维图像,然后依次对图像进行灰度变换、图像增强、血管分割和三维重建得到脑血管三维图像。
本发明的目的还在于提供一种上述脑血管疾病成像方法应用的造影剂,所述造影剂为以含有金纳米粒子的聚乳酸为油相,以含有非离子型碘造影剂的水溶液为水相,以2-[甲氧基(聚氧乙烯)丙基]-三甲氧基硅烷为改性剂,制备成的硅氧烷修饰的聚乳酸微泡。
为实现上述目的,本发明采用如下的技术方案:
一种基于造影技术的脑血管疾病成像方法,包括以下步骤:
s1.从静脉注射造影剂,待造影剂到达脑血管区域后,对脑血管区域进行x射线断层扫描,得到不同层面的脑血管横截面二维图像;
s2.对步骤s1所述每个层面的脑血管横截面二维图像依次进行灰度变换和图像增强处理,得到每个层面的脑血管横截面预处理图像;
s3.对步骤s2所述每个层面的脑血管横截面预处理图像进行血管分割,得到每个层面的脑血管图像;
s4.将步骤s3所述每个层面的脑血管图像进行三维重建,得到脑血管三维图像。
作为本发明的进一步改进,在步骤s2中,所述灰度变换采用分段线性变换。
作为本发明的进一步改进,在步骤s2中,所述图像增强处理是利用梯度算子|▽t|、曲率检测因子λ2和血管多尺度因子σ,设计边缘检测算子,对血管进行多尺度边缘检测,滤除没有边缘结构的含有造影剂的软组织噪声。
作为本发明的进一步改进,所述边缘检测算子的公式如下:
作为本发明的进一步改进,在步骤s3中,所述血管分割采用基于二阶微分的拉普拉斯算子对脑血管横截面预处理图像进行分割。
作为本发明的进一步改进,在步骤s4中,所述三维重建采用光线投射法。
一种以上所述的基于造影技术的脑血管疾病成像方法中应用的造影剂,所述造影剂为以含有金纳米粒子的聚乳酸为油相,以含有非离子型碘造影剂的水溶液为水相,以2-[甲氧基(聚氧乙烯)丙基]-三甲氧基硅烷为改性剂,制备成的硅氧烷修饰的聚乳酸微泡。
作为本发明的进一步改进,所述造影剂的制备方法包括以下步骤:
(1)将金纳米粒子加入到含有聚乳酸的三氯甲烷溶液中,作为油相;
(2)将非离子型碘造影剂加入到注射用水,得到质量分数为70%-90%的造影剂水溶液,作为水相;
(3)将步骤(2)所述水相加入到步骤(1)所述油相中,超声处理得到聚乳酸微泡;
(4)将步骤(3)所述聚乳酸微泡加入到浓度为4%-8%(w/v)的2-[甲氧基(聚氧乙烯)丙基]-三甲氧基硅烷的乙醇溶液中,使溶液中的乙醇完全挥发掉,此过程中,2-[甲氧基(聚氧乙烯)丙基]-三甲氧基硅烷在所述聚乳酸微泡表面固化交联,得到硅氧烷修饰的聚乳酸微泡。
作为本发明的进一步改进,在步骤(1)中,所述油相中金纳米粒子的浓度为2-6mg/ml,聚乳酸的浓度为30-60mg/ml。
作为本发明的进一步改进,在步骤(3)中,所述聚乳酸微泡和乙醇溶液的体积比为1:2.5-1:4。
有益效果
与现有技术相比,本发明提供的基于造影技术的脑血管疾病成像方法及应用的造影剂具有如下有益效果:
(1)本发明提供的基于造影技术的脑血管疾病成像方法,采用ct造影成像的方法,首先采用自制的造影剂静脉注射后,采集不同层面的脑血管横截面二维图像,然后依次对图像进行分阶段线性灰度变换和边缘检测算子滤除软组织噪声处理,再采用基于二阶微分的拉普拉斯算子进行血管分割,最后将二维血管图像进行三维重建得到脑血管三维图像。如此操作,采用分阶段线性灰度变换,能够对脑血管横截面二维图像进行灰度改善,提升血管像素的灰度值,压缩非血管像素的灰度值,从而有效的抑制了非血管像素的灰度值,保留了过渡区间的灰度值,并一定程度上增强了血管目标的灰度值。采用边缘检测算子滤除软组织区域,由于血管在边缘区域会产生灰度的陡变,陡变度可以利用梯度算子进行检测,从而得到边缘明确的血管,很大程度的平滑血管边缘,凸显血管结构。当检测到血管内的像素时,曲率检测因子λ2的值相对较大,导致梯度t较小,从而不影响血管的增强;当检测到血管外的像素点时,由于软组织没有固定的边缘和走向,所以不存在曲率检测因子λ2,从而通过梯度t过滤这些像素点,实现了软组织噪声的去除。采用二阶微分的拉普拉斯算子对于血管图像的细节可以产生更强的响应,能够分割得到高精度的血管图像。
(2)本发明提供的脑血管疾病成像方法应用的造影剂,将金纳米粒子聚乳酸溶液作为油相,非离子型碘造影剂水溶液作为水相,得到金纳米粒子和聚乳酸包裹非离子型碘造影剂的聚乳酸微泡,再以2-[甲氧基(聚氧乙烯)丙基]-三甲氧基硅烷修饰聚乳酸微泡表面,能够提高造影剂在血液中的生物相容性和稳定性。金纳米粒子作为聚乳酸微泡的外层,不仅能够增强造影,而且能够延长体内血液循环时间从而克服了传统碘造影剂排除快的缺陷。另外,金纳米粒子很容易与各种功能生物分子作用,获得组织靶向或多模成像功能,从而可以为血管疾病的诊断提供准确、丰富的信息。
附图说明
图1为本发明提供的基于造影技术的脑血管疾病成像方法的流程框图。
具体实施方式
以下将对本发明各实施例的技术方案进行清楚、完整的描述,显然,所描述的实施例仅仅是本发明的一部分实施例,而不是全部的实施例;基于本发明的实施例,本领域普通技术人员在没有做出创造性劳动的前提下所得到的所有其它实施例,都属于本发明所保护的范围。
ct造影是选用x射线束对造影部位以垂直照射,并利用高灵敏度的射线探测仪对造影部位以某一厚度进行环绕平扫,得到穿透人体部位后衰减过的射线束,再利用光电转换理论将接受到的射线束转换为电信号,再利用模/数变换,将电信号进行转换,最后以数字图像形式输出,得到ct图像。一般地,一次扫描可以得到连续的厚度相同的多张横切图像,这些横切图像可以进行三维重建等操作。在生成ct图像过程中,模拟信号转换的数字信号中,每一个数字信号都可以对应灰度范围内的某一灰度值,单个数字信号在灰度图像中映射为像素,像素时ct二维横切图像的处理单元。在一列横切图像中,选取连续几个大小相同、位置对应的像素构成块,将序列图像分为完全相同的长方体,这些长方体称为体素,图像进行三维操作时,是以体素为单元进行处理的。
基于此,本发明提供的一种基于造影技术的脑血管疾病成像方法如图1所示,包括以下步骤:
s1.从静脉注射造影剂,待造影剂到达脑血管区域后,对脑血管区域进行x射线断层扫描,得到不同层面的脑血管横截面二维图像;
s2.对步骤s1所述每个层面的脑血管横截面二维图像依次进行灰度变换和图像增强处理,得到每个层面的脑血管横截面预处理图像;
s3.对步骤s2所述每个层面的脑血管横截面预处理图像进行血管分割,得到每个层面的脑血管图像;
s4.将步骤s3所述每个层面的脑血管图像进行三维重建,得到脑血管三维图像。
作为本发明的进一步改进,在步骤s2中,所述灰度变换采用如式(1)所示的分段线性函数对脑血管横截面二维图像进行分段线性变换:
如对原始输入的脑血管横截面二维图像i(x,y)进行变换时,a、b代表需要调整的灰度范围区间的端点值,c、d代表调整好的灰度范围区间的端点,决定对脑血管横截面二维图像中某个灰度区间的像素进行拉伸或者是压缩,是灰度变换的重点。采用此种变换,能够对脑血管横截面二维图像进行灰度改善,提升血管像素的灰度值,压缩非血管像素的灰度值,从而有效的抑制了非血管像素的灰度值,保留了过渡区间的灰度值,并一定程度上增强了血管目标的灰度值。
当造影剂在血管中流动时,造影剂不可避免的会渗出血管到血管周围的软组织,如造影剂渗出达到一定程度时,血管周围的组织也会在ct造影过程中被保留下来,成为影响血管影像的主要干扰因素,尤其在相比较来说比较细的血管区域这种干扰更加明显。渗透到软组织中的造影剂会影响视觉效果,但是,含有造影剂的软组织是扩散式分布的,没有固定的区域边缘,血管却是具有明确的边缘结构。根据这个特性,本发明设计一个边缘检测算子专门针对血管边缘结构进行检测,滤除没有边缘结构的含有造影剂的软组织区域。
因此,作为本发明的进一步改进,在步骤s2中,所述图像增强处理是利用梯度算子|▽t|、曲率检测因子λ2和血管多尺度因子σ,设计边缘检测算子,对血管进行多尺度边缘检测,滤除没有边缘结构的含有造影剂的软组织噪声。所述边缘检测算子的公式如式(2)所示:
采用式(2)进行边缘检测增强时,由于血管在边缘区域会产生灰度的陡变,陡变度可以利用梯度算子进行检测,从而得到边缘明确的血管,很大程度的平滑血管边缘,凸显血管结构。当检测到血管内的像素时,曲率检测因子λ2的值相对较大,导致梯度t较小,从而不影响血管的增强;当检测到血管外的像素点时,由于软组织没有固定的边缘和走向,所以不存在曲率检测因子λ2,从而通过梯度t过滤这些像素点,实现了软组织噪声的去除。
作为本发明的进一步改进,在步骤s3中,所述血管分割采用基于二阶微分的拉普拉斯算子,如式(3)所示,对脑血管横截面预处理图像进行分割:
优选地,在采用基于二阶微分的拉普拉斯算子进行血管分割时,先采用高斯滤波器对脑血管横截面预处理图像进行平滑处理,如式(4)所示:
式中,σ为图像的标准差,在实际平滑过程中,σ过小,则偏离中心的所有像素权重会非常的小,当σ小到一定程度时,滤波操作则会退化为对图像进行点运算,无法起到平滑噪声的作;但如果σ过大,邻域较小时,在邻域内的高斯模板将会退化为均值模板,会造成边缘模糊的效果,所以本发明σ值优选为0.6-0.7,有助于达到较好的平滑效果。
作为本发明的进一步改进,在步骤s4中,所述三维重建采用光线投射法。该方法的思想是在投影平面对每个像素以投影角度分别发出射线,穿过体数据,对每条射线上数据值进行比较,选一个最大的值作为响应像素显示值。最大密度投影法最主要的优点是计算量小,计算速度快。
一种以上所述的基于造影技术的脑血管疾病成像方法中应用的造影剂,所述造影剂为以含有金纳米粒子的聚乳酸为油相,以含有非离子型碘造影剂的水溶液为水相,以2-[甲氧基(聚氧乙烯)丙基]-三甲氧基硅烷为改性剂,制备成的硅氧烷修饰的聚乳酸微泡。
作为本发明的进一步改进,所述造影剂的制备方法包括以下步骤:
(1)将金纳米粒子加入到含有聚乳酸的三氯甲烷溶液中,作为油相;
(2)将非离子型碘造影剂加入到注射用水,得到质量分数为70%-90%的造影剂水溶液,作为水相;
(3)将步骤(2)所述水相加入到步骤(1)所述油相中,超声处理得到聚乳酸微泡;
(4)将步骤(3)所述聚乳酸微泡加入到浓度为4%-8%(w/v)的2-[甲氧基(聚氧乙烯)丙基]-三甲氧基硅烷的乙醇溶液中,使溶液中的乙醇完全挥发掉,此过程中,2-[甲氧基(聚氧乙烯)丙基]-三甲氧基硅烷在所述聚乳酸微泡表面固化交联,得到硅氧烷修饰的聚乳酸微泡。
作为本发明的进一步改进,在步骤(1)中,所述油相中金纳米粒子的浓度为2-6mg/ml,聚乳酸的浓度为30-60mg/ml。
作为本发明的进一步改进,在步骤(3)中,所述聚乳酸微泡和乙醇溶液的体积比为1:2.5-1:4。
将金纳米粒子聚乳酸溶液作为油相,非离子型碘造影剂水溶液作为水相,得到金纳米粒子和聚乳酸包裹非离子型碘造影剂的聚乳酸微泡。再以2-[甲氧基(聚氧乙烯)丙基]-三甲氧基硅烷修饰聚乳酸微泡表面,能够提高造影剂在血液中的生物相容性和稳定性。金纳米粒子不仅具有增强造影的能力,而且它能够延长体内血液循环时间从而克服了传统碘造影剂排除快的缺陷。另外,金纳米粒子很容易与各种功能生物分子作用,获得组织靶向或多模成像功能,从而可以为血管疾病的诊断提供准确、丰富的信息。
实施例1
请参阅图1所示,一种基于造影技术的脑血管疾病成像方法,包括以下步骤:
s1.从静脉注射造影剂,待造影剂到达脑血管区域后,对脑血管区域进行x射线断层扫描,得到不同层面的脑血管横截面二维图像;所述造影剂通过以下步骤制备:
(1)将金纳米粒子加入到含有聚乳酸的三氯甲烷溶液中,作为油相;所述油相中金纳米粒子的浓度为4mg/ml,聚乳酸的浓度50mg/ml;
(2)将碘海醇加入到注射用水,得到质量分数为80%的造影剂水溶液,作为水相;
(3)将步骤(2)所述水相滴加到步骤(1)所述油相中,滴加完毕后立即用探头超声对样品进行超声处理,得到聚乳酸微泡;
(4)将步骤(3)所述聚乳酸微泡加入到浓度为6%(w/v)的2-[甲氧基(聚氧乙烯)丙基]-三甲氧基硅烷的乙醇溶液中(所述聚乳酸微泡和乙醇溶液的体积比为1:3),置于通风橱中搅拌,使溶液中的乙醇完全挥发掉,在此过程中,2-[甲氧基(聚氧乙烯)丙基]-三甲氧基硅烷在所述聚乳酸微泡表面固化交联,得到硅氧烷修饰的聚乳酸微泡。
s2.采用下式所示的分段线性函数对对步骤s1所述每个层面的脑血管横截面二维图像进行分段线性变换:
式中,a、b代表需要调整的灰度范围区间的端点值,c、d代表调整好的灰度范围区间的端点;
采用采用下式所示的边缘检测算子对进行边缘检测增强处理,得到每个层面的脑血管横截面预处理图像:
式中,|▽t|为梯度算子、λ2为曲率检测因子,σ为血管多尺度因子;
s3.采用下式所示的高斯滤波函数对步骤s2所述每个层面的脑血管横截面预处理图像进行平滑处理:
式中,σ为图像的标准差,取值为0.7;
然后采用下式所示的基于二阶微分的拉普拉斯算子对平滑后的每个层面的脑血管横截面预处理图像进行血管分割,得到每个层面的脑血管图像:
s4.采用光线投射法将步骤s3所述每个层面的脑血管图像进行三维重建,得到脑血管三维图像。
综上所述,本发明采用自制的造影剂,将金纳米粒子聚乳酸溶液作为油相,非离子型碘造影剂水溶液作为水相,得到金纳米粒子和聚乳酸包裹非离子型碘造影剂的聚乳酸微泡,再以2-[甲氧基(聚氧乙烯)丙基]-三甲氧基硅烷修饰聚乳酸微泡表面,能够提高造影剂在血液中的生物相容性和稳定性,并能够增强造影,延长体内血液循环时间。以此造影剂进行ct造影成像,对采集的二维图像进行分阶段线性灰度变换和边缘检测算子滤除软组织噪声处理,再采用基于二阶微分的拉普拉斯算子进行血管分割,最后将二维血管图像进行三维重建得到脑血管三维图像。能够有效的抑制非血管像素的灰度值,提升血管像素的灰度值,并有效滤除血管周围的软组织区域,从而得到高精度的脑血管二维图像。
以上所述,仅为本发明较佳的具体实施方式,但本发明的保护范围并不局限于此,任何熟悉本技术领域的技术人员在本发明揭露的技术范围内,根据本发明的技术方案及其发明构思加以等同替换或改变,都应涵盖在本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!