肠道菌群调节剂与间充质干细胞的组合物及其应用的制作方法
本发明属于生物医药技术领域,尤其涉及肠道菌群调节剂与间充质干细胞的组合物及其应用。
发明背景
哺乳动物胃肠道内存在多种活跃的微生物群落,包括细菌、古生菌、真核生物、病毒等,被称为“肠道微生物群”,其数量约为1014,这些微生物编码的基因总数是人体自身基因的100倍左右。这些微生物中又以细菌数量最多,构成了肠道菌群。它们与宿主长期共同进化了,形成了复杂而互利的关系,也被认为是宿主的“新器官”。肠道菌群对维持机体的稳态具有重要作用,包括食物的消化吸收,刺激免疫系统的成熟,调解代谢,抵御病原微生物在肠道内的定植和增殖等。然而,当肠道菌群的生态平衡被打破,肠道微生物组成发生改变时上述功能也受到影响,这被称为肠道菌群失调。在某些情况下,如抗生素过度使用、饮食结构不当导致肠道菌群结构紊乱,会促进疾病的发生并加速疾病的进展,而调节紊乱的肠道菌群则有利于疾病的治疗。
糖尿病是一组以高血糖为特征的代谢性疾病,糖尿病的症状表现为“三多一少”,多见于1型糖尿病,2型糖尿病常不十分明显或仅有部分表现,高血糖则是由于胰岛素分泌缺陷或其生物作用受损,或两者兼有引起。其中,i型糖尿病(type1diabetesmellitus,t1dm)是一种自身免疫性疾病,其特征表现为t淋巴细胞或者其它免疫细胞浸润并攻击胰岛β细胞,导致胰岛β细胞破坏、数量减少,最终引发胰岛素的绝对缺乏。虽然t1dm的发病原因目前仍不明确,但主流观点认为t1dm的发病原因是一种受环境因素影响的多基因疾病,相关学者研究表明,遗传风险因素对疾病是必要的,但不是充分的,许多环境影响因素,包括病毒感染、饮食、妊娠如妊娠感染以及抗生素的使用等,已被提出作为t1dm候选的病因。另外,还有研究表明,t1dm患者的肠道菌群结构与健康者相比有显著差别,表现为拟杆菌门比例增加,而厚壁菌们比例减少,同时肠道菌群多样性较低,稳定性较差。非肥胖糖尿病小鼠(non-obesediabeticmice,nod小鼠)是一种自发性糖尿病小鼠,研究显示在其发病前使用抗生素处理扰乱其健康的肠道菌群,可以加速t1dm的进展,增加发病率。这些研究都表明表明肠道菌群与t1dm之间存在显著的联系。
当前,治疗t1dm最常用的方法依然是胰岛素治疗,该治疗可使患者血糖尽量恢复到正常水平,同时避免低血糖的发生。然而,虽然外源性的胰岛素可以改善血糖水平,但是由于该方法无法改善胰岛β细胞分泌胰岛素的功能,因此难以应对时刻波动的血糖变化。胰岛和胰腺的移植虽然可以改善胰岛素分泌能力,但是由于供体的缺乏和手术风险难以普及。近年来,间充质干细胞(mesenchymalstemcells,mscs)被广泛应用于多种疾病的治疗研究中,其良好的免疫调节能力被认为在自身免疫性疾病的治疗中具有广阔的应用前景。在链脲佐菌素(stz)诱导的t1dm小鼠模型中,mscs移植可以减少胰岛炎症、提高血清胰岛素水平和胰岛内胰岛素含量,进而缓解高血糖症状。但是,到目前为止,由于临床试验的效果不理想,全世界仍没有批准的可用于t1dm治疗的干细胞药物产品。如何增强mscs的治疗效果是亟待解决的问题。
技术实现要素:
本发明的目的之一在于克服现有技术中所述的缺陷,从而提供一种肠道菌群调节剂与间充质干细胞的组合物,该组合物适用于治疗糖尿病,有效增强间充质干细胞治疗t1dm的稳定性,尤其是自身免疫性的i型糖尿病,可减轻胰岛炎症,使更多的胰岛β细胞得以保存,为间充质干细胞的临床转化和应用提供支持。
为了实现上述目的,本发明提供如下技术方案:
一种组合物,所述的组合物包括由间充质干细胞组成的第一剂;和,
由肠道菌群调节剂组成的第二剂。
在一些实施方案中,所述肠道菌群调节剂为肠道益生菌和/或广谱抗生素。
肠道益生菌一般是指在人体肠胃生长的、对人体健康起到正面作用的细菌或真菌。抗生素(antibiotics)是由微生物(包括细菌、真菌、放线菌属)或高等动植物在生活过程中所产生的具有抗病原体或其它活性的一类次级代谢产物,能干扰其他生活细胞发育功能的化学物质,主要用于治疗各种细菌感染或致病微生物感染类疾病,一般情况下对其宿主不会产生严重的副作用;广谱抗生素指的是抗菌谱比较宽的药物,简单说就是能够抵抗大部分细菌的药物,例如氯霉素、金霉素、土霉素、四环素、甲砜霉素等。不仅能强力抑制大部分革兰氏阴性菌和革兰氏阳性菌,而且能抑制立克次体、螺旋体和某些原虫。
在一些实施方案中,所述肠道益生菌选自双歧杆菌、乳酸菌、链球菌、芽孢杆菌中的一种或几种;
优选地:所述双歧杆菌选自长双歧杆菌、短双歧杆菌、婴儿双歧杆菌、齿双歧杆菌、动物双歧杆菌等、乳双歧杆菌、青春双歧杆菌、比菲德氏b菌中的一种或几种;
优选地:所述乳酸菌选自嗜酸杆菌、罗伊乳杆菌、鼠李糖乳杆菌、约氏乳酸杆菌、凝结芽孢杆菌、保加利亚乳杆菌中的一种或几种;
优选地:所述链球菌为粪链球菌;
优选地:所述芽孢杆菌选自克劳氏芽孢杆菌、凝结芽孢杆菌、枯草杆菌中的一种或几种;
在一些实施方案中,所述广谱抗生素为多肽类广谱抗生素、大环内酯类广谱抗生素、8含磷多糖类广谱抗生素、聚醚类广谱抗生素、氨基苷类广谱抗生素、化学合成类广谱抗生素中的一种或几种。
在一些实施方案中,所述广谱抗生素选自氨苄西林溶液、甲硝唑溶液、新霉素溶液、万古霉素溶液组成的混合剂;所述混合剂中氨苄西林溶液、甲硝唑溶液、新霉素溶液和万古霉素溶液的浓度比依次为1:1:1:0.4-0.6。
在一些实施方案中,所述间充质干细胞选自脂肪间充质干细胞、骨髓间充质干细胞、脐带间充质干细胞、胎盘间充质干细胞、牙髓间充质干细胞、皮肤间充质干细胞、尿液间充质干细胞、骨膜间充质干细胞中的一种或多种,优选脂肪间充质干细胞。
在一些实施方案中,所述组合物中的肠道菌群调节剂为广谱抗生素,所述广谱抗生素中的溶质与所述间充质干细胞的比例为(80-1000)mg:(0.5-5)×106个。
在一些实施例中,所述组合物中广谱抗生素溶质的质量为130mg,间充质干细胞的个数为1×106个。
在一些实施例中,所述组合物中的肠道菌群调节剂为光密度值为0.8以上的双歧杆菌,所述双歧杆菌与所述间充质干细胞的比例为1×109-12cfu:(0.5-5)×106个。
在一些实施例中,所述组合物中包含1×106个间充质干细胞和1×109cfu双歧杆菌。
将所述组合物应用时,可以将所述间充质干细胞任选地通过静脉注射、肌肉注射、皮下注射、鞘内注射或输注以及器官内输注所组成的组中的途径进行给药。例如,对于静脉注射,可以通过静脉全身给药或者尾静脉注射。其中,器官内输注包括输注至解剖学空间中,例如,胆囊、胃肠腔、食道、肺系统(通过吸入)和/或膀胱。广谱抗生素通过口服或者静脉注射给药,益生菌通过口服消化道给药。
在一些实施方案中,组合物中的两种试剂以单一药物组合物的形式提供,并且在一些实施方案中,可以预期是包含两种试剂中的每一种的试剂盒或组合的分配器包装。应当理解,本发明的内容涵盖两种试剂中的任一种对受试者的共同施用,无论这种施用是以单一制剂还是以分开的制剂组合,以及这种施用是同时的还是交错的。
在一些实施例中,所述间充质干细胞取自抽脂患者多余的脂肪组织。
在一些实施例中,所述间充质干细胞的代数为第3-6代。
在一些实施例中,还提供了所述组合物在制备治疗i型糖尿病药物中的应用。
在一些实施例中,所述组合物还包含药学上可接受的载体;所述组合物的剂型优选地选自冻干粉针、注射剂、片剂或胶囊。
在一些实施例中,所述剂型选自注射剂或片剂。
在一些实施例中,还提供了所述的间充质干细胞的提取方法,包括如下步骤:
(1)向脂肪组织中加入酶进行消化,然后进行离心过滤和重悬;
(2)将重悬后的细胞进行体外培养,当细胞汇合大于80%时,加入胰蛋白酶对细胞进行消化,然后接种到新的培养皿中进行传代培养;
(3)当传代培养至第三代时,用pbs冲洗2-5次,并用0.2-0.3wt%的胰蛋白酶进行消化,得到待鉴定的间充质干细胞;
(4)将所述待鉴定的间充质干细胞依次进行固定和封闭,并在4-6℃下避光孵育表面标记物抗体,同时以cd90-fitc、cd44-pe、cd73-apc、cd105-cy5.5为同型对照物做相应的同型对照,当表面标记物抗体为cd90、cd44、cd73、cd105,且表达在95%以上时,鉴定得间充质干细胞。
在一些实施例中,步骤(1)中所述酶的体积为所述脂肪组织的三倍以上,所述酶包括质量比为1.8-2.2:1的分散酶和一型胶原酶。
在一些实施例中,步骤(1)中所述消化为在35-38℃的温度下,以400-500rpm/min的速度震荡30min以上,所述离心过滤包括先在无菌条件下使用70nm的细胞筛进行过滤,然后将悬液以2400-2600rpm/min的速度离心6-8min,所述重悬在含有10-12wt%胎牛血清的α-mem培养基中进行。
在一些实施例中,步骤(2)中所述体外培养为将重悬后的细胞移入新的培养皿中进行培养直至细胞贴壁生长成长梭形,其中培养的温度为35-38℃,二氧化碳的体积分数为4-6%。
在一些实施例中,步骤(4)中所述的固定为使用3-5wt%的多聚甲醛固定细胞10-20min,所述封闭为使用0.8-12wt%的牛血清白蛋白封闭20-30min。
一方面,本发明还提供了肠道菌群调节剂在制备间充质干细胞服用品的伴随药物方面的用途。
本发明实施例中的“间充质干细胞服用品”包括但不限于能使间充质干细胞进入动物体内的产品或方法。作为示范性的例子,能使间充质干细胞服用品进入动物体内的产品包括冻干粉针、注射剂、片剂或胶囊。作为示范性的例子,能使干细胞服用品进入动物体内的方法包括口服和注射。
本发明实施例中的“伴随药物”包括随另外一种或多种药物一同进入体内的药物。伴随药物可以同时或几乎同时进入体内。作为示范性的例子,几乎同时进入可以是一个接一个地进入;或在同一天的不同时刻进入体内。例如,可以将多个药剂或其活性成分配制成一种制剂,或者两种或多种制剂至少基本上同时进入体内。例如,相互在约1小时内。
在一些实施例中,所述的间充质干细胞服用品选自脂肪间充质干细胞、骨髓间充质干细胞、脐带间充质干细胞或牙髓间充质干细胞。
在一些实施例中,所述的间充质干细胞服用品为用以摄入动物体的脂肪间充质干细胞;优选地,所述动物为哺乳动物;优选地,所述哺乳动物为人。
一方面,本发明还提供了一种干细胞服用系统,其包括:间充质干细胞服用品,和,伴随品;所述的伴随品选自广谱抗生素和/或双歧杆菌;所述的间充质干细胞服用品包含脂肪间充质干细胞、骨髓间充质干细胞、脐带间充质干细胞或牙髓间充质干细胞;所述广谱抗生素或双歧杆菌如前所述。
一方面,本发明还提供了一种促进间充质干细胞服用品预防和治疗i型糖尿病的方法,所述方法包括,在服用间充质干细胞服用品期间,同时或几乎同时服用肠道菌群调节剂。
附图说明
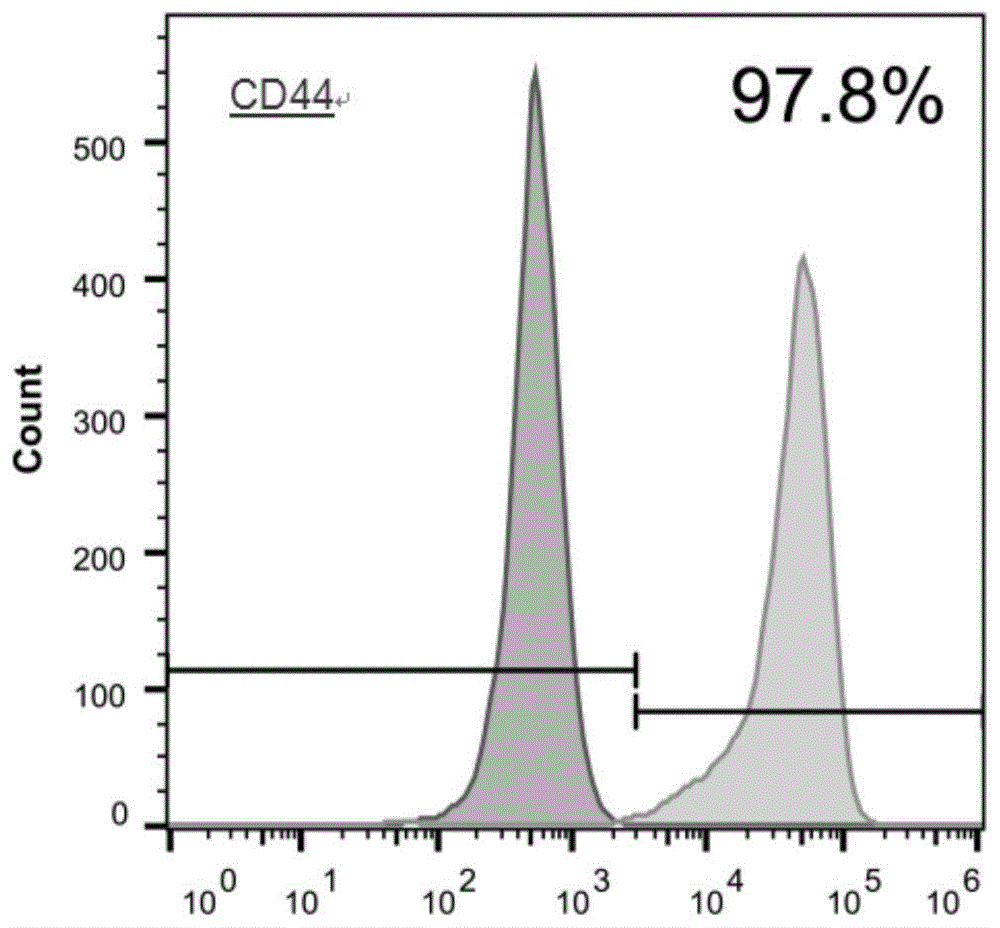
图1a为实施例2流式细胞检测中cd44阳性细胞比例;
图1b为实施例2流式细胞检测中cd73阳性细胞比例;
图1c为实施例2流式细胞检测中cd90阳性细胞比例;
图1d为实施例2流式细胞检测中cd105阳性细胞比例;
图2a为实施例1-4中采用链脲佐菌素、adscs和广谱抗生素对nod/ltj小鼠进行分阶段处理的流程示意图;
图2b为实施例3中所述pbs组、adscs组、adscs+abx组、co-housed组四组小鼠的血糖变化对照图;
图2c为实施例3中所述pbs组、adscs组、adscs+abx组、co-housed组四组小鼠的胰腺he染色结果,以及相应的胰岛炎症评分对照图;
图2d为实施例3中所述pbs组、adscs组、adscs+abx组、co-housed组四组小鼠的胰腺胰岛素免疫组化染色结果及β细胞染色评分定量图;
图2e为实施例3中所述pbs组、adscs组、adscs+abx组、co-housed组四组小鼠的血清胰岛素elisa检测结果对照图;
图3a为实施例4中adscs组、adscs+氨苄西林+万古霉素组、adscs+新霉素组与adscs+甲硝唑组的血糖变化对照图;
图4a为实施例5中pbs组、adscs组、adscs+abx组与abx组的血糖变化对照图;
图5a为实施例6中所述pbs组、adscs组、adscs+abx组、co-housed组四组小鼠的粪便细菌定量结果对照图;
图5b为实施例6中所述pbs组、adscs组、adscs+abx组、co-housed组四组小鼠粪便细菌α多样性分析对照图;
图5c为实施例6中所述pbs组、adscs组、adscs+abx组、co-housed组四组小鼠粪便细菌β多样性分析对照图;
图5d为实施例6中adscs组、adscs+abx组与co-housed组的差异菌(双歧杆菌)丰度对照图;
图6a为实施例7中adscs组、adscs+abx组、co-housed组与adscs+b.breve组的双歧杆菌(b.breve)肠道定植检测结果图;
图6b为实施例7中所述adscs组、adscs+abx组与adscs+b.breve组的血糖变化对照图;
图6c为实施例7中所述adscs组、adscs+abx组与adscs+b.breve组的胰腺经he染色结果以及相应的胰岛炎症评分对照图
图6d为实施例7中所述adscs组、adscs+abx组与adscs+b.breve组的胰腺胰岛素免疫组化染色结果以及β细胞染色评分定量图;
图7a为实施例8中所述adscs组、adscs+abx组、adscs+b.breve组中血清fitc-dextran浓度对照图;
图7b为实施例8中所述adscs组、adscs+abx组与adscs+b.breve组中血清内毒素浓度对照图;
图7c为实施例8中所述adscs组、adscs+abx组与adscs+b.breve组中结肠组织经阿利新蓝染色得到的扫描图和黏液层厚度的比对图;
图8a实施例9中所述为adscs组、adscs+abx组与adscs+b.breve组中胰腺组织细菌负荷的比对图;
图8b为实施例9中所述adscs组、adscs+abx组与adscs+b.breve组中胰腺组织eub338探针原位杂交染色图和在高倍视野下观测的细菌数量的比对图;
图8c为实施例9中所述adscs组、adscs+abx组与adscs+b.breve组中胰腺组织经mafa免疫组化染色得到的扫描图和阳性细胞的百分含量比对图。
具体实施方式
以下通过具体的实施例进一步说明本发明的技术方案,具体实施例不代表对本发明保护范围的限制。其他人根据本发明理念所做出的一些非本质的修改和调整仍属于本发明的保护范围。
本发明实施例中的间充质干细胞(msc,mesenchymalstemcells)来源于发育早期的中胚层,属于多能干细胞,间充质干细胞在体内或体外特定的诱导条件下,可分化为脂肪、骨、软骨、肌肉、肌腱、韧带、神经、肝、心肌、内皮等多种组织细胞,连续传代培养和冷冻保存后仍具有多向分化潜能,可作为理想的种子细胞用于衰老和病变引起的组织器官损伤修复。adscs为脂肪间充质干细胞(adiposederivedstemcells,adscs)。脂肪间充质干细胞是来源于脂肪组织的多能干细胞,具有自我更新和多向分化能力,并能分泌多种生物活性因子,在组织损伤、修复方面蕴含着广阔的应用前景。在本发明的以下实施例中,脂肪间充质干细胞取自具有脂肪充填病人的多余或废弃的脂肪组织(伦理号:pkussirb-201948106),提取脂肪间充质干细胞用α-mem培养基(minimumessentialmedium)培养。
本发明中的t1dm为i型糖尿病(type1diabetesmellitus,t1dm)。
本发明中的b.breve为短型双歧杆菌。
本发明实施例中所有动物实验都得到了北京大学医学部伦理委员会的批准(伦理号:la2019190)。
本发明中的pbs是磷酸缓冲盐溶液(phosphatebuffersaline),一般作为溶剂,起溶解保护试剂的作用。它是生物化学研究中使用最为广泛的一种缓冲液,主要成分为na2hpo4、kh2po4、nacl和kcl。
本发明的氨苄西林为广谱半合成青霉素,别名:氨苄青、安比西林、安必仙、沙维西林、赛米西林、氨苄西、潘别丁、ab-pc,是一种β-内酰胺类抗生素,毒性极低。抗菌谱与青霉素相似,它是第一个对革兰氏阳性细菌有“广谱”抗菌作用的青霉素,包括肺炎链球菌、化脓性链球菌、一些金黄色葡萄球菌的分离株(但不耐青霉素或耐甲氧西林菌株)、真杆菌和一些肠球菌。它是为数不多的对多药耐药的粪肠球菌和粪肠杆菌有效的抗生素之一。对一些革兰氏阴性菌如:脑膜炎奈瑟菌、一些流感嗜血杆菌和一些肠杆菌科有抗菌作用。
甲硝唑为硝基咪唑衍生物,可抑制阿米巴原虫的氧化还原反应,使原虫氮链发生断裂。抗菌谱包括脆弱类杆菌和其他类杆菌属、梭形杆菌、产气芽胞杆菌、真杆菌、消化球菌属和消化链球菌属等。其杀菌浓度稍高于抑菌浓度。甲硝唑对缺氧情况下生长的细胞和厌氧微生物起杀灭作用,它在人体中还原时生成的代谢物,也具有抗厌氧菌作用,但对需氧菌和兼性厌氧菌无作用。
新霉素由弗氏链霉菌产生,属于氨基糖苷类抗生素。其抗菌谱与其它氨基糖苷类药物相似,新霉素对革兰氏阴性菌有良好的抗菌活性,对革兰氏阳性菌有部分抗菌作用。新霉素与卡那霉素有完全交叉抗药性,与链霉素有部分交叉抗药性。
万古霉素限用于耐甲氧苯青霉素的金黄色葡萄球菌(mrsa)所致的系统感染和难辨梭状芽孢杆菌所致的肠道感染和系统感染。对葡萄球菌属包括金葡菌和凝固酶阴性葡萄球菌中甲氧西林敏感及耐药株、各种链球菌、肺炎链球菌及肠球菌属等多数革兰阳性菌均有良好抗菌作用,对难辨校状芽孢杆菌、炭疽杆菌、白喉杆菌等作用也良好。
“包含”或“包括”旨在表示组合物(例如介质)和方法包括所列举的要素,但不排除其他要素。当用于定义组合物和方法时,“基本上由……组成”意味着排除对于所述目的的组合具有任何重要意义的其他要素。因此,基本上由本文定义的元素组成的组合物不排除不会实质上影响要求保护的本发明的基本和新颖特征的其他材料或步骤。“由……组成”是指排除其他组成部分的微量元素和实质性的方法步骤。由这些过渡术语中的每一个定义的实施方案都在本发明的范围内。
实施例1糖尿病小鼠模型的构建:
选取7-8周龄的雌性nod/ltj小鼠(非肥胖型糖尿病nod小鼠,non-obesediabeticmouse,nod小鼠),购自北京大学医学部实验动物中心,在无特定病原微生物的环境下饲养,恒温恒湿,保持昼夜(12:12)节律。小鼠适应一周后,连续4天进行腹腔链脲佐菌素(streptozotocin,stz;40mg/kg;sigma-aldrich,美国)注射,以加速糖尿病的进展。注射7天后通过尾静脉取血检测血糖水平,连续3天血糖水平为>13.9mmol/l的小鼠被诊断为糖尿病。
实施例2脂肪间充质干细胞(adiposederivedstemcells,adscs)的提取与鉴定:
a)将取自抽脂患者多余的脂肪组织在超净台中用生理盐水清洗3次,然后加入三倍于脂肪体积的酶(0.4mg/ml分散酶:0.2mg/ml一型胶原酶=1:1)进行消化,于恒温震荡仪上37℃,450rpm,消化30min。在无菌条件下使用70nm细胞筛进行过滤,过滤后悬液在2500rpm/min离心5min,弃去上清,加入含10%胎牛血清的α-mem培养基重悬。将重悬后的细胞移入新的10cm培养皿中,置于细胞孵箱中37℃培养,二氧化碳体积分数5%。adscs贴壁生长后成长梭形,当细胞汇合度越80%时使用0.25%的胰蛋白酶消化细胞,以1:3的接种比例接种到新的10cm培养皿中进行传代培养。
b)为鉴定adscs,将传代培养至第三代的adscs用pbs洗3次,用0.25%的胰蛋白酶消化后收集细胞。使用4%的多聚甲醛固定细胞10-20min,然后使用1%的bsa封闭20-30min,于4℃下避光孵育表面标记物抗体及相应的同型对照:cd90-fitc、cd44-pe、cd73-apc、cd105-cy5.5。所有抗体购自bdbiosciences。用accuric6流动细胞仪(bdbiosciences)进行检测。流式细胞鉴定结果显示间充质干细胞表面标记cd44,cd73,cd90,cd105表达在95%以上(图1a、图1b、图1c、图1d),鉴定为adscs。
实施例3广谱抗生素混合剂处理可以增强adscs治疗t1dm的效果:
a)分组设置:在实施例1的基础上,选取已发病的糖尿病小鼠进行随机分组:
pbs组:该组小鼠尾静脉注射pbs作为阴性对照组,该组称为pbs组;
adscs组:该组小鼠发病后通过尾静脉注射含1.0×106adscs的pbs悬液100μl,共注射两次,间隔一个周,该组称为adscs组;
adscs+abx组:为了调节肠道菌群,在首次注射adscs的同时,在饮用水中加入广谱抗生素混合剂(abx,氨苄西林(1mg/ml)、甲硝唑(1mg/ml)、新霉素(1mg/ml)和万古霉素(0.5mg/ml))作为肠道菌群调节剂,处理1周,该组称为adscs+abx组;
co-housed组:为了研究肠道菌群在adscs治疗中的作用,我们将接受抗生素处理的adscs+abx组小鼠与未经抗生素处理的adscs组小鼠进行混笼饲养,利用小鼠食粪的属性将adscs组小鼠的肠道菌群重新定植到adscs+abx组小鼠肠道中,改组成为co-housed组。
实施例1-4中采用链脲佐菌素、adscs、广谱抗生素(包括单一组分、同类型抗菌属和混合剂)对nod/ltj小鼠进行分阶段处理的流程示意图请参阅图2a。
b)治疗效果评价:血糖检测结果显示adscs治疗可以有效降低t1dm小鼠血糖,同时adscs+abx组小鼠血糖较单独adscs治疗的小鼠血糖进一步低,而co-housed组小鼠血糖在抗生素喂养期间短暂下降,而在混笼后逐渐上升,接近adscs组小鼠血糖(图2b);he染色和胰岛炎症评分(评分标准参照
实施例4单一组分或同类型抗菌属组合的广谱抗生素无大幅度增强adscs治疗t1dm的效果:
为了探究广谱抗生素混合剂中各组分对于adscs治疗t1dm效果的影响,我们根据四种抗生素作用的细菌类型将其分为三组,其中氨苄西林+万古霉素一组,主要针对革兰氏阳性菌;新霉素一组,主要针对革兰氏阴性菌;甲硝唑一组,主要针对厌氧菌。将上述抗生素溶液分别与adscs联合使用,观测联合使用后小鼠血糖水平变化。具体实施方案如下:
a)分组设置:选取已发病的糖尿病小鼠随机分为以下4组:
adscs组:该组小鼠发病后通过尾静脉注射含1.0×106adscs的pbs悬液100μl,共注射两次,间隔一个周,该组称为adscs组;
adscs+氨苄西林+万古霉素组:为了调节肠道菌群,在首次注射adscs的同时,在饮用水中加入氨苄西林(1mg/ml)和万古霉素(0.5mg/ml)作为肠道菌群调节剂,处理1周,该组称为adscs+氨苄西林+万古霉素组;
adscs+甲硝唑组:为了调节肠道菌群,在首次注射adscs的同时,在饮用水中加入甲硝唑(1mg/ml)作为肠道菌群调节剂,处理1周,该组称为adscs+氨苄西林+万古霉素组;
adscs+新霉素组:为了调节肠道菌群,在首次注射adscs的同时,在饮用水中加入新霉素(1mg/ml)作为肠道菌群调节剂,处理1周,该组称为adscs+氨苄西林+万古霉素组。
b)治疗效果评价:血糖变化结果显示,氨苄西林+万古霉素、新霉素或者甲硝唑分别与adscs联合使用后,小鼠血糖与adscs组相似,并没有进一步下降(图3a)。结合实施例3的结果,说明只有氨苄西林、万古霉素、新霉素和甲硝唑的混合剂可以进一步增强adscs的治疗效果。
实施例5单独使用广谱抗生素混合剂对治疗t1dm效果不明显:
为了排除抗生素混合剂自身对于t1dm小鼠血糖的影响,我们设计了不使用adscs,单独使用广谱抗生素混合剂的abx组,观测小鼠血糖变化,具体实施方案如下:
a)分组设置:选取已发病的糖尿病小鼠进行随机分组:
pbs组:该组小鼠尾静脉注射pbs作为阴性对照组,称为pbs组;
adscs组:该组小鼠发病后通过尾静脉注射含1.0×106adscs的pbs悬液100μl,共注射两次,间隔一个周,该组称为adscs组;
adscs+abx组:为了调节肠道菌群,在首次注射adscs的同时,在饮用水中加入广谱抗生素混合剂(abx,氨苄西林(1mg/ml)、甲硝唑(1mg/ml)、新霉素(1mg/ml)和万古霉素(0.5mg/ml)作为肠道菌群调节剂,处理1周,该组称为adscs+abx组;
abx组:该组小鼠不接受adscs治疗,仅在饮用水中加入广谱抗生素混合剂(abx,氨苄西林(1mg/ml)、甲硝唑(1mg/ml)、新霉素(1mg/ml)和万古霉素(0.5mg/ml))作为肠道菌群调节剂,处理1周,该组称为abx组;
b)治疗效果评价:血糖变化结果显示,不使用adscs单独使用abx处理的小鼠血糖与pbs组没有显著差别,说明单独使用abx处理没有降低血糖的作用(图4a)。结合实施例3、4的结果,说明将adscs与abx联合使用才可以达到更优的治疗效果。
实施例6广谱抗生素混合剂处理改变肠道菌群:
abx的使用会改变肠道菌群的结构和丰度。为了探究abx使用后肠道菌群是如何变化的以及那种细菌的改变可能导致了adscs+abx联合使用后增强的治疗效果,我们收集1周和两周时间点四组小鼠粪便,提取粪便dna进行16srrnareal-timepcr定量检测和16srrna测序。real-time结果显示抗生素处理1w后粪便内菌量显著下降,而在抗生素水撤除1周后,即第二周(2w)时菌量逐渐恢复,与其他几组无统计学差异(图5a)。16srrna测序结果,2w时α和β多样性显示adscs单独处理并没有显著改变菌群结构,而adscs+abx处理后形成了一个独特的菌群(图5b和5c)。差异菌分析结果显示adscs+abx组小鼠粪便中双歧杆菌丰度显著高于adscs组和co-housed组(图5d)。
实施例7短双歧杆菌处理可以增强干细胞治疗效果:
基于上述研究结果,我们拟使用短双歧杆菌(bifidobacterim.breve,b.breve)和adscs同时处理小鼠,观察小鼠血糖变化。经所述方式处理的小鼠命名为adscs+b.breve组,其中b.breve(1.3001)购自中国普通微生物菌种保藏管理中心,使用mrs培养基(含0.05%半胱氨酸)在厌氧环境下37℃培养。使用1.0×109的b.breve对第一次adscs治疗后的小鼠进行灌胃处理1周。在2周时间点收集小鼠粪便,提取粪便dna,通过real-timepcr和水平凝胶电泳检测确认b.breve在小鼠肠道成功定植(图6a)。
结果显示adscs+b.breve组小鼠血糖显著低于adscs组,与adscs+abx组血糖相似(图6b)。胰腺组织he染色及胰岛炎症评分结果显示adscs+b.breve处理后小鼠胰岛炎症评分>75%的胰岛比例较adscs组减少(图6c),而胰岛素染色结果也表明abx/b.breve处理后胰岛β细胞染色较adscs组强(图6d)。这一结果说明adscs+abx处理后双歧杆菌比例的增加是adscs治疗效果增强的原因,而b.breve灌胃处理可以进一步增强adscs治疗t1dm的治疗效果,。
实施例8广谱抗生素混合剂/b.breve处理可以降低肠道通透性:
t1dm病人以及动物模型多伴随肠道通透性的增加。通过使用异硫氰酸荧光素标记的葡聚糖(fitc-dextran,4kd)灌胃检测肠道通透性,结果显示,adscs+abx组小鼠和adscs+b.breve组血清fitc-dextran荧光强度最低,表明相较于单独adscs治疗的小鼠adscs+abx/b.breve处理降低了肠道通透性(图7a)。血清内毒素检测显示了同样的结果,即adscs+abx/b.breve组小鼠血清内毒素水平较adscs组低(图7b)。再次说明adscs+abx/b.breve处理降低了小鼠肠道通透性。阿利新蓝染色结果也显示adscs+abx/b.breve处理后小鼠肠道粘液层增厚(图7c)。上述说明adscs+abx/b.breve处理通过增厚结肠粘液层,降低了小鼠肠道通透性。
实施例9广谱抗生素混合剂/b.breve处理可以减少肠道菌群在胰腺的异位定植,增加胰岛素的转录:
肠道通透性增加时肠道内的细菌会通过肠道屏障侵入包括胰腺在内的远端脏器,因此,肠道通透性的改变与远端脏器功能密切相关。为了检测肠道菌群在胰腺异位定植的改变,我们进行了real-timepcr定量检测和细菌通用探针eub338染色。real-timepcr定量检测结果(图8a)和细菌通用探针eub338染色结果(图8b)都显示adscs+abx/b.breve胰腺中细菌数量较adscs组减少。mafa是β细胞胰岛素基因的重要转录因子,mafa免疫组化染色结果表明adscs+abx/b.breve组小鼠阳性细胞数多于adscs组(图8c),这与图6d中胰岛素的染色结果一致。
综上所述,在adscs治疗的同时给予广谱抗生素混合剂或者益生菌b.breve处理均可以增强adscs降低血糖、减轻胰岛炎症的治疗效果。abx/b.breve的处理通过降低肠道通透性,减少肠道菌群在胰腺的异位定植,进而增强胰岛素的转录和表达,最终进一步增强了adscs治疗t1dm的效果。
由此可以看出,本发明针对间充质干细胞在治疗i型糖尿病临床应用中存在的治疗效果不佳的问题,通过使用广谱抗生素或双歧杆菌调节肠道菌群,进而增强了人脂肪间充质干细胞治疗一型糖尿病的效果。该发明为强调了肠道菌群在间充质干细胞治疗i型糖尿病过程中的重要作用,也为间充质干细胞治疗i型糖尿病的临床转化应用奠定了基础。
鉴于可以应用所公开的发明的原理的许多可能的实施例,应当认识到,所示的实施例仅是本发明的优选示例,而不应视为限制本发明的范围。相反,本发明的范围由所附权利要求书限定。因此,我们要求保护所有落入这些权利要求的范围和精神内的发明。
- 还没有人留言评论。精彩留言会获得点赞!