一种复合佐剂及使用该复合佐剂的新冠COVID-19重组蛋白疫苗的制作方法
dna作为一种危险刺激信号进行识别,进而刺激机体产生免疫保护反应。
9.本发明所述铝佐剂选自氢氧化铝和磷酸铝,优选为氢氧化铝。从免疫应答机理上来讲,铝佐剂的免疫应答偏向于t辅助细胞2型(th2)应答,其特征是th2型细胞因子,例如il-4和il-5的分泌以及igg1和ige型抗体的产生。研究表明氢氧化铝佐剂可以激活th2细胞分泌il-4,并诱导mhc-ii类分子和cd83,cd86等的表达,最终可诱导型体液免疫应答,但单细胞毒性t淋巴细胞(ctl)应答微弱或者不存在。而cpg odn能够促进树突状细胞、巨噬细胞以及b细胞的成熟和活化,上调cd80、cd86、cd40和mhc
-ⅱ
分子的表达,促进il-6、il-12、ifn-γ等thl型细胞因子的分泌,诱导机体产生thl型免疫反应。此外,cpg odn经内吞作用摄入免疫细胞后,被细胞中内体/溶酶体上的tlr9识别并与其结合,导致tlr9二聚体化,最终促使相关免疫细胞分泌一系列的细胞因子及趋化因子,触发胞内的杀菌机制或诱发炎症反应,产生强ctl诱导效应。
10.本发明将传统铝佐剂与cpg寡聚脱氧核苷酸结合使用,可以实现在免疫机理上的互补,同时激发细胞免疫和体液免疫,产生更强的免疫效果。通过平衡th1型和th2型免疫应答,从而降低发生ade风险。
11.作为本发明的优选方案,所述cpg寡聚脱氧核苷酸中含有至少2个cpg单元,其链长至少为20bp,且所述cpg寡聚脱氧核苷酸中所有核苷酸均为硫代修饰。
12.作为本发明的优选方案,所述cpg寡聚脱氧核苷酸的序列选自:
13.seq7:5
’-
tgactgtgaacgttcgagatga-3’;或
14.seq8:5
’-
tcgacgttcgtcgttcgtcgttc-3’;或
15.seq9:5’tcgtcgttttgtcgttttgtcgtt-3’。
16.作为本发明的优选方案,所述cpg寡聚脱氧核苷酸与铝佐剂的质量比为1:(0.01~1)。进一步优选地,所述cpg寡聚脱氧核苷酸与铝佐剂的质量比为1:(0.06~0.09)、1:(0.1~0.15)、1:(0.2~0.5)或1:(0.6~0.9)。具体而言,所述cpg寡聚脱氧核苷酸与铝佐剂的质量比可以为1:0.06、1:0.09、1:0.1、1:0.15、1:0.2、1:0.5、1:0.6或1:0.9。本发明通过对cpg寡聚脱氧核苷酸与铝佐剂的结合配比方案进行研究,确定了上述最高效的复合佐剂配比方案,以确保复合佐剂可产生强烈的免疫增强作用。
17.本发明的第二目的是提供所述复合佐剂作为疫苗的免疫增强剂或免疫佐剂的应用,或者在提高疫苗的抗原或疫苗的免疫原性中的应用。
18.作为本发明的优选方案,所述疫苗为新冠covid-19重组蛋白疫苗。将所述复合佐剂用作新冠covid-19重组蛋白疫苗的佐剂,可以更好的激发细胞免疫,产生更强的免疫效果。该方案制备方法简单,质量易于控制,易于规模化生产。可用于有效预防和治疗新型冠状病毒covid-19感染引起的肺炎,甚至是严重呼吸道感染。为在我国乃至全世界范围内的疾病的防控提供了技术保障。
19.本发明的第三目的是提供使用所述复合佐剂的疫苗。本发明提供的疫苗中由于采用了所述复合佐剂,可以达到增强免疫效果,延长免疫时间,减少抗原用量的效果。
20.作为本发明的优选方案,所述疫苗中,所述复合佐剂的剂量为0.3mg/剂~6mg/剂。
21.作为本发明的优选方案,所述疫苗中,抗原的含量为1μg/剂~80μg/剂。
22.本发明的第四目的是提供使用所述复合佐剂的新冠covid-19重组蛋白疫苗。本发明提供的新冠covid-19重组蛋白疫苗中由于采用了所述复合佐剂,可以达到增强免疫效
果,延长免疫时间,减少抗原用量的效果。
23.作为本发明的优选方案,所述新冠covid-19重组蛋白疫苗的抗原包含covid-19的s蛋白的受体结合结构域和igg的fc片段;或者,包含s蛋白的ace2受体结合结构域和/或表面抗原决定簇,所述s蛋白为sars的s蛋白或covid-19的s蛋白。
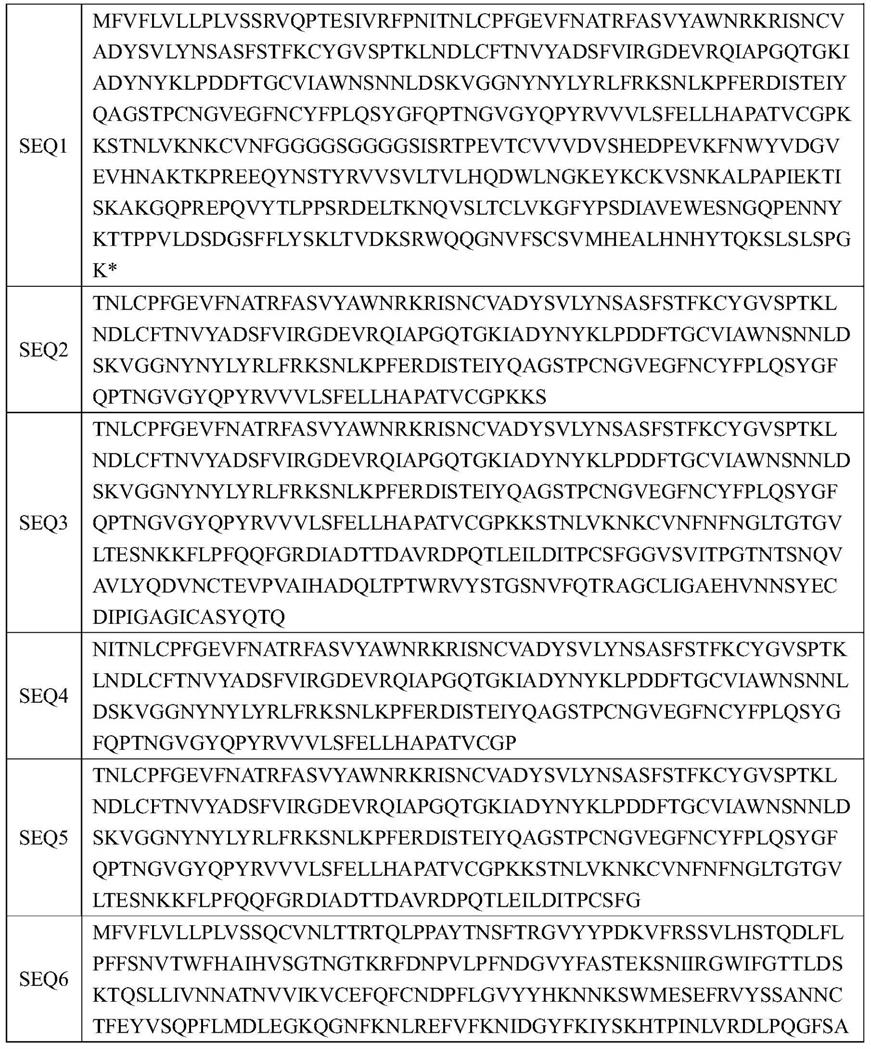
24.作为本发明的优选方案,所述疫苗的抗原具有seq1、seq2、seq3、seq4、seq5和seq6中的一个或多个氨基酸序列,或与其相似度为90%以上的氨基酸序列。本发明优选的seq1氨基酸序列编码了一种融合蛋白,该融合蛋白包含covid-19的s蛋白的受体结合结构域和igg的fc片段。本发明优选的seq2、seq3、seq4、seq5和seq6氨基酸序列是2003sars-cov和covid-19各自的s蛋白的氨基酸序列中保守性较高的序列。这些序列虽然长短不一,但是覆盖了spike蛋白与ace2受体结合的部位以及主要的蛋白表面抗原决定簇。
25.上述氨基酸序列参见本发明的序列表,具体如下表1所示。
26.表1:目的氨基酸序列
27.[0028][0029]
作为本发明的优选方案,所述新冠covid-19重组蛋白疫苗中,所述复合佐剂的剂量为0.3mg/剂~6mg/剂。具体而言,所述重组蛋白疫苗中所述复合佐剂的含量可以为0.8mg/剂,0.95mg/剂,3.3mg/剂,3.45mg/剂,5.3mg/剂,或5.45mg/剂。
[0030]
作为本发明的优选方案,所述新冠covid-19重组蛋白疫苗中含有0.25~5mg/剂的cpg寡聚脱氧核苷酸佐剂。具体而言,所述重组蛋白疫苗中cpg寡聚脱氧核苷酸佐剂的含量可以为0.25mg/剂,0.5mg/剂,1mg/剂,3mg/剂,2mg/剂或5mg/剂。
[0031]
作为本发明的优选方案,所述新冠covid-19重组蛋白疫苗中含有0.10~0.45mg/剂的氢氧化铝佐剂。具体而言,所述重组蛋白疫苗中氢氧化铝佐剂的含量可以为0.15mg/剂,0.3mg/剂或0.45mg/剂。
[0032]
作为本发明的优选方案,所述新冠covid-19重组蛋白疫苗中,抗原的含量为1μg/剂~80μg/剂,优选为20μg/剂~40μg/剂。具体而言,所述重组疫苗中抗原的含量可以为2.5μg/剂,10μg/剂,20μg/剂,40μg/剂或80μg/剂。
[0033]
作为本发明的优选方案,所述新冠covid-19重组蛋白疫苗为液体制剂,可以采用多种剂型形式。具体而言,所述重组蛋白疫苗可以是肌肉内液体注射剂、静脉内液体注射剂、鼻腔内液体注射剂、皮内液体注射剂或皮下液体注射剂。在实际应用时,可以根据转染效率、局部免疫监视等临床需要进行调整和选择,如选择单一的剂型进行注射免疫,或者选择多种混合剂型进行注射免疫。
[0034]
本发明的第五目的是提供使用所述复合佐剂的新冠covid-19重组蛋白疫苗在制备用于预防和/或治疗covid-19感染引起的疾病的药物中的应用。所述疾病优选为肺炎及综合征,严重急性呼吸道感染,肠道疾病,心脏衰竭,肾衰竭或严重急性呼吸道综合征。
[0035]
本发明提供的使用所述复合佐剂的新冠covid-19重组蛋白疫苗,能够有效诱导机体产生细胞免疫和体液免疫,并且可以快速制备,适用于新型冠状病毒covid-19的疫情的控制。
附图说明
[0036]
图1为不同cpg佐剂与氢氧化铝佐剂配比方案的covid-19重组疫苗免疫balb/c小鼠的血清igg效价示意图。
[0037]
图2为血清中特异性表达s蛋白细胞因子的结果示意图。
具体实施方式
[0038]
以下实施例用于说明本发明,但不用来限制本发明的范围。
[0039]
以下各实施例以及对比例2中,cpg寡聚脱氧核苷酸(佐剂)的序列为5
’-
tgactgtgaacgttcgagatga-3’。
[0040]
以下各实施例以及对比例中,疫苗抗原具有如seq6所示的序列。
[0041]
实施例1
[0042]
本实施例提供了一种由cpg寡聚脱氧核苷酸与氢氧化铝组成的复合佐剂;其中,cpg寡聚脱氧核苷酸与氢氧化铝的质量比为1:0.6。
[0043]
本实施例进一步提供了一种使用所述复合佐剂和新型冠状病毒covid-19重组疫苗的组合方式。
[0044]
具体为:将cpg寡聚脱氧核苷酸佐剂和氢氧化铝佐剂加入经0.22μm滤膜过滤的疫苗原液,使cpg佐剂浓度为0.5mg/剂,氢氧化铝佐剂含量为0.3mg/剂,疫苗抗原含量20μg/剂。将本实施例所得疫苗编号记为20200401。
[0045]
实施例2
[0046]
本实施例提供了一种由cpg寡聚脱氧核苷酸与氢氧化铝组成的复合佐剂;其中,cpg寡聚脱氧核苷酸与氢氧化铝的质量比为1:0.6。
[0047]
本实施例进一步提供了一种使用所述复合佐剂和新型冠状病毒covid-19重组疫苗的组合方式。
[0048]
具体为:将cpg寡聚脱氧核苷酸佐剂和氢氧化铝佐剂加入经0.22μm滤膜过滤的疫苗原液,使cpg佐剂浓度为0.5mg/剂,氢氧化铝佐剂含量为0.3mg/剂,疫苗抗原含量40μg/剂。将本实施例所得疫苗编号记为20200402。
[0049]
实施例3
[0050]
本实施例提供了一种由cpg寡聚脱氧核苷酸与氢氧化铝组成的复合佐剂;其中,cpg寡聚脱氧核苷酸与氢氧化铝的质量比为1:0.9。
[0051]
本实施例进一步提供了一种使用所述复合佐剂和新型冠状病毒covid-19重组疫苗的组合方式。
[0052]
具体为:将cpg寡聚脱氧核苷酸佐剂和氢氧化铝佐剂加入经0.22μm滤膜过滤的疫苗原液,使cpg佐剂浓度为0.5mg/剂,氢氧化铝佐剂含量为0.45mg/剂,疫苗抗原含量20μg/剂。将本实施例所得疫苗编号记为20200403。
[0053]
实施例4
[0054]
本实施例提供了一种由cpg寡聚脱氧核苷酸与氢氧化铝组成的复合佐剂;其中,cpg寡聚脱氧核苷酸与氢氧化铝的质量比为1:0.9。
[0055]
本实施例进一步提供了一种使用所述复合佐剂和新型冠状病毒covid-19重组疫苗的组合方式。
[0056]
具体为:将cpg寡聚脱氧核苷酸佐剂和氢氧化铝佐剂加入经0.22μm滤膜过滤的疫苗原液,使cpg佐剂浓度为0.5mg/剂,氢氧化铝佐剂含量为0.45mg/剂,疫苗抗原含量40μg/剂。将本实施例所得疫苗编号记为20200404。
[0057]
实施例5
[0058]
本实施例提供了一种由cpg寡聚脱氧核苷酸与氢氧化铝组成的复合佐剂;其中,cpg寡聚脱氧核苷酸与氢氧化铝的质量比为1:0.1。
[0059]
本实施例进一步提供了一种使用所述复合佐剂和新型冠状病毒covid-19重组疫苗的组合方式。
[0060]
具体为:将cpg寡聚脱氧核苷酸佐剂和氢氧化铝佐剂加入经0.22μm滤膜过滤的疫苗原液,使cpg佐剂浓度为3mg/剂,氢氧化铝佐剂含量为0.3mg/剂,疫苗抗原含量20μg/剂。将本实施例所得疫苗编号记为20200405。
[0061]
实施例6
[0062]
本实施例提供了一种由cpg寡聚脱氧核苷酸与氢氧化铝组成的复合佐剂;其中,cpg寡聚脱氧核苷酸与氢氧化铝的质量比为1:0.1。
[0063]
本实施例进一步提供了一种使用所述复合佐剂和新型冠状病毒covid-19重组疫苗的组合方式。
[0064]
具体为:将cpg寡聚脱氧核苷酸佐剂和氢氧化铝佐剂加入经0.22μm滤膜过滤的疫苗原液,使cpg佐剂浓度为3mg/剂,氢氧化铝佐剂含量为0.3mg/剂,疫苗抗原含量40μg/剂。将本实施例所得疫苗编号记为20200406。
[0065]
实施例7
[0066]
本实施例提供了一种由cpg寡聚脱氧核苷酸与氢氧化铝组成的复合佐剂;其中,cpg寡聚脱氧核苷酸与氢氧化铝的质量比为1:0.15。
[0067]
本实施例进一步提供了一种使用所述复合佐剂和新型冠状病毒covid-19重组疫苗的组合方式。
[0068]
具体为:将cpg寡聚脱氧核苷酸佐剂和氢氧化铝佐剂加入经0.22μm滤膜过滤的疫苗原液,使cpg佐剂浓度为3mg/剂,氢氧化铝佐剂含量为0.45mg/剂,疫苗抗原含量20μg/剂。将本实施例所得疫苗编号记为20200407。
[0069]
实施例8
[0070]
本实施例提供了一种由cpg寡聚脱氧核苷酸与氢氧化铝组成的复合佐剂;其中,cpg寡聚脱氧核苷酸与氢氧化铝的质量比为1:0.15。
[0071]
本实施例进一步提供了一种使用所述复合佐剂和新型冠状病毒covid-19重组疫苗的组合方式。
[0072]
具体为:将cpg寡聚脱氧核苷酸佐剂和氢氧化铝佐剂加入经0.22μm滤膜过滤的疫苗原液,使cpg佐剂浓度为3mg/剂,氢氧化铝佐剂含量为0.45mg/剂,疫苗抗原含量40μg/剂。将本实施例所得疫苗编号记为20200408。
[0073]
实施例9
[0074]
本实施例提供了一种由cpg寡聚脱氧核苷酸与氢氧化铝组成的复合佐剂;其中,cpg寡聚脱氧核苷酸与氢氧化铝的质量比为1:0.06。
[0075]
本实施例进一步提供了一种使用所述复合佐剂和新型冠状病毒covid-19重组疫
苗的组合方式。
[0076]
具体为:将cpg寡聚脱氧核苷酸佐剂和氢氧化铝佐剂加入经0.22μm滤膜过滤的疫苗原液,使cpg佐剂浓度为5mg/剂,氢氧化铝佐剂含量为0.3mg/剂,疫苗抗原含量20μg/剂。将本实施例所得疫苗编号记为20200409。
[0077]
实施例10
[0078]
本实施例提供了一种由cpg寡聚脱氧核苷酸与氢氧化铝组成的复合佐剂;其中,cpg寡聚脱氧核苷酸与氢氧化铝的质量比为1:0.06。
[0079]
本实施例进一步提供了一种使用所述复合佐剂和新型冠状病毒covid-19重组疫苗的组合方式。
[0080]
具体为:将cpg寡聚脱氧核苷酸佐剂和氢氧化铝佐剂加入经0.22μm滤膜过滤的疫苗原液,使cpg佐剂浓度为5mg/剂,氢氧化铝佐剂含量为0.3mg/剂,疫苗抗原含量40μg/剂。将本实施例所得疫苗编号记为20200410。
[0081]
实施例11
[0082]
本实施例提供了一种由cpg寡聚脱氧核苷酸与氢氧化铝组成的复合佐剂;其中,cpg寡聚脱氧核苷酸与氢氧化铝的质量比为1:0.09。
[0083]
本实施例进一步提供了一种使用所述复合佐剂和新型冠状病毒covid-19重组疫苗的组合方式。
[0084]
具体为:将cpg寡聚脱氧核苷酸佐剂和氢氧化铝佐剂加入经0.22μm滤膜过滤的疫苗原液,使cpg佐剂浓度为5mg/剂,氢氧化铝佐剂含量为0.45mg/剂,疫苗抗原含量20μg/剂。将本实施例所得疫苗编号记为20200411。
[0085]
实施例12
[0086]
本实施例提供了一种由cpg寡聚脱氧核苷酸与氢氧化铝组成的复合佐剂;其中,cpg寡聚脱氧核苷酸与氢氧化铝的质量比为1:0.09。
[0087]
本实施例进一步提供了一种使用所述复合佐剂和新型冠状病毒covid-19重组疫苗的组合方式。
[0088]
具体为:将cpg寡聚脱氧核苷酸佐剂和氢氧化铝佐剂加入经0.22μm滤膜过滤的疫苗原液,使cpg佐剂浓度为5mg/剂,氢氧化铝佐剂含量为0.45mg/剂,疫苗抗原含量40μg/剂。将本实施例所得疫苗编号记为20200412。
[0089]
对比例1
[0090]
本对比例提供了一种使用氢氧化铝佐剂和新型冠状病毒covid-19重组疫苗的组合方式。
[0091]
具体为:将氢氧化铝佐剂加入经0.22μm滤膜过滤的疫苗原液,使氢氧化铝佐剂含量为0.45mg/剂,疫苗抗原含量20μg/剂。将本对比例所得疫苗编号记为20200413。
[0092]
对比例2
[0093]
本对比例提供了一种使用cpg寡聚脱氧核苷酸佐剂和新型冠状病毒covid-19重组疫苗的组合方式。
[0094]
具体为:将cpg寡聚脱氧核苷酸佐剂加入经0.22μm滤膜过滤的疫苗原液,使cpg佐剂浓度为5mg/剂,疫苗抗原含量20μg/剂。将本对比例所得疫苗编号记为20200414。
[0095]
实验例1:佐剂效果在小鼠模型上的免疫学评价
[0096]
1、中和抗体效价测定
[0097]
将各实施例和对比例提供的共14组疫苗分别用生理盐水做1:4、1:16、1:64稀释,使用1ml注射器,接种balb/c小鼠,每组10只,按照0,7天免疫,每只腹腔注射一个剂量,第1次免疫后4周采血,检测中和抗体。中和抗体效价gmt大于8的视为阳性,视为有保护效果。结果如表2所示。
[0098]
表2:covid-19重组疫苗免疫balb/c小鼠的中和效价
[0099][0100][0101]
结果显示,上述不同有效成分和佐剂含量的covid-19疫苗免疫balb/c小鼠,均能产生足够高的中和抗体效价。佐剂含量高的疫苗免疫原性相对高于含量低的同样有效成份的疫苗。本发明提供疫苗均能诱导balb/c小鼠产生有保护能力的中和抗体。
[0102]
2、igg抗体效价测定
[0103]
将各实施例和对比例提供的共14组疫苗进行igg抗体效价测定。igg抗体效价检测方法如下:
[0104]
将新冠病毒按蛋白浓度1μg/ml 100μl/孔,包被于酶标板,2-8℃包被过夜或37℃包被2小时以上,洗板拍干,采用含1%bsa或10%小牛血清的0.01m pbs进行封闭,200μl/孔封闭,37℃封闭1-2小时,甩去其中液体,排干待用。将待检样品及阴性血清对照采用上述封闭液系列稀释,100μl每孔加入封闭后的酶标板,37℃孵育60-70分钟,洗板拍干;加入对应抗种属的hrp酶标抗体,37℃孵育45-60分钟,洗板拍干;加入显色a/b液各50μl,37℃显色10-15分钟后,加入2m h2so4终止。结果分析:样品od值≥阴性血清相同稀释倍数下od值的2.1倍时的最高稀释倍数即为样品的igg抗体效价。若阴性对照od值小于0.05,则按0.05计算。
[0105]
结果如图1所示。图1所示的柱状图中,每一组疫苗对应的igg抗体效价结果由左右两栏组成,其中左侧栏代表7天(7d),右侧栏代表14天(14d)。
[0106]
实验例2:细胞因子检测
[0107]
将各实施例和对比例提供的共14组疫苗按照0、7天免疫,28天采血的程序分别免疫balb/c小鼠,采集细胞上清进行细胞免疫检测。采用细胞内细胞因子染色法和流式细胞法检测血清中特异性表达s蛋白细胞因子的cd4+t细胞。
[0108]
1、脾淋巴细胞的分离
[0109]
颈椎脱臼处死小鼠,于70%酒精浸泡约3min。将小鼠于生物安全柜内无菌取出脾脏,放到置于无菌平皿中的200目细胞筛上。加入10ml rpmi1640完全培养基,用注射器活塞将脾轻柔地研磨成单个细胞,再用10ml rpmi1640完全培养基冲洗细胞筛,以获得更多的脾细胞。将脾细胞悬液转移至50ml离心管中,500g水平离心5min。弃上清,细胞用3m|1
×
红细胞裂解液重悬,室温裂解5min,加入27ml rpmi1640完全培养基,500g水平离心5min。弃上清,细胞再用20ml rpmi1640完全培养基清洗一次,用适量培养基重悬,经200目细胞筛过滤至10ml试管中,取50μl稀释20倍后进行计数,待用。
[0110]
2、小鼠脾细胞的体外刺激
[0111]
将以上分离的小鼠脾细胞取适量稀释至4
×
106cells/ml,每孔0.5ml加入到24孔板中。每只小鼠分别设置特异ctl表位刺激孔和无刺激孔。特异表位浓度为每条肽2μg/ml,无刺激加入等量的dmso。作为阳性对照,加入pma和ionomycin刺激孔,其中pma浓度为100ng/ml,ionomycin浓度为1μg/ml。同时每孔加入1μl brilliant violet 421tm anti-mouse cd107a。细胞于37℃、5%co2细胞培养箱中培养1小时后,每孔各加入适量的golgistop和(或)golgiplug作为细胞因子分泌的阻断剂。总共培养6小时后进行相关抗原的染色,用于细胞内细胞因子的流式细胞术检测。
[0112]
3、细胞表面抗原和细胞内细胞因子染色
[0113]
脾细胞经体外刺激6小时后,转移至流式管中,4℃,500g离心5分钟,弃上清。用pbs+2%fbs按说明书推荐的使用量先稀释好适量的荧光标记抗体percp/cy5.5-conjugated anti-cd3(clone 145-2c11)和fitc conjugated anti-cd8(clone 53-6.7),每管加入50μl,轻轻混匀,4℃放置30分钟。30分钟后,每管加入3ml pbs+2%fbs,4℃,500g离心5分钟,弃上清。每管加入200μl cytofix/cytopermtm fixation and permeabilizaiton solution,
于4℃放置20分钟,对细胞进行固定和穿孔。20分钟后,每管加入1ml1
×
perm/washtm buffer,4℃,600g离心5分钟,弃上清。用1
×
perm/washtm buffer按说明书推荐使用量先稀释好适量的pe conjugated anti-ifn-γ(clone xmg1.2)抗体,每管加50μl,轻轻混匀,于4℃放置30分钟。最后,每管分别用1ml1
×
perm/washtm buffer和3ml的pbs各洗一次,弃上清后用200μl pbs重悬,上机检测。为了在检测时调节各染料间的荧光补偿,设置不染色管、单染percp/cy5.5-conjugated anti-cd3管、单染fitc conjugated anti-cd8管和单染peconjugated anti-ifn-γ管,其中pe conjugated anti-ifn-γ单染管使用的是阳性刺激的细胞。
[0114]
4、流式细胞术检测
[0115]
使用bd facs cantotm进行流式细胞术检测。首先各通道调节合适的电压,使用单荧光染色样品调节各染料间的荧光补偿,然后依次上样,收集数据。
[0116]
5、细胞内细胞因子染色流式细胞术检测结果
[0117]
细胞内细胞因子染色流式细胞术检测结果如图2所示。由本实验例的结果可知,新型冠状病毒covid-19重组蛋白疫苗可诱导提高血清抗体水平。而使用复合佐剂的新冠疫苗免疫小鼠可产生高水平的特异性抗体,免疫效果明显强于单独使用氢氧化铝佐剂和cpg寡聚脱氧核苷酸的对照疫苗。本实验显示了复合佐剂在新型冠状病毒covid-19重组蛋白疫苗中的良好作用。
[0118]
虽然,上文中已经用一般性说明、具体实施方式及试验,对本发明作了详尽的描述,但在本发明基础上,可以对之作一些修改或改进,这对本领域技术人员而言是显而易见的。因此,在不偏离本发明精神的基础上所做的这些修改或改进,均属于本发明要求保护的范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1