高浓度胰岛素制剂的制作方法
高浓度胰岛素制剂
发明领域
1.本发明涉及酰化胰岛素的药物组合物的领域,以及使用这样的组合物治疗疾病的方法。本发明还涉及制备这样的药物组合物的领域。
2.发明背景
3.目前,1型糖尿病和2型糖尿病的治疗越来越依赖于所谓的强化胰岛素治疗。根据该方案,患者每日接受多次胰岛素注射治疗,包括每日注射一次或两次长效胰岛素来满足基础胰岛素需求,并辅以速效胰岛素的餐时(bolus)注射来满足与膳食相关的胰岛素需求。
4.长效胰岛素组合物是本领域公知的。相应地,长效胰岛素组合物的一种主要类型包括胰岛素晶体或无定形胰岛素的可注射水性悬浮液。在这些组合物中,所用的胰岛素化合物通常是鱼精蛋白胰岛素、锌胰岛素或鱼精蛋白锌胰岛素。其他长效胰岛素组合物有例如和与人胰岛素相比,它们具有延长的作用谱。
5.结晶胰岛素,无论是注射时鱼精蛋白结晶还是注射时胰岛素组合物结晶,都具有许多缺点,如潜在的免疫原性反应、均一性、组织刺激和反应等。
6.另一类长效胰岛素组合物是ph值低于生理ph的溶液,由于该溶液注射时ph值升高,胰岛素将从该溶液中沉淀出来。这些溶液的一个缺点是,注射时在组织中形成的沉淀物的颗粒大小分布——因而药物的释放谱——以某种不可预测的方式取决于注射部位的血流量和其他参数。另一个缺点是,胰岛素的固体颗粒可能充当局部刺激物,从而导致注射部位的组织发炎。
7.胰岛素是在胰腺朗格汉斯岛中产生的一种51个氨基酸的肽激素。作为单体,其主要功能是通过结合并激活跨膜受体来促进葡萄糖分子跨脂肪和肌肉组织的细胞膜的转运。
8.胰岛素的独特性质是它能够缔合成六聚体,以这种形式,该激素在生物合成和储存过程中免遭化学和物理降解。对胰岛素的x射线晶体学研究表明,该六聚体由通过三重旋转轴关联的三个二聚体组成。这些二聚体通过位于三重轴上的其核心处的两个锌离子的相互作用而紧密缔合。
9.当以高浓度药物制剂的形式注射到皮下组织中时,人胰岛素是自缔合的,此时解离成单体的速度相对较慢。胰岛素的六聚体和二聚体穿透毛细血管壁的速度比单体更慢。
10.锌和酚类添加剂经常在治疗性胰岛素制剂中用于促进六聚体的形成,从而防止储存过程中发生降解。然而,在这种形式下,在六聚体通过皮下组织扩散并解离成二聚体和单体的同时,所注射的胰岛素的作用延迟。
11.胰岛素制剂的强度以单位(u)表示,其中一单位对应于0.035mg人胰岛素。因此,100u/ml的人胰岛素制剂具有浓度为3.5mg/ml的人胰岛素。德谷胰岛素(nεb29-十六烷二酰基-γ-glu-(desb30)人胰岛素)可作为100u/ml产品和200u/ml产品商购获得。
12.胰岛素制剂通常如下制备:在酸性条件下将胰岛素溶解在少量水中。然后将锌添加到制剂中,随后进行中和并添加防腐剂,如苯酚和间甲酚。然而,浓缩胰岛素制剂在储存和使用时往往不稳定,同样重要的是,pk谱随胰岛素浓度而变化。
13.wo2008/132224公开了包含喷雾干燥胰岛素的药物组合物,用于制备用于治疗糖
尿病的高浓度胰岛素溶液。
14.wo2007/074133公开了包含德谷胰岛素的药物组合物。
15.具有在储存和使用期间稳定的浓缩胰岛素制剂是有利的。这样的浓缩制剂降低了需要更换一次性注射笔的频率以及更换耐用注射装置中的药筒的频率。此外,在许多情况下,注射装置的实质性开发需要高度浓缩的胰岛素组合物。
16.当胰岛素制剂中的胰岛素浓度增加时,药代动力学谱通常会发生改变。更具体地,对于给定剂量的胰岛素,当制剂中的胰岛素浓度增加时,cmax和auc(生物利用度)趋于降低。对于通常会加入需要不同胰岛素浓度的不同给药装置中的胰岛素产品来说,按比例缩放胰岛素浓度时药代动力学性质的变化是一个挑战。
17.本发明涉及nεb29-十六烷二酰基-γ-glu-(desb30)人胰岛素的某些药物组合物,其解决了现有技术的问题。
技术实现要素:
18.令人惊讶地发现,可以制备出pk谱与相应的常规u200产品基本相似,同时在储存和使用过程中仍保持稳定的高浓度可溶性胰岛素制剂。
19.因此,在第一方面,本发明提供了可溶性胰岛素制剂,其包含:
20.·
浓度为1800nmol/ml至4200nmol/ml的nεb29-十六烷二酰基-γ-glu-(desb30)人胰岛素,
21.·
浓度为4.0zn/6ins至7.0zn/6ins的锌离子,
22.·
浓度为110mm至220mm的烟酰胺或浓度为0.02μg/ml至1μg/ml的曲前列环素(treprostinil),
23.·
浓度为6mm至40mm的柠檬酸盐,且ph在7.0至8.0的范围内。
24.在本发明的第一实施方案中,所述锌离子的浓度为5.0zn/6ins至5.5zn/6ins。
25.在本发明的另一实施方案中,所述锌离子的浓度为5.0zn/6ins至6.0zn/6ins。
26.在另一实施方案中,可溶性胰岛素制剂包含浓度为110mm至220mm的烟酰胺。
27.在另一实施方案中,可溶性胰岛素制剂的ph在7.4至7.8的范围内。
28.在另一实施方案中,可溶性胰岛素制剂进一步包含酚类防腐剂或酚类防腐剂混合物。
29.在另一实施方案中,所述酚类防腐剂或酚类防腐剂混合物是苯酚与间甲酚的混合物。
30.在另一方面,本发明提供了降低哺乳动物的血糖水平的方法,该方法是通过向需要这样的治疗的受试者施用治疗有效剂量的根据本发明的可溶性胰岛素制剂。
31.采用本发明,糖尿病患者能够在nεb29-十六烷二酰基-γ-glu-(desb30)人胰岛素的例如u200制剂与u500制剂之间切换,而无需调整剂量。
32.另外,需要极高剂量例如超过160u/日的基础胰岛素的个体现在能够通过单次每日剂量实现这一目标。
33.此外,由于典型的胰岛素笔或药筒通常容纳3ml,因此单个笔或药筒中的胰岛素将远远超过600u,例如对于u500产品为1500u,这意味着笔或药筒需要更换的频率降低。另外,当笔或药筒快用完时,个人不必像往常一样分割剂量。
附图说明
34.图1a.用测试制剂a-h的数据获得的德谷胰岛素的72小时pk谱(平均值)。
35.图1b.用测试制剂a-h的数据获得的德谷胰岛素的24小时pk谱(平均值
±
sem)。
36.图2.用测试制剂a、b、f、g和h的数据获得的德谷胰岛素的24小时pk谱。
37.图3.用测试制剂1-8的数据获得的德谷胰岛素的72小时pk谱(平均值)。
38.图4.用测试制剂1、2、6和7的数据获得的德谷胰岛素的24小时pk谱(平均值
±
sem)。
具体实施方式
39.在第一方面,本发明提供了可溶性胰岛素制剂,其包含:
40.·
浓度为1800nmol/ml至4200nmol/ml的nεb29-十六烷二酰基-γ-glu-(desb30)人胰岛素,
41.·
浓度为4.0zn/6ins至7.0zn/6ins的锌离子,
42.·
浓度为110mm至220mm的烟酰胺或浓度为0.02μg/ml至1μg/ml的曲前列环素,
43.·
浓度为6mm至40mm的柠檬酸盐,且
44.ph在7.0至8.0的范围内。
45.在另一方面,本发明涉及可溶性胰岛素制剂,其包含:
46.·
浓度为3000nmol/ml的nεb29-十六烷二酰基
[0047]-γ-glu-(desb30)人胰岛素,
[0048]
·
浓度为5.5zn/6ins的锌离子,
[0049]
·
浓度为211mm的烟酰胺,
[0050]
·
浓度为6mm的柠檬酸盐,且ph为7.6。
[0051]
在另一方面,本发明涉及可溶性胰岛素制剂,其包含:
[0052]
·
浓度为3000nmol/ml的nεb29-十六烷二酰基
[0053]-γ-glu-(desb30)人胰岛素,
[0054]
·
浓度为5.5zn/6ins的锌离子,
[0055]
·
浓度为161mm的烟酰胺,
[0056]
·
浓度为20mm的柠檬酸盐,且ph为7.6。
[0057]
对于胰岛素制剂,胰岛素的浓度通常以每毫升的单位数即u/ml给出。对于nεb29-十六烷二酰基-γ-glu-(desb30)人胰岛素,100单位(100u)相当于3.66mg或600nmol的nεb29-十六烷二酰基-γ-glu-(desb30)人。
[0058]
对于包含锌的胰岛素制剂来说,通常相对于以六聚体计算的胰岛素浓度(即胰岛素浓度除以6)来陈述锌浓度。该摩尔比被称为“zn/6ins”,即描述锌相对于六分之一胰岛素浓度的相对摩尔浓度。
[0059]
当胰岛素制剂中的胰岛素浓度增加时,药代动力学谱通常会发生改变。更具体地,对于给定剂量的胰岛素,当制剂中的胰岛素浓度增加时,cmax和auc(生物利用度)趋于降低。这意味着即使施用相同量的胰岛素,u500制剂的降糖效果也将低于u200制剂。因此,这两种制剂将不是生物等效的。
[0060]
这种可缩放性的缺乏对胰岛素制剂来说是一个挑战,因为胰岛素会加入非常需要
不同胰岛素浓度的许多不同的给药装置中。
[0061]
本发明人发现,对于nεb29-十六烷二酰基-γ-glu-(desb30)人胰岛素的可溶性制剂,添加柠檬酸盐和烟酰胺会导致cmax和auc(生物利用度)提高,从而能够制备与相同胰岛素的u200制剂生物等效的高度浓缩的nεb29-十六烷二酰基-γ-glu-(desb30)人胰岛素制剂。添加曲前列环素也得到了相同的观察结果。
[0062]
可溶性胰岛素制剂包含浓度为1800nmol/ml至4200nmol/ml的nεb29-十六烷二酰基-γ-glu-(desb30)人胰岛素。在一些实施方案中,所述nεb29-十六烷二酰基-γ-glu-(desb30)人胰岛素的浓度为2400nmol/ml至3600nmol/ml或2700nmol/ml至3300nmol/ml。在另一实施方案中,nεb29-十六烷二酰基-γ-glu-(desb30)人胰岛素的浓度为约3000nmol/ml。
[0063]
如本文所用的术语“约”意指加上或减去10%,例如加上或减去5%。因此,术语“约100u”是指90u至110u。
[0064]
可溶性胰岛素制剂包含锌,其可作为例如醋酸锌或氯化锌添加。可溶性制剂可包含在4.0zn/6ins至7.0zn/6ins的范围内的锌离子。在一个实施方案中,所述锌离子的浓度为4.0zn/6ins至6.0zn/6ins。在另一实施方案中,所述锌离子的浓度为4.7zn/6ins至5.7zn/6ins。在另一实施方案中,所述锌离子的浓度为5.0zn/6ins至6.0zn/6ins。在又一实施方案中,所述锌离子的浓度为5.0zn/6ins至5.5zn/6ins。在另一实施方案中,根据本发明的可溶性胰岛素制剂具有5.0zn/6ins的锌离子浓度。在另一实施方案中,根据本发明的可溶性胰岛素制剂具有5.5zn/6ins的锌离子浓度。在另一实施方案中,根据本发明的可溶性胰岛素制剂具有6.0zn/6ins的锌离子浓度。
[0065]
根据本发明的可溶性胰岛素制剂包含浓度为110mm至220mm的烟酰胺或浓度为0.02μg/ml至1μg/ml的曲前列环素。在一个实施方案中,可溶性胰岛素制剂包含烟酰胺。在实施方案中,可溶性胰岛素制剂可包含浓度为135mm至195mm或150mm至180mm的烟酰胺。在另一实施方案中,可溶性制剂包含浓度为110mm至140mm或190mm至220mm的烟酰胺。在另一实施方案中,可溶性制剂包含浓度为110mm至170mm的烟酰胺。在另一实施方案中,可溶性制剂包含浓度为150mm至220mm的烟酰胺。
[0066]
在另一实施方案中,可溶性制剂包含浓度为约160mm的烟酰胺。在另一实施方案中,可溶性制剂包含浓度为161mm的烟酰胺。在另一实施方案中,可溶性制剂包含浓度为约200nm的烟酰胺。在另一实施方案中,可溶性制剂包含浓度为204mm的烟酰胺。在另一实施方案中,可溶性制剂包含浓度为约210nm的烟酰胺。在另一实施方案中,可溶性制剂包含浓度为211mm的烟酰胺。
[0067]
在另一实施方案中,可溶性胰岛素制剂包含曲前列环素。在另一实施方案中,可溶性胰岛素制剂包含浓度为0.02μg/ml至0.5μg/ml、0.04μg/ml至0.3μg/ml、0.05μg/ml至0.2μg/ml或0.1μg/ml至1μg/ml的曲前列环素。在另一实施方案中,可溶性胰岛素制剂包含浓度为0.1μg/ml的曲前列环素。
[0068]
如本文所述的可溶性胰岛素制剂包含浓度为6mm至40mm的柠檬酸盐。术语柠檬酸盐应被理解为包括柠檬酸盐以及柠檬酸。在一个实施方案中,可溶性胰岛素制剂包含浓度为15mm至30mm、6mm至20mm或20mm至40mm的柠檬酸盐。如本文所述的可溶性胰岛素制剂包含浓度为6mm的柠檬酸盐。如本文所述的可溶性胰岛素制剂包含浓度为10mm的柠檬酸盐。如本
文所述的可溶性胰岛素制剂包含浓度为20mm的柠檬酸盐。
[0069]
本发明的可溶性胰岛素制剂具有在7.0至8.0的范围内的ph。在一个实施方案中,ph为7.2至8.0、7.4至7.8、7.0至7.5、7.4至8.0或7.4至7.8。在另一实施方案中,可溶性胰岛素制剂的ph为7.6。
[0070]
由于可溶性胰岛素制剂是无菌液体,因此它们可以包含防腐剂或可以不含任何防腐剂。在一个实施方案中,根据本发明的可溶性胰岛素制剂进一步包含酚类防腐剂或酚类防腐剂混合物。在一个实施方案中,所述酚类防腐剂是苯酚。在另一实施方案中,防腐剂是酚类防腐剂混合物,如苯酚与间甲酚的混合物。在另一实施方案中,该防腐剂是苯酚与间甲酚的混合物,并且苯酚的浓度为1.3mg/ml至2.0mg/ml,且间甲酚的浓度为1.5mg/ml至2.3mg/ml。在另一实施方案中,该防腐剂是苯酚与间甲酚的混合物,并且苯酚的浓度为1.8mg/ml,且间甲酚的浓度为2.05mg/ml。
[0071]
在一些实施方案中,可溶性胰岛素制剂包含另外的等张剂。在一个实施方案中,所述等张剂是甘油。当可溶性胰岛素制剂的其他组分的浓度确定时,添加这种等张剂的需要是显而易见的。在另一实施方案中,可溶性胰岛素制剂不包含另外的等张剂。
[0072]
在一个实施方案中,可溶性胰岛素制剂不包含另外的缓冲剂。
[0073]
在一方面,本发明提供了降低哺乳动物的血糖水平的方法,该方法是通过向需要这样的治疗的受试者施用治疗有效剂量的如本文所述的可溶性胰岛素制剂。
[0074]
在一方面,本发明提供了治疗受试者的糖尿病的方法,其包括向所述受试者施用如本文所述的可溶性胰岛素制剂。
[0075]
另一方面提供了可溶性胰岛素制剂,其用于治疗或预防包括应激诱发的高血糖症在内的高血糖症、2型糖尿病、糖耐量减低、1型糖尿病,以及烧伤、手术创伤和其他需要合成代谢作用的疾病或损伤、心肌梗死、卒中、冠心病和其他心血管病症,以及治疗危重糖尿病和非糖尿病患者。
[0076]
本发明的胰岛素制剂可以如本领域已知的那样制备,例如,如实施例中所述。
[0077]
本发明将概括于以下实施方案中:
[0078]
1.可溶性胰岛素制剂,其包含:
[0079]
·
浓度为1800nmol/ml至4200nmol/ml的nεb29-十六烷二酰基-γ-glu-(desb30)人胰岛素,
[0080]
·
浓度为4.0zn/6ins至7.0zn/6ins的锌离子,
[0081]
·
浓度为110mm至220mm的烟酰胺或浓度为0.02μg/ml至1μg/ml的曲前列环素,
[0082]
·
浓度为6mm至40mm的柠檬酸盐,且
[0083]
·
ph在7.0至8.0的范围内。
[0084]
2.根据实施方案1所述的可溶性胰岛素制剂,其中所述nεb29-十六烷二酰基-γ-glu-(desb30)人胰岛素的浓度为2400nmol/ml至3600nmol/ml。
[0085]
3.根据前述实施方案中任一项所述的可溶性胰岛素制剂,其中所述nεb29-十六烷二酰基-γ-glu-(desb30)人胰岛素的浓度为2700nmol/ml至3300nmol/ml。
[0086]
4.根据前述实施方案中任一项所述的可溶性胰岛素制剂,其中所述nεb29-十六烷二酰基-γ-glu-(desb30)人胰岛素的浓度为约3000nmol/ml。
[0087]
5.根据前述实施方案中任一项所述的可溶性胰岛素制剂,其中所述锌离子的浓度
为5.0zn/6ins至6.5zn/6ins。
[0088]
6.根据前述实施方案中任一项所述的可溶性胰岛素制剂,其中所述锌离子的浓度为5.0zn/6ins至6.0zn/6ins。
[0089]
7.根据前述实施方案中任一项所述的可溶性胰岛素制剂,其中所述锌离子的浓度为4.7zn/6ins至5.7zn/6ins。
[0090]
8.根据前述实施方案中任一项所述的可溶性胰岛素制剂,其中所述锌离子的浓度为5.0zn/6ins或5.5zn/6ins。
[0091]
9.根据前述实施方案中任一项所述的可溶性胰岛素制剂,其包含烟酰胺。
[0092]
10.根据前述实施方案中任一项所述的可溶性胰岛素制剂,其包含浓度为135mm至195mm或150mm至180mm的烟酰胺。
[0093]
11.根据前述实施方案中任一项所述的可溶性胰岛素制剂,其包含浓度为110mm至140mm或190mm至220mm的烟酰胺。
[0094]
12.根据前述实施方案中任一项所述的可溶性胰岛素制剂,其包含浓度为150mm至220mm的烟酰胺。
[0095]
13.根据前述实施方案中任一项所述的可溶性胰岛素制剂,其包含浓度为110mm至170mm的烟酰胺。
[0096]
14.根据实施方案1-8中任一项所述的可溶性胰岛素制剂,其包含曲前列环素。
[0097]
15.根据实施方案14所述的可溶性胰岛素制剂,其包含浓度为0.02μg/ml至0.5μg/ml、0.04μg/ml至0.3μg/ml、0.05μg/ml至0.2μg/ml或0.1μg/ml至1μg/ml的曲前列环素。
[0098]
16.根据前述实施方案中任一项所述的可溶性胰岛素制剂,其包含浓度为15mm至30mm、6mm至20mm或20mm至40mm的柠檬酸盐。
[0099]
17.根据前述实施方案中任一项所述的可溶性胰岛素制剂,其包含浓度为6mm的柠檬酸盐。
[0100]
18.根据前述实施方案中任一项所述的可溶性胰岛素制剂,其包含浓度为10mm的柠檬酸盐。
[0101]
19.根据前述实施方案中任一项所述的可溶性胰岛素制剂,其包含浓度为20mm的柠檬酸盐。
[0102]
20.根据前述实施方案中任一项所述的可溶性胰岛素制剂,其具有7.2至8.0、7.4至7.8、7.0至7.5、7.4至8.0或7.4至7.8的ph。
[0103]
21.根据实施方案20所述的可溶性胰岛素制剂,其ph为7.6。
[0104]
22.根据前述实施方案中任一项所述的可溶性胰岛素制剂,其进一步包含酚类防腐剂或酚类防腐剂混合物。
[0105]
23.根据实施方案22所述的可溶性胰岛素制剂,其中所述酚类防腐剂是苯酚。
[0106]
24.根据实施方案22所述的可溶性胰岛素制剂,其中所述酚类防腐剂混合物是苯酚和间甲酚。
[0107]
25.根据实施方案23所述的可溶性胰岛素制剂,其中苯酚的浓度为1.3mg/ml至2.0mg/ml,且间甲酚的浓度为1.5mg/ml至2.3mg/ml。
[0108]
26.根据实施方案25所述的可溶性胰岛素制剂,其中苯酚的浓度为1.8mg/ml,且间甲酚的浓度为2.05mg/ml。
[0109]
27.根据前述实施方案中任一项所述的可溶性胰岛素制剂,其包含另外的等张剂。
[0110]
28.根据实施方案27所述的可溶性胰岛素制剂,其中所述等张剂是甘油。
[0111]
29.根据实施方案1-26中任一项所述的可溶性胰岛素制剂,其不包含另外的等张剂。
[0112]
30.根据前述实施方案中任一项所述的可溶性胰岛素制剂,其不包含另外的缓冲剂。
[0113]
31.根据实施方案1所述的可溶性胰岛素制剂,其包含:
[0114]
浓度为3000nmol/ml的nεb29-十六烷二酰基-γ-glu-(desb30)人胰岛素,
[0115]
浓度为5.5zn/6ins的锌离子,
[0116]
浓度为211mm的烟酰胺,
[0117]
浓度为6mm的柠檬酸盐,且ph为7.6。
[0118]
32.根据实施方案1所述的可溶性胰岛素制剂,其包含:
[0119]
浓度为3000nmol/ml的nεb29-十六烷二酰基-γ-glu-(desb30)人胰岛素,
[0120]
浓度为5.5zn/6ins的锌离子,
[0121]
浓度为161mm的烟酰胺,
[0122]
浓度为20mm的柠檬酸盐,且ph为7.6。
[0123]
33.降低哺乳动物的血糖水平的方法,所述方法是通过向需要这样的治疗的受试者施用治疗有效剂量的根据前述实施方案中任一项所述的可溶性胰岛素制剂。
[0124]
34.治疗受试者的糖尿病的方法,其包括向所述受试者施用根据实施方案1-32中任一项所述的可溶性胰岛素制剂。
[0125]
35.根据实施方案1-32中任一项所述的可溶性胰岛素制剂,其用于治疗或预防包括应激诱发的高血糖症在内的高血糖症、2型糖尿病、糖耐量减低、1型糖尿病,以及烧伤、手术创伤和其他需要合成代谢作用的疾病或损伤、心肌梗死、卒中、冠心病和其他心血管病症,以及用于治疗危重糖尿病和非糖尿病患者。
[0126]
实施例
[0127]
实施例1-用于猪研究的制剂
[0128]
本研究的目的是通过猪研究来比较u100、u200和3000nmol/l德谷胰岛素的类似制剂(u500),评价将苯酚与间甲酚的组合替换为单独苯酚的影响,评价降低相对锌浓度(zn/6ins)的影响,评价添加烟酰胺的影响,以及进一步评价添加柠檬酸盐的影响。事先应通过使用测试和储存来测试制剂的物理和化学稳定性。
[0129]
将德谷胰岛素添加至水中,直到浓度为约8mm且溶解。用0.2nnaoh将ph调节至7.6,将储备溶液过滤除菌并测定含量。将过量的水、甘油(20%(w/vol))、苯酚(500mm)、间甲酚(160mm)、烟酰胺(1000mm)、柠檬酸三钠(100mm)和醋酸锌(20mm,用盐酸调节至ph 6.6)按照提及的顺序添加到德谷胰岛素储备溶液中。醋酸锌逐步加入。然后用0.2n氢氧化钠/盐酸将ph调节至7.6,用水调节体积,并将制剂过滤除菌。将制剂装入胰岛素笔的3ml药筒中。
[0130]
通过在每个药筒中向1ml制剂中添加25μl空气并旋转1分钟/天,将一部分药筒在30℃下进行12周的使用测试。定期通过目测检查药筒,在此期间没有发现任何制剂出现变化或颗粒形成。通过在30℃下在12周内测定共价高分子量产物(hmwp)来测试制剂的化学稳定性,均发现稳定且大致相同的低共价二聚体形成率。
[0131]
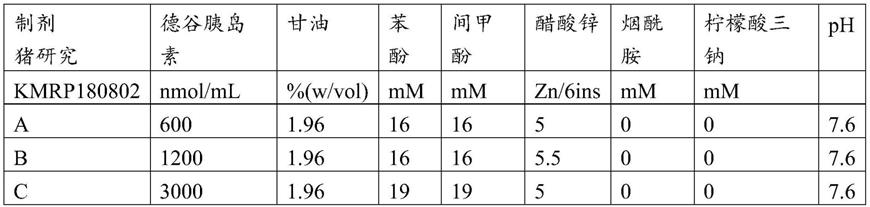
表1.制剂
[0132][0133][0134]
实施例2-动物实验,kmrp180802研究
[0135]
16只雌性家猪(平均体重约80kg)在研究前禁食过夜,并在测试胰岛素制剂给药后8小时进食。为了研究德谷胰岛素的不同制剂,根据表2中概述的时间表,采用平衡、非随机化交叉设计,使每只猪接受表1中描述的制剂。
[0136]
表2.猪实验的给药时间表。
[0137][0138]
*由于低暴露表明给药失败而被排除
[0139]
#第16号猪在这几天被换成新猪
[0140]
在研究期间有一只猪必须更换,因此总共研究了17只猪。
[0141]
在早上向猪给药,并如图1所示取得样品,使用利用两种抗体的特异性发光氧通道免疫测定来测量德谷胰岛素。
[0142]
对通过非房室分析(phoenix软件)得出的auc进行数据分析,并且由于制剂与预期浓度略有不同,因此计算了剂量归一化的auc(auc/剂量)。
[0143]
结果
[0144]
制剂a和b的比较表明,制剂b的pk曲线比u100制剂更扁平,但总的剂量归一化auc没有明显差异(图1a和表3)。制剂b含有5.5个zn/6个胰岛素分子(类似于u200),而制剂a含有5个zn/6个胰岛素分子(类似于u100)。通过在具有5个zn/6个胰岛素分子的制剂c中将胰岛素浓度提高到3000nmol/ml,观察到更扁平的pk曲线,但此时明显地生物利用度相对于制剂a和b降低约18%(图1a和表3)。这种相对较大的降低表明,难以制备与1200nmol/ml制剂生物等效的3000nmol/ml德谷胰岛素制剂,并且相比于u200制剂,将会需要更高剂量的u500制剂来实现同等降糖效果。从19mm苯酚和19mm间甲酚改变为60mm苯酚和0mm间甲酚没有进一步影响pk谱(与制剂b相比,auc/剂量降低约20%),但zn的减少部分地提高了生物利用度,并且相对于制剂a和b,添加柠檬酸盐或烟酰胺更强地提高了生物利用度。制剂g和h与制剂b相比观察到的auc降低程度低于用制剂f观察到的降低程度,制剂g仅降低10%,制剂h仅降低2%。
[0145]
猪表现出在人类中未见的德谷胰岛素吸收的早期峰值。因此,cmax的估计和比较有不确定性。考虑到第二个峰值(最大暴露发生在给药后10-12小时左右),我们观察到制剂f的降低约为制剂b的38%。cmax在制剂g(与制剂b相比仅降低10%)和制剂h(与制剂b相比仅降低21%)中增大。在图1b和图2中可见这些差异。为清楚起见,图1b示出了仅绘制到24小时的全部平均数据,而图2示出了制剂a、b、f、g和h的数据,该数据仅绘制到24小时。
[0146]
表3.通过非房室分析计算的剂量归一化auc
[0147][0148]
结论
[0149]
当将德谷胰岛素的浓度从1200nmol/ml(u200)提升至3000nmol/ml(u500)时,观察到相对生物利用度降低和后期cmax降低,这使得u500制剂与u200制剂不是生物等效的,并且与u200制剂相比,将会需要更高剂量的u500制剂来实现同等降糖效果。通过显示柠檬酸盐和烟酰胺均能几乎恢复auc且部分恢复cmax,我们解决了上述问题,这引导我们测试柠檬酸盐与烟酰胺的组合以制备与u200生物等效的u500制剂,其中相同剂量的u500制剂和u200将提供同等降糖效果。
[0150]
实施例3-用于jstu190601猪研究的制剂
[0151]
本研究的目的是比较德谷胰岛素u200和3000nmol/l德谷胰岛素的类似制剂
(u500),评价两个水平的柠檬酸盐的影响,评价添加烟酰胺至等张并省略甘油的影响,评价柠檬酸盐与烟酰胺的两种组合的影响,并最后通过额外的猪研究测试添加曲前列环素的影响。事先应通过使用测试和储存来测试制剂的物理和化学稳定性。
[0152]
将德谷胰岛素添加至水中,直到浓度为约7mm且溶解。用0.2nnaoh将ph调节至7.8,将储备溶液过滤除菌并测定含量。将过量的水、甘油(20%(w/vol))、苯酚(500mm)、甲酚(160mm)、醋酸锌(20mm,通过盐酸调节至ph 6.6,逐步添加)、烟酰胺(1000mm)、柠檬酸三钠(300mm)和曲前列环素(10μg/ml)按照提及的顺序添加到德谷胰岛素储备溶液中。然后用0.2n氢氧化钠/盐酸将ph调节至7.6,用水调节体积,并将制剂过滤除菌。将制剂装入胰岛素笔的3ml药筒中。
[0153]
表4.制剂
[0154][0155]
实施例4
–
动物实验
[0156]
本研究在16只spf来源的雌性lyd猪中进行,这些猪来自lars jonsson,70,lynge,denmark。在适应期开始时,猪的体重在59.5-68.5kg的范围内,首个给药日的预期最小体重为70kg。在研究期间有四只额外的动物可用,由于出现导管故障和/或感染,其中三只被纳入研究。
[0157]
动物在研究前禁食过夜,并在测试胰岛素制剂给药后8小时进食。为了研究德谷胰岛素的不同制剂,根据表5中概述的时间表,采用平衡、非随机化交叉设计,使每只猪接受表4中描述的制剂。
[0158]
表5.jstu190601实验的给药时间表
[0159]
[0160][0161]
使用四只额外动物中的三只替换导管故障的动物,因此总共研究了19只猪。由于注射导管故障,总共有七次给药没有进行。来自第8组的一只动物从数据分析中被省略,因为当天在胰岛素给药后超过150分钟仍无法在该动物中取样。
[0162]
结果:
[0163]
图3示出了来自jstu190601实验的pk曲线。实施例2示出了添加柠檬酸盐或烟酰胺如何提高生物利用度,而在jstu190601中,我们测试了柠檬酸盐与烟酰胺的组合。表6显示了如何滴定柠檬酸盐和烟酰胺的浓度以使u500制剂的auc与u200制剂相匹配。具体来说,对于auc,包含柠檬酸盐和烟酰胺两者的制剂6和制剂7都与制剂1无显著差异,并且u500德谷胰岛素制剂7的auc与u200德谷胰岛素制剂1在数值上相差2%以内。
[0164]
表6通过非房室分析计算的auc
[0165][0166]
使用anova模型与制剂1的事后比较
[0167]
****p《0.0001
[0168]
***p《0.001
[0169]
**p《0.01
[0170]
ns,在0.05水平下不显著
[0171]
猪表现出在人类中未见的德谷胰岛素吸收的早期峰值。因此,cmax的估计和比较有不确定性。为清楚起见,图4示出了制剂1、2、6和7的数据,该数据仅绘制到24小时。考虑到第二个峰值(最大暴露发生在给药后10-12小时左右),我们观察到u500制剂2的降低约为u200制剂1的42%(p《0.001)。cmax在含有6mm柠檬酸盐和211mm烟酰胺的u500制剂6中增加(与制剂1相比仅降低4%,无统计学意义),并且在含有20mm柠檬酸盐和161mm烟酰胺的制剂7中进一步增加(与制剂1相比增加10%,无统计学意义)。
[0172]
我们注意到,当将烟酰胺和柠檬酸盐均添加到制剂中时,可以将auc和后期cmax均调整到与德谷胰岛素u200制剂中的值足够接近地匹配,使得在我们所探索的制剂空间中具有烟酰胺和柠檬酸盐浓度的德谷胰岛素u500制剂可以在临床试验中展现出与u200生物等效。
[0173]
结论:
[0174]
实施例4示出,通过适当地选择德谷胰岛素u500制剂中的柠檬酸盐与烟酰胺的组合,可以将cmax和auc两者与u200德谷胰岛素制剂的这两个参数匹配,从而证明可以制备与u200生物等效的德谷胰岛素u500制剂。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1