一种治疗便秘的中药组合物及其制备方法
1.本发明属于医药领域,具体涉及一种治疗便秘的中药组合物及其制备方法。
背景技术:
2.便秘指的是大便秘结不通,是由于传导功能失常导致的以大便排出困难、排便时间或排便间隔时间延长为特征的病症,《国际疾病分类(icd-10)应用指导手册》将其列为一个独立病种,便秘超过6个月即为慢性便秘。慢性便秘是全球最普遍的胃肠道疾病之一,便秘的患病率从2.6%到26.9%不等,与性别和年龄两个因素密切相关。女性慢性便秘的总患病率几乎是男性的两倍。慢性便秘随着年龄的增长呈指数增长,在65岁以上的人群中,患病率高达50%。每年用于便秘诊断测试的费用将近70亿美元,花在处方和抗便秘药物上有5亿美元。便秘能显著增加大肠息肉等相关大肠疾病的发病率,也是诱发心血管疾病的重要因素,如心力衰竭等;便秘引起的肠道菌群变化可导致动脉粥样硬化等事件的发生。加强对慢性便秘有效治疗方法的研究具有十分重要的意义。
3.当前,治疗慢性便秘使用的药物没有统一的规定,化学药物和中药在临床上均广泛应用,在慢性便秘的治疗上发挥着积极作用。但前者因疗效有限和产生不良副作用,只有不到一半的患者对治疗满意;中医药在治疗便秘的同时,不仅可以调节人体的机能状态,还可改善胃肠道,恢复其正常功能。目前用于治疗便秘的中药组方多数以清热泻下为主,即使用包含大黄、番泻叶、芦荟等刺激性泻剂,在泻下的同时容易伤正,且或多或少有副作用,如大黄单味药或含有大黄的复方,易导致胃肠绞痛、腹泻等。文献分析表明,国内具有通便功能的药品及保健食品的中药组方中,多数以大黄、番泻叶、芦荟、决明子等含有蒽醌类成分的中药配伍组成,长期服用蒽醌类泻下药会导致结肠黑变病,增加发生结肠息肉、腺瘤及结肠癌的危险性,长期使用带来一定的风险。慢性便秘的恢复需要一定的时间,中药治疗也应结合润肠、养血等治疗方法,标本兼顾,整体调整才能达到治疗的目的。
技术实现要素:
4.本发明的目的在于提供一种治疗便秘的中药组合物及其制备方法。本发明的中药组合物选取药食两用或可用于保健食品的中药进行组合,既可保证其安全性,又对机体有一定的改善作用,润肠通便、养血补益于一体,标本同调。因此,本中药组合物适合长期服用,且不含蒽醌类化合物,降低了服用风险,且对慢性便秘具有很好的改善效果。本发明所含中药药性温和,适用于更广泛人群。
5.本发明所提供的中药组合物,由以下质量份的原料药制成:辣木叶27-108份、当归13.5-54份、火麻仁13.5-54份;
6.具体地,本发明所提供的中药组合物,由以下a-i组任意一组的原料药制成:
7.a组:辣木叶27g、当归13.5g、火麻仁13.5g,
8.b组:辣木叶27g、当归27g、火麻仁27g;
9.c组:辣木叶27g、当归54g、火麻仁27g;
10.d组:辣木叶54g、当归13.5g、火麻仁27g;
11.e组:辣木叶54g、当归27g、火麻仁54g;
12.f组:辣木叶54g、当归54g、火麻仁13.5g;
13.g组:辣木叶108g、当归13.5g、火麻仁54g;
14.h组:辣木叶108g、当归27g、火麻仁13.5g;
15.i组:辣木叶108g、当归54g、火麻仁27g。
16.优选地,所述中药组合物由以下c组原料药制成:
17.c组:辣木叶27g、当归54g、火麻仁27g。
18.本发明组方中,当归养血(补)、火麻仁润肠(润)、辣木叶通便化浊(通),都有通便作用,但方向不一,围绕一个目标,多个方向形成合力,相须相使。
19.上述中药组合物通过包括如下步骤的方法制备得到:
20.分别称取辣木叶、当归和火麻仁,混合,加水煎煮,过滤,收集滤液,将所得药液浓缩,加入乙醇进行醇沉,离心,收集上清液,膜过滤,取滤液,即得。
21.上述方法中,所述煎煮具体可进行两次,每次1h;
22.其中,第一次煎煮用水量为药材总质量的10倍;第二次煎煮用水量为药材总质量的8倍;
23.所述浓缩为将所得药液浓缩至密度为1.10g/ml;
24.乙醇的终浓度为体积分数50%;
25.所述离心的条件可为12000rpm离心10min;
26.所述膜过滤采用0.45μm微孔膜进行。
27.上述中药组合物在制备预防和/或治疗便秘的药物中的应用也属于本发明的保护范围。
28.所述应用中,所述便秘具体可为低纤维饮食引起的便秘。
29.所述便秘可为慢性便秘。
30.本中药组合物选取药食两用或可用于保健食品的中药进行组合,既可保证其安全性,又对机体有一定的改善作用,润肠通便、养血补益于一体,标本同调。具体而言,中药组合物原料中辣木叶为新资源食品,当归列入“可用于保健食品的物品名单”,火麻仁列入“既是食品又是药品的物品名单”,具有较高安全性,且不含蒽醌类成分。因此,本中药组合物具有润肠通便,补血养血的功效,适合长期服用,降低了服用风险,且对慢性便秘具有很好的改善效果。
附图说明
31.图1为对照品与样品色谱图的对照。
32.图2为阴性样品与样品色谱图的对照,阴性样品在322nm(阿魏酸)、255nm(异槲皮苷)和265nm(紫云英苷)的色谱图。
33.图3为阿魏酸、异槲皮苷、紫云英苷对照品标准曲线。
34.图4为低纤维饲料造模对小鼠粪便参数的影响。
35.(左图:粪便粒数;右图:口-肛传输时间;与空白组比较,用*表示)。
36.图5a、b辣木叶不同配比的组方对小鼠粪便参数的影响。
37.(左图:粪便粒数;右图:粪便含水率;与空白组比较,用*表示;与模型组比较,用#表示)。
具体实施方式
38.下面结合具体实施方式对本发明进行进一步的详细描述,给出的实施例仅为了阐明本发明,而不是为了限制本发明的范围。以下提供的实施例可作为本技术领域普通技术人员进行进一步改进的指南,并不以任何方式构成对本发明的限制。
39.下述实施例中的实验方法,如无特殊说明,均为常规方法,按照本领域内的文献所描述的技术或条件或者按照产品说明书进行。下述实施例中所用的材料、试剂等,如无特殊说明,均可从商业途径得到。
40.实施例1、提取工艺参数的确定
41.以干浸膏得率和紫云英苷、异槲皮苷、阿魏酸含量作为评价指标,采用正交设计优化辣木叶组方水提工艺参数。
42.1.仪器与材料
43.1.1主要仪器
44.岛津高效液相色谱仪,pda检测器(美国waters公司);赛多利斯p-power分析天平(德国赛多利斯公司);kq 3200de超声波清洗仪(昆山超声仪器有限公司)。
45.2000ml电热套;旋转蒸发仪;喷雾干燥机(真空干燥箱);高效液相色谱仪;超声波清洗器;恒温水浴锅;电子天平;分析天平;电热鼓风干燥箱;干燥器;蒸发皿。
46.1.2材料与试剂
47.甲醇(fisher,批号:194253,色谱级);水(杭州娃哈哈集团有限公司);紫云英苷对照品(批号:chb181115,含量:≥98%,成都克洛玛生物科技有限公司);异槲皮苷对照品(批号:chb180628,含量:≥98%,成都克洛玛生物科技有限公司);阿魏酸(批号:chb180206,含量:≥98%,成都克洛玛生物科技有限公司);辣木叶(pkm1,云南天佑科技);当归(2007011,河北百草康神药业有限公司);火麻仁(2007012,河北百草康神药业有限公司)
48.2.实验方法
49.2.1紫云英苷、异槲皮苷、阿魏酸含量测定方法学的建立
50.2.1.1供试品溶液的制备
51.称取辣木叶组方药材100g(辣木叶:当归:火麻仁=2:1:1),以正交实验中方法5(正交实验共设计了9个实验,选取其中的方法5进行条件考察)提取,过滤,合并滤液,放置室温,测量药液体积。精密量取药液3ml,甲醇7ml,12000rpm离心10min,取上清液,0.45μm微孔膜滤膜过滤,取续滤液,即得。
52.2.1.2对照品溶液的制备
53.精密称取阿魏酸1mg,置25ml量瓶中,加甲醇溶解定容至刻度线,摇匀,得到0.04mg/ml的阿魏酸对照品母液。精密称取异槲皮苷对照品2.8mg,紫云英苷对照品1.2mg,量取阿魏酸对照品母液6.75ml,置100ml量瓶中,加甲醇溶解定容至刻度线,摇匀,即得0.028mg/ml的异槲皮苷对照品、0.012mg/ml的紫云英苷对照品、0.0027mg/ml的阿魏酸对照品混合溶液。
54.2.1.3阴性样品溶液的制备
55.按照处方比例辣木叶:当归:火麻仁=2:1:1,分别称取缺辣木叶、缺当归、缺火麻仁的阴性处方3份,按“2.1.1”项方法制成阴性样品溶液。结果见图1及图2。图1为对照品与样品色谱图的对照,说明样品中出现了对照品中的这三个成分;图2为阴性样品与样品色谱图的对照,说明样品中阿魏酸来自于当归,紫云英苷和异槲皮苷来自辣木叶,此为专属性实验。
56.2.1.4色谱条件
57.aligent tc-c18色谱柱(4.6
×
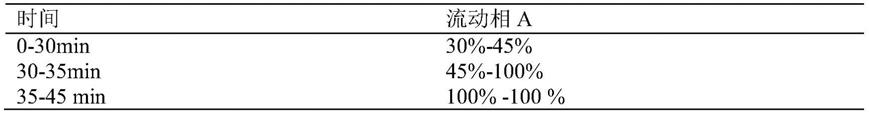
250mm,5μm),流动相为甲醇(a)-0.05%甲酸水溶液(b)。流速:1ml/min;柱温:30℃;检测波长:322nm(阿魏酸),255nm(异槲皮苷),265nm(紫云英苷);进样量:10μl。梯度洗脱程序见表1。
58.表1流动相洗脱梯度条件
[0059][0060]
2.1.5线性关系考察
[0061]
用移液管精密吸取混合对照品溶液(0.408mg/ml的异槲皮苷对照品、0.159mg/ml的紫云英苷对照品、0.0432mg/ml的阿魏酸对照品混合溶液)各10、50、200、500、1000、2000μl至量瓶中,加甲醇稀释并定容至2ml,获得质量浓度分别为2μg/ml、10μg/ml、40μg/ml、100μg/ml、200μg/ml、400μg/ml的异槲皮苷对照品溶液;质量浓度分别为0.8μg/ml、4μg/ml、16μg/ml、40μg/ml、80μg/ml、160μg/ml的紫云英苷对照品溶液;质量浓度分别为0.2μg/ml、1μg/ml、4μg/ml、10μg/ml、20μg/ml、40μg/ml的阿魏酸对照品溶液。按“2.1.4”项下色谱条件进样分析,测定峰面积。以进样量(μg)为横坐标x,色谱峰面积(a)为纵坐标y,进行线性回归,得到阿魏酸线性回归方程:y=59436x-15124(r2=0.9997);异槲皮苷线性回归方程:y=26888x-72090(r2=0.9997);紫云英苷线性回归方程:y=22799x-22711(r2=0.9997)。
[0062]
2.1.6精密度考察
[0063]
取同一对照品溶液,按“2.1.4”项下色谱条件,连续进样6次,测定阿魏酸峰面积值的rsd为0.29%,异槲皮苷峰面积值的rsd为0.22%,紫云英苷峰面积值的rsd为0.20%。
[0064]
2.1.7稳定性试验
[0065]
取同一供试品溶液、混合对照品溶液,按“2.1.4”项下色谱条件,分别于0、3、6、9、12、15、18、21、24h进样测定,计算日内稳定性rsd值;分别于第1、2、3天进样测定,计算日间稳定性rsd值。日内稳定性中,阿魏酸对照品峰面积值的rsd值为0.49%,异槲皮苷对照品峰面积值的rsd值为0.59%,紫云英苷对照品峰面积值的rsd值为0.31%。供试品中阿魏酸峰面积值的rsd值为0.89%,异槲皮苷峰面积值的rsd值为0.26%,紫云英苷峰面积值的rsd值为2.40%。日间稳定性中,阿魏酸对照品峰面积值的rsd值为0.53%,异槲皮苷对照品峰面积值的rsd值为0.78%,紫云英苷对照品峰面积值的rsd值为0.34%。供试品中阿魏酸峰面积值的rsd值为2.58%,异槲皮苷峰面积值的rsd值为0.92%,紫云英苷峰面积值的rsd值为2.26%。
[0066]
2.1.8重复性实验
[0067]
辣木叶组方,根据“2.1.1”项下方法制备6份供试品溶液,按“2.1.4”项下色谱条件进样测定供试品中阿魏酸的含量为5.06μg/ml,峰面积值的rsd值为1.92%;异槲皮苷的含
量为57.57μg/ml,峰面积值的rsd值为1.62%;紫云英苷的含量为27.79μg/ml,峰面积值的rsd值为1.61%。
[0068]
2.1.9加样回收率试验
[0069]
精密吸取辣木叶组方提取液1.5ml,共6份,分别加入等量的异槲皮苷、紫云英苷、阿魏酸对照品,按“2.1.1”项方法制备。按“2.1.4”项下色谱条件进样测定。
[0070]
计算异槲皮苷、紫云英苷、阿魏酸的加样回收率。
[0071][0072]
表2阿魏酸加样回收率
[0073][0074]
表3异槲皮苷加样回收率
[0075][0076]
表4紫云英苷加样回收率
[0077][0078]
2.1.10样品测定
[0079]
分别精密吸取对照品溶液及正交试验样品,按照“2.1.1”项方法制备供试品溶液,进样测定。每个样品重复进样2次,计算各成分在样品中的含量。
[0080]
2.2水提工艺优化
[0081]
2.2.1出膏率
[0082]
测定水提液总体积,精密吸取复方水提液25ml,置已恒定质量的蒸发皿中,100℃水浴蒸发水分。常压105℃干燥至恒定质量,取出,置干燥器中冷却1h,迅速称定质量,计算出膏率。
[0083]
出膏率=[(取样体积/总体积)
×
干膏质量]/药材质量
×
100%
[0084]
2.2.2正交试验
[0085]
选择考察提取时间(a)、提取次数(b)及加水倍数(c)3个因素,进行l9(34)正交实验,结合紫云英苷、异槲皮苷、阿魏酸的含量及出膏率进行综合计算,综合评分=(干浸膏得
率/干浸膏得率最大值)
×
3+(紫云英苷含量/紫云英苷含量最大值)
×
2+(异槲皮苷含量/异槲皮苷含量最大值)
×
2+(阿魏酸含量/阿魏酸含量最大值)
×
3,正交因素水平见表5,正交结果见表6,方差分析见表7。
[0086]
表5l9(34)正交试验因素水平表
[0087][0088]
表6l9(34)正交实验结果
[0089][0090]
表7方差分析
[0091][0092]
2.2.2提取工艺的确定
[0093]
根据表6中极差(r)的大小,各因素对工艺影响程度为b>a>c,且提取次数具有显著性差异。取各因素较高水平的组合,以及生产工艺成本及正交实验均值差异大小,确定最佳水提工艺为a2b2c2。考虑到药材的吸水量,最终确定水提工艺为一煎10倍,二煎8倍,各煎煮1h。
[0094]
2.2.3验证试验
[0095]
为了验证试验结果的准确性及可靠性,称取组方药材3份,按优选的最佳工艺进行提取,测定各项指标,结果见表8,由表8可知,3批验证试验综合评分平均值为9.47,rsd为1.96%。并考察了第三煎中阿魏酸、异槲皮苷、紫云英苷的含量和出膏率(表9),结果表明,第三煎中阿魏酸、异槲皮苷、紫云英苷的含量和出膏率都较低,考虑到生产成本,因此煎煮2次为更优方法。
[0096]
表8验证结果
[0097][0098]
表9第三煎中阿魏酸、异槲皮苷、紫云英苷的含量及出膏率
[0099][0100]
2.3醇沉工艺
[0101]
2.3.1药液密度(指)的考察
[0102]
按照最佳工艺提取辣木叶组方,浓缩,将药液浓缩后配成密度为1.06、1.10、1.14g/ml,用乙醇沉淀(60%终浓度),静置12h,离心取上清,进行含量测定及出膏率测定,结果见表10,结果表明优选密度为1.10g/ml。
[0103]
表10不同密度醇沉结果
[0104][0105]
2.3.2药液含醇量的考察
[0106]
按照最佳工艺提取辣木叶组方,浓缩,将药液配置成3份,密度为1.10g/ml,加入乙醇使终浓度为50%、60%、70%,进行含量测定及出膏率测定,结果见表11,结果表明醇沉终浓度为50%。
[0107]
表11不同乙醇终浓度醇沉结果
[0108][0109][0110]
2.3.3验证试验
[0111]
按照处方比例,称取药材100g,按照上述最佳水提工艺制备,浓缩后将密度配置为1.10g/ml,加入乙醇至含醇量为50%,静置12h,离心。进行3次重复试验,测定出膏率及异槲皮苷、紫云英苷、阿魏酸的含量,结果见表12。
[0112]
表12醇沉实验验证
[0113][0114]
实施例2、辣木叶、当归及火麻仁组方优化实验研究
[0115]
icr小鼠,体重为20g
±
2g,雌性,120只,采用正交设计,优化确定辣木叶、当归、火麻仁的最佳配比;实验动物常规饲养2-3天,于实验前称量动物体重,随机分组,编号,并记录。设计3因素、3水平的9次正交试验,选用l9(34)正交表。本实验以此剂量为基础,拟定3个剂量水平,通过一个三因素三水平的正交试验表l9(34)安排试验,以排便时间、粪便粒数、粪便质量和粪便含水量为指标,考察配伍关系,并优选配伍剂量。
[0116]
表13正交实验设计
[0117][0118]
进行造模及分组,除空白对照组给予常规饲料饲养外,其余各组给予低纤维特制饲料[玉米淀粉(41.5%),蔗糖(10.0%),糊精(10.0%)乳酪蛋白(24.5%),玉米油(6.0%),矿物质混合物(7.0%)维生素混合物(1.0%)]饲养,连续喂养14天,一周称量一次体重、摄食量及饮水量。按l9(34)正交设计的试验序号表,取实验动物120只,各组按正交表中相对应的剂量配伍而成的药物进行灌胃给药,随机分为12组,每组10只,造模后连续灌胃给药1周,1次/天,0.1ml/10g。
[0119]
低纤维饲料配方出处:
[0120]
kakino m,tazawa s,maruyama h,et al.laxative effects of agarwood on low-fiber diet-induced constipation in rats[j].bmc complement altern med,2010,10:68
[0121]
表14
[0122][0123]
注:
[0124]
a组:辣木叶27g、当归13.5g、火麻仁13.5g,比例为2:1:1
[0125]
b组:辣木叶27g、当归27g、火麻仁27g;比例为1:1:1
[0126]
c组:辣木叶27g、当归54g、火麻仁27g;比例为1:2:1
[0127]
d组:辣木叶54g、当归13.5g、火麻仁27g;比例为4:1:2
[0128]
e组:辣木叶54g、当归27g、火麻仁54g;比例为2:1:2
[0129]
f组:辣木叶54g、当归54g、火麻仁13.5g;比例为1:1:4
[0130]
g组:辣木叶108g、当归13.5g、火麻仁54g;比例为8:1:4
[0131]
h组:辣木叶108g、当归27g、火麻仁13.5g;比例为8:4:1
[0132]
i组:辣木叶108g、当归54g、火麻仁27g;比例为4:2:1
[0133]
制备工艺:分别称取辣木叶、当归和火麻仁,混合,加药材总质量的10倍的水煎煮1h,过滤,收集滤液,向滤渣中加入药材总质量的8倍的水煎煮1h,过滤,收集滤液,将所得药液浓缩至密度为1.10g/ml,加入乙醇进行醇沉(乙醇的终浓度为50%),12000rpm离心10min,收集上清液,采用0.45μm微孔膜过滤,取滤液,即得。
[0134]
进行排便观察:记录排便时间、粪便粒数、粪便质量和粪便含水量,收集小鼠6小时。称量粪便重量,于60℃干燥24h,根据排便时间、粪便粒数、粪便质量和粪便含水量评价造模是否成功及给药后的通便作用;取结肠,分离距回肠2cm处的结肠3cm,其中1cm置于多聚甲醛中待检;2cm的样本放入液氮速冻,移入-80℃冰箱保存待检。记录体重、摄食量、饮水量,记录6h粪便粒数、粪便重量、粪便含水量、排便时间,记录胃肠运动:检测小肠碳末推进率。
[0135]
实验结果表明:模型组、阳性对照药组、辣木叶及当归火麻仁不同配比组(a组~i组)小鼠给予低纤维饲料喂饲11天后,与空白组比较,小鼠粪便粒数显著性降低(p《0.05),口-肛传输时间显著性增长(p《0.05),结果见表-15,说明低纤维饲料喂可导致小鼠出现便秘状态,造模(正常传输型便秘)成功。
[0136]
参照表14的给药计划,各组小鼠连续灌胃受试物7天,每天1次。末次给药进行排便结果观察。与空白组比较,模型组小鼠粪便数、粪便含水量均显著降低(p《0.05);与模型组比较,阳性药(番泻叶)组、d组(4:1:2)、e组(2:1:2)的粪便粒数显著升高(p《0.05),其他各组均有升高趋势。与模型组比较,阳性药(番泻叶)组、b组(1:1:1)、d组、e组、f组(1:1:4)小鼠的粪便含水率显著升高(p《0.05),d组小鼠的粪便湿重显著升高(p《0.05)。观察小肠推进率,可发现与模型组比较,辣木叶、当归与火麻仁不同配比组(a组~i组)小鼠的小肠推进率均显著性升高(p《0.05)。上述结果表明,不同配比的辣木叶组方可显著改善低纤维诱导小鼠的便秘症状,详见表-16。
[0137]
表15低纤维饲料造模对小鼠粪便参数的影响
[0138][0139]
注:与空白组比较,*p<0.05,**p<0.01
[0140]
表16不同配比的辣木叶、当归及火麻仁组合物对便秘小鼠粪便参数的影响
[0141][0142][0143]
注:与空白组比较,*p<0.05,**p<0.01;与模型组比较,
#
p<0.05,
##
p<0.01)
[0144]
表18粪便参数归一化处理
[0145][0146]
value=粪便粒数+粪便含水量+粪便湿重-口肛传输时间
[0147]
归一化处理公式参考文献:
[0148]
汤荣志.数据归一化方法对提升svm训练效率的研究[d].山东师范大学,2017。
[0149]
将给药组的粪便参数进行线性归一化处理(表18),结果显示当辣木叶、当归和火麻仁以1:2:1比例(c组)进行配伍时,通便效果较为明显。
[0150]
以上对本发明进行了详述。对于本领域技术人员来说,在不脱离本发明的宗旨和范围,以及无需进行不必要的实验情况下,可在等同参数、浓度和条件下,在较宽范围内实施本发明。虽然本发明给出了特殊的实施例,应该理解为,可以对本发明作进一步的改进。总之,按本发明的原理,本技术欲包括任何变更、用途或对本发明的改进,包括脱离了本技术中已公开范围,而用本领域已知的常规技术进行的改变。按以下附带的权利要求的范围,可以进行一些基本特征的应用。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1