抗核仁素剂-PEG缀合的纳米颗粒
抗核仁素剂-peg缀合的纳米颗粒
背景技术:
1.核仁素[37]是一种丰富的非核糖体核仁蛋白,是核糖体基因转录和前核糖体rna包装的位点。这种710个氨基酸组成的磷蛋白具有多结构域的结构,该结构由组蛋白样n-末端、含4个rna识别基序的中心结构域和富含甘氨酸/精氨酸的c-末端构成,表观分子量为110kd。虽然核仁素存在于每个有核细胞中,但核仁素在细胞表面的表达与肿瘤细胞的存在和侵袭性相关[38]。
[0002]
细胞表面核仁素的存在与肿瘤细胞的相关性已被用于通过检测质膜上核仁素的存在来确定细胞肿瘤状态的方法[38]。这一观察结果还提供了基于施用特异性靶向核仁素的化合物的新的癌症治疗策略[39]。
[0003]
核酸适体为折叠成独特三维结构的短的合成寡核苷酸,其可以被特定的靶蛋白所识别。因此,它们的靶向机制类似于单克隆抗体,但它们可能比单克隆抗体具有显著的优势,包括体内清除更快,肿瘤穿透性更好,无免疫原性,以及更容易合成和储存。
[0004]
设计为形成三重螺旋的富含鸟苷的寡核苷酸(gros)已知与核仁素结合。这种结合核仁素的能力被认为是其对于培养的前列腺癌细胞意想不到的抗增殖作用的能力的原因[40]。该抗增殖作用与三重介质或反义机制不一致,显然gro通过另一作用方式抑制增殖。据推测,表现出形成更高阶的含g-四分体结构的倾向的gro通过适体机制起作用,其由于gro结构的形状特异性识别而与核仁素结合,与细胞表面核仁素的结合进而诱导细胞凋亡。gro的抗增殖作用已在源自前列腺癌(du145)、乳腺癌(mda-mb-231、mcf-7)或宫颈癌(hela)的细胞系中得到证实,并且与gro结合细胞表面核仁素的能力相关[40]。
[0005]
此前开发了as1411(gro26b,序列号:10),其为一种gro核仁素结合dna适体,具有针对癌细胞的抗增殖活性,且对非恶性细胞几乎没有影响。as1411摄取似乎在癌细胞中通过巨胞饮作用发生,而在非恶性细胞中通过非巨胞饮途径发生,导致选择性杀死癌细胞,而不影响非恶性细胞的生存能力[41]。as1411是第一个在人体中测试的抗癌适体,且as1411的临床试验结果(包括对肾细胞癌或急性骨髓性白血病患者的ii期研究)显示了有前景的临床活性,且没有严重副作用。尽管有少量显著和持久的临床反应,对as1411的总体响应率较低,这可能是由于as1411的效力低造成的。
[0006]
与颗粒缀合的抗核仁素剂,例如与金纳米颗粒缀合的适体,对癌症和肿瘤具有抗增殖作用。参见bates等人于2012年6月1日提交的国际申请,其国际公开号为wo 2012/167173,标题为“anti-nucleolin agent-conjugated nanoparticles”。特别地,缀合适体的金纳米颗粒具有与单独的适体(抗核仁素寡核苷酸)相似或更强的抗增殖作用,仅在1/10至1/100剂量下即显示出类似作用。此外,这些试剂(优选具有缀合到颗粒上或连接到抗核仁素剂上的荧光染料)也可以用作体内和体外的显像剂。另请参见[49]。
[0007]
与包含金属的颗粒缀合的抗核仁素剂,例如与金纳米颗粒缀合的适体,是治疗癌症的有效的放射增敏剂。该纳米颗粒被癌细胞选择性吸收,并增强放射治疗(rt)对这些细胞的作用。这增强了放射治疗的有效性,和/或允许在放射治疗期间使用较低有效剂量的辐射。此外,该纳米颗粒还可以任选地包含钆,在mri扫描期间增强附近水分子的弛豫性(加快
弛豫速率),并且当存在于被扫描样品中时有助于提高对比度。另外,金纳米颗粒和gd离子都增强x射线的吸收和散射,并且当存在于使用基于x射线的成像技术(例如ct扫描)扫描或成像的样品中时提高对比度。抗核仁素剂(癌症靶向)和钆(mri造影增强)的组合产生了癌症靶向mri造影剂。此外,抗核仁素剂(癌症靶向)和金纳米颗粒(x射线造影增强)以及任选的钆(mri造影增强和x射线造影增强)的组合产生了癌症靶向mri和x射线(ct扫描)造影剂。参见bates等人于2016年5月5日提交的国际申请,国际公开号为wo 2016/179394,标题为“anti-nucleolin agent-conjugated nanoparticles as radio-sensitizers and mriand/or x-ray contrast agents”。
[0008]
as1411还被用作癌症靶向剂,用于通过抗癌药物或复合物选择性地治疗癌细胞。例如,含有plga纳米颗粒的药物已使用as1411功能化并与聚乙二醇(peg)缀合以特异性靶向癌细胞,然后plga在细胞内降解时释放药物[46,48]。
[0009]
药物的聚乙二醇(peg)修饰(通常称为聚乙二醇化)已被广泛用于通过防止药物的快速肾清除来改善溶解度和体内稳定性。此外,聚乙二醇化有助于隐藏药物免于免疫系统,使得患者在治疗过程中产生中和药物有效性的免疫反应的可能性较小(这对于高分子量药物例如生物工程酶和抗体来说尤其成问题)。此外,聚乙二醇化在肿瘤中产生渗透及滞留增强(epr)效应,利用肿瘤的脉管系统渗漏及缺乏有效淋巴引流来增强有效的肿瘤靶向。例如,已经研究将peg用螯合基团修饰而与铜离子螯合,然后与as1411复合,以用于靶向肿瘤细胞[47]。
[0010]
胶质母细胞瘤(gbm)是最常见的成人原发性脑肿瘤,通常预后为14个月,5年存活率《5%[20-24]。最有希望的治疗方案为手术结合化疗和放疗[25,26]。完全切除并不总是可行的,并且化疗/放疗具有潜在的毒性[27-30]。gbm的特征为信号通路的异常修饰,使得发生gbm的增殖、转移和存活[24,31-34]。
技术实现要素:
[0011]
在第一方面,本发明为一种组合物,其包含与纳米颗粒缀合的抗核仁素剂和peg。所述纳米颗粒的平均直径为1至50纳米。
[0012]
在第二方面,本发明为一种组合物,其包含与纳米颗粒缀合的抗核仁素剂和peg。所述纳米颗粒包括至少一种选自金属、元素和氧化物的无机材料。
[0013]
在第三方面,本发明为一种治疗癌症的方法,包括向有需要的患者施用有效量的任何前述组合物。
[0014]
在第四方面,本发明为一种治疗癌症的方法,包括向有需要的患者施用有效量的任何前述组合物,然后进行放射治疗。
[0015]
在第五方面,本发明为一种通过mri和/或x射线成像技术在体内对癌症成像的方法,包括向受试者施用任何前述组合物,并通过mri和/或x射线成像技术形成所述受试者体内存在的所述组合物的图像。
[0016]
定义
[0017]
术语“缀合的”意指“化学键合”。
[0018]
术语“抗核仁素寡核苷酸”是指“与核仁素结合的寡核苷酸”。
[0019]
术语“等效适体浓度”是指缀合物中存在的抗核仁素寡核苷酸的浓度。
[0020]
聚乙二醇,也称为peg,可以与药物、纳米颗粒或者其他物质缀合。当与peg缀合时,通常被称为聚乙二醇化的,并且含有-(ch2ch2o)-部分。除非另外说明,peg的分子量理解为缀合前peg的数均分子量(mn),优选如制造商或销售商所标注。
[0021]
肿瘤和癌症包括实体的、增殖异常的组织变化和扩散性肿瘤。肿瘤和癌症的实例包括黑色素瘤、淋巴瘤、浆细胞瘤、肉瘤、神经胶质瘤、胶质母细胞瘤、胸腺瘤、白血病、乳腺癌、前列腺癌、结肠癌、肝癌、食道癌、脑癌、肺癌、卵巢癌、子宫内膜癌、膀胱癌、肾癌、宫颈癌、肝细胞瘤和其他肿瘤。关于肿瘤和癌症的更多实例参见例如stedman[42]。
[0022]“治疗肿瘤”或“治疗癌症”是指显著抑制肿瘤或癌症的生长和/或转移和/或杀死癌细胞。生长抑制可以通过肿瘤体积的减小或转移发生率的降低来表示。肿瘤生长可以例如通过常规程序检查肿瘤体积(例如用游标卡尺获得二维测量值)来确定。转移可以通过检查继发位点的肿瘤细胞或通过体外检查活检肿瘤细胞的转移潜能来确定。
[0023]“化疗剂”为可有效用于治疗人类癌症的化学化合物。
[0024]“药学上可接受的载体”包括任何和所有与所施用的药物相容的溶剂、分散介质、包衣、抗细菌剂和抗真菌剂、等渗剂和吸收延迟剂。这种载体或稀释剂的优选实例包括水、盐水、林格氏溶液和葡萄糖溶液。也可以将补充的活性化合物掺入组合物中。
[0025]“药物”、“治疗组合物”和“药物组合物”之间可互换使用,以表示在受试者中发挥治疗作用的化合物、物质、混合物或制剂。
[0026]“抗体”以最广泛的含义使用,是指单克隆抗体、多克隆抗体、多特异性抗体、抗体片段和化学修饰抗体,其中所述化学修饰基本上不干扰抗体或抗体片段的选择性和特异性。
[0027]“抗核仁素剂”包括与核仁素相互作用的任何分子或化合物。这种试剂包括例如抗核仁素抗体、适体(例如gro)和核仁素靶向蛋白。
[0028]“基于x射线的成像技术”包括使用x射线直接或间接形成图像的所有成像技术,包括例如ct扫描(也称为x射线计算机断层扫描或计算机化轴向断层扫描(cat扫描))。
附图说明
[0029]
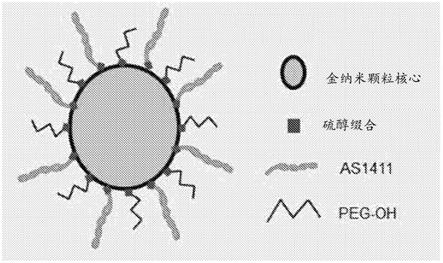
图1为共缀合的金纳米颗粒的草图展现。
[0030]
图2a为不同比例的as1411与peg的ζ电势(mv)图。图2a显示了两个独立的颗粒合成的平均值,数值以平均值
±
标准偏差表示。
[0031]
图2b为不同比例的as1411与peg的流体动力学尺寸(nm)图。图2b显示了两个独立的颗粒合成的平均值,数值以平均值
±
标准偏差表示。
[0032]
图2c为不同比例的as1411与peg的多分散性指数图。图2c显示了两个独立的颗粒合成的平均值,数值以平均值
±
标准偏差表示。
[0033]
图2d为基于缀合寡核苷酸的dtt分离和分离前后的uv-vis光谱分析的负载到金纳米颗粒上的as1411分子的估测数量的图。图2d显示了两个独立的颗粒合成的平均值,数值以平均值
±
标准偏差表示。
[0034]
图2e为颗粒合成的uv-vis分析图,示出210-450纳米的颗粒吸光度。
[0035]
图2f为颗粒合成的uv-vis分析图,示出450-1000纳米的颗粒吸光度和金的表面等离子体共振波长。
[0036]
图3示出了用共缀合的aunp颗粒处理后u87mg的体外代谢活性。数据以平均值
±
标准偏差表示(n=3)。条形代表经处理的u87mg的绝对xtt吸光度,其与u87mg的生存力成比例关系。6x和9x颗粒的具有统计学显著性的细胞毒性通过双向anova分析确定,α=0.05,*表示p《0.0001(与0和10μm的as组相比)。使用graph pad prism软件确定显著性。
[0037]
图4示出了显著的6x和9x颗粒的ec50分析。曲线代表每组最佳拟合的非线性回归线。对于9x和6x颗粒,ec50值分别确定为1303nm(r2=0.8722)和212nm(r2=0.9181)寡核苷酸。使用graph pad prism软件完成分析。
[0038]
图5示出了经颗粒处理的u87mg的10x明视野图像,其显示了72小时后的细胞形态和密度。使用nikon荧光显微镜和nis元素软件来获得图像。除10μmas1411条件外,aunp处理显示~1000nm寡核苷酸浓度。比例尺表示100微米。
[0039]
图6示出了用9xas/cro aunp处理后u87mg的体外代谢活性。数据以平均值
±
标准偏差表示(n=5)。条形代表处理的u87mg的绝对xtt吸光度,其与u87mg的生存力成比例。9x颗粒的统计学显著特异性通过双向anova分析确定,α=0.05,*表示p《0.001(当9x与等效的cro组相比时)。使用graph pad prism软件确定显著性。
[0040]
图7示出了9x共缀合的aunp颗粒的ec50分析。曲线代表最佳拟合的非线性回归线。ec50值被确定为935nm寡核苷酸(r2=0.7015),cro曲线不可获得。使用graph pad prism软件完成分析。
具体实施方式
[0041]
本发明利用缀合到颗粒上的抗核仁素剂和peg,例如缀合到金纳米颗粒的适体和peg,对癌症和肿瘤具有抗增殖作用。peg/抗核仁素剂缀合物也可称为共缀合物。添加peg作为共缀合物可增强与纳米颗粒缀合的抗核仁素剂的药代动力学而进一步提高体内功效(例如通过增加循环半衰期)或避免在器官例如肝和/或肺中积累。此外,与单独的适体(抗核仁素寡核苷酸)或甚至缀合适体的金纳米颗粒相比,缀合适体/peg的金纳米颗粒尤其具有相似、或更强的抗增殖作用,且仅在1/10至1/100剂量下即可表现出相似作用。此外,这些试剂(优选具有缀合到颗粒上或者连接到抗核仁素剂或peg上的荧光染料)也可用作体内和体外的显像剂。它们也可用作增强放射治疗(rt)的试剂,以及用作x射线和ct扫描的造影剂。最后,如果还与钆缀合,它们可以用于增强mri扫描中的对比度。
[0042]
与纳米颗粒缀合的peg和抗核仁素剂之间的摩尔比可变化。例如,抗核仁素剂与peg的比例可以为1:1、2:1、3:1、4:1、5:1、6:1、7:1、8:1、9:1、10:1、11:1或12:1。或者,peg与抗核仁素剂的比例可以为1:1、2:1、3:1、4:1、5:1、6:1、7:1、8:1、9:1、10:1、11:1或12:1。优选地,所述抗核仁素剂为as1411。优选地,所述纳米颗粒是直径为4、5、10、15、20或100nm的金纳米颗粒。为了治疗胶质母细胞瘤或其他脑癌,所述纳米颗粒的直径优选为4、5或10nm以增强透过血脑屏障的渗透能力。
[0043]
当将抗核仁素剂(例如as1411)和/或peg缀合到纳米颗粒(例如金纳米颗粒)上时,通常使得纳米颗粒的表面饱和于缀合至表面的试剂。因此,当形成试剂(例如as1411和peg)的混合物时,对试剂的比例进行控制,而这控制了与纳米颗粒缀合的试剂的比例,以及每个纳米颗粒上每种试剂的数量。例如,在缀合有as1411和peg的4nm金纳米颗粒的情况下,缀合的试剂分子的总数将是12,因此与纳米颗粒缀合的as1411和peg分子的总数将是12。用于确
定as1411:peg比例的命名规则是基于与纳米颗粒缀合的as1411分子总数。在4nm金纳米颗粒的情况下,“12x”意指12个as1411分子,并且as1411:peg的比例为12:0;类似地,“9x”、“6x”、“3x”和“0x”分别具有9、6、3和0个as1411分子且as1411:peg的比例分别为9:3、6:6、3:9和0:12(或者分别为3:1、1:1、1:3和0)。对于较大的金纳米颗粒,例如5nm或10nm的金纳米颗粒,可以缀合的试剂总量更大,因此“9x”意味着as1411:peg的比例更小。尽管在合成过程中形成缀合物的分布,那些偏离于最普遍的缀合比例的纳米颗粒可以通过“盐析”,利用具有不同缀合比例的纳米颗粒的不同ζ电势来进行分离。
[0044]
可使用任何分子量的peg。优选地,peg分子量为200至20,000,更优选1000至10,000,包括2000、3000、4000、5000、6000、7000、8000和9000以及其间的值。应当理解,这些分子量值为数均分子量,其表示以测量精度的有效数字所示出的值,并且这种组合物具有与所报道的分子量类似的peg分子分布。
[0045]
放射治疗(rt)可以采用任何形式的放射,例如x射线(例如兆伏能量的x射线)、近距离放射治疗、质子放射和中子放射。也可以使用通常被认为是亚临床的放射治疗剂量和/或能量;由于所述抗核仁素剂-peg缀合的纳米颗粒增强了放射治疗的有效性,因此该剂量对于杀死或减少癌细胞和肿瘤的生长是有效的。
[0046]
含有钆的抗核仁素剂-peg缀合的纳米颗粒是有效的mri造影剂,并且也可以用于对癌细胞进行成像,包括单个癌细胞。例如,可以向患者施用含有钆的抗核仁素剂-peg缀合的纳米颗粒,以确定淋巴结中是否存在癌细胞,从而避免仅为了确定淋巴结中是否含有癌细胞的目的而切除淋巴结。另一个用途是可以避免活检的需要。可将含有钆的抗核仁素剂-peg缀合的纳米颗粒施用于患者,以确定癌症是否存在于肿块中,是否已经转移到身体的其他位置,或者确定是否已经在手术期间切除了所有来自肿瘤的癌症。
[0047]
任选含有钆的抗核仁素剂-peg缀合的纳米颗粒是有效的x射线造影剂,并且也可用于对癌细胞进行成像,包括单个癌细胞。例如,可向患者施用任选含有钆的抗核仁素剂-peg缀合的纳米颗粒,以确定淋巴结中是否存在癌细胞,从而避免仅为了确定淋巴结中是否含有癌细胞的目的而切除淋巴结。另一个用途是可以避免活检的需要。可将任选含有钆的抗核仁素剂-peg缀合的纳米颗粒施用于患者,以确定癌症是否存在于肿块中,是否已经转移到身体的其他部位,或者确定是否已经在手术期间切除了所有来自肿瘤的癌症。
[0048]
抗核仁素剂包括(i)适体,如gro;(ii)抗核仁素抗体;和(iii)核仁素靶向蛋白。所述适体的实例包括富含鸟苷的寡核苷酸(gros)。合适的寡核苷酸的实例和化验也在miller等人[43]中给出。gro的特征包括:
[0049]
(1)具有至少一个ggt基序,
[0050]
(2)优选具有4-100个核苷酸,但是具有更多核苷酸也是可能的,
[0051]
(3)任选进行化学修饰以提高稳定性。
[0052]
特别有用的gro形成g-四分体结构,如可逆热变性/复性曲线在295nm处所示出[40]。在电泳迁移率变动分析中,优选的gro还与端粒寡核苷酸进行竞争以结合靶细胞蛋白[40]。在某些情况下,将gro核苷酸整合到更大的核酸序列中可能是有利的;例如,在不使与核仁素结合的位点变性的情况下促进gro核酸与底物的结合。寡核苷酸的实例如表1中所示;优选的寡核苷酸包括表1中的序列号1-7、9-16、19-30和31。
[0053]
表1:结合核仁素的非反义gro和非结合的对照
1,2,3
[0054]
[0055][0056]1表示与质膜核仁素结合良好的gro。2表示核仁素对照(非质膜核仁素结合)。没有1或2标记的3gro序列具有一些抗增殖活性。
[0057]
也可以使用任何与核仁素结合的抗体。在某些情况下,单克隆抗体是优选的,因为它们结合单一的、特异性的和确定的表位。然而,在其他情况下,可以使用能够与核仁素上多于一个表位相互作用的多克隆抗体。许多抗核仁素抗体是市售的,或者容易制造。参见例如sutkowski等人的美国专利申请公开号us 2013/0115674。表2列出了一些市售的抗核仁
素抗体。
[0058]
表2:市售抗核仁素抗体
[0059]
[0060][0061]
除抗体以外,核仁素靶向蛋白为特异性和选择性结合核仁素的蛋白质。实例包括核糖体蛋白s3、肿瘤导向f3肽[44,45]和肌球蛋白h9(一种非肌肉肌球蛋白,在肿瘤发生期间,与血管生成血管中的内皮细胞的细胞表面核仁素结合)。
[0062]
抗核仁素剂可以缀合到由多种固体材料所制成的颗粒上,包括:(1)金属和元素;(2)氧化物;(3)半导体和(4)聚合物。金属和元素(优选为非磁性金属和元素)包括金、银、钯、铱、铂及其合金;元素包括硅、硼和碳(例如金刚石、石墨烯和碳纳米管)及其固体化合物。氧化物包括二氧化钛、二氧化硅、氧化锌、氧化铁、氧化锆、氧化镁、氧化铝及其复合氧化物,例如钛酸钡。半导体包括量子点、硫化锌、硅/锗合金、氮化硼、氮化铝及其固溶体。聚合物包括聚乙烯、聚苯乙烯、聚丙烯酰胺、聚丙烯酸酯和聚甲基丙烯酸酯以及聚硅氧烷。优选地,所述颗粒是无毒的。所述颗粒的平均粒径优选为1-100nm,更优选1-50nm,包括4、5、6、7、8、9、10、12、15、18、20、25、30、35、40、45、50、55、60、65、70、75、80、85、90和95nm。
[0063]
已通过各种技术将寡核苷酸和蛋白质连接到固体材料(例如金属和元素、氧化物、半导体和聚合物)上。这些技术可用于将抗核仁素剂连接到颗粒上。进一步将染料(例如花青染料)与抗核仁素剂-peg缀合的纳米颗粒(缀合物)连接,使得所述缀合物可用作体内和体外的显像剂。
[0064]
通过形成抗核仁素剂-peg缀合的纳米颗粒和药学上可接受的载体的混合物,例如药物组合物,可将抗核仁素剂-peg缀合的纳米颗粒用于配制药物组合物,用于治疗癌症和肿瘤,并靶向表达细胞表面核仁素的癌细胞。治疗受试者癌症的方法包括施用治疗有效量的抗核仁素剂-peg缀合的纳米颗粒。
[0065]
特别优选的组合物为与金纳米颗粒缀合的适体。金纳米颗粒(gnps)表现出低的毒性、多样化的表面化学、光吸收/散射特性和可调的尺寸。适体可以有效覆盖金颗粒并防止聚集,并且安全、稳定、易于合成且无免疫原性。与替代手段相比,缀合适体的gnp提供许多优势,例如与单独的as1411相比在癌细胞中增强的抗增殖活性以及提高的体内功效,使得在小鼠中建立的乳腺癌异种移植物持久消退且没有副作用。与正常细胞相比,缀合适体的gnp对癌细胞具有高度选择性,并且当与花青染料连接时为优异的显像剂,例如cy2、cy3、cy5、cy7、alexa680、alexa750、680和800cw(li-cor biosciences,lincoln,ne)。缀合适体的gnp可以用作显像剂,并且可以作为组合物(还含有药学上可接受的载体)进行给药。在体内对癌症成像的方法中,可以向受试者施用所述显像剂,形成该受试者体内存在的显像剂的图像。
[0066]
除非另有说明,本文所述的组合物的量和比例都是以重量计的。因此,当纳米颗粒
的重量变化时,每个纳米颗粒的抗核仁素剂的数量可以随之变化,即使当等效抗核仁素剂的浓度(或等效适体浓度)在其他方面相同时也是如此。例如,每个纳米颗粒的抗核仁素剂分子的数量可以从2至10,000或10至1000变化,包括20、30、40、50、60、70、80、90、100、200、300、400、500、600、700、800和900。
[0067]
将药物组合物配制成与其预期的给药途径相匹配,包括静脉内、皮内、皮下、口服、吸入、经皮、经粘膜和直肠给药。用于肠胃外、皮内或皮下施用的溶液和悬浮液可以包括无菌稀释剂,例如注射用水、生理盐水、聚乙二醇、甘油、丙二醇或其他合成溶剂;抗菌剂,例如苯甲醇或对羟基苯甲酸甲酯;抗氧化剂,例如抗坏血酸或亚硫酸氢钠;缓冲剂,例如醋酸盐、柠檬酸盐或磷酸盐;以及张力调节剂,例如氯化钠或葡萄糖。ph值可用酸或碱调节,例如盐酸或氢氧化钠。
[0068]
适于注射的药物组合物包括用于即时制备无菌注射溶液或分散体的无菌水溶液或分散体。对于静脉给药,合适的载体包括生理盐水、抑菌水、cremophor(basf;parsippany,nj)或磷酸盐缓冲盐水(pbs)。在所有的情况下,组合物必须是无菌的,并且应该为流体,以便使用注射器进行给药。这种组合物在生产和储存过程中应该是稳定的,并且优选被保存免受微生物如细菌和真菌的污染。所述载体可以为含有例如水、多元醇(如甘油、丙二醇和液态聚乙二醇)以及其他相容的合适混合物的分散介质。各种抗细菌剂和抗真菌剂(例如对羟基苯甲酸酯、氯丁醇、苯酚、抗坏血酸和硫柳汞)可能会含有微生物污染。等渗剂例如糖、多元醇(如甘露醇、山梨醇)和氯化钠可包含在组合物中。可延迟吸收的组合物包括诸如单硬脂酸铝和明胶的试剂。
[0069]
无菌注射溶液可通过将所需量的活性剂和其它治疗成分与所需的一种或多种成分掺合在适当的溶剂中,然后灭菌来制备。用于制备无菌注射溶液的无菌固体的制备方法包括真空干燥和冷冻干燥以产生固体。
[0070]
本文所述的药物组合物还可包含其它治疗活性化合物,和/或可与本文所述适于治疗癌症和肿瘤的物理技术联合使用。常用的治疗活性化合物的实例包括:长春瑞滨丝裂霉素、喜树碱、环磷酰胺甲氨蝶呤、枸橼酸他莫昔芬、5-氟尿嘧啶、伊立替康、阿霉素、氟他胺、紫杉醇多西他赛、长春花碱、甲磺酸伊马替尼蒽环霉素、来曲唑、三氧化二砷阿那曲唑、双羟萘酸曲普瑞林、奥佐米星、盐酸伊立替康活卡介苗醋酸亮丙瑞林植入物(viadur)、贝沙罗汀依西美坦盐酸托泊替康盐酸吉西他滨盐酸柔红霉素(daunorubicin)、盐酸吉西他滨枸橼酸托瑞米芬(fareston)、卡铂顺铂(和)、奥沙利铂和任何其他含铂肿瘤学药物、曲妥珠单抗拉帕替尼吉非替尼西妥昔单抗帕尼单抗西罗莫司依维莫司凡德他尼(zactimatm)、威罗非尼(zelboraftm)、克唑替尼伏立诺他贝伐单抗放射治疗、热疗、基因治疗和光动力治疗。
[0071]
在癌症治疗中,治疗剂的合适剂量水平通常为每天对于每千克患者体重约0.01至500毫克,可以单剂量或多剂量给药。优选地,剂量水平可为每天约0.1至约250mg/kg;更优
选每天约0.5至约100mg/kg。合适的剂量水平可以为每天约0.01至250mg/kg、每天约0.05至100mg/kg或每天约0.1至50mg/kg。在此范围内,剂量可以为每天0.05至0.5mg/kg、0.5至5mg/kg或5至50mg/kg。所述化合物可以每天1至4次的方案给药,优选每天1或2次。还优选采用连续输注来进行给药。
[0072]
药物制剂可以预先包装成易于给药的形式,其量对应于单次剂量,适于单次给药,这被称为单位剂型。单位剂型可以封装在玻璃或塑料制成的安瓿、一次性注射器或小瓶中。
[0073]
然而,对于任何特定的患者,其特定的剂量水平和给药频率可以变化,并且将取决于多种因素,包括所用特定化合物的活性、该化合物的代谢稳定性和作用时间、年龄、体重、总体健康状况、性别、饮食、给药方式和时间、排泄速率、药物组合、特定病症的严重程度以及经受治疗的患者。
[0074]
实施例
[0075]
目的:合成并优化共缀合peg:as1411金纳米颗粒(aunps),其具有gbm靶向能力,同时允许加入针对胶质母细胞瘤细胞类型的联合治疗。
[0076]
材料
[0077]
haucl4·
3h2o购自alfaaesar(tewksbury,ma)。柠檬酸、三钠盐(na3c6h5o7)、硼氢化钠(nabh4)、二硫苏糖醇(dtt)和无水碳酸氢钠(nahco3)购自sigmaaldrich(st.louis,mo)。10.0x磷酸盐缓冲溶液(ph 7.4)。超纯水(barnstead,电阻率18.2mω-cm)用于制备所有的水溶液。盐酸(hcl)和硝酸(hno3)均为分析纯,购自vwr(rednor,pa)。王水溶液(3份hcl和1份hno3)用于清洗所有用于gnp合成的玻璃器皿。硫醇聚乙二醇-4-醇(sh-peg-oh;分子量210.3g/mol;95%纯度)购自broadpharm(san diego,ca)并通过公司说明书制备。integrated dna technologies(coralville,ia)提供常规dna骨架(磷酸二酯)、5'-硫醇c6 s-s修饰(硫代mc6-d)、5'-6t间隔区(用于as1411和cro)且经高效液相色谱纯化的寡核苷酸。寡核苷酸序列为5'-ggtggtggtggttgtggtggtggtgg(as1411;序列号:10)和5'-cctcctcctccttctcctcctcctcc(cro;序列号:17),其各自在5'末端用6个胸腺嘧啶碱基和在3'末端用3个胸腺嘧啶碱基进行修饰。荧光团修饰的寡核苷酸(cy5-as1411和cy5-cro)为3'修饰荧光花青素-5(cy5)的结构相似的寡核苷酸,从integrated dnatechnologies获得。illustranap-25dna尺寸排阻色谱重力柱购自ge healthcare life sciences(pittsburgh,pa)。带有ultracel-30(30000mwco)的amicon ultra 15.0ml离心过滤器购自merck millipore(billerica,ma)。用紫外可见光谱仪(varian cary 50 bio uv,agilent technologies,santa clara,ca)测量纳米颗粒制剂和寡核苷酸的紫外吸收谱。使用nanobrook zeta pals zeta电位分析仪(brookhaven instruments,holtsville,ny)对纳米颗粒制剂进行动态光散射和ζ电位测量。u87mg胶质母细胞瘤癌细胞购自atcc(manassas,va)。达尔伯克改良伊格尔培养基、热灭活胎牛血清、10x胰蛋白酶、青霉素/链霉素购自thermo fisher scientific(waltham,ma)。gbm细胞在corning incorporated(tewksbury,ma)的t25或t75无菌培养板中进行传代培养。u87mg在来自vwr(rednor,pa)的无菌培养板中培养用于明视野显微镜和代谢研究,或在购自matek life sciences(ashland,ma)的10mm玻璃底面、多聚-d-赖氨酸包被的matek培养皿中培养用于共聚焦研究。使用从biotum(fremont,ca)获得的2,3-双-(甲氧基-4-硝基-5-磺苯基-2h-四唑-5-甲酰苯胺)(xtt)通过分光光度测量法测量经纳米颗粒或对照处理的u87mg的代谢活性。
[0078]
as1411和peg共缀合的gnp的合成
[0079]
使用先前报道的方案无菌合成4纳米(nm)柠檬酸盐封端的gnp[35,36]。硫醇修饰的as1411(sh-as1411)在购买时含有二硫键用于储存和稳定性,在缀合前通过将sh-as1411、1.0m dtt、0.25m磷酸盐缓冲液(pb)和纳米纯超纯水的所需混合物煮沸1小时然后再冷却1小时来分裂二硫键。使用illustranap-25dna重力柱和0.1m pb(作为洗脱剂)通过尺寸排阻色谱法分离sh-as1411。根据生产说明书,将sh-peg醇稀释在dmso中。然后,将分裂和纯化的sh-as1411和sh-peg醇以不同比例(见下段)与gnp缀合,生成双组分as1411/peg涂层。在96小时内逐步加入10x磷酸盐缓冲盐水(pbs),直至达到1x浓度,然后在水浴中进行10分钟的最大超声处理。以13,500g离心20分钟,然后进行三次1x pbs洗涤,并在每次洗涤后再次离心,以除去任何未缀合的组分。
[0080]
合成了多种peg/as1411共缀合的gnp制剂,其不同之处在于peg和as1411的负载比例。如通过紫外可见(uv-vis)光谱法所测量地,as1411在gnp上的最大可能负载量,保持恒定为胶体溶液中的金浓度的12倍(表示为12x)。将此12x负载分成多种peg:as1411比例,使得在本文全文中保留以下实验条件:peg无负载且as1411最大负载(0:1或12x)、peg最大负载且as1411无负载(1:0或0x),以及三种不同的as1411:peg负载比例(1:3或3x、1:1或6x、3:1或9x)。对于as1411低于12x最大值的制剂,引入peg以满足12x最大负载的要求。一旦确定最佳负载比例,即可按照与上述类似地合成带有sh-peg和cro序列的共缀合gnp以及荧光共缀合和对照的gnp(分别为sh-as1411-cy5或sh-cro-cy5,exc./em.650/670)。
[0081]
纳米颗粒表征
[0082]
用运行zetapals软件的nanobrookzetapals zeta电位分析仪(brookhaven instruments,holtsville,ny)测量所有的纳米颗粒类型的粒径(以纳米为单位)、ζ电位(以毫伏为单位)以及多分散指数(无单位)。由varian cary 50bio uv(agilent technologies,santa clara,ca)光谱仪报告的吸收光谱对缀合进行了验证。通过在1xpbs和1.0m dtt的混合物中处理72小时而从gnp分裂出寡核苷酸,然后通过uv-vis测量分裂和分离的寡核苷酸(利用illustra nap-25dna重力柱,以0.1m磷酸盐缓冲液作为洗脱剂),评估每个gnp制剂的寡核苷酸负载量。使用比尔定律由紫外测量结果计算寡核苷酸的摩尔数,并与胶体溶液中存在的金的摩尔数进行比较,以确定每个gnp的平均as1411或cro。
[0083]
细胞培养
[0084]
在含10%热灭活胎牛血清和1%青霉素/链霉素的达尔伯克改良伊格尔培养基(dmem)中培养u87mg。使用0.25%胰蛋白酶对所有传代培养物进行传代,并以5000细胞/cm2的最小密度进行接种。将u87mg以1000个细胞/孔的密度接种到无菌透明的聚苯乙烯96孔板或10mmmatek玻璃底面培养皿上。在培养前,使接种在玻璃底面培养皿上的细胞粘附1小时。在gnp处理之前,将接种在平板或培养皿上的u87mg培养2天,以使细胞适应培养条件。
[0085]
细胞毒性和特异性研究
[0086]
使用0-5000微摩尔(μm)as1411的纳米颗粒制剂及dmem,将96孔板中的细胞和对照孔培育72小时,不更换培养基。对照细胞用10μmas1411、代表最高金浓度的裸gnp进行处理,或者不处理。xtt吸光度的数据从运行softmaxpro 7.0软件的molecular devices spectramax m2光谱仪获得,并针对gnp对细胞板的干扰进行基线校正。通过双向anova分析确定gnp制剂对u87mg具有统计学显著性的细胞毒性。通过比较带有as1411的最优确定的共
缀合gnp的细胞毒性和带有cro的细胞毒性,验证了as1411的特异性。ic
50
(或有效抑制50%存活的浓度)分析使用针对windows的graphpad prism version 7.0.0,graphpad software(san diego,california;www.graphpad.com)以确定最优的共缀合gnp的有效性。
[0087]
显微镜研究
[0088]
在xtt处理前72小时,使用具有coolsnap hq ccd照相机(roper,duluth,ga)的nikon te200荧光显微镜(melville,ny)(带有nis elements软件)在96孔板中获得用gnp制剂和对照处理的u87mg的10x明场图像。使用配有活细胞室的nikon a1r光谱共聚焦显微镜验证了共缀合的cy5-as1411或cy5-cro gnp的细胞摄取和细胞毒性。将接种到matek培养皿上的u87mg以细胞毒性研究所报道的此前已确定的ic
50
进行处理,并以每30分钟1幅图像的速率在20x放大下成像72小时。对于每种情况,从5个独立的xy位置获取图像。然后使用nikon elements软件,将图像转换为.avi视频并观察粒子分布。对于所有情况,选择0、24、48和72小时的代表性照片。
[0089]
统计分析
[0090]
所有数据在microsoft excel中收集和处理。使用graphpad prism完成适当的统计检验,显著性水平为α=0.05。数据呈现为平均值+/-标准偏差。所报告的统计检验为带有bonferroni事后检验的双向anova。需要时描述样本大小。
[0091]
结果
[0092]
为确定gbm应用的peg-as1411-gnp的最优配置,将人类gbm代表细胞系(u87mg)暴露于具有不同peg和as1411组分负载比例的gnp。合成了多种peg/as1411共缀合gnp制剂,其不同之处在于peg和as1411的负载比例。peg是一种防污分子,由此保护颗粒免于蛋白质聚集,并用作表面改性剂以使gnp能够进一步修饰以进行额外的抗gbm治疗。如通过uv-vis光谱法所测量,as1411和peg在gnp上的最大可能负载量保持恒定为胶体溶液中存在的金浓度的12倍(表示为12x)。将此12x负载分成多种peg:as1411比例,使得在整个结果中保持以下实验条件:peg无负载且as1411最大负载(0:1或12x)、peg最大负载且as1411无负载(1:0或0x)以及三种不同的as1411:peg负载比例(1:3或3x、1:1或6x、3:1或9x)。对as1411低于12x最大值的制剂,引入peg满足最大负载要求。gnp的示意图(图1)示出了提议的局部剖视特征。然后,完成了细胞毒性和明视野成像,并结合颗粒合成特性确定gbm应用的最佳颗粒设计。为验证优化颗粒上的as1411特异性保留,用带有as1411或cro(对照寡核苷酸序列)的优化gnp制剂完成了细胞毒性研究。然后,完成了活细胞成像研究,验证了所优化设计的peg-as1411-gnp的总体摄取和分布。
[0093]
图2a和图2b分别示出了ζ电势(mv)和流体动力学尺寸(nm)测量值(mv)。幅度大于10表明更稳定的合成。这些数据显示最小程度的尺寸变化。
[0094]
多分散性指数如图2c所示。多分散性是无单位的,测量范围从0到1。每个aunp的as1411如图2d所示。
[0095]
dtt使得缀合的as1411分离。分离前后的紫外-可见光谱分析分别示于图2e和图2f。紫外-可见光谱显示了经金的表面等离子体共振(~520nm)和dna(~260nm)验证的负载。
[0096]
图3示出了共缀合(as1411和peg)的aunp对u87mg细胞代谢活性的影响。图4示出了共缀合的aunp对于这些细胞的ec50分析。图5示出了经颗粒处理的u87mg细胞的10x明视野
图像。xtt吸光度越低,代谢活性越低,细胞杀伤作用越大。
[0097]
图6示出了使用9x as/cro aunp处理后u87mg的体外代谢活性。图7为示出了9x共缀合aunp颗粒的ec50分析的曲线图。
[0098]
结果表明,与抗核仁素剂缀合的纳米颗粒相比,抗核仁素剂-peg缀合的纳米颗粒具有令人惊讶和意想不到的改进。特别是在2500nm和5000nm浓度as1411下,所有形式抗核仁素剂-peg缀合的纳米颗粒在杀死细胞上的效力几乎是抗核仁素剂缀合的纳米颗粒的2倍,如图3所示。这是令人惊讶和意想不到的,因为聚乙二醇化的益处原本仅预期在体内,而不是如此处所示的体外。此外,活细胞共聚焦研究已经验证了抗核仁素剂-peg缀合的纳米颗粒的选择性。预期在其他类型的癌症中也会有类似的结果。
[0099]
参考文献
[0100]
1.hendrik heinz,nanoparticle decoration with surfactants:molecular interactions,assembly,and applications;surface science reports,volume 72,issue 1,2017,pages 1-5.
[0101]
2.singh,priyanka et al,biological synthesis of nanoparticles from plants and microorganisms;trends in biotechnology,volume 34,issue 7,588-599.
[0102]
3.ding,y.,et al.,gold nanoparticles for nucleic acid delivery.molecular therapy,2014.22(6):p.1075-1083.
[0103]
4.roca,m.anda.j.haes,probing cells with noble metal nanoparticle aggregates.nanomedicine,2008.3(4):p.555-565.
[0104]
5.delong,r.k.,et al.,functionalized gold nanoparticles for the binding,stabilization,and delivery oftherapeutic dna,rna,and other biological macromolecules.nanotechnol sci appl,2010.3:p.53-63.
[0105]
6.sperling,r.a.,et al.,electrophoretic separation of nanoparticles with a discrete number of functional groups.advancedfunctional materials,2006.16(7):p.943-948.
[0106]
7.aslan,k.,c.c.luhrs,and v.h.p
é
rez-luna,controlled and reversible aggregation of biotinylated gold nanoparticles with streptavidin.the journal of physical chemistry b,2004.108(40):p.15631-15639.
[0107]
8.gole,a.and c.j.murphy,azide-derivatized gold nanorods:functional materials for"click"chemistry.langmuir,2008.24(1):p.266-72.
[0108]
9.brennan,j.l.,et al.,bionanoconjugation via click chemistry:the creation of functional hybrids of lipases and gold nanoparticles.bioconjug chem,2006.17(6):p.1373-5.
[0109]
10.goldshmit,y.,et al.,interfering with the interaction between erbb1,nucleolin and ras as a potential treatment for glioblastoma.oncotarget,2014.5(18):p.8602-13.
[0110]
11.benedetti,e.,et al.,nucleolin antagonist triggers autophagic cell death in human glioblastoma primary cells and decreased in vivo tumor growth in orthotopic brain tumor model.oncotarget,2015.6(39):p.42091-104.
temozolomide for glioblastoma.n engl j med,2005.352(10):p.987-96.
[0126]
27.ahmed,r.,et al.,malignant gliomas:current perspectives in diagnosis,treatment,and early response assessment using advanced quantitative imaging methods.cancer manag res,2014.6:p.149-70.
[0127]
28.wadajkar,a.s.,et al.,tumor-targeted nanotherapeutics:overcoming treatment barriers for glioblastoma.wiley interdiscip rev nanomed nanobiotechnol,2017.9(4).
[0128]
29.fernandes,c.,et al.,current standards of care in glioblastoma therapy,in glioblastoma,s.de vleeschouwer,editor.2017,codon publications
[0129]
30.hart,m.g.,et al.,temozolomide for high grade glioma.cochrane database of systematic reviews,2013(4).
[0130]
31.lee,y.s.anda.dutta,micrornas in cancer.annu rev pathol,2009.4:p.199-227.
[0131]
32.moller,h.g.,et al.,a systematic review of microrna in glioblastoma multiforme:micro-modulators in the mesenchymal mode of migration and invasion.mol neurobiol,2013.47(1):p.131-44.
[0132]
33.shea,a.,et al.,micrornas in glioblastoma multiforme pathogenesis and therapeutics.cancer med,2016.5(8):p.1917-46.
[0133]
34.comprehensive genomic characterization defines human glioblastoma genes and core pathways.nature,2008.455(7216):p.1061-8.
[0134]
35.kim,h.,et al.,integrative genome analysis reveals an oncomir/oncogene cluster regulating glioblastoma survivorship.proc natl acad sci u s a,2010.107(5):p.2183-8.
[0135]
36.li,y.,et al.,microrna-34a inhibits glioblastoma growth by targeting multiple oncogenes.cancer res,2009.69(19):p.7569-76.
[0136]
37.bandman o,yue h,corley n c,shah p,“human nucleolin-like protein”u.s.pat.no.5,932,475(3 aug.1999).
[0137]
38.bates p j,miller d m,trent j o,xu x,“a new method for the diagnosis and prognosis of malignant diseases”international application,int’l pub.no.wo 03/086174a2(23 oct.2003).
[0138]
39.bates p j,miller d m,trent j o,xu x,“method for the diagnosis and prognosis of malignant diseases”u.s.patent app.pub.,pub.no.us 2005/0053607 a1(10 mar.2005).
[0139]
40.bates p j,kahlon j b,thomas s d,trent j o,miller d m,"antiproliferative activity of g-rich oligonucleotides correlates with protein binding"j.biol.chem.274:26369-77(1999).
[0140]
41.reyes-reyes e m,teng y,bates p j,“a new paradigm for aptamer therapeutic as1411 action:uptake by macropinocytosis and its stimulation by a nucleolin-dependent mechanism”cancer res 70(21):8617-29(2010).
[0141]
42.stedman,t.l.2000.stedman's medical dictionary.lippincott williams&wilkins,philadelphia.xxxvi,[127],2098.
[0142]
43.miller d m,bates p j,trent j o,xu x,“method for the diagnosis and prognosis of malignant diseases”u.s.patentapp.pub.,pub.no.us 2003/0194754 a1(16 oct.2003).
[0143]
44.cooper et al.[2014],front.chem.14,2,86.
[0144]
45.alkilany,a.m.and c.j.murphy,toxicity and cellular uptake of gold nanoparticles:what we have learned so far?journal of nanoparticle research,2010.12(7):p.2313-2333.
[0145]
46.guo,j.et al.,aptamer-functionalized peg-plga nanoparticles for enhanced anti-glioma drug delivery.biomaterials 32(2011)8010-8020.
[0146]
47.takafuji,y.,jo,j-i and tabata,y.simple peg modification of dna aptamer based on copper ion coordination for tumor targeting.j.biomaterials science 22(2011)1179-1195.
[0147]
48.aravind,a.et al.,as1411 aptamer tagged plga-lecithin-peg nanoparticles for tumor cell targeting and drug delivery.biotechnology and bioengineering 109(11)pp.2920-2931(november 2012).
[0148]
49.malik,m.t.,et al.as1411-conjugated gold nanospheres and their potential for breast cancer therapy.oncotarget 6(26)pp.22270-22281(2015).
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1