动态血糖监测系统传感器及其制备方法与流程
1.本发明涉及传感器技术领域,尤其是涉及一种动态血糖监测系统传感器及其制备方法。
背景技术:
2.传感器是动态血糖监测系统(cgms)的核心组件之一,其作用是在体内产生葡萄糖浓度依赖的电流信号。传感器的性能直接影响产品的最终质量,它制备的难易程度直接影响产品的产能高低。因此,如何快速、高效、稳定的制备传感器是一个非常关键的问题。
3.现有技术中,传感器的制备主要以dexcom、abbott和medtronic三家公司的制备方法为代表。其中,dexcom公司的传感器主要以丝材为基础,其工艺繁杂,制备过程中只能一根一根做,产能较低,若想扩大产能只能通过并联很多生产线,这样无疑使得成本大幅度增加。abbott公司的传感器的制备方法中涉及到打孔、至少6层套印、激光切割、碳注等高精度、高难度的加工工艺,对设备和工艺的要求较高,导致生产过程中的工艺控制需要非常严格,且设备昂贵,成本高;另外,由于套印偏差的缘故,印刷的版面不能做太大,否则丝网板的形变会导致套印无法满足要求,故产能也无法有效的提升。medtronic公司的传感器需要制备过程图形化,图形化可选的方案包括掩板、激光消蚀等,但无论是哪种图形化方案,制备的成本都比较高。
4.有鉴于此,特提出本发明以解决上述技术问题中的至少一个。
技术实现要素:
5.本发明的第一目的在于提供一种动态血糖监测系统传感器的制备方法,以缓解现有技术中存在的上述技术问题。
6.本发明的第二目的在于提供一种动态血糖监测系统传感器。
7.为了实现上述目的,本发明的技术方案为:
8.本发明提供了一种动态血糖监测系统传感器的制备方法,包括以下步骤:
9.(a)提供一柔性基板;
10.在所述柔性基板的第一侧面上形成工作电极,在所述柔性基板的第二侧面上形成对电极;
11.(b)在所述工作电极的部分区域形成酶层并使其固定化,得到电极基材;
12.(c)将电极基材进行裁切并形成外膜,得到动态血糖监测系统传感器。
13.进一步的,步骤(a)中,所述柔性基板的材质包括聚酰亚胺、聚酯、聚氨酯或聚乙烯中的任意一种。
14.进一步的,步骤(a)中,形成所述工作电极的材料包括铂、碳、石墨、银、氯化银、钽、金、钛、钯、铱、溴化银、碘化银或氯化汞中的任意一种或至少两种的组合。
15.进一步的,步骤(a)中,形成所述对电极的材料包括碳、石墨、铂、银、氯化银、钽、金、钛、钯、铱、溴化银、碘化银或氯化汞中的任意一种或至少两种的组合。
16.进一步的,步骤(b)中,所述酶层包括葡萄糖氧化酶层,所述酶层的厚度为5-50000nm。
17.进一步的,步骤(b)中,在所述工作电极的部分区域形成酶层并使其固定化,然后在所述酶层的一侧形成绝缘层,得到电极基材;
18.或,在所述工作电极的部分区域形成绝缘层后再形成酶层,并使酶层固定化,得到电极基材。
19.进一步的,步骤(c)中,先将电极基材进行裁切i以使其具有梳齿结构,然后在电极基材的酶层上形成外膜后,再进行裁切ⅱ以使电极基材的各梳齿彼此分离,得到动态血糖监测系统传感器;
20.或,步骤(c)中,先将电极基材进行裁切i以使其具有梳齿结构,再进行裁切ⅱ以使电极基材的各梳齿彼此分离,然后在各梳齿的酶层上形成外膜,得到动态血糖监测系统传感器。
21.进一步的,步骤(c)中,将电极基材进行裁切后采用具有生物相容性的热缩管进行绝缘处理,再形成外膜;
22.优选的,用于形成外膜的外膜液包括nafion、聚氨酯、聚碳酸脂、聚氯乙烯、聚乙烯或聚苯乙烯中的任意一种或者至少两种的组合。
23.进一步的,步骤(c)中,形成外膜后还包括形成保护膜的步骤,用于形成保护膜的保护液包括聚氨酯、聚碳酸脂、聚氯乙烯、聚乙烯、聚苯乙烯或硅烷中的任意一种或者至少两种的组合。
24.本发明提供了一种动态血糖监测系统传感器,采用上述动态血糖监测系统传感器的制备方法制得。
25.与现有技术相比,本发明的有益效果为:
26.(1)本发明提供了一种动态血糖监测系统传感器的制备方法,先将工作电极和对电极分别设置于柔性基板的第一侧面和第二侧面上,再将酶层设置于工作电极上,然后进行裁切和形成外膜,得到动态血糖监测系统传感器;其中,将工作电极和对电极设置于柔性基板两个不同的侧面上,使得电极通过位置进行区分而无须进行图形化,且由于采用版面较大的柔性基板进行制备,可实现产能的提升;先进行酶层设置再进行裁切,由于柔性基板是一体的,可使得酶层形成过程中试剂分散均一性高,受“咖啡环”效应和酶层台阶的影响较小,从而提高酶层的各向同性,也大大降低了制备难度。另外,该制备方法使用版面较大的柔性基材,完全不需要考虑套位的过程。且该制备方法不需要高精度的激光切割、高精度的印刷机等设备,工艺简单,生产成本低。
27.(2)本发明提供了一种动态血糖监测系统传感器,采用上述动态血糖监测系统传感器的制备方法制得。鉴于上述制备方法所具有的优势,使得该动态血糖监测系统传感器单批次产量大幅提高,同时动态血糖监测系统传感器监测的稳定性以及准确性均有明显提升。
附图说明
28.为了更清楚地说明本发明具体实施方式或现有技术中的技术方案,下面将对具体实施方式或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的
附图是本发明的一些实施方式,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他的附图。
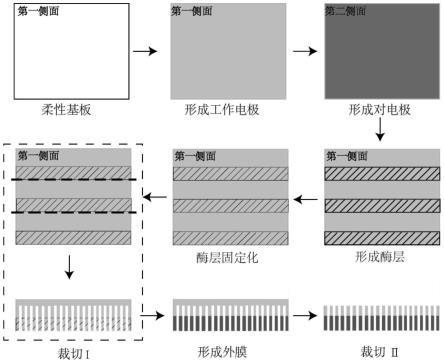
29.图1为本发明实施例1提供的一种动态血糖监测系统传感器的制备方法。
具体实施方式
30.下面将结合实施例对本发明的技术方案进行清楚、完整地描述,显然,所描述的实施例是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。在本发明的描述中,术语“第一”、“第二”等仅用于区分描述,而不能理解为指示或暗示相对重要性。
31.现有技术中通常将传感器基材进行图形化(切割)后再进行酶层的设置,但发明人在实际中发现,采用现有技术制备的传感器中一部分酶层会出现各项异性的问题,该问题的出现会导致形成不均匀的酶层,反应区域不可控,影响电极性能,进而影响传感器监测的稳定性以及准确性。为探寻这一问题产生的原因,发明人通过大量的创造性劳动后发现,当酶层点液的大小大于电极大小时会存在咖啡环效应和试剂(形成酶层的溶液)点液不均一,从而使得酶层以致传感器出现各项异性(未切割和切割后的部分会有台阶)的问题。若使酶层点液的大小小于图形化(切割)后的电极尺寸时,此时咖啡环效应虽然不明显,但是对点液量控制的精度和对位的精度要求就会比较高,大大增加了制备难度。为了解决上述问题,特提出本发明。
32.根据本发明的第一个方面,提供了一种动态血糖监测系统传感器的制备方法,包括以下步骤:
33.(a)提供一柔性基板;
34.在柔性基板的第一侧面上形成工作电极,在柔性基板的第二侧面上形成对电极;
35.(b)在工作电极的部分区域形成酶层并使其固定化,得到电极基材;
36.(c)将电极基材进行裁切并形成外膜,得到动态血糖监测系统传感器。
37.具体的,步骤(a)中,采用柔性基板可以为动态血糖监测系统传感器提供一个柔性的基底,使得传感器柔性可弯曲,在植入生物体内减少不适感。
38.同时,在确保柔性基板的尺寸满足后续加工的前提下,选用尺寸(版面)尽量大的柔性基板有利于传感器的规模制备,实现产能的提升。柔性基板的长度和宽度可为数百毫米。典型但非限制性的柔性基板的尺寸(长*宽)为400*150mm。
39.工作电极和对电极分别设置于柔性基板的两个侧面(第一侧面和第二侧面)上。第一侧面和第二侧面可以理解为柔性基板的正反面。工作电极和对电极均为独立的电极,互不导通。
40.步骤(b)中,经过固定化的酶层设置于工作电极上,并使工作电极的部分暴露。
41.步骤(c)中,由于电极基材的尺寸较大,故根据所需要形状尺寸将其进行裁切后并形成外膜后,得到动态血糖监测系统传感器。需要说明的是,电极基材的裁切和形成外膜的步骤不分先后,根据实际裁切方式进行确定。
42.外膜可包裹住电极基材上的酶层,防止传感器使用过程中出现酶泄漏,影响传感器性能。
43.本发明提供的动态血糖监测系统传感器的制备方法,先将工作电极和对电极分别设置于柔性基板的第一侧面和第二侧面上,再将酶层设置于工作电极上,然后进行裁切和形成外膜,得到动态血糖监测系统传感器;其中,将工作电极和对电极设置于柔性基板两个不同的侧面上,使得电极通过位置进行区分而无须进行图形化,且由于采用版面较大的柔性基板进行制备,可实现产能的提升;先进行酶层设置再进行裁切,由于柔性基板是一体的,可使得酶层形成过程中试剂分散均一性高,受“咖啡环”效应和酶层台阶的影响较小,从而提高酶层的各向同性,进而提高该动态血糖监测系统传感器监测的稳定性以及准确性,同时也大大降低了制备难度。另外,该制备方法使用版面较大的柔性基材,完全不需要考虑套位的过程。且该制备方法不需要高精度的激光切割、高精度的印刷机等设备,工艺简单,生产成本低。
44.作为本发明的一种可选实施方式,步骤(a)中,柔性基板的材质包括聚酰亚胺、聚酯、聚氨酯或聚乙烯中的任意一种。
45.作为本发明的一种可选实施方式,柔性基板的长度为150-500mm,宽度为150-500mm。
46.通过对柔性基板材质以及尺寸的限定,使得在满足设备生产的同时可生产尽可能多的传感器。
47.作为本发明的一种可选实施方式,步骤(a)中,形成工作电极的材料包括铂、碳、石墨、银、氯化银、钽、金、钛、钯、铱、溴化银、碘化银或氯化汞中的任意一种或至少两种的组合,优选为铂;
48.优选的,工作电极的厚度为1-1000nm;典型但非限制性的工作电极的厚度为1nm、10nm、50nm、100nm、200nm、500nm、600nm、800nm或1000nm。
49.优选的,工作电极在第一侧面的形成方式包括物理气相沉积、化学气相沉积、电镀、浸涂或丝网印刷中的任意一种。
50.其中,物理气相沉积又包括溅射或蒸镀等方法。
51.作为本发明的一种可选实施方式,步骤(a)中,形成所述对电极的材料包括碳、石墨、铂、银、氯化银、钽、金、钛、钯、铱、溴化银、碘化银或氯化汞中的任意一种或至少两种的组合,优选包括银和氯化银;
52.优选的,对电极的厚度为1-1000nm;
53.优选的,对电极在第二侧面上的形成方式包括物理气相沉积、化学气相沉积、电镀、浸涂或丝网印刷中的任意一种。
54.当对电极为银/氯化银电极时,也可以通过物理气相沉积、化学气相沉积、电镀、浸涂或丝网印刷的方式先制备银层,而后通过氯化的方式最终形成银/氯化银电极。上述氯化的方式可包括化学法、电化学法或掺杂法等。
55.通过对工作电极和对电极具体种类、厚度以及形成方式的限定,使得该传感器达到较优的状态,从而达到较高的测量精度、较长的稳定性。
56.作为本发明的一种可选实施方式,步骤(b)中,酶层包括但不限于葡萄糖氧化酶层。酶层的形成可以采用涂布、印刷、点液等方式进行。
57.作为本发明的一种可选实施方式,步骤(b)中,采用交联的方式使酶层固定化。
58.优选的,可将形成有酶层的柔性基板放置在密闭的交联剂气体环境下进行交联固
化;
59.优选的,交联剂包括戊二醛。
60.在工作电极上还可形成绝缘层。
61.作为本发明的一种可选实施方式,步骤(b)中,在工作电极的部分区域形成酶层并使其固定化,然后在酶层的一侧形成绝缘层,得到电极基材;
62.或,在工作电极的部分区域形成绝缘层后再形成酶层,并使酶层固定化,得到电极基材。
63.绝缘层的结构可以在工作电极和对电极的外侧面均采用,也可在工作电极和对电极的一侧面采用;工作电极和对电极两者外侧印刷的绝缘层可以完全相同,也不用完全相同;绝缘层可以根据实际需要改变形成方式、所在位置和形状大小,甚至可以不设置绝缘层。
64.绝缘层可将工作电极和对电极之间进行电气绝缘,并控制工作电极面积保持一定,而无需通过植入深度来控制工作电极面积。
65.优选的,绝缘层的材质包括氮化硅、氧化硅、聚乙烯、聚氯乙烯、聚丙烯、聚四氟乙烯、乙烯-四氟乙烯共聚物或聚酰亚胺中的任意一种或至少两种的组合。
66.作为本发明的一种可选实施方式,绝缘层为氮化硅绝缘层。
67.作为本发明的一种可选实施方式,绝缘层采用物理气相沉积、化学气相沉积、电镀、浸涂或丝网印刷的方式形成。
68.由于电极基材是一体的,故需要根据传感器形状尺寸大小对其进行裁切,裁切的方式可以有多种。
69.作为本发明的一种可选实施方式,步骤(c)中,先将电极基材进行裁切i以使其具有梳齿结构,然后在电极基材的酶层上形成外膜后,再进行裁切ⅱ以使电极基材的各梳齿彼此分离,即将批量生产的电极基材分割开,得到动态血糖监测系统传感器。
70.作为本发明的另一种可选实施方式,步骤(c)中,先将电极基材进行裁切i以使其具有梳齿结构,再进行裁切ⅱ以使电极基材的各梳齿彼此分离,然后在各梳齿的酶层上形成外膜,得到动态血糖监测系统传感器。
71.上述梳齿结构包括若干个平行且间隔设置的梳齿和连接各梳齿的连接部,梳齿的大小与单个动态血糖监测系统传感器大小保持一致。将梳齿的两端分别称为根部和顶部,梳齿的顶部通过连接部相互连接使梳齿结构成为一体,而梳齿的根部是彼此分离的。酶层位于梳齿根部的部分区域内,也可位于梳齿的顶部或其他区域。需要说明的是,梳齿的形状不作具体限定,附图中的梳齿形状仅为一种示例,可根据实际传感器要求设置梳齿的形状以及大小。
72.可将电极基材置于用于形成外膜的外膜液中以形成外膜,然后再将进行裁切ⅱ以使电极基材的各梳齿彼此分离,得到动态血糖监测系统传感器。或者,先将电极基材进行裁切i以使其具有梳齿结构后,直接进行裁切ⅱ以使电极基材的各梳齿彼此分离,然后再将其置于用于形成外膜的外膜液中以形成外膜,所形成的外膜需要将梳齿上的酶层覆盖即可。
73.作为本发明的一种可选实施方式,外膜的形成方式包括浸涂。
74.作为本发明的一种可选实施方式,用于形成外膜的外膜液包括nafion、聚氨酯、聚碳酸脂、聚氯乙烯、聚乙烯或聚苯乙烯中的任意一种或者至少两种的组合。
75.浸涂的深度以保证外膜液将梳齿上的酶层覆盖即可,优选的,电极基材在外膜液中的浸涂深度为0.1-10mm。典型但非限制性的浸涂深度为0.1mm、0.5mm、1mm、2mm、4mm、5mm、6mm、8mm或10mm。
76.作为本发明的一种可选实施方式,步骤(c)中,将电极基材进行裁切后采用具有生物相容性的热缩管进行绝缘处理,再形成外膜。
77.采用具有生物相容性的热缩管进行绝缘处理,可以控制工作电极面积一定,保证每个传感器的一致性。
78.作为本发明的一种可选实施方式,热缩管的材质包括聚乙烯(pe)、聚氯乙烯(pvc)、聚对苯二甲酸乙二醇酯(pet)、铁氟龙或乙烯-醋酸乙烯共聚物(eva)中的任意一种或至少两种的组合。
79.作为本发明的一种可选实施方式,步骤(c)中,形成外膜后还包括形成保护膜的步骤。保护膜用于增加尖端保护,防止刺入人体时破坏外膜和酶层。
80.优选的,用于形成保护膜的保护液包括聚氨酯、聚碳酸脂、聚氯乙烯、聚乙烯、聚苯乙烯或硅烷中的任意一种或者至少两种的组合;
81.优选的,形成保护膜的方式包括浸涂;
82.优选的,电极基材在保护液中的浸涂深度为0.1-10mm。典型但非限制性的浸涂深度为0.1mm、0.5mm、1mm、2mm、4mm、5mm、6mm、8mm或10mm。
83.根据本发明的第二个方面,提供了一种动态血糖监测系统传感器,采用上述动态血糖监测系统传感器的制备方法制得。
84.鉴于上述动态血糖监测系统传感器的制备方法所具有的优势,使得该动态血糖监测系统传感器单批次产能大幅提高,单批次产能可达50-300万pcs,同时动态血糖监测系统传感器监测的稳定性以及准确性均有明显提升。
85.下面将结合实施例和对比例对本发明的技术方案进行进一步地说明。
86.实施例1
87.本实施例提供了一种动态血糖监测系统传感器的制备方法,工艺流程图如图1所示,包括以下步骤:
88.(a)提供一柔性基板;柔性基板的尺寸为400*150mm,柔性基板的材质为聚酰亚胺;
89.在柔性基板的第一侧面上形成工作电极,在柔性基板的第二侧面上形成对电极;
90.其中,工作电极为铂电极,铂电极采用丝网印刷工艺形成,工作电极的厚度为100nm;对电极为银/氯化银电极,对电极采用丝网印刷工艺形成,对电极的厚度为100nm。
91.(b)在工作电极的部分区域形成酶层,酶层的厚度为100nm,然后将形成酶层的柔性基板放置于密闭的交联剂气体环境下进行交联,以使酶层固定化,得到电极基材;其中,酶层为葡萄糖氧化酶层,酶层的形成方式为点液,交联剂为戊二醛;
92.(c)将电极基材先进行裁切使其长度为400mm、宽度为30mm,再进行裁切以使其具有梳齿结构,梳齿结构中的锯齿的长度为25mm,宽度为0.3mm;
93.将裁切后具有梳齿结构的电极基材置于外膜液(nafion)中进行浸涂以形成外膜,电极基材在外膜液中的浸涂深度为3mm;
94.将形成外膜的电极基材进行裁切,以使电极基材的各梳齿彼此分离,得到动态血糖监测系统传感器。
95.实施例2
96.本实施例提供了一种动态血糖监测系统传感器的制备方法,除了步骤(b)中在工作电极的部分区域形成酶层,酶层的厚度为100nm,然后将形成酶层的柔性基板放置于密闭的交联剂气体环境下进行交联,以使酶层固定化,然后在远离酶层靠近裁切截面形成绝缘层,得到电极基材;其中,酶层为葡萄糖氧化酶层,酶层的形成方式为点液,交联剂为戊二醛,绝缘层为氮化硅绝缘层,绝缘层的厚度为100mm,绝缘层采用浸涂的方式形成;
97.其余步骤以及工艺参数与实施例1相同。
98.实施例3
99.本实施例提供了一种动态血糖监测系统传感器的制备方法,除了步骤(c)中将裁切后具有梳齿结构的电极基材采用具有生物相容性的热缩管进行绝缘处理,再置于外膜液中进行浸涂以形成外膜;其中,热缩管的材料为聚乙烯,处理方法为将一定长度的热缩管套设在具有梳齿结构的电极基材上,然后用加热工具(热风枪)对准热缩管进行均匀的加热,使其逐渐收缩;
100.其余步骤以及工艺参数与实施例1相同。
101.实施例4
102.本实施例提供了一种动态血糖监测系统传感器的制备方法,除了步骤(c)中将形成外膜的电极基材置于保护液中进行浸涂以形成保护膜,然后再将形成保护膜的电极基材进行裁切;其中,电极基材在保护液中的浸涂深度为5mm,用于形成保护膜的保护液包括聚氨酯;
103.其余步骤以及工艺参数与实施例1相同。
104.实施例5
105.本实施例提供了一种动态血糖监测系统传感器的制备方法,包括以下步骤:
106.(a)提供一柔性基板;柔性基板的尺寸为400*150mm,柔性基板的材质为聚酰亚胺;
107.在柔性基板的第一侧面上形成工作电极,在柔性基板的第二侧面上形成对电极;
108.其中,工作电极为铂电极,铂电极采用磁控溅射工艺形成,工作电极的厚度为10nm;对电极为银/氯化银电极,对电极采用狭缝精密涂布工艺形成,对电极的厚度为10nm。
109.(b)在工作电极的部分区域形成酶层,酶层的厚度为100nm,然后将形成酶层的柔性基板放置于密闭的交联剂气体环境下进行交联,以使酶层固定化,得到电极基材;其中,酶层为葡萄糖氧化酶层,酶层的形成方式为点液,交联剂为戊二醛;
110.(c)将电极基材先进行裁切使其长度为400mm、宽度为30mm,再进行裁切以使其具有梳齿结构,梳齿结构中的锯齿的长度为25mm,宽度为0.3mm;
111.将电极基材再进行裁切,电极基材的各梳齿彼此分离;
112.将裁切后的各梳齿置于外膜液中进行浸涂以在各梳齿的酶层上形成外膜,各梳齿在外膜液中的浸涂深度为3mm,得到动态血糖监测系统传感器。
113.对比例1
114.本对比例提供了一种动态血糖监测系统传感器的制备方法,包括以下步骤:
115.(a)提供一柔性基板;柔性基板的尺寸为400*150mm,柔性基板的材质为聚酰亚胺;
116.在柔性基板的第一侧面上形成工作电极,在柔性基板的第二侧面上形成对电极;
117.其中,工作电极为铂电极,铂电极采用丝网印刷工艺形成,工作电极的厚度为
100nm;对电极为银/氯化银电极,对电极采用丝网印刷工艺形成,对电极的厚度为100nm。
118.(b)将柔性基板先进行裁切使其长度为400mm、宽度为30mm,再进行裁切以使其具有梳齿结构,梳齿结构中的锯齿的长度为25mm,宽度为0.3mm;
119.然后将具有梳齿结构的柔性基板进行裁切,以使柔性基板的各梳齿彼此分离;
120.(c)在各梳齿工作电极的部分区域形成酶层,酶层的厚度为100nm,然后将形成酶层的梳齿放置于密闭的交联剂气体环境下进行交联,以使酶层固定化,得到电极基材;其中,酶层为葡萄糖氧化酶层,酶层的形成方式为点液,交联剂为戊二醛;
121.将各电极基材置于外膜液(nafion)中进行浸涂以形成外膜,电极基材在外膜液中的浸涂深度为3mm,得到动态血糖监测系统传感器。
122.实验例1
123.对各实施例和对比例中所述方法制备出的传感器植入人体后进行监测,具体结果如表1所示。其中,动态血糖监测系统传感器的准确性可通过相对差异的平均绝对值(mard)来衡量的,mard代表传感器葡萄糖浓度值和ysi生化分析仪测得的配对血糖值之间的平均相对差异;线性范围是指动态血糖监测系统传感器在有效使用时间内体外葡萄糖测量的范围;产能是指同一批次传感器制备的数量。
124.表1
[0125][0126]
从表1中数据可以看出,相较于对比例而言,采用本发明各实施提供的制备方法制得的动态血糖监测系统传感器的准确性更高、线性范围更宽及产能更高。
[0127]
最后应说明的是:以上各实施例仅用以说明本发明的技术方案,而非对其限制;尽管参照前述各实施例对本发明进行了详细的说明,本领域的普通技术人员应当理解:其依然可以对前述各实施例所记载的技术方案进行修改,或者对其中部分或者全部技术特征进行等同替换;而这些修改或者替换,并不使相应技术方案的本质脱离本发明各实施例技术方案的范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1