非天然人参皂苷3β,20S-Di-O-Glc-DM治疗胰腺癌的用途
非天然人参皂苷3
β
,20s-di-o-glc-dm治疗胰腺癌的用途
技术领域
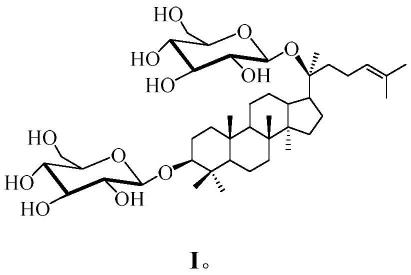
1.本发明涉及非天然人参皂苷3β,20s-di-o-d-吡喃葡萄糖基-达玛-24-烯-3β,20s-二醇(3β,20s-di-o-β-d-glucopyranosyl-dammar-24-ene-3β,20s-diol,简称为3β,20s-di-o-glc-dm)在制备抗胰腺癌药物中的应用,属于医药技术领域。
背景技术:
2.国际癌症研究机构(iarc)最新资料显示,2020年全球因胰腺癌导致的死亡人数约为47万,位居第七位。胰腺癌是我国常见的恶性肿瘤,因其早期症状不明显,所以临床中大部分诊断为胰腺癌的患者多为晚期阶段,就诊时已失去手术时机,是诊断和治疗都很困难的消化道恶性肿瘤,在肿瘤领域素有“癌症之王”的称号。胰腺癌的发病率和死亡率近年来明显上升,其早期的确诊率不高,恶性程度高,手术死亡率较高,预后差,五年生存率低于5%,加之缺乏理想的治疗靶点,治疗也较为困难。目前根本的治疗原则仍然是以外科手术治疗为主,结合放化疗等综合治疗。但无论是手术、介入治疗或是化疗,对胰腺癌的治疗效果都不理想,吉西他滨是胰腺癌目前临床首选化疗药物,可通过抑制dna连接而起到抑制肿瘤细胞复制的作用,但单独吉西他滨化疗的有效率低于15%,目前临床正探究以吉西他滨为基础的联合化疗方案。近年来分子靶向药物已经成为治疗胰腺癌新的热点,目前正在研发针对表皮生长因子受体egfr、血管内皮生长因子vegf等靶点的药物。基因治疗多数仍然停留在临床前期,少有进入临床ⅰ期或ⅱ期试验。免疫疗法也是当前热门的肿瘤治疗手段,免疫检查点抑制剂对多种恶性肿瘤具有较好疗效。单独免疫疗法在胰腺癌中的收效甚微,但免疫调节剂治疗、疫苗治疗、过继免疫治疗和免疫检查点抑制剂等免疫疗法与其他治疗方法的联用在治疗胰腺癌中取得了一定的效果,是未来胰腺癌治疗的发展方向之一。
3.药理学研究证明,人参的主要活性成分是人参皂苷。人参皂苷属于三萜类化合物,是人参属植物(如人参、三七或西洋参等)的一类重要次级代谢产物。根据苷元基本骨架不同,人参皂苷可分为两种类型:一类是达玛烷型四环三萜类皂苷;另一类是齐墩果烷型五环三萜类皂苷。达玛烷型皂苷在人参皂苷中占大多数,是其中的主要活性成分。达玛烷型皂苷包括原人参二醇型皂苷和原人参三醇型皂苷。迄今为止,从人参属植物中分离得到的达玛烷型皂苷已达110多种。
4.达玛烷型人参皂苷的抗肿瘤活性受苷元羟基和取代糖基的位置及数量影响。不同的人参皂苷具有不同的药理活性。作为原人参二醇的直接前体,达玛烯二醇-ii在c3和c20位各有一个羟基,这两个羟基都可以被糖基化,但在人参中从未分离到过达玛烯二醇-ii糖苷。我们通过合成生物学技术实现了在达玛烯二醇-ii的c3位和c20位分别连接一个葡萄糖基,获得非天然人参皂苷3β,20s-di-o-glc-dm,其与天然人参皂苷结构不同,具有较好的抗胰腺癌活性。
技术实现要素:
5.本发明解决的技术问题是提供了式i所示化合物或其药学上可接受的盐在制备抗
胰腺癌药物中的应用。
6.为解决本发明的技术问题,本发明提供了如下技术方案:
7.本发明的第一方面提供了式i所示化合物或其药学上可接受的盐在制备用于预防或治疗胰腺癌的药物中的应用,
[0008][0009]
式i所示化合物的化学名为3β,20s-di-o-β-d-吡喃葡萄糖基-达玛-24-烯-3β,20s-二醇(3β,20s-di-o-β-d-glucopyranosyl-dammar-24-ene-3β,20s-diol,在本文中也简称为3β,20s-di-o-glc-dm)。
[0010]
所述胰腺癌包括导管腺癌、胰母细胞瘤、大嗜酸性颗粒细胞性癌或腺泡细胞癌。
[0011]
本发明的另一方面提供了药物组合物在制备用于预防或治疗胰腺癌的药物中的应用,所述药物组合物包含式i所示化合物及其药学上可接受的盐,以及至少一种药学上可接受的载体。
[0012]
所述的药物组合物的剂型包括片剂、胶囊、粉剂、颗粒剂、滴丸、糊剂、散剂。
[0013]
本文所述的化合物、组合物、应用和方法可施用至患有或被诊断为患有胰腺癌的受试者。本领域技术人员已知用于将本文所述的式i所示化合物或其药学上可接受的盐给予至受试者的多种手段。此类给药手段可以包括但不限于:口服给予、胃肠外给予、静脉内给予、肌内给予、皮下给予、经真皮给予、气道给予(气溶胶)、肺部给予、皮肤给予、局部给予、注射给予或瘤内给予。给予可以是局部的或全身性的。在一些实施方式中,优选的给予是口服给予。
[0014]
在一些实施方式中,式i所示化合物或其药学上可接受的盐是作为唯一的活性成分单独给予患者的。
[0015]
在一些实施方式中,在给予式i所示化合物或其药学上可接受的盐之前、之后或同时,可以进一步向受试者给予第二试剂和/或治疗,例如作为组合治疗的一部分。第二试剂和/或治疗可以包括化学治疗剂和/或放射疗法和/或外科手术。
[0016]
本文所使用的“化学治疗剂”是指降低或减少癌细胞的生长、生存和/或转移的物质。化学治疗剂可以包括毒素、小分子和/或多肽。第二试剂和/或治疗的非限制性实例可包括:放射疗法;外科手术;紫杉烷类抗肿瘤药、长春碱类抗肿瘤药、铂配合物和/或嘧啶拮抗物。
[0017]
在本发明的一些实施方式中,紫杉烷类抗肿瘤药包括但不限于紫杉醇和多西紫杉醇;长春碱类抗肿瘤药包括但不限于长春碱、长春新碱、长春地辛和长春瑞滨;铂配合物包括但不限于米铂、顺铂、卡铂、奈达铂和奥沙利铂;嘧啶拮抗物包括但不限于阿糖胞苷、安西他滨、卡培他滨、吉西他滨、氟尿嘧啶、双呋氟尿嘧啶、去氧氟尿苷、替加氟和卡莫氟。
[0018]
此外,治疗的方法可以进一步包括使用放射物或放射疗法。此外,治疗的方法可以进一步包括使用外科手术治疗。
[0019]
在某些实施方式中,本文所述的式i所示化合物或其药学上可接受的盐的有效剂量可以一次给予患者。在某些实施方式中,式i所示化合物或其药学上可接受的盐的有效剂量可以重复给予患者。对于全身给予,可以给予患者治疗有效量的式i所示化合物或其药学上可接受的盐,包括0.1mg/kg至50mg/kg,例如0.1mg/kg、0.5mg/kg、1.0mg/kg、2.0mg/kg、2.5mg/kg、5mg/kg、10mg/kg、15mg/kg、20mg/kg、25mg/kg、30mg/kg、40mg/kg、50mg/kg或更多。
[0020]
在一些实施方式中,在初始治疗方案之后,可以在不太频繁的基础上给予治疗。例如,在每两周治疗进行三个月后,治疗可每月重复一次至六个月或一年或更长时间。根据本文所述的方法的治疗可以降低肿瘤标志物的水平或病症的症状,例如降低至少10%、至少15%、至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少70%、至少80%、至少90%或更多。
[0021]
给予式i所示化合物或其药学上可接受的盐的量可根据疾病的严重程度、疾病的响应、任何治疗相关的毒性、患者的年龄和健康状态来确定。
[0022]
本文所述的式i所示化合物或其药学上可接受的盐的剂量可以由临床医师确定并在必要时进行调整,以适应观察到的治疗效果。至于治疗持续时间和治疗的频率,一般由熟练的临床医师监测受试者以确定何时治疗以提供治疗效果,并确定是否增加或减少剂量、增加或降低给予频率、不继续治疗、恢复治疗或对治疗方案作出其它改变。给药计划可以每周一次至每天一次变化,这取决于许多临床因素,例如受试者对组分的敏感性。活性作用期望的剂量可一次给予或分成亚剂量,例如2-4个亚剂量并在一段时间内(例如,以一天内的适当时间间隔或其它适当的计划)给予。在一些实施方式中,给予可以是长期的,例如在数周或数月的时间段内每天一次或多次给药和/或治疗。给药和/或治疗计划的实例是在1周、2周、3周、4周、1个月、2个月、3个月、4个月、5个月、6个月或更长的时间段内,每天给予一次、每天两次、每天三次、每天四次或更多次给予。组合物可以在一段时间内给予,例如在5分钟、10分钟、15分钟、20分钟或25分钟内。
[0023]
在本发明的一些实施方式中,所述的药物组合物是适于口服的制剂,包括片剂、胶囊剂、粉剂、颗粒剂、滴丸、糊剂、散剂等,优选片剂和胶囊剂。其中片剂可以是普通片剂、分散片、泡腾片、缓释片、控释片或肠溶片,胶囊剂可以是普通胶囊、缓释胶囊、控释胶囊或肠溶胶囊。所述的口服制剂可使用本领域公知的药学上可接受的载体通过常规方法制得。药学上可接受的载体包括填充剂、吸收剂、润湿剂、粘合剂、崩解剂、润滑剂等。填充剂包括淀粉、乳糖、甘露醇、微晶纤维素等;吸收剂包括硫酸钙、磷酸氢钙、碳酸钙等;润湿剂包括水、乙醇等;粘合剂包括羟丙甲纤维素、聚维酮、微晶纤维素等;崩解剂包括交联羧甲基纤维素钠、交联聚维酮、表面活性剂、低取代羟丙基纤维素等;润滑剂包括硬脂酸镁、滑石粉、聚乙二醇、十二烷基硫酸钠、微粉硅胶、滑石粉等。药用辅料还包括着色剂、甜味剂等。
[0024]
在一些实施方式中,所述药物组合物是适于口服的固体制剂。该组合物可以是片剂或胶囊的形式。在一个特定的实施方式中,所述药物组合物是胶囊。在本发明的一个特定实施方式中,口服固体制剂的药学上可接受的载体包括甘露醇、微晶纤维素、羟丙基纤维素、硬脂酸镁。
[0025]
在一些实施方式中,提供了一种预防或治疗胰腺癌的配制成单位剂量形式的药物组合物。在一些实施方式中,该单位剂量形式的药物组合物含有2毫克至20毫克的式i所示化合物或其药学上可接受的盐。在一些实施方式中,该单位剂量形式的药物组合物含有5毫克至20毫克的式i所示化合物或其药学上可接受的盐。在一些实施方式中,该单位剂量形式的药物组合物含有8毫克至20毫克的式i所示化合物或其药学上可接受的盐,优选10毫克至16毫克的式i所示化合物或其药学上可接受的盐,较优选10毫克至14毫克的式i所示化合物或其药学上可接受的盐。在一个特定的实施方式中,该单位剂量形式的药物组合物含有10毫克的式i所示化合物或其药学上可接受的盐。在一个特定的实施方式中,该单位剂量形式的药物组合物含有12毫克的式i所示化合物或其药学上可接受的盐。在一个特定的实施方式中,该单位剂量形式的药物组合物含有14毫克的式i所示化合物或其药学上可接受的盐。在一个特定的实施方式中,该单位剂量形式的药物组合物含有16毫克的式i所示化合物或其药学上可接受的盐。例如,对于片剂或胶囊而言,“单位剂量形式的药物组合物”意味着每片片剂或每颗胶囊。
[0026]“药学上可接受的载体”是指其用于制备药物组合物,该药物组合物通常是安全、无毒并且不在生物学上或其它方面不合乎需要,并且包括其对于人类药物使用是可接受的。药学上可接受的载体和稀释剂包括盐水、水性缓冲溶液、溶剂和/或分散媒介物。本领域公知此类载体和稀释剂的使用。可作为药学上可接受的载体的材料的一些非限制性实例包括:(1)糖,例如乳糖、葡萄糖和蔗糖;(2)淀粉,例如玉米淀粉和马铃薯淀粉;(3)纤维素及其衍生物,例如羧甲基纤维素钠、甲基纤维素、乙基纤维素、微晶纤维素和醋酸纤维素;(4)黄蓍胶粉;(5)麦芽;(6)明胶;(7)润滑剂,例如硬脂酸镁、十二烷基硫酸钠和滑石;(8)赋形剂,例如可可脂和栓蜡;(9)油,例如花生油、棉籽油、红花油、芝麻油、橄榄油、玉米油和大豆油;(10)二醇,例如丙二醇;(11)多元醇,例如甘油、山梨糖醇、甘露醇和聚乙二醇(peg);(12)酯,例如油酸乙酯和月桂酸乙酯;(13)琼脂;(14)缓冲剂,例如氢氧化镁和氢氧化铝;(15)海藻酸;(16)无热原水;(17)等渗盐水;(18)林格氏溶液;(19)乙醇;(20)ph缓冲溶液;(21)聚酯、聚碳酸酯和/或聚酸酐;(22)填充剂,例如多肽和氨基酸;(23)血清成分,例如血清白蛋白、hdl和ldl;(24)c
2-c
12
醇,例如乙醇;以及(25)用于药物制剂中的其它无毒相容物质。润湿剂、着色剂、脱模剂、包衣剂、甜味剂、调味剂、芳香剂、防腐剂和抗氧化剂也可以存在于制剂中。术语例如“赋形剂”、“载体”、“药学上可接受的载体”等在本文中可互换使用。
[0027]“药学上可接受的盐”包括但不限于与无机酸或有机酸形成的酸加成盐,所述无机酸例如盐酸、氢溴酸、硫酸、硝酸、磷酸等,所述有机酸例如乙酸、三氟乙酸、丙酸、己酸、庚酸、环戊烷丙酸、乙醇酸、丙酮酸、乳酸、丙二酸、琥珀酸、苹果酸、马来酸、富马酸、酒石酸、柠檬酸、苯甲酸、肉桂酸、扁桃酸、甲磺酸、乙磺酸、1,2-乙二磺酸、2-羟基乙磺酸、苯磺酸、对氯苯磺酸、对甲苯磺酸、3-苯基丙酸、三甲基乙酸、叔丁基乙酸、十二烷基硫酸、葡糖酸、谷氨酸、羟基萘甲酸、水杨酸、硬脂酸等。
[0028]“治疗或预防有效量”意指化合物被给予人用于治疗或预防疾病时,足以实现对该疾病的治疗或预防的量。
[0029]“治疗”意指治疗上有效量的化合物的任何施用,并且包括:
[0030]
(1)抑制正经历或显示出所述疾病的病理学或症状学的人体中的该疾病(即,阻滞所述病理学和/或症状学的进一步发展),或
[0031]
(2)改善正经历或显示出所述疾病的病理学或症状学的人体中的该疾病(即,逆转所述病理学和/或症状学)。
[0032]“预防”意指本技术所述化合物或制剂进行给药以预防疾病或与疾病相关的一个或多个症状,且包括:预防疾病或疾病状态在哺乳动物中出现,特别是当这类哺乳动物易患有该疾病状态,但尚未被诊断为已患有该疾病状态时。
[0033]
有益技术效果
[0034]
本发明涉及非天然人参皂苷3β,20s-di-o-glc-dm在制备抗胰腺癌药物中的应用。本发明提供的3β,20s-di-o-glc-dm能够有效治疗胰腺癌。
具体实施方式
[0035]
实施例1 3β,20s-di-o-β-d-吡喃葡萄糖基-达玛-24-烯-3β,20s-二醇(化合物i)的制备
[0036][0037]
参照文献(huichao liang等.production of a bioactive unnatural ginsenoside by metabolically engineered yeasts based on a new udp-glycosyltransferase from bacillus subtilis.metabolic engineering,2017,44:60-69)中的方法制备得到3β,20s-di-o-β-d-吡喃葡萄糖基-达玛-24-烯-3β,20s-二醇。
[0038]
实验例1 3β,20s-di-o-glc-dm体内抗胰腺癌活性评价
[0039]
评价非天然人参皂苷3β,20s-di-o-glc-dm对小鼠胰腺癌pan02移植瘤的生长抑制作用。实验动物使用购自中国食品药品检定研究院(大兴)的体重为17-20g的雄性c57bl/6jnifdc小鼠(动物合格证号:111251201100346671),伦理审查表编号为00003132。无菌条件下剥离接种于小鼠腋下的pan02肿瘤,剥除筋膜,匀浆研磨,按照1∶3比例用无菌生理盐水稀释制成肿瘤细胞悬液,每只小鼠于左侧腋背部接种0.2ml瘤液,接种当天记为d0。接种后d1天将动物随机分组,每组7只小鼠,称重,并开始给药。
[0040]
动物饲养场地:中国医学科学院药物研究所的spf级屏障设施环境,按照该动物设施的标准进行饲养。每笼5-6只,由专人饲养管理。动物室光照充足,通风和空调设备良好,室温18-25℃,相对湿度50%-70%。
[0041]
实验共分为6组:溶剂对照组(30%peg400);吉西他滨组(75.0mg/kg;第2、5、8、10天腹腔注射0.2ml/20g);人参皂苷rg3组(10.0mg/kg;阳性对照);3β,20s-di-o-glc-dm组(5.0mg/kg、10.0mg/kg和20.0mg/kg)除吉西他滨外,其它组每日0.4ml/20g灌胃给药一次,连续11天。实验结束后颈椎脱位处死小鼠,称重,剥取肿瘤组织和胸腺并称重。根据重量计算肿瘤抑制率(%)和胸腺指数。体重、瘤重、胸腺指数用均值
±
标准差表示,并进行各组与溶剂对照组之间的t检验。
[0042][0043]
胸腺指数=胸腺重量(mg)/体重(g)
×
10
[0044]
结果显示,5.0mg/kg 3β,20s-di-o-glc-dm处理的实验组,对小鼠胰腺癌pan02的抑制率为46.88%,高于以10.0mg/kg rg3(10.0mg/kg是rg3的最佳剂量)处理的阳性对照组(44.49%)。10.0mg/kg rg3处理的阳性对照组,小鼠胸腺指数为24.50
±
7.67;以5.0mg/kg 3β,20s-di-o-glc-dm处理的实验组,小鼠胸腺指数为29.74
±
9.75,高于阳性对照rg3组(表1)。以上结果表明,即使在剂量低于阳性对照rg3时,非天然人参皂苷3β,20s-di-o-glc-dm对小鼠胰腺癌pan02的抑制活性也强于rg3。
[0045]
表1 3β,20s-di-o-glc-dm对小鼠胰腺癌pan02的生长抑制作用及对小鼠胸腺指数的影响
[0046][0047]
t检验:*p《0.05**p《0.01***p《0.001与溶剂对照组比较
[0048]
以上详细描述了本发明的优选实施方式,但是,本发明并不限于上述实施方式中的具体细节,在本发明的技术构思范围内,可以对本发明的技术方案进行多种简单变型,这些简单变型均属于本发明的保护范围。
[0049]
此外,本发明的各种不同的实施方式之间也可以进行任意组合,只要其不违背本发明的思想,其同样应当视为本发明所公开的内容。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1