一种独一味提取物、制剂及其制备方法
1.本发明涉及医药领域,具体涉及一种独一味提取物、制剂及其制 备方法。
背景技术:
2.独一味(lamiophlomis rotata)为唇形科独一味属仅有的一种植 物,又名独步通,藏语亦称“大巴”“打布巴”。早在1000多年前 的藏医学名著《晶珠本草》和《四部医典》中就有记载。现代医学证 明,藏药独一味具有较好的止血、镇痛、活血化瘀、抗菌消炎及显著 提高机体免疫功能的作用。用独一味制成的片剂(泡腾片、咀嚼片、 含片、分散片等)、胶囊(软胶囊、硬胶囊)、滴丸、颗粒剂等独一 味制剂使用范围广泛,主要用于妇科、外科、内科、皮肤科、肿瘤科、 五官科等各种疼痛的治疗。例如,酒精肝患者常见气滞血瘀,并且随 着肝脏损伤逐渐严重血瘀程度会逐渐加深。研究早已证明独一味对于 预防和治疗肝纤维化等肝损伤有明显效果,能够有效降低肝脏ast、 alt水平,具有一定的保肝护肝作用,因此以独一味为主要活性成分 制备的药物适合酒精肝患者服用。
3.目前,以独一味为主要活性成分的制剂均面临着对独一味有效成 分的提取问题。而当前国内外对独一味的研究主要集中在其化学成分 分离和药理药效等方面,对如何更好地提取其有效成分的研究相对较 少。因此,本发明在“绿色化学”的理念下,不采用复杂设备,且能 进一步提高独一味有效成分提取的转化率,为临床的应用提供了很好 的保障。
4.近年来,有关独一味提取工艺的报道或条件苛刻且流程繁琐冗长, 或采用超声、微波、超临界等现代技术辅助提取,后者虽能够在一定 程度上提高提取效果,然而高端设备的引入也给实际生产造成了成本 的提高。
5.邱建国等在文章《独一味不同提取物中总环烯醚萜苷、总黄酮和 总苯乙醇苷的测定》(中国实验方剂学杂志.2011;17(13):32-35)中采 用70%乙醇溶液为溶媒,通过醇提法工业化提取独一味中总环烯醚萜 苷类成分,结果表明,山栀苷甲酯和8-o-乙酰山栀苷甲酯的转移率分 别为76.36%和68.74%,提取效果一般。
6.古启祥等在文章《独一味活性成分的提取优化及其止血活性研究》 (轻工科技.2020;36(1):19-27)中采用正交试验对乙醇回流提取工艺 进行了优化,结果表明,乙醇回流提取较超声辅助醇提法和水煎煮法 能获得较高干浸膏率,其最佳提取工艺为:浓度70%的乙醇为溶媒, 提取次数3次,料液比1:20,在最佳提取条件下出膏率38.87%。但 是该方法提取溶液采用较高浓度的有毒有机溶剂,且耗费溶剂量大, 提取次数相对较多,总体看来不利于临床应用。
7.国内专利中,cn 109771474 a采用80℃以上的水作为提取溶液, 对未经粉粹的独一味进行三次提取,发现提取温度100℃时提取效果 最佳;但该提取技术是针对独一味提取物中黄酮类有效成分的转移率 更佳,但对环烯醚萜类有效成分即山栀苷甲酯和8-o-乙酰山栀苷甲酯 的提取效果不佳。cn 1255100 a中分别采用了水煮提取、乙醇回流 和渗漉提取,并结合大孔树脂吸附等方法进行提纯,虽然使得提取效 果有一定提升,但操作流程相对较为繁杂,且同样也是以木犀草素等 黄酮类有效成分含量为提取工艺的考察指标。
8.综上,目前行业上现有的独一味提取物的提取方法依旧存在着诸 多弊端,实现高效环保的独一味有效提取仍是一个重要研究方向。
技术实现要素:
9.本发明的目的是提供一种独一味提取物、制剂及其制备方法,以 解决目前行业上存在的提取条件苛刻、提取流程繁琐冗长、需要复杂 设备辅助等问题。
10.为了实现上述目的,第一方面,本发明首先提供一种独一味提取 物的提取方法,其包括:
11.将独一味粉末先在40~60℃下浸泡,再进行一次以上的回流提取, 以得到粗提物。
12.本发明发现,上述方法对独一味提取物中有效成分尤其是山栀苷 甲酯和8-o-乙酰山栀苷甲酯的转移率有很好的提升效果。
13.在具体实施时,本领域技术人员能够根据需要,将所述粗提物进 行纯化、浓缩等后续操作,以得到效果较优的独一味提取物。
14.作为优选,所述提取的次数为两次,每次提取的时间为0.5~2h。
15.作为优选,以药材重量为基准,所述提取的水量为8~15倍重量份。
16.作为优选,所述浸泡时间为0.5~2h。
17.作为优选方案,在压力0.8~1.0mpa、温度30~35℃的条件下,通 过孔径为0.22~0.45μm的滤膜对所述粗提物进行超滤处理,并收集滤 液。
18.通过上述方式进行超滤后,能够在去除杂质的同时,更有利于富 集独一味提取物中的有效成分。
19.作为优选,在得到所述滤液后,在温度65~75℃、真空度 0.06~0.08mpa的条件下,将所述滤液浓缩成相对密度为1.25~1.28的稠 膏。
20.第二方面,本发明还提供了一种独一味提取物,其是由上述提取 方法提取得到的。
21.第三方面,本发明还提供了含有所述独一味提取物的独一味制剂。
22.在具体实施时,本领域技术人员能够根据需要,将所述独一味制 剂制成片剂(泡腾片、咀嚼片、含片、分散片等)、胶囊(软胶囊、 硬胶囊)、滴丸、颗粒剂等。
23.进一步的,本发明还提供了一种独一味颗粒剂,其含有所述独一 味提取物、第一辅料与第二辅料。
24.所述第一辅料选自糊精、乳糖、麦芽糊精、β-环糊精的一种或几 种。
25.所述第二辅料选自可溶性淀粉、甘露醇、微晶纤维素的一种或几 种。
26.作为优选,所述第一辅料为糊精、乳糖。
27.作为优选,所述第二辅料为可溶性淀粉。
28.优选地,所述独一味提取物、第一辅料和第二辅料的重量比为1: 0.4~2:0.2~1。更优选地,所述独一味提取物、第一辅料和第二辅 料的重量比为1:0.5:0.2。
29.本发明发现,所述独一味颗粒剂服用后吸收快,可迅速起效,且 作用持久。且服用口感好,溶化性好,在储存过程也不会出现吸潮结 块的现象,货架期长达24个月。
30.第四方面,本发明还提供了所述独一味颗粒剂的制备方法,其包 括:
31.将所述独一味提取物、第一辅料以及第二辅料溶于体积分数为 25~55%的乙醇溶液,并进行制粒。
32.优选地,所述独一味提取物与乙醇溶液的重量比为1:0.2~0.5;
33.将所述制粒步骤结束得到的颗粒在真空度-0.08~-0.10mpa,温度 50~55℃下的条件下进行干燥。
34.将所述干燥步骤结束后的颗粒,进行过筛整粒,包装后即得所述 的独一味颗粒剂。
35.第五方面,本发明还提供所述的独一味提取物在制备药物中应用, 所述药物被用于预防或治疗酒精肝。
36.进一步的,本发明还提供所述的独一味提取物、独一味制剂或独 一味颗粒剂在治疗酒精肝等肝损伤方面的应用。
37.基于上述技术方案,本发明的有益效果如下:
38.(1)本发明发现使用所述的的提取方法,对独一味提取物中有 效成分山栀苷甲酯、8-o-乙酰山栀苷甲酯分别可高达93.5%和88.6% 以上的转移率,提取效果显著。同时,所述提取方法与现有技术相比, 避免了有毒的有机溶剂的介入,减少安全隐患的同时符合当下绿色环 保的要求;且不需要使用复杂设备与技术等,提取流程相对简单易操 作,可以有效保障临床上的应用。
39.(2)本发明提供的独一味颗粒剂具有携带、服用方便,作用持 久,给药剂量准确等优点;且服用后吸收快,能迅速起效,产品口感 好,溶解性好,储存过程不会出现吸潮结块的现象,具有较为均一的 质量,货架期长达24个月,市场前景广阔。
附图说明
40.图1为独一味hplc色谱图,其中图a为独一味混合标准品hplc 色谱图,图b为独一味供试品hplc色谱图;1表示山栀苷甲酯,2表 示8-o-乙酰山栀苷甲酯。
41.图2为独一味配方颗粒对模型小鼠肝组织中gsh的影响。
42.图3为独一味配方颗粒对模型小鼠肝组织中sod的影响。
43.图4为独一味配方颗粒对模型小鼠肝组织中mda的影响。
44.图5为独一味配方颗粒对模型小鼠肝组织中炎症因子的影响,其 中图a为独一味配方颗粒对模型小鼠肝组织中的il-1β含量的影响;图 b为独一味配方颗粒对模型小鼠肝组织中的il-6含量的影响;图c为独 一味配方颗粒对模型小鼠肝组织中的tnf-α的影响。
45.图6为独一味配方颗粒对模型小鼠血清中ast和alt的影响。
具体实施方式
46.以下实施例用于说明本发明,但不用来限制本发明的范围。
47.实施例中未注明具体技术或条件者,按照本领域内的文献所描述 的技术或条件,或者按照产品说明书进行。所用试剂或仪器未注明生 产厂商者,均为可通过正规渠道商购买得到的常规产品。
48.实施例1一种独一味提取物的提取方法
49.本实施例首先提供一种独一味提取物的提取方法及使用所述提 取方法提取得到
的独一味提取物,其具体提取方法如下:
50.1、粗提:
51.取粉碎、过筛后的独一味粉末,加入12倍等量(以重量计,后同) 的40℃的水,浸泡20min,回流提取30min,过滤后得到第一滤液和第 一滤渣,再向第一滤渣中加入10倍等量的水,回流提取20min,过滤 获得第二滤液,然后将第一滤液和第二滤液合并得到独一味的粗提物。
52.2、纯化:
53.取步骤1中的粗提物进行超滤处理,超滤滤膜孔径为0.45μm,超 滤压力为1.0mpa,超滤温度为35℃,超滤结束后收集滤液。
54.3、浓缩:
55.将步骤2中的滤液,在温度70℃、真空度0.08mpa的条件下,采用 旋转蒸发仪减压浓缩至稠膏,搅拌均匀,分装至棕色西林瓶中,置于 真空冷冻干燥机中冻干,取出,轧上铝盖,即得所述独一味提取物。
56.本实施例通过一种hplc色谱方法,检测了独一味提取物中有效 成分山栀苷甲酯和8-o-乙酰山栀苷甲酯的浓度,具体方法如下:
57.1、色谱条件
58.色谱柱:zorbax extend-c18色谱柱(4.6
×
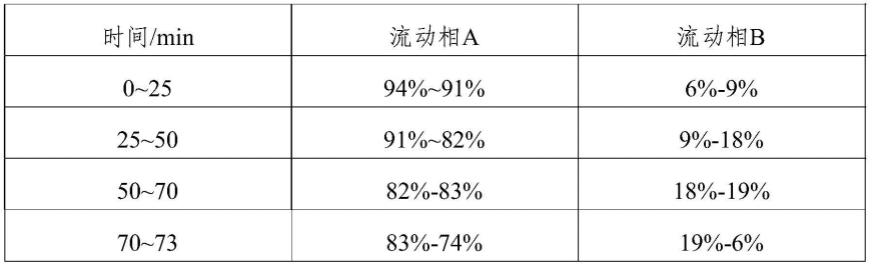
250mm2,5μm); 柱温:30℃;流动相:以0.1%磷酸水溶液为流动相a、乙腈为流动相 b;进样量:10μl,检测波长:235nm,按表1中规定进行洗脱。
59.表1梯度洗脱表
[0060][0061][0062]
2、标准品溶液制备
[0063]
取山栀苷甲酯对照品、8-o-乙酰山栀苷甲酯对照品适量,精密称 定,加甲醇制成每1ml各含30μg的混合溶液,即得。
[0064]
3、供试品溶液制备
[0065]
取冻干粉0.1g,置于25ml锥形瓶中,加入50%甲醇20ml超声 10min溶解,转移至25ml容量瓶中,用50%甲醇定容至刻度,滤过, 取续滤液。
[0066]
4、线型关系考察
[0067]
分别配制0.208mg/ml、0.198mg/ml的山栀苷甲酯、8-o-乙酰山 栀苷甲酯对照品溶液作为母液,依次对两种对照品溶液稀释5个浓度, 分别精密吸取10μl注入液相色谱仪,测定峰面积,以浓度为横坐标, 峰面积为纵坐标,进行回归计算,得到山栀苷甲酯、8-o-乙酰
山栀苷 甲酯回归方程,结果表明各化合物在相应浓度范围内线性关系良好, 线性方程结果见表2,独一味标准品与供试品的hplc色谱图见图1 中的图a与图b。
[0068]
表2线性关系考察结果
[0069]
检测指标回归方程相关系数线性范围/μg
·
ml-1
山栀苷甲酯y=13901x-204070.999913~2088-o-乙酰山栀苷甲酯y=13888x+260200.999912.375~198
[0070]
实施例2~9,对比例1:不同条件下的提取结果
[0071]
在对比例1及实施例2~9中列举了发明人尝试过的不同提取条件 下(浸泡温度、浸泡时间、提取时间、料液比)的提取方案,其均按 照实施例1的提取方法、表3中给出的参数条件提取得到。
[0072]
同时,以有效成分山栀苷甲酯和8-o-乙酰山栀苷甲酯的转移率以 及含量等为指标,对对比例1及实施例1~9的提取结果进行了测定,并 按如下公式,分别计算出膏率,测定山栀苷甲酯、8-o-乙酰山栀苷甲 酯含量转移率,按照出膏率和转移率(3:7)计算加权综合评分,结 果见表3。
[0073][0074][0075][0076]
从表3中可以看出,实施例1~9中,浸泡温度对其影响 50℃》40℃》30℃,浸泡时间对其影响30min》40min》20min,提取时间 对其影响30(20)min》40(30)min》50(40)min,料液比对其影响 为16(14)》12(10)》14(12)。对比例1在相同条件下采用了常 规室温浸泡的方法,其提取效果较40~60℃内的提取结果相对不理想, 综合评分不高。其中,料液比的表述方式指第一次浸泡的料液比(第 二次浸泡的料液比),提取时间的表述也同样适用该表述方法。
[0077]
表3不同提取条件下的提取结果
[0078][0079][0080]
实施例10所述独一味颗粒剂及其制备方法
[0081]
本实施例首先提供了一种独一味颗粒剂,其含有所述独一味提取 物、糊精、乳糖和可溶性淀粉,其中所述独一味提取物与糊精重量比 为1:0.2,所述独一味提取物与乳糖重量比为1:0.3,所述独一味提 取物与可溶性淀粉的重量比为1:0.2。
[0082]
本实施例进一步提供了所述独一味颗粒剂的制备方法,其包括:
[0083]
1、将所述独一味提取物,加入糊精、乳糖和可溶性淀粉以及体 积分数为50%的乙醇,进行制粒;所述独一味提取物与体积分数为50% 的乙醇重量比为1:0.5。
[0084]
2、将制粒步骤得到的颗粒,置于真空干燥箱中,设置真空度为
ꢀ‑
0.08mpa,干燥温度为55℃,干燥时间24h,干燥结束,取出冷却至 室温,备用。
[0085]
3、将干燥结束后的颗粒,过筛整粒后进行包装,检验合格后入 库储存。
[0086]
实施例11
[0087]
本实施例首先提供了一种独一味颗粒剂,其含有所述独一味提取 物、糊精、乳糖和可溶性淀粉,其中所述独一味提取物与糊精重量比 为1:0.3,所述独一味提取物与乳糖重量比为1:0.2,所述独一味提 取物与可溶性淀粉的重量比为1:0.3。
[0088]
本实施例进一步提供了所述独一味颗粒剂的制备方法,其包括:
[0089]
1、将所述独一味提取物,加入糊精、乳糖和可溶性淀粉以及体 积分数为50%的乙醇,进行制粒;所述独一味提取物与体积分数为50% 的乙醇重量比为1:0.5。
[0090]
2、将制粒步骤得到的颗粒,置于真空干燥箱中,设置真空度为
ꢀ‑
0.08mpa,干燥温度为55℃,干燥时间24h,干燥结束,取出冷却至 室温,备用。
[0091]
3、将干燥结束后的颗粒,过筛整粒后进行包装,检验合格后入 库储存。
[0092]
实施例12
[0093]
本实施例首先提供了一种独一味颗粒剂,其含有所述独一味提取 物、糊精、乳糖和可溶性淀粉,其中所述独一味提取物与糊精重量比 为1:0.3,所述独一味提取物与乳糖重量比为1:0.4,所述独一味提 取物与可溶性淀粉的重量比为1:0.1。
[0094]
本实施例进一步提供了所述独一味颗粒剂的制备方法,其包括:
[0095]
1、将所述独一味提取物,加入糊精、乳糖和可溶性淀粉以及体 积分数为50%的乙醇,进行制粒;所述独一味提取物与体积分数为50% 的乙醇重量比为1:0.5。
[0096]
2、将制粒步骤得到的颗粒,置于真空干燥箱中,设置真空度为
ꢀ‑
0.08mpa,干燥温度为55℃,干燥时间24h,干燥结束,取出冷却至 室温,备用。
[0097]
3、将干燥结束后的颗粒,过筛整粒后进行包装,检验合格后入 库储存。
[0098]
试验例1所述独一味颗粒剂稳定性的效果验证
[0099]
本试验例首先提供一种长期试验稳定性的验证方法及结果,包括:
[0100]
将试验例1置于温度(25
±
2)℃和相对湿度(60
±
10)%条件下放 置24个月,分别于0,3,6,9,12,18,24个月取样,并与0月比较, 结果见表5。
[0101]
由表5可知:所述独一味颗粒剂长期试验24个月性状、溶解性、 鉴别、山栀苷甲酯与8-o-乙酰山栀苷甲酯含量、微生物限度各项指标 均无显著变化,含量也未见明显改变,均符合生产用质量标准草案的 各项相关规定,故所述独一味颗粒剂长期试验24个月质量稳定。
[0102]
表5长期稳定性试验
[0103][0104][0105]
本试验进一步提供一种加速试验稳定性的验证方法及结果,包括:
[0106]
将试验例1置于温度(40
±
2)℃和相对湿度(75
±
5)%条件下放置 6个月,分别于0,1,2,3,6个月取样,并与0月比较,结果见表 6。
[0107]
由表6可知,所述独一味颗粒剂加速试验6个月性状、溶化性、 鉴别、山栀苷甲酯与8-o-乙酰山栀苷甲酯含量、微生物限度各项指标 均无显著变化,均符合生产用质量标准草案的各项相关规定,故所述 独一味颗粒剂加速试验6个月质量稳定。根据加速试验结果初步确定 所述独一味颗粒剂的有效期为2年。
[0108]
表6加速稳定性试验
[0109][0110]
试验例2所述独一味颗粒剂的药效学验证
[0111]
本试验例提供一种所述独一味颗粒剂对酒精性肝损伤模型小鼠 的的药效试验验证,包括:
[0112]
1、实验动物:c57bl/6小鼠,雄性,6~8周龄,体重为18g-22g。
[0113]
2、实验分组:实验小鼠随机分为6组,每组12只,分别为空白组、 模型组、阳性对照组、独一味配方颗粒低、中、高剂量组。上述实施 例获得的所有独一味配方颗粒按低、中、高剂量组灌胃,剂量分别为 27mg/kg/d,135mg/kg/d和270mg/kg/d,灌胃体积为10ml/kg;阳性对 照组联苯双酯灌胃剂量为10mg/kg/d;空白组和模型组每日灌胃小鼠 给予相同体积的蒸馏水,1h后,除空白组外其余5组按照10ml/kg,连 续给药及造模49d。末次造模后,禁食16h,采用摘除眼球法取血于2ml 离心管中,分离血清;取血完毕,颈椎脱臼法处死小鼠,及时剖检取 出肝脏,左叶固定,其余匀浆,进行各指标的检测和病理组织学检查。
[0114]
3、测定指标:用相应试剂盒分别测定各组小鼠肝组织匀浆中丙 二醛(mda),还原型谷胱甘肽(gsh),超氧化物歧化酶(sod),肿瘤 坏死因子-α(tnf-α),白介素-1β(il-1β)和白介素-6(il-6)含量;血清中 alt和ast含量。
[0115]
4、统计分析:应用spss18.0统计软件,计量方式采用“均数
±ꢀ
标准差”表示,多组间比较采用单因素方差法,组间两两比较方差齐 性时用lsd方法分析,方差不齐时用dunnett’s方法分析。
[0116]
5、实验结果
[0117]
(1)独一味配方颗粒对模型小鼠肝组织中gsh和sod的影响。
[0118]
从图2和图3可以看出,与空白组相比,模型组的gsh和sod含量 显著降低(p《0.01),与模型组相比,联苯双脂组和独一味配方颗粒低、 中、高剂量组中gsh和sod含量均有不同程度的升高,其中独一味配 方颗粒低剂量组较模型组相比,能够显著提高gsh含量(p《0.01),独 一味配方颗粒高剂量组较模型组相比,能够显著提高sod含量 (p《0.01)。
[0119]
(2)独一味配方颗粒对模型小鼠肝组织中mda的影响。
[0120]
从图4可以看出,与空白组相比,模型组的mda含量显著升高 (p《0.01),与模型组相比,联苯双脂组和独一味配方颗粒低、中、高 剂量组均能够显著降低小鼠肝组织中mda含量(p《0.01)。
[0121]
(3)独一味配方颗粒对模型小鼠肝组织中炎症因子的影响。
[0122]
从图5可以看出,与空白组相比,模型组的il-1β含量升高(p《0.01), 与模型组相比,独一味配方颗粒低、中、高剂量组均能够显著降低 il-1β(p《0.01);联苯双脂组和独一味配方颗粒高剂量组较模型组相比, il-6含量显著降低(p《0.01);此外,与空白组相比,模型组的tnf-α 含量升高,与模型组相比,联苯双脂组和独一味配方颗粒低、中、高 剂量组均
能够显著降低tnf-α的含量(p《0.01)。
[0123]
(4)独一味配方颗粒对模型小鼠血清中ast和alt的影响。
[0124]
从图6可以看出,与空白组相比,模型组的ast和alt含量升高 (p《0.01),与模型组相比,联苯双脂组和牡蛎肽低、中、高剂量组均 能够显著降低ast和alt含量(p《0.01)。通过上述试验例可以证明, 独一味配方颗粒对酒精性肝损伤小鼠具有保护作用,能够降低小鼠血 清中alt和ast含量,提高过氧化物酶sod和gsh含量,降低mda 含量,缓解机体氧化应激,并降低小鼠肝组织中炎症因子il-1β、il-6 和tnf-α水平。
[0125]
本发明的独一味提取物颗粒剂制备工艺适合生产要求,质量检查 方法方便且易于操作、产品合格率高。
[0126]
虽然,上文中已经用一般性说明及具体实施方案对本发明作了详 尽的描述,但在本发明基础上,可以对之作一些修改或改进,这对本 领域技术人员而言是显而易见的。因此,在不偏离本发明精神的基础 上所做的这些修改或改进,均属于本发明要求保护的范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1