一种锍盐类阳离子聚合物修饰的Fe3O4磁性纳米粒子及其制备方法和应用与流程
一种锍盐类阳离子聚合物修饰的fe3o4磁性纳米粒子及其制备方法和应用
技术领域
1.本发明属于医用生物材料的技术领域,涉及一种锍盐类阳离子聚合物修饰的fe3o4磁性纳米粒子及其制备方法和应用。
背景技术:
2.细菌感染和粘附是导致人类生命健康威胁的主要原因之一。除致病性细菌危害之外,粘附在表层的细菌极易堆叠形成生物膜,从而导致伤口感染,引起多种感染性疾病。针对细菌致病性这一问题,抗生素的产生大大降低了致病性危害,但抗生素的过度依赖和滥用导致细菌进化出了耐药性,甚至有多重耐药菌的产生。近年来,一直缺乏新的抗生素来对抗现有抗生素所造成的耐药性问题,若抗生素的使用不加以控制,最终传染病将再次成为威胁生命的疾病。阳离子聚合物模仿天然抗菌肽设计而成,因其膜破坏基质的光谱抗菌活性,故其产生耐药性的机会较少。但部分阳离子聚合物其杀菌速率较慢,耗时长是限制其广泛应用的一大因素。
3.此外,与生物膜感染有关的疾病比如结肠炎、牙龈炎和中耳炎等疾病种类繁多,数量巨大。据统计,人类所有微生物感染中有80%是由生物膜引起的。大多数游离细菌可以附着在表面上,聚集生长成多细胞群落,也就是生物膜的细胞外聚合物基质(eps)。eps由胞外多糖、核酸、蛋白质和脂类组成,构成细菌的保护性微环境,并促进细菌对外来抗菌药物产生强大的耐药性。因此,传统抗生素对细菌生物膜的治疗效果显著下降,换言之,抗生素治疗于生物膜而言具有难渗透、高浓度等问题。
4.近年来,纳米技术的进步为细菌感染治疗带来了新的希望,但其有限的穿透力仍是一大困处,故而开发有效治疗生物膜感染的新型抗菌纳米材料仍然是一个挑战。fe3o4磁性纳米粒子因其超顺磁性、高比表面积和生物相容性而作为抗菌剂载体,与诸多抗菌剂连用均表现出优异的杀菌效果。在外部磁场作用下,fe3o4磁性纳米粒子可以实现强大的穿透力,靶向进入生物膜。如webster等人将fe3o4磁性纳米粒子用于医疗器械相关感染的治疗,在外部磁场的帮助下,可穿透20μm厚的生物膜,进而导致生物膜厚度的细菌被完全消灭。这些研究表明fe3o4磁性纳米粒子在对抗生物膜感染方面具有极好的潜力。
技术实现要素:
5.本发明针对现有技术的不同,提供了一种锍盐类阳离子聚合物修饰的fe3o4磁性纳米粒子,可以用于细菌/真菌富集、杀菌和清除生物膜,同时也有着很好的生物相容性。
6.为解决上述技术问题,本发明的目的通过下述技术方案得以实现:
7.一种锍盐类阳离子聚合物修饰的fe3o4磁性纳米粒子,
[0008][0009]
如式ⅰ所述的锍盐类阳离子聚合物通过静电相互作用修饰在fe3o4磁性纳米表面,得到如式ⅱ所示的锍盐类阳离子聚合物修饰的fe3o4磁性纳米粒子。
[0010]
本发明还提供了上述锍盐类阳离子聚合物修饰的fe3o4磁性纳米粒子的制备方法,所述方法包括以下步骤:
[0011]
(1)1,6-己二硫醇和1,5-己二烯在光引发剂的加入下,紫外光引发得到前体聚合物;通过加入碘甲烷对前体聚合物进行硫盐化,得到如式ⅰ所示的锍盐类阳离子聚合物;
[0012]
(2)式i所示的锍盐类阳离子聚合物与表面带有负电荷的磁性fe3o4纳米粒子通过静电相互作用结合,得到如式ⅱ所示的锍盐类阳离子聚合物修饰的磁性fe3o4纳米粒子。
[0013]
在上述的一种锍盐类阳离子聚合物修饰的fe3o4磁性纳米粒子的制备方法中,所述表面带有负电荷的磁性fe3o4纳米粒子的制备方法是:
[0014][0015]
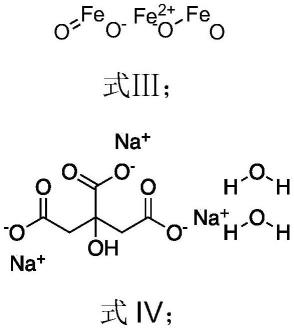
二价铁与三价铁在碱性条件下、一定温度下通过共沉法制备得到如式ⅲ所示的磁性fe3o4纳米粒子;采用柠檬酸钠对磁性fe3o4纳米粒子进行修饰,得到如式iv所示的表面带有负电荷的磁性fe3o4纳米粒子。
[0016]
优选的,所述二价铁采用七水合硫亚铁,三价铁采用六水合三氯化铁。所述碱性条件采用25%-28%的氨水溶液,所述一定温度采用60-80℃。
[0017]
在述的一种锍盐类阳离子聚合物修饰的fe3o4磁性纳米粒子的制备方法中,所述步骤(2)包括:柠檬酸钠修饰的磁性fe3o4纳米粒子与锍盐类阳离子聚合物分散在水溶液中,通过静电相互作用结合,得到锍盐类阳离子聚合物修饰的磁性fe3o4纳米粒子;所述柠檬酸钠修饰的磁性fe3o4纳米粒子与锍盐类阳离子聚合物的质量比为1:1;优选的,所述柠檬酸钠修
饰的磁性fe3o4纳米粒子与锍盐类阳离子聚合物的浓度均为5mg/ml。
[0018]
在上述的一种锍盐类阳离子聚合物修饰的fe3o4磁性纳米粒子的制备方法中,所述柠檬酸钠对磁性fe3o4纳米粒子进行修饰的方法是:磁性fe3o4纳米粒子超声分散在超纯水中,加入柠檬酸钠,继续超声,反应生成带负电荷的柠檬酸钠修饰的磁性fe3o4纳米粒子;所述柠檬酸钠与磁性fe3o4纳米粒子的摩尔比为2:3。
[0019]
本发明还提供了锍盐类阳离子聚合物修饰的fe3o4磁性纳米粒子的应用。
[0020]
一种锍盐类阳离子聚合物修饰的fe3o4磁性纳米粒子的应用,如式ⅱ所示的锍盐类阳离子聚合物修饰的fe3o4磁性纳米粒子应用于细菌/真菌快速富集及杀菌。其方法及原理是:锍盐类阳离子聚合物修饰的fe3o4磁性纳米粒子表层带有大量的正电荷,而细菌/真菌细胞膜为负电,当二者接触时,通过静电相互作用迅速结合在一起。在外加磁场作用下,磁吸fe3o4纳米粒子,迅速将细菌富集并从溶液中分离;同时带有正电的阳离子聚合物破坏细菌/真菌细胞膜,从而达到杀菌的效果。
[0021]
一种锍盐类阳离子聚合物修饰的fe3o4磁性纳米粒子的应用,如式ⅱ所示的锍盐类阳离子聚合物修饰的fe3o4磁性纳米粒子应用于清除生物膜。其方法及原理是:一定浓度的细菌/真菌悬液于96孔板培养,隔天换液,培养生成72h成熟的生物膜。移取上层溶液后,加入不同浓度锍盐类阳离子聚合物修饰的fe3o4磁性纳米粒子的pbs溶液。在磁场作用下,使纳米粒子左右移动,在生物膜中进行通道挖掘,加深锍盐类阳离子聚合物修饰的fe3o4磁性纳米粒子在生物膜中的渗透深度,同时加快其渗透速度。将锍盐类阳离子聚合物更快、更深地递送至生物膜内部,以达到更优的生物膜清除效果。
[0022]
本发明和现有技术相比,具有如下有益效果:
[0023]
1、本发明采用共沉淀法合成fe3o4纳米粒子后,进一步柠檬酸钠修饰得到表面带有负电荷的性fe3o4纳米粒子,再通过静电相互作用得到锍盐类阳离子聚合物修饰的fe3o4磁性纳米粒子,其合成方法简单,操作容易,最后以静电相互作用结合,既不破坏锍盐类阳离子聚合物的结构,又环保易操作,具有良好的应用前景。
[0024]
2、本发明提供的锍盐类阳离子聚合物修饰的fe3o4磁性纳米粒子可以使细菌/真菌快速富集,采用较低的粒子浓度既可以实现可观的细菌/真菌吸附,同时在锍盐类阳离子聚合物修饰的fe3o4磁性纳米粒子与细菌接触的瞬间即可实现细菌的快速富集。另外,采用同样浓度的粒子也能够有效杀死吸附的细菌/真菌。
[0025]
3、本发明提供的锍盐类阳离子聚合物修饰的fe3o4磁性纳米粒子可以有效清除生物膜,同时具有理想的渗透深度和渗透速度,可以将锍盐类阳离子聚合物更快、更深地递送至生物膜内部,以达到更优的生物膜清除效果。
[0026]
4、本发明提供的锍盐类阳离子聚合物修饰的fe3o4磁性纳米粒子生物相容性好,毒性低,是一种理想的新型抗菌剂。
附图说明
[0027]
附图1为实施例5中锍盐类阳离子聚合物修饰的fe3o4磁性纳米粒子细菌富集动力学结果;
[0028]
附图2为实施例7中锍盐类阳离子聚合物修饰的fe3o4磁性纳米粒子血红细胞溶血性能。
具体实施方式
[0029]
下面通过具体实施方式的描述对本发明作进一步说明,但这并非是对本发明的限制,本领域技术人员根据本发明的基本思想,可以做出各种修改或者改进,但是只要不脱离本发明的基本思想,均在本发明的范围之内。
[0030]
实施例1
[0031]
锍盐类阳离子聚合物的制备,具体操作步骤如下:
[0032]
称取1,6-己二硫醇(2.5mmol)和1,5-己二烯(2.5mmol),溶于二氯甲烷,随后加入苯基双(2,4,6-三甲基苯甲酰基)氧化膦(0.01625mmol),室温环境下,紫外灯照射反应2h,得到的聚合物中间体加入4ml的n,n-二甲基甲酰胺作为溶剂,向体系中加入过量的碘甲烷(10mmol),室温下反应48h,反应结束后,该反应液先后用氯化钠溶液(0.1m)和去离子水透析2天,将得到的溶液冷冻干燥,得到锍盐类阳离子聚合物,产率为80%。
[0033]
实施例2
[0034]
柠檬酸钠修饰的fe3o4磁性纳米粒子的制备,具体操作步骤如下:
[0035]
a、称取6mmol六水合三氯化铁和3mmol七水合硫亚铁于反应瓶中,加入150ml的去离子水,氮气氛围下搅拌30min。将反应温度升温至80℃,继续保持n2环境,加入10ml的氨水(25%-28%),剧烈搅拌1h后冷却至室温。生成的沉淀物用磁铁磁吸分离,用乙醇和水洗涤、离心、重新分散,重复几次后,真空烘箱60℃干燥,得到fe3o4纳米粒子。
[0036]
b、称取1.2mmol干燥的fe3o4纳米粒子超声分散在80ml超纯水中,加入1.8mmol柠檬酸钠,继续超声1h。反应后的产物经超纯水洗涤、离心、重新分散,重复几次后,分散在超纯水中。最后得到柠檬酸钠修饰的fe3o4纳米粒子表面带有负电荷,其粒径与zeta电位如表1所示。
[0037]
表1柠檬酸钠修饰的fe3o4纳米粒子的性能
[0038]
性能粒径(nm)pdizeta电位(mv)实施例2129.50.383-24.9
[0039]
从表1测试结果可以看出,本发明实施例2所制备的柠檬酸钠修饰的fe3o4纳米粒子,其粒径约为129.5nm,zeta电位为-24.9mv,表明带有负电的fe3o4磁性纳米粒子成功合成。
[0040]
实施例3
[0041]
锍盐类阳离子聚合物修饰的fe3o4磁性纳米粒子的制备,具体步骤如下:
[0042]
将实施例2中的分散在超纯水中柠檬酸钠修饰的fe3o4纳米粒子稀释至5mg/ml,再称取5mg的锍盐类阳离子聚合物溶于1ml的超纯水,将二者混合搅拌后得到锍盐类阳离子聚合物修饰的fe3o4磁性纳米粒子。反应结束后,经超纯水洗涤、离心、重新分散,重复几次后,最终分散在pbs缓冲液(ph=7.4)中。锍盐类阳离子聚合物修饰的fe3o4磁性纳米粒子的粒径与zeta电位如表2所示。
[0043]
表2锍盐类阳离子聚合物修饰的fe3o4纳米粒子的性能
[0044]
性能粒径(nm)pdizeta电位(mv)实施例3235.80.48529.9
[0045]
从表2测试结果可以看出,本发明实施例3所制备的锍盐类阳离子聚合物修饰的fe3o4纳米粒子,其粒径约为235.8nm,zeta电位为29.9mv。表面电位的变化表明带锍盐类阳
离子聚合物修饰的fe3o4磁性纳米粒子成功合成。
[0046]
实施例4
[0047]
锍盐类阳离子聚合物修饰的fe3o4磁性纳米粒子细菌/真菌富集和快速杀菌实验,具体操作如下:
[0048]
1)将实施例3中锍盐类阳离子聚合物修饰的fe3o4磁性纳米粒子高浓度pbs溶液稀释为不同浓度置于96孔板中,待用;
[0049]
2)将培养过夜的细菌/真菌溶液离心去除tsb/sdb,用pbs稀释至目标浓度;
[0050]
3)将稀释好的菌液加入到含fe3o4纳米粒子的96孔板中,室温静置5min,用磁铁在孔板底部磁吸30s,取上层清液涂在tsb/sdb琼脂板上,纯的细菌/真菌溶液涂板作为对照组,所有的样品及对照组于37℃/28℃水培箱孵育24h。磁吸的底层纳米粒子用pbs清洗两次,重新分散后涂在琼脂板,同样置于37℃/28℃水培箱孵育24h。24h后,计算琼脂板上细菌/真菌菌落数目。
[0051]
本实施例中共选用三种菌,分别是:革兰氏阳性菌(s.aureus)、革兰氏阴性菌(e.coli)和真菌(c.albicans),上层清液和下层沉淀菌落数目≤0.1%的最低粒子浓度结果如表3所示。
[0052]
表3锍盐类阳离子聚合物修饰的fe3o4磁性纳米粒子的细菌/真菌富集及杀菌结果
[0053][0054][0055]
从表3实验结果可以看出,在锍盐类阳离子聚合物修饰的fe3o4磁性纳米粒子的浓度为256μg/ml时,与对照组相比,实验组能够达到对溶液中细菌99.9%的吸附,5min即可实现对革兰氏阳性菌(s.aureus)、革兰氏阴性菌(e.coli)和真菌(c.albicans)的快速富集,并且在相同浓度下能够有效杀死吸附的细菌/真菌。
[0056]
实施例5
[0057]
锍盐类阳离子聚合物修饰的fe3o4磁性纳米粒子的细菌/真菌富集动力学,以细菌s.aureus为例,具体步骤如下:
[0058]
1)从实施例3中可以得知s.aureus杀菌率≥99.9%的最低粒子浓度为256μg/ml,故将锍盐类阳离子聚合物修饰的fe3o4磁性纳米粒子用pbs稀释至256μg/ml;
[0059]
2)将培养过夜的s.aureus细菌溶液离心去除tsb,用pbs稀释至目标浓度;
[0060]
3)将稀释好的菌液加入到fe3o4纳米粒子pbs溶液中,把刚加入的时间设置为0min,分别设置0-5min六个实验组,初始细菌溶液作为对照组。分别在0,1,2,3,4,5min六个时间点用磁铁磁吸孔板底部,取上层清液涂板,培养24h后,计算琼脂板上的菌落数目。
[0061]
具体实验结果如图1所示。
[0062]
从图1实验结果可以看出,在锍盐类阳离子聚合物修饰的fe3o4磁性纳米粒子在与s.aureus混合0min时,也就是与细菌接触的瞬间即可实现细菌的快速富集(富集率≥99.9%)。该结果表明锍盐类阳离子聚合物修饰的fe3o4磁性纳米粒子可在外加磁场环境下实现对溶液中细菌的快速富集。
[0063]
实施例6
[0064]
锍盐类阳离子聚合物修饰的fe3o4磁性纳米粒子在成熟生物膜清除方面的应用,具体操作如下:
[0065]
1)将培养过夜的细菌/真菌溶液稀释至目标浓度,置于96孔板中,37℃/28℃的水培箱中培养72h,每隔24h更换一次培养液,以此在96孔板底部形成成熟的生物膜;
[0066]
2)将培养成熟的生物膜移取上层溶液,加入不同浓度的锍盐类阳离子聚合物修饰的fe3o4磁性纳米粒子pbs溶液,在其底部用磁铁磁吸带动纳米粒子左右移动,该过程持续5min。轻轻吹打均匀后静置10min,再次进行5min的磁吸移动,重复上述操作,总时间为30min。其中,不加纳米粒子的pbs缓冲液组作为对照组;
[0067]
3)30min后,移去上层悬液后,用pbs清洗两遍,在加入一定量的pbs,超声分散15min使底部生物膜脱落;
[0068]
4)将脱落的生物膜溶液吹打均匀,取一定量的溶液涂在琼脂板上,24h后计算菌落数目。
[0069]
本实施例中生物膜清除率≥99.9%时,锍盐类阳离子聚合物修饰的fe3o4磁性纳米粒子的最低浓度如表4所示。
[0070]
表4锍盐类阳离子聚合物修饰的fe3o4磁性纳米粒子对细菌/真菌生物膜清除效果
[0071][0072][0073]
从表4中可以看出,实施例中制备的锍盐类阳离子聚合物修饰的fe3o4磁性纳米粒子对于细菌/真菌生物膜均具有一定程度的清除效果。其中,对于e.coli生物膜,粒子浓度为256μg/ml即可达到99.9%的清除效果,而s.aureus和c.albicans生物膜也分别在512μg/ml和2048μg/ml时达到理想的清除效果。
[0074]
实施例7
[0075]
实施例3中的锍盐类阳离子聚合物修饰的fe3o4磁性纳米粒子进行红细胞溶血试验,具体操作如下:
[0076]
1)取2ml的绵羊血红细胞离心,pbs洗涤,再次离心,上述操作重复4次;
[0077]
2)将洗涤后的血红细胞重新分散在pbs缓冲液中,锍盐类阳离子聚合物修饰的fe3o4磁性纳米粒子用pbs稀释至不同浓度;
[0078]
3)将血红细胞与fe3o4纳米粒子pbs溶液以1:49混合均匀,其中血红细胞与pbs缓冲液混合作为阴性对照,血红细胞与超纯水混合作为阳性对照。室温下共培育2h后离心,取上清液置于96孔板,测试其在540nm处的吸光度。溶血率计算公式如下:
[0079][0080]
溶血结果如图2所示。
[0081]
红细胞溶血率越高代表该物质的生物相容性越差,毒性越高。从图2实验结果可以看出,本发明实施例制备的锍盐类阳离子聚合物修饰的fe3o4磁性纳米粒子在浓度为1000μg/ml时,其溶血率依旧低于50%。这表明该锍盐类阳离子聚合物修饰的fe3o4磁性纳米粒子其生物相容性较好,满足抗菌剂的使用要求。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1