一种多功能诊疗一体化核壳树状分子纳米平台及其制备方法
本发明属于肿瘤诊疗一体化领域,特别涉及一种多功能诊疗一体化核壳树状分子纳米平台及其制备方法。
背景技术:
1、在纳米医学领域,各种纳米平台已经被广泛用于癌症的成像和治疗。其中,聚酰胺-胺(pamam)树状大分子因其具有完美的球状结构、单分散性以及良好水溶性、非免疫原性和易官能化等特点,在基因递送、药物传递、分子影像和肿瘤诊疗等生物医学领域表现出极大的应用潜力。而基于pamam树状大分子构建的核壳结构树状大分子(cstds)不但继承了单代树状大分子高度可修饰性、无免疫原性等优点,还克服了单代树状大分子有限药物负载量、基因传递效率低等局限。因此,利用树状大分子作为反应性构件,开发多功能性cstds纳米平台,并将其应用于前沿生物医学领域已成为科研工作者研究的最新方向之一。
2、目前,已利用β-环糊精(β-cd)和金刚烷(ad)或苯并咪唑(bm)之间强烈的超分子主客体相互作用构建cstds。研究表明,在第3代(g3)氨基封端的pamam树状大分子部分表面修饰ad或bm,第5代(g5)氨基封端的pamam树状大分子表面部分修饰β-cd后,可利用ad或bm和β-cd的主客体识别,合成以g5为核、g3为壳的g5-cd/ad-g3 cstds或g5-cd/bm-g3 cstds。和单独的g5-cd或ad-g3树状大分子相比,g5-cd/ad-g3 cstds基因传递效率分别提高了20倍和170倍(chen f.et al.j.mater.chem.b,2017,5,8459)。g5-cd/bm-g3 cstds也被证明比单独的g5和g5-cd/ad-g3 cstds拥有更好的抗癌药物负载能力和肿瘤渗透能力(wang j.etal.nanoscale 2019,11,22343-22350)。而且,g5-cd/ad-g3作为纳米平台还可以实现基因和药物共递送并用于三阴性乳腺癌细胞的基因-化疗的联合治疗(song c.etal.j.mater.chem.b.2020,8,2768-2774)。但遗憾的是,由于纳米平台本身的限制(如表面电势过高、无主动靶向性能、抗蛋白吸附能力差等),这些cstds平台负载药物和/或基因后,没有用于体内联合治疗评价。
3、尽管构建诊疗一体化的纳米平台在个性化医疗和精准治疗等方面展现巨大的应用潜力。但目前用于临床实验的纳米药物其治疗效果仍然很不理想。就现有的纳米材料(如cstds)而言,不加修饰的纳米材料被用于体内后,是否能够有效地在肿瘤病灶区发挥作用也是纳米药物应用于药物传递、疾病诊断等方面的关键。蛋白对材料的非特异性吸附会导致纳米材料被非目标细胞吞噬或者聚集,从而引起免疫响应和其他不利结果。有研究报道,通过对纳米材料表面修饰两性离子,可以降低体内网状内皮系统(res)以及各种蛋白对材料的非特异性吸附而减少材料被清除,延长血液循环时间,增加纳米药物在病灶区域的聚集,达到在肿瘤部位的高渗透和高保留效果。此外,超声靶向微泡破坏技术(utmd)已被证明是增强药物在肿瘤区域富集的新策略。其作用机制是在超声作用下,造影微泡与超声的能量相互作用引起微泡爆破,微泡爆破瞬间产生的微射流、微冲力作用在血管壁或细胞膜表面产生声空化效应,增加了细胞膜的通透性,从而促进纳米材料在肿瘤部位的渗透。所以借助utmd技术可以促进纳米颗粒在肿瘤部位的渗透,从而达到增强的治疗效果。
4、检索国内外相关文献和专利表明:多重修饰的多功能诊疗一体化核壳树状分子纳米平台用于mr成像介导的化疗/基因治疗的联合治疗,目前尚未见报道。联合utmd技术,促进新型多功能诊疗一体化核壳树状分子纳米平台在肿瘤部位的渗透,增强mr成像和联合治疗的效果,目前尚未见报道。
技术实现思路
1、本发明所要解决的技术问题是提供一种多功能诊疗一体化核壳树状分子纳米平台及其制备方法,该纳米平台在联合超声靶向微泡破坏技术后,提高了纳米复合物的肿瘤靶向性和在肿瘤部位的积累,为构建精准高效的诊疗一体化纳米平台提供了新选项。
2、本发明提供了一种多功能诊疗一体化核壳树状分子纳米平台,所述纳米平台包括螯合钆离子和修饰两性离子的核壳树状分子pcstd-gd以及化疗药物阿霉素dox和microrna21基因抑制剂mir 21i。
3、所述pcstd-gd和dox的摩尔比为1:10~1:20;所述pcstd-gd和mir 21i的n/p比为0.125:1~30:1。
4、本发明还提供了一种多功能诊疗一体化核壳树状分子纳米平台的制备方法,包括如下步骤:
5、(1)将第三代聚酰胺-胺树状大分子溶于二甲基亚砜dmso中,然后在磁力搅拌条件下,逐滴加入同样溶于dmso中的羟基琥珀酰亚胺-四氮杂环十二烷四乙酸酯dota-nhs进行反应,透析、冻干处理,得到g3-dota;
6、(2)将金刚烷乙酸ad-cooh分散在dmso中,然后在磁力搅拌条件下,逐滴加入1-(3-二甲基丙基)-3-乙基碳二亚胺盐酸盐edc·hcl和n-羟基丁二酰亚胺nhs的dmso溶液活化,将活化的ad-cooh溶液缓慢加入到g3-dota溶液中反应,透析、冻干处理,得到ad-g3-dota;
7、(3)将β-环糊精β-cd分散在dmso中,逐滴加入羰基咪唑cdi的dmso溶液活化,将活化的β-cd溶液加入到g5.nh2溶液中,继续反应,透析、冻干处理,得到g5-cd;
8、(4)将步骤(2)中ad-g3-dota和步骤(3)中g5-cd分别用超纯水溶解后混合,反应,透析、冻干处理,得到g5-cd/ad-g3-dota核壳树状分子,即cstd;
9、(5)将步骤(4)中cstd溶于超纯水中,然后将两性离子1,3-丙烷磺内酯1,3-ps逐滴加入到cstd溶液中,反应,透析、冻干处理,得到1,3-ps-cstd,即pcstd;
10、(6)将步骤(5)中pcstd和硝酸钆gd(no3)3·6h2o分别用超纯水溶解后混合,反应,透析、冻干处理,得到pcstd-gd;
11、(7)将步骤(6)中pcstd-gd溶于超纯水中,与甲醇溶解的去质子化的dox·hcl溶液混合,敞口反应,离心处理,取上清液进行冻干处理,得到pcstd-gd/dox复合物;
12、(8)将步骤(7)中pcstd-gd/dox与mir 21i进行孵育,得到pcstd-gd/dox/mir 21i复合物。
13、所述步骤(1)中g3.nh2和dota-nhs的摩尔比为1:3~6;反应温度为室温,反应时间为24~30h;透析采用截留量为1000da的纤维素透析膜在超纯水中透析(用去离子水透析3天,每天3次,每次2l去离子水)。
14、所述步骤(2)中ad-cooh、edc·hcl、nhs和g3-dota的摩尔比为1~2:20:20:1;活化温度为室温,活化时间为2~4h;反应温度为室温,反应时间为2~4d;透析采用截留量为1000da的纤维素透析膜在超纯水中透析三天。
15、所述步骤(3)中β-cd、cdi和g5.nh2的摩尔比为25~30:250~300:1;活化温度为室温,活化时间为4~6h;反应温度为室温,反应时间为48~60h;透析采用截留量为8000-10000da的纤维素透析膜在超纯水中透析三天。
16、所述步骤(4)中ad-g3-dota与g5-cd的摩尔比为1:12~15;反应温度为室温,反应时间为48~60h;透析采用截留量为10000da的纤维素透析膜在超纯水中透析三天。
17、所述步骤(5)中1,3-ps与cstd的摩尔比为1:90~100;反应温度为室温,反应时间为24-30h;透析采用截留1000da的纤维素透析膜在超纯水中透析三天。
18、所述步骤(6)中pcstd与gd(no3)3·6h2o的摩尔比为1:60~70;反应温度为室温,反应时间为24-30h;透析采用截留量为1000da的纤维素透析膜在超纯水中透析三天。
19、所述步骤(7)中pcstd-gd核壳树状分子与dox的摩尔比为1:10~20;敞口反应为避光敞口室温搅拌过夜,反应结束后离心的转速为7500~8500r/min,离心时间为8~20min。
20、所述步骤(8)中pcstd-gd/dox与mir 21i的孵育为:将pcstd-gd/dox和mir 21i分别用焦碳酸二乙酯depc水溶解,然后按照不同的氮磷比将两种溶液混合均匀后于室温孵育20~30min。
21、本发明的技术方案之二提供了多功能诊疗一体化核壳树状分子-基因复合物,其采用如上所述的制备方法制备得到。
22、本发明的技术方案之三提供了多功能诊疗一体化核壳树状分子-药物与基因共负载复合物,其采用如上所述的制备方法制备得到。
23、本发明的技术方案之四提供了联合utmd技术后,多功能诊疗一体化核壳树状分子纳米平台在肿瘤mr成像、化疗及基因治疗中的应用。制备的一系列核壳树状分子纳米平台及其复合物具有抗蛋白吸附、mr成像、化疗及基因治疗性能,联合utmd技术后,进行了体外抗三阴性乳腺癌研究和通过静脉注射的方式用于原位三阴性乳腺癌模型的mr成像、化疗及基因治疗的联合治疗。
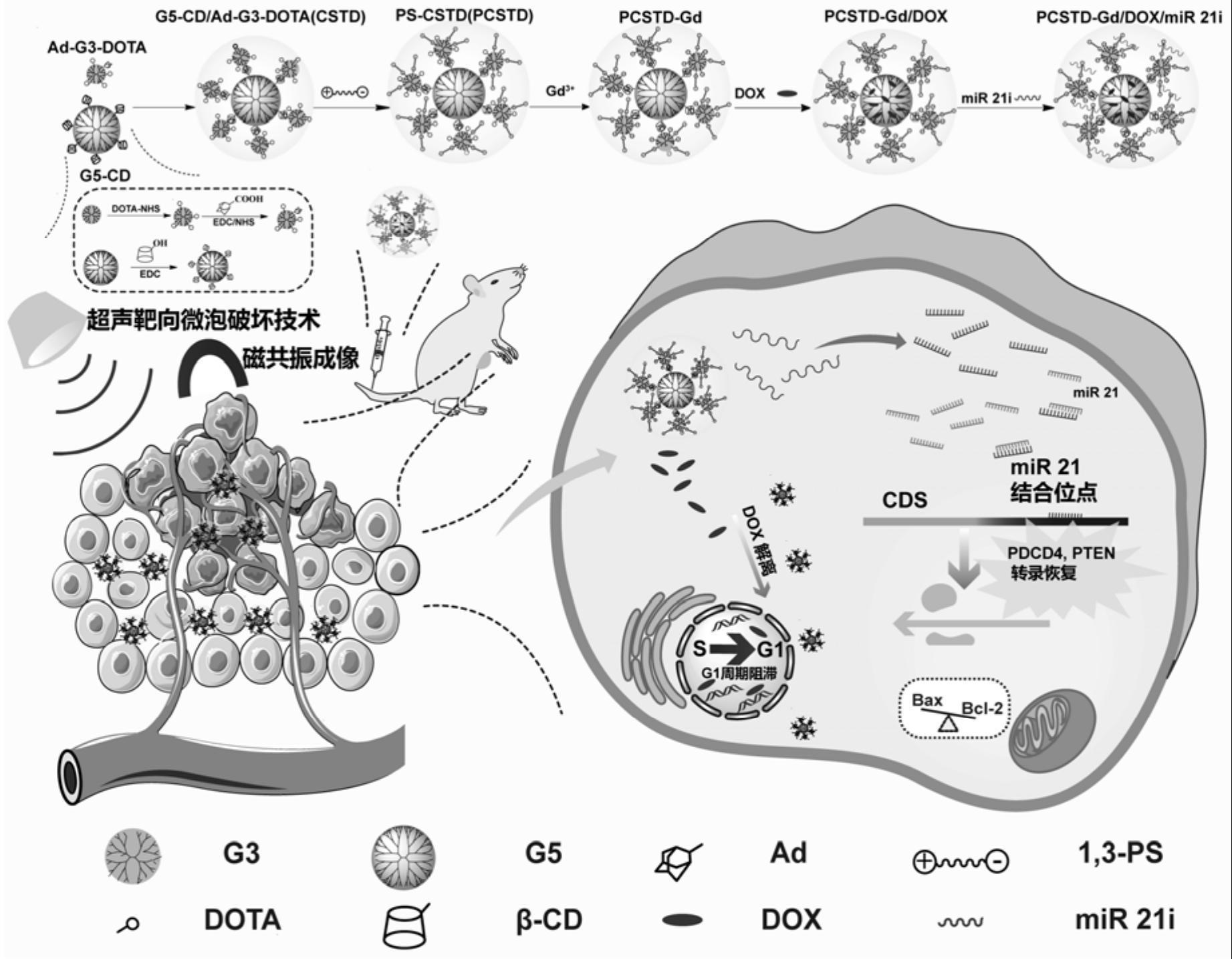
24、本发明利用修饰了螯合剂(dota)和ad的氨基末端的壳组分树状分子(ad-g3-dota)和修饰了β-cd的氨基末端的核组分树状分子(g5-cd)通过超分子自组装形成核壳树状分子纳米平台(g5-cd/ad-g3-dota,cstd),并在表面进一步修饰两性离子1,3-ps和螯合gd3+,最终形成集磁共振(mr)成像功能和抗蛋白吸附功能于一体的多功能诊疗一体化纳米平台。利用多功能诊疗一体化核壳树状分子纳米平台用于抗非特异性蛋白吸附,共负载造影剂(gd)、抗癌药物阿霉素(dox)和基因抑制剂(mir 21i),并联合utmd技术,大大改善了成像和联合治疗效果。通过对核壳树状分子的理性设计和精准合成,该发明克服了核壳树状分子在应用上的一些缺陷,并且将目前临床上诊断和治疗两个分离的过程/功能集成于一个纳米材料,利用多重修饰,构建了多功能诊疗一体化核壳树状分子纳米平台。
25、有益效果
26、(1)本发明利用修饰了螯合剂的氨基末端的壳组分树状分子,通过超分子自组装与核组分树状分子形成了核壳树状分子,进而表面修饰两性离子并螯合钆离子,构建出具有抗蛋白吸附性能和mr成像性能的核壳树状分子纳米平台。其次,本发明利用核壳树状分子纳米平台的内部空腔和静电相互作用分别物理包裹抗癌药物dox和压缩了基因抑制剂mir 21i用于三阴性乳腺癌的化疗与基因治疗的联合治疗。最后,本发明联合utmd技术,进一步增强了多功能诊疗一体化核壳树状分子纳米平台在肿瘤部位的渗透,用于增强的三阴性乳腺癌的mr成像、化疗与基因治疗的联合治疗。通过对核壳树状分子纳米材料的理性设计和应用,该发明克服了核壳树状分子在应用上的一些缺陷,并且将对临床上的药物副作用和单一治疗效果有限这两大难题有潜在的指导意义,在实现肿瘤联合治疗、诊疗一体化方面具有潜在的应用前景。
27、(2)本发明工艺简单,成本低廉,易于操作分离,具有良好的发展前景;本发明制备的两性离子修饰的核壳树状分子具有良好的抗污性能,可以抵抗网状内皮系统的清除,延长血液循环时间;制备的多功能核壳树状分子纳米平台具有mr成像功能、药物缓释性能和基因转染功能,可实现诊疗一体化;本发明联合utmd技术后,可进一步增强纳米平台在肿瘤部位的聚集和渗透,增强多功能核壳树状分子纳米平台成像和联合治疗效果。
- 还没有人留言评论。精彩留言会获得点赞!