一种负泊松比结构人工椎间盘及其制备方法
本发明属于人工椎间盘,特别涉及一种负泊松比结构人工椎间盘及其制备方法。
背景技术:
1、椎间盘是连接脊柱相邻椎体之间的软骨组织,由中央的胶状髓核和外周的纤维环构成,能够分散脊柱载荷以维持脊柱稳态。椎间盘疾病,尤其是椎间盘突出,是现代社会中最常见的脊柱疾病之一,据统计,它影响着全球数以百万计的成年人,成为导致工作能力丧失和生活质量下降的重要因素。椎间盘突出主要发生在腰椎和颈椎区域,是由于椎间盘的退化、损伤或磨损导致。随着年龄的增长,椎间盘逐渐失去水分,变得更脆弱,外部的纤维环容易发生裂纹,进而导致椎间盘内部的髓核组织突出,压迫附近的神经根或脊髓。在许多情况下,椎间盘突出的治疗包括物理治疗、药物治疗和生活方式调整。然而,对于某些患者来说,保守治疗可能无法提供长期的缓解,特别是在神经症状明显或脊柱稳定性受到威胁的情况下。因此在保守治疗失败的情况下,椎间盘手术是一种较为理想的治疗方式,其中人工椎间盘置换手术,是一种效果明确的手术方式。
2、在临床上,椎间盘置换手术用的人工椎间盘通常是金属椎间盘,此种人工椎间盘虽然具有稳定的化学性质,但是由于其缺乏高弹性,因此人体脊柱承载的向压力负荷得不到充分的缓冲,长此以往会导致相邻节段疾病,包括椎体退变、新生骨赘形成、椎间盘突出等。此外,金属植入物还无法完全恢复脊柱的正常生理运动功能。
3、由于金属人工椎间盘存在上述问题,因而非金属人工椎间盘的研究越来越受到重视和发展,例如,《bioactive materials》公开了一种3d生物打印双生长因子释放椎间盘支架〔见bioactive materials. 第6卷第1期(2021)179-190〕,该椎间盘支架模型的髓核(np)和纤维环(af) 采用3d 生物打印墨水打印,所述3d 生物打印墨水由ctgf@pda nps(或tgf-β3@pda nps)、骨髓间充质干细胞和水凝胶混合形成。《nanoscale》公开了一种仿生纳米纤维构建的组织工程椎间盘支架〔见nanoscale. 第35卷第九期(2017)13095-13103〕,该组织工程椎间盘支架用i型胶原同心环排列的电纺支架和藻酸盐水凝胶组合形成。然而这些仿生的人工椎间盘都是传统的正泊松比结构的设计,由于正泊松比材料在受到纵向压缩载荷时会发生横向膨胀,因此这种结构设计的人工椎间盘在植入体内一段时间后会发生塌陷,甚至内部的髓核会因挤压而破坏。
技术实现思路
1、本发明的目的在于克服现有技术的不足,提供一种负泊松比结构人工椎间盘及其制备方法,以便能获得兼具生物相容性和力学性能稳定的人工椎间盘,并简化制备工艺。
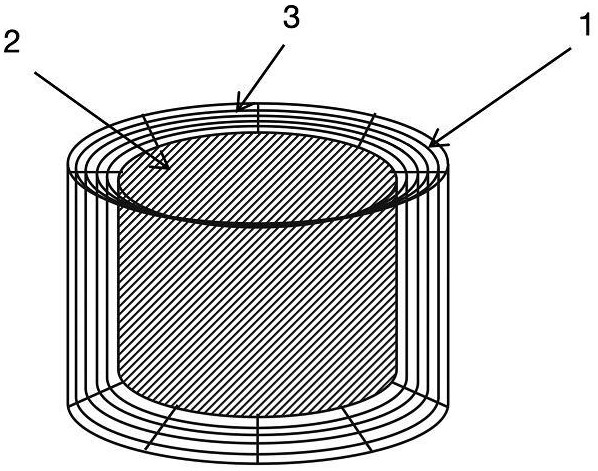
2、本发明所述负泊松比结构人工椎间盘,由接枝醛基的负泊松比结构圆环形支架与位于所述圆环形支架中心孔内和包覆在所述圆环形支架表面的醛基化海藻酸钠/明胶复合水凝胶通过化学键结合而成;接枝醛基的负泊松比结构圆环形支架是由聚己内酯制作的多个负泊松比结构同心圆环片相贴套装并连接成一体后通过醛基化处理形成。
3、所述负泊松比结构,包括内凹结构、手性结构、旋转多边形结构、折纸结构、穿孔板结构和片状褶皱结构。其中,内凹结构是通常使用的负泊松比结构。负泊松比材料在轴向压缩时会发生横向收缩变形,在物体撞击时,负泊松比材料会因冲击物体产生纵向压缩而形成横向收缩,接触点附近的材料向物体汇聚从而使接触点局部密度增加出现致密化,以增加材料压痕阻力,不易产生压陷凹痕。
4、上述负泊松比结构的人工椎间盘中,聚己内酯制作的负泊松比结构同心圆环片的厚度为2mm ~ 2.5mm,数量为5个~ 6个。
5、上述负泊松比结构的人工椎间盘中,由聚己内酯制作的多个负泊松比结构同心圆环片相贴套装并连接成一体的负泊松比结构圆环形支架,其外径、中心孔孔径和高度根据患者椎间盘的尺寸确定。
6、上述负泊松比结构的人工椎间盘中,表面包覆有海藻酸钠/明胶复合水凝胶的负泊松比结构圆环形支架对应于椎间盘的纤维环(af),位于所述圆环形支架中心孔内的海藻酸钠/明胶复合水凝胶对应于椎间盘的髓核(np)。
7、本发明所述负泊松比结构人工椎间盘的制备方法,步骤如下:
8、(1)负泊松比结构圆环形支架的制备;
9、以聚己内酯粉末为原料,通过3d打印得到由聚己内酯制作的多个负泊松比结构同心圆环片相贴套装并连接成一体的负泊松比结构圆环形支架;
10、(2)负泊松比结构圆环形支架的醛基化处理;
11、将1,6-己二胺溶于异丙醇中配制成质量浓度10%的1,6-己二胺异丙醇溶液,将步骤(1)制备的负泊松比结构圆环形支架浸泡在所述1,6-己二胺异丙醇溶液中,在室温下磁搅拌10h~12h,然后用去离子水超声清洗去除未反应的1,6-己二胺,再放入真空干燥箱中在37 ℃干燥10h~12h,得到的氨解支架;
12、将氨解支架放入质量浓度2%的戊二醛水溶液中于室温浸泡10h~12 h,然后用去离子水超声清洗去除未反应的戊二醛,再放入真空干燥箱中于37℃干燥20h~24h,得到接枝醛基的负泊松比结构圆环形支架;
13、(3)醛基化海藻酸钠/明胶复合水凝胶的制备;
14、将海藻酸钠溶于无水乙醇中配制成浓度0.2g/ml的海藻酸钠乙醇溶液,将氧化剂高碘酸钠溶于去离子水中配制成浓度0.1g/ml~ 0.12 g/ml的高碘酸钠水溶液,将海藻酸钠乙醇溶液与高碘酸钠水溶液按体积比1:9~10 计量,然后将计量好的高碘酸钠水溶液在搅拌下加入海藻酸钠乙醇溶液,并在避光环境中继续搅拌6h~8h得反应液,随后将反应液离心后收集沉淀物,并用无水乙醇重复离心洗涤去除未反应的高碘酸钠,再经冷冻干燥得到醛基化海藻酸钠粉末;
15、将醛基化海藻酸钠粉末和硼砂溶于37℃去离子水中,配制成醛基化海藻酸钠质量浓度为4%、硼砂质量浓度为2%的混合液,将明胶溶于50℃~55℃的去离子水中配制成质量浓度12%的明胶水溶液,按明胶水溶液所含明胶与混合液所含醛基化海藻酸钠的质量比为1:1~3计量明胶水溶液和混合液,然后将明胶水溶液在搅拌下加入混合液并混合均匀,在37℃下静置 6h~8 h,再于室温静置20h~24 h,即得到醛基化海藻酸钠/明胶复合水凝胶;
16、(4)负泊松比结构人工椎间盘的形成;
17、将接枝醛基的负泊松比结构圆环形支架置于醛基化海藻酸钠/明胶复合水凝胶中,在37℃下静置6h~8h后再于室温静置 20h~24 h,在此过程中,醛基化海藻酸钠/明胶复合水凝胶进入接枝醛基的负泊松比结构圆环形支架中心孔并包覆其表面,醛基化海藻酸钠/明胶复合水凝胶中的氨基与接枝醛基的负泊松比结构圆环形支架上的醛基发生席夫碱反应形成亚胺键实现化学键结合,即形成负泊松比结构人工椎间盘。
18、上述方法中,步骤(3)冷冻干燥的温度为-50℃~-80℃,时间为24h~26 h。
19、本发明所述人工椎间盘克服了现有金属人工椎间盘和正泊松比结构人工椎间盘存在的不足,其应力应变趋势符合软骨组织,受到纵向压缩载荷时发生横向收缩,醛基化海藻酸钠/明胶复合水凝胶具有优异的抗压缩性能以及高回弹性和抗疲劳特性,与支架的结合强度显著提升。
20、本发明具有以下有益效果:
21、1、由于本发明中的醛基化海藻酸钠/明胶复合水凝胶由明胶和醛基化海藻酸钠通过亚胺键结合,因而具有优异的抗压缩性能以及高回弹性和抗疲劳特性(见实施例2)。
22、2、实验表明,本发明所述方法制备的醛基化海藻酸钠/明胶复合水凝胶和负泊松比结构人工椎间盘均具有良好的生物相容性(见实施例2)。
23、3、由于本发明所述负泊松比结构人工椎间盘由接枝醛基的负泊松比结构圆环形支架与位于所述圆环形支架中心孔内和包覆在所述圆环形支架表面的醛基化海藻酸钠/明胶复合水凝胶通过化学键结合而成,因而不仅呈现出与复合水凝胶一致的粘弹性行为,符合软骨组织的应力应变趋势,刚度达到 3.87± 0.75 mpa,与椎间盘力学需求相当,在受到纵向压缩载荷时会发生横向收缩,而且复合水凝胶与支架的结合强度显著提升,可有效避免物理结合在载荷作用下发生分相的问题。
24、4、由于本发明所述负泊松比结构人工椎间盘具有优良的力学性能和生物相容性,且复合水凝胶与支架的结合强度好,因而替代退变的椎间盘可获得良好的治疗效果。
25、5、本发明所述方法原料易于获取,制备工艺简单,便于操作,有利于实施应用。
- 还没有人留言评论。精彩留言会获得点赞!