二氧化氯水溶液及其制造方法与流程
本公开涉及一种在花粉、灰尘、皮屑、真菌等过敏诱发物质的处理;病原菌、病毒、有害化学物质(例如烟草(tabacco)烟雾、甲醛)等有害物质的处理;环境净化、室内外及食品的除臭、防霉及防腐等中广泛使用的二氧化氯水溶液及其制造方法。
背景技术:
二氧化氯(clo2)具有强大的氧化力,因此广泛用于花粉、灰尘、皮屑、真菌等过敏诱发物质的处理;病原菌、病毒、有害化学物质(例如烟草烟雾、甲醛)等有害物质的处理;环境净化、室内外及食品的除臭、防霉及防腐等。提出有含有在如此广泛的用途中使用的二氧化氯的组合物及其制造方法。
例如,日本专利特开平11-278808号公报(专利文献1)提出一种在构成成分中具有溶存二氧化氯气体、亚氯酸盐及ph调整剂的纯二氧化氯液剂;含有所述纯二氧化氯液剂及高吸水性树脂的凝胶状组合物;含有所述纯二氧化氯液剂及发泡剂的发泡性组合物;以及用于装入所述纯二氧化氯液剂、所述凝胶状组合物、及所述发泡性组合物的容器。
而且,国际公开wo2008/111358号(专利文献2)提出了一种二氧化氯用的稳定化组合物,即便自包含溶存二氧化氯的药剂持续以气体的形式排放二氧化氯,也可将所述药剂中的二氧化氯浓度保持为大致固定,所述二氧化氯用的稳定化组合物包括亚氯酸盐与ph调整剂的组合,ph调整剂是25℃下的5%水溶液的ph为2.5~6.8的具有缓冲性的酸或其盐。
现有技术文献
专利文献
专利文献1:日本专利特开平11-278808号公报
专利文献2:国际公开wo2008/111358号
技术实现要素:
发明所要解决的问题
根据日本专利特开平11-278808号公报(专利文献1),作为ph调整剂使用了柠檬酸,因此存在纯二氧化氯液剂、含有所述纯二氧化氯液剂及高吸水性树脂的凝胶状组合物、含有所述纯二氧化氯液剂及发泡剂的发泡性组合物中的初期二氧化氯的浓度变高并且其后二氧化氯的浓度下降的问题。
根据国际公开wo2008/111358号(专利文献2),作为ph调整剂使用了磷酸或其盐,因此存在虽然能够在ph为2.5~6.8的广区域中将二氧化氯用的稳定化组合物的二氧化氯浓度保持为大致固定,但担心带给环境负荷的问题。
本公开为了解决所述课题,以提供一种不使用磷酸或其盐作为ph调整剂而稳定地维持二氧化氯的浓度的二氧化氯水溶液及其制造方法。
解决问题的技术手段
本公开的一形式的二氧化氯水溶液包含二氧化氯、pka为2.5以上的弱酸的钾盐及亚氯酸盐,ph为4.0以上且7.5以下。
在所述二氧化氯水溶液中,所述弱酸的钾盐可设为柠檬酸钾。
在所述二氧化氯水溶液中,可将钾的浓度设为10ppm以上。
本公开的一形式的二氧化氯水溶液的制造方法包括:第一步骤,准备包含二氧化氯的第一水溶液;第二步骤,通过将第一水溶液与包含pka为2.5以上的弱酸的钾盐的第二水溶液混合,制备ph为4.0以上且7.5以下的中间水溶液;以及第三步骤,通过将中间水溶液与包含亚氯酸盐的第三水溶液混合,或者通过在将所述中间水溶液与所述第三水溶液混合后进而添加所述第二水溶液,制备ph为4.0以上且7.5以下的二氧化氯水溶液。
在所述二氧化氯水溶液的制造方法中,所述弱酸的钾盐可设为柠檬酸钾。
发明的效果
根据本公开,可提供一种不使用磷酸或其盐作为ph调整剂而稳定地维持二氧化氯的浓度的二氧化氯水溶液及其制造方法。
附图说明
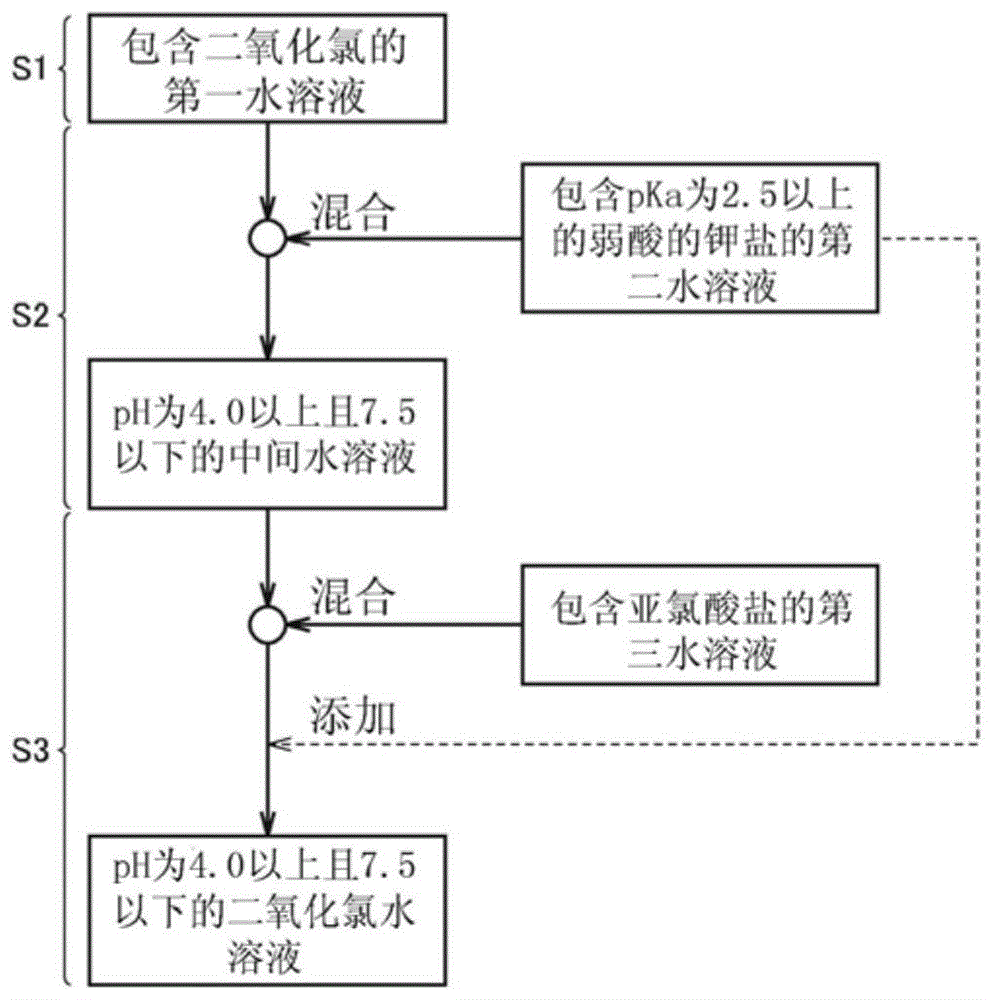
[图1]图1是表示本公开的一形式的二氧化氯水溶液的制造方法的一例的流程图。
具体实施方式
<实施方式1:二氧化氯水溶液>
作为本公开的一实施方式的二氧化氯水溶液包含二氧化氯、pka为2.5以上的弱酸的钾盐及亚氯酸盐,ph为4.0以上且7.5以下。本实施方式的二氧化氯水溶液包含二氧化氯、作为ph调整剂的pka为2.5以上的弱酸的钾盐、及亚氯酸盐,将ph调整为4.0以上且7.5以下,因此不使用磷酸或其盐作为ph调整剂而稳定地维持二氧化氯的浓度。此处,磷酸的pka为2.1,因此实施方式1的二氧化氯水溶液中未含磷酸或其盐中的任一者。
(二氧化氯)
二氧化氯水溶液中所含的二氧化氯(clo2)以溶存于二氧化氯水溶液中的溶存二氧化氯的形式存在。在室温(例如25℃)大气中,二氧化氯水溶液中的溶存二氧化氯因其一部分以气体的形式被排放至水溶液外(大气中)而减少,但如后所述那样通过ph平衡而自亚氯酸盐中的亚氯酸离子(clo2-)补充。
二氧化氯水溶液通过所述溶存二氧化氯及所述以气体形式排放至水溶液外的二氧化氯,而发挥花粉、灰尘、皮屑、真菌等过敏诱发物质的处理;病原菌、病毒、有害化学物质(例如烟草(tabacco)烟雾、甲醛)等有害物质的处理;环境净化、室内外及食品的除臭、防霉及防腐等的作用效果。
二氧化氯水溶液中所含的二氧化氯的浓度并无特别限制,就提高由二氧化氯产生的所述作用效果的观点而言,优选为10ppm以上,更优选为50ppm以上,进而优选为100ppm以上,就稳定地维持二氧化氯的浓度的观点而言,优选为2000ppm以下,更优选为1000ppm以下,进而优选为400ppm以下。此处,二氧化氯水溶液中所含的二氧化氯(clo2)的浓度是在190ml~200ml的离子交换水中添加碘化钾0.5g与ph为7的缓冲水溶液1ml,其次添加1ml~10ml的二氧化氯水溶液,并立刻利用0.1n硫代硫酸钠水溶液进行滴定,根据滴定量aml通过以下的式(1)
(clo2[ppm])=a×0.1×67450/(二氧化氯水溶液的质量[g])…(1)
算出。另外,所述ph为7的缓冲水溶液是使用将磷酸氢二钠(na2hpo4)4.57g及磷酸二氢钾(kh2po4)9.228g溶解于离子交换水中将总量制成1000ml的缓冲水溶液。
(pka为2.5以上的弱酸的钾盐)
就稳定地维持作为ph调整剂而包含在二氧化氯水溶液中的二氧化氯的浓度的观点而言,二氧化氯水溶液中所含的pka为2.5以上的弱酸的钾盐(k盐)优选为多元酸的钾盐,例如柠檬酸(pka1为2.90、pka2为4.35、pka3为5.69)的钾盐即柠檬酸钾、苹果酸(pka1为3.23、pka2为4.77)的钾盐即苹果酸钾、琥珀酸(pka1为3.99、pka2为5.20)的钾盐即琥珀酸钾等,更优选为柠檬酸钾。此处,在柠檬酸钾中有柠檬酸一钾(monopotassiumcitrate)、柠檬酸二钾(dipotassiumcitrate)及柠檬酸三钾(tripotassiumcitrate)三种,这些中,进而优选为柠檬酸二钾及柠檬酸三钾。而且,钾盐可为无水盐,也可为有水盐。此处,在为多元酸的情况下,pka为2.5以上是指各阶段中的pkak(k为1以上的整数)全部为2.5以上即最小的pkak为2.5以上。
作为ph调整剂,一般而言,就容易获得的观点而言,使用弱酸的钠盐(na盐)。发明人们当初制作了包含二氧化氯、亚氯酸盐及作为ph调整剂的pka为2.5以上的弱酸的钠盐即柠檬酸钠的二氧化氯水溶液,但难以稳定地维持所述二氧化氯水溶液中的二氧化氯的浓度。
关于通过使用pka为2.5以上的弱酸的钾盐(k盐)代替pka为2.5以上的弱酸的钠盐(na盐)作为ph调整剂,为何可稳定维持二氧化氯水溶液中的二氧化氯的浓度,详细情况虽不明,但认为是由于因在包含通过大气中的二氧化碳进行溶解而生成的碳酸的水溶液中,钠盐会形成碳酸氢盐,相对于此钾盐不会形成碳酸氢盐、相较于钠,钾容易被水润湿而更良好地被水合从而更稳定地存在于水溶液中等,而可将二氧化氯水溶液的ph更稳定地维持在规定的区域(具体而言是ph为4.0以上且7.5以下的区域)。本发明人们发现通过使用pka为2.5以上的弱酸的钾盐代替pka为2.5以上的弱酸的钠盐作为ph调整剂可极其稳定地维持二氧化氯水溶液中的二氧化氯的浓度这一即使本领域技术人员也未预测到的显著的效果,由此完成了本发明。
二氧化氯水溶液中所含的pka为2.5以上的弱酸的钾盐在水溶液中解离而生成pka为2.5以上的弱酸离子与钾(k)离子。在二氧化氯水溶液中作为离子而存在的钾的浓度并无特别限制,就通过ph缓冲效果稳定地维持二氧化氯的浓度的观点而言,优选为10ppm以上,更优选为100ppm以上,进而优选为200ppm以上,特别优选为500ppm以上,就抑制ph缓冲效果的提高的观点而言,优选为10质量%(100000ppm)以下,更优选为1质量%(10000ppm)以下,进而优选为5000ppm以下,特别优选为2500ppm以下。此处,二氧化氯水溶液中所含的钾的浓度是通过荧光x射线分析、原子吸光分析等进行测定。
(亚氯酸盐)
二氧化氯水溶液中所含的亚氯酸盐只要为可解离能够在水溶液中通过ph平衡来补充二氧化氯的亚氯酸离子(clo2-)的亚氯酸盐,则并无特别限制,可列举亚氯酸钠(naclo2)、亚氯酸钾(kclo2)、亚氯酸锂(liclo2)等除氢外的第一族元素(碱金属元素)的亚氯酸盐、亚氯酸钙(ca(clo2)2)、亚氯酸锶(sr(clo2)2)、亚氯酸钡(ba(clo2)2)、亚氯酸镁(mg(clo2)2)等第二族元素的亚氯酸盐等。这些中,就解离度大的观点而言,优选为除氢外的第一族元素(碱金属元素)的亚氯酸盐,进而,就容易被水合的观点而言,更优选为亚氯酸钾,在除氢外的第一族元素(碱金属元素)的亚氯酸盐中,亚氯酸钠特别容易获得,在使用上也无问题。
二氧化氯水溶液中所含的亚氯酸盐在水溶液中解离而生成亚氯酸离子(clo2-)与抗衡离子。所述亚氯酸离子的浓度并无特别限制,就通过ph平衡自亚氯酸离子补充二氧化氯而稳定地维持二氧化氯的浓度的观点而言,优选为100ppm以上,更优选为500ppm以上,进而优选为2000ppm以上,就抑制亚氯酸盐的剩余的观点而言,优选为10质量%(100000ppm)以下,更优选为2.5质量%(25000ppm)以下,进而优选为1质量%(10000ppm)以下。此处,二氧化氯水溶液中所含的亚氯酸离子(clo2-)的浓度是在所述为了测定二氧化氯水溶液中所含的二氧化氯(clo2)的浓度而进行了滴定的水溶液中,加入2ml~3ml的2.5n盐酸水溶液,在暗处静置5分钟后,再次利用0.1n硫代硫酸钠水溶液进行滴定,根据滴定量bml,通过以下的式(2)
(clo2-[ppm])=(b/4-a)×0.1×67450/(二氧化氯水溶液的质量[g])…(2)
算出。另外,式(2)中的a与式(1)中的a相同。
(二氧化氯水溶液的ph)
二氧化氯水溶液因ph调整剂即pka为2.5以上的钾盐的ph缓冲作用,ph为4.0以上且7.5以下。二氧化氯水溶液的ph就稳定地维持二氧化氯的浓度的观点而言,为4.0以上,优选为5.0以上,更优选为5.5以上,就提高由二氧化氯产生的所述作用效果的观点而言,为7.5以下,优选为不足7.0,更优选为6.5以下。
<实施方式2:二氧化氯水溶液的制造方法>
参照图1,作为本公开的另一实施方式的二氧化氯水溶液的制造方法包括:第一步骤s1,准备包含二氧化氯的第一水溶液;第二步骤s2,通过将第一水溶液与包含pka为2.5以上的弱酸的钾盐的第二水溶液混合,制备ph为4.0以上且7.5以下的中间水溶液;以及第三步骤s3,通过将中间水溶液与包含亚氯酸盐的第三水溶液混合,或者通过在将中间水溶液与第三水溶液混合后进而添加第二水溶液,制备ph为4.0以上且7.5以下的二氧化氯水溶液。本实施方式的二氧化氯水溶液的制造方法通过在将ph保持为规定的区域(具体而言ph为4.0以上且7.5以下的区域)的状态下,依次混合包含二氧化氯的第一水溶液、第一水溶液与包含pka为2.5以上的弱酸的钾盐的第二水溶液、及包含亚氯酸盐的第三水溶液,而可效率良好地制造稳定地维持二氧化氯的浓度的ph为4.0以上且7.5以下的稳定化二氧化氯。
(第一步骤)
在第一步骤s1中,准备包含二氧化氯的第一水溶液。包含二氧化氯的第一水溶液中,关于包含溶存二氧化氯的水溶液可通过现有的制造方法来制造。例如,通过利用现有的方法将包含亚氯酸盐(例如亚氯酸钠)的水溶液与包含酸(例如盐酸)的水溶液混合,使亚氯酸盐与酸反应,可制备包含二氧化氯(具体而言是溶存二氧化氯)的水溶液。
第一水溶液中所含的二氧化氯的浓度并无特别限制,就稳定地维持二氧化氯的浓度的观点而言,优选为500ppm以上,更优选为1000ppm以上,进而优选为2000ppm以上,而且,就稳定地维持二氧化氯的浓度的观点而言,优选为5质量%(50000ppm)以下,更优选为2质量%(20000ppm)以下,进而优选为1质量%(10000ppm)以下。此处,第一水溶液中所含的二氧化氯的浓度是通过与所述测定二氧化氯水溶液中所含的二氧化氯的浓度的方法同样的方法进行测定。而且,就使制造步骤中的ph调整容易的观点而言,第一水溶液的ph优选为4.0以上且7.5以下。另外,测定第一水溶液至第三水溶液及中间水溶液的ph的方法并无特别限制,可采用利用ph计的测定等现有的方法。
(第二步骤)
在第二步骤s2中,通过将第一水溶液与包含pka为2.5以上的弱酸的钾盐的第二水溶液混合,制备ph为4.0以上且7.5以下的中间水溶液。混合第一水溶液与第二水溶液的方法并无特别限制,可采用现有的混合方法。
第二水溶液中所含的pka为2.5以上的弱酸的钾盐在水溶液中解离而生成pka为2.5以上的弱酸离子与钾(k)离子。在第二水溶液中作为离子而存在的钾的浓度并无特别限制,就将ph缓冲作用维持得高的观点而言,优选为0.1质量%(1000ppm)以上,更优选为1质量%(10000ppm),进而优选为2质量%(20000ppm)以上,就抑制ph缓冲效果的提高的观点而言,优选为30质量%(300000ppm)以下,更优选为20质量%(200000ppm)以下,进而优选为10质量%(100000ppm)以下。此处,第二水溶液中所含的钾的浓度是通过荧光x射线分析、原子吸光分析等进行测定。而且,第二水溶液的ph就使制造步骤中的ph调整容易的观点而言,优选为4.0以上且7.5以下。此处,pka为2.5以上的弱酸的钾盐如在实施方式1中所述那样优选为柠檬酸钾、苹果酸钾、琥珀酸钾等,更优选为柠檬酸钾。所述柠檬酸钾中有柠檬酸一钾(monopotassiumcitrate)、柠檬酸二钾(dipotassiumcitrate)及柠檬酸三钾(tripotassiumcitrate)三种,这些中,进而优选为柠檬酸二钾及柠檬酸三钾。
(第三步骤)
在第三步骤s3中,通过将中间水溶液与包含亚氯酸盐的第三水溶液混合,或者通过在将中间水溶液与第三水溶液混合后进而添加第二水溶液,制备ph为4.0以上且7.5以下的二氧化氯水溶液。混合中间水溶液与第三水溶液的方法并无特别限制,可采用现有的混合方法。而且,在所述混合液中进而添加第二水溶液的方法并无特别限制,可采用现有的添加方法。
第三水溶液中所含的亚氯酸盐在水溶液中解离而生成亚氯酸离子(clo2-)与抗衡离子。所述亚氯酸离子的浓度并无特别限制,就通过ph平衡自亚氯酸离子补充二氧化氯而稳定地维持二氧化氯的浓度的观点而言,优选为250ppm以上,更优选为1000ppm以上,进而优选为3000ppm以上,就抑制亚氯酸盐的剩余的观点而言,优选为20质量%(200000ppm)以下,更优选为15质量%(150000ppm)以下,进而优选为10质量%(100000ppm)以下。此处,第三水溶液中所含的亚氯酸离子的浓度是通过与所述测定二氧化氯水溶液中所含的亚氯酸离子的浓度的方法同样的方法进行测定。而且,就使制造步骤中的ph调整容易的观点而言,第三水溶液的ph优选为4.0以上且7.5以下。
在本实施方式的二氧化氯水溶液的制造方法中,就稳定且效率良好地制备ph为4.0以上且7.5以下的二氧化氯水溶液的观点而言,中间水溶液的ph为4.0以上且7.5以下。详细而言,就在制造时也抑制二氧化氯浓度的增加而稳定地进行维持的观点而言,为4.0以上,优选为5.0以上,更优选为5.5以上。而且,就制造时也抑制二氧化氯浓度的减少而稳定地进行维持的观点而言,为7.5以下,优选为不足7.0,更优选为6.5以下。
实施例
(实施例1)
1.二氧化氯水溶液的制作
参照图1,首先,作为第一步骤s1,在加压条件(1mpa)下,在通过使16质量%的亚氯酸钠水溶液(80ml/min)与10质量%的盐酸水溶液(77ml/min)反应而获得的二氧化氯水溶液中加入离子交换水,由此制备以4995ppm的浓度包含二氧化氯的高浓度二氧化氯水溶液。将所述高浓度二氧化氯水溶液5092g通过静静地流入至离子交换水90735g中而予以稀释,制备以265ppm的浓度包含二氧化氯的第一水溶液95827g。继而,作为第二步骤s2,将所述第一水溶液与以12.6质量%(126000ppm)的浓度包含作为ph调整剂的柠檬酸三钾的第二水溶液2405g通过螺旋搅拌静静地混合,制备ph为6.10的中间水溶液98232g。此处,第二水溶液是通过在离子交换水3000g中均匀溶解柠檬酸三钾一水合物432g而获得。继而,作为第三步骤s3,将所述中间水溶液与以25质量%(250000ppm)的浓度包含亚氯酸钠的第三水溶液2910g通过螺旋搅拌静静地混合,由此制作ph为6.06的二氧化氯水溶液101142g。另外,当在所述中间水溶液中混合所述第三水溶液后的二氧化氯水溶液的ph未成为规定的范围(具体而言ph为4.0以上且7.5以下,优选为5.0以上且不足7.0,更优选为5.5以上且6.5以下)的情况下,通过进一步适量添加所述第二水溶液而将二氧化氯水溶液的ph制成规定的范围(具体而言ph为4.0以上且7.5以下,优选为5.0以上且不足7.0,更优选为5.5以上且6.5以下)。
2.二氧化氯水溶液中二氧化氯及亚氯酸离子的浓度以及ph的经时变化将所述获得的二氧化氯水溶液300g放入至容量300ml的带螺旋帽(screwcap)的丙烯制容器中,对螺旋帽施加2.5n的扭矩压力进行密封。调查将所述密封容器分别静置于20℃的恒温槽内或50℃的恒温槽内时所述容器内的二氧化氯水溶液中的二氧化氯(clo2)及亚氯酸离子(clo2-)的浓度的经时变化。以如下方式测定二氧化氯水溶液中的二氧化氯的浓度。
二氧化氯水溶液中所含的二氧化氯(clo2)的浓度是在190ml~200ml的离子交换水中添加碘化钾0.5g与ph为7的缓冲水溶液1ml,其次添加1ml~10ml的二氧化氯水溶液,并立刻利用0.1n硫代硫酸钠水溶液进行滴定,根据滴定量aml通过以下的式(1)
(clo2[ppm])=a×0.1×67450/(二氧化氯水溶液的质量[g])…(1)
算出。另外,所述ph为7的缓冲水溶液是使用将磷酸氢二钠(na2hpo4)4.57g及磷酸二氢钾(kh2po4)9.228g溶解于离子交换水中将总量制成1000ml的缓冲水溶液。
二氧化氯水溶液中所含的亚氯酸离子(clo2-)的浓度是在所述为了测定二氧化氯水溶液中所含的二氧化氯(clo2)的浓度而进行了滴定的水溶液中,加入2ml~3ml的2.5n盐酸水溶液,在暗处静置5分钟后,再次利用0.1n硫代硫酸钠水溶液进行滴定,根据滴定量bml,通过以下的式(2)
(clo2-[ppm])=(b/4-a)×0.1×67450/(二氧化氯水溶液的质量[g])…(2)
算出。另外,式(2)中的a与式(1)中的a相同。
在所述式(1)及式(2)中,为了算出用于滴定的二氧化氯水溶液的质量,以如下方式测定所述二氧化氯水溶液的比重。即,利用量筒(graduatedcylinder)计量所述二氧化氯水溶液100ml,测定其质量,将测定出的质量除以所计量的体积,由此算出比重。所算出的比重为1.02。而且,二氧化氯水溶液的ph是通过ph计(堀场制作所股份有限公司制造ph/orpmeterd-72)进行测定。而且,关于初期的二氧化氯水溶液中所含的钾的浓度,在通过荧光x射线分析及原子吸光分析进行测定时,为1100ppm,与根据第二水溶液的钾的浓度计算二氧化氯水溶液的钾的浓度而得的计算值1082ppm很一致。
将分别在20℃的恒温槽内或50℃的恒温槽内静置时的所述此容器内的二氧化氯水溶液中所含的二氧化氯(clo2)及亚氯酸离子(clo2-)的浓度以及二氧化氯水溶液的ph的经时变化汇总于表1。
[表1]
参照表1,包含二氧化氯、作为ph调整剂的pka为2.5以上的弱酸的钾盐(例如柠檬酸钾)、及亚氯酸盐,ph为4.0以上且7.5以下的二氧化氯水溶液在气体环境温度20℃及50℃中的任一静置条件下,二氧化氯(clo2)的浓度均经时变化小,得到了稳定的维持。而且,在气体环境温度20℃及50℃中的任一静置条件下,均未见ph的下降。进而,在气体环境温度50℃的静置条件下,亚氯酸离子(clo2-)的浓度下降,理解为由亚氯酸盐中的亚氯酸离子对二氧化氯进行了补充。
(比较例1)
1.二氧化氯水溶液的制作
以与实施例1同样的方式,制备以浓度为4995ppm的浓度包含二氧化氯的高浓度二氧化氯水溶液5092g,并通过静静地流入至离子交换水90735g中进行稀释,制作了以195ppm的浓度包含二氧化氯、ph为6.03g的二氧化氯水溶液95827g。
2.二氧化氯水溶液中二氧化氯及亚氯酸离子的浓度以及ph的经时变化
针对所述获得的二氧化氯水溶液,以与实施例1同样的方式,测定二氧化氯水溶液中所含的二氧化氯(clo2)及亚氯酸离子(clo2-)的浓度以及二氧化氯水溶液的ph的经时变化,汇总于表2。
[表2]
参照表2,不含ph调整剂的二氧化氯水溶液在气体环境温度20℃及50℃中的任一静置条件下,二氧化氯(clo2)的浓度均大幅下降,并观察到ph的下降。而且,通过二氧化氯的解离而产生的亚氯酸离子的浓度无经时变化。
(比较例2)
1.二氧化氯水溶液的制作
首先,作为第一步骤,在加压条件(1mpa)下,在通过使16质量%的亚氯酸钠水溶液(80ml/min)与10质量%的盐酸水溶液(77ml/min)反应而获得的二氧化氯水溶液中加入离子交换水,由此制备以4995ppm的浓度包含二氧化氯的高浓度二氧化氯水溶液。将所述高浓度二氧化氯水溶液432g通过静静地流入至离子交换水9040g中而予以稀释,制备以228ppm的浓度包含二氧化氯的第一水溶液9472g。继而,作为第二步骤,将所述第一水溶液与以12.6质量%(126000ppm)的浓度包含作为ph调整剂的柠檬酸三钠的第二水溶液261g通过螺旋搅拌静静地混合,制备ph为6.10的中间水溶液9733g。此处,第二水溶液是通过在离子交换水750g中均匀溶解柠檬酸三钠二水合物108g而获得。继而,作为第三步骤,将所述中间水溶液与以25质量%(250000ppm)的浓度包含亚氯酸钠的第三水溶液288g通过螺旋搅拌静静地混合,由此制作ph为6.10的二氧化氯水溶液10021g。另外,当在所述中间水溶液中混合所述第三水溶液后的二氧化氯水溶液的ph未成为规定的范围(具体而言ph为4.0以上且7.5以下,优选为5.0以上且不足7.0,更优选为5.5以上且6.5以下)的情况下,通过进一步适量添加所述第二水溶液而将二氧化氯水溶液的ph制成规定的范围(具体而言ph为4.0以上且7.5以下,优选为5.0以上且不足7.0,更优选为5.5以上且6.5以下)。
2.二氧化氯水溶液中二氧化氯及亚氯酸离子的浓度以及ph的经时变化
针对所述获得的二氧化氯水溶液,以与实施例1同样的方式测量二氧化氯水溶液中所含的二氧化氯(clo2)及亚氯酸离子(clo2-)的浓度以及二氧化氯水溶液的ph经时变化,汇总于表3。
[表3]
参照表3,包含二氧化氯、作为ph调整剂的pka为2.5以上的弱酸的钠盐(例如柠檬酸钠)、及亚氯酸盐,ph为4.0以上且7.5以下的二氧化氯水溶液在气体环境温度20℃及50℃中的任一静置条件下,二氧化氯(clo2)的浓度均经时变化小于比较例1但大于实施例1,未得到稳定的维持。另外,在气体环境温度20℃及50℃中的任一静置条件下,均未见ph的下降。而且,在气体环境温度50℃的静置条件下,亚氯酸离子(clo2-)的浓度下降,理解为由亚氯酸盐中的亚氯酸离子对二氧化氯进行了补充。
根据比较例2与实施例1的对比可明确,在使用了作为ph调整剂的pka为2.5以上的弱酸的钠盐(例如柠檬酸三钠)的二氧化氯水溶液中,二氧化氯(clo2)的浓度是不稳定的,但在使用了作为ph调整剂的pka为2.5以上的弱酸的钾盐(例如柠檬酸三钾)的二氧化氯水溶液中,二氧化氯(clo2)的浓度得到了稳定的维持。
应认为此次所公开的实施方式及实施例在所有的方面均为例示,非限制性者。本发明的范围是由权利要求表示而非所述实施方式及实施例,并且意图包含与权利要求均等的意思及范围内的所有的变更。
符号的说明
s1:第一步骤
s2:第二步骤
s3:第三步骤。
- 还没有人留言评论。精彩留言会获得点赞!