含铬污泥制备硫酸铬钾的方法
1.本发明涉及的是一种重金属回收领域的技术,具体是一种含铬污泥制备硫酸铬钾的方法。
背景技术:
2.资源化回收利用含铬污泥,将其制备为应用广泛的高附加值的化工产品,不但能解决环境污染问题,而且可以提高含铬污泥的资源化利用水平。现有技术利用含铬污泥与硫酸溶液混合加热浸出可溶的三价铬,制备碱式硫酸铬,由于工艺简单,重金属分离不彻底,所制备的碱式硫酸铬纯度低,通常仅能用于低档的铬鞣剂。硫酸铬钾是一种高附加值的三价铬盐产品,广泛应用于三价铬电镀、三价铬钝化以及媒染剂、定影剂、高档鞣革剂、食品添加剂、采油压裂液交联剂中,还用于玻璃、陶瓷等领域。现有的硫酸铬钾的制备方法主要采用化工原料重铬酸钾在硫酸的存在下,用高纯还原剂还原重铬酸钾进行制备,但该方法需要价格昂贵的化工原料重铬酸钾;另一方面,由于硫酸铬钾溶解度大,通常需要采用高浓度条件下的结晶工艺进行结晶,然而硫酸铬钾在高浓度条件下结晶难,而一旦结晶又易成坨,形成大块晶体,严重影响产品的外观和市场价格。外观紫红色光亮、颗粒均匀细小的硫酸铬钾结晶是市场欢迎的高附加值产品而又是制备的难点。而采用含铬污泥为起始原料,其杂质含量高,会进一步影响所制备硫酸铬钾产品的纯度。
技术实现要素:
3.本发明针对现有技术存在的上述不足,提出一种含铬污泥制备硫酸铬钾的方法,具有纯度高、结晶颗粒均匀和紫红色光泽外观的特点。
4.本发明是通过以下技术方案实现的:
5.本发明涉及一种含铬污泥制备硫酸铬钾的方法,将含铬污泥溶于强酸溶液后过滤得到含有三价铬离子以及铁、铜、镍离子的滤液,向其中缓慢加入naoh,滤液ph由2.0调至4.0,形成氢氧化铬沉淀;向氢氧化铬沉淀中加入水和浓硫酸并在溶解后加入硫酸钾得到硫酸铬钾溶液;最后经搅拌结晶处理得到紫红色光亮外观、颗粒均匀细小的(kcr(so4)2.12h2o)。
6.所述的缓慢加入是指:naoh加入量和速度按照每小时ph上升速率0.25~0.40
△
ph/h进行控制,naoh加入时间为5~8h。
7.所述的缓慢加入,优选同时以速率10转/min搅拌。
8.所述的氢氧化铬沉淀、浓硫酸、硝酸钾和水的比例为2:3:1:18~20。
9.所述的搅拌结晶处理是指:搅拌、静置间歇操作,每次静置时间18~24小时,然后短时间搅拌,转速5~15转/min,其中前四次的搅拌时间均为8
‑
12min,第五次搅拌之前先加入结晶总量0.2%的硫酸铬钾晶种,然后搅拌15
‑
20min,第六次之后的搅拌时间均为15
‑
20min;共持续搅拌、静置间歇操作6~8次。
10.所述方法,具体包括:
11.步骤1)三价铬离子浸出:将含铬污泥溶于强酸溶液,搅拌反应,溶解的ph值控制在2;过滤,得到含有三价铬离子以及铁、铜、镍等杂质离子的滤液a,使固液分离;
12.步骤2)氢氧化铬沉淀的制备与杂质离子的分离:将步骤1)得到的滤液a稀释至含cr
3+
量1~3%,缓慢加入naoh溶液,具体为:naoh加入量和速度按照每小时ph上升速率0.25~0.40
△
ph/h进行控制,naoh加入时间为5~8h且同时以速率10转/min进行搅拌,使得ph由2.0上升至最终4.0并形成氢氧化铬沉淀;洗涤压滤得到易溶于酸的氢氧化铬沉淀b;
13.步骤3)硫酸铬钾溶液的制备:以步骤2)得到的氢氧化铬沉淀b为原料,以cr(oh)3:h2so4:k2so4:h2o摩尔比=2:3:1:18~20的比例进行溶解。按照上述比例在cr(oh)3中分别加入水和浓h2so4,搅拌至溶解,温度控制70~80℃,加入k2so4,搅拌溶解得到硫酸铬钾溶液c。
14.步骤4)硫酸铬钾结晶:步骤3)得到的硫酸铬钾溶液c,静置冷却18~24小时至室温;之后搅拌、静置间歇操作,每次静置时间18~24小时,然后短时间搅拌,转速5~15转/min,其中前四次的搅拌时间均为8
‑
12min,第五次搅拌之前先加入结晶总量0.2%的硫酸铬钾晶种,然后搅拌15
‑
20min,第六次之后的搅拌时间均为15
‑
20min;共持续搅拌、静置间歇操作6~8次,最终得紫红色光亮外观、颗粒均匀细小的硫酸铬钾的晶体沉淀,机械甩干,得硫酸铬钾(kcr(so4)2.12h2o)。
附图说明
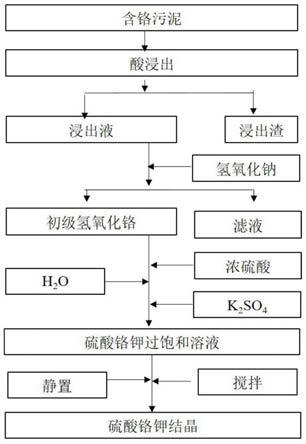
15.图1为本发明的制备工艺示意图。
具体实施方式
实施例1
16.本实施例具体包括以下步骤:
17.步骤1)三价铬离子浸出:将含铬污泥溶于强酸溶液,搅拌反应,溶解的ph值控制在2;过滤,得到含有三价铬离子以及铁、铜、镍等杂质离子的滤液a,使固液分离;
18.步骤2)氢氧化铬沉淀的制备与杂质离子的分离:将步骤1)得到的滤液a稀释至含cr
3+
量2%,缓慢加入naoh溶液直至ph由2.0上升至最终4.0同时搅拌速率10转/min,其中:naoh加入量和速度按照每小时ph上升速率0.3
△
ph/h进行控制,naoh加入时间为约7h,形成氢氧化铬沉淀;洗涤压滤得到易溶于酸的氢氧化铬沉淀b;
19.步骤3)硫酸铬钾溶液的制备:以步骤2)得到的氢氧化铬沉淀b为原料,以cr(oh)3:h2so4:k2so4:h2o摩尔比=2:3:1:19的比例进行溶解。按照上述比例在cr(oh)3中分别加入水和浓h2so4,搅拌至溶解,温度控制75℃,加入k2so4,搅拌得到硫酸铬钾溶液c。
20.步骤4)硫酸铬钾结晶:步骤3)得到的硫酸铬钾溶液c,静置冷却22小时至室温;之后搅拌、静置间歇操作,每次静置时间22小时,然后短时间搅拌,转速10转/min,其中前四次的搅拌时间均为10min,第五次搅拌之前先加入结晶总量0.2%的硫酸铬钾晶种,然后搅拌18min,第六次之后的搅拌时间均为18min;共持续搅拌、静置间歇操作7次,最终得紫红色光亮外观、颗粒均匀细小的硫酸铬钾的晶体沉淀,机械甩干,得硫酸铬钾(kcr(so4)2.12h2o)。
21.本实施例铬的回收率>99%,制备的硫酸铬钾(kcr(so4)2.12h2o)晶体为紫红色光亮外观、颗粒均匀,纯度>99%。对照例1
22.对照例具体包括以下步骤:
23.步骤1)三价铬离子浸出:将含铬污泥溶于强酸溶液,搅拌反应,溶解的ph值控制在2;过滤,得到含有三价铬离子以及铁、铜、镍等杂质离子的滤液a,使固液分离;
24.步骤2)氢氧化铬初级沉淀的制备与杂质离子分离:在步骤1)得到的滤液中,加入20%naoh溶液至ph值4,搅拌反应0.5h,形成氢氧化铬沉淀,洗涤压滤得到氢氧化铬沉淀b。
25.步骤3)硫酸铬钾溶液的制备:以步骤2)得到的氢氧化铬沉淀b为原料,以cr(oh)3:h2so4:k2so4:h2o摩尔比=2:3:1:19的比例进行溶解。按照上述比例在cr(oh)3中分别加入水和浓h2so4,搅拌至溶解,温度控制75℃,加入k2so4,搅拌得到硫酸铬钾溶液c。
26.步骤4)硫酸铬钾结晶:步骤3)得到的硫酸铬钾溶液c,连续静置5天出现少量结晶,第7天出现坨状大块结晶,机械甩干,粉碎后,得紫灰色杂散光泽外观、粉状硫酸铬钾。
27.本对照例铬的回收率~97%,硫酸铬钾纯度>94%,硫酸铬钾结晶为坨状大块晶体(尺寸>10cm),使用前需要由机械粉碎为粉状硫酸铬钾固体颗粒,外观紫灰色杂散光泽,市场接受程度低。对照例2
28.对照例具体包括以下步骤:
29.步骤1)三价铬离子浸出:将含铬污泥溶于强酸溶液,搅拌反应,溶解的ph值控制在2;过滤,得到含有三价铬离子以及铁、铜、镍等杂质离子的滤液a,使固液分离;
30.步骤2)氢氧化铬沉淀的制备与杂质离子的分离:将步骤1)得到的滤液a稀释至含cr
3+
量2%,缓慢加入naoh溶液直至ph由2.0上升至最终4.0同时搅拌速率10转/min,其中:naoh加入量和速度按照每小时ph上升速率0.3
△
ph/h进行控制,naoh加入时间为约7h,形成氢氧化铬沉淀;洗涤压滤得到易溶于酸的氢氧化铬沉淀b;
31.步骤3)硫酸铬钾溶液的制备:以步骤2)得到的氢氧化铬沉淀b为原料,以cr(oh)3:h2so4:k2so4摩尔比=2:3:1的比例进行反应,其中cr(oh)3先溶解于稀h2so4制备硫酸铬溶液,然后加入固体k2so4,制备硫酸铬钾溶液(硫酸铬钾25℃溶解度24.39g/100g水),硫酸铬钾溶液经高温浓缩至213~231g/100g水,得硫酸铬钾溶液c。
32.步骤4)硫酸铬钾结晶:步骤3)得到的硫酸铬钾溶液c,连续静置5天出现少量结晶,第7天出现坨状大块结晶,机械甩干,粉碎后,得紫灰色杂散光泽外观、粉状硫酸铬钾。
33.本对照例铬的回收率~99%,硫酸铬钾纯度~99%,硫酸铬钾结晶为坨状大块晶体(尺寸>10cm),使用前需要由机械粉碎为粉状硫酸铬钾固体颗粒,外观紫灰色杂散光泽,市场接受程度低;与实施例1相比,蒸发浓缩水的能耗至少9倍以上。对照例3
34.对照例具体包括以下步骤:
35.步骤1)三价铬离子浸出:将含铬污泥溶于强酸溶液,搅拌反应,溶解的ph值控制在2;过滤,得到含有三价铬离子以及铁、铜、镍等杂质离子的滤液a,使固液分离;
36.步骤2)氢氧化铬沉淀的制备与杂质离子的分离:将步骤1)得到的滤液a稀释至含cr
3+
量2%,缓慢加入naoh溶液直至ph由2.0上升至最终4.0同时搅拌速率10转/min,其中:naoh加入量和速度按照每小时ph上升速率0.3
△
ph/h进行控制,naoh加入时间为约7h,形成氢氧化铬沉淀;洗涤压滤得到易溶于酸的氢氧化铬沉淀b;
37.步骤3)硫酸铬钾溶液的制备:以步骤2)得到的氢氧化铬沉淀b为原料,以cr(oh)3:
h2so4:k2so4:h2o摩尔比=2:3:1:19的比例进行溶解。按照上述比例在cr(oh)3中分别加入水和浓h2so4,搅拌至溶解,温度控制75℃,加入k2so4,搅拌得到硫酸铬钾溶液c。
38.步骤4)硫酸铬钾结晶:步骤3)得到的硫酸铬钾溶液c,静置冷却22小时至室温;之后搅拌、静置间歇操作,每次静置时间22小时,然后短时间搅拌,转速10转/min,搅拌时间均为10min;共持续搅拌、静置间歇操作10次,未出现硫酸铬钾结晶。
39.本对照例未出现硫酸铬钾结晶。对照例4
40.对照例具体包括以下步骤:
41.步骤1)三价铬离子浸出:将含铬污泥溶于强酸溶液,搅拌反应,溶解的ph值控制在2;过滤,得到含有三价铬离子以及铁、铜、镍等杂质离子的滤液a,使固液分离;
42.步骤2)氢氧化铬沉淀的制备与杂质离子的分离:将步骤1)得到的滤液a稀释至含cr
3+
量2%,缓慢加入naoh溶液直至ph由2.0上升至最终4.0同时搅拌速率10转/min,其中:naoh加入量和速度按照每小时ph上升速率0.3
△
ph/h进行控制,naoh加入时间为约7h,形成氢氧化铬沉淀;洗涤压滤得到易溶于酸的氢氧化铬沉淀b;
43.步骤3)硫酸铬钾溶液的制备:以步骤2)得到的氢氧化铬沉淀b为原料,以cr(oh)3:h2so4:k2so4:h2o摩尔比=2:3:1:19的比例进行溶解。按照上述比例在cr(oh)3中分别加入水和浓h2so4,搅拌至溶解,温度控制75℃,加入k2so4,搅拌得到硫酸铬钾溶液c。
44.步骤4)硫酸铬钾结晶:步骤3)得到的硫酸铬钾溶液c,静置冷却至室温;之后搅拌、静置间歇操作,每次静置时间11小时,然后搅拌11小时,转速10转/min,共持续搅拌与静置12次,未出现硫酸铬钾结晶。
45.本对照例未出现硫酸铬钾结晶。实施例2
46.本实施例具体包括以下步骤:
47.步骤1)三价铬离子浸出:将含铬污泥溶于强酸溶液,搅拌反应,溶解的ph值控制在2;过滤,得到含有三价铬离子以及铁、铜、镍等杂质离子的滤液a,使固液分离;
48.步骤2)氢氧化铬沉淀的制备与杂质离子的分离:将步骤1)得到的滤液a稀释至含cr
3+
量1%,缓慢加入naoh溶液,加入naoh溶液,ph由2.0上升至最终4.0同时搅拌速率10转/min,其中:naoh加入量和速度按照每小时ph上升速率0.25
△
ph/h进行控制,naoh加入时间为8h,形成氢氧化铬沉淀;洗涤压滤得到易溶于酸的氢氧化铬沉淀b;
49.步骤3)硫酸铬钾溶液的制备:以步骤2)得到的氢氧化铬沉淀b为原料,以cr(oh)3:h2so4:k2so4:h2o摩尔比=2:3:1:18的比例进行溶解。按照上述比例在cr(oh)3中分别加入水和浓h2so4,搅拌至溶解,温度控制80℃,加入k2so4,搅拌得到硫酸铬钾溶液c。
50.步骤4)硫酸铬钾结晶:步骤3)得到的硫酸铬钾溶液c,静置冷却18小时至室温;之后搅拌、静置间歇操作,每次静置时间18小时,然后短时间搅拌,转速5转/min,其中前四次的搅拌时间均为8min,第五次搅拌之前先加入结晶总量0.2%的硫酸铬钾晶种,然后搅拌15min,第六次之后的搅拌时间均为15min;共持续搅拌、静置间歇操作6次,最终得紫红色光亮外观、颗粒均匀细小的硫酸铬钾的晶体沉淀,机械甩干,得硫酸铬钾(kcr(so4)2.12h2o)。
51.本实施例铬的回收率>99%,制备的硫酸铬钾(kcr(so4)2.12h2o)晶体为紫红色光亮外观、颗粒均匀,纯度>99%。
实施例3
52.本实施例具体包括以下步骤:
53.本发明涉及一种含铬污泥制备硫酸铬钾的方法,其工艺包括如下步骤:
54.步骤1)三价铬离子浸出:将含铬污泥溶于强酸溶液,搅拌反应,溶解的ph值控制在2;过滤,得到含有三价铬离子以及铁、铜、镍等杂质离子的滤液a,使固液分离;
55.步骤2)氢氧化铬沉淀的制备与杂质离子的分离:将步骤1)得到的滤液a稀释至含cr
3+
量3%,缓慢加入naoh溶液,加入naoh溶液,ph由2.0上升至最终4.0同时搅拌速率10转/min,其中:naoh加入量和速度按照每小时ph上升速率0.40
△
ph/h进行控制,naoh加入时间为5h,形成氢氧化铬沉淀;洗涤压滤得到易溶于酸的氢氧化铬沉淀b;
56.步骤3)硫酸铬钾溶液的制备:以步骤2)得到的氢氧化铬沉淀b为原料,以cr(oh)3:h2so4:k2so4:h2o摩尔比=2:3:1:20的比例进行溶解。按照上述比例在cr(oh)3中分别加入水和浓h2so4,搅拌至溶解,温度控制70℃,加入k2so4,搅拌得到硫酸铬钾溶液c。
57.步骤4)硫酸铬钾结晶:步骤3)得到的硫酸铬钾溶液c,静置冷却24小时至室温;之后搅拌、静置间歇操作,每次静置时间24小时,然后短时间搅拌,转速15转/min,其中前四次的搅拌时间均为12min,第五次搅拌之前先加入结晶总量0.2%的硫酸铬钾晶种,然后搅拌20min,第六次之后的搅拌时间均为20min;共持续搅拌、静置间歇操作8次,最终得紫红色光亮外观、颗粒均匀细小的硫酸铬钾的晶体沉淀,机械甩干,得硫酸铬钾(kcr(so4)2.12h2o)。
58.本实施例铬的回收率>99%,制备的硫酸铬钾(kcr(so4)2.12h2o)晶体为紫红色光亮外观、颗粒均匀,纯度>99%。
59.与现有技术相比,本发明利用提出了在较高温条件下,通过kcr(so4)2.12h2o自带结晶水溶解kcr(so4)2,形成kcr(so4)2.12h2o高浓度过饱和溶液,并利用本发明的结晶程序,形成均匀有序的kcr(so4)2.12h2o结晶颗粒的方法。具体来说,本发明根据kcr(so4)2.12h2o的组成,通过含铬污泥制备的cr(oh)3为原料,以cr(oh)3:h2so4:k2so4:h2o原料摩尔比=2:3:1:18~20在70~80℃高温进行反应,形成kcr(so4)2.12h2o溶液,由于反应体系中仅保留相当于12~13个h2o分子,即比kcr(so4)2.12h2o晶体12个结晶h2o仅多0~1h2o分子,由此构成了室温下的过饱和溶液(相当于溶解213~231g/100g水);之后通过控制结晶程序,获得纯度高、结晶颗粒均匀和紫红色光泽外观的硫酸铬钾;本发明不需要高温浓缩,因而能耗低,并避免了现有技术需由室温下制备溶液(25℃最高浓度24.39g/100g水)然后浓缩脱水耗能程序,且结晶过程无法得到外观紫红色光泽外观、均匀结晶颗粒的问题;本发明同时还避免了采用有毒的六价铬还原制备硫酸铬钾存在的环保问题。
60.本发明针对硫酸铬钾结晶难、而一旦结晶易成坨的问题,设计了过饱和硫酸铬钾溶液,超长时间晶体成核、晶种培养以及晶种生长、多晶控制的结晶工艺。首先通过室温超长时间18~24小时冷却静置,使过饱和溶液均匀分散以利于晶核形成,然后以低速超短时间的搅拌8
‑
12min,便于多晶形成,防止单晶形成;长时间静置、暂短搅拌重复至第五次,引入晶种,促进晶种生长,并通过增加搅拌时间至15
‑
20min,防止结晶不均匀和大晶体出现;最终经历长达约7~10天搅拌、静置操作后,形成紫红色光亮外观、颗粒均匀的硫酸铬钾晶体沉淀。
61.本发明在含铬污泥制备氢氧化铬初级沉淀的过程中,采用较低重金属离子浓度,通过控制沉淀ph始终处于2~4的范围内,并根据每阶段金属离子浓度及反应过程,进一步
控制naoh加入量和速度控制ph的增长变化,实现了全过程碱浓度的有效控制,避免了可能发生的局部ph剧烈变化,现有技术ph变化范围宽泛,特别是反应后期ph变化剧烈,碱浓度与的cr
3+
浓度不匹配,造成颗粒间相互聚集、交联、老化的问题,反应体系反应过程ph始终波动小,反应缓慢温和、晶化时间长,得到的沉淀粒度细、分散均匀、结晶度好、均匀一致、纯度高,易溶于弱酸,为后续硫酸铬钾的制备奠定了良好的基础。现有三价铬的氢氧化物沉淀工艺,尽管也采用了加碱沉淀工艺,但现有技术采用向三价铬盐溶液中直接加入碱沉淀的方法制备氢氧化铬,反应过程碱浓度难以均匀控制,造成颗粒间相互聚集、交联、老化形成难溶于弱酸(如醋酸)的大颗粒氢氧化铬沉淀,并形成cr
3+
与fe
3+
、ni
2+
、cu
2+
的氢氧化物共沉淀;尽管采用低浓度cr
3+
与低浓度碱溶液反应或者将碱液和cr
3+
同时加入水中,有利于降低氢氧化铬沉淀的交联和聚集,但是过低浓度的cr
3+
和碱液需消耗大量水,且仍无法解决反应过程或反应后期,浓度分布不均导致的交联和聚集问题;而采用氨(胺)类沉淀剂,又会产生氨氮污水排放的问题。
1.上述具体实施可由本领域技术人员在不背离本发明原理和宗旨的前提下以不同的方式对其进行局部调整,本发明的保护范围以权利要求书为准且不由上述具体实施所限,在其范围内的各个实现方案均受本发明之约束。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1