宿主DNA作为克罗恩氏病的生物标记物的制作方法
本发明涉及诊断患者患有克罗恩氏病和/或诊断患有克罗恩氏病的患者的疾病状态的新方法。
背景技术:
克罗恩氏病(cd)是一种慢性炎性肠病(ibd),其可能会影响从口腔至肛门胃肠道的任何部位。发病年龄一般在15-30岁之间,均等地流行于女性和男性中。发现欧洲和北美的发病率最高,每100000人中有超过300人(molodecky等人,2012)。cd通常会导致腹痛、严重腹泻和体重紊乱。该疾病的病因未知并且是多因素的:环境因素、宿主遗传学和肠道微生物群都已被证明可以影响疾病的风险及其严重程度(cho,j.h.&brant,s.r.(2011))。
cd的临床诊断由血清学、放射学、内镜检查和组织学检查结果所支持。目前,没有独立的实验室开发的测试允许进行cd诊断。在现有的实验室测试中,血清crp、粪便钙网蛋白和乳铁蛋白是最广泛使用的标记物,但它们不是cd特异性的。可以通过克罗恩氏病的活动性指数(cdai)(一种由多个参数组合得到的分数)或者仅由临床参数组成的harvey-bradshaw指数(hbi),来测量疾病的活动性(laas等人,2014)。
此外,在诊断患有cd的患者中,单独监测临床症状不足以可信地评估疾病活动性。患者自我报告疾病活动性低通常在内窥镜检查期间呈现肠道损伤。生物标记物比如排泄物的钙网蛋白是有用的,但非特异性,并且它们的增加与晚期恶化(flare)发生时的全身/粘膜炎症有关。内窥镜检查能够检测粘膜愈合,这被认为是疾病缓解最强大可靠的征兆;然而,由于需要肠道准备和全身麻醉,常规重复的内窥镜监测是不可行的。新的成像工具,比如mri,已经被证明是有效的,但它昂贵、耗时且使用受限,而排除常规使用。作为最有希望的方法而提出的mr肠动描记法也涉及肠道准备和侵入性结肠镜检查。
因此,鉴于这些疾病的复发性和缓解性(remitting),通过准确的监测和治疗调整,对cd的严格控制是管理这些患者的关键。然而,由于上述原因,目前的诊断方法都不能令人满意。
因此,患者和医疗保健提供者积极寻找可以评估疾病活动性和监测患者护理的非侵入性工具。
更准确地说,仍然需要鉴定cd的标记物,其允许以非侵入性、简单和准确的方式诊断患者的疾病。这正是本发明的主题。
此外,需要鉴定这样的生物标记物,其可以帮助区分患有活跃型cd的患者和患有所述疾病静止期的患者。事实上,这些信息可以帮助临床医师诊断cd的阶段,预测所述变化的发生,以便从不同的治疗方案中进行选择(强化型或常规型),而无需进行内窥镜分析。本发明满足了这一需求。
现有技术中已观察到宿主dna在患者粪便样本中的增加,其中所述患者患有已知引起肠粘膜炎症状态的疾病。
在599名住院患者的前瞻性群体中,每位患者在入院后7天内获得单一直肠拭子。宿主dna比例与肠道微生物群多样性呈负相关。排泄大量人dna的患者富含肠球菌属和大肠埃希氏菌属,而瘤胃球菌属和odoribacter则耗尽。排泄物中人dna的定量可以作为评估肠道炎症的简单且非侵入性方法(vincent等人,2014)。
来自结肠直肠癌患者的粪便样本还含有提高浓度的人dna(klaassen等人2003)。
患有克罗恩氏病的患者粪便样本中宿主dna的量迄今为止从未被评估过。然而,已经观察到来自cd患者的粪便样本也含有提高浓度的人dna。这是非常令人惊讶的,因为cd患者(与溃疡性结肠炎相比)肠道损伤的总面积小,而在克罗恩氏病中排泄物中可见的出血是非常罕见的。
通过定量的宏基因组分析,还通过qpcr,本发明人分析了从健康对照和cd患者收集的一些粪便样本中的人dna丰度。此外,在患有侵袭性克罗恩氏病与所述疾病静止期的患者中获得的粪便样本中评估了宿主dna丰度。
这样做,本发明人观察到,人dna在粪便样本中的存在和量是克罗恩氏病的标记物,同样,正是利用这种的标记物可以区分患有侵袭性克罗恩氏病与所述疾病静止期的患者。
综上所述,他们证明宿主dna在cd患者排泄物中的存在可能被用作cd、其活动性或严重程度的标记物。
附图说明
图1公开了在来自健康和nash对照组(左侧)和克罗恩氏病患者(右侧)的粪便样本中发现的百分比人dna的盒子图(boxplot)。
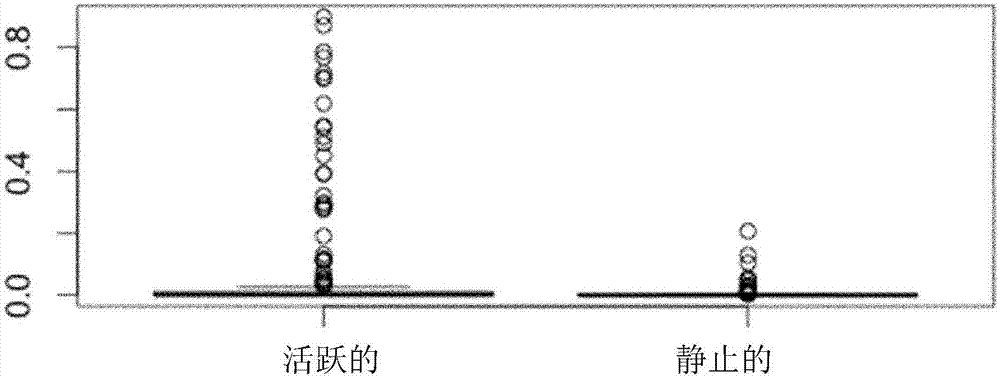
图2公开了在研究的粪便样本中发现的宿主dna的相对丰度水平(以%计),疾病活跃期(左侧)和静止期(右侧)的克罗恩氏病患者。使用钙网蛋白水平和hbi分数的组合分数确定疾病状态(活跃期与静止期)。
图3公开了在研究的粪便样本中发现的人dna百分比与钙网蛋白水平。
图4公开了使用人dna百分比作为cd群体中疾病活动性的预测分数的roc曲线。对于组合分数,auc具有0.67的值。
图5公开了为了测量宿主dna丰度,vp5和vp9的qpcr分析定量数据之间的相关性。
图6公开了vp5qpcr分析定量数据和通过illumina测序测量的人dna相对丰度的百分比之间的相关性。
图7公开了vp9qpcr分析定量数据和通过illumina测序测量的人dna相对丰度的百分比之间的相关性。
图8公开了通过qpcr分析获得的排泄物钙网蛋白的mrna水平(s100a8和s100a9mrna水平的测量)和通过elisa获得的排泄物钙网蛋白的蛋白水平(a:s100a8;b:s100a9)之间的相关性。
技术实现要素:
测量方法,尤其是诊断cd的方法
第一方面,本发明涉及一种用于针对患有或疑似患有克罗恩氏病(cd)的受试者产生定量数据的方法,所述方法包括:在所述受试者的生物样本中进行至少一种分析,以确定宿主dna相对丰度,其中定量数据表示宿主dna相对丰度,优选与参考值相比。
换句话说,本发明涉及一种体外方法,其用于分析来自患有或疑似患有克罗恩氏病(cd)的受试者的生物样本,所述方法包括:
a)从所述受试者获得生物样本,
b)确定所述样本中宿主dna的相对丰度,
以及
c)确定所述相对丰度是否高于参考值。
更准确地说,本发明涉及一种体外诊断受试者中克罗恩氏病(cd)的方法,所述方法包括:
a)从所述受试者获得生物样本,
b)确定所述样本中宿主dna的相对丰度,
以及
c)当所述相对丰度高于参考值时,诊断所述受试者患有克罗恩氏病。
该方法优于现有技术的诊断方法,因为它是非侵入性的、经济上可接受、并具有高度的特异性。
如本文所用,术语“宿主dna”是指肠道微生物群中宿主的dna,其不同于微生物的或病毒的dna。如果待测试的受试者是人患者,则术语“宿主dna”具体指“人dna”。
可以从所述感兴趣的生物样本中提取dna,例如通过使用godonjj等人1997中描述的提取方案。其它方案仍然可以使用并且是众所周知的。值得注意的是,对于随后的分析,微生物dna和宿主dna不需要进行物理分离。
通过任何常规方式,比如检测cpg甲基化或细菌16s核糖体dna,可以将哺乳动物dna与微生物dna区分开。也可以使用qpcr靶向人dna或β球蛋白、β-肌动蛋白和htert基因中的alu(str)重复区(klaassenchw等人,2003;shewalejg等人,journalofforensicscience,2007,vol.52(2))。纳米链(nanostring)技术也是有用的。
可以通过任何公知的方法进行宿主和微生物dna的定量。本领域已知的用于定量样本中dna链的最常用的方法包括northern印迹和原位杂交(parker&barnes,methodsinmolecularbiology106:247-283(1999))、基于pcr的方法,比如定量聚合酶链反应(qpcr)(heid等人,genomeresearch6:986-994(1996))和基于核酸的多重技术,比如多重pcr和dna微阵列。或者,可以使用可识别序列特异性双链体(包括dna双链体或dna-蛋白质双链体)的抗体。用于基于测序的分析的代表性方法包括链终止方法、鸟枪测序方法、从头测序、下一代测序方法(包括大规模并行签名测序(mpss)、polony测序、454焦磷酸测序、illumina(solexa)测序、solid测序、离子半导体测序、dna纳米球测序、helioscope单分子测序、单分子实时(smrt)测序、rnap测序、纳米孔dna测序、杂交测序和微流体sanger测序)。
如以下实施例所示,还可以通过以下从dna库(pool)中测量宿主dna:i)使用高通量测序技术对存在于粪便样本中的dna进行测序,以及ii)通过这些测序技术获得的短读取与人基因组进行比对。在这种情况下,可以通过对绘制(map)到人基因组单一参考序列上的读取进行计数(h),产生剩余读取的数目(b),并通过读取的总数(h+b)对读取h的数目进行归一化,而计算“宿主dna的相对丰度”。
如本文所述,术语“宿主dna丰度”是指所述样本中存在的宿主dna相较于dna总量(包括尤其是细菌和真菌dna)的相对量。在本申请中,因此优选称为宿主dna的“相对丰度”(或“相对量”)。
优选地,利用人特异性核酸片段比如引物和/或探针,通过qpcr测量宿主dna丰度。
如本文所使用的,可互换的术语“核酸”、“核酸序列”、“核苷酸”、“核苷酸序列”是指精确连续的天然核苷酸(例如a、t、g、c和u),其对应于单链或双链dna,比如cdna、基因组dna、核糖体dna或质粒dna、以及所述dna的转录产物,比如rna。根据本发明的核酸可以通过任何已知的方法进行分离和制备,包括但不限于任何合成方法、任何重组方法、任何离体生成方法等、及其组合。
在宿主dna中进行qpcr所需或有用的探针和引物在本发明的上下文中被称为“核酸片段”。
通过“核酸片段”,本文中更通常地指与感兴趣的核酸杂交的核酸。例如,这样的核酸片段长度可以是至少10个核苷酸,或者优选长度至少为15个核苷酸。它们也可以是至少25个或至少50个核苷酸长度。
根据本发明的核酸片段对宿主dna是特异性的,优选对人宿主dna,因为它们允许将存在于生物样本中的宿主dna和其它dna(即非宿主dna)区分开,其中所述其它dna比如真菌和/或细菌dna(即微生物dna)。换句话说,本发明的核酸片段将与宿主dna杂交,但不会(或基本上不)结合存在于生物样本中大部分其它dna(即非宿主dna),比如真菌和/或细菌dna(即微生物dna)。
在本发明的上下文中,核酸片段优选在严格杂交条件下与宿主dna杂交。严格杂交条件的一个实例是,在约50℃至约65℃,更优选约55℃至约65℃的温度下,使用例如约0.9摩尔的盐溶液进行尝试杂交。然而,技术人员将能够改变这样的条件,以便考虑比如核酸片段长度、碱基组成、存在的离子类型等变量。
“引物”更具体地指,用作感兴趣的核酸(即本文的宿主dna)扩增起始点的核酸片段。本发明的核引物的实例包括但不限于序列seqidno:1、seqidno:2、seqidno:4和seqidno:5的引物。这种引物可按照“引物组”的形式而使用以扩增宿主dna。本发明引物组的实例包括但不限于引物组(seqidno:1、seqidno:2)和(seqidno:4、seqidno:5)。
“探针”更具体地指,可用于检测感兴趣的核酸的核酸片段,即本文中的宿主dna。该术语包括各种衍生形式,例如“荧光探针”。当与如上定义的引物组组合使用时,所述探针可用于定量感兴趣的核酸。本发明的探针的实例包括但不限于序列seqidno:3和seqidno:6的探针。探针可以被同位素、放射性标记、比如生物素的结合部分、比如地高辛的半抗原、发光的、质量标签、磷光或荧光部分、或单独的荧光染料(例如,mgb、fam、vic、tet、ned、tamra、joe、hex、rox等)或与其它染料组合进行标记。这些标记提供可通过荧光、放射性、比色法、重量分析、x射线衍射或吸收、磁性、酶活性、质谱、结合亲和力等可检测的信号,并且便于检测或定量感兴趣的核酸。
在本发明的优选实施方案中,使用至少一种选自序列seqidno:1至seqidno:6的核酸片段、其变体及其互补序列的核酸片段,通过定量pcr(qpcr)测量宿主dna丰度。
更优选地,使用与序列seqidno:3的探针组合的引物组(seqidno:1、seqidno:2)和/或使用与序列seqidno:6的探针组合的引物组(seqidno:4、seqidno:5),通过定量pcr(qpcr)来测量宿主dna丰度。
术语“互补”是指,例如,第一核酸序列的每个核苷酸与方向相反的第二核酸序列的互补碱基配对。互补核苷酸是a和t(或a和u)或c和g。
根据本发明的核酸片段的“变体”包括但不限于与所述核酸片段比对之后具有至少99%同一性、并且保留其与感兴趣的核酸(此处为宿主dna)杂交的能力的核酸序列。变体的实例是简并核酸片段。
本发明的方法可以应用于任何受试者,无论是人还是动物。然而,在优选的实施方案中,它适用于人患者,尤其是疑似患有cd的人,或需要确认患有cd的人。更准确地说,本发明的方法适用于监测显示出增强水平的炎症标记物的人患者,其中所述炎症标记物比如血小板计数、平均血小板体积、红细胞沉降率(esr)、血清血小板生成素、血清促红细胞生成素、c-反应性蛋白和血清类黏蛋白(α1酸性糖蛋白)、tnfα、白细胞介素(特别是il1、il2、il6、il8、il10、il15)以及排泄物的炎症标记物,如乳铁蛋白和钙网蛋白。诊断cd的精确方法详见laas等人,2014,其通过引用并入本文。更优选地,受试者不患有以下病理中的至少一种:癌症或癌前病变,特别是结肠癌、结肠直肠癌或结肠直肠腺瘤、溃疡性结肠炎、微小结肠炎(比如胶原性结肠炎或淋巴细胞性结肠炎)、缺血性结肠炎、改道性结肠炎(diversioncolitis)、过敏性结肠炎、白塞病、结肠直肠息肉、乳糜泻、肠易激综合征(ibs)及其任何组合。
在优选的实施方案中,发明方法的步骤a)中使用的生物样本是粪便样本。事实上,这样的样本可以通过来自患者完全无害的收集来获得。优选地,收集所述粪便样本并存储在适当的缓冲液中,所述缓冲液不变性或影响其中所含的dna(在该目的中,可以使用例如rna
如本文所用,术语“参考值”是指可用于鉴定已知宿主dna较少(poor)的样本的特定值或数据集。例如从健康受试者获得的历史丰度数据中获得该参考值。它可以是单截止值,比如中位数或平均值。它可以是单个数字,等同地适用于每个样本。在优选的实施方案中,该参考值是预先确定的值。通常,这个预先确定的值是约1%。
原则上,健康受试者的粪便样本没有宿主dna。因此,受试者的粪便样本中宿主dna的存在暗示着所述受试者可能患有肠道相关疾病。本发明还包括涉及检测粪便样本中宿主dna的存在的旨在诊断受试者中cd的所有方法。换句话说,涉及使用宿主dna作为cd标记物的任何诊断方法都包含在本发明内。
在本发明的背景下,当比参考值高(优选10倍,更优选高20倍)时,这意味着待测试的受试者的宿主dna的相对丰度“高于参考值”。在优选的实施方案中,当上面定义的宿主dna的相对丰度高于1%,优选高于10%,更优选高于20%时,可以得出结论待测试的受试者患有cd。
其它方面,宿主dna的量与参考值进行比较。所述比较可以由本领域技术人员使用统计方法进行,特别是可以使用roc曲线来确定灵敏度和特异性的最佳截止值。
在具体实施方案中,本发明的方法包括:在患有或疑似患有克罗恩氏病(cd)的受试者的粪便样本中进行至少一种分析,以确定宿主dna相对丰度,其中定量数据代表宿主dna相对丰度,优选和约1%的参考值进行比较。
换句话说,本发明涉及一种用于体外分析来自患有或疑似患有克罗恩氏病(cd)的受试者的生物样本的方法,所述方法包括:
a)从所述受试者获得粪便样本,
b)确定所述样本中宿主dna的相对丰度,
以及
c)确定所述相对丰度是否高于约1%的参考值。
更具体而言,在具体的实施方案中,本发明的方法包括以下步骤:
a)从人患者获得粪便样本,
b)通过任何以上公开的常规方法确定所述样本中人dna的相对丰度,
以及
c)当所述相对丰度高于约1%时,诊断所述患者患有克罗恩氏病。
测量方法,尤其是监测cd状态的方法
另一方面,本发明涉及一种针对患有或疑似患有不稳定状态的克罗恩氏病(cd)的受试者而产生定量数据的方法,所述方法包括:进行至少一种分析以确定所述受试者的生物样本中宿主dna相对丰度,其中定量数据表示宿主dna相对丰度,优选与参考值进行比较。
换句话说,本发明涉及一种体外分析来自患有或疑似患有不稳定状态的克罗恩氏病的受试者的生物样本的方法,所述方法包括步骤:
a)从所述受试者获得生物样本,
b)确定所述样本中宿主dna的相对丰度,
以及
c)确定所述相对丰度是否高于参考值。
在优选的实施方案中,所述参考值为约10%。
本发明还涉及一种针对患有或疑似患有不稳定状态的克罗恩氏病(cd)的受试者而产生定量数据的方法,所述方法包括:进行至少一种分析以确定所述受试者的生物样本中宿主dna相对丰度,其中定量数据表示宿主dna相对丰度,优选与第一参考值和第二参考值进行比较。
在优选的实施方案中,所述第一参考值为约10%,所述第二参考值为约1%。
换句话说,本发明涉及一种用于体外分析来自患有或疑似患有不稳定状态的克罗恩氏病的受试者的生物样本的方法,所述方法包括步骤:
a)从所述受试者获得生物样本,
b)确定所述样本中宿主dna的相对丰度,
以及
c)确定所述相对丰度是否低于第一参考值并高于第二参考值。
在优选的实施方案中,所述第一参考值为约10%,所述第二参考值为约1%。
更具体地,本发明人获得的结果允许鉴定生物标记物(宿主dna),所述生物标记物特别是以非侵入性方式区分患有非活跃(静止状态)克罗恩氏病的患者和患有侵袭性克罗恩氏病(紧急恶化期有关的状态)的患者。因此,其结果是监测疾病阶段的特定值。
在本发明的上下文中,“稳定”患者被定义为在几周内其疾病活动性稳定的cd患者(患者处于“稳定状态”)。而“不稳定”的患者(或患者“处于不稳定状态”)是在接下来的几周内改变或加强其治疗的cd患者,其血液检查显示在接下来的几周内有升高的活动性,和/或其自我评价显示连续样本中健康下降和/或钙网蛋白水平已经升高,和/或具有全身性粘膜炎症,更特别是全身性粘膜溃疡。也可以根据结肠镜分数比如cdeis或ses-cd来定义稳定或不稳定。
因此,本发明更具体地针对一种旨在诊断患有cd的受试者中这两种特定状态的方法。
更准确地说,本发明涉及一种体外诊断受试者中克罗恩氏病活动性的方法,所述方法包括步骤:
a)从所述受试者获得生物样本,
b)确定所述样本中宿主dna的相对丰度,
以及
c)当所述相对丰度高于参考值时,诊断所述受试者患有不稳定状态的克罗恩氏病。
上述方法优于现有技术,因为它们是非侵入性的、经济上可接受的、并且具有高特异性。
上述所有实施方案,特别是本发明的诊断方法,也适用于本方法,特别是用于监测克罗恩氏病的活动性。
特别地,所述受试者可以是疑似患有cd、或需要确认患有cd或已被诊断患有cd的人患者。更准确地说,本发明的方法适用于监测显示增强水平的炎症标记物的人患者,其中所述炎症标记物比如血小板计数、平均血小板体积、红细胞沉降率(esr)、血清血小板生成素、血清促红细胞生成素、c-反应性蛋白和血清类黏蛋白(α1酸性糖蛋白)、tnfα、白细胞介素(特别是il1、il2、il6、il8、il10、il15)以及排泄物的炎症标记物,如乳铁蛋白和钙网蛋白。诊断cd的精确方法详见laas等人,2014,其通过引用并入本文。
此外,生物样本优选为粪便样本,更优选如上所述处理。
在优选的实施方案中,如上所述,确定宿主dna的相对丰度。
当确定宿主dna的相对丰度,并直接或间接地和参考值比较时,本发明人发现本发明的这些方法是高度敏感和特异性的。
如本文所使用的,术语“参考值”是指可用于鉴定具有稳定cd的样本的特定值或数据集。例如,从已经毫无疑义地被诊断为稳定cd的患者或者患者库获得的历史丰度数据中获得该参考值。例如,通过测量处于cd稳定状态的患者粪便样本中宿主dna的相对丰度而获得该参考值。它可以是单截止值,比如中位数或平均值。它可以是单个数字,等同地适用于每个样本。所述参考值也是预先确定的值。通常,这个预先确定的值是约10%。
在优选的实施方案中,如上所限定的,当宿主dna的相对丰度高于10%,优选高于18%,更优选高于20%时,可以得出结论待测试的患者患有不稳定的cd。
在一个具体实施方案中,本发明的方法包括:在患有或疑似患有不稳定状态克罗恩氏病的受试者的粪便样本中进行至少一种分析以确定宿主dna相对丰度,其中定量数据表示宿主dna相对丰度,优选与约10%的参考值进行比较。
换句话说,本发明涉及一种用于体外分析患有或疑似患有不稳定状态克罗恩氏病的受试者中生物样本的方法,所有方法包括步骤:
a)从所述受试者获得粪便样本,
b)确定所述样本中宿主dna的相对丰度,
以及
c)确定所述相对丰度是否高于约10%的参考值。
更确切地说,在这个具体的实施方案中,本发明的体外诊断方法能够诊断人患者中的克罗恩氏病的不稳定状态,包括以下步骤:
a)通过任何上述方法测量所述患者粪便样本中人dna的相对丰度,
以及
b)当所述相对丰度高于10%时,确定所述患者患有不稳定cd。
相反,本发明还允许针对患有或疑似患有不稳定状态的克罗恩氏病(cd)的受试者而产生定量数据,或换句话说,分析来自所述受试者的生物样本,特别是用于诊断稳定的cd。在这种情况下,当所述受试者的生物样本中测量的宿主dna的相对丰度高于用于诊断cd的参考值(通常为1%)但是低于用于诊断疾病不稳定状态的参考值(通常为10%)时,可以得出结论受试者患有稳定的cd。
如上所述,本发明的方法可以包括(或排除)这样的步骤,其由获得粪便样本并从所述样本提取核酸分子组成。
原则上,静止(非活动性)cd的受试者粪便样本具有0至10%之内的宿主dna相对丰度(例如,取决于测量技术)。然而,受试者的粪便样本中存在中间水平的宿主dna(通常在1%至10%之间)提示所述受试者可能患有cd,并且所述cd处于静止状态。此外,受试者的粪便样本中存在高水平的宿主dna(通常超过10%)提示所述受试者可能患有cd,并且所述cd处于活跃状态。因此,本发明涵盖旨在诊断受试者中cd状态的的涉及在粪便样本中检测宿主dna存在的所有方法。换句话说,涉及使用宿主dna作为cd状态的标记物的任何诊断方法都包含在本发明内。
测量方法,尤其是用于设计治疗的方法
在另一个实施方案中,本发明的诊断方法可用于针对患有克罗恩氏病的受试者调整治疗。
在这个实施方案中,本发明的方法因此包括针对待诊断的受试者而设计治疗的附加步骤,所述治疗经调整以适应(比如通过本发明的方法)经诊断的cd的特定状态。
因此,根据这一方面,本发明涉及一种治疗患有克罗恩氏病的受试者的方法,包括:
i)根据上述方法,针对患有或疑似患有不稳定或稳定状态的克罗恩氏病(cd)的受试者而产生定量数据,
以及
ii)用适当的治疗来对所述受试者进行治疗,所述适当的治疗选自执业医生所通常决定的(attributed)那些治疗。
换句话说,本发明涉及一种治疗患有克罗恩氏病的受试者的方法,包括:
i)根据上述方法,对患有或疑似患有不稳定或稳定状态的克罗恩氏病的受试者的生物样本进行分析,
以及
ii)用适当的治疗来对所述受试者进行治疗,所述适当的治疗选自执业医生所通常决定的那些治疗。
更优选,本发明包括用于治疗患有克罗恩氏病的受试者的方法,所述方法包括以下步骤:
i)根据上述方法诊断受试者中cd的活动性,
以及
ii)当诊断所述cd的状态后,用适当的治疗来对所述受试者进行治疗,所述适当的治疗选自执业医生所通常决定的那些治疗。
例如,当cd患者被诊断为不稳定状态时,则适应的治疗可以是选自以下的药理学治疗:硫唑嘌呤、美沙拉嗪、阿巴他汀、阿达木单抗、阿那白滞素、赛妥珠单抗、依那西普、戈立木单抗、英夫利昔单抗、利妥昔单抗、托珠单抗、那他珠单抗、皮质类固醇、环孢菌素、氨甲蝶呤、他克莫司、抗jak(托法替尼)、抗整联蛋白(vedolizu单抗、rhumabbeta7、madcam-1拮抗剂)或抗il12/il23(优特克单抗、abt874)。
或者,当克罗恩氏病患者被诊断为稳定状态时,适应的治疗将是生活方式干预,例如不同热量限制强度和大量营养素组成(低碳水化合物、低脂肪、饱和脂肪饮食)的饮食。
此外,可以使用本发明的方法用于测试患有cd的受试者的治疗效果,特别是处于不稳定状态的cd,或评估患者对治疗的反应。
在本实施方案中,本发明的方法包括以下步骤:
i)根据上述方法,在施用治疗前后,针对患有或疑似患有不稳定状态克罗恩氏病(cd)的受试者而产生定量数据,
以及
ii)当施用治疗前的状态不稳定,但施用治疗后变得稳定时,得出治疗对所述受试者有效的结论。
换句话说,本发明的方法包括:
i)根据上述方法,在施用治疗前后,对患有或疑似患有不稳定状态的克罗恩氏病的受试者生物样本进行分析,
以及
ii)当施用治疗前的状态不稳定,但施用治疗后变得稳定时,得出治疗对所述受试者有效的结论。
更准确地说,本发明的方法包括:
i)根据上述方法,在施用治疗前后,诊断cd的活动性,
以及
ii)当施用治疗前的状态不稳定,但施用治疗后变得稳定时,得出治疗对所述受试者有效的结论。
当克罗恩氏病患者在施用治疗前被诊断为“不稳定”,并且施用治疗后变得“稳定”时,则所述患者对所述治疗有响应。因此,优选维持有效的治疗。
相反,当克罗恩氏病患者在施用治疗前被诊断为“不稳定”,并且施用治疗后维持“不稳定”时,则所述患者对所述治疗不响应,最好将所述治疗替换成另一种治疗或将其与另一种治疗相结合。
值得注意的是,当克罗恩氏病患者在施用治疗前被诊断为“稳定”时,不值得施用任何化学治疗,因为生活方式干预就足够了。
组合的测量方法,尤其是用于诊断
本发明人进一步提出,将宿主dna丰度的测量与通常用于诊断cd和/或cd状态(即,活跃型与静止状态)的另一标记物的测量进行组合。
在一个具体实施方案中,本发明因此涉及一种针对患有或疑似患有克罗恩氏病(cd)的受试者而产生定量数据的方法,所述方法包括:
a)在所述受试者的生物样本中进行至少一种分析,以确定宿主dna的相对丰度,其中第一定量数据表示宿主dna的相对丰度,优选和参考值进行比较;以及
b)在所述受试者的另一生物样本中进行至少一种分析,以确定钙网蛋白水平或组合临床分数,其中第二定量数据表示所述钙网蛋白水平,优选与150μg/ml进行比较,或所述组合临床分数优选与预先确定的分数进行比较。
换句话说,本发明涉及一种分析患有或疑似患有克罗恩氏病(cd)的受试者生物样本的方法,所述方法包括:
a)从所述受试者获得生物样本,
b)确定所述样本中宿主dna的相对丰度,
c)在所述受试者的另一生物样本中确定钙网蛋白水平或组合临床分数,
以及
d)确定所述相对丰度是否高于参考值、和所述钙网蛋白水平是否高于150μg/ml或所述组合临床分数是否高于预先确定的分数。
更确切地说,本发明涉及一种用于诊断受试者中克罗恩氏病(cd)的方法,包括:
a)从所述受试者获得生物样本,
b)确定所述样本中宿主dna的相对丰度,
c)在所述受试者的另一生物样本中确定钙网蛋白水平或组合临床分数,
以及
d)当所述相对丰度高于参考值时,以及当所述钙网蛋白水平高于150μg/ml时或者所述组合临床分数高于预先确定的分数时,诊断所述受试者患有克罗恩氏病。
在优选的实施方案中,所述参考值为约1%。
本领域技术人员将很容易理解,以μg/ml(或以μg/g)表示的钙网蛋白水平是指钙网蛋白的蛋白水平,或换句话说是指钙网蛋白的蛋白表达水平。蛋白表达水平可以通过本领域众所周知的任何方法进行评估,特别是由reeves等人(2000)和schena(2005)综述的。这些方法通常涉及使感兴趣的生物学样本与一种或多种可检测的试剂接触,所述试剂适合于测量蛋白表达水平,比如抗体,并且随后基于所检测的试剂的水平确定蛋白的表达水平,优选在归一化之后。通常涉及使用抗体的方法的实例包括但不限于western印迹、免疫印迹、酶联免疫吸附分析(elisa)、酶联免疫斑点(elispot)、放射免疫分析(ria)、免疫组织化学和免疫沉淀。不一定涉及使用抗体的、适合于测量蛋白表达水平的其它方法也可以使用,包括但不限于荧光激活细胞分选(facs)、显微镜比如原子力显微镜、流式细胞术、微细胞计数、蛋白结合分析、配体结合分析、微阵列、聚丙烯酰胺凝胶电泳比如sds-page、表面等离子共振(spr)、
在另一个优选实施方案中,宿主dna相对丰度和钙网蛋白水平可以在受试者的同一生物样本中进行测量。
因此,本发明还涉及一种用于针对患有或疑似患有克罗恩氏病(cd)的受试者产生定量数据的方法,所述方法包括:
a)在所述受试者的生物样本中进行至少一种分析,以确定宿主dna的相对丰度,其中第一定量数据表示宿主dna的相对丰度,优选和参考值进行比较;以及
b)在所述样本中进行至少一种分析,以确定钙网蛋白水平或组合临床分数,其中第二定量数据表示所述钙网蛋白水平,优选与150μg/ml进行比较,或所述组合临床分数优选与预先确定的分数进行比较。
换句话说,本发明涉及一种分析患有或疑似患有克罗恩氏病(cd)的受试者生物样本的方法,所述方法包括:
a)从所述受试者获得生物样本,
b)确定所述样本中宿主dna的相对丰度,
c)在所述样本中确定钙网蛋白水平或组合临床分数,
以及
d)确定所述相对丰度是否高于参考值、和所述钙网蛋白水平是否高于150μg/ml或所述组合临床分数是否高于预先确定的分数。
更确切地说,本发明涉及一种用于诊断受试者中克罗恩氏病(cd)的方法,包括:
a)从所述受试者获得生物样本,
b)确定所述样本中宿主dna的相对丰度,
c)在所述样本中确定钙网蛋白水平或组合临床分数,
以及
d)当所述相对丰度高于参考值时,以及当所述钙网蛋白水平高于150μg/ml时或者所述组合临床分数高于预先确定的分数时,诊断所述受试者患有克罗恩氏病。
在优选的实施方案中,所述参考值为约1%。
在优选的实施方案中,在待测试的受试者的粪便样本中测量钙网蛋白。在更优选的实施方案中,如上所述,在相同的粪便样本中进行宿主dna和钙网蛋白检测。然而,这可能需要进行两种单独类型的检测,一种用于测量宿主dna相对丰度(例如通过qpcr),以及一种用于测量钙网蛋白的蛋白水平(例如通过elisa)。
因此,另一方面,本发明提出了测量钙网蛋白的基因水平,从而可以在本发明的方法中进行单一类型的检测。更优选地,这样的检测在相同的容器中进行,甚至更优选在相同的生物样本比如粪便样本中进行。
在这方面,即使这些类型的功能实体(即由所述基因编码的基因和蛋白)的行为不能彼此预测,本发明人出乎意料地发现钙网蛋白的蛋白和基因水平彼此相关。实际上,本领域众所周知的是,蛋白一经转录,其表达水平仍然可以在翻译水平上被调节,并且相应的蛋白可以进行翻译后修饰,而改变半衰期和区域划分。
因此,根据这方面,本发明涉及一种针对患有或疑似患有克罗恩氏病(cd)的受试者产生定量数据的方法,所述方法包括:
a)在所述受试者的生物样本中进行至少一种分析,以确定宿主dna的相对丰度,其中第一定量数据表示宿主dna的相对丰度,优选和第一参考值进行比较;以及
b)在所述样本(优选此处的)或所述受试者的另一生物样本中进行至少一种分析,以确定钙网蛋白基因水平或组合临床分数,其中第二定量数据表示所述钙网蛋白基因水平,优选与第二参考值进行比较,或所述组合临床分数优选与预先确定的分数进行比较。
换句话说,本发明涉及一种分析患有或疑似患有克罗恩氏病(cd)的受试者生物样本的方法,所述方法包括:
a)从所述受试者获得生物样本,
b)确定所述样本中宿主dna的相对丰度,
c)在所述样本(优选此处的)或所述受试者的另一生物样本中确定钙网蛋白基因水平或组合临床分数,
以及
d)确定所述相对丰度是否高于第一参考值,以及所述钙网蛋白基因水平是否高于第二参考值或所述组合临床分数是否高于预先确定的分数。
更确切地说,本发明涉及一种用于诊断受试者中克罗恩氏病(cd)的方法,包括:
a)从所述受试者获得生物样本,
b)确定所述样本中宿主dna的相对丰度,
c)在所述样本(优选此处的)或所述受试者的另一生物样本中确定钙网蛋白基因水平或组合临床分数,
以及
d)当所述相对丰度高于第一参考值时,以及当所述钙网蛋白水平高于第二参考值时或者所述组合临床分数高于预先确定的分数时,诊断所述受试者患有克罗恩氏病。
在优选的实施方案中,关于宿主dna的所述第一参考值如上所定义,更优选为约1%。
基因水平或基因表达水平可以通过本领域熟知的任何方法测量,比如上述用于测量宿主和微生物dna的那些。编码钙网蛋白的基因在本领域是众所周知的。特别地,已知人钙网蛋白形成由s100钙结合蛋白a8(s100a8,也称为钙粒蛋白a)和s100钙结合蛋白a9(s100a9,也称为钙粒蛋白b或迁移抑制因子相关蛋白14(mrp14))组成的异二聚体。以genbank登录号cr407674,版本号:cr407674.1可获得人s100a8基因的核苷酸序列,而以ncbi参考序列登录号nm_002965,版本号:nm_002965.3可获得人s100a9基因之一。
在优选的实施方案中,第二参考值是一个特定的值或数据集,其可用于鉴定已知属于健康受试者的样本(即未患有克罗恩氏病)。因此,所述参考值可以由本领域技术人员容易地确定。它可以是一个单一的截止值,比如中位数或平均值。它可以是单个数字,等同地适用于每个样本。在优选的实施方案中,该参考是预先确定的值。因此,本文“高于第二参考值”表示钙网蛋白基因水平超过所述参考值。
用于测量宿主dna相对丰度和/或钙网蛋白基因水平的特别优选的技术是qpcr,使用例如特异于编码钙网蛋白的基因的核酸片段(比如引物和/或探针)。
“组合临床分数”,这里是指这样的任何分数,其将生物学参数与临床参数结合以产生与cd中的疾病严重程度或粘膜治愈相关的分数。它可以是例如钙网蛋白水平(在患有cd的患者中通常高于150μg/ml)、hbi(通常在患有cd的患者中高于4)、性别、年龄、疾病持续时间、血小板计数、白蛋白、血小板、crp、直肠出血的组合(摘要op05,第七届ecco大会)。
“预先确定的分数”,这里是指通过任何统计或算法方法将这些多重参数组合而产生的值。例如,钙网蛋白为150μg/ml,hbi为4。
另一方面,本发明涉及一种针对患有或疑似患有不稳定状态克罗恩氏病的受试者产生定量数据的方法,所述方法包括:
a)在所述受试者的生物样本中进行至少一种分析,以确定宿主dna的相对丰度,其中第一定量数据表示宿主dna的相对丰度,优选和参考值进行比较;以及
b)在所述受试者的另一生物样本中进行至少一种分析,以确定钙网蛋白水平或组合临床分数,其中第二定量数据表示所述钙网蛋白水平,优选与150μg/ml或250μg/g进行比较,或所述组合临床分数优选与预先确定的分数进行比较。
换句话说,本发明涉及一种体外分析患有或疑似患有不稳定状态的克罗恩氏病(cd)的受试者生物样本的方法,所述方法包括步骤:
a)从所述受试者获得生物样本,
b)确定所述样本中宿主dna的相对丰度,
c)在所述受试者的另一生物样本中确定钙网蛋白水平或组合临床分数,
以及
d)确定所述相对丰度是否高于参考值,以及所述钙网蛋白水平是否高于150μg/ml或250μg/g或所述组合临床分数是否高于预先确定的分数。
更准确地说,本发明涉及用于体外诊断受试者中克罗恩氏病活动性的方法,包括步骤:
a)从所述受试者获得生物样本,
b)确定所述样本中宿主dna的相对丰度,
c)在所述受试者的另一生物样本中确定钙网蛋白水平或组合临床分数,
以及
d)当所述相对丰度大于参考值时,并且当所述钙网蛋白水平大于150μg/ml或250μg/g时或者所述组合临床分数高于预先确定的分数时,诊断所述受试者患有不稳定状态的克罗恩氏病。
在优选的实施方案中,所述参考值为约10%。
在另一个优选实施方案中,可以在受试者的相同生物样本中测量宿主dna相对丰度和钙网蛋白水平。
因此,本发明还涉及一种针对患有或疑似患有不稳定状态的克罗恩氏病的受试者而产生定量数据的方法,所述方法包括:
a)在所述受试者的生物样本中进行至少一种分析,以确定宿主dna的相对丰度,其中第一定量数据表示宿主dna的相对丰度,优选和参考值进行比较;以及
b)在所述样本中进行至少一种分析,以确定钙网蛋白水平或组合临床分数,其中第二定量数据表示所述钙网蛋白水平,优选与150μg/ml或250μg/g进行比较,或所述组合临床分数优选与预先确定的分数进行比较。
换句话说,本发明涉及一种分析患有或疑似患有不稳定状态的克罗恩氏病的受试者生物样本的方法,所述方法包括步骤:
a)从所述受试者获得生物样本,
b)确定所述样本中宿主dna的相对丰度,
c)在所述样本中确定钙网蛋白水平或组合临床分数,
以及
d)确定所述相对丰度是否高于参考值,以及所述钙网蛋白水平是否高于150μg/ml或250μg/g或所述组合临床分数是否高于预先确定的分数。
更准确地说,本发明涉及用于体外诊断受试者中克罗恩氏病活动性的方法,包括步骤:
a)从所述受试者获得生物样本,
b)确定所述样本中宿主dna的相对丰度,
c)在所述样本中确定钙网蛋白水平或组合临床分数,
以及
d)当所述相对丰度大于参考值时,并且当所述钙网蛋白水平大于150μg/ml或250μg/g时或者所述组合临床分数高于预先确定的分数时,诊断所述受试者患有不稳定状态的克罗恩氏病。
在优选的实施方案中,所述参考值为约10%。
在优选的实施方案中,在待测试的受试者的粪便样本中测量钙网蛋白。在更优选的实施方案中,如上所述,在相同的粪便样本中进行宿主dna和钙网蛋白检测。然而,这可能需要进行两种单独类型的检测,一种用于测量宿主dna相对丰度(例如通过qpcr),以及一种用于测量钙网蛋白的蛋白水平(例如通过elisa)。
因此,另一方面,本发明提出了测量钙网蛋白的基因水平,从而可以在本发明的方法中进行单一类型的检测。更优选地,这样的检测在相同的容器中进行,甚至更优选在相同的生物样本比如粪便样本中进行。
因此,根据此方面,本发明涉及一种针对患有或疑似患有不稳定状态克罗恩氏病的受试者产生定量数据的方法,所述方法包括:
a)在所述受试者的生物样本中进行至少一种分析,以确定宿主dna的相对丰度,其中第一定量数据表示宿主dna的相对丰度,优选和第一参考值进行比较;以及
b)在所述样本(优选此处的)或所述受试者的另一生物样本中进行至少一种分析,以确定钙网蛋白基因水平或组合临床分数,其中第二定量数据表示所述钙网蛋白基因水平,优选与第二参考值进行比较,或所述组合临床分数优选与预先确定的分数进行比较。
换句话说,本发明涉及一种分析患有或疑似患有不稳定状态的克罗恩氏病(cd)的受试者生物样本的方法,所述方法包括:
a)从所述受试者获得生物样本,
b)确定所述样本中宿主dna的相对丰度,
c)在所述样本(优选此处的)或所述受试者的另一生物样本中确定钙网蛋白基因水平或组合临床分数,
以及
d)确定所述相对丰度是否高于第一参考值,以及所述钙网蛋白基因水平是否高于第二参考值或所述组合临床分数是否高于预先确定的分数。
更确切地说,本发明涉及一种用于诊断受试者中不稳定状态的克罗恩氏病(cd)的方法,包括:
a)从所述受试者获得生物样本,
b)确定所述样本中宿主dna的相对丰度,
c)在所述样本(优选此处的)或所述受试者的另一生物样本中确定钙网蛋白基因水平或组合临床分数,
以及
d)当所述相对丰度高于第一参考值时,以及当所述钙网蛋白水平高于第二参考值时或者所述组合临床分数高于预先确定的分数时,诊断所述受试者患有不稳定状态的克罗恩氏病。
在优选的实施方案中,关于宿主dna的所述第一参考值如上所定义,更优选为约10%;以及关于钙网蛋白的所述第二参考值优选是患有静止型克罗恩氏病(即,患有稳定状态的克罗恩氏病)的受试者中观察到的钙网蛋白基因水平。
“组合临床分数”,这里是指这样的任何分数,其将生物学参数与临床参数结合以产生与cd中的疾病严重程度或粘膜治愈相关的分数。它可以是例如钙网蛋白水平、hbi、性别、年龄、疾病持续时间、血小板计数、白蛋白、血小板、crp、直肠出血的组合(摘要op05,第七届ecco大会)。
“预先确定的分数”,这里是指通过任何统计或算法方法将这些多重参数组合而产生的值(参见例如,摘要op05,第七届ecco大会中提及的参数和值)。
另一方面,本发明涉及一种针对患有或疑似患有稳定状态克罗恩氏病的受试者产生定量数据的方法,所述方法包括:
a)在所述受试者的生物样本中进行至少一种分析,以确定宿主dna的相对丰度,其中第一定量数据表示宿主dna的相对丰度,优选和参考值进行比较;以及
b)在所述受试者的另一生物样本中进行至少一种分析,以确定钙网蛋白水平或组合临床分数,其中第二定量数据表示所述钙网蛋白水平,优选与150μg/ml或250μg/g进行比较,或所述组合临床分数优选与预先确定的分数进行比较。
换句话说,本发明涉及一种体外分析患有或疑似患有稳定状态的克罗恩氏病的受试者生物样本的方法,所述方法包括步骤:
a)从所述受试者获得生物样本,
b)确定所述样本中宿主dna的相对丰度,
c)在所述受试者的另一生物样本中确定钙网蛋白水平或组合临床分数,
以及
d)确定所述相对丰度是否高于参考值,以及所述钙网蛋白水平是否低于150μg/ml或250μg/g或所述组合临床分数是否低于预先确定的分数。
更准确地说,本发明涉及用于体外诊断受试者中克罗恩氏病活动性的方法,包括步骤:
a)从所述受试者获得生物样本,
b)确定所述样本中宿主dna的相对丰度,
c)在所述受试者的另一生物样本中确定钙网蛋白水平或组合临床分数,
以及
d)当所述相对丰度大于参考值时,并且当所述钙网蛋白水平低于150μg/ml或250μg/g时或者所述组合临床分数低于预先确定的分数时,诊断所述受试者患有稳定状态的克罗恩氏病。
在优选的实施方案中,所述参考值为约1%。
在另一个优选实施方案中,可以在受试者的相同生物样本中测量宿主dna相对丰度和钙网蛋白水平。
因此,本发明还涉及一种针对患有或疑似患有稳定状态的克罗恩氏病的受试者而产生定量数据的方法,所述方法包括:
a)在所述受试者的生物样本中进行至少一种分析,以确定宿主dna的相对丰度,其中第一定量数据表示宿主dna的相对丰度,优选和参考值进行比较;以及
b)在所述样本中进行至少一种分析,以确定钙网蛋白水平或组合临床分数,其中第二定量数据表示所述钙网蛋白水平,优选与150μg/ml或250μg/g进行比较,或所述组合临床分数优选与预先确定的分数进行比较。
换句话说,本发明涉及一种分析患有或疑似患有稳定状态的克罗恩氏病(cd)的受试者生物样本的方法,所述方法包括:
a)从所述受试者获得生物样本,
b)确定所述样本中宿主dna的相对丰度,
c)在所述样本中确定钙网蛋白水平或组合临床分数,
以及
d)确定所述相对丰度是否高于参考值,以及所述钙网蛋白水平是否低于150μg/ml或250μg/g或所述组合临床分数是否低于预先确定的分数。
更准确地说,本发明涉及用于诊断受试者中稳定状态的克罗恩氏病(cd)的方法,包括:
a)从所述受试者获得生物样本,
b)确定所述样本中宿主dna的相对丰度,
c)在所述样本中确定钙网蛋白水平或组合临床分数,
以及
d)当所述相对丰度大于参考值时,并且当所述钙网蛋白水平低于150μg/ml或250μg/g时或者所述组合临床分数低于预先确定的分数时,诊断所述受试者患有稳定状态的克罗恩氏病。
在优选的实施方案中,所述参考值为约1%。
在优选的实施方案中,在待测试的受试者的粪便样本中测量钙网蛋白。在更优选的实施方案中,如上所述,在相同的粪便样本中进行宿主dna和钙网蛋白检测。然而,这可能需要进行两种单独类型的检测,一种用于测量宿主dna相对丰度(例如通过qpcr),以及一种用于测量钙网蛋白的蛋白水平(例如通过elisa)。
因此,另一方面,本发明提出了测量钙网蛋白的基因水平,从而可以在本发明的方法中进行单一类型的检测。更优选地,这样的检测在相同的容器中进行,甚至更优选在相同的生物样本比如粪便样本中进行。
因此,根据此方面,本发明涉及一种针对患有或疑似患有稳定状态克罗恩氏病的受试者产生定量数据的方法,所述方法包括:
a)在所述受试者的生物样本中进行至少一种分析,以确定宿主dna的相对丰度,其中第一定量数据表示宿主dna的相对丰度,优选和第一参考值进行比较;以及
b)在所述样本(优选此处的)或所述受试者的另一生物样本中进行至少一种分析,以确定钙网蛋白基因水平或组合临床分数,其中第二定量数据表示所述钙网蛋白水平,优选与第二参考值和/或第三参考值进行比较,或所述组合临床分数优选与预先确定的分数进行比较。
换句话说,本发明涉及一种分析患有或疑似患有稳定状态的克罗恩氏病(cd)的受试者生物样本的方法,所述方法包括:
a)从所述受试者获得生物样本,
b)确定所述样本中宿主dna的相对丰度,
c)在所述样本(优选此处的)或所述受试者的另一生物样本中确定钙网蛋白基因水平或组合临床分数,
以及
d)确定所述相对丰度是否高于第一参考值,以及所述钙网蛋白基因水平是否低于第二参考值和/或高于第三参考值或所述组合临床分数是否低于预先确定的分数。
更确切地说,本发明涉及一种用于诊断受试者中稳定状态的克罗恩氏病(cd)的方法,包括:
a)从所述受试者获得生物样本,
b)确定所述样本中宿主dna的相对丰度,
c)在所述样本(优选此处的)或所述受试者的另一生物样本中确定钙网蛋白基因水平或组合临床分数,
以及
d)当所述相对丰度高于第一参考值时,以及当所述钙网蛋白水平低于第二参考值和/或高于第三参考值时或者所述组合临床分数低于预先确定的分数时,诊断所述受试者患有稳定状态的克罗恩氏病。
在优选的实施方案中,对于稳定状态,关于宿主dna的所述第一参考值如上所定义(1%);关于钙网蛋白的所述第二参考值优选是患有活跃型克罗恩氏病(即,患有不稳定状态的克罗恩氏病)的受试者中观察到的钙网蛋白基因水平;和/或关于钙网蛋白的所述第三参考值优选是健康受试者(即,不患有克罗恩氏病)中观察到的钙网蛋白基因水平。
“组合临床分数”,这里是指这样的任何分数,其将生物学参数与临床参数结合以产生与cd中的疾病严重程度或粘膜治愈相关的分数。它可以是例如钙网蛋白水平、hbi、性别、年龄、疾病持续时间、血小板计数、白蛋白、血小板、crp、直肠出血的组合(摘要op05,第七届ecco大会)。
“预先确定的分数”,这里是指通过任何统计或算法方法将这些多重参数组合而产生的值(参见例如,摘要op05,第七届ecco大会中提及的参数和值)。
这些方法适用于任何受试者,人或动物。然而,在优选的实施方案中,它们适用于人患者,尤其是疑似患有cd的人,或需要确认患有cd的人,或已经诊断为cd的人。
用于本发明方法的生物样本优选是粪便样本。
在优选的实施方案中,通过使用上述基于多核苷酸杂交分析的谱(profiling)方法和/或多核苷酸的测序,确定相对dna丰度。
如上述,根据本领域技术人员通常已知的任何方法测量钙网蛋白水平。优选,钙网蛋白的蛋白水平表示为μg/ml或μg/g。
这些方法与现有技术相比具有显著的优点,特别是与仅仅涉及测量粪便样本中钙网蛋白水平的那些方法相比较。实际上,如本领域技术人员所知,这样的诊断方法不够灵敏,并且给出假阳性结果。
此外,本发明人已经观察到,两个测量(步骤b)和步骤c))没有反映出简单的相关性:人dna的百分比在钙网蛋白高于150μg/ml的样本中显著提高,这反映出具有肠道炎症征兆的患者粪便中存在更多的人dna。因此,尽管这两种测量相关,但它们似乎并不是恰好捕获临床疾病的相同临床特征。
测量宿主dna相对丰度和钙网蛋白基因水平的优选技术是qpcr。
本发明方法中使用的试剂盒
可以例如通过使用预包装试剂盒来进行上述方法,所述试剂盒包含本发明的核酸片段或由本发明的核酸片段组成。
因此,本发明涉及用于本发明任何方法的试剂盒,所述试剂盒包含或由以下组成:
a)至少一种与宿主dna特异性杂交的核酸片段;
以及
b)进行所述方法的说明书。
如本文所使用的,术语“说明书”是指可用于传达如何进行本发明方法的出版物、记录、图表或任何其它介质。所述说明书可以例如附加到包含所述试剂盒的容器中。优选地,使用所述试剂盒的说明书包括参考值。
根据优选的实施方案,与宿主dna特异性杂交的所述核酸片段选自序列seqidno:1至seqidno:6的核酸片段、其变体及其互补序列。
更优选地,所述试剂盒包含或由以下组成:
a)引物组(seqidno:1、seqidno:2)和序列seqidno:3的探针;和/或引物组(seqidno:4、seqidno:5)和序列seqidno:6的探针;以及
b)进行所述方法的说明书。
然而,甚至更优选地,上述试剂盒可进一步包含:
c)至少一种能够特异性确定钙网蛋白的蛋白或基因水平的试剂。
术语“能够特异性地确定钙网蛋白水平的试剂”或“能够特异确定钙网蛋白表达水平的试剂”是指特异性识别钙网蛋白并允许在蛋白质或基因水平上定量其表达水平的试剂或试剂套装。这些试剂可以是例如特异性识别蛋白质钙网蛋白的抗体、适体或亲和体,或者识别编码钙网蛋白的基因的核酸片段,比如引物和/或探针。在本发明的上下文中,当所述试剂1)显示出结合和/或杂交活性的阈值水平,和/或2)与已知和钙网蛋白相关的靶分子没有显著交叉反应,则认为所述试剂是钙网蛋白“特异性的”或“特异性识别”钙网蛋白。这种试剂的结合亲和力可以容易地通过本领域技术人员来确定,例如通过scatchard分析。试剂的交叉反应性也可以由本领域技术人员容易地确定,因此需要在本文中进一步详细描述。能够特异性确定钙网蛋白表达水平的试剂的实例包括但不限于,抗钙网蛋白抗体(比如来自invitrogen的mac387igg1)和与编码钙网蛋白的基因特异性地杂交的核酸片段,比如上述s100a8和/或s100a9。
本发明进一步涉及如上所述的试剂盒在本发明任何方法中的用途(特别是体外用途)。
实施例
实施例1
1.材料和方法
1.1.群体
1.1.1cd群体
所有参与者都是“crohnometer1”研究的一部分,其目的是从克罗恩氏病患者的不同人群中收集粪便样本,以调查其肠道微生物群。研究的纳入标准是克罗恩氏病的临床诊断、和参与者签署知情同意书。crohnometer1是一项纵向研究,平均每个参与者在8个月的时间段内提供8个粪便样本。共包括99名参与者并提供粪便样本。在99名参与者中,68人的粪便样本进行了测序。总共438个样本被测序。
每次将粪便样本提供给研究时,各研究参与者填写问卷。问卷捕获了有关患者健康和粪便特征的信息。特别是以下信息用于评估疾病活动性/炎症状态:
-测量钙网蛋白水平(以患者粪便计)(钙网蛋白是表示炎症的蛋白质标记物);
-记录每个患者的harvey-bradshaw指数(hbi)。hbi是一种复合自动评估的指标,其反映了患者的一般健康状况。该分数基于对一般健康情况(well-being)的评估、腹痛的评估、每天液体粪便的数量、腹部肿块的存在、和并发症的存在。广泛用于克罗恩氏病患者状况的评估。
1.1.2健康对照群体
由健康个体组成对照个体组。主要排除标准是使用处方药和重大疾病史。从相同的个体收集多个样本,产生总共137个样本。
1.1.3nash对照群体
对另外两个来自更大研究的nash患者进行了测序。更大的nash研究称为nash2,其目的是从nash患者的不同群体中收集粪便样本,以调查其肠道微生物群,并鉴定nash与单纯性脂肪变性患者之间的差异。从那两名患者中获得6个样本。该群体尽管小,其被选择用作不位于肠道的炎症性疾病的对照群体。
1.2样本收集和制备
1.2.1排泄物取样
每三个星期,为cd群体的受试者提供含有dna稳定剂和书面说明的专用收集试剂盒,从而从家里收集粪便样本。在经过验证的dna保存缓冲液(通常为rna
同样的收集试剂盒用于对照群体。
1.2.2dna提取
将每个排泄物样本的冷冻等份试样悬浮于250μl硫氰酸胍0.1mtris(ph7.5)和40μl10%n-月桂酰肌氨酸中。然后,将悬浮液进行剧烈的珠粒振摇(beating)以从微生物细胞释放dna,并使用标准方案(godon等人,1997)进行dna提取。通过nanodrop和agilent和琼脂糖凝胶电泳评估dna完整性和浓度。
1.3illumina测序
在hiseq2500illumina测序仪上在iso17025认证实验室进行测序。他们使用iso17025认证的方法hshov4pe100。dna文库的制备遵循制造商的指导(illumina)。测序设备提供者所建议的工作流程用于进行不同的步骤:簇生成、模板杂交、等温扩增、线性化、封闭和变性以及测序引物的杂交。使用提供者的pipeline进行碱基识别(base-calling)。为每个样本生成了4000万个最小双端(paired-end)读取的目标。测序读取长度为100bp。
1.4生物信息学处理
使用enterome的内部pipeline处理原始读取。简要地说,pipeline基于mocat(kultima等人,2012)和内部脚本的汇编。它由使用mocatv1.3的质量控制、绘图(mapping)和基因丰度计算组成,包括illumina接头(adapter)和人基因组(hg19)的列表。绘制到人基因组上的读取数目基于在90%长度上95%的同一性,质量控制步骤之后进行返回,质量控制步骤包括修剪具有低质量分数的碱基。使用1—绘制到hg19的读取数目/修剪后的读取数目来计算样本中人读取的百分比。
2.结果
2.1对照与克罗恩氏病患者(cd)的比较
使用wilcoxon秩和检验,我们比较了来自健康对照的137个样本、来自nash患者的6个、以及来自cd患者的438个样本。cd相对于健康对照的p值具有高度显著性(p值=1.667e-12),图1。表1提供了两个群体的总结统计。
表1:绘制到人基因组hg19上的读取百分比的总结统计
来自健康对照的样本中99%在其总粪便dna中均含有小于1%的人dna,相比之下克罗恩氏病样本为84%。因此,截止值为1%,可以捕获16%的克罗恩氏病样本。因此,粪便中dna的存在是高度特异性的。
2.2克罗恩氏病患者(cd)中的疾病严重程度相关性
鉴于克罗恩氏病患者与健康对照在粪便样本中人dna百分比方面存在高度显著的差异,研究了与疾病严重程度的关系,以评估宿主dna相对丰度的度量是否可以用作疾病活动性的标记物。
为此,根据三个标准将患者分为疾病的活跃型组:1)他们是否具有150以上的钙网蛋白水平,
2)他们是否具有4以上的hbi分数,
3)他们是否具有4以上的hbi分数,或他们的钙网蛋白水平在150以上(组合分数)。
基于wilcoxon秩和检验,静止型患者粪便样本(n=227)和cd活跃期患者的粪便样本(n=211)中人dna百分比(相对丰度)之间的差异高度显著(参见图2,p-val=1.034e-09)。
具有超过20%人dna的样本中的95%来自活跃型患者。
具有超过10%人dna的样本中的90%来自活跃型患者。
具有超过1%人dna的样本中的80%来自活跃型患者。
roc曲线(图4)是视觉上的呈现,其表示基于各种截止值的真和假阳性数目。从左下角可以看出,具有非常高的特异性(100%,但灵敏度低,只有约10%的患者被捕获)。直线代表“非信息”分数。
单独考察钙网蛋白水平时,并将其与人dna(图3)进行比较,这两种测量并不反映简单的相关性,但钙网蛋白高于150μg/ml(p值=1.041e-07)的样本中人dna的百分比显著提高,这反映了这样的事实,即在具有肠道炎症征兆的患者粪便中存在更多的人dna。有趣的是,尽管这两种测量相关,但它们似乎并不是恰好捕获临床疾病的相同临床特征,因为从图3可以看出一些样本具有非常高的钙网蛋白水平并且没有人dna。
实施例2
1.材料和方法
1.1群体
如上述,参与者是“crohnometer1”研究的一部分。共11个粪便样本进行了测序。群体符合与实施例1相同的标准。
1.2样本收集和制备
1.2.1排泄物取样和dna提取
根据和上述实施例1中详述的相似过程,进行排泄物取样和dna提取。
1.2.2在宿主dna上进行qpcr
使用
以400nm终浓度运行引物,探针具有200nm终浓度。
每个反应跨越10万个拷贝至6.10个拷贝的标准曲线和样本一同运行,标准品之间的稀释因子为4x。样本归一化为4.84ng/μl的浓度,这至少为10倍稀释度。
表2.用于宿主dna的qpcr定量的引物和探针
使用阈值法生成来自cfx管理软件(bio-rad)的数据cq值。阈值设置为230。从cfx管理软件(bio-rad)获得标准曲线。使用标准曲线在cfx管理中计算样本浓度。
1.2.3qpcr数据的统计分析
基于绘制到人基因组的读取数目除以样本中总读取数目来计算估计的人dna百分比。使用validprime分析,该百分比与人dna的定量相关。
通常根据数据的线性回归分析来确定使用另一变量(qpcr分析)的值来预测变量(人dna)的值的能力,假设两个变量之间存在线性响应。统计分析在r中进行。
2.结果
2.1通过qpcr特异性引物进行的宿主dna丰度定量
图5显示了使用vp5和vp9引物和探针进行的qpcr分析之间产生的定量数据中的统计学显著相关性(相关性=0.964)。
图6和图7显示使用vp5(图6)或vp9(图7)引物和探针进行的qpcr分析产生的定量数据以及通过实施例1中提出的方法测量的人dna百分比(即illumina测序)中的统计学显著相关性(对于vp5分析,相关性=0.909,以及对于vp9分析为0.927)。
因此,使用上述表2中所述的vp5和vp9引物和探针,通过qpcr测量宿主dna丰度,可以允许进行诊断克罗恩氏病,并监测所述疾病的活动性。
实施例3
1.材料与方法
1.1群体
如上述,参与者是“crohnometer1”研究的一部分。共15个粪便样本进行了测序。群体符合与实施例1相同的标准。
1.2样本收集和制备
1.2.1排泄物取样和rna提取
根据和上述实施例1中详述的相似过程,进行排泄物取样。
然后根据制造商的说明,进行了一些修改,用
1.2.2rna质量和归一化
在分光光度计(dropsense96,trineannv)上分析15个提取的rna/dna样本的吸光度和纯度。在凝胶电泳(bioanalyzer,agilenttechnologies)上以rin值测量rna的质量。根据吸光度测量,将样本归一化为约66.67ng/μl。
1.2.3cdna合成
使用tataagrandscriptcdna合成试剂盒#a103(tataabiocenterab)将所有样本逆转录成cdna。在cdna合成之前,根据制造商的说明书,使用heat&rungdna去除试剂盒(catno80200-50,articzymes)进行dna酶处理。反应中加入了最大负载量的rna,使其能够获得尽可能高的cq值。将试剂混合。在t100(bio-radlaboratories,inc)上在20μl反应体积中进行逆转录。应用表3中的温度程序进行cdna合成。
1.2.4qpcr
在逆转录后,15个样本进行9×稀释。使用tataa
使用经设计用于扩增s100a8和s100a9基因的引物和探针进行qpcr,s100a8和s100a9基因编码形成钙网蛋白异二聚体的蛋白。可以由本领域技术人员基于这些基因的公知核苷酸序列而容易地设计所述引物和探针。
表3.编码s100a8和s100a9蛋白的基因
在cfx管理软件(bio-rad)上使用阈值法生成原始数据。用genex软件(multidanalyzesab)分析qpcr数据,并用genorm和normfinder进行参考基因的验证,以评估最稳定表达的基因。
1.2.5统计分析
对于每个基因,将三份的值进行平均。将cq值连同通过管家基因归一化的值(deltacq值),与测量钙网蛋白的蛋白水平时获得的log10转化的elisa值(参见实施例1,150μg/ml的值)进行比较。计算spearman相关性。另外,使用250μg/g的截止值将患者分为炎症或非炎症(dhaliwal等人,2015),并对每个基因的cq值进行wilcoxon秩和检验以比较两个组。统计分析在r中进行。
2.结果
2.1通过qpcr特异性引物定量钙网蛋白的基因水平
对于所有12(s100a9)至15(s100a8)的测试样本,s100a8和s100a9基因具有cq值。stati
表4.统计数据
图8显示,基因s100a8和s100a9中排泄物mrna水平与排泄物钙网蛋白水平(蛋白水平)之间的统计学显著相关性。
因此,通过qpcr测量钙网蛋白的基因水平,更特别是s100a8和/或s100a9的基因水平,可以允许诊断克罗恩氏病,更具体地,优选当和宿主dna相对丰度的测量组合时,可以允许用于监测所述疾病的活动性。
与实施例2中所述的测量宿主dna丰度的qpcr测试相组合,优选在单个管中,可以进一步容易地进行这种测试。
参考文献
cho,j.h.,&brant,s.r.(2011).recentinsightsintothegeneticsofinflammatoryboweldisease.gastroenterology,140(6),1704–12.doi:10.1053/j.gastro.2011.02.046
hmp,aframeworkforhumanmicrobiomeresearch.nature.2012jun13;486(7402):215-21
klaassench,jeuninkma,prinsencf,ruerstj,tanac,strobbelj,thunnissenfb.quantificationofhumandnainfecesasadiagnostictestforthepresenceofcolorectalcancer.clinchem.2003jul;49(7):1185-7.
laas等人.diagnosisandclassificationofcrohn’sdisease.autoimmunrev.2014apr-may;13(4-5):467-71
molodeckyna,等人.increasingincidenceandprevalenceoftheinflammatoryboweldiseaseswithtime,basedonsystematicreview.gastroenterology.2012jan;142(1):46-54.e42;quize30.doi:10.1053/j.gastro.2011.10.001
vincentc,mehrotras,loovg,dewark,mangesar.excretionofhostdnainfecesisassociatedwithriskofclostridiumdifficileinfection.journalofimmunologyresearch2014sept;论文id246203
shewalejg,schneidae,wilsonj,walkerja,batzermaandsinhask,人genomicdnaquantitationsystem,h-quant:developmentandvalidationforuseinforensiccasework;journalofforensicscience,2007,vol.52(2)
reevesj.r和bartlettj.m.s.methodsinmolecularmedicine;第39卷,第51章,471-483(2000)
schenam.proteinmicroarrays;jonesandbartlettlearning.(2005)
godonjj,zumsteine,dabertp,habouzitf和molettar,molecularmicrobialdiversityofananaerobicdigestorasdeterminedbysmall-subunitrdnasequenceanalysis.appl.environ.microbiol.1997,63(7):2802.
parkerrm&barnesnm,mrna:detectionbyinsituandnorthernhybridization.methodsinmolecularbiology106:247-283(1999)
heidca,stevensj,livakkj,williamspm..,realtimequantitativepcr,genomeresearch6:986-994(1996)
kultimajr,sunagawas,lij,chenw,chenh,mendedr,arumugamm,panq,liub,qinj,wangj,borkp.;mocat:ametagenomicsassemblyandgenepredictiontoolkit.plosone.2012;7(10):e47656
dhaliwala.,zeinoz.,tomkinsc.,cheungm.,nwokoloc.,smiths.,harmstonc和arasaradnamr.p.frontlinegastroenterol.;2015,6(1):14-19.epub2014。
序列表
<110>恩特姆生物科学公司
<120>宿主dna作为克罗恩氏病的生物标记物
<130>d34578
<140>pct/ep2016/051989
<141>2016-01-29
<150>ep15305142.0
<151>2015-01-30
<160>6
<170>patentinversion3.5
<210>1
<211>16
<212>dna
<213>人工序列
<220>
<223>vp5正向引物
<400>1
aacttggtgcggaggt16
<210>2
<211>18
<212>dna
<213>人工序列
<220>
<223>vp5反向引物
<400>2
atcgcttctgatggacac18
<210>3
<211>27
<212>dna
<213>人工序列
<220>
<223>vp5探针
<400>3
ccgccagactgcaatccatcaatgaca27
<210>4
<211>17
<212>dna
<213>人工序列
<220>
<223>vp9正向引物
<400>4
gcggaaacacaagggaa17
<210>5
<211>20
<212>dna
<213>人工序列
<220>
<223>vp9反向引物
<400>5
ttagaggcaaaagcaaagaa20
<210>6
<211>27
<212>dna
<213>人工序列
<220>
<223>vp9探针
<400>6
acagctaattaaaattgcacagttcct27
- 还没有人留言评论。精彩留言会获得点赞!