强直性脊柱炎的诊断标志物的制作方法
本发明属于诊断领域,涉及一种强直性脊柱炎的诊断工具,还涉及血液中matk基因在制备强直性脊柱炎诊断工具中的应用。
背景技术:
强直性脊柱炎又名别赫捷列夫氏(vonbechterev)病或马-施二氏(maritstrumpell)病,是一种慢性、进行性,中轴关节受累的慢性炎症性疾病。主要影响骨盆的骶髂关节、脊柱关节和椎旁组织。主要症状为下腰痛、脊椎僵硬及运动范围受限、x线显示两侧骶髂关节炎(sacroilitis)为其特征。由于该病一般先侵犯骶髂关节,并重点累及脊柱,最终导致脊柱骨性强直,故目前国内外多称之为强直性脊柱炎(ankglosingspondytitis,as)。
强直性脊柱炎(ankylosingspondylitis,as)是一种自身免疫性疾病,多发于16-40岁的青壮年,男女患病比例约为4-10:1。as在白种人群中的发病率约为1%-3%,我国as患病率约为0.2-0.6%,其中60%以上的患者伴有髋关节受累,致使20%以上as患者残疾。as属多基因疾病,具有明显的遗传倾向,虽然通常认为遗传与免疫因素在as发病中起主导作用,但确切的病因与发病机制仍不清楚。
但该病从发病到明确诊断往往需要5-7年的时间。虽然近几年,国内外在本病的诊断及治疗方法上均有不少进展,但由于本病是慢性进展性疾病,致残率较高,目前仍缺乏特异治疗,到后期病情不可逆转,严重影响患者生活自理能力和工作能力,给患者及家人带来沉重的精神和经济负担。因此早期诊断和合理治疗对延缓病理进展、降低致残、改善预后起到至关重要的作用。
技术实现要素:
本发明首次发现matk基因在强直性脊柱炎患者的血液中的含量比正常人低很多,matk基因的差异表达可作为诊断强直性脊柱炎的一种方法,据此可以开发诊断强直性脊柱炎的工具。
具体的,本发明提供了检测matk基因表达的产品在制备诊断强直性脊柱炎的工具中的应用。
进一步,上面所提到的检测产品包括:通过rt-pcr、实时定量pcr、免疫检测、原位杂交、芯片或高通量测序平台检测matk基因的表达水平以诊断强直性脊柱炎的产品。
进一步,所述用rt-pcr诊断强直性脊柱炎的产品至少包括一对特异扩增matk基因的引物;所述用实时定量pcr诊断强直性脊柱炎的产品至少包括一对特异扩增matk基因的引物;所述用免疫检测诊断强直性脊柱炎的产品包括:与matk蛋白特异性结合的抗体;所述用原位杂交诊断强直性脊柱炎的产品包括:与matk基因的核酸序列杂交的探针;所述用芯片诊断强直性脊柱炎的产品包括:蛋白芯片和基因芯片;其中,蛋白芯片包括与matk蛋白特异性结合的抗体,基因芯片包括与matk基因的核酸序列杂交的探针。
在本发明的具体实施方案中,所述用实时定量pcr诊断强直性脊柱炎的产品至少包括一对特异扩增matk基因的引物的序列如seqidno.1和seqidno.2所示。
优选地,所述诊断工具包括芯片、试剂盒、试纸或高通量测序平台。其中,高通量测序平台是一种特殊的诊断工具,检测matk基因表达的产品可以应用于该平台实现对matk基因的表达情况的检测。随着高通量测序技术的发展,对一个人的基因表达谱的构建将成为十分便捷的工作。通过对比疾病患者和正常人群的基因表达谱,容易分析出哪个基因的异常与疾病相关。因此,在高通量测序中获知matk基因的异常与强直性脊柱炎相关也属于matk基因的用途,同样在本发明的保护范围之内。
本发明还提供了一种诊断强直性脊柱炎的工具,所述产品包括芯片、试剂盒、试纸、或高通量测序平台。
其中,所述芯片包括基因芯片、蛋白质芯片;所述基因芯片包括固相载体以及固定在固相载体的寡核苷酸探针,所述寡核苷酸探针包括用于检测matk基因转录水平的针对matk基因的寡核苷酸探针;所述蛋白质芯片包括固相载体以及固定在固相载体的matk蛋白的特异性抗体;所述基因芯片可用于检测包括matk基因在内的多个基因(例如,与强直性脊柱炎相关的多个基因)的表达水平。所述蛋白质芯片可用于检测包括matk蛋白在内的多个蛋白质(例如与强直性脊柱炎相关的多个蛋白质)的表达水平。通过将多个与强直性脊柱炎的标志物同时检测,可大大提高强直性脊柱炎诊断的准确率。
其中,所述试剂盒包括基因检测试剂盒和蛋白免疫检测试剂盒;所述基因检测试剂盒包括用于检测matk基因转录水平的试剂;所述蛋白免疫检测试剂盒包括matk蛋白的特异性抗体。进一步,所述试剂包括使用rt-pcr、实时定量pcr、免疫检测、原位杂交或芯片方法检测matk基因表达水平过程中所需的试剂。优选度,所述试剂包括针对matk基因的引物和/或探针。根据matk基因的核苷酸序列信息容易设计出可以用于检测matk基因表达水平的引物和探针。
所述高通量测序平台包括检测matk基因表达水平的试剂。
所述试纸包括试纸载体和固定在试纸载体上的寡核苷酸,所述寡核苷酸能够检测matk基因的转录水平。
与matk基因的核酸序列杂交的探针可以是dna、rna、dna-rna嵌合体、pna或其它衍生物。所述探针的长度没有限制,只要完成特异性杂交、与目的核苷酸序列特异性结合,任何长度都可以。所述探针的长度可短至25、20、15、13或10个碱基长度。同样,所述探针的长度可长至60、80、100、150、300个碱基对或更长,甚至整个基因。由于不同的探针长度对杂交效率、信号特异性有不同的影响,所述探针的长度通常至少是14个碱基对,最长一般不超过30个碱基对,与目的核苷酸序列互补的长度以15-25个碱基对最佳。所述探针自身互补序列最好少于4个碱基对,以免影响杂交效率。
进一步,所述matk蛋白的特异性抗体包括单克隆抗体、多克隆抗体。所述matk蛋白的特异性抗体包括完整的抗体分子、抗体的任何片段或修饰(例如,嵌合抗体、scfv、fab、f(ab’)2、fv等。只要所述片段能够保留与matk蛋白的结合能力即可。用于蛋白质水平的抗体的制备时本领域技术人员公知的,并且本发明可以使用任何方法来制备所述抗体。
在本发明的具体实施方案中,所述针对matk基因的引物序列如下:正向引物序列如seqidno.1所示,反向引物如seqidno.2所示。
用于诊断强直性脊柱炎的matk基因及其表达产物的来源包括但不限于血液、组织液、尿液、唾液、脊髓液等可以获得基因组dna的体液。在本发明的具体实施方案中,用于诊断强直性脊柱炎的matk基因及其表达产物的来源是血液。在发明的具体实施方案中,血液是取自强直性脊柱炎患者和正常人的血液。
本发明的matk基因的具体序列可在国际公共核酸序列数据库genebank中查询到。
本发明的matk蛋白包括matk蛋白本身与matk蛋白的部分肽,matk蛋白的部分肽含有与强直性脊柱炎相关的功能域。
本发明的matk蛋白包括matk蛋白(序列可以在ncbi上查询到)以及matk蛋白的任何功能等同物。所述功能等同物包括matk蛋白保守性变异蛋白质、或其活性片段,或其活性衍生物,等位变异体、天然突变体、诱导突变体、在高或低的严紧条件下能与matk的dna杂交的dna所编码的蛋白质。
通常,已知的是,一个蛋白质中一个或多个氨基酸的修饰不会影响蛋白质的功能。本领域技术人员会认可改变单个氨基酸或小百分比的氨基酸或对氨基酸序列的个别添加、缺失、插入、替换是保守修饰,其中蛋白质的改变产生具有相似功能的蛋白质。提供功能相似的氨基酸的保守替换表是本领域公知的。
本发明的matk蛋白也包括对氨基酸序列的非保守修饰,只要经过修饰的蛋白质仍然能够保留matk蛋白的生物学活性即可。在此类修饰蛋白质中突变的氨基酸数目通常是10个或者更少,例如6个或者更少,例如3个或者更少。
通过添加一个氨基酸或多个氨基酸残基修饰的蛋白质的例子是matk蛋白的融合蛋白。对于与matk蛋白融合的肽或者蛋白质没有限制,只要所得的融合蛋白保留matk蛋白的生物学活性即可。
在本发明的上下文中,“诊断强直性脊柱炎”既包括判断受试者是否已经患有强直性脊柱炎、也包括判断受试者是否存在患有强直性脊柱炎的风险。
附图说明
图1显示利用qpcr检测matk基因在强直性脊柱炎患者和正常人中的表达差异;
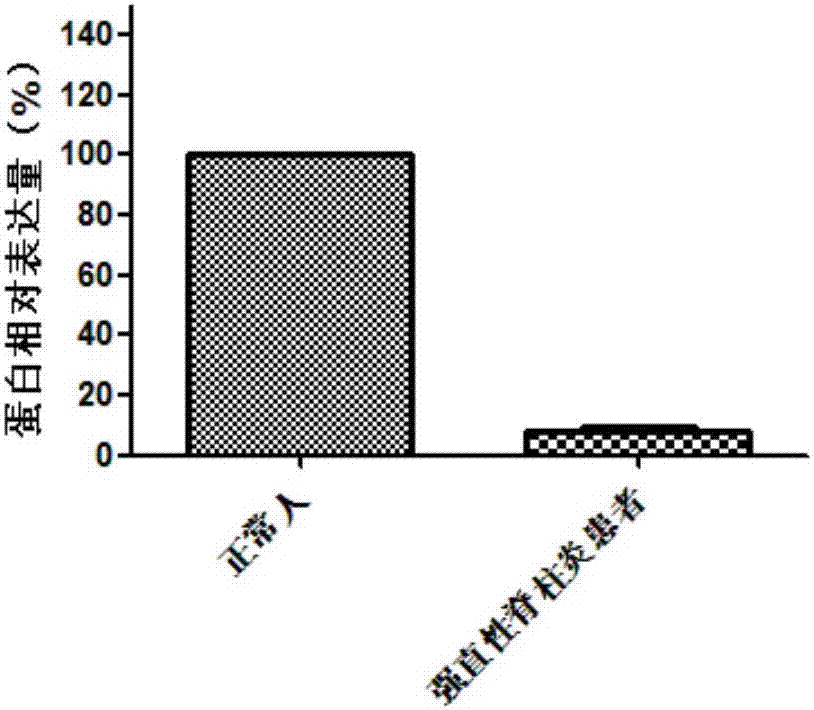
图2显示利用westernblot检测matk蛋白在强直性脊柱炎患者和正常人中的表达差异。
具体的实施方式
下面结合附图和实施例对本发明作进一步详细的说明。以下实施例仅用于说明本发明而不用于限制本发明的范围。实施例中未注明具体条件的实验方法,通常按照常规条件,例如sambrook等人,分子克隆:实验室手册(newyork:coldspringharborlaboratorypress,1989)中所述的条件,或按照制造厂商所建议的条件。
实施例1筛选强直性脊柱炎患者和正常人中差异表达的基因
1、样本采集:
病例样本全部采集自门诊病人,患者的诊断由富有临床经验的风湿病科医师根据1984年提出修订的纽约标准作出,并通过多次随访确诊。对照样本来自南方中心样本库中年龄、性别匹配,无关节炎病史的个体。
在知情同意的基础上随机收集了5个病人和7个正常对照个体的外周血样本。
2、全血总rna提取
取空腹血2ml经edta.na2抗凝,全血0.3ml采用3s柱离心式血液总rna抽提试剂盒(k3620上海博彩生物科技有限公司)抽取rna,rna提取物于-80℃保存。
3、rna样品的质量分析
利用nanodrop2000对所提rna的浓度和纯度进行检测,琼脂糖凝胶电泳检测rna完整性,agilent2100测定rin值。单次建库要求rna总量5μg,浓度≥200ng/μl,od260/280介于1.8~2.2之间。
4、片段化rna
illumina平台是针对短序列片段进行测序,mrna平均长度可能达几kb,因此需要对其进行随机打断。利用金属离子,可以将rna随机断裂成200bp左右的小片段。
5、反转合成cdna
在逆转录酶的作用下,利用随机引物,以mrna为模板反转合成一链cdna,进行二链合成时,dntps试剂中用dutp代替dttp,使cdna第二链中碱基包含a/u/c/g。
6、连接adaptor
双链的cdna结构为粘性末端,加入endrepairmix将其补成平末端,随后在3’末端加上一个a碱基,用于连接y字形的接头。
7、ung酶消化cdna二链
在pcr扩增前,用ung酶将cdna第二链消化,从而使文库中仅包含cdna第一链。
8、illuminax-ten上机测序
illuminax-ten测序平台,进行2*150bp测序。
9、生物信息学分析
测序数据获得以后的rawdata分析过程如下所示:
(1)用cutadapt对reads的5’和3’段进行trim,trim掉质量<20的碱基,并且删掉n大于10%的reads;
(2)tophat比对到参考基因组上。所用的参考基因组版本为grch38.p7,fasta和gff文件下载自ncbi;
(3)cuffquant定量mrna的表达量并标准化输出;
(4)在r环境下用degseq包比较对照组跟疾病组mrna的表达差异。显著差异mrna筛选条件:p-value<0.05。
10、结果
rna-seq结果显示,强直性脊柱炎患者和正常人之间共筛选出523个差异表达基因,其中,上调表达基因为342个,下调表达基因为181个。根据p-value排序,选择matk基因进行大样本验证。
实施例2大样本验证差异表达基因
1、样本采集
病例样本全部采集自门诊病人,患者的诊断由富有临床经验的风湿病科医师根据1984年提出修订的纽约标准作出,并通过多次随访确诊。对照样本来自南方中心样本库中年龄、性别匹配,无关节炎病史的个体。
在知情同意的基础上随机收集了30个病人和45个正常对照个体的外周血样本。
2、全血总rna提取
取空腹血2ml经edta.na2抗凝,全血0.3ml采用3s柱离心式血液总rna抽提试剂盒(k3620上海博彩生物科技有限公司)抽取rna,rna提取物于-80度保存。
3、应用rt-pcr
全血总rna合成cdna使用takara反转录反应试剂盒(drr037s大连宝生物工程有限公司)。总反应体系为20μl,包括2*sybrpremixextaptm,1-100ngcdna,50pmol/μl引物。两步法pcr循环条件:预变性95度30s,1个循环;变性95度5s,退火/延伸60度20s共40个循环。溶解曲线分析95度1s,65度15s,95度1s。
引物序列如下:
扩增matk基因的正向引物序列为5’-gagagggagagtttggag-3’(seqidno.1),反向引物序列为5’-gctgtcacatcacacttg-3’(seqidno.2);
扩增gapdh基因的正向引物序列为5’-aaagggtcatcatctctg-3’(seqidno.3),反向引物序列为5’-gctgttgtcatacttctc-3’(seqidno.4)。
4、相对定量分析
相对定量分析采用lightcyclerrelativequantification(version1.5)软件,标准化比值计算公式采用2-△△ct法,△ct(患者样本)=ct目的基因-ct内参基因,△ct(校正品)=ct目的基因-ct内参基因,△△ct=△ct(患者样本)-△ct(校正品)
5、结果
结果如图1所示,与正常人相比,强直性脊柱炎患者血液中matk基因表达量明显下调,差异具有统计学意义。
实施例2血液中matk蛋白的差异表达
1、单核细胞分离
外周血10ml,注入盛肝素的无菌小瓶中,加盖后立即轻轻摇匀。用无菌吸管加入等体积的hbss(nacl8.0g,na2hpo40.132g,kh2po40.06g,kcl0.4g,酚红1ml,nahco30.35g,d-葡萄糖1.0g,溶于1000ml双蒸水),以降低红细胞的凝聚。吸取8ml淋巴细胞分层液置50ml离心管中,将稀释血液沿管壁缓慢加入,保持界面清楚,勿使两者相混,在20℃2000r/min离心30min,小心吸取分层液与血浆交接部位混浊的灰白色层,即淋巴细胞层,加入另一支离心管中,用5倍体积的hbss洗涤2次,依次以2000r/min、1500r/min在室温下离心10min,以便去除大部分混杂的血小板,用10ml双蒸水与细胞团块混合1min,使残余红细胞裂解,然后迅速加入等量1.8%nacl溶液,2000r/min离心,去上清,经细胞计数后用hbss溶液调整细胞至1×106个/ml备用。
3、单核细胞总蛋白质提取
将上述实验所得细胞悬液(浓度为1×106个/ml)室温1000r/min离心10min,弃上清后加入100μl裂解缓冲液,4℃震荡1h,用超声波仪破碎细胞,每次10s,共10次,于4℃12000r/min离心1h;取上清用brandford法定量蛋白,分装成2.5μg/μl,-80℃冰箱保存备用。
4、westernblot检测
将提取的蛋白定量进行sds-page电泳,之后进行转膜、封闭、一抗孵育、二抗孵育、显色。
5、统计学处理
将蛋白条带的灰度值使用imagej软件进行分析,以β-actin为内参,将目的白条带的灰度值进行归一化处理。结果数据都是以平均值±标准差的方式来表示,采用spss13.0统计软件来进行统计分析的,两者之间的差异采用t检验,认为当p<0.05时具有统计学意义。
6、结果
结果如图2所示,与正常人相比,强直性脊柱炎患者血液中matk蛋白含量降低,差异具有统计学意义(p<0.05)。
上述实施例的说明只是用于理解本发明的方法及其核心思想。应当指出,对于本领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以对本发明进行若干改进和修饰,这些改进和修饰也将落入本发明权利要求的保护范围内。
sequencelisting
<110>北京泱深生物信息技术有限公司
<120>强直性脊柱炎的诊断标志物
<160>4
<170>patentinversion3.5
<210>1
<211>18
<212>dna
<213>人工序列
<400>1
gagagggagagtttggag18
<210>2
<211>18
<212>dna
<213>人工序列
<400>2
gctgtcacatcacacttg18
<210>3
<211>18
<212>dna
<213>人工序列
<400>3
aaagggtcatcatctctg18
<210>4
<211>18
<212>dna
<213>人工序列
<400>4
gctgttgtcatacttctc18
- 还没有人留言评论。精彩留言会获得点赞!