一种基于微流控技术的凹槽微丝的简易可控制备方法与流程
本发明属于微流控技术领域,具体涉及一种基于微流控技术的凹槽微丝的简易可控制备方法。
背景技术:
再生医学和人工器官的基本目标之一就是控制细胞在组织内的空间排布。为此,就需要对细胞行为进行调控,例如细胞的粘附、迁移、增殖和分化等。在细胞培养的过程中,有序构建的细胞外基质(ecm)就是一种重要的调控手段,它对于成功构建多功能组织或器官至关重要。目前,用于有序构建组织或器官的支架材料种类及其形貌已有多种形式,例如聚酯类的静电纺丝基底、plla多孔支架和凹槽状水凝胶材料等。其中,尺寸在微米级的凹槽表面,对于神经细胞、肌肉细胞等纤维状细胞的生长和定向诱导具有很好的效果。如果带有凹槽的表面位于同样是微米级的水凝胶微丝表面,则不仅可以实现细胞的定向诱导,还可以直接作为支架材料完成构建体外组织后的体内移植。目前,凹槽表面微丝已经在神经轴突引导、神经细胞培养、成骨细胞取向生长等方面得到了应用。
然而传统制备凹槽状微丝的方法需要用到静电纺丝或者高分子溶液溶剂快速挥发的制备方法,这些方法所能使用的高分子材料不具备水凝胶的生物相容性、保水性和营养物质良好透过的性质,具有其局限性。利用微流控湿法纺丝的方式则可以成功制备水凝胶微丝。但是,如果需要微丝表面具有一定的凹槽结构,则所使用的微流控芯片通道内部也需要具有相反的凹槽结构,这样的芯片制备方式复杂,并且对于凹槽的高度、深度等的调整困难,可能需要重新制备相应尺寸的微流控芯片,过程复杂。本发明以更加简单便捷的方式来制备凹槽状微丝,用于细胞定向诱导培养。
技术实现要素:
本发明的目的在于提供一种简易的基于微流控技术的凹槽丝合成新方法。通过对流速和浓度等参数的简单调节,可以控制凹槽的深度和宽度等参数,经过表面修饰的凹槽丝可以用于纤维状细胞的定向诱导培养或移植。
本发明一种基于微流控技术的凹槽微丝的简易可控制备方法,包括下列步骤:
(1)多平行通道微流控芯片的加工:利用常规软光刻的方法,制得具有多个平行通道的具有高低落差的pdms芯片,该芯片主要由鞘流入口,水凝胶预聚体入口,微丝出口,水凝胶预聚体通道,鞘流通道和主通道组成;鞘流入口通过鞘流通道与主通道相连接,水凝胶预聚体入口通过水凝胶预聚体通道与主通道相连接;其中水凝胶预聚体入口和水凝胶预聚体通道高度低于其余部分,水凝胶预聚体入口用于通入不同浓度的水凝胶预聚体溶液,高低浓度相间通入,鞘流入口用于通入含有交联剂的鞘流;微丝出口接入与鞘流液体相同的液体收集池中,用以进一步交联水凝胶,形成稳定的微丝;
(2)水凝胶材料的选择:本方法需要可以进行快速交联的水凝胶材料,原位固化将流体的形状保留下来。因此选用了可以用二价离子快速鳌合交联的海藻酸钠和果胶作为制备材料。选用的海藻酸钠粘度范围55-1000cps、浓度范围0.5-6%;果胶粘度范围100-1000cps、浓度0.5-4%;
(3)水凝胶凹槽微丝的可控制备:将配制好的海藻酸钠或果胶溶液经过0.45μm滤膜过滤后,用注射泵通过水凝胶预聚体入口注入水凝胶预聚体通道中,高浓度与低浓度溶液相间通入,或果胶与海藻酸钠相间通入,用以制备单一材料或杂合微丝;通过鞘流入口在鞘流通道通入含有氯化钙的异丙醇与水,异丙醇与水的体积比为9:1-5:5,氯化钙浓度为1-4%;水凝胶预聚体通道中的水凝胶流速范围1-5μl/min,鞘流通道中鞘流流速范围500-3000μl/min;在形成液体层流后,快速将流体脱水固化得到水凝胶微丝;通过调节所用水凝胶预聚体的浓度及其流速,控制凹槽丝的形貌参数;如图3所示;
(4)凹槽丝表面修饰:由于海藻酸钠和果胶的细胞粘附性差,凹槽丝需经过表面修饰才能使用;具体做法是先用0.1%聚-l-鸟氨酸氢溴酸盐溶液室温浸泡10min,再用5mg/ml的层粘连蛋白溶液处理1h。
芯片主通道宽度1-3mm,高度125-200μm,水凝胶预聚体通道宽50-200μm,高25-100μm,鞘流通道宽度300-600μm,高度125-200μm,平行通道个数3-9条,如图1和图2所示;两个相同的pdms芯片需要正面相对,用氧等离子封接到一起使用。
经表面修饰后的凹槽微丝其表面形貌和机械性能都将具有局部的差异,因此可以用于体外神经细胞、肌肉细胞等的定向诱导培养或者体内移植。
本发明利用多平行通道微流控芯片,间隔地通入高浓度和低浓度的水凝胶预聚体溶液,在形成液体层流后,快速将流体脱水固化得到水凝胶微丝。由于微丝中不同部分原始流体中溶质的量不同,在脱水固化过程中形变程度不同,因而在微丝表面会具有高低不平的凹槽结构,通过改变不同入口水凝胶预聚体的浓度和流速等,可以调节凹槽的深度和宽度等。此外,通过制备具有不同通道数量的芯片,可以对微丝表面的凹槽数量进行调控。该方法制备的微丝在体外神经细胞、肌肉细胞等的定向诱导培养中具有很大的应用价值。
附图说明
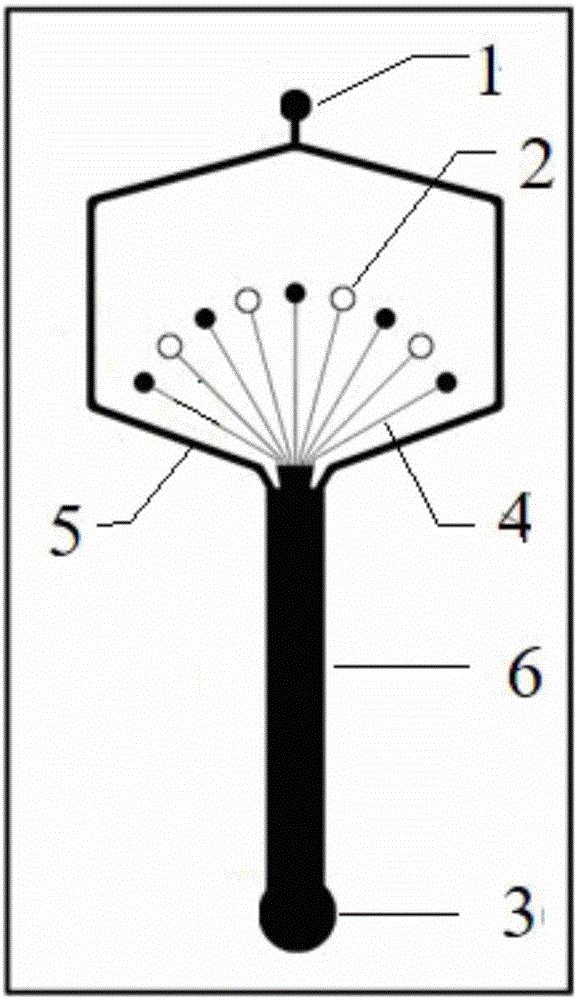
图1是九平行通道芯片结构示意图,
其中:1代表鞘流入口;2代表水凝胶预聚体入口,其中实心圆入口通入高浓度溶液,空心圆入口通入低浓度溶液;3代表微丝出口;4代表水凝胶预聚体通道;5代表鞘流通道;6代表主通道。
图2是具有不同数量水凝胶预聚体平行通道的芯片示意图,其中:a三平行通道芯片;b五平行通道芯片;c七平行通道芯片。
图3是通过改变平行流中充当棱和槽的流体的流速来调节凹槽宽度,其中:a固定棱流速,改变槽流速;b固定槽流速,改变棱流速。
图4是实施例1中凹槽微丝形貌表征,其中:a明场表征图(标尺:300μm);bsem表征图。
图5是实施例2中凹槽微丝形貌表征,其中:a明场表征图(标尺:200μm);b凹槽丝截面sem表征。
具体实施方式
在多个平行通道相间的入口通入浓度高低不同的海藻酸钠或果胶溶液,在出口处经含有异丙醇和氯化钙的鞘流边固化边脱水,得到表面带有凹槽状结构的微丝,用于后续细胞定向诱导培养。下面结合附图和实施例对本发明作进一步说明。
实施例1
一种基于微流控技术的凹槽微丝的简易可控制备方法,其特征在于:包括下列步骤:
(1)多平行通道微流控芯片的加工:利用常规软光刻的方法,制得具有多个平行通道的具有高低落差的pdms芯片,该芯片主要由鞘流入口1,水凝胶预聚体入口2,微丝出口3,水凝胶预聚体通道4,鞘流通道5和主通道6组成;鞘流入口1通过鞘流通道5与主通道6相连接,水凝胶预聚体入口2通过水凝胶预聚体通道4与主通道6相连接;其中水凝胶预聚体入口2和水凝胶预聚体通道4高度低于其余部分,水凝胶预聚体入口2用于通入不同浓度的水凝胶预聚体溶液,高低浓度相间通入,鞘流入口1用于通入含有交联剂的鞘流;微丝出口3接入与鞘流液体相同的液体收集池中,用以进一步交联水凝胶,形成稳定的微丝。
使用7条平行通道的芯片。芯片主通道宽度2.5mm,高度150μm,水凝胶预聚体通道宽100μm,高50μm,鞘流通道宽度400μm,高度150μm,如图1所示;两个相同的pdms芯片需要正面相对,用氧等离子封接到一起使用;
(2)水凝胶材料的选择:本方法需要可以进行快速交联的水凝胶材料,原位固化将流体的形状保留下来。因此选用了可以用二价离子快速鳌合交联的海藻酸钠和果胶作为制备材料。选用的海藻酸钠有两种0.5%naa(850cps)、2%naa(55cps);
(3)水凝胶凹槽微丝的可控制备:配制好的海藻酸钠溶液经过0.45μm滤膜过滤后,用注射泵通入位于内侧的平行通道中,高浓度与低浓度溶液相间通入(实心圆入口通入高浓度溶液,空心圆入口通入低浓度溶液),用以制备微丝。外侧鞘流通道中通入含有4%氯化钙的水溶液,中间每个平行通道的流速3μl/min(每个入口相同),鞘流流速2000μl/min。
(4)凹槽丝表面修饰:由于海藻酸钠的细胞粘附性差,凹槽丝需经过表面修饰才能使用。具体做法是先用0.1%聚-l-鸟氨酸氢溴酸盐溶液室温浸泡10min,再用5mg/ml的层粘连蛋白溶液处理1h。
(5)表征:对制备的微丝进行表面形貌表征,如图4所示。
实施例2
一种基于微流控技术的凹槽微丝的简易可控制备方法,其特征在于:包括下列步骤:
(1)多平行通道微流控芯片的加工:利用常规软光刻的方法,制得具有多个平行通道的具有高低落差的pdms芯片,利用常规软光刻的方法,制得具有多个平行通道的具有高低落差的pdms芯片,该芯片主要由鞘流入口1,水凝胶预聚体入口2,微丝出口3,水凝胶预聚体通道4,鞘流通道5和主通道6组成;鞘流入口1通过鞘流通道5与主通道6相连接,水凝胶预聚体入口2通过水凝胶预聚体通道4与主通道6相连接;其中水凝胶预聚体入口2和水凝胶预聚体通道4高度低于其余部分,水凝胶预聚体入口2用于通入不同浓度的水凝胶预聚体溶液,高低浓度相间通入,鞘流入口1用于通入含有交联剂的鞘流;微丝出口3接入与鞘流液体相同的液体收集池中,用以进一步交联水凝胶,形成稳定的微丝;使用7条平行通道的芯片。芯片主通道宽度2.5mm,高度150μm,水凝胶预聚体通道宽100μm,高50μm,鞘流通道宽度400μm,高度150μm,如图1所示;两个相同的pdms芯片需要正面相对,用氧等离子封接到一起使用;
(2)水凝胶材料的选择:本方法需要可以进行快速交联的水凝胶材料,原位固化将流体的形状保留下来。因此选用了可以用二价离子快速鳌合交联的海藻酸钠和果胶作为制备材料。选用的海藻酸钠有两种0.5%naa(1000cps)、2%naa(55cps);
(3)水凝胶凹槽微丝的可控制备:配制好的海藻酸钠溶液经过0.45μm滤膜过滤后,用注射泵通入位于内侧的平行通道中,高浓度与低浓度溶液相间通入(实心圆入口通入高浓度溶液,空心圆入口通入低浓度溶液),用以制备微丝。外侧鞘流通道中通入含有2%氯化钙的90%异丙醇溶液,中间每个平行通道的流速3μl/min(每个入口相同),鞘流流速1000μl/min。
(4)凹槽丝表面修饰:由于海藻酸钠的细胞粘附性差,凹槽丝需经过表面修饰才能使用。具体做法是先用0.1%聚-l-鸟氨酸氢溴酸盐溶液室温浸泡10min,再用5mg/ml的层粘连蛋白溶液处理1h。
(5)表征:对制备的微丝进行表面形貌表征,如图5所示。
- 还没有人留言评论。精彩留言会获得点赞!