核酸扩增的制作方法
背景技术:
核酸,例如脱氧核糖核酸(dna)或核糖核酸(rna),有时被从样本中提取并使用聚合酶链反应或任何等温扩增进行扩增。使用例如聚合酶链反应的核酸扩增可用于促进核酸的分离或定量。这种扩增可在诸如遗传测试、组织分型、传染病鉴定、遗传指纹识别和个人定制治疗方案的开发、法医分析、食品安全、环境测试等领域中提供益处。
附图说明
图1是示例性核酸扩增器的一些部分的示意图。
图2是示例性核酸扩增方法的流程图。
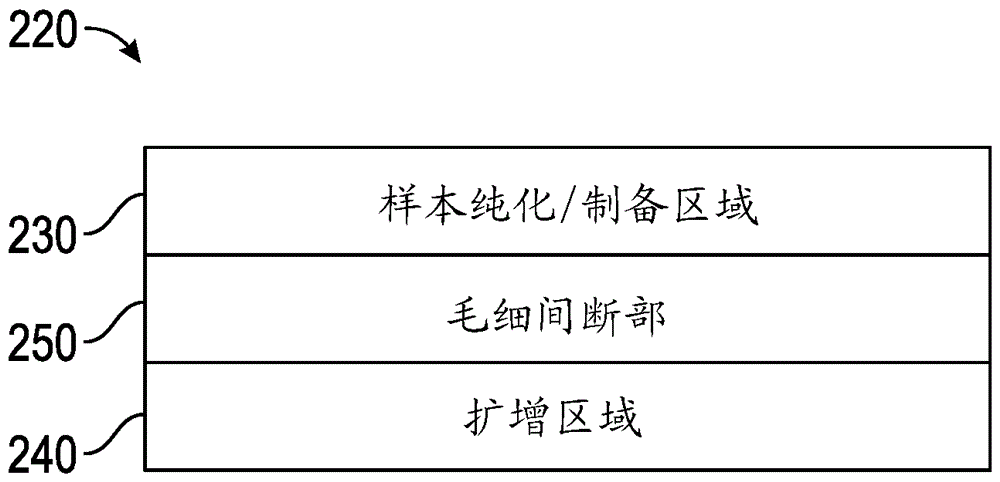
图3是示例性核酸扩增器的一些部分的示意图。
图4是用于处理样本的示例性方法的流程图。
图5是示例性核酸扩增器的一些部分的示意图。
图6是示例性核酸扩增器的一些部分的示意图。
图7是示例性核酸扩增器的一些部分的示意图。
图8是示例性核酸扩增器的一些部分的示意图。
图9是示例性核酸扩增器的一些部分的示意图。
遍及所有附图,相同的附图标记表示相似的但不必相同的元件。附图不一定按比例绘制,并且一些部件的尺寸可能被放大以更清楚地示出所示的示例。此外,附图提供了与说明书一致的示例和/或实施方式;然而,说明书不限于附图中提供的示例和/或实施方式。
具体实施方式
本文公开了用于从稀释样本中分离和浓缩至少一种核酸并使用例如聚合酶链反应(pcr)或等温核酸扩增技术扩增所述核酸的示例性微流体装置和微流体方法。使用流体喷射器在微流体装置上促进核酸的分离和/或浓缩,该流体喷射器通过喷嘴或其它喷口喷射样本的非核酸部分。使用流体喷射器促进更快速地分离和浓缩核酸。然后,经浓缩的核酸可以在添加核酸扩增试剂和应用等温过程或应用pcr热循环的情况下被扩增。
核酸的分离和浓缩(样本制备)发生在样本制备区,而核酸的扩增发生在扩增区。所公开的微流体装置和方法利用毛细间断部(capillarybreak)将样本制备区与扩增区分离。一旦制备了样本,毛细间断部就被破坏,并且经分离的核酸可以被输送到扩增区。
由微流体装置处理的较小的流体体积允许用较少样本和较少量的核酸扩增试剂进行测试。然而,在一些实施方式中,较小的流体体积可能对通过(一个或多个)流体喷射器喷口的流体蒸发更敏感。在核酸扩增和热处理期间,较小体积的流体甚至更容易蒸发。如果不加以控制,这种蒸发可能导致核酸扩增试剂变得过于浓缩,以致于干扰随后对经扩增的核酸的检测。在一些情况下,如果不加以控制,这种蒸发可能导致完全损失掉包含经浓缩的核酸和核酸扩增试剂的流体体积。
所公开的微流体装置和方法还可通过将流体喷射器的喷嘴或喷口与微流体装置的扩增区或扩增区域在空间上分开或分离来解决这种蒸发问题,其中,包含经浓缩的核酸的流体在热处理期间经历高温。所公开的微流体装置利用流体喷射器和扩增区或扩增区域之间的毛细间断部来提供这种流体分离。在一些实施方式中,在扩增区和排气口之间提供第二毛细间断部,从而在扩增区充满包含经浓缩的核酸的流体时促进气体穿过毛细间断部的排气。
使用流体喷射和使用毛细间断部以将流体喷射器与扩增区分离促进了在集成的微流体装置或流体芯片中的快速样本浓缩和核酸扩增。在低试剂体积和定制的以及复杂的分配方案的情况下,微流体装置可以实现稀释的核酸样本的核酸分离、浓缩和扩增。
所公开的微流体装置和方法可以采用微流体通道。微流体通道可以通过在流体芯片的衬底中进行蚀刻、微制造(例如,光刻)、微机械加工过程或其任意组合而形成。一些示例性衬底可以包括硅基衬底、玻璃基衬底、砷化镓基衬底和/或用于微制造装置和结构的其他此类合适类型的衬底。因此,微流体通道、腔室、喷口和/或其它此类特征可由流体芯片的衬底中制造的表面限定。此外,如本文所用,微流体通道可对应于尺寸足够小(例如,纳米尺度、微米尺度、毫米尺度等)的通道,以促进小体积的流体(例如,皮升级、纳升级、微升级、毫升级等)的传输。
本文描述的示例微流体装置或芯片可包括微流体通道,流体致动器可设置在微流体通道中。在这样的实施方式中,设置在微流体通道中的流体致动器的致动可以在微流体通道中产生流体移位。流体致动器可以包括基于压电膜的致动器、基于热电阻器的致动器、静电膜致动器、机械/冲击驱动的膜致动器、电化学致动器、磁致伸缩驱动致动器、或者可以响应于电致动而导致流体移位的其他这样的元件。
本文公开了一种核酸扩增器,其包括样本制备区、流体喷射器、扩增区以及在扩增区和流体喷射器之间的毛细间断部。本文公开了一种示例性核酸扩增器,其具有由毛细间断部分开的样本制备区和扩增区。
本发明公开了一种示例性方法核酸扩增方法,其包括:将核酸与样本的非核酸部分分离,利用流体致动器将样本的非核酸部分通过喷口排出,将流体施加到经分离的核酸,将核酸扩增试剂添加到流体中,以及在通过毛细间断部与喷口分开的热处理区域中加热具有经分离的核酸和核酸扩增试剂的流体。
图1是示例性核酸扩增器20的示意图。核酸扩增器20是微流体装置或微流体芯片的一部分,其从稀释样本中进行核酸分离和浓缩,并且通过应用pcr或任何等温扩增来进一步扩增经浓缩的核酸。核酸扩增器20利用流体喷射器来促进从稀释样本中更快地分离和浓缩核酸。核酸扩增器20利用毛细间断部将流体喷射器与扩增区分开,从而在制备样本的同时控制或抑制流体流入扩增区。在一些应用中,毛细间断部还控制或限制热循环期间的蒸发。核酸扩增器20包括样本纯化/制备区30、流体喷射器34、扩增区40和毛细间断部50。
样本纯化/制备区30包括扩增器20的一个区域,该区域进行样本的制备和纯化,以将样本的核酸部分与稀释样本的非核酸部分分离。经分开或经分离的核酸保留在纯化/制备区内,而稀释样本的非核酸部分被流体喷射器34冲洗或以其它方式去除。
在一个实施方式中,区域30包括容纳核酸吸附珠和保持结构的区域,所述保持结构抑制这种吸附珠行进到流体喷射器34。例如,在一个实施方式中,样本纯化/制备区30可以包括彼此布置或间隔开的支柱或柱,以便抑制这样的吸附珠行进到流体喷射器34。在一个实施方式中,吸附珠被提供为扩增器20的一部分,在接收可能包含核酸的样本之前被容纳在区域30内。在另一个实施方式中,在将样本置于区域30内之前,将吸附珠添加到样本。
在其它实施方式中,可以利用其它结构或过程将核酸与稀释样本的非核酸部分分离并浓缩。例如,在其它实施方式中,区域30可以包括嵌入的网格状或纤维状过滤器或嵌入膜,核酸选择性地粘附到所述过滤器。在其它实施方式中,例如在样本包含很少细菌或小百分比的非核酸成分的情况下,可以省略分离,其中,核酸可以通过蒸发而被浓缩。
如虚线所示,样本纯化制备区30流体地联接到流体喷射器34。术语“流体地联接”是指两个或多个流体传送体积直接连接到彼此或通过中间体积或空间连接到彼此,使得流体可从一个体积流入另一个体积。在一个实施方式中,区域30直接联接到流体喷射器34。在一个实施方式中,流体喷射器34邻近区域30或被容纳在区域30中。
流体喷射器34包括用于将流体(例如包含样本的非核酸部分的流体)选择性地从区域30中喷出的装置。在一个实施方式中,流体喷射器34可以将这种流体喷射到尿布或其它废物容器。在所示的示例中,流体喷射器34包括喷口52和流体致动器54。喷口52包括开口,所喷射的流体通过该开口。喷口52可以是喷嘴或喷嘴开口的形式。流体致动器54包括使流体移位通过喷口52的部件。流体致动器54可以包括基于压电膜的致动器、基于热电阻器的致动器、静电膜致动器、机械/冲击驱动的膜致动器、电化学致动器、磁致伸缩驱动致动器、或者可以响应于电致动而导致流体移位的其他这样的元件。尽管扩增器20被示出为包括单个流体喷射器34,但是应当理解,扩增器20可以包括多个流体喷射器34以增加稀释样本中的核酸可以被浓缩的速率。
扩增区40包括扩增器20的体积或部分,其中,在区域30中产生的经分离和经浓缩的核酸通过pcr或等温扩增过程而被扩增。对于这种核酸扩增,将经分离和经浓缩的核酸与核酸扩增试剂组合,所述核酸扩增试剂有时称为主混合物,其包括热稳定的核酸聚合酶,例如taq聚合酶。核酸扩增试剂还可以包括引物(primer),例如短核酸片段(核酸寡核苷酸),其包含与待扩增的目标核酸互补的序列。核酸扩增试剂也可以包括其它成分,例如(1)脱氧核苷酸三磷酸或dntps(包含三磷酸基团的核苷酸),即构造块,dna聚合酶从其合成新的dna链;(2)提供用于核酸聚合酶的活性和稳定性的合适化学环境的缓冲溶液;(3)二价阳离子,如镁(mg)或锰(mn)离子(mg2+或mn2+);和(4)一价阳离子,如钾(k+)离子。
在一个实施方式中,在区域40内将核酸扩增试剂添加到经分离和经浓缩的核酸。在另一个实施方式中,在核酸被沉积或引导到区40中之前,将核酸扩增试剂添加到经分离和经浓缩的核酸。在一些实施方式中,核酸扩增试剂可以在扩增器20的微流体通路或储器中被冷冻干燥,其中,核酸扩增试剂在进入扩增区40之前与包含核酸的流体混合。在其它实施方式中,核酸扩增试剂被预供应到区40,等待核酸的到达。例如,在一个实施方式中,核酸扩增试剂在扩增区40内被冷冻干燥,为包含核酸的流体的到达做好准备。
为了进行核酸扩增,扩增区40促进经浓缩的核酸和核酸扩增试剂的混合物的热循环。在一个实施方式中,扩增区40包括至少一个加热器,其可以被选择性地控制以根据等温扩增过程或pcr来加热混合物。例如,在一个实施方式中,扩增区40可包括至少一个热电阻器,其响应于被供应电流而输出热量。在其它实施方式中,扩增区40可以包括其它类型的加热器。在其它实施方式中,扩增区40可以包括导热表面或定位成邻近导热表面,其中,至少一个外部加热器用于选择性加热导热表面以进行热循环。
毛细间断部50在扩增区40和流体喷射器34的喷口52之间延伸并且将扩增区40与流体喷射器34的喷口52分开。毛细间断部50可以由收缩部形成,该收缩部的尺寸被设计成使得在气液界面之间或沿着气液界面形成毛细弯月面。毛细弯月面抑制流体流动越过或通过收缩部,直到弯月面响应于在气液界面处的液体压力超过压力阈值而被破坏,该压力阈值取决于收缩部以及在界面任一侧上的气体和液体的特性。在扩增期间,包含核酸和核酸扩增试剂的流体混合物经受可能导致高蒸发速率的高热。在一些实施方式中,毛细间断部50通过将扩增区40与流体喷射器34的喷口52分开和分离来减少这种蒸发。
图2是示例性核酸扩增方法100的流程图。方法100促进使用微流体芯片或装置从稀释样本中分离和浓缩核酸,并使用pcr扩增核酸。方法100促进从稀释样本中分离和浓缩核酸,同时减少在核酸被扩增时加热样本期间否则可能发生的蒸发。尽管方法100被描述为由扩增器20执行,但是应当理解,方法100同样可以用本文所述的任何包括流体喷射器的扩增器或利用流体喷射器喷射流体的其他扩增器来执行。
如框104所示,将核酸与样本的非核酸部分分离。在扩增器20中,这种分离发生在区域30内。在一个实施方式中,可以用核酸吸附珠将核酸与样本的非核酸部分分离,目标核酸吸附到核酸吸附珠而样本的其余非目标部分保留在样本的流体中。在另一个实施方式中,可以使用过滤器或膜将核酸与样本的非核酸部分分离。
如框106所示,流体喷射器的流体致动器将样本的非核酸部分通过喷口喷射。如上文关于扩增器20所述,样本的非核酸部分可以被喷射到尿布或储器。可以利用具有流体致动器的流体喷射器来喷射样本的非核酸部分,流体致动器可以包括基于压电膜的致动器、基于热电阻器的致动器、静电膜致动器、机械/冲击驱动的膜致动器、电化学致动器、磁致伸缩驱动致动器、或者可以响应于电致动而导致流体移位的其他这样的元件。在一些实施方式中,可以利用多个流体喷射器来提高样本被纯化/制备的速率。
在一些实施方式中,流体喷射器可以进一步用于喷射洗涤或清洁溶液或流体。当核酸保持吸附到吸附珠或其它结构时,可以用由流体致动器54通过喷口52喷射的清洁流体来洗涤或清洁制备区30的那些部分。可以进行这种操作以进一步增加样本的非核酸部分相对于经分开和分离的目标核酸被去除的可能性。
如框110所示,可将核酸扩增试剂添加到经分开的或经分离的核酸。在一个实施方式中,核酸扩增试剂是施加到经分离的核酸的流体的一部分。在另一个实施方式中,可以首先将流体添加到核酸,然后将流体和核酸的混合物与核酸扩增试剂组合。在一些实施方式中,核酸扩增试剂可以在被添加到包含经分离的核酸的流体之前被冷冻干燥。
如框114所示,将热施加到具有经分离的核酸和核酸扩增试剂的流体以扩增核酸。在一些实施方式中,作为等温扩增过程的一部分施加热。在一些实施方式中,作为热循环过程的一部分施加热,例如利用pcr。在每个这样的实施方式中,被施加热量的扩增区通过毛细间断部与制备区和喷口分开。毛细间断部可以由收缩部形成,该收缩部的尺寸被设计成使得在气液界面之间或沿着气液界面形成毛细弯月面。毛细弯月面抑制流体流动越过或通过收缩部,直到弯月面响应于在气液界面处的液体压力超过压力阈值而被破坏,该压力阈值取决于收缩部以及在界面任一侧上的气体和液体的特性。
在施加热和扩增期间,包含核酸和核酸扩增试剂的流体混合物经受可能导致高蒸发速率的高热。在一些实施方式中,毛细间断部通过将热循环区与喷口分开和分离来减少这种蒸发。
图3是示出另一示例性核酸扩增器220的示意图。核酸扩增器220包括样本纯化/制备区230、扩增区240和毛细间断部250。样本纯化/制备区230包括扩增器220的区域,该区域进行样本的制备和纯化以将样本的核酸部分与稀释样本的非核酸部分分离。经分开或经分离的核酸保留在纯化/制备区内,而稀释样本的非核酸部分由流体喷射器冲洗或以其它方式去除。在一个实施方式中,区域230类似于上述区域30。
扩增区240类似于上述扩增区40。扩增区240包括扩增器20的体积或部分,其中,通过施加热来扩增在区域30中产生的经分离和浓缩的核酸,无论是作为等温扩增过程的一部分还是pcr热循环过程的一部分。如上所述,扩增区240促进在区域230中产生的经分离或经浓缩的核酸和核酸扩增试剂的混合物的加热。如上所述,在一些实施方式中,可在核酸进入40上的扩增区240之前或在核酸进入扩增区240之后将核酸扩增试剂添加到核酸。在一些实施方式中,核酸扩增试剂可以在区域240中或在扩增器220的通向区域240的其它体积中被冷冻干燥。
毛细间断部250在样本纯化制备区230和扩增区240之间延伸并将样本纯化制备区230与扩增区240分离。毛细间断部部分250与上述毛细间断部50的相似之处在于,毛细间断部250可以由收缩部形成,该收缩部的尺寸被设计成使得在气液界面之间或沿着气液界面形成毛细弯月面。收缩部减小了液气界面的可能发生蒸发的区域,同时毛细弯月面抑制流体流动越过或通过收缩部,直到弯月面响应于气液界面处的液体压力超过压力阈值而被破坏,该压力阈值取决于收缩部以及在界面任一侧上的气体和液体的特性。在一些实施方式中,毛细间断部250可以进一步减少扩增区240内的流体的蒸发,否则这种蒸发可能通过设置在区域230中的开口发生,所述开口例如是喷口或流体喷射器开口、排气口、填充开口等。
图4是用于处理流体样本的示例性方法300的流程图,其中,样本在分开的区域中经历两个单独的过程。例如,方法300可用于处理流体样本,其中,流体样本在第一区域或第一区中经历制备,并且在第二区域或第二区中经历扩增。方法300利用毛细间断部来分开和分离集成的微流体装置的两个不同的处理区域。尽管特别地在核酸扩增(其中流体在通过毛细间断部与纯化/制备区分离的扩增区中经受加热)的上下文中描述了方法300,但是应当理解,方法300同样可以在微流体装置上进行的其它流体过程(其中流体在两个不同区中被不同地处理)中进行,。
如框304所示,在微流体装置的第一区域中(例如在微流体芯片的第一区域中)制备和/或纯化流体样本。第一区域可以流体地连接到开口或喷口或者可以包括开口或喷口,蒸发所导致的蒸气可以通过所述开口或喷口逸出,从而进一步增强流体的后续蒸发。例如,第一区域可以包括填充开口、排气口或喷嘴,流体通过填充开口从外部沉积到第一区域中,流体由流体致动器通过喷嘴喷射。
在一个实施方式中,可在第一区域中将核酸与稀释样本分离并浓缩,所述第一区域例如是如上所述的扩增器220的区域230。如上文关于扩增器220所述,第一区域流体地连接到流体喷射器34。在另一实施方式中,可以根据所遵循的处理协议以其它方式制备流体。
如框306所示,一旦制备,流体被引导到微流体装置或芯片的第二区域。第二区域可以是流体经历增加流体蒸发速率的过程的区域。例如,扩增器220包括扩增区240,在那里,流体经历热循环,使流体经受增加流体蒸发速率的热。
如框308所示,在第一区域和第二区域之间形成毛细间断部。在一个实施方式中,在毛细间断部已经形成之后,将所制备的样本引导到第二区域(在框306中),其中,毛细间断部被暂时破坏以允许所制备的样本移动至第二区域中,其中,一旦所制备的样本已经进入第二区域,则重新建立毛细间断部。在另一实施方式中,一旦所制备的样本已经进入第二区域,则初始地形成毛细间断部。
如框310所示,在第二区域中处理样本。这种处理发生在毛细间断部将第二区域与第一区域分离从而将第二区域中的流体与第一区域中的开口或喷口分离的同时。在方法300是pcr扩增的特定实施方式中,这种处理包括第二区域中的流体的热循环。在其他实施方式中,样本和第二区域的处理可以包括在样本上执行的其他过程,例如其他加热协议或过程。
图5示意性地示出了示例性核酸扩增器420的一些部分。扩增器420包括衬底422、样本纯化/制备区430、流体喷射器434、核酸扩增区440、毛细间断部450、毛细间断部开启器452、样本供应源460、洗涤流体供应源464、洗涤流体阀465、洗脱流体供应源466、洗脱流体阀467、核酸扩增试剂供应源468、核酸扩增试剂阀470和控制器472。
衬底422包括基座或底座,在其上形成扩增器420的其余部件,以便提供用于执行核酸分离、浓缩和扩增的集成的微流体芯片。在一个实施方式中,衬底422可以包括硅,在一些实施方式中,衬底422可以由多种材料构成,其中,形成在衬底422中的微流体通道或通路以及微流体储器由环氧树脂或光致抗蚀剂材料例如su8形成。在其它实施方式中,衬底422可以包括硅基衬底、玻璃基衬底、砷化镓基衬底和/或其它这种合适类型的衬底,其中,微流体通道可以通过执行蚀刻、微制造(例如,光刻)、微机械加工过程或其任何组合来形成。由衬底422支撑的部件可以被控制,并且通过导电迹线或电线以及电源(未示出)来提供电力,导电迹线或电线形成在随携的衬底422上并连接到控制器472。
样本纯化/制备区430类似于上述区30,除了区430被特别地示出为呈包括核酸分离器474的缝槽的形式。核酸分离器474使用核酸吸附珠476(其一部分示意性地示出)和吸附珠保持器478将核酸与稀释样本的非核酸部分分开和分离。核酸吸附珠476由材料形成或被涂覆,使得目标核酸吸附到珠476。如上所述,核酸吸附珠476可以在添加稀释样本之前存在于区域430内,或者可以在将稀释样本引入区域430之前添加到稀释样本。核酸吸附珠保持器478抑制珠476(和所吸附的目标核酸)从区430行进到流体喷射器434。在所示的示例中,保持器478包括在区430和容纳流体喷射器434的微流体通道或室之间的支柱或柱。在其它实施方式中,保持器478可以包括其它形式的过滤器,其阻挡珠476通过,同时允许包含非核酸部分的流体从其穿过而行进到流体喷射器434。
在另外的实施方式中,核酸分离器474可以具有其他形式。例如,在其它实施方式中,核酸分离器474可以包括吸附目标核酸的网或其它过滤材料。在其它实施方式中,核酸分离器可以包括嵌入膜。在一些实施方式中,例如在稀释样本包括很少的细菌使得核酸可以通过蒸发而被浓缩的情况下,可以省略核酸分离器474。
流体喷射器434分配或喷射稀释样本的与目标核酸分离的非核酸部分。流体喷射器434流体地连接到样本制备区430。每个流体喷射器434包括喷口52和流体致动器54(如上所述)。
核酸扩增区440用于对由样本制备区430输出的经分离和经浓缩的核酸进行热循环和扩增。核酸扩增区440包括热处理(热循环或等温)区域480、加热器482、排气口484、毛细间断部484。热处理区域480包括接收由样本制备区430输出的经分离和经浓缩的核酸的区域。在所示的示例中,热处理区域480包括蛇形微流体通路,用于在核酸和核酸扩增试剂经历热处理时容纳它们。在其它实施方式中,核酸扩增区440可具有其它形状。
热处理区域480与加热器482相关联,其中,核酸与核酸扩增试剂一起经历加热以扩增或倍增核酸。在一个实施方式中,加热器482包括形成在衬底422中的至少一个热电阻器,其将热输出到区域480。在pcr扩增过程中,改变加热器44的热输出以进行pcr热循环。
排气口484包括流体连通或流体地联接到热处理区域480的开口。排气口484将空气从热处理区域480排出,促进经浓缩的核酸流入热处理区域480的蛇形通路。在其它实施方式中,微流体通路的形状可以变化,并且可以由小的连接的腔室或一个大的储器的阵列或任何其它构造组成。
毛细间断部486在热处理区域480和排气口484之间延伸并将它们分离。毛细间断部486类似于上述毛细间断部50,因为毛细间断部486可以由收缩部形成,该收缩部的尺寸被设计成使得在气液界面之间或沿着气液界面形成毛细弯月面。收缩部减小了液气界面的可能发生蒸发的区域,同时毛细弯月面抑制流体流动越过或通过收缩部,直到弯月面响应于气液界面处的液体压力超过压力阈值而被破坏,该压力阈值取决于收缩部以及在界面任一侧上的气体和液体的特性。
毛细间断部450在样本制备区430和扩增区440的热处理区域480之间延伸并将它们分离。毛细间断部450类似于上述毛细间断部50,因为毛细间断部450可以由收缩部形成,该收缩部的尺寸被设计成使得在气液界面之间或沿着气液界面形成毛细弯月面。收缩部减小了液气界面的可能发生蒸发的区域,同时毛细弯月面抑制流体流动越过或通过收缩部,直到弯月面响应于气液界面处的液体压力超过压力阈值而被破坏,该压力阈值取决于收缩部以及在界面任一侧上的气体和液体的特性。
毛细间断部开启器452选择性地且可控地开启毛细间断部450以促进流体流入热处理区域480。毛细间断部开启器452包括用于产生跨过毛细间断部450的弯月面的气液界面的流体压力差以破坏弯月面的装置或部件。在所示的示例中,毛细间断部开启器452包括流体致动器,其使流体移位以将流体的压力增加到足以破坏跨过毛细间断部450的弯月面的程度。流体致动器可以包括基于压电膜的致动器、基于热电阻器的致动器、静电膜致动器、机械/冲击驱动的膜致动器、磁致伸缩驱动致动器、电化学致动器、或者可以响应于电致动而导致流体移位的其他这样的元件。在其它实施方式中,毛细间断部开启器452可以包括加热器,其将流体加热到足够程度以便破坏毛细弯月面。
样本供应源460包括微流体芯片422的用于供应包含或可能传输待扩增核酸的稀释样本的区域。样本供应源460流体地连接到样本制备区430。在一个实施方式中,样本供应源460包括容纳样本的储器。在另一个实施方式中,样本供应源460包括入口端口,样本可以通过该入口端口被引入到扩增器420。
洗涤流体供应源464包括微流体芯片422的用于供应洗涤流体的区域。洗涤流体包括用作溶剂的流体或冲洗核酸分离器474的表面(例如吸附珠476)并将其从非核酸污染物中清洁的其它流体。洗涤流体供应源464流体地连接到样本制备区430。在一种实施方式中,洗涤流体供应源464包括容纳洗涤流体的储器。在另一实施方式中,洗涤流体供应源464包括入口端口,洗涤流体可以通过该入口端口被引入到扩增器420。
洗涤流体阀465选择性地控制洗涤流体从洗涤流体供应源464到样本制备区430的流动。在所示的示例中,洗涤流体阀465包括毛细间断部487、排气口488和毛细间断部开启器489。毛细间断部487在结构和功能类似于毛细间断部450和484。毛细间断部487形成一对相继的毛细间断部,从而减少了阀465意外打开的可能性。每个毛细间断部487包括收缩部,该收缩部的尺寸被设计成使得在跨过收缩部的气液界面处形成弯月面。排气口488包括邻近收缩部且在收缩部之间的开口。当毛细间断部被毛细间断部开启器489破坏时,排气口488从毛细间断部之间排出气体。
毛细间断部开启器489选择性地和可控地开启毛细间断部487,以促进流体流入样本制备区430。毛细间断部开启器489类似于毛细间断部开启器452。毛细间断部开启器489包括用于产生跨过毛细间断部487的弯月面的气液界面的流体压力差以相继地破坏弯月面的装置或部件。在所示的示例中,毛细间断部开启器489包括流体致动器,该流体致动器使流体移位以将流体的压力增加到足以破坏跨过毛细间断部487的弯月面的程度。流体致动器可以包括基于压电膜的致动器、基于热电阻器的致动器、静电膜致动器、机械/冲击驱动的膜致动器、磁致伸缩驱动致动器、电化学致动器、或者可以响应于电致动而导致流体移位的其他这样的元件。在其它实施方式中,毛细间断部开启器489可以包括加热器,其将流体加热到足够程度以便破坏毛细弯月面。
洗脱流体供应源466包括微流体芯片422的用于供应洗脱流体的区域。洗脱流体包括用作溶剂的流体或将经浓缩的核酸携带到扩增区440中的其它流体。在利用核酸吸附珠在制备区430中将核酸与稀释样本分开和分离的实施方式中,洗脱流体从珠去除或洗脱核酸,并将核酸从制备区430输送到扩增区440。
洗脱流体供应源466流体地连接到样本制备区430。在一个实施方式中,洗脱流体供应源466包括容纳洗涤流体的储器。在另一实施方式中,洗脱流体供应源466包括入口端口,洗脱流体可通过该入口端口被引入到扩增器420。
洗脱流体阀467选择性地控制洗脱流体从洗脱流体供应源466到样本制备区430的流动。在所示的示例中,洗脱流体阀467包括毛细间断部490、排气口491和毛细间断部开启器492。毛细间断部490在结构和功能上类似于毛细间断部450和487。毛细间断部490形成一对相继的毛细间断部,从而减少阀467意外打开的可能性。每个毛细间断部490包括收缩部,该收缩部的尺寸被设计成使得在跨过收缩部的气液界面处形成弯月面。排气口491包括邻近收缩部且在收缩部之间的开口。当毛细间断部被毛细间断部开启器492破坏时,排气口491从毛细间断部之间排出气体。
毛细间断部开启器492选择性地和可控地开启毛细间断部490以促进流体流入样本制备区430。毛细间断部开启器492类似于毛细间断部开启器452。毛细间断部开启器492包括用于产生跨过毛细间断部490的弯月面的气液界面的流体压力差以相继地破坏弯月面的装置或部件。在所示的示例中,毛细间断部开启器492包括流体致动器,其使流体移位以将流体的压力增加到足以破坏跨过毛细间断部490的弯月面的程度。流体致动器可以包括基于压电膜的致动器、基于热电阻器的致动器、静电膜致动器、机械/冲击驱动的膜致动器、磁致伸缩驱动致动器、电化学致动器、或者可以响应于电致动而导致流体移位的其他这样的元件。在其他实施方式中,毛细间断部开启器492可以包括加热器,其将流体加热到足够程度以便破坏毛细弯月面。在核酸扩增试剂包括用于从分离器474(例如从珠476)洗脱核酸并将核酸输送至扩增区440的洗脱流体的实施方式中,可以省略洗脱流体供应源466和洗脱流体阀467。
核酸扩增试剂(r)供应源468包括微流体芯片422的用于供应核酸扩增试剂的区域。核酸扩增试剂(有时称为主混合物)包括热稳定的核酸聚合酶,例如taq聚合酶。核酸扩增试剂还可以包括引物,例如短核酸片段(核酸寡核苷酸),其包含与待扩增的目标核酸互补的序列。核酸扩增试剂还可以包括其它成分,例如(1)脱氧核苷酸三磷酸或dntps(包含三磷酸基团的核苷酸),即构造块,dna聚合酶从其合成新的dna链;(2)提供用于核酸聚合酶的活性和稳定性的合适化学环境的缓冲溶液;(3)二价阳离子,如镁(mg)或锰(mn)离子(mg2+或mn2+);和(4)一价阳离子,如钾(k+)离子。
核酸扩增试剂供应源468流体地连接到样本制备区430。在一个实施方式中,核酸扩增试剂供应源468包括容纳试剂流体的储器。在另一实施方式中,扩增试剂供应源468包括入口端口,试剂可以通过该入口端口被引入到扩增器420。
核酸扩增试剂阀470选择性地控制试剂流体从核酸扩增试剂供应源468到样本制备区430的流动。在所示的示例中,核酸扩增试剂阀470包括毛细间断部494、排气口496和毛细间断部开启器498。毛细间断部494在结构和功能上类似于毛细间断部450和484,除了毛细间断部494包括一对相继的毛细间断部,从而减少阀470意外打开的可能性。每个毛细间断部494包括收缩部,该收缩部的尺寸被设计成使得在跨过收缩部的气液界面处形成弯月面。排气口496包括邻近收缩部且在收缩部之间的开口。当毛细间断部被毛细间断部开启器498破坏时,排气口496从毛细间断部之间排出气体。
毛细间断部开启器498选择性地且可控地开启毛细间断部494以促进流体流入样本制备区430中。毛细间断部开启器498类似于毛细间断部开启器452。毛细间断部开启器498包括用于产生跨过每个毛细间断部494的弯月面的气液界面的流体压力差以相继地破坏弯月面的装置或部件。在所示的示例中,毛细间断部开启器498包括流体致动器,其使流体移位以将流体的压力增大到足以破坏跨过毛细间断部494的弯月面的程度。流体致动器可以包括基于压电膜的致动器、基于热电阻器的致动器、静电膜致动器、机械/冲击驱动的膜致动器、磁致伸缩驱动致动器、电化学致动器、或者可以响应于电致动而导致流体移位的其他这样的元件。在其他实施方式中,毛细间断部开启器498可以包括加热器,其将流体加热到足够程度以便破坏毛细弯月面。
在所示的示例中,扩增器420利用核酸扩增试剂供应源468和核酸扩增试剂阀470来选择性地将核酸扩增试剂供应到正在被扩增的核酸。在一个实施方式中,在混合物流体进入扩增区440之前,核酸扩增试剂被供应到由来自供应源466的流体携带的经浓缩的核酸。在另一个实施方式中,在流体已经进入扩增区440之后,核酸扩增试剂被供应到由来自供应源466的流体携带的经浓缩的核酸。
在一些实施方式中,扩增器420可以包括在扩增区域480内的冷冻干燥的核酸扩增试剂499。在一个实施方式中,包含在扩增区440的扩增区域480内的冷冻干燥的核酸扩增试剂499可以包括扩增增强材料的完全混合物。例如,冷冻干燥的pcr级499可包括热稳定的核酸聚合酶,如taq聚合酶。核酸扩增试剂499还可以包括引物,例如短核酸片段(核酸寡核苷酸),其包含与待扩增的目标核酸互补的序列。核酸扩增试剂499还可以包括其它成分,例如(1)脱氧核苷三磷酸,或dntps,即构造块,dna聚合酶从其合成新的dna链;(2)提供用于核酸聚合酶的活性和稳定性的合适化学环境的缓冲溶液;(3)二价阳离子,如镁(mg)或锰(mn)离子(mg2+或mn2+);和(4)一价阳离子,如钾(k+)离子。在一些实施方式中,核酸扩增试剂499的各种组分或成分可以沿着扩增区域480相继地或顺序地定位,以提供这样的化学品或生物材料向携带或可能携带经浓缩的核酸的流体的分阶段添加。
在一个实施方式中,冷冻干燥的核酸扩增试剂499可以补充通过或者由供应源468供应的核酸扩增试剂。在另一实施方式中,可以省略供应源468和阀470。在一个实施方式中,冷冻干燥的核酸扩增试剂499可以包括用于pcr扩增的一组化学品或生物材料的第一部分,而供应源468提供用于pcr扩增的该组化学品或生物材料的第二不同的部分。例如,在一个实施方式中,可以在扩增区域480中对可能更适于冷冻干燥或者可能更适于润湿的那些化学成分进行冷冻干燥,而可以通过供应源468提供较不适于冷冻干燥的其他化学成分或生物材料。
控制器472包括处理单元和相关联的指令,所述指令控制在芯片422上执行的功能中的至少一些。控制器472的处理单元遵循包含在非暂时性计算机可读介质上的这种指令,以控制流体致动器54,控制毛细间断部开启器489、毛细间断部开启器496和毛细间断部开启器452。控制器472的处理单元通过芯片422上的导电电线或迹线连接到每个这样的部件。
在一个实施方式中,控制器472执行上述方法100。在一个实施方式中,控制器472接收输入,该输入指示样本何时已经被引入样本制备区430。在其它实施方式中,控制器472连接到传感器431,该传感器431感测样本被引入样本制备区430。在足以允许核酸分开、分离和浓缩的预定时间过去之后(例如在一个实施方式中吸附到珠476),控制器472输出控制信号,导致致动器54将非核酸部分喷射到尿布、储器或另一通路中。
在一个实施方式中,由样本供应源460引入的样本包括已经经历裂解的细胞。在另一个实施方式中,样本中的细胞在样本制备区430内经历裂解。例如,样本的细胞可在样本制备区430中经历化学裂解,例如用表面活性剂的化学裂解。
在从传感器431接收到指示样本的非核酸部分已经被充分地喷射和排出的输入或信号时,控制器472可以输出控制信号,从而导致毛细间断部开启器489破坏毛细间断部487的弯月面以打开阀465,从而将来自供应源464的洗涤流体供应到样本制备区430。在一种实施方式中,洗涤流体464的引入可以由传感器431感测,并被传送到控制器472。洗涤流体还确保去除样本的非核酸部分。控制器472可以输出控制信号,从而导致流体致动器54进一步通过喷口52喷射洗涤流体。洗涤循环可重复进行,直到制备区430已被充分洗涤和清洁并被排空。
在样本制备区430的清洁之后,控制器472可以进一步输出控制信号,从而导致毛细间断部开启器492打开阀467,从而将洗脱流体从供应源466供应到样本制备区430。洗脱流体从任何核酸保持器/过滤器/珠释放或洗脱核酸。在一个实施方式中,流体从吸附珠476释放核酸。
当核酸从保持器(例如珠476)释放时,控制器472输出控制信号,从而导致毛细间断部开启器498打开阀470,从而将包含核酸扩增试剂的流体从供应源468供应到样本制备区430。核酸扩增试剂流体在样本制备区430中与核酸混合。在试剂流体具有一组分以便从任何核酸保持器/过滤器(例如从吸附珠476)释放或洗脱核酸的实施方式中,可以省略通过阀467的致动从供应源466供应洗脱流体。.
如上所述,在一些实施方式中,在扩增区域480包括冷冻干燥的核酸扩增试剂499的情况下,该步骤可以被修改或省略。在这种实施方式中,(从供应源468、从样本供应源460或另一端口或储器提供的)流体可以省略核酸扩增试剂,其中,流体释放核酸并将核酸携带到扩增区域480中,在那里,流体然后与冷冻干燥的核酸扩增试剂混合。流体(无论是包含核酸扩增试剂还是省略核酸扩增试剂)的体积被控制,以便基本上并且在一个实施方式中完全地填装(prime)扩增区域480,而不打开或破坏跨过毛细间断部486的弯月面。
当核酸扩增试剂在制备区430中与所释放的核酸混合时,如根据来自传感器431的信号确定的,控制器472输出控制信号,从而致动毛细间断部开启器452。在一个实施方式中,控制器472输出控制信号,从而致动流体致动器以便破坏跨过毛细间断部450的弯月面,从而促进包含核酸扩增试剂和核酸的流体混合物流入扩增区域480。在一个实施方式中,样本制备区430用流体回填,例如用水回填,以进一步抑制热循环期间的蒸发。
当混合核酸扩增试剂(无论来自供应源468和/或来自冷冻干燥的试剂499)时,控制器472可输出这样的控制信号,从而导致加热器482加热或热循环扩增区域480内的流体混合物。在一些实施方式中,控制器472可以包括位于扩增区域480内的至少一个传感器433,其向控制器472指示扩增区域480中的流体混合物的存在、其扩增状态和/或流体混合物的当前温度。在这种等温加热或热循环期间,由于存在非常少的排气口,所以减少了从扩增区域480的蒸发。跨过毛细间断部486的弯月面减少了通过排气口484的蒸发,而在扩增区域480的填装之后重新建立的跨过毛细间断部450的弯月面减少了通过喷口52的蒸发。
当加热或热循环完成时,感测或检测目标核酸的存在和量(如果有的话)。在一个实施方式中,微流体芯片422包括窗口或透明部分,其促进扩增区域480内的目标核酸的光学感测或检测。由扩增器420进行的扩增可用于促进核酸的分离或定量。这种扩增可在诸如遗传测试、组织分型、传染病鉴定、遗传指纹识别和个人定制治疗方案的开发等领域中提供益处。
图6示意性地示出了示例性核酸扩增器520的一些部分。核酸扩增器520包括衬底422、样本纯化/制备区530、流体喷射器434、核酸扩增区540、毛细间断部550、毛细间断部开启器552、样本供应源460、洗涤流体供应源464、洗涤流体阀465、洗脱流体供应源466、洗脱流体阀467、核酸扩增试剂供应源468、核酸扩增试剂阀470和控制器572。扩增器520的与扩增器20的部件相对应的那些部件被类似地编号。
样本纯化/制备区530包括微流体芯片422的区域,在该区域中将目标核酸与通过样本供应源460引入的样本的其余非核酸部分分开或分离。在所示的示例中,区430包括长形缝槽533、一系列u形微流体通路535、核酸分离器574和细胞裂解器537。缝槽533连接到样本供应源460、洗涤流体供应源464和核酸扩增试剂供应源468。微流体通路535的一个端部连接到缝槽533并且第二相对终端容纳流体喷射器434。
核酸分离器574分离器将核酸与稀释样本的非核酸部分分离。在一个实施方式中,核酸分离器574包括核酸吸附珠476(其一部分示意性地示出)和吸附珠保持器578。核酸吸附珠476由材料形成或被涂覆,使得目标核酸吸附到珠476。核酸吸附珠476可以在添加稀释样本之前存在于区430内,或者可以在将稀释样本引入区430之前被添加到稀释样本。核酸吸附珠476由保持器578保持在缝槽533和/或通路535中。
核酸吸附珠保持器578抑制珠476(和所吸附的目标核酸)从区430行进到流体喷射器434。在所示的示例中,保持器578包括在通路535内、在缝槽533和流体喷射器434之间的支柱或柱。在其它实施方式中,保持器478可以包括其它形式的过滤器,其阻挡珠476通过,同时允许包含非核酸部分的流体从其穿过行进到流体喷射器434。
在其它实施方式中,核酸分离器574可以具有其他形式。例如,在其它实施方式中,核酸分离器574可以包括吸附目标核酸的网或其它过滤材料。在其它实施方式中,核酸分离器可以包括嵌入膜。在一些实施方式中,例如在稀释样本包括很少的细菌使得核酸可以通过蒸发被浓缩的情况下,可以省略核酸分离器574。
流体喷射器434分配或喷射稀释样本的与目标核酸分离的非核酸部分。流体喷射器434存在于通路535的端部,保持器578位于流体喷射器434和缝槽533之间。每个流体喷射器434包括喷口52和流体致动器54(如上所述)。
细胞裂解器537包括由微流体芯片422支撑的部件,其用于裂解通过样本供应源460引入的样本内所包含的细胞。细胞裂解器537将热和/或搅拌施加到裂解物细胞。在所示的示例中,细胞裂解器537包括搅动流体的流体致动器。在一个实施方式中,细胞裂解器537包括热阻流体致动器,其搅动以及加热流体以裂解样本的细胞。形成细胞裂解器537的流体致动器沿着缝槽533和保持器578之间的通路535中的每一个顺序地或串行地定位。如图6所示,细胞裂解器的数量可以变化。沿着每个通路535顺序地定位的多个细胞裂解器537促进细胞的分阶段裂解,其中,沿着每个单独的通路535的不同细胞裂解器可以具有不同的特性或者可以由控制器572以不同的方式致动,这取决于沿着每个通路535的串列中的单独细胞裂解器的相对位置。在一个实施方式中,细胞裂解器被同时致动或激发。在另一个实施方式中,细胞裂解器被顺序地致动或激发。
核酸扩增区540用于对由样本制备区530输出的经分离和经浓缩的核酸进行热循环和扩增。核酸扩增区540包括热处理区域580、(一个或多个)加热器482、排气口484和毛细间断部586。热处理区域580包括单独且不同的微流体通路,其接收由样本制备区530输出的经分离和经浓缩的核酸。在其它实施方式中,热处理区域580可具有其它形状。
每个热处理区域580与加热器482相关联,其中,核酸与核酸扩增试剂一起经历热循环以扩增或倍增核酸。在一个实施方式中,加热器482包括形成在衬底422中的至少一个热电阻器,其将热输出到区域480。由加热器482输出的热可以本质是等温的,或者可以改变以进行pcr热循环。在一个实施方式中,每个这样的区域580包括专用加热器,其中,不同的加热器可以彼此独立地操作以在不同的区域中执行不同的热循环。在另一实施方式中,这样的区域580共享单个加热器。
排气口484包括流体连通或流体地联接到热循环区域580的开口。排气口484将空气从热循环区域580排出,从而促进经浓缩的核酸流入不同的热循环区域580。
毛细间断部586在它们各自的热循环区域580和排气口44之间延伸并将它们分离。毛细间断部584类似于上述毛细间断部50,因为毛细间断部586可以由收缩部形成,该收缩部的尺寸被设计成使得在气液界面之间或沿着气液界面形成毛细弯月面。收缩部减小了液气界面的可能发生蒸发的区域,同时毛细弯月面抑制流体流动越过或通过收缩部,直到弯月面响应于气液界面处的液体压力超过压力阈值而被破坏,该压力阈值取决于收缩部以及在界面任一侧上的气体和液体的特性。
毛细间断部550在样本制备区430和扩增区540的热处理区域580之间延伸并将它们分离。毛细间断部550各自类似于上述毛细间断部50,因为每个毛细间断部550可以由收缩部形成,该收缩部的尺寸被设计成使得在气液界面之间或沿着气液界面形成毛细弯月面。收缩部减小了液气界面的可能发生蒸发的区域,同时毛细弯月面抑制流体流动越过或通过收缩部,直到弯月面响应于气液界面处的液体压力超过压力阈值而被破坏,该压力阈值取决于收缩部以及在界面任一侧上的气体和液体的特性。
毛细间断部开启器552选择性地且可控地开启它们各自的毛细间断部550,以促进流体流入各自的热处理区域580。毛细间断部开启器552各自包括用于产生跨过毛细间断部550的弯月面的气液界面的流体压力差以破坏弯月面的装置或部件。在所示的示例中,每个毛细间断部开启器552包括流体致动器,该流体致动器使流体移位以将流体的压力增大到足以破坏跨过毛细间断部550的弯月面的程度。流体致动器可以包括基于压电膜的致动器、基于热电阻器的致动器、静电膜致动器、机械/冲击驱动的膜致动器、磁致伸缩驱动致动器、电化学致动器、或者可以响应于电致动而导致流体移位的其他这样的元件。在其它实施方式中,毛细间断部开启器552可以包括加热器,其将流体加热到足够程度以便破坏毛细弯月面。
在一些实施方式中,可以省略毛细间断部开启器552,其中,细胞裂解器537还用作毛细间断部开启器。例如,在一些实施方式中,可以通过在致动或激发细胞裂解器537的同时致动流体喷射器434来维持每个毛细间断部550处的弯月面,使得任何压力增加都不足以破坏跨过毛细间断部550的弯月面。为了破坏跨过毛细间断部550的弯月面以允许流体流入扩增区域580,可以致动细胞裂解器537(流体致动器的形式,例如热电阻器)中的至少一个,而不致动或激发流体喷射器434,其中,细胞裂解器537被致动以便提供足够的流体移位力并且压力增大以破坏弯月面并打开各自的毛细间断部550。
控制器572类似于控制器472,因为控制器572包括处理单元和相关联的指令,所述指令控制在芯片422上执行的功能中的至少一些。控制器572的处理单元遵循包含在非暂时性计算机可读介质上的这种指令,以控制流体致动器54,以控制毛细间断部开启器489、毛细间断部开启器496、毛细间断部开启器492、细胞裂解器537和毛细间断部开启器552。控制器572的处理单元通过芯片422上的导电电线或迹线连接到每个这样的部件。
在一个实施方式中,控制器572执行上述方法100。在一个实施方式中,控制器572接收输入,该输入指示样本何时已经被引入样本制备区530中。在其它实施方式中,控制器572连接到传感器431,该传感器431感测样本引入到样本制备区530中。当样本在样本制备区530内、在缝槽533和通路535内时,控制器572输出控制信号,从而选择性地致动细胞裂解器537以裂解样本中的细胞。在一些实施方式中,当使用化学品或其它机制来裂解细胞时,可以省略裂解器537。在经过足以允许核酸分开、分离和浓缩的预定时间之后,例如吸附到珠476之后,控制器572输出控制信号,从而导致致动器54将非核酸部分喷射到尿布、储器或另一通路中。
当从传感器431接收到指示样本的非核酸部分已经被充分地喷射和排放的输入信号时,控制器572可以输出控制信号,从而导致毛细间断部开启器489破坏毛细间断部487的弯月面以打开阀465,从而将洗涤流体从供应源464供应到样本制备区430。在一种实施方式中,洗涤流体464的引入可以由传感器431感测,并被传送到控制器572。洗涤流体还确保去除样本的非核酸部分。控制器572可输出控制信号,从而导致流体致动器54进一步通过喷口52喷射洗涤流体。洗涤循环可重复进行,直到制备区530已被充分洗涤和清洁并被排空。
在清洁样本制备区430之后,控制器572可以进一步输出控制信号,从而导致毛细间断部开启器492打开阀467,从而将洗脱流体从供应源466供应到样本制备区530。洗脱流体从任何核酸保持器/过滤器/珠释放或洗脱核酸。在一个实施方式中,流体从吸附珠476释放核酸。
当核酸从保持器(例如珠476)释放时,控制器572输出控制信号,从而导致毛细间断部开启器498打开阀470,从而将包含核酸扩增试剂的流体从供应源468供应到样本制备区530。核酸扩增试剂流体在样本制备区530中与核酸混合。在试剂流体具有一组分以便从任何核酸保持器/过滤器(例如从吸附珠476)释放或洗脱核酸的实施方式中,可以省略通过阀467的致动从供应源466供应洗脱流体。
核酸扩增试剂流体在样本制备区430中与核酸混合。如上所述,在一些实施方式中,在扩增区域580包括冷冻干燥的核酸扩增试剂499的情况下,该步骤可以被修改或省略。在这种实施方式中,(从供应源468、从样本端口460或另一端口或储器提供的)流体可以省略核酸扩增试剂,其中,流体释放核酸并将核酸携带到扩增区域480中,在那里,流体然后与冷冻干燥的核酸扩增试剂混合。流体(无论是包含核酸扩增试剂还是省略核酸扩增试剂)的体积被控制,以便基本上并且在一个实施方式中完全地填装(prime)扩增区域480,而不打开或破坏跨过毛细间断部486的弯月面。
当核酸扩增试剂在制备区530中与所释放的核酸混合时,如根据来自传感器431的信号确定的,控制器572输出控制信号,从而致动毛细间断部开启器452。在一个实施方式中,控制器572输出控制信号,从而致动流体致动器,以便破坏跨过每个毛细间断部550的弯月面,从而促进包含核酸扩增试剂和核酸的流体混合物流入扩增区域580中。在一个实施方式中,样本制备区域制备区530用流体回填,例如用水回填,以进一步抑制热循环期间的蒸发。
当混合核酸扩增试剂(无论来自供应源468和/或来自冷冻干燥的试剂499)时,控制器572可输出这样的控制信号,从而导致加热器482热循环扩增区域580内的流体混合物。在一些实施方式中,控制器572可以与位于每个扩增区域580内的至少一个传感器433通信,该传感器433向控制器572指示扩增区域580中的流体混合物的存在、其扩增状态和/或流体混合物的当前温度。在这种热循环期间,由于存在非常少的排气端口,所以减少了来自扩增区域580的蒸发。跨过毛细间断部584的弯月面减少了通过排气口484的蒸发,而在扩增区域480的填装后重新建立的跨过毛细间断部550的弯月面减少了通过喷口52的蒸发。
当完成热循环时,感测或检测目标核酸的存在和量(如果有的话)。在一个实施方式中,微流体芯片422包括窗口或透明部分,其促进光学感测或检测扩增区域580内的目标核酸。由扩增器520进行的扩增可用于促进核酸的分离或定量。这种扩增可在诸如遗传测试、组织分型、传染病鉴定、遗传指纹识别和个人定制治疗方案的开发、法医分析、食品安全、环境测试等领域中提供益处。
图7示意性地示出了示例性核酸扩增器620的一些部分。扩增器620类似于上述扩增器520,除了扩增器620包括样本纯化/制备区630。扩增器620的与扩增器520或扩增器420的部件相对应的那些其余部件被类似地编号。
样本纯化/制备区630包括微流体芯片422的区域,在该区域中将目标核酸与通过样本供应源460引入的样本的其余非核酸部分分开或分离。在所示的示例中,区630包括长形缝槽533、一系列u形微流体通路635、核酸分离器674和细胞裂解器537。缝槽533连接到样本供应源460、洗涤流体供应源464和核酸扩增试剂供应源468。每个微流体通路635的两个端部均连接到缝槽533,其中,第一端部容纳至少一个细胞裂解器537并且第二相对端部容纳流体喷射器434。
核酸分离器674分离器将核酸与稀释样本的非核酸部分分离。在一个实施方式中,核酸分离器674包括核酸吸附珠476(其一部分示意性地示出)和吸附珠保持器678。核酸吸附珠476由材料形成或被涂覆,使得目标核酸吸附到珠476。核酸吸附珠476可以在添加稀释样本之前存在于区630内,或者可以在将稀释样本引入区630之前被添加到稀释样本。核酸吸附珠476由保持器578保持在缝槽533中。
核酸吸附珠保持器678抑制珠476(和所吸附的目标核酸)从缝槽533行进到容纳流体喷射器434的微流体通路635。在所示的示例中,保持器578包括在通路535内邻近缝槽533的支柱或柱。在其它实施方式中,保持器478可以包括其它形式的过滤器,其阻挡珠476通过,同时允许包含非核酸部分的流体从其穿过行进到通路635。
在其它实施方式中,核酸分离器674可以具有其他形式。例如,在其它实施方式中,核酸分离器674可以包括吸附目标核酸的网或其它过滤材料。在其它实施方式中,核酸分离器可以包括嵌入膜。在一些实施方式中,例如在稀释样本包括很少的细菌使得核酸可以通过蒸发被浓缩的情况下,可以省略核酸分离器674。
流体喷射器434分配或喷射稀释样本的与目标核酸分离的非核酸部分。流体喷射器434存在于通路635的端部。每个流体喷射器434包括喷口52和流体致动器54(如上所述)。
细胞裂解器537包括由微流体芯片422支撑的部件,其用于裂解通过样本供应源460引入的样本内所包含的细胞。细胞裂解器537将热和/或搅拌施加到裂解物细胞。在所示的示例中,细胞裂解器537包括搅动流体的流体致动器。在一个实施方式中,细胞裂解器537包括热阻流体致动器,其搅动以及加热流体以裂解样本的细胞。形成细胞裂解器537的流体致动器沿着通路635中的每一个顺序地或相继地定位。如图6所示,细胞裂解器的数量可以变化。沿着每个通路635顺序地定位的多个细胞裂解器537促进细胞的分阶段裂解,其中,沿着每个单独的通路635的不同细胞裂解器可以具有不同的特性或者可以由控制器572以不同的方式致动,这取决于沿着每个通路635的串列中的单独细胞裂解器的相对位置。在一个实施方式中,细胞裂解器被同时致动或激发。在另一个实施方式中,细胞裂解器被顺序地致动或激发。
细胞制备区630促进样本从缝槽533通过通路635并回到缝槽533的循环。当流体样本循环通过这样的通路635时,流体样本可以经历由细胞裂解器537进行的重复的裂解循环。同时,吸附珠476被保持在缝槽533内,在发生细胞裂解的区域之外。一旦流体样本和细胞已经充分经历裂解,控制器572就可以致动流体喷射器4342喷射样本的非核酸部分。在已经用洗涤流体清洁了样本制备区630之后,控制器572可以供应核酸扩增试剂流体,以便与经分离和经浓缩的核酸混合。此后,控制器572可以致动毛细间断部开启器552以开启毛细间断部550,使得核酸扩增试剂流体和所携带的核酸流入扩增区540中以用于如上所述的扩增。如上所述,在一些实施方式中,在细胞裂解器537也用作毛细间断部开启器的情况下,可以省略毛细间断部开启器552。
图8示意性地示出了示例性核酸扩增器720的一些部分。核酸扩增器720类似于核酸扩增器520,除了核酸扩增器720包括样本纯化/制备区730。扩增器720的与扩增器520的部件相对应的那些其余部件被类似地编号。
样本纯化/制备区730包括微流体芯片422的区域,在该区域中将目标核酸与通过样本供应源460引入的样本的其余非核酸部分分开或分离。在所示的示例中,区730包括长形缝槽533、一系列u形微流体通路635、流体喷射通路737、核酸分离器774和细胞裂解器537(如上所述)。缝槽533连接到样本供应源460、洗涤流体供应源464和核酸扩增试剂供应源468。每个微流体通路635的两个端部均连接到缝槽533。流体喷射通路737从通路635分支并具有终端或盲端。流体喷射通路737提供流体可被喷射到通路635所提供的再循环路径之外的区域。
核酸分离器774将核酸与稀释样本的非核酸部分分开或分离。在一个实施方式中,核酸分离器774包括核酸吸附珠476(其一部分示意性地示出)和吸附珠保持器778。核酸吸附珠476由材料形成或被涂覆,使得目标核酸吸附到珠476。核酸吸附珠476可以在添加稀释样本之前存在于区730内,或者可以在将稀释样本引入区730之前被添加到稀释样本。核酸吸附珠476由保持器778和毛细间断部550的收缩区域保持在缝槽533和/或通路635中。
核酸吸附珠保持器778抑制珠476(和所吸附的目标核酸)从区730行进到流体喷射器434。在所示的示例中,保持器778包括在通路737内或在通路737和635的汇合处的支柱或柱,位于通路635的部分和流体喷射器434之间,所述流体喷射器434定位在通路737内。在其它实施方式中,保持器478可以包括其它形式的过滤器,其阻挡珠476通过,同时允许包含非核酸部分的流体从其穿过行进到流体喷射器434。
在其它实施方式中,核酸分离器774可以具有其他形式。例如,在其它实施方式中,核酸分离器774可以包括在缝槽533或通路635内吸附目标核酸的网或其它过滤材料。在其它实施方式中,核酸分离器可以包括嵌入膜。在一些实施方式中,例如在稀释样本包括很少的细菌使得核酸可以通过蒸发被浓缩的情况下,可以省略核酸分离器574。
流体喷射器434分配器喷射稀释样本的与目标核酸分离的非核酸部分。流体喷射器434存在于通路737的端部,而保持器778定位在流体喷射器434和通路635之间。每个流体喷射器434包括喷口52和流体致动器54(如上所述)。
样本制备区730促进样本从缝槽533通过通路635并回到缝槽533的循环。当流体样本循环通过这样的通路635时,流体样本可以经历由细胞裂解器537进行的重复的裂解循环。同时,吸附珠476被保持在缝槽533和通路635内。一旦流体样本和细胞已经充分经历裂解,控制器572就可以致动流体喷射器434以喷射样本的非核酸部分。在已经用洗涤流体清洁了样本制备区730之后,控制器572可以供应核酸扩增试剂流体,以便与经分离和经浓缩的核酸混合。此后,控制器572可以致动毛细间断部开启器552以开启毛细间断部550,使得核酸扩增试剂流体和所携带的核酸流入扩增区540中以用于如上所述的加热和扩增。如上所述,在一些实施方式中,在细胞裂解器537也用作毛细间断部开启器的情况下,可以省略毛细间断部开启器552。
图9示意性地示出了示例性核酸扩增器820的一些部分。扩增器820类似于上述扩增器620,除了扩增器820包括样本纯化/制备区830。扩增器820的与扩增器620或其它公开的扩增器的部件相对应的那些其余部件被类似地编号。
样本纯化/制备区830包括微流体芯片422的区域,在该区域中将目标核酸与通过样本供应源460引入的样本的其余非核酸部分分开或分离。在所示的示例中,区830包括长形缝槽533、一系列u形微流体通路635、流体喷射通路837、核酸分离器874和细胞裂解器537。缝槽533连接到样本供应源460、洗涤流体供应源464和核酸扩增试剂供应源468。每个微流体通路635的两个端部均连接到缝槽533。
流体喷射通路837在缝槽533的与通路635相对的一侧上从缝槽533延伸。流体喷射通路837提供了流体可以被喷射到由通路635提供的再循环路径之外的区域。流体喷射通路837容纳流体喷射器434。因为流体喷射通路837沿着缝槽533的相对侧延伸,所以流体通路837和位于其内的流体喷射器434被进一步分离并且相对于核酸扩增区540远程定位以进一步减少在区540中的热循环期间可能发生的蒸发。
核酸分离器874将核酸与稀释样本的非核酸部分分开或分离。在一个实施方式中,核酸分离器874包括核酸吸附珠476(其一部分示意性地示出)和吸附珠保持器878。核酸吸附珠476由材料形成或被涂覆,使得目标核酸吸附到珠476。核酸吸附珠476可以在添加稀释样本之前存在于区730内,或者可以在将稀释样本引入区830之前被添加到稀释样本。核酸吸附珠476由保持器878保持在缝槽533中。
核酸吸附珠保持器878抑制珠476(和所吸附的目标核酸)从缝槽533行进到流体喷射器434。在所示的示例中,保持器878包括在缝槽533内,位于缝槽533和流体喷射器434之间,例如在通路837内、在缝槽533内或在通路837和缝槽533的汇合处的支柱或柱。在其它实施方式中,保持器478可以包括其它形式的过滤器,其阻挡珠476通过,同时允许包含非核酸部分的流体从其穿过行进到流体喷射器434。
在其它实施方式中,核酸分离器774可以具有其他形式。例如,在其它实施方式中,核酸分离器874可以包括在缝槽533内吸附目标核酸的网或其它过滤材料。在其它实施方式中,核酸分离器可以包括嵌入膜。在一些实施方式中,例如在稀释样本包括很少的细菌使得核酸可以通过蒸发被浓缩的情况下,可以省略核酸分离器874。
流体喷射器434分配器喷射稀释样本的与目标核酸分离的非核酸部分。流体喷射器434存在于通路837的端部,而保持器778定位在流体喷射器434和缝槽533之间。每个流体喷射器434包括喷口52和流体致动器54(如上所述)。
样本制备区730促进样本从缝槽533通过通路635并回到缝槽533的循环。当流体样本循环通过这样的通路635时,流体样本可以经历由细胞裂解器537进行的重复的裂解循环。同时,吸附珠476被保持在缝槽533。一旦流体样本和细胞已经充分经历裂解,控制器572就可以致动流体喷射器434以喷射样本的非核酸部分。在已经用洗涤流体清洁了样本制备区830之后,控制器572可以供应核酸扩增试剂流体,以便与经分离和经浓缩的核酸混合。此后,控制器572可以致动毛细间断部开启器552以开启毛细间断部550,使得核酸扩增试剂流体和所携带的核酸流入扩增区540中以用于如上所述的加热和扩增。如上所述,在一些实施方式中,在细胞裂解器537也用作毛细间断部开启器的情况下,可以省略毛细间断部开启器552。
尽管已经参考示例性实施方式描述了本公开,但是本领域技术人员将会认识到,在不脱离所要求保护的主题的精神和范围的情况下,可以在形式和细节上进行改变。例如,尽管不同的示例性实施方式可能已经被描述为包括提供一个或多个益处的一个或多个特征,但是可以设想,所描述的特征可以彼此互换,或者在所描述的示例性实施方式中或在其他替代实施方式中替代地彼此组合。因为本公开的技术相对复杂,所以并非技术中的所有变化都是可预见的。参考示例性实施方式描述并在以下权利要求中阐述的本公开显然旨在尽可能宽泛。例如,除非另外特别指出,否则引用单个特定元件的权利要求也涵盖了多个这样的特定元件。权利要求中的术语“第一”、“第二”、“第三”等仅区分不同的元件,并且除非另有说明,不与本公开中元件的特定顺序或特定编号特别相关联。
- 还没有人留言评论。精彩留言会获得点赞!