一种光控调节细胞膜次氯酸根荧光探针及其制备方法和应用与流程
本发明涉及一种光控调节细胞膜次氯酸根荧光探针及其制备方法和应用,属于有机荧光探针技术领域。
背景技术:
次氯酸根作为生物体内重要的活性氧化物(ROS)参与生物体内各种生命活动,对人体的动态平衡具有重要的作用。生物体内的次氯酸是由H2O2和Cl-在髓过氧物酶(MPO)的催化下生成的。次氯酸根含量与各种疾病息息相关。过量的次氯酸会引起各种组织损伤、心血管疾病、关节炎、癌症和肺损伤等疾病。鉴于次氯酸的重要性,检测生命体内次氯酸的含量变化已经成为众多科研工作者的研究课题。
细胞膜细胞膜主要由酯类(占化学组成的50%)、蛋自质(42%)和糖类 (2%-8%)组成。是细胞内外分别的界限和细胞的门户,控制各种蛋白、阴离子、阳离子、氨基酸等的进出,从而保持细胞内的动态平衡和正常的生命活动。
鉴于细胞膜和次氯酸根的重要性,对于检测细胞膜上的次氯酸根是一个重要的课题和挑战。细胞膜上探针和次氯酸根探针都已经有了报道,细胞膜探针,比如检测Ca2+,蛋白、脂筏等,关于次氯酸根探针的文献更是不计其数,但是都不能够做到精确检测细胞上的次氯酸根,受到来自于非细胞膜上的次氯酸根的干扰,从而不具有说服力。所以,设计一种精确检测细胞膜上次氯酸根的荧光探针是十分有必要的。
技术实现要素:
本发明解决的技术问题是:本发明提供一种可定位细胞膜,并通过光调控精确检测细胞膜次氯酸根的荧光探针及其制备方法和应用。
为了解决上述技术问题,本发明提出的技术方案是:一种光控调节细胞膜次氯酸根荧光探针,所述荧光探针为HOCMem荧光探针,结构式如式(Ⅰ)所示:
为了解决上述技术问题,本发明提出的另一技术方案是:所述的HOCMem 荧光探针的制备方法包括如下步骤:将荧光素衍生物、三乙胺和苯甲酰氯冰浴条件下依次加入到二氯甲烷溶液中,过夜反应,然后萃取、旋干除去溶剂,通过硅胶柱层析方法提纯目标产物HOCMem。
优选的,所述荧光素衍生化合物的制备方法如下:
(1)荧光素、胆固醇甲酰氯和三乙胺溶解在DMF中,室温搅拌过夜,萃取,旋干,柱层析得到靶向荧光素;
(2)靶向荧光素溶解在甲醇中,滴加水合肼,回流过夜,旋干、硅胶柱层析得到靶向荧光素酰肼;
(3)靶向荧光素酰肼,4,5-二甲氧基-2-硝基苯,碳酸铯溶解在无水DMF中,室温反应过夜,过滤、萃取旋干,柱层析得到荧光素衍生物。
优选的,所述步骤(1),荧光素与胆固醇甲酰氯的物质的量比为1:1。
优选的,步骤(2),靶向荧光素与水合肼的物质的量比为1:1.2–1:2,后处理直接旋干柱层析,不需要萃取。
优选的,步骤(3),靶向荧光素酰肼与苯甲酰氯的物质的量比为1:1.2–1: 2,在冰浴条件下滴加苯甲酰氯,然后在25℃下反应过夜。
为了解决上述技术问题,本发明提出的另一技术方案是:所述的HOCMem 荧光探针用于非疾病治疗和诊断的在生理体系中定位检测细胞膜上的次氯酸根离子的应用。
优选的,定位检测细胞膜上的次氯酸根离子而避免来自非细胞膜次氯酸根离子的干扰。
有益效果:
(1)所述步骤(2)靶向荧光素与水合肼的物质的量比为1:1.2–1:2,后处理直接旋干柱层析,不需要萃取,不然难以分层,造成大量的产物损失。
(2)所述步骤(3)靶向荧光素酰肼与苯甲酰氯的物质的量比为1:1.2–1: 2,一定要在冰浴条件下滴加苯甲酰氯,然后在25℃下反应过夜,不然会出现很多副产物,影响产物的产率和提纯。
(3)本发明的精确检测细胞膜次氯酸根HOCMem荧光探针具有很好的生物相容性,次氯酸根的高选择性,对细胞无毒副作用。
(4)本发明荧光探针具有很好的靶向性,成功定位细胞膜。共聚焦显微成像显示靶向和商业化细胞膜染料具有很高的重合度,高达91%。
(5)本发明荧光探针只检测细胞膜上的次氯酸根,避免了非细胞膜上的次氯酸根的干扰。
附图说明
下面结合附图对本发明的作进一步说明。
图1是实施案例1制备的HOCMem(5μM)在光照60秒后对不同次氯酸根浓度的EtOH:H2O=1:1溶液中的不同响应时间的荧光光谱图。
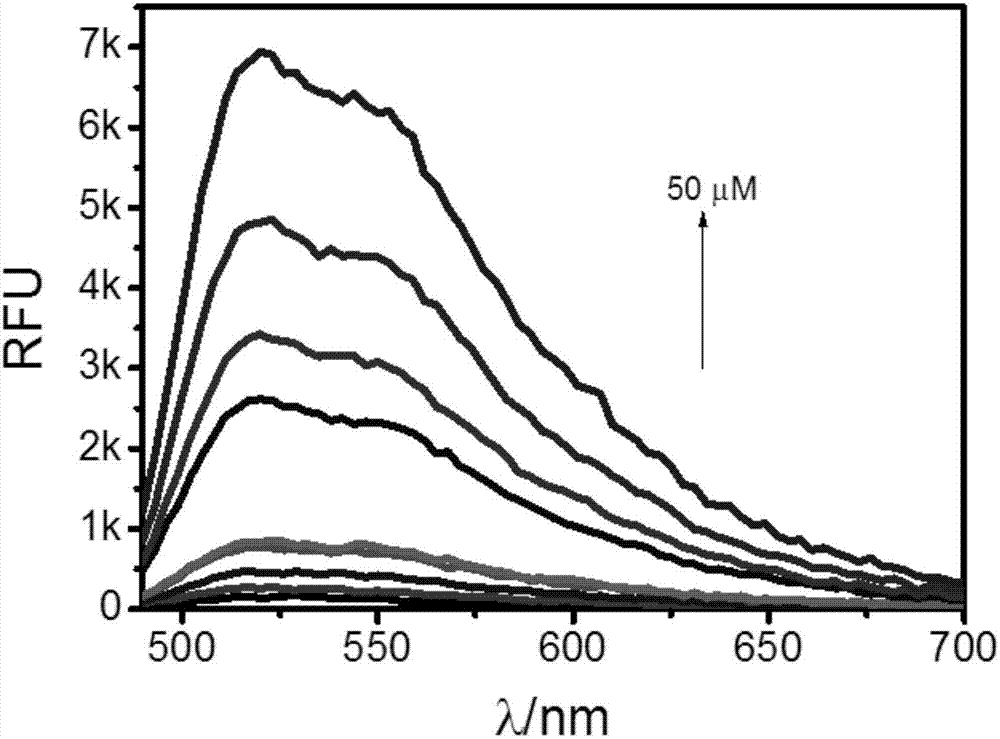
图2是实施案例1制备的HOCMem(10μM)在光照60秒后不同次氯酸根浓度的EtOH:H2O=1:1溶液的荧光光谱图。
图3是实施案例1制备的HOCMem(10μM)在光照60秒后对100um的各种离子响应的荧光光谱图。
图4是实施案例1制备的HOCMem(10μM)在光照5min后细胞中的共聚焦显微成像。
具体实施方式
实施例1
通过光调控精确检细胞膜次氯酸根的荧光探针的制备方法如下:
(1)将三乙胺(0.5mL)、荧光素(1g)和胆固醇甲酰氯(1.35g)加入100mL 烧瓶中,反应溶剂为在DMF(40mL),反应在冰浴中搅拌7小时。等反应结束后,进行萃取,干燥,过滤。旋蒸除去有机溶剂,通过柱层析纯化。1H NMR(300 MHz,CDCl3):δ=8.03(d,J=3Hz,1H),7.63(m,2H),7.1 6(m,2H),6.67 (m,5H),5.43(s,1H),4.62(dd,J1=4.5Hz,J2=3Hz,1H),2.51(d,J=3Hz,2H),2.23(m,1H),1.84(m,6H),1.51(m,6H),0.94(m,25H),0.69(s,3H)。13CNMR(75MHz,CDCl3):δ=170.15,158.51,153.15,152.79,152.36,152.27,152.03,139.11,135.44,130.05,129.23,126.51,125.26,124.18,123.51,116.95, 11.6.85,112.91,110.48,110.06,103.29,79.66,56.83,56.31,50.15,42.47, 39.86,39.66,38.02,36.95,39.69,36.34,35.92,32.05,31.99,31.64,29.82, 28.35,28.14,27.75,24.42,23.98,22.94,22.69,21.20,19.40,18.86,12.00。
(2)将靶向荧光素(1.0g,1.3mmol)在甲醇(50mL)中的溶液在干燥的氮气气氛下在干燥的250mL烧瓶中搅拌。随后在剧烈搅拌下,10分钟滴注4.0mL 肼水合物(80%)。然后将反应物加热至86℃并在该温度下继续进行。将混合物溶液冷却至室温。在减压下除去有机溶液的溶剂,柱层析纯化。1H NMR(300 MHz,CDCl3):δ(ppm):7.95(t,J=3Hz,1H),7.81(s,1H),7.48(t,J=3Hz, 2H),7.11(m,1H),6.82(dd,J1=4.5Hz,J2=1.5Hz,1H),6.70(dd,J1=4.5Hz, J2=0.9Hz,2H),6.50(m,2H),5.42(d,J=1.5Hz,1H),4.60(dd,J1=6Hz, J2=3Hz,Hz,1H),3.69(bs,NH2),2.49(dd,J1=10.5Hz,J2=4.5Hz,2H), 1.97(m,7H),1.45(m,11H),0.98(m,20H),0.69(s,3H).13CNMR(300MHz, CDCl3):δ(ppm):166.94,158.22,153.03,152.89,152.81,151.80,150.89,139.13, 133.33,129.33,129.07,128.44,128.26,124.04,123.54,123.48,116.96,116.28, 112.93,110.20,109.30,103.63,79.55,65.75,56.83,56.32,50.14,42.47, 39.87,39.66,38.02,36.95,36.69,36.33,35.92,32.05,31.99,28.35,28.13, 27.74,24.42,23.98,22.93,22.69,21.02,19.40,18.86,12.00。
(3)在干燥氮气氛围下,靶向荧光素酰肼(300mg),Cs2CO3(350mg)和 1-(1-溴乙基)-4,5-二甲氧基-2-硝基苯(100mg)溶解在无水DMF(15ml)溶液中。室温反应搅拌过夜,等反应停止后,进行萃取,无水硫酸钠干燥,过滤。旋蒸把有机溶剂除尽,柱层析纯化。1H NMR(300MHz,CDCl3):δ(ppm):7.91(t, J=4.2Hz,1H),7.66(s,1H),7.45(t,J=3.2Hz,2H),7.01(m,3H),6.78(d, J=2.3Hz,1H),6.52(m,2H),6.46(m,2H),6.15(d,J=4.2Hz,1H),5.39(t, J=11.4Hz 1H),4.55(m,1H),.387(m,6H),3.70(s,2H),2.47(s,2H),1.83 (m,4H),1.47(m,3H),1.51(m,5H),1.35(s,9H),1.07(m,11H),0.87(m, 9H),0.67(m,3H)。13CNMR(300MHz,CDCl3):δ(ppm):166.38,166.31,158.46, 152.58,150.44,148.12,139.50,139.46,139.04,134.10,132.93,128.10,123.83, 123.31,123.25,116.82,116.40111.14,108.22,108.00,103.20,103.12,79.20, 72.12,56.69,56.39,56.31,56.16,50.00,42.31,39.71,39.50,37.87,36.80, 36.54,36.18,36.75,31.84,27.58,23.81,23.39,23.36,22.78,22.63,21.04, 19.24,18.71,11.84。
(4)本发明的制备精确检测细胞膜次氯酸根的荧光探针反应式如下::
将荧光素衍生物(100mg)和三乙胺(0.5mL)加入到烧瓶中,加入二氯甲烷(5mL)使其完全溶解,将混合物在干燥氮气氛下搅拌3分钟。将苯甲酰氯(100 mg)的DCM(1.5mL)溶液滴加到溶液中。混合物在室温下搅拌6小时。加入饱和氯化铵水溶液(80mL)。将混合物进一步用乙酸乙酯(50mL)萃取。用无水Na2SO4干燥,过滤。在减压下除去溶剂柱层析纯化。1H NMR(300MHz, CDCl3):δ(ppm):8.10(dd,J1=18Hz,J2=9Hz,2H),7.62(m,2H),7.48(t, J=5.5Hz,1H),7.32(m,3H),7.14(m,5H),7.02(t,J=1.5Hz,1H),6.48(dd, J1=8Hz,J2=6Hz,3H),6.15(t,J=7.5Hz,1H),5.42(s,1H),4.58(s,1H), 3.86(t,J=22.6Hz,6H),2.49(s,2H),2.01(m,4H),1.67(m,3H),1.51(m, 6H),1.27(m,11H),0.91(m,9H),0.69(s,3H)。13CNMR(300MHz,CDCl3):δ(ppm):158.73,154.18,153.81,153.37,153.25,152.25,151.99,151.91, 149.09,148.85,139.03,134.97,134.02,131.84,131.70,131.69,130.86,130.14, 129.37,128.47,128.07,127.02,127.67,124.66,124.07,123.36,116.48,115.77, 112.45,112.14,109.27,108.16,108.05,102.14,101.98,79.17,71.94,56.67, 56.37,56.13,49.99,42.30,39.69,39.48,37.87,36.79,36.53,36.16,35.74, 31.82,31.39,29.64,28.17,27.96,27.68,24.24,23.79,23.35,23.25,22.76, 22.51,21.03,19.23,18.69,11.83。
实施例2
一种光控调节细胞膜次氯酸根探针对次氯酸根的响应光谱测试。
(1)HOCMem荧光探针对不同次氯酸根浓度的不同时间的荧光响应曲线 (图1)
首先配置EtOH:H2O=1:1,pH=7的溶液,将探针母液用EtOH:H2O=1:1的溶液稀释到10μM,光照60s,分别加入1-5当量的次氯酸根,用酶标仪测试荧光,得到HOCMem荧光探针对不同次氯酸根浓度的不同时间的荧光曲线。
(2)HOCMem荧光探针浓度对不同次氯酸根浓度的荧光光谱图(图2)
配置5μM HOCMem荧光探针,光照60s,分别加入8,16,32,100μM的次氯酸根溶液,用酶标仪测试。得到HOCMem荧光探针对不同次氯酸根浓度的荧光曲线。
(3)HOCMem荧光探针浓度对不同离子的荧光光谱图(图3)
配置10μM HOCMem的荧光探针,光照60s,分别加入10倍当量的不同离子,用酶标仪测试荧光,得到HOCMem荧光探针浓度对不同离子的荧光光谱图。
(4)HOCMem荧光探针在细胞膜上的共聚焦显微成像(图4)
向含有Hela细胞的培养皿中加HOCMem荧光探针,与细胞培养液混合均匀后,染色1个小时,用pH=7.35的缓冲溶液冲洗3次,将该培养皿在共聚焦显微镜下成像,取出培养皿,UV光照5分钟后,静置1个小时,再次将该培养皿在共聚焦显微镜下成像。
本发明的不局限于上述实施例所述的具体技术方案,凡采用等同替换形成的技术方案均为本发明要求的保护范围。
- 还没有人留言评论。精彩留言会获得点赞!