一组用于检测眼内液中EB病毒的LAMP引物及应用的制作方法
本发明涉及生物技术领域中,一组用于检测眼内液中eb病毒的lamp引物及应用。
背景技术:
eb病毒(epstein-barrvirus,ebv),又称人类疱疹病毒4型(humanherpesvirus4,hhv-4),它是一种γ亚科嗜淋巴细胞病毒属的dna致病病毒,具有在体内外专一性的感染人类及某些灵长类b细胞的生物学特性。主要通过唾液传播,无症状感染多发生在幼儿,3~5岁幼儿90%以上曾感染eb病毒,90%以上的成人体内都有病毒抗体。随着抗生素和激素类药物的广泛应用,病毒性眼内炎症越来越常见于眼科临床,且上升为主要致盲眼疾之一。
目前临床针对病毒的检测方法主要是分离培养和血清学诊断。这些检测方法繁琐,检测时间长,灵敏度低,容易发生漏检和错检,无法满足快速检测的要求。近几年发展起来的分子检测技术,特别是pcr技术,在微生物快速鉴定和检测方面的应用,为病毒的快速检测开辟了新的途径。但是,pcr存在检测时间长、易污染、假阳性率高的缺点,使其应用受到限制。环介导等温扩增技术(loop-mediatedisothermalamplification,lamp)是近年来发展出的一种敏感、特异、简便、快捷的核酸扩增技术,其原理是在一种具有链置换活性的dna聚合酶的作用下,识别6-8个区域的4-6条引物,在等温条件下快速、特异地扩增目的基因,可推广应用于快速、准确的检测病毒。
技术实现要素:
本发明的目的是提供一组用于检测眼内液中eb病毒的lamp引物组及应用。
本发明提供的lamp引物组,由引物f3-1、引物b3-1、引物fip-1、引物bip-1、引物lf-1和引物lb-1组成;
所述引物f3-1为如下(a1)或(a2):
(a1)序列表的序列1所示的单链dna分子;
(a2)将序列1经过一个或几个核苷酸的取代和/或缺失和/或添加且与序列1具有相同功能的单链dna分子;
所述引物b3-1为如下(a3)或(a4):
(a3)序列表的序列2所示的单链dna分子;
(a4)将序列2经过一个或几个核苷酸的取代和/或缺失和/或添加且与序列2具有相同功能的单链dna分子;
所述引物fip-1为如下(a5)或(a6):
(a5)序列表的序列3所示的单链dna分子;
(a6)将序列3经过一个或几个核苷酸的取代和/或缺失和/或添加且与序列3具有相同功能的单链dna分子;
所述引物bip-1为如下(a7)或(a8):
(a7)序列表的序列4所示的单链dna分子;
(a8)将序列4经过一个或几个核苷酸的取代和/或缺失和/或添加且与序列4具有相同功能的单链dna分子;
所述引物lf-1为如下(a9)或(a10):
(a9)序列表的序列5所示的单链dna分子;
(a10)将序列5经过一个或几个核苷酸的取代和/或缺失和/或添加且与序列5具有相同功能的单链dna分子;
所述引物lb-1为如下(a11)或(a12):
(a11)序列表的序列6所示的单链dna分子;
(a12)将序列6经过一个或几个核苷酸的取代和/或缺失和/或添加且与序列6具有相同功能的单链dna分子。
所述引物组中,所述引物f3-1、所述引物b3-1、所述引物fip-1、所述引物bip-1、所述引物lf-1和所述引物lb-1的摩尔比可为0.5:0.5:2:2:1:1。
本发明还保护所述引物组的应用,所述应用为如下(b1)至(b6)中的任意一种:
(b1)在鉴别eb病毒中的应用;
(b2)在制备用于鉴别eb病毒的试剂盒中的应用;
(b3)在鉴定待测细菌是否为eb病毒中的应用;
(b4)在制备用于鉴定待测细菌是否为eb病毒的试剂盒中的应用;
(b5)在鉴定待测样本是否含有eb病毒中的应用;
(b6)在制备用于鉴定待测样本是否含有eb病毒的试剂盒中的应用。
上述应用,所述待测样本可为眼部临床样本培养物、眼液体或抽吸物。
本发明还保护含有所述引物组的试剂盒;所述试剂盒的用途为如下(c1)或(c2)或(c3):
(c1)鉴别eb病毒;
(c2)鉴定待测细菌是否为eb病毒;
(c3)鉴定待测样本是否含有eb病毒。
所述试剂盒还可包括lamp反应体系中非引物外的其他试剂。
上述试剂盒中,所述待测样本可为眼部临床样本培养物、眼液体或抽吸物。
本发明还保护所述试剂盒在如下(c1)或(c2)或(c3)中的应用:
(c1)鉴别eb病毒;
(c2)鉴定待测细菌是否为eb病毒;
(c3)鉴定待测样本是否含有eb病毒。
上述应用,所述待测样本可为眼部临床样本培养物、眼液体或抽吸物。
本发明还保护所述引物组的制备方法,所述方法包括将各条引物分别独立包装。
本发明还保护所述试剂盒的制备方法,所述方法包括将所述引物组的的各条引物分别独立包装。
本发明中,在利用所述引物组或所述试剂盒鉴别eb病毒时,可按照包括如下步骤的方法进行:
(1)提取待测样本的基因组dna;
(2)以步骤(1)得到的基因组dna为模板,采用所述引物组或所述试剂盒进行lamp扩增反应,然后进行如下判断:
如果可以实现以所述基因组dna为模板的特异性扩增,所述待测样本为或候选为eb病毒;
如果不可以实现以所述基因组dna为模板的特异性扩增,所述待测样本不为或候选不为eb病毒。
在利用所述引物组或所述试剂盒鉴定待测细菌是否为eb病毒时,可按照包括如下步骤的方法进行:
(1)提取待测细菌的基因组dna;
(2)以步骤(1)得到的基因组dna为模板,采用所述引物组或所述试剂盒进行lamp扩增反应,然后进行如下判断:
如果可以实现以所述基因组dna为模板的特异性扩增,所述待测细菌为或候选为eb病毒;
如果不可以实现以所述基因组dna为模板的特异性扩增,所述待测细菌不为或候选不为eb病毒。
在利用所述引物组或所述试剂盒鉴定待测样本是否含有eb病毒时,可按照包括如下步骤的方法进行:
(1)提取待测样本的基因组dna;
(2)以步骤(1)得到的基因组dna为模板,采用所述引物组或所述试剂盒进行lamp扩增反应,然后进行如下判断:
如果可以实现以所述基因组dna为模板的特异性扩增,所述待测样本含有或候选含有eb病毒;
如果不可以实现以所述基因组dna为模板的特异性扩增,所述待测样本不含有或候选不含有eb病毒。
上文中,具体可通过如下方法判断“阳性扩增”:用荧光pcr仪检测荧光信号,如果出现阳性扩增曲线则为阳性扩增。所述阳性扩增曲线具体可为s型扩增曲线。
以上任一所述采用引物组进行lamp扩增的反应体系中,所述引物组中各引物的浓度为:0.5μm所述引物f3-1、0.5μm所述引物b3-1、2μm所述引物fip-1、2μm所述引物bip-1、1μm所述引物lf-1、1μm所述引物lb-1。
以上任一所述采用引物组进行lamp扩增的反应体系的10μl反应体系中可含有1μl10×thermopolbuffer,0.8m甜菜碱,0.5mg/mlbsa,4mmmgso4,0.3μl20×evagreen,1.5mmdntps,0.32u/mlbstdna聚合酶大片段,1μl所述引物组溶液,50pg-50ng模板dna,余量为水。其中,10×thermopolbuffer可为thermo产品,20×evagreen可为合肥博美生物科技有限责任公司产品。
以上任一所述lamp扩增的反应程序具体可为:65℃恒温50min。反应过程中,采用荧光pcr仪检测荧光信号。
本发明提供了一组用于检测眼内液中eb病毒的lamp引物组及应用。本发明所述的lamp引物组包括外引物f3和b3,内引物fip和bip以及环引物lf和lb,在检测eb病毒时具有高特异性和高灵敏度。应用本发明的lamp引物组及方法,可快速、准确的检测出eb病毒。
附图说明
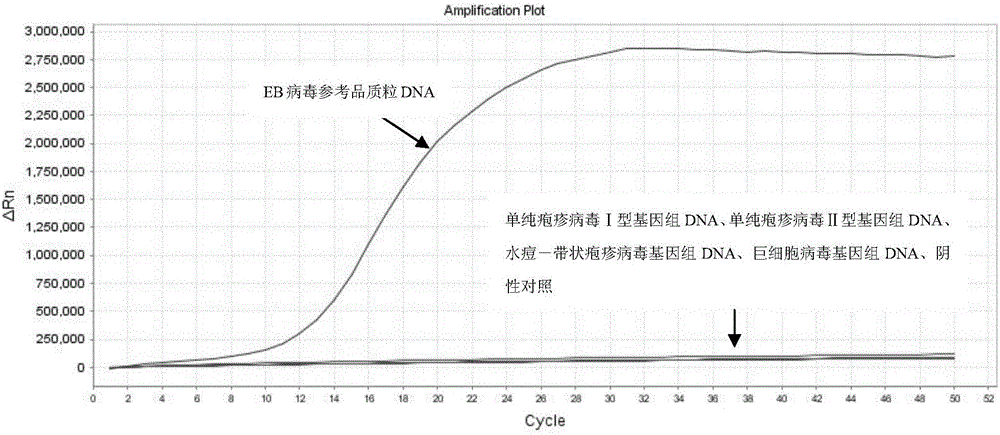
图1为实施例3的lamp扩增曲线图。
图2为实施例5的lamp扩增曲线图。
具体实施方式
以下的实施例便于更好地理解本发明,但并不限定本发明。下述实施例中的实验方法,如无特殊说明,均为常规方法。下述实施例中所用的试验材料,如无特殊说明,均为自常规生化试剂商店购买得到的。以下实施例中的定量试验,均设置三次重复实验,结果取平均值。
pgem-teasyvector载体:promega公司,产品货号a1360。
实施例1、鉴定eb病毒的引物组制备
进行大量序列分析、比对获得了用于鉴定eb病毒的若干引物。将各个引物进行预实验,比较灵敏度、特异性等性能,最终得到用于鉴定eb病毒的lamp引物组。
用于鉴定eb病毒的引物组,包括2条外引物(f3-1、b3-1),2条内引物(fip-1、bip-1)和2条环引物(lf-1、lb-1),各条引物序列如下所示(5’→3’):
引物f3-1(序列表的序列1):gttcgcgttgctaggcc;
引物b3-1(序列表的序列2):aaggggaaaagttagaaactg;
引物fip-1(序列表的序列3):ataccaggggcagtggtccctctcagtccagcgcgttta;
引物bip-1(序列表的序列4):gtcctgcagctatttctggtcgctagggagaggtagaagac;
引物lf-1(序列表的序列5):ggctgctgtctggcttacg;
引物lb-1(序列表的序列6):atcagagcgccaggagtc。
该引物组中,引物f3-1、引物b3-1、引物fip-1、引物bip-1、引物lf-1和引物lb-1的摩尔比为0.5:0.5:2:2:1:1,各引物均独立包装。
实施例2、检测方法建立
利用实施例1的鉴定eb病毒的引物组检测eb病毒的方法包括:
1、提取待测病毒的基因组dna或提取待测生物样本的总dna。
2、取步骤1得到的总dna,作为模板,采用实施例1中制备的引物组进行lamp扩增。
10μllamp扩增的反应体系包括:1μl10×thermopolbuffer(thermo),0.8m甜菜碱,0.5mg/mlbsa,4mmmgso4,0.3μl20×evagreen(合肥博美生物科技有限责任公司),1.5mmdntps,0.32u/mlbstdna聚合酶大片段,引物混合物(f3-1、b3-1、fip-1、bip-1、lf-1和lb-1的混合物),2ng模板dna,余量为ddh2o。反应体系中各引物的浓度如下:0.5μmf3-1、0.5μmb3-1、2μmfip-1、2μmbip-1、1μmlf-1、1μmlb-1。
lamp扩增的反应程序:65℃恒温50min。反应过程中,采用荧光pcr仪检测荧光信号。
如果采用引物组可以得到阳性扩增曲线,表明待测病毒为eb病毒或待测样本感染了eb病毒。
如果采用引物组可以得到阳性扩增曲线,表明待测病毒为eb病毒或待测样本含有eb病毒,如果不可以得到阳性扩增曲线,表明待测病毒为eb病毒或待测样本含有eb病毒。
实施例3、鉴定eb病毒的引物组的特异性
eb病毒参考品质粒构建:将序列表的序列7所示的eb病毒的dna片段插入至pgem-teasyvector载体的apai和saci酶切位点之间,得到参考品质粒。
待测样本分别为:eb病毒参考品质粒dna、单纯疱疹病毒ⅰ型基因组dna、单纯疱疹病毒ⅱ型基因组dna、水痘-带状疱疹病毒基因组dna、巨细胞病毒基因组dna。其中,单纯疱疹病毒ⅰ型、单纯疱疹病毒ⅱ型、水痘-带状疱疹病毒和巨细胞病毒参考品质粒dna均记载于文献“朱艳敏,吴亦栋,尚世强.检测7种疱疹病毒的基因芯片法及其初步应用[j].临床检验杂志,2009(5):363-365.”中,提取各病毒的基因组dna,即得到待测样本。
以待测样本为模板,采用实施例2的检测方法进行检测,并利用无菌水作为阴性对照。
结果见图1。图1中,横坐标为循环数,纵坐标为荧光信号强度。由图1可见,eb病毒参考品质粒dna得到s型扩增曲线,扩增结果为阳性,单纯疱疹病毒ⅰ型参考品质粒dna、单纯疱疹病毒ⅱ型参考品质粒dna、水痘-带状疱疹病毒参考品质粒dna和巨细胞病毒参考品质粒dna均没有得到s型扩增曲线,扩增结果为阴性。结果表明,本发明的鉴定eb病毒的引物组具有很高的特异性。
实施例4、鉴定eb病毒的引物组的灵敏度
待测样本为:实施例3的eb病毒参考品质粒dna。
1、用无菌水10倍梯度稀释参考品质粒dna,得到各稀释液。
2、分别取步骤1得到的各稀释液作为模板,采用实施例2的检测方法进行检测,并利用无菌水作为阴性对照。
由于采用的稀释度不同,形成如下不同的反应体系:
反应体系1中,参考品质粒dna的含量为:10000个拷贝;
反应体系2中,参考品质粒dna的含量为:1000个拷贝;
反应体系3中,参考品质粒dna的含量为:500个拷贝;
反应体系4中,参考品质粒dna的含量为:100个拷贝。
参考品质粒按上述体系进行检测。
结果表明,eb病毒参考品质粒的dna含量为500-10000个拷贝时均得到s型扩增曲线,含量为100个拷贝时和阴性对照没有得到s型扩增曲线。该结果表明本发明的鉴定eb病毒的引物组的可检测到500拷贝的eb病毒,具有较高的灵敏度。
实施例5、临床样本检测
待测样本为:经过临床鉴定为eb病毒的眼部抽吸物样本(eb病毒阳性样本)和经过临床鉴定不存在eb病毒的健康者的眼部抽吸物样本。
以待测样本的dna为模板,采用实施例2的检测方法进行检测,利用实施例3的eb病毒参考品质粒dna作为阳性对照,无菌水作为阴性对照。
结果见图2。图2中,横坐标为循环数,纵坐标为荧光信号强度。由图2可见,只有eb病毒阳性样本以及阳性对照得到s型扩增曲线,健康者样本和阴性对照没有得到s型扩增曲线,健康者样本的检测结果与临床鉴定结果相符。结果表明,本发明的鉴定eb病毒的引物组在进行eb病毒鉴定时,结果准确可靠。
对比例1、利用其他引物鉴定eb病毒
待测样本为:实施例3的eb病毒参考品质粒dna。
1、用无菌水10倍梯度稀释eb病毒参考品质粒dna,得到eb病毒参考品质粒dna稀释液;
2、以步骤的稀释液为模板,分别采用本发明的鉴定eb病毒的引物组、引物组a和引物组b,按照实施例2的检测方法进行检测,反应体系中eb病毒参考品质粒dna的拷贝数为500,并利用无菌水作为阴性对照。
引物组a序列信息如下:
a-f3:5′-tgtgacccttgggcctgg-3′
a-b3:5′-ctggctctttggcaggcc-3′
a-fip:5′-ccatagactcccatgtaattacatgggagtctatgg-3′
a-fip:5′-gacagggcgcgcatggcccaaaagtagaggctca-3′
a-lf:5′-cgggctgctgtctggctta-3′
a-lb:5′-cagagcgccaggagtcat-3′
引物组b序列信息如下:
b-f3:5′-atctaaggccaggagagg-3′
b-b3:5′-tagcagcagcgcagcc-3′
b-fip:5′-agccccaaagcgggtgattacctgttactgc-3′
b-fip:5′-accatagacccgcttcggcctaaaacccccag-3′
b-lf:5′-cgggctgttactgtctggc-3′
b-lb:5′-cagagcgcatccaggagt-3′
结果表明,本发明的鉴定eb病毒的引物组得到s型扩增曲线,引物组a、引物组b和阴性对照没有得到s型扩增曲线。
<110>一组用于检测眼内液中eb病毒的lamp引物及应用
<120>北京智德臻和医学检验所有限公司
<160>7
<170>patentinversion3.5
<210>1
<211>17
<212>dna
<213>人工序列
<220>
<223>
<400>1
gttcgcgttgctaggcc17
<210>2
<211>21
<212>dna
<213>人工序列
<220>
<223>
<400>2
aaggggaaaagttagaaactg21
<210>3
<211>39
<212>dna
<213>人工序列
<220>
<223>
<400>3
ataccaggggcagtggtccctctcagtccagcgcgttta39
<210>4
<211>41
<212>dna
<213>人工序列
<220>
<223>
<400>4
gtcctgcagctatttctggtcgctagggagaggtagaagac41
<210>5
<211>19
<212>dna
<213>人工序列
<220>
<223>
<400>5
ggctgctgtctggcttacg19
<210>6
<211>18
<212>dna
<213>人工序列
<220>
<223>
<400>6
atcagagcgccaggagtc18
<210>7
<211>860
<212>dna
<213>人工序列
<220>
<223>
<400>7
tgtgacccttgggcctggctccccatagactcccatgtaagcctgcctcgagtaggtgcc60
tccagagccccttttgcccccctggcggcccagcccgacccccgggcgcccccaaacttt120
gtccagatgtccaggggtccccgagggcgaggcccagccccctcccacccctgtccactg180
ccccggtccccccagaagcccccaaaagtagaggctcaggccatgcgcgccctgtcacca240
ggcctgccaaagagccagatctaaggccaggagaggcagccccaaagcgggtgcagtaac300
aggtaatctctggtagtgatttggacccaaaatctgacactttagagctctggaggactt360
taaaactctaaaaatcaaaactttagaggcgaatgggcgccattttgtccccacgcgcgc420
ataatggcggacctaggcctaaaacccccaggaagcgggtctatggttggctgcgctgct480
gctatctttagaggggaaaagaggaataagcccccagacaggggagtgggcttgtttgtg540
acttcaccaaaggtcagggcccaagggggttcgcgttgctaggccaccttctcagtccag600
cgcgtttacgtaagccagacagcagccaattgtcagttctagggagggggaccactgccc660
ctggtataaagtggtcctgcagctatttctggtcgcatcagagcgccaggagtccacaca720
aatgtaagagggggtcttctacctctccctagccctccgccccctccaaggactcgggcc780
cagtttctaacttttccccttccctccctcgtcttgccctgcgcccggggccaccttcat840
caccgtcgctgactccgcca860
- 还没有人留言评论。精彩留言会获得点赞!