一组用于检测眼内液中结核分枝杆菌的LAMP引物及应用的制作方法
本发明涉及生物技术领域中,一组用于检测眼内液中结核分枝杆菌的lamp引物及应用。
背景技术:
结核分枝杆菌(mycobacteriumtuberculosis)俗称结核杆菌,是引起结核病的病原菌,可侵犯全身各器官。结核杆菌感染在眼部最常见的病变是葡萄膜炎,也可引起眼睑、结膜、角膜、巩膜和表层巩膜、眼眶、视神经等的病变。视力突然下降,睫状充血,房水轻度混浊,角膜后沉着物为羊脂状,视网膜水肿,黄斑黄色渗出病灶,血红细胞沉降率快,x射线显示肺活动性结核灶,皮肤结核菌素试验阳性,诊断为结核性视网膜脉络膜炎及肺结核,要给予抗结核治疗。早期正确诊断和有效治疗可使绝大多数患者得以康复。延迟诊断、贻误治疗及疾病迅速进展可导致死亡。结核性葡萄膜炎经积极正确治疗后视力预后通常较好。
目前临床针对结核分枝杆菌的检测方法主要是分离培养、涂片镜检和血清学诊断。这些检测方法繁琐,检测时间长,灵敏度低,容易发生漏检和错检,无法满足快速检测的要求。近几年发展起来的分子检测技术,特别是pcr技术,在微生物快速鉴定和检测方面的应用,为细菌的快速检测开辟了新的途径。但是,pcr存在检测时间长、易污染、假阳性率高的缺点,使其应用受到限制。环介导等温扩增技术(loop-mediatedisothermalamplification,lamp)是近年来发展出的一种敏感、特异、简便、快捷的核酸扩增技术,其原理是在一种具有链置换活性的dna聚合酶的作用下,识别6-8个区域的4-6条引物,在等温条件下快速、特异地扩增目的基因,可推广应用于快速、准确的检测细菌。
技术实现要素:
本发明的目的是提供一组用于检测眼内液中结核分枝杆菌的lamp引物组及应用。
本发明提供的lamp引物组,由引物f3-1、引物b3-1、引物fip-1、引物bip-1、引物lf-1和引物lb-1组成;
所述引物f3-1为如下(a1)或(a2):
(a1)序列表的序列1所示的单链dna分子;
(a2)将序列1经过一个或几个核苷酸的取代和/或缺失和/或添加且与序列1具有相同功能的单链dna分子;
所述引物b3-1为如下(a3)或(a4):
(a3)序列表的序列2所示的单链dna分子;
(a4)将序列2经过一个或几个核苷酸的取代和/或缺失和/或添加且与序列2具有相同功能的单链dna分子;
所述引物fip-1为如下(a5)或(a6):
(a5)序列表的序列3所示的单链dna分子;
(a6)将序列3经过一个或几个核苷酸的取代和/或缺失和/或添加且与序列3具有相同功能的单链dna分子;
所述引物bip-1为如下(a7)或(a8):
(a7)序列表的序列4所示的单链dna分子;
(a8)将序列4经过一个或几个核苷酸的取代和/或缺失和/或添加且与序列4具有相同功能的单链dna分子;
所述引物lf-1为如下(a9)或(a10):
(a9)序列表的序列5所示的单链dna分子;
(a10)将序列5经过一个或几个核苷酸的取代和/或缺失和/或添加且与序列5具有相同功能的单链dna分子;
所述引物lb-1为如下(a11)或(a12):
(a11)序列表的序列6所示的单链dna分子;
(a12)将序列6经过一个或几个核苷酸的取代和/或缺失和/或添加且与序列6具有相同功能的单链dna分子。
所述引物组中,所述引物f3-1、所述引物b3-1、所述引物fip-1、所述引物bip-1、所述引物lf-1和所述引物lb-1的摩尔比可为0.5:0.5:2:2:1:1。
本发明还保护所述引物组的应用,所述应用为如下(b1)至(b6)中的任意一种:
(b1)在鉴别结核分枝杆菌中的应用;
(b2)在制备用于鉴别结核分枝杆菌的试剂盒中的应用;
(b3)在鉴定待测细菌是否为结核分枝杆菌中的应用;
(b4)在制备用于鉴定待测细菌是否为结核分枝杆菌的试剂盒中的应用;
(b5)在鉴定待测样本是否含有结核分枝杆菌中的应用;
(b6)在制备用于鉴定待测样本是否含有结核分枝杆菌的试剂盒中的应用。
上述应用,所述待测样本可为眼部临床样本培养物、眼液体或抽吸物。
本发明还保护含有所述引物组的试剂盒;所述试剂盒的用途为如下(c1)或(c2)或(c3):
(c1)鉴别结核分枝杆菌;
(c2)鉴定待测细菌是否为结核分枝杆菌;
(c3)鉴定待测样本是否含有结核分枝杆菌。
所述试剂盒还可包括lamp反应体系中非引物外的其他试剂。
上述试剂盒中,所述待测样本可为眼部临床样本培养物、眼液体或抽吸物。
本发明还保护所述试剂盒在如下(c1)或(c2)或(c3)中的应用:
(c1)鉴别结核分枝杆菌;
(c2)鉴定待测细菌是否为结核分枝杆菌;
(c3)鉴定待测样本是否含有结核分枝杆菌。
上述应用,所述待测样本可为眼部临床样本培养物、眼液体或抽吸物。
本发明还保护所述引物组的制备方法,所述方法包括将各条引物分别独立包装。
本发明还保护所述试剂盒的制备方法,所述方法包括将所述引物组的的各条引物分别独立包装。
本发明中,在利用所述引物组或所述试剂盒鉴别结核分枝杆菌时,可按照包括如下步骤的方法进行:
(1)提取待测样本的基因组dna;
(2)以步骤(1)得到的基因组dna为模板,采用所述引物组或所述试剂盒进行lamp扩增反应,然后进行如下判断:
如果可以实现以所述基因组dna为模板的特异性扩增,所述待测样本为或候选为结核分枝杆菌;
如果不可以实现以所述基因组dna为模板的特异性扩增,所述待测样本不为或候选不为结核分枝杆菌。
在利用所述引物组或所述试剂盒鉴定待测细菌是否为结核分枝杆菌时,可按照包括如下步骤的方法进行:
(1)提取待测细菌的基因组dna;
(2)以步骤(1)得到的基因组dna为模板,采用所述引物组或所述试剂盒进行lamp扩增反应,然后进行如下判断:
如果可以实现以所述基因组dna为模板的特异性扩增,所述待测细菌为或候选为结核分枝杆菌;
如果不可以实现以所述基因组dna为模板的特异性扩增,所述待测细菌不为或候选不为结核分枝杆菌。
在利用所述引物组或所述试剂盒鉴定待测样本是否含有结核分枝杆菌时,可按照包括如下步骤的方法进行:
(1)提取待测样本的基因组dna;
(2)以步骤(1)得到的基因组dna为模板,采用所述引物组或所述试剂盒进行lamp扩增反应,然后进行如下判断:
如果可以实现以所述基因组dna为模板的特异性扩增,所述待测样本含有或候选含有结核分枝杆菌;
如果不可以实现以所述基因组dna为模板的特异性扩增,所述待测样本不含有或候选不含有结核分枝杆菌。
上文中,具体可通过如下方法判断“阳性扩增”:用荧光pcr仪检测荧光信号,如果出现阳性扩增曲线则为阳性扩增。所述阳性扩增曲线具体可为s型扩增曲线。
以上任一所述采用引物组进行lamp扩增的反应体系中,所述引物组中各引物的浓度为:0.5μm所述引物f3-1、0.5μm所述引物b3-1、2μm所述引物fip-1、2μm所述引物bip-1、1μm所述引物lf-1、1μm所述引物lb-1。
以上任一所述采用引物组进行lamp扩增的反应体系的10μl反应体系中可含有1μl10×thermopolbuffer,0.8m甜菜碱,0.5mg/mlbsa,4mmmgso4,0.3μl20×evagreen,1.5mmdntps,0.32u/mlbstdna聚合酶大片段,1μl所述引物组溶液,50pg-50ng模板dna,余量为水。其中,10×thermopolbuffer可为thermo产品,20×evagreen可为合肥博美生物科技有限责任公司产品。
以上任一所述lamp扩增的反应程序具体可为:65℃恒温50min。反应过程中,采用荧光pcr仪检测荧光信号。
本发明提供了一组用于检测眼内液中结核分枝杆菌的lamp引物组及应用。本发明所述的lamp引物组包括外引物f3和b3,内引物fip和bip以及环引物lf和lb,在检测结核分枝杆菌时具有高特异性和高灵敏度。应用本发明的lamp引物组及方法,可快速、准确的检测出结核分枝杆菌。
附图说明
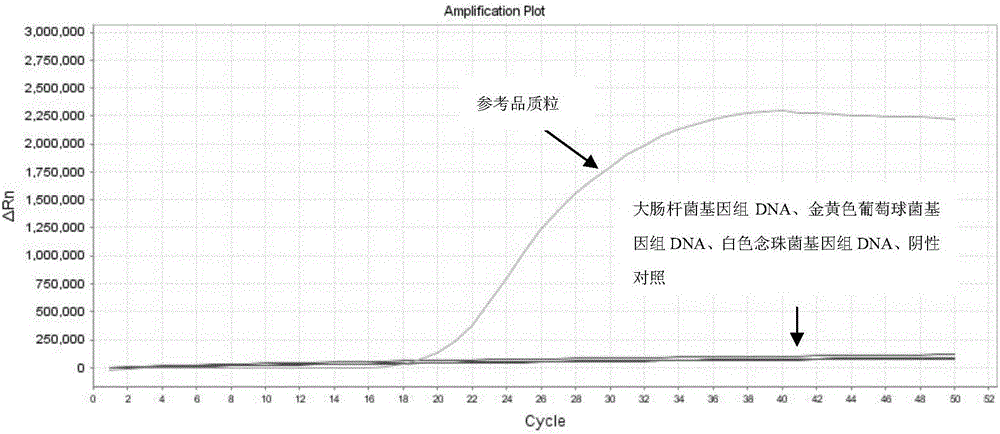
图1为实施例3的lamp扩增曲线图。
图2为实施例5的lamp扩增曲线图。
具体实施方式
以下的实施例便于更好地理解本发明,但并不限定本发明。下述实施例中的实验方法,如无特殊说明,均为常规方法。下述实施例中所用的试验材料,如无特殊说明,均为自常规生化试剂商店购买得到的。以下实施例中的定量试验,均设置三次重复实验,结果取平均值。
pgem-teasyvector载体:promega公司,产品货号a1360。
实施例1、鉴定结核分枝杆菌的引物组的制备
进行大量序列分析、比对获得了用于鉴定结核分枝杆菌的若干引物。将各个引物进行预实验,比较灵敏度、特异性等性能,最终得到用于鉴定结核分枝杆菌的lamp引物组。
用于鉴定结核分枝杆菌的引物组,包括2条外引物(f3-1、b3-1),2条内引物(fip-1、bip-1)和2条环引物(lf-1、lb-1),各条引物序列如下所示(5’→3’):
引物f3-1(序列表的序列1):agtacaccgttttcgcc;
引物b3-1(序列表的序列2):gttgaccatgaggtcgtc;
引物fip-1(序列表的序列3):gcgtcagtcttgagttgatcgccaccaacgccgcattc;
引物bip-1(序列表的序列4):ctcagcagcatcctgacctctgatgggtgccgtcga;
引物lf-1(序列表的序列5):ggccgccggcagctt;
引物lb-1(序列表的序列6):cacgtgatagccggccag。
该引物组中,引物f3-1、引物b3-1、引物fip-1、引物bip-1、引物lf-1和引物lb-1的摩尔比为0.5:0.5:2:2:1:1,各引物均独立包装。
实施例2、检测方法建立
利用实施例1的鉴定结核分枝杆菌的引物组检测结核分枝杆菌的方法包括:
1、提取待测细菌的基因组dna或提取待测样本的总dna。
2、取步骤1得到的总dna,作为模板,采用实施例1中制备的引物组进行lamp扩增。
10μllamp扩增的反应体系包括:1μl10×thermopolbuffer(thermo),0.8m甜菜碱,0.5mg/mlbsa,4mmmgso4,0.3μl20×evagreen(合肥博美生物科技有限责任公司),1.5mmdntps,0.32u/mlbstdna聚合酶大片段,引物混合物(f3-1、b3-1、fip-1、bip-1、lf-1和lb-1的混合物),2ng模板dna,余量为ddh2o。反应体系中各引物的浓度如下:0.5μmf3-1、0.5μmb3-1、2μmfip-1、2μmbip-1、1μmlf-1、1μmlb-1。
lamp扩增的反应程序:65℃恒温50min。反应过程中,采用荧光pcr仪检测荧光信号。
如果采用引物组可以得到阳性扩增曲线,表明待测细菌为结核分枝杆菌或待测样本含有结核分枝杆菌,如果不可以得到阳性扩增曲线,表明待测细菌不为结核分枝杆菌或待测样本不含有结核分枝杆菌。
实施例3、鉴定结核分枝杆菌的引物组的特异性
结核分枝杆菌参考品质粒dna构建:将序列表的序列7所示的结核分枝杆菌的dna片段插入至pgem-teasyvector载体的apai和saci酶切位点之间,得到结核分枝杆菌参考品质粒dna。
待测样本分别为:结核分枝杆菌参考品质粒dna、大肠杆菌基因组dna、金黄色葡萄球菌基因组dna、白色念珠菌基因组dna。其中,大肠杆菌和金黄色葡萄球菌记载在“吴伟,何梅凤,唐细兰,等.眼部细菌感染病原菌分布及耐药性分析[j].中国医院药学杂志,2010,30(20):1786-1788.”一文中;白色念珠菌记载在“张志明,李建平,朱建伟.16srrna在检测肺炎克雷伯菌引起血流感染中的应用[j].中国热带医学,2011,11(3):272-273.”一文中,提取各菌株的基因组dna,即得到各待测样本。
以各待测样本作为模板dna,采用实施例2的检测方法进行检测,并利用无菌水作为阴性对照。
结果见图1。图1中,横坐标为循环数,纵坐标为荧光信号强度。由图1可见,结核分枝杆菌参考品质粒dna得到s型扩增曲线,扩增结果为阳性,大肠杆菌基因组dna、金黄色葡萄球菌基因组dna、肺炎链球菌基因组dna均没有得到s型扩增曲线,扩增结果为阴性。结果表明,本发明的鉴定结核分枝杆菌的引物组具有很高的特异性。
实施例4、鉴定结核分枝杆菌的引物组的灵敏度
待测样本为:实施例3的结核分枝杆菌参考品质粒dna。
1、用无菌水10倍梯度稀释各待测样本,得到各稀释液。
2、分别取步骤1得到的各稀释液作为模板,采用实施例2的检测方法进行检测,并利用无菌水作为阴性对照。
由于采用的稀释度不同,形成如下不同的反应体系:
反应体系1中,结核分枝杆菌参考品质粒dna的含量为:10000个拷贝;
反应体系2中,结核分枝杆菌参考品质粒dna的含量为:1000个拷贝;
反应体系3中,结核分枝杆菌参考品质粒dna的含量为:500个拷贝;
反应体系4中,结核分枝杆菌参考品质粒dna的含量为:100个拷贝。
结核分枝杆菌参考品质粒dna按上述体系进行检测。
结果表明,反应体系中结核分枝杆菌参考品质粒dna的含量为500-10000个拷贝时均得到s型扩增曲线,含量为100个拷贝时和阴性对照没有得到s型扩增曲线。该结果表明本发明的鉴定结核分枝杆菌的引物组可检测到500拷贝的结核分枝杆菌,具有较高的灵敏度。
实施例5、模拟阳性样本检测
待测样本为:经过临床鉴定不存在结核分枝杆菌的健康者的眼部抽吸物样本和在健康者的眼部抽吸物样本中加入结核分枝杆菌参考品质粒dna制备而成的模拟阳性样本。
以待测样本的dna为模板,采用实施例2的检测方法进行检测,利用实施例3的结核分枝杆菌参考品质粒dna作为阳性对照,无菌水作为阴性对照。
结果见图2。图2中,横坐标为循环数,纵坐标为荧光信号强度。由图2可见,只有结核分枝杆菌模拟阳性样本以及阳性对照得到s型扩增曲线,健康者样本和阴性对照没有得到s型扩增曲线,健康者样本的检测结果与临床鉴定结果相符。结果表明,本发明的鉴定结核分枝杆菌的引物组在进行结核分枝杆菌鉴定时,结果准确可靠。
对比例1、利用其他引物鉴定结核分枝杆菌
待测样本为:实施例3的结核分枝杆菌参考品质粒dna。
1、用无菌水10倍梯度稀释结核分枝杆菌参考品质粒dna,得到结核分枝杆菌参考品质粒dna稀释液;
2、以步骤1的稀释液为模板,分别采用本发明的鉴定结核分枝杆菌的引物组、引物组a和引物组b按照实施例2的检测方法进行检测,反应体系中结核分枝杆菌参考品质粒dna的拷贝数为500,并利用无菌水作为阴性对照。
引物组a序列信息如下:
a-f3:5′-atgatcaacgttc-3′
a-b3:5′-cagccattgccg-3′
a-fip:5′-caaaccggccgcagcagcgagcctcg-3′
a-fip:5′-ggtaacgggcgccagcgagcctcg-3′
a-lf:5′-ccgggccggcagctt-3′
a-lb:5′-cacgcctgatagccggag-3′
引物组b序列信息如下:
b-f3:5′-ccgcagcggacctg-3′
b-b3:5′-agcttgcccgacagag-3′
b-fip:5′-gtcgtgggtgcgcgctctgtcgggcaagct-3′
b-fip:5′-agcttgcccgacagagccgaggtcagggtact-3′
b-lf:5′-cgctaacgaacgcg-3′
b-lb:5′-ctggtgtcttgc-3′
结果表明,本发明的鉴定结核分枝杆菌的引物组可以得到得到s型扩增曲线,而引物组a和引物组b以及阴性对照均没有得到s型扩增曲线。
<110>一组用于检测眼内液中结核分枝杆菌的lamp引物及应用
<120>北京智德臻和医学检验所有限公司
<160>7
<170>patentinversion3.5
<210>1
<211>17
<212>dna
<213>人工序列
<220>
<223>
<400>1
agtacaccgttttcgcc17
<210>2
<211>18
<212>dna
<213>人工序列
<220>
<223>
<400>2
gttgaccatgaggtcgtc18
<210>3
<211>38
<212>dna
<213>人工序列
<220>
<223>
<400>3
gcgtcagtcttgagttgatcgccaccaacgccgcattc38
<210>4
<211>36
<212>dna
<213>人工序列
<220>
<223>
<400>4
ctcagcagcatcctgacctctgatgggtgccgtcga36
<210>5
<211>15
<212>dna
<213>人工序列
<220>
<223>
<400>5
ggccgccggcagctt15
<210>6
<211>18
<212>dna
<213>人工序列
<220>
<223>
<400>6
cacgtgatagccggccag18
<210>7
<211>663
<212>dna
<213>人工序列
<220>
<223>
<400>7
atgatcaacgttcaggccaaaccggccgcagcagcgagcctcgcagccatcgcgattgcg60
ttcttagcgggttgttcgagcaccaaacccgtgtcgcaagacaccagcccgaaaccggcg120
accagcccggcggcgcccgttaccacggcggcaatggctgaccccgcagcggacctgatt180
ggtcgtgggtgcgcgcaatacgcggcgcaaaatcccaccggtcccggatcggtggccgga240
atggcgcaagacccggtcgctaccgcggcttccaacaacccgatgctcagtaccctgacc300
tcggctctgtcgggcaagctgaacccggatgtgaatctggtcgacaccctcaacggcggc360
gagtacaccgttttcgcccccaccaacgccgcattcgacaagctgccggcggccactatc420
gatcaactcaagactgacgccaagctgctcagcagcatcctgacctaccacgtgatagcc480
ggccaggcgagtccgagcaggatcgacggcacccatcagaccctgcaaggtgccgacctg540
acggtgataggcgcccgcgacgacctcatggtcaacaacgccggtttggtatgtggcgga600
gttcacaccgccaacgcgacggtgtacatgatcgatacggtgctgatgcccccggcacag660
taa663
- 还没有人留言评论。精彩留言会获得点赞!
- 一种敲除c‑di‑AMP分解酶的重组耻垢分枝杆菌株及其应用的制造方法与工艺
- 检测结核分枝杆菌感染的抗原多肽池及其应用的制造方法与工艺
- 一种猕猴桃分枝定位器的制造方法与工艺
- 一种xanthone类化合物及其单晶的制备方法与作为抗海分枝杆菌药物的应用与制造工艺
- 一种糖肽类抗生素耐药基因检测试剂盒的制造方法与工艺
- 分枝杆菌快速分离培养方法与制造工艺
- 一种用于检测潜在结核的特异性标志物及其应用的制造方法与工艺
- 结核分枝杆菌抗原蛋白Rv2941及其T细胞表位肽的应用的制造方法与工艺
- 一种微流控芯片上基于荧光量子点磁性富集并分离结核分枝杆菌TB的方法及装置与制造工艺
- 二肽meso‑DAP‑D‑Ala和/或四肽L‑Ala‑D‑Glu‑L‑Lys‑D‑Ala的新用途的制造方法与工艺