一种xanthone类化合物及其单晶的制备方法与作为抗海分枝杆菌药物的应用与流程
本发明涉及一种xanthone类化合物及其单晶的制备方法与作为抗海分枝杆菌药物的应用,特别是涉及一种对海分枝杆菌(mycobacteriummarinum)具有极强的抑制作用的xanthone类化合物及其单晶制备方法与应用。
背景技术:
结核分枝杆菌导致的结核病仍然是全球公共卫生的严重威胁。据who最新报道,在2014年,约有960万新病例发生,150万人死于该病,有48万人发展为多重抗药性结核病。我国占有全世界人口的20%,结核病对我国亦构成极大的威胁。然而,研究结核分枝杆菌(mycobacteriumtuberculosis)的感染机制是困难的,原因是结核分枝杆菌生长缓慢,需较高的生物安全措施,成本高,动物模型少等。海分枝杆菌(mycobacteriummarinum)为一种腐生性非典型分枝杆菌,天然宿主为鱼类、两栖类,人类感染属机会感染。基因组比较分析表明海分枝杆菌(m.marinum)与结核分枝杆菌(m.tuberculosis)的亲缘关系很近,这两种病原菌引起的疾病特征在某些方面也很相似,如肉芽肿。利用海分枝杆菌对结核分枝杆菌发病机理的决定性因素研究是一种优良模型,且安全系数高。现如今,随着在家庭中通过鱼缸养殖观赏鱼的流行,感染海分枝杆菌的几率也在增加,其导致人类慢性的皮肤损伤,脓毒性关节炎等。临床上大多数有效的抗海分枝杆菌治疗为联合使用利福平、克拉霉素等抗生素,且需立即用药。由于海分枝感染还不是很普遍,加上多样化的临床表现,往往会导致误诊或者延迟治疗,导致病情恶化而难以治愈。因而寻找更高效的抗海分枝杆菌药物尤其是结构新颖的抗海分枝杆菌药物已成为急需解决的课题。海洋微生物独特的生存环境(高压、高盐、缺氧、避光等),促使海洋微生物代谢产生大量结构新颖、活性很好的化合物,为开发新型抗海分枝杆菌药物或者潜在的抗结核药物提供了重要来源。但是关于海洋微生物来源的具有抗海分枝杆菌活性的化合物的报道还相当少,尤其是具有潜在开发成为抗结核药物的海洋来源化合物的报道。(who.globaltuberculosiscontrol2015.robinl.;lalitar.,currentopinioninmicrobiology(2008),11(3),277-283.stinear,t.p.;seemann,t.,etal.genomeresearch(2008),18(5),729741.rieraj.;conesax.,etal.archivesoforthopaedicandtraumasurgery(2016),136(1),131134.babamahmoodif.;nikkhahanb.;babamahmoodia.,iranianredcrescentmedicaljournal(2014),16(2),e10120.fengy.m.;xuh.s.,etal.diagnosticmicrobiologyandinfectiousdisease(2011),71,267272.cheungj.p.;fungb.,etal.journaloforthopaedicsurgery(2010),18(1),98103.andpreviousannualreports)。
技术实现要素:
本发明的目的在于提供一种来源于海洋真菌的xanthone类化合物及其单晶的制备方法与作为抗海分枝杆菌活性的应用,它能满足现有技术的上述需求。菌种保藏信息:保藏单位名称:中国微生物菌种保藏管理委员会普通微生物中心;保藏单位地址:北京市朝阳区北辰西路1号院3号中国科学院微生物研究所;保藏日期:2014年4月3日;保藏编号:cgmcc8994;分类命名:penicilliumsp.本发明提供式i化合物1和2或其药学上可接受的盐:
本发明提供式i化合物1和2的制备方法,其特征在于先在菌种培养基中对真菌penicilliumsp.(ta33-1)进行菌种培养,再在发酵培养基中对该真菌进行发酵培养,将所得菌丝体用氯仿-甲醇混合液(1:1)浸提3次减压浓缩后,用乙酸乙酯萃取3次得粗浸膏;乙酸乙酯相粗浸膏分别进行正相硅胶柱层析、sephadexlh-20凝胶柱层析后,再经hplc高效液相制备色谱,将所得洗脱液浓缩,即为化合物1和2。
上述制备方法中菌种培养基优选含有葡萄糖0.1%–5.0%(重量百分比,下同)、酵母膏0.01%–1%、蛋白胨0.01%–1%、琼脂0.1%–3.0%、氯化钠0.05%–5%,其余为水,培养温度优选为0–30°c,培养时间优选为3–15天;发酵培养基优选含有大米1.0%–80.0%(重量百分比,下同)、氯化钠0.05%–5%,其余为水,培养温度优选为0–30°c,培养时间优选为20–100天;所述的正相硅胶柱层析采用的固定相优选200–300目硅胶,流动相优选体积比为20%–100%的乙酸乙酯-石油醚混合溶剂;所述sephadexlh-20凝胶柱层析采用的流动相优选体积比为氯仿:甲醇=1:1的混合溶剂;所述hplc高效液相制备色谱中采用的色谱柱:常规odsc18柱,优选为kromasil10×250mm,5μm,流速优选为1.0–5.0ml/min,流动相优选体积比为20%–70%的甲醇-水混合溶剂。
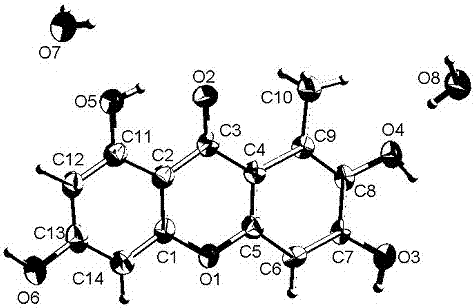
本发明的另一实施方案提供式ⅰ化合物1的晶体,晶体数据:空间群为p-1,晶胞参数为a=7.123(4)å,b=8.069(4)å,c=11.596(6)å,α=93.86(3)º,β=93.56(3)º,γ=102.58(3)º,v=646.99(505)å3,z=2,dc=1.593g/cm3,f(000)=324,μ=1.144mm–1。
本发明的另一实施方案提供上述式i化合物1晶体的制备方法,其特征在于将式i化合物1溶于甲醇、乙醇、水、四氢呋喃或丙酮中的任一种或几种,静置缓慢结晶即可得到式i化合物1的晶体。
上述晶体的制备方法中静置缓慢结晶的条件优选在0–30oc下,静置1–30天。
本发明从海洋真菌中获得xanthone类化合物对海分枝杆菌具有强的抑制活性,可用作抗海分枝杆菌药物,应用前景广阔。
本发明的另一实施方式中提供一种抗海分枝杆菌药物,其特征在于包括式ⅰ化合物1和2或其药学上可接受的盐作为有效成分。
本发明中术语“药学上可接受的盐”是指非毒性的无机或有机酸和/或碱的加成盐。可参见“saltselectionforbasicdrugs”,int.j.pharm.1986,33,201–217。
附图说明
图1为式i化合物1的xrd图。
上述的xanthone类化合物在制备抗海分枝杆菌药物中的应用。
具体实施方式
为了便于对本发明的进一步理解,下面提供的实施例对其做了更详细的说明。但是这些实施例仅供更好地理解发明而并非用来限定本发明的范围或实施原则,本发明的实施方式不限于以下内容。
实施例1
(1)花柳珊瑚内生真菌penicilliumsp.(ta33-1)的菌种培养
菌种培养所用的培养基含有葡萄糖1.0%(重量百分比,下同)、酵母膏0.2%、蛋白胨0.2%、琼脂1.0%、氯化钠3.0%,其余为水,使用时制成试管斜面,真菌菌株在30°c下培养3天。
(2)花柳珊瑚内生真菌penicilliumsp.(ta33-1)的发酵
发酵培养所用的培养基含有大米40.0%(重量百分比,下同)、氯化钠3.0%,其余为水;真菌菌株于28°c培养90天。
(3)式i化合物1和2的提取分离
取60瓶步骤(2)得到的菌丝体,用氯仿-甲醇混合液(1:1)浸提3次减压浓缩后,用乙酸乙酯萃取3次得粗浸膏;乙酸乙酯相粗浸膏分别进行正相硅胶柱层析(固定相为200–300目硅胶;流动相为100%乙酸乙酯溶剂)、sephadexlh-20凝胶柱层析(氯仿:甲醇=1:1的混合溶剂,体积比)后,再经hplc高效液相制备色谱分离(色谱柱为kromasil10×250mm,5μm,流速为2.0ml/min,流动相为35%的甲醇-水混合溶剂,体积比),将所得洗脱液浓缩,得黄色结晶,即为式i化合物1和2。
式i化合物1和2的结构确证数据:
化合物1:黄色晶体;1hnmr(500mhz,acetone-d6,δ,ppm,j/hz):13.60(1h,s,h-8),6.80(1h,s,h-4),6.28(1h,d,j=1.5hz,h-5),6.17(1h,d,j=1.5hz,h-7),2.78(3h,s,h-11).13cnmr(125mhz,acetone-d6,δ,ppm,j/hz)183.5(c,c-9),165.1(c,c-6),164.8(c,c-8),158.1(c,c-10a),153.5(c,c-4a),152.6(c,c-3),141.8(c,c-2),125.7(c,c-1),112.5(c,c-1a),103.9(c,c-9a),100.9(ch,c-4),98.5(ch,c-7),93.6(ch,c-5),13.9(ch3,c-11).
化合物2:黄色晶体;1hnmr(500mhz,acetone-d6,δ,ppm,j/hz):13.58(1h,s,h-8),6.32(1h,d,j=2.0hz,h-5),6.16(1h,d,j=2.0hz,h-7),2.73(1h,s,h-1),13cnmr(125mhz,acetone-d6,δ,ppm,j/hz):183.1(c,c-9),164.1(c,c-8),163.8(c,c-6),157.1(c,c-10a),141.7(c,c-2),115.4(c,c-1a),111.2(c,c-1),103.1(c,c-9a),97.6(ch,c-7),92.9(ch,c-5),12.3(ch3,c-11).
实施例2
(1)花柳珊瑚内生真菌penicilliumsp.(ta33-1)的菌种培养
菌种培养所用的培养基含有葡萄糖0.1%–5.0%(重量百分比,下同)、酵母膏0.01%–1%、蛋白胨0.01%–1%、琼脂0.1%–3.0%、氯化钠0.05%–5%,其余为水,使用时制成试管斜面,真菌菌株在0–30°c下培养3–15天。
(2)花柳珊瑚内生真菌penicilliumsp.(ta33-1)的发酵
发酵培养所用的培养基含有大米1.0%–80.0%(重量百分比,下同)、氯化钠0.05%–5%,其余为水,真菌菌株于0–30°c培养20–100天。
(3)式i化合物1和2的提取分离
取10–60瓶步骤(2)所得的将所得菌丝体用氯仿-甲醇混合液(1:1)浸提3次减压浓缩后,用乙酸乙酯萃取3次得粗浸膏;乙酸乙酯相粗浸膏浓缩后分别进行正相硅胶柱层析(固定相为本领域常规正相硅胶,流动相为50%–100%的乙酸乙酯-石油醚混合溶剂,体积比)、sephadexlh-20凝胶柱层析(流动相为氯仿:甲醇=1:1的混合溶剂,体积比)后,再经hplc高效液相制备色谱(色谱柱为本领域常规odsc18柱,流速为1.0–5.0ml/min,流动相为20%–70%的甲醇-水混合溶剂,体积比),将所得洗脱液浓缩,得黄色结晶,即为式i化合物1和2。
其中式ⅰ化合物1和2的结构确证数据与实施例1中相应数据一致。
实施例1–2中未具体指明的其他菌种培养、发酵条件,以及正相硅胶柱色谱分离、sephadexlh-20凝胶柱层析分离、高效液相色谱分离等其他实验操作条件均为本领域常规的实验操作条件,本领域的技术人员可以根据实际需要,进行合理的选择。
实施例3
取式ⅰ化合物11.5mg溶解在装有500μl甲醇、乙醇、水、四氢呋喃或丙酮中任一种的小瓶中,于0°c下静置30天后,缓慢结晶即得式i化合物1的晶体。
实施例4
取式ⅰ化合物13mg溶解在装有1000μl甲醇、乙醇、四氢呋喃或丙酮中任一种或几种的小瓶中,于30°c下静置1天后,缓慢结晶即得式ⅰ化合物1的晶体。
上述晶体的晶体数据:空间群为p-1,晶胞参数为a=7.123(4)å,b=8.069(4)å,c=11.596(6)å,α=93.86(3)º,β=93.56(3)º,γ=102.58(3)º,v=646.99(505)å3,z=2,dc=1.593g/cm3,f(000)=324,μ=1.144mm–1。
实施例5
在菌种培养基中对海洋真菌penicilliumsp.(ta33-1)进行菌种培养,再在发酵培养基中对该真菌进行发酵培养,将所得发酵液过滤,除去菌体,将滤液浓缩后,用乙酸乙酯萃取;萃取液浓缩后分别进行正相硅胶柱层析、sephadexlh-20凝胶柱层析后,再经hplc高效液相制备色谱,将所得洗脱液浓缩,得黄色晶体,即为式ⅰ化合物1和2,其结构确证数据与实施例1中相应数据一致。其中所述菌种培养基中含有葡萄糖、酵母膏、蛋白胨、琼脂、粗海盐、水,所述发酵培养基中含有大米、粗海盐、蛋白胨、水;所述的色谱分离为正相硅胶柱色谱分离、sephadexlh-20凝胶柱层析和高效液相色谱分离。
为了探索更广泛的适用于制备本发明式ⅰ化合物1和2的方法,本实施例中菌种培养基、发酵培养基中各成分的添加,均按本领域中常规比例添加或按任意比例添加,色谱分离时所用硅胶的规格、sephadexlh-20凝胶的规格、色谱柱的型号及洗脱溶剂的选择,均为本领域的常规选择。实验结果表明,上述常规选择的制备方法,均能得到发明的黄色晶体,即式ⅰ化合物1和2,其结构确证数据与实施例1中相应数据一致,仅仅存在个别化合物在纯度及收率方面的微小差异。
实施例1–3的结果表明,按照本领域常规的菌种培养、发酵条件,常规的正相硅胶柱色谱分离、sephadexlh-20凝胶柱色谱分离、高效液相色谱分离的条件对海洋真菌penicilliumsp.(ta33-1)进行菌种培养、发酵、分离纯化,均能得到本发明式ⅰ结构的化合物1和2。本发明式ⅰ化合物1和2的制备方法,优选实施例1–2中记载的方法。
实施例6
本发明式ⅰ化合物1和2的抗海分枝杆菌活性按照如下文献测试方法测试:wangc,wangj,huangy,chenh.,liy.,zhongl.,cheny.,chens.,wangj.,kangj.,pengy.,yangb.,liny.,shez.,laix.,anti-mycobacterialactivityofmarinefungus-derived4-deoxybostrycinandnigrosporin.molecules,2013,18(2):17281740.
试验结果显示,本发明制备的式i化合物1和2对海分枝杆菌感染具有很强的抑制作用,其mic分别为40.75μm和50.61μm,阳性药利福平为2.34μm。
实验表明,本发明的xanthone类化合物1和2对海分枝杆菌感染具有很强的抑制活性,可将其制成抗海分枝杆菌药物,甚至抗结核杆菌药物,并且花柳珊瑚内生真菌penicilliumsp.(ta33-1)可进行大规模发酵生产,保证了式i化合物1和2的天然来源,具有广阔的应用前景。
- 还没有人留言评论。精彩留言会获得点赞!