微量生物样本DNA模板的制备方法及眼部HSV感染检测试剂盒与流程
本发明涉及眼部病毒感染的分子检测技术,特别是微量标本dna提取方法及眼部hsv感染检测试剂盒。
技术背景
由于眼部结构复杂,且受血脑屏障影响,眼部组织标本的很多检测指标与血液的检测指标相关性很低,大量临床数据研究发现,血液检查不能准确反映眼部的真实病因,特别是感染性眼病的病因;另一方面,眼部标本体积微小,标本种类多种多样,包括各种组织、各种体液(玻璃体、房水、泪液等)、各种膜类(视网膜、角膜内皮等)、多部位分泌物等,眼部液体类样本中病毒dna含量极低,而固体样本中病毒dna难以提出,且样本内容物及其复杂,同时受限于取样量极小(其中固体标本一般不超过1mm3;除了泪液,眼部液体标本一般能取的量约为20-100ul,最多不超过200ul),很难满足血液、尿液检验所要求的大体积和均一种类,因此对眼部标本采用常规血液检测方法进行检测,假阴性比例非常高,常常延误治疗。目前尚未见到适合于微量标本,特别是取自眼部的微量标本的病毒检测技术。
单纯疱疹病毒(herpessimplexvirus简称hsv),是人类最常见的病原体。hsv主要有两个血清型:hsv-1和hsv-2。hsv可引起口腔、唇、眼、脑及腰以上部位感染。
由hsv感染所导致的眼病复发率高、致盲率高,是当今最严重的感染性眼病之一。此病多由单纯疱疹i型病毒(hsv-1)感染所致,分为原发和复发两种类型。原发感染常发生于幼儿,表现为唇部疱疹、皮肤疱疹或急性滤泡性结膜炎。原发感染后病毒通常潜伏在三叉神经节或者角膜内,当机体抵抗力下降时,如发烧、疲劳、月经、局部用皮质类固醇或创伤刺激之后,病毒活化,引起多种形式的角膜炎、眼内炎,最大的特点是易反复发作。此病在发达国家的发病率为6/105~20/105,患病率为149/105。复发性hsv-1感染通常表现为溃疡性角膜炎或基质型角膜炎,角膜基质细胞免疫反应引起的炎症常致使角膜新生血管形成、角膜水肿、角膜组织损害、角膜混浊并最终导致失明。
hsv一种高复发率和高致盲性疾病,因为其临床表现常不典型,目前做眼部病毒感染的检测,依然采用血液检测,但是大量临床数据研究发现,血液检查不能准确反映眼部的真实病因,特别是感染性眼病的病因,易漏诊误诊。
获得眼部感染的准确检测结果,是后序采取正确治疗手段的前提;但是目前尚缺乏专门针对眼部组织病毒感染的高灵敏检测手段,也未见到以眼部微量样本为标本,采用常规pcr高灵敏度地检测病毒感染的报道。
技术实现要素:
根据上述领域的空白,临床上急需开发一种适合于眼部微量且多样标本的病毒dna提取方法和高灵敏度病毒检测试剂盒,鉴于此,本发明提供一种适合于眼部各类标本进行hsv病毒检测的方法、荧光探针检测试剂盒及dna提取方法,本发明请求保护的技术方案如下:
一种微量生物样本dna模板的制备方法,包括如下步骤:
(1)将待测微量生物样本放入容器中,加入10-30μl蛋白酶k、100-300μl裂解缓冲液al,于56℃处理至少10分钟;所述微量生物样本指体积不超过10ul-200ul的液体状样本或体积不超过1mm3的固体状样本;
(2)加入与裂解缓冲液等体积的无水乙醇,震荡混匀10-20s,瞬时离心;
(3)将步骤(2)所得的液体放于离心柱中,放入2ml收集管,6000-9000rpm离心0.5-2min;
样本量>140μl情况下,重复上述步骤(3)一至二次;
(4)加入300-600μl洗脱缓冲液1,6000-9000rpm,0.5-2min,弃滤液及收集管,换新的收集管;
(5)加入300-600μl洗脱缓冲液2,10000-15000rpm,离心1-5min,弃滤液及收集管;
(6)换新的1.5ml液离心管,空离10000-15000rpm,离心0.5-2min,弃滤液及离心管;
(7)换一新的1.5ml离心管,加入50-100μl洗脱缓冲液3,室温放置0.5-2min,6000-9000rpm离心0.5-2min得到待测微量生物样本的dna
其中:
所述裂解缓冲液为含10%sds的tris饱和酚;
所述洗脱缓冲液1的配方为:饱和酚:氯仿:异戊醇以体积比25:24:1的混合液;
所述洗脱缓冲液2为无水乙醇;
所述洗脱缓冲液3为ph8.0,含1mmol/ledta的10mmol/ltris-hcl溶液。
优选地,所述步骤如下:
(1)将待测微量生物样本放入容器中,加入20μl蛋白酶k、200μl裂解缓冲液,于56℃处理至少10分钟;
(2)加入与裂解缓冲液等体积的无水乙醇,震荡混匀10-20s,瞬时离心;
(3)将步骤(2)所得的液体放于离心柱中,放入2ml收集管,6000-9000rpm离心0.5-2min;如果样本量>140μl,重复上述步骤(3);
(4)加入500μl洗脱缓冲液1,8000rpm,离心1min,弃滤液及收集管,换新的收集管;
(5)加入500μl洗脱缓冲液2,14000rpm,离心3min,弃滤液及收集管;
(6)换新的1.5ml液离心管,空离14000rpm,离心1min,弃滤液及离心管;
(7)换新的1.5ml离心管,加入50-100μl洗脱缓冲液3,室温放置1min,离心8000rpm,1min得到待测微量生物样本的dna。
优选地,所述待测微量生物样本为液体状样本,步骤(1)中于56℃处理10min之后,再放入70℃环境中处理10min。
优选地,所述待测微量生物样本为固体状组织,步骤(1)中于56℃处理5-12个小时。
优选地,其特征在于,所述液体样本指眼部分泌物、房水、泪液和/或玻璃体;所述固体组织指视网膜、角膜内皮、翼状胬肉、结膜、虹膜和/或眼部肿物。
本发明的另一方面,公开一种用于制备微量生物样本dna模板的试剂组合,其特征在于,包含如下试剂;
裂解缓冲液:含10%sds的tris饱和酚,
洗脱缓冲液1:饱和酚:氯仿:异戊醇以体积比25:24:1的混合液;
洗脱缓冲液2:无水乙醇,
洗脱缓冲液3:ph8.0,含1mmol/ledta的10mmol/ltris-hcl溶液,
所述眼部微量样本指体积不超过10ul-200ul的液体样本或体积不超过1mm3的固体类样本;
所述液体样本指眼部分泌物、房水、泪液和/或玻璃体;
所述固体组织指视网膜、角膜内皮、翼状胬肉、结膜、虹膜和/或眼部肿物。
本发明的再一方面,公开一种用于检测眼部微量样本hsv感染的pcr扩增试剂,其特征在于:包含以下引物探针组,序列如下:
primer-f:ccataaactgggagtagcggt
primer-r:gtggtcttcaaggagaacatc
探针:cgccccgtacaagttcaagg
所述眼部微量样本指体积不超过10ul-200ul的液体样本或体积不超过1mm3的固体类样本;
所述液体样本指眼部分泌物、房水、泪液和/或玻璃体;
所述固体组织指视网膜、角膜内皮、翼状胬肉、结膜、虹膜和/或眼部肿物。
优选地,用于每个反应的pcr扩增体系含有:
所述pcr扩增试剂在使用前加入眼部微量样本dna模板及蒸馏水使反应总体积达到20个体积单位。优选地,所述体积单位可以是1微升、1.5微升、2微升或2.5微升。
本发明的再一方面,提供一种用于通过眼部微量样本检测眼部hsv感染的试剂盒,其特征在于:包含
前述任一用于检测眼部微量样本hsv感染的扩增试剂,
以及前述的用于制备用于制备眼部微量样本dna模板的试剂组,
其中所述眼部微量样本指体积不超过10ul-200ul的液体样本或体积不超过1mm3的固体类样本。
优选地,还包含为每个检测反应设置对照反应的对照模版,具体如下:
阳性对照模版:hsv病毒dna片段,用于对检测体系和仪器的质量控制,保证结果的准确性,避免假阴性结果
阳性对照模版:阳性眼部体液;
空白对照模版:超纯水;
阴性对照模版:阴性眼部液体样本;
弱阳性对照模版:阳性眼部体液的稀释液,其临界值设置在△t=38-40。
本发明还提供一种用于通过眼部微量样本检测眼部hsv感染的pcr方法,其特征在于,
采用前述任一制备方法制备眼部微量样本dna模板;
采用前述任一的pcr扩增试剂或者前述任一的试剂盒对所述眼部微量样本dna模板进行实时定量pcr检测。
优选地,所述pcr反应的程序如下:
37℃×2min
94℃×2min,上述两个温度和时间循环40次
93℃×15sec,
60℃检测荧光。
本发明一个主要的贡献在于,提出了以取自眼部的微量样本为材料提取dna制备pcr模板,并采用实时定量pcr(realtime-pcr)检测眼部病毒感染。
由于眼部结构复杂,且受血脑屏障影响,眼部组织标本的很多检测指标与血液的检测指标相关性很低,大量临床数据研究发现,血液检查不能准确反映眼部的真实病因,特别是感染性眼病的病因;另一方面,眼部标本体积微小,标本种类多种多样,包括各种组织、各种体液(玻璃体、房水、泪液等)、各种膜类(视网膜、角膜内皮等)、多部位分泌物等,其中固体标本一般不超过1mm3;除了泪液,眼部液体标本一般能取的量约为20-100ul,最多不超过200ul,很难满足血液、尿液检验所要求的大体积和均一种类的要求,因此对眼部标本采用常规血液检测方法进行检测,假阴性比例非常高,常常延误治疗。目前尚未见到适合于微量标本,特别是适合取自眼部各种形态的微量标本的病毒检测技术。
基于此,发明人摸索了适合微量组织样本的dna提取方法,从提取试剂如蛋白酶k、裂解液、洗脱缓冲液的体积、时间、温度,用量方面进行了摸,提出一种简便易于操作的提取微量组织dna的方法,该方法适合提取眼部多种临床标本的dna模版,所得模板用于本发明的pcr检测,能够高灵敏地检测出眼部微量组织中的hsv病毒感染情况。
比如10ul泪液中的dna,其足够作为4个pcr反应的模版,并且成功地通过泪液检测了解到眼部的病毒感染情况。该方法该dna提取方法,不仅仅适用于眼部多种微量标本,对于难以获得的其它生物标本,比如取自婴儿的组织样本,微小生物的组织样本,都非常适合,对患者无创或者创伤最小化。
本发明另一个主要的贡献在于,还提供一种用于检测病毒感染,特别是hsv感染的试剂盒,以及提供了检测hsv的pcr扩增试剂,引物探针组,结合上述dna提取方法,进行检测。实验数据显示,无论是当时采集的临床眼部微量样品,还是采集24-48小时以上从其它城市医院或医院送来的多种眼部微量样品,都能够稳定、灵敏地检测hsv感染情况,方法具有良好的稳定性和可靠性。
鉴于眼部样本的微量、珍贵,为了减少检测过程中由于人为操作失误、试剂污染、失效等原因引起的结果误判以及样本浪费。本发明的试剂盒优选实施例中,为每个检测反应设置了多个对照模版,其中:
阳性对照模版:试剂盒中阳性对照品,是已知病毒dna;作用是质控检测体系,试剂及设备的有效性,防止假阴性结果
阳性对照模版:阳性眼部体液;用于提示眼部标本检测体系的有效性,从而排除假阴性。
空白对照模版:超纯水;用于提示反应试剂中是否存在污染,从而同时结果是否存在提示假阳性。
阴性对照模版:阴性眼部液体样本;用于显示眼部标本正常存在的噪音,并提示是否有污染导致的假阳性。
弱阳性对照模版:由于眼部标本体积微小,阳性弱,因此要做弱阳性对照,来判定检测的灵敏度。
本发明的再一个主要的贡献在于,提供一种检测微量组织样本中hsv感染的pcr方法,在pcr体系和程序上作出了调整,能够准确检测到微量样本中的hsv感染情况。
附图说明
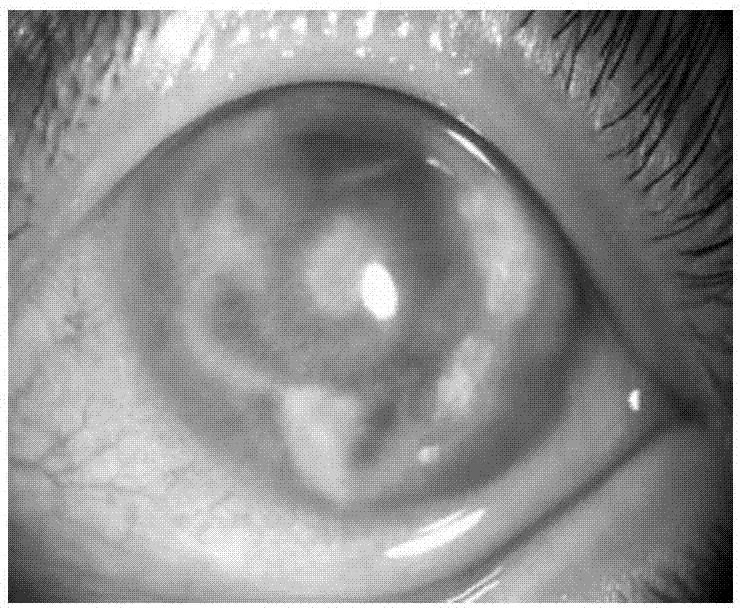
图1.hsv病毒性角膜炎患者的眼球,
其中可见中央区混浊及水肿消退。采用本发明的方法对眼部标本进行病毒检测确诊后,对眼内局部及全身抗病毒药联合1%醋酸泼尼松龙一个月后改用0.1%艾氟治疗两个月。
图2.是图1所示眼球确诊后经治疗,中央区混浊及水肿消退,视恢复至0.8。
图3.其中一例待测样本的hsv感染pcr检测结果示意图。
具体实施方式
以下通过具体实施例示例性说明本发明的技术方案,但不作为对本发明专利权范围的限制。
裂解缓冲液:含10%sds的tris饱和酚,
洗脱缓冲液1:饱和酚:氯仿:异戊醇以体积比25:24:1的混合液;
洗脱缓冲液2:无水乙醇,
洗脱缓冲液3:ph8.0,含1mmol/ledta的10mmol/ltris-hcl溶液。
对照核酸提取试剂盒:购自达安基因股份有限公司。
对照血清hsv检测试剂盒:购自达安基因股份有限公司。
实施例1.眼部微量液体待测标本dna提取方法
材料:
待测标本:采集自收治患者,泪液、房水2、玻璃体。
(1)将采集的待测标本放入容器中,加入10-30μl蛋白酶k、100-300μl裂解缓冲液al,于56℃处理10分钟以上;
(2)加入与裂解缓冲液等体积的无水乙醇,震荡混匀10-20s,瞬时离心;
(3)将步骤(2)所得的液体放于离心柱中,放入2ml收集管,6000-9000rpm离心0.5-2min;
如果样本量>140μl,重复步骤(3);
(4)加入300-600μl洗脱缓冲液1,6000-9000rpm,0.5-2min,弃滤液及收集管,换新的收集管;
(5)加入300-600μl洗脱缓冲液2,10000-15000rpm,离心1-5min,弃滤液及收集管;
(6)换新的1.5ml液离心管,空离10000-15000rpm,离心0.5-2min,弃滤液及离心管;
(7)换一新的1.5ml离心管,加入50-100μl洗脱缓冲液3,室温放置0.5-2min,离心6000-9000rpm,0.5-2min得到待测微量生物样本的dna模版,最终能获得50-100μldna模版。
(8)取1ul样品,通过dna含量检测仪器nanodrop2000检测od260、od280,计算得到dna浓度为30-70ng/μl)
对照:采用核酸提取试剂盒购自上海之江生物科技有限公司。作为对照试剂,根据其说明书操作dna提取以及pcr扩增。
检测结果:
可以看出,采用常规试剂盒提取眼部微量样本,所得dna纯度显著低于本发明方法所得提取物。特别是对照方法所得提取物的od280值明显高于本发明方法所得提取物的od280值。说明本发明提供的dna提取方法能够有效地将dna与其它细胞成分及蛋白分离,针对微量样本的特殊性,该步骤的改进是pcr检测方法灵敏度、特异性高的保障。
实施例2.眼部微量固体待测标本dna提取方法
材料:
待测标本:采集自收治患者,角膜内皮、翼状胬肉、结膜分泌物、眼部肿物,采集量约为1×1mm;
步骤:
(1)将采集的待测标本放入容器中,加入10-30μl蛋白酶k、100-300μl裂解缓冲液al,于56℃处理6-12小时;
(2)加入与裂解缓冲液等体积的无水乙醇,震荡混匀10-20s,瞬时离心;
(3)将步骤(2)所得的液体放于离心柱中,放入2ml收集管,6000-9000rpm离心0.5-2min;
(4)加入300-600μl洗脱缓冲液1,6000-9000rpm,0.5-2min,弃滤液及收集管,换新的收集管;
(5)加入300-600μl洗脱缓冲液2,10000-15000rpm,离心1-5min,弃滤液及收集管;
(6)换新的1.5ml液离心管,空离10000-15000rpm,离心0.5-2min,弃滤液及离心管;
(7)换一新的1.5ml离心管,加入50-100μl洗脱缓冲液3,室温放置0.5-2min,离心6000-9000rpm,0.5-2min得到待测微量生物样本的dna80μl。
(8)取1ul样品,通过dna含量检测仪器nanodrop2000检测od260、od280。
对照:采用核酸提取试剂盒购自达安基因股份有限公司。作为对照试剂,根据其说明书操作dna提取。
检测结果:
可以看出,采用常规试剂盒提取眼部微量样本,所得dna纯度比本发明方法所提得提取物的低。对照方法提取结膜囊分泌物,眼部肿物所得的提取物的od280值得明显高于本发明,即提取物中蛋白质或氨基酸含量较高,用作扩增模版,容易影响扩增的灵敏度。而本发明的方法对于取自眼部的各种组织微量样本,都能够获得高纯度模版。
实施例3.用于通过眼部微量样本检测眼部hsv感染的试剂盒
dna提取试剂组:
裂解缓冲液:含10%sds的tris饱和酚,
洗脱缓冲液1:饱和酚:氯仿:异戊醇以体积比25:24:1的混合液;
洗脱缓冲液2:无水乙醇,
洗脱缓冲液3:ph8.0,含1mmol/ledta的10mmol/ltris-hcl溶液。
用于pcr扩增的特异性引物和探针
primer-f:ccataaactgggagtagcggt
primer-r:gtggtcttcaaggagaacatc
探针:cgccccgtacaagttcaagg
实施例4.用于通过眼部微量样本检测眼部hsv感染的试剂盒
1.dna提取试剂组:
裂解缓冲液:含10%sds的tris饱和酚,
洗脱缓冲液1:饱和酚:氯仿:异戊醇以体积比25:24:1的混合液;
洗脱缓冲液2:无水乙醇,
洗脱缓冲液3:ph8.0,含1mmol/ledta的10mmol/ltris-hcl溶液。
2.用于pcr扩增的特异性引物和探针:
primer-f:ccataaactgggagtagcggt;
primer-r:gtggtcttcaaggagaacatc。
探针:cgccccgtacaagttcaagg
3.pcr扩增对照模版:
阳性对照模版:已知hsv病毒dna片段(对照试剂盒自带)对检测体系和仪器的质量控制,保证结果的准确性,避免假阴性结果;
阳性对照模版:阳性眼部液体样本;
弱阳性对照模版:阳性眼部体液的稀释液,其临界值设置在△t=38-40。
空白对照模版:超纯水;
阴性对照模版:阴性眼部液体样本;
实施例5.标本中hsv病毒的检测方法的建立
标本为临床诊断为血液中感染hsv的患者血清,共5例。
步骤1.采用实施例1中的方法制备样本dna模板:
步骤2.引物探针:
primer-f:ccataaactgggagtagcggt
primer-r:gtggtcttcaaggagaacatc
探针:cgccccgtacaagttcaagg
步骤3:反应体系配制
并设置5个对照反应管,反应体系同上,模板分别为:
阳性对照模版:已知hsv病毒dna片段(对照试剂盒自带)
阳性对照模版:阳性眼部液体样本;
弱阳性对照模版:阳性眼部体液的稀释液,其临界值设置在△t=38-40。
空白对照模版:超纯水;
阴性对照模版:阴性眼部液体样本;
步骤4.pcr程序:
37℃2min
94℃2min
循环上述两个温度和时间,循环30-40次
93℃15sec,60℃检测荧光
对照方法:
同样的5例血清试剂:
对照提取方法:采用核酸提取试剂盒购自达安基因股份有限公b。作为对照试剂,根据其说明书操作dna提取。
对照检测方法:以医院常用的血清hsv检测试剂盒作为对照方法,购自达安基因股份有限公司,步骤为试剂盒内附实验步骤。
检测结果如下表:
表格中,随着血清标本量递减至10微升,本发明的方法对于液体标本的最低检测限为10ul;可见本发明的检测方法检测准确性4/5=0.80,即80%。
对照试剂盒仅仅能检测2ml血清标本量,随着样本量递减,无法获得有意义的检测结果。
同样也进行了“对照提取方法+本发明pcr方法”:结果与“对照提取方法+对照检测方法”的结果一致,说明现有常规方法提取大量样本所得模板液可以进行有效检测,但是当样本量无法达到毫升级别时,提取所得模板液不能进行有效检测。
实施例6临床眼部标本检测验证
dna来自临床收治患者眼部标本,提取方法见实施例1.
实验方法同实施例5。
对照方法:医院常用的血清hsv检测试剂盒作为对照方法,购自达安基因股份有限公司,步骤为试剂盒内附的实验操作步骤。
检测结果如下:
图3示意了其中一例阳性样本的检测结果:阳性检测样本与弱阳性对照相近。
实施例7眼部病毒感染和血液中病毒感染有较大差异
样本:来自1名临床收治患者不同阶段的房水和血液
检测方法:本发明方法:dna来自临床收治患者的眼部标本和血液,提取方法见实施例1。
对照方法:采用医院常用的血清hsv检测试剂盒作为对照方法,购自达安基因股份有限公司,步骤为试剂盒内附实验步骤。
样本检测结果
第一阶段治疗前:眼部和静脉血均检出hsv阳性;
第二阶段:是根据常规治疗方法,对患者给予全身抗hsv病毒药-1%醋酸泼尼松龙一个月后改用0.1%艾氟治疗两个月之后对眼部标本和静脉血检测,结果显示经治疗后血液中hsv转阴,但是全身抗病毒治疗对眼部hsv感染无效。
第三阶段:在眼内局部给予抗病毒药物一次或几次后,对眼部标本和静脉血检测,眼部hsv感染转阴。
以上数据显示,眼部感染情况和血液感染并不同步。如果按照目前医院常用检测方法仅仅检测血液感染,根据检测结果对全身整用抗病毒药,对于眼部感染并不管用。因此,准确检出眼部感染是有效治疗的关键。
而采用常规方法和试剂盒检测眼部标本,检测不到眼部hsv感染,也就无法对其眼部进行对应的治疗。
检测后治疗
采样本发明检测方法检测呈hsv感染阳性的患者,对其给予针对hsv的个体化治疗方案,如给予感染部位局部更昔洛韦、阿昔洛韦等抗病毒药物注射,并于给药后定期采集眼部标本进行病毒检测,检测用药后病毒dna情况,根据检测结果进行用药周期、浓度的调整,直至检测结果转阴,如图1-2所示:
图1.hsv病毒性角膜炎患者的眼球,其中可见中央区混浊及水肿消退。采用本发明的方法对眼部标本进行病毒检测确诊后,对眼内局部及全身抗病毒药联合1%醋酸泼尼松龙一个月后改用0.1%艾氟治疗两个月。
图2.是图1所示眼球确诊后经治疗,中央区混浊及水肿消退,视恢复至0.8.
说明本发明的方法能够超越常规技术,准确检测眼部微量样本中的低浓度病毒感染,从而为后续治疗方案提供准确依据。
sequencelisting
<110>北京大学第三医院
<120>微量生物样本dna模板的制备方法及眼部hsv感染检测试剂盒
<130>p170281-bys
<160>3
<170>patentinversion3.3
<210>1
<211>21
<212>dna
<213>artificialsequence
<220>
<223>primer-f
<400>1
ccataaactgggagtagcggt21
<210>2
<211>21
<212>dna
<213>artificialsequence
<220>
<223>primer-r
<400>2
gtggtcttcaaggagaacatc21
<210>3
<211>20
<212>dna
<213>artificialsequence
<220>
<223>探针
<400>3
cgccccgtacaagttcaagg20
- 还没有人留言评论。精彩留言会获得点赞!