一种抗氧化及耐高温胁迫的非编码RNAOsiR及其用途的制作方法
本发明属于基因工程技术领域,具体涉及一种抗氧化及耐高温胁迫的非编码RNA osiR基因的及其用途。
背景技术:
细菌非编码RNA(non-conding RNA,ncRNA),是一些大小在40-500个核苷酸范围内的分子量相对较小的非编码RNA分子,通常位于蛋白编码基因的间区,具有茎-环形成的复杂高级结构,大多数具有不依赖于ρ因子的终止子结构。近年来的研究发现,细菌中非编码RNA可以作为转录后调控因子,通过多种机制调控基因的表达,在生命活动中发挥着重要作用。
技术实现要素:
本发明发现了一种非编码RNA新基因,其表达受氧化胁迫诱导,参与细菌的抗氧化及耐高温胁迫过程,命名为osiR基因,该基因大小为251bp,Genbank ID:MF964218。非编码RNA osiR基因的DNA序列为SEQ ID NO:1,其转录的RNA序列如SEQ ID NO:2所示。
本发明发现该RNA基因在工程菌株改造方面具有广泛的应用潜力,可特异响应氧胁迫信号,明显提高菌株的抗氧化能力,并能够显著提高宿主菌的高温胁迫抗性。
具体发明工作如下:
1.构建表达osiR基因的重组工程菌株
1)通过PCR克隆出的完整的osiR基因的DNA片段序列进行酶切,插入表达载体pRADZ3中,构建重组质粒pRADZ3-OsiR。
2)将导入osiR基因的重组质粒pRADZ3-OsiR转入受体大肠杆菌Trans10,获得工程菌株Trans-OsiR(详见实施例1);
2、表达osiR基因重组工程菌株Trans-OsiR的胁迫抗性分析
1)利用不同浓度的H2O2进行冲击,研究重组工程菌株Trans-OsiR的氧化胁迫抗性(详见实例2)
2)利用48℃摇床培养,研究重组工程菌株Trans-OsiR的高温胁迫抗性(详见实例3)
实验结果表明:非编码RNA osiR基因能够显著提高宿主细胞抵抗氧化胁迫和高温胁迫的能力,在提高菌株胁迫抗性方面具有良好的应用前景。
序列表信息
SEQ ID NO.1:非编码RNA osiR基因的DNA序列。
SEQ ID NO.2:非编码RNA osiR基因转录后的RNA序列。
附图说明:
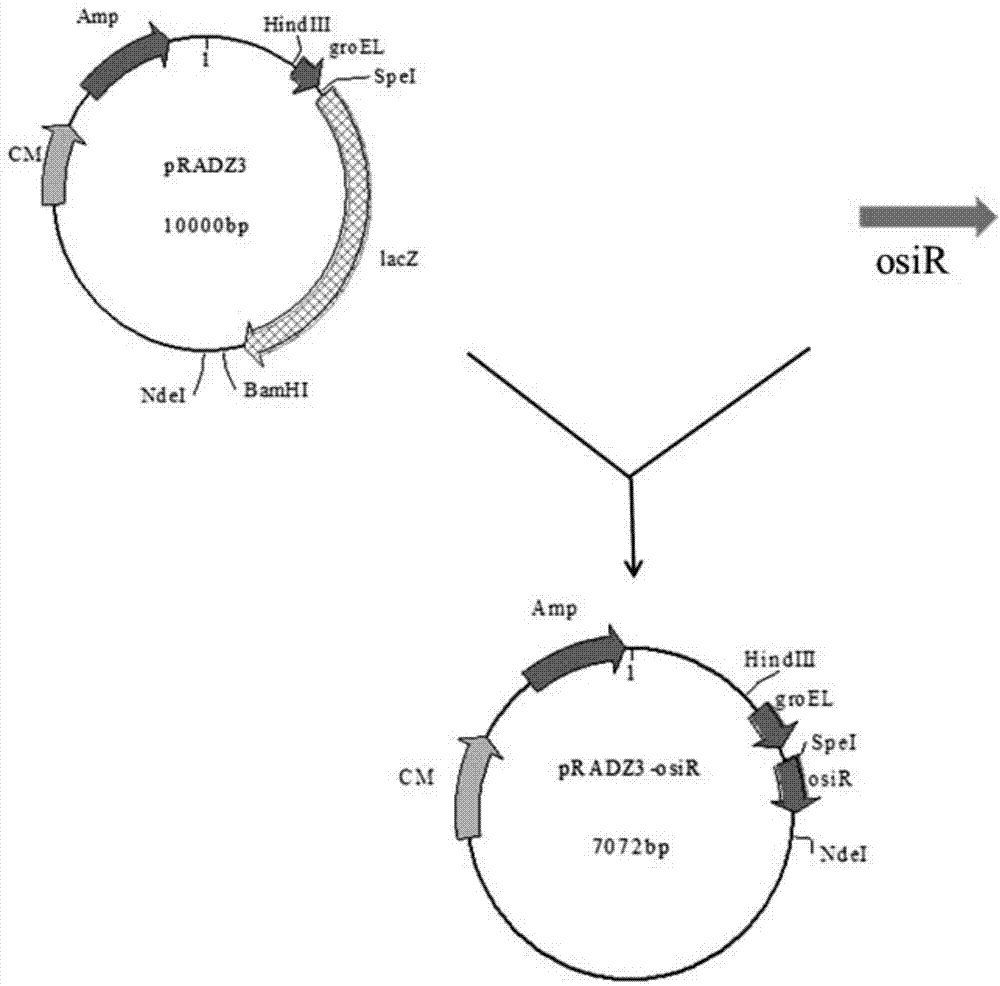
图1重组表达载体pRADZ3-OsiR构建示意图;
图2重组表达载体pRADZ3-OsiR双酶切验证图。M1:Trans 15K maker;M2:Trans 100bp maker;1:pRADZ3-OsiR未酶切;2:pRADZ3-OsiR双酶切;
图3表达OsiR的工程菌Trans-OsiR的氧化胁迫抗性图。Trans-OsiR为表达osiR的重组菌株;Trans-Z3为含有空载体的对照菌株;
图4表达OsiR的工程菌Trans-OsiR的高温胁迫抗性图。Trans-OsiR为表达osiR的重组菌株;Trans-Z3为含有空载体的对照菌株。
具体实施方式
下面结合具体实施例,进一步阐述本发明。应理解,这些实施例仅用于举例说明本发明的方法,而不用于限制本发明的范围。凡未注明具体实验条件的,均为按照本领域技术人员熟知的常规条件。
穿梭质粒pRADZ3:本实验室保存;
大肠杆菌Trans10:为北京全式金公司市售产品。
实施例1表达osiR基因的大肠杆菌重组工程菌株的构建
一、实验材料
大肠杆菌Trans10:为北京全式金公司市售产品。
PCR模板DNA:耐辐射异常球菌基因组DNA
二、实验方法
1.根据已公布的耐辐射异常球菌基因组设计1对PCR特异性引物:
OsiR-F:5’CGGACTAGTGACATGTATTCGTCTGACC 3’
OsiR-R:5’CGCCATATGCCTGGCCGAGCTCACCGG 3’
2.通过PCR方法从耐辐射异常球菌基因组DNA中扩增出目的基因序列。
反应条件:95℃10min,[95℃30sec,58℃30sec,72℃0.5min]35个循环,72℃10min。
3.PCR产物经胶回收后,利用SpeI和NdeI酶进行双酶切。获得含有粘性末端的osiR基因,连接于pRADZ3载体上,构建大肠杆菌高表达载体pRADZ3-OsiR(图1)。将该表达载体转化大肠杆菌Trans10,构建表达osiR基因的重组工程菌株。挑去阳性克隆菌株,提取质粒DNA筛选不同的重组子,利用SpeI和NdeI酶进行双酶切及测序验证。
三、实验结果
利用PCR技术成功克隆了耐辐射异常球菌osiR基因,成功构建了表达osiR的重组大肠杆菌工程菌株。经PCR、酶切,测序验证插入序列正确,将该菌株命名为Trans-OsiR。含有pRADZ3空质粒的对照菌株命名为Trans-Z3。
四、实验结论
完成表达osiR的重组大肠杆菌工程菌株的构建。
实施例2表达osiR基因重组工程菌株Trans-OsiR的氧化胁迫抗性分析
一、实验材料
重组工程菌株:实施例1得到的表达osiR基因的Trans-osiR菌株
对照菌株:实施例1所述含空质粒的Trans-Z3菌株。
二、实验方法
1.培养
分别挑取固体平板上单菌落接种于含Amp的液体LB培养基中,37℃恒温摇床培养过夜
2.氧化胁迫(H2O2冲击)
将种子液转接于新的LB培养基,培养至OD600约0.6左右。各取1mL菌体加入终浓度为10、15、20mM H2O2冲击10min,
3.结果观测,与空白对比
每个处理进行倍比梯度稀释至10-5。未经氧化处理的样品为空白对照。吸取每个处理的稀释梯度样品8μL点在LB固体平板上,37℃培养观测菌株的氧化胁迫抗性。
三、实验结果
如图3所示:
10mM H2O2氧化胁迫下,重组菌株Trans-OsiR与对照菌株Trans-Z3相比,其生存率提高了10倍。
15mM和20mM浓度的H2O2氧化胁迫下,重组菌株Trans-OsiR与对照菌株Trans-Z3相比,其生存率提高了2个数量级,约100倍。
四、实验结论
H2O2氧化冲击实验结果显示,非编码RNA基因osiR的表达显著提高宿主大肠杆菌的氧化胁迫抗性。
实施例3表达osiR基因重组工程菌株Trans-OsiR的高温胁迫抗性分析
一、实验材料
重组工程菌株:实施例1得到的表达osiR基因的Trans-OsiR菌株
对照菌株:实施例1所述含空质粒的Trans-Z3菌株。
二、实验方法
1.培养
分别挑取固体平板上单菌落接种于含Amp的液体LB培养基中,37℃恒温摇床培养过夜。
2.48℃高温胁迫
将种子液转接于新的LB培养基,培养至OD600约0.8左右。各取5mL菌液放置于48℃摇床冲击4h。
3.结果观测,与空白对比
每个处理进行倍比梯度稀释至10-5。未经氧化处理的样品为空白对照。吸取每个处理的稀释梯度样品8μL点在LB固体平板上,37℃培养观测菌株的高温胁迫抗性。
三、实验结果
如图4所示:
48℃高温胁迫下,重组菌株Trans-OsiR与对照菌株Trans-Z3相比,其生存率提高了2个数量级,约100倍。
四、实验结论
48℃高温冲击实验结果显示,非编码RNA基因osiR的表达显著提高宿主大肠杆菌的高温胁迫抗性。
序列表
<110> 中国农业科学院生物技术研究所
<120> 一种抗氧化及耐高温胁迫的非编码RNA OsiR及其用途
<160> 2
<170> PatentIn version 3.1
<210> 1
<211> 251
<212> DNA
<213> 耐辐射异常球菌(Deinococcus radiodurans)
<400> 1
atgtattcgt ctgacctcga cctcaccacc aaagccctca tgcgcgaaca ggcccttcac 60
gagccgcagg ccatgacctc atgggaagct catgaccgcc gcgaaagccg cagcgtgcgc 120
cgcgccctga actggctgga acgccgcctg cgccggagcg cttgaggccg catcatttgc 180
ccacgcagaa gttgcgaaac acagcgtcca ccacatcttc ctgcacgtcc tgaccggtga 240
gctcggccag g 251
<210> 2
<211> 532
<212> RNA
<213> 耐辐射异常球菌(Deinococcus radiodurans)
<400> 2
auguauucgu cugaccucga ccucaccacc aaagcccuca ugcgcgaaca ggcccuucac 60
gagccgcagg ccaugaccuc augggaagcu caugaccgcc gcgaaagccg cagcgugcgc 120
cgcgcccuga acuggcugga acgccgccug cgccggagcg cuugaggccg caucauuugc 180
ccacgcagaa guugcgaaac acagcgucca ccacaucuuc cugcacgucc ugaccgguga 240
gcucggccag g 251
- 还没有人留言评论。精彩留言会获得点赞!