一种用于肝癌早期筛查的试剂盒及其使用方法与流程
本发明属于分子生物学领域,具体涉及一种用于肝癌早期筛查的试剂盒及其使用方法。
背景技术
肝细胞肝癌(hepatocellularcarcinoma,hcc)是威胁人类生命常见的恶性肿瘤之一,而多数原发性肝癌患者早期症状不明显,确诊时大多数患者已经达到中晚期,因此实现早期诊断、获得根治性切除是患者长期生存的唯一希望。由于缺乏特异性的肿瘤标志物,多数患者确诊时已属晚期,丧失了根治性切除的机会。
目前,肝癌诊断方法包括影像学检查、病理学检查及实验室检查。但早期肝癌影像学表现不典型,且部分检查具有辐射性及价格昂贵的缺点。肝穿刺活组织检查是诊断hcc的金标准,但早期肝癌病灶小,穿刺活检难度大,且具有一定程度的创伤性,不易被患者接受。肿瘤标志物检测对肝癌影像学及病理学诊断具有重要的补充价值,并且通过监测肝癌标志物,能比其他方法提前发现肿瘤或肿瘤的复发、转移,提高预测和诊断的准确性,从而提高疗效,改善预后。在原发性肝癌诊断中,临床应用最广泛的肿瘤标志物是甲胎蛋白(afp),但其诊断敏感性和特异性不太令人满意,诊断肝癌的灵敏度和特异度分别为41%~65%和80%~94%。
近年来的研究发现,肿瘤患者外周血浆中存在游离的肿瘤dna,并且具有与肿瘤细胞dna相同的基因改变,因此检测肿瘤患者外周循环dna为肿瘤的早期微创诊断提供了新的手段。
afp仍是临床应用最为普遍的诊断肝癌的肿瘤标志物,其以400μg/l为临床诊断肝癌临界值;afp≥400μg/l时,诊断率较高;而对于部分早期、可切除患者,即afp<400μg/l易被漏诊。因而,寻求灵敏度和特异度更高的肿瘤标志物对肝癌的早期诊断具有重要意义,尤其对afp<400μg/l患者。
技术实现要素:
本发明主要目的是,提供一种用于肝癌早期筛查的试剂盒及其使用方法。本发明首次发现scand3的甲基化程度与肝癌发生相关,并且可通过检测外周血中scand3甲基化程度,用于肝癌的早期检测和诊断。
为了实现上述目的,本发明采用以下技术方案:
本发明目的之一,提供一种用于肝癌早期筛查的甲基化标志物,所述甲基化标志物为scand3。
本发明目的之二,提供以上所述的甲基化标志物在制备肝癌早期筛查诊断试剂中的应用。
本发明目的之三,提供一组用于检测以上所述甲基化标志物的引物及探针,所述引物序列如下:正向引物序列如seqidno.1所示,反向引物序列如seqidno.2所示;所述荧光探针序列为seqidno.3,探针5′端标记fam,3′端标记mgb。
本发明目的之四,提供以上所述的引物及探针在制备用于肝癌早期筛查的试剂盒的应用。
本发明目的之五,提供一种试剂盒,包括以上所述的引物及探针,还包括检测gapdh的正向引物及探针,pcrmastermix,裂解液,蛋白酶k,漂洗液,亚硫酸氢盐溶液和ddh2o。
本发明目的之六,提供以上所述试剂盒的使用方法,步骤如下:
(1)样本中基因组dna的提取:取患者样本,利用裂解液、蛋白酶k、漂洗液和ddh2o提取,得基因组dna溶液;
(2)dna甲基化修饰:取步骤(1)提取得到的基因组dna溶液用亚硫酸氢盐溶液进行修饰,得到甲基化修饰后的dna;
(3)将步骤(2)修饰后的dna进行pcr扩增。
优选的,步骤(1)所述样本为外周血细胞。
优选的,pcr反应液为:pcrmastermix20μl,引物及探针各1μl,荧光定量反应液3μl,总量/人份26μl;pcr反应条件为:
本发明目的之七,提供所述的试剂盒在制备肝癌早期筛查试剂中的应用。
本发明目的之八,提供所述试剂盒在制备检测scand3甲基化试剂中的应用
外周血中存在游离的肿瘤dna,通过检测外周血中基因的甲基化程度来诊断肝癌,不但可以减轻肝癌患者诊断的痛苦,而且可实现对肝癌的早期、快速诊断,利于患者早发现早治疗。但是外周血中不同基因甲基化程度不一定能真实反映组织的真实甲基化情况。本发明人在探究基因甲基化与肝癌发生的关系中,筛选得到scand3基因,通过实验首次发现该基因甲基化程度与肝癌的发生相关。在进一步研究中,发现scand3基因在afp<400μg/l肝癌患者中甲基化程度较高,高于已知肝癌标志物基因slit2和dapk,由此可知,scand3在肝癌的早期诊断更具潜力。
与现有技术相比,本发明具有以下优势:
(1)本发明以scand3为靶基因,用于肝癌诊断,具有灵敏度高和特异性强的优点,尤其是在afp<400μg/l患者中,scand3甲基化发生率高达60%;由此可知,本发明以scand3为靶基因,适用于肝癌的诊断,尤其适用于早期肝癌的诊断。
(2)本发明以患者外周血为样本,为微创诊断,可大大减少患者疼痛程度,降低患者诊断费用,并且可以实现快速诊断。
附图说明
构成本发明的一部分的说明书附图用来提供对本发明的进一步理解,本发明的示意性实施例及其说明用于解释本发明,并不构成对本发明的不当限定。
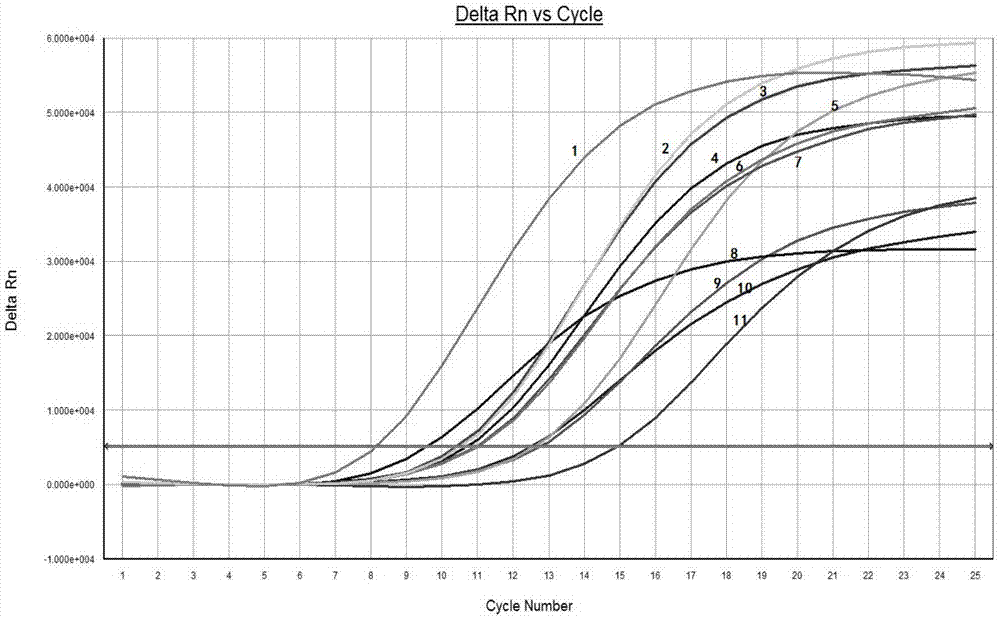
图1为rt-pcr扩增曲线图:1-7为afp≥400μg/l肝癌患者样品中1-7号样品,8-11为afp<400μg/l肝癌患者中11-14号样品。
具体实施方式
应该指出,以下详细说明都是示例性的,旨在对本发明提供进一步的说明。除非另有指明,本文使用的所有技术和科学术语具有与本发明所属技术领域的普通技术人员通常理解的相同含义。
需要注意的是,这里所使用的术语仅是为了描述具体实施方式,而非意图限制根据本发明的示例性实施方式。如在这里所使用的,除非上下文另外明确指出,否则单数形式也意图包括复数形式,此外,还应当理解的是,当在本说明书中使用术语“包含”和/或“包括”时,其指明存在特征、步骤、操作和/或它们的组合。
为了使得本领域技术人员能够更加清楚地了解本发明的技术方案,以下将结合具体的实施例与对比例详细说明本发明的技术方案。
实施例1scand3及其引物和探针
本发明首次发现scand3甲基化可用于肝癌的早期筛查和诊断。
用于检测scand3甲基化的引物序列如下:
正向引物序列为:5’-gttataaattgagcggtaagatatttgc-3’,如seqidno:1序列所示;
反向引物序列为:5’-cctcgcccaaactactccg-3’,如seqidno:2序列所示;,
荧光探针序列为:5’-aatcgaggttatgacggata-3’,如seqidno:3序列所示;荧光探针的5’端标记fam(荧光报告基团),3’端标记mgb(荧光淬灭基团)。
本发明筛选过程中所用其它引物及探针如下:
第一组引物及探针:
正向引物序列如seqidno.4所示(5’-gcgagatagaaaatcgaggttatgac-3’),
反向引物序列如seqidno.5所示(5’-tataaacccctctccctctccg-3’),
荧光探针序列为如seqidno.6所示(5’-aaggaaacgaagatcggagta-3’),荧光探针的5’端标记fam(荧光报告基团),3’端标记mgb(荧光淬灭基团)。
实施例2一种用于肝癌早期筛查的试剂盒
所述试剂盒包括正向引物,序列为如seqidno.1所示,反向引物,序列为seqidno.2以及荧光探针,序列为seqidno.3;所述探针5′端标记fam,3′端标记mgb;此外还包括检测gapdh的正向引物及探针,pcrmastermix,裂解液,蛋白酶k,漂洗液,亚硫酸氢盐溶液和ddh2o;检测gapdh的正向引物及探针可采用本领域内已知的引物及探针即可。
实施例3所述试剂盒的使用方法
实施例2所述试剂盒的使用方法,具体如下:
(1)外周血细胞基因组dna的提取:取外周血细胞,利用裂解液、蛋白酶k、漂洗液和ddh2o提取,得基因组dna溶液;
具体步骤为:
吸取200μl外周血样本,置于1.5ml离心管中,加入1ml裂解液1,然后持续涡旋振荡混匀1min,充分混匀,然后将1.5ml离心管置于70℃水浴5min。
将1.5ml离心管从水浴锅内取出,12,000rpm离心5min,缓慢吸取300μl上清液至新的1.5ml离心管中。
向新的1.5ml离心管中依次加入200μl裂解液2和20μl蛋白酶k,涡旋混匀。
将新的1.5ml离心管置于70℃水浴10min。
添加200μl异丙醇,涡旋混匀。
将上一步所得溶液全部加入一个吸附柱中(将吸附柱套入收集管中),12,000rpm离心30sec,弃废液。
向吸附柱中加入600μl漂洗液,12,000rpm离心30sec,弃废液。
重复上述操作,12,000rpm离心2min,弃废液;将吸附柱室温静置2min,以彻底挥发吸附柱中残留的漂洗液。
将吸附柱转入1.5ml离心管中,向吸附膜中间位置悬空滴加50μl洗脱液,室温静置2min,12,000rpm离心2min,将溶液收集到离心管中。
(2)dna甲基化修饰:取步骤(1)提取得到的基因组dna溶液用亚硫酸氢盐溶液进行修饰,得到甲基化修饰后的dna;
将步骤(1)提取的dna洗脱液全部转移至0.2ml离心管中,添加150μl亚硫酸氢盐溶液;通过轻弹离心管或移液器轻柔吹打操作混匀后短暂离心。
将离心管放置于温度循环变温器中并按照以下条件设置:
①98℃10min
②64℃1.5h
③4℃(≦20h)
向吸附柱中加入500μl结合液,再将上一步的混合液转移至吸附柱中,盖上管盖并颠倒混匀,12,000rpm离心30sec,弃废液。
向吸附柱中加入600μl漂洗液,12,000rpm离心30sec,弃废液。
重复上述操作一次,12,000rpm离心2min,弃废液;将吸附柱室温静置2min,以彻底挥发吸附柱中残留的漂洗液。
将吸附柱转入1.5ml离心管中,向吸附膜中间位置悬空滴加30μl洗脱液,室温静置2min,12,000rpm离心2min后将溶液收集到离心管中。
(3)将步骤(2)修饰后的dna进行pcr扩增。
按照下列表格配置pcr反应液:
表1
pcr反应液充分混匀后,按每管26μl体积分装于pcr八联管中,并做好标记后转移至样本处理区。
将待检bisdna(甲基化转化后的dna)样本,按每孔2μl的量加入到分装好的pcr八联管中,压紧管盖,并短暂离心,将管壁液体离心至管底。
将pcr八联管放置在仪器样本槽的相应位置,并记录好摆放次序。仪器检测通道选择:reporterdye1:fam,quencherdye1:none;reporterdye2(gapdh)cy5,quencherdye2:none;passivereference:none。对应检测孔的设定:在扩增反应开始前,将待检样本和质控品设定为“unknown”。
按以下条件设置pcr反应
表2
试验例1
收集自芜湖达健医学检验实验室2017年5月~2018年5月临床病理诊断为肝癌患者(20人,其中afp<400μg/l患者10人,afp≥400μg/l)、肝炎患者(5人)及正常人(20人)的外周血。
按实施例3方法进行检测,各样本的详细检测结果的ct值见表3。
表3各样本荧光定量pcr检测结果的ct值
(2)根据表3,按照如下公式计算得到灵敏度和特异性:
灵敏度=检测结果为阳性的肝癌样本数/相应肝癌样本总数;
特异性=检测结果为阴性的非肝癌样本数/总的非肝癌样本总数;
结果如表4所示。
表4本发明检测肝癌的特异性和灵敏度
由表3、表4检测结果中可以看出,scand3在afp≥400μg/l肝癌患者中,检测灵敏度为70%,在afp<400μg/l肝癌患者中,检测灵敏度为60%。由上述结果可知,scand3在肝癌早期诊断中具有较好的应用潜力。
试验例2
以本发明试验例1所述的样本进行检测,采用实施例1中第一组引物及探针进行肝癌的检测,检测结果如下表5所示。
表5第一组引物特异性和灵敏度检测结果
由上述表5可知,与第一组引物及探针相比,本发明所用引物及探针具有更好的灵敏度和特异性。
最后说明的是,以上所述仅为本发明的优选实施例而已,并不用于限制本发明,尽管参照前述实施例对本发明进行了详细的说明,对于本领域的技术人员来说,其依然可以对前述实施例所记载的技术方案进行修改,或者对其中部分进行等同替换。凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。上述虽然对本发明的具体实施方式进行了描述,但并非对本发明保护范围的限制,所属领域技术人员应该明白,在本发明的技术方案的基础上,本领域技术人员不需要付出创造性劳动即可做出的各种修改或变形仍在本发明的保护范围以内。
sequencelisting
<110>安徽达健医学科技有限公司
<120>一种用于肝癌早期筛查的试剂盒及其使用方法
<130>
<160>6
<170>patentinversion3.3
<210>1
<211>28
<212>dna
<213>人工序列
<400>1
gttataaattgagcggtaagatatttgc28
<210>2
<211>19
<212>dna
<213>人工序列
<400>2
cctcgcccaaactactccg19
<210>3
<211>20
<212>dna
<213>人工序列
<400>3
aatcgaggttatgacggata20
<210>4
<211>26
<212>dna
<213>人工序列
<400>4
gcgagatagaaaatcgaggttatgac26
<210>5
<211>22
<212>dna
<213>人工序列
<400>5
tataaacccctctccctctccg22
<210>6
<211>21
<212>dna
<213>人工序列
<400>6
aaggaaacgaagatcggagta21
- 还没有人留言评论。精彩留言会获得点赞!