鸡胸软骨肽及其制备方法和应用与流程
本发明属于制药领域,具体涉及鸡胸软骨肽及其制备方法和用途,尤其是在制备治疗骨关节炎的药物中的应用。
背景技术:
:骨关节炎(osteoarthritis,oa)为一种退行性病变,系由于增龄、肥胖、劳损、创伤、关节先天性异常、关节畸形等诸多因素引起的关节软骨退化损伤、关节边缘和软骨下骨反应性增生,又称骨关节病、退行性关节炎、老年性关节炎、肥大性关节炎等。临床表现为缓慢发展的关节疼痛、压痛、僵硬、关节肿胀、活动受限和关节畸形等。骨关节炎的主要病理改变为软骨退行性变性和消失,以及关节边缘韧带附着处和软骨下骨质反应性增生形成骨赘,并由此引起关节疼痛、僵直畸形和功能障碍。该病在临床上,可分为原发性和继发性二类。原发性骨关节炎系指随年龄老化而不和其他疾病相关的关节病变,继发性骨关节炎则由损伤、炎症、遗传及代谢、内分泌等疾病所引起。骨关节炎的患病率随着年龄增长而增加,女性比男性多见。世界卫生组织统计,50岁以上人群中,骨关节炎的发病率为50%,55岁以上的人群中,发病率为80%。我国骨关节炎的发病情况约占总人口的10%,为1亿人左右。1990年,我国只有4000多万骨关节炎患者,而2000年已达到8000万,患者人数达到了1亿多人。目前市面上的骨关节炎药物以非甾体类药物为主。非甾体类抗炎药(nsaids)是指一类不含糖皮质激素而具有抗炎、解热、镇痛作用的药物,如阿司匹林,布洛芬,萘普生等。但非甾体类药物在骨关节炎的治疗中仅用于止痛,并不能完全阻止关节的损害及病情的恶化。此外非甾体类药物具有一定副作用,表现为容易产生眩晕、认知障碍、嗜睡、肝肾过敏发硬、恶心及增高血压的情况。技术实现要素:有鉴于此,本发明的目的在于针对现有技术的问题,提供一种鸡胸软骨多肽及其制备方法与在制备治疗骨关节炎的药物中的应用。为实现本发明的目的,本发明采用如下技术方案:一种鸡胸软骨肽,ⅱ型胶原蛋白含量≥50%,硫酸软骨素含量≥20%。本发明还提供了一种鸡胸软骨肽的制备方法,鸡胸软骨粉碎,加水,调节ph至7.0,加热至55℃,加入碱性蛋白酶和风味蛋白酶酶解,灭酶后离心取上清液绢布过滤后取透过液即得鸡胸软骨肽溶液。其中,作为优选,所述加水量为鸡胸软骨骨渣质量的2-3倍。作为优选,所述碱性蛋白酶的添加量为鸡胸软骨骨渣质量的0.2%~0.3%;所述风味蛋白酶的添加量为鸡胸软骨骨渣质量的0.3%~0.5%;作为优选,所述碱性蛋白酶和风味蛋白酶的质量比为1:1~5:3。在一些实施方案中,所述碱性蛋白酶的添加量为鸡胸软骨骨渣质量的0.2%,所述风味蛋白酶的添加量为鸡胸软骨骨渣质量的0.5%;在一些实施方案中,所述碱性蛋白酶的添加量为鸡胸软骨骨渣质量的0.3%,所述风味蛋白酶的添加量为鸡胸软骨骨渣质量的0.3%。作为优选,本发明所述鸡胸软骨肽的制备方法中所述酶解条件为55℃下保温3小时。酶解后需要对碱性蛋白酶和风味蛋白酶进行灭酶。本领域技术人员可以采用本领域公知的方法进行灭酶。在一些实施方案中,所述灭酶具体为95℃下加热15min。本发明所述鸡胸软骨肽的制备方法在灭酶后通过离心取上清液绢布过滤后取透过液即得鸡胸软骨肽溶液。其中作为优选,所述离心为8000r/min下离心15min。作为优选,所述绢布过滤为过200目绢布。进一步,本发明所述的制备方法还包括浓缩、干燥的步骤。在一些实施方案中,所述浓缩、干燥具体为真空浓缩至固形物约为40%,喷雾干燥。本发明还提供了上述制备方法制得的鸡胸软骨肽。在某一具体实施方案中,本发明检测了制得的鸡胸软骨肽对mmp-1抑制活性、对关节炎小鼠血清炎症因子水平的影响以及组织病理切片观察对大鼠骨关节炎的影响,结果显示制得的鸡胸软骨肽均有很好的mmp-1抑制活性,可达70%以上,对关节炎小鼠血清炎症因子水平均低于模型组,组织病理切片也显示了明显改善,表明本发明所述鸡胸软骨肽具有良好的抗炎作用。因此本发明还提供了所述鸡胸软骨肽在制备治疗骨关节炎的药物中的应用。由上述技术方案可知,本发明提供了一种鸡胸软骨肽及其制备方法与应用。本发明所述鸡胸软骨肽ⅱ型胶原蛋白含量≥50%,硫酸软骨素含量≥20%。我国为畜禽消费大国,消费总量几乎达到世界畜禽消费总量的1/4。鸡胸软骨为肉鸡加工中的主要副产物之一。本发明利用生物控制酶解技术制备富含ⅱ型胶原蛋白肽以及硫酸软骨素的鸡胸软骨肽。实验表明本发明制得的鸡胸软骨肽具有良好的抗炎作用可用于制备治疗骨关节炎的药物。因此本发明不仅可以提高鸡胸软骨的附加值,更能拓宽其应用范围,具有积极的社会意义和广阔的市场前景。附图说明为了更清楚地说明本发明实施例或现有技术中的技术方案,下面将对实施例或现有技术描述中所需要使用的附图作简单地介绍。图1示正常组膝关节切片图;图2示模型组膝关节切片图;图3示鸡胸软骨肽a组膝关节切片图;图4示鸡胸软骨肽b组膝关节切片图。具体实施方式本发明公开了鸡胸软骨肽及其制备方法和应用。本领域技术人员可以借鉴本文内容,适当改进工艺参数实现。特别需要指出的是,所有类似的替换和改动对本领域技术人员来说是显而易见的,它们都被视为包括在本发明。本发明的方法及产品已经通过较佳实施例进行了描述,相关人员明显能在不脱离本
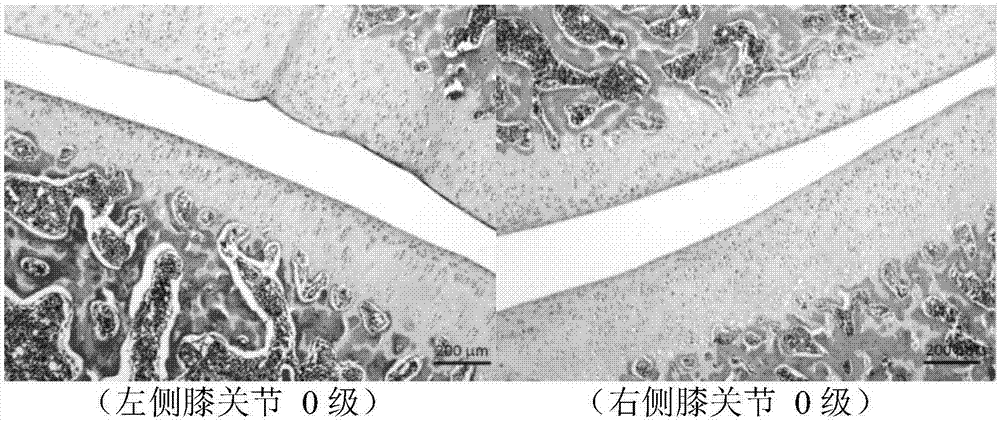
发明内容、精神和范围内对本文所述的方法进行改动或适当变更与组合,来实现和应用本发明技术。为了进一步理解本发明,下面将结合本发明实施例,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例,本发明的实施方式不限于此。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。如无特殊说明,本发明实施例中所涉及的试剂均为市售产品,均可以通过商业渠道购买获得。实施例1一种具有抗关节炎作用的鸡胸软骨肽的制备方法,包括以下步骤:(1)鸡胸软骨洗净后沥干、绞碎;(2)加入2倍水,调节体系ph值至7.0,水浴搅拌加热至55℃,加入鸡胸软骨肉糜质量0.2%的碱性蛋白酶(诺维信公司)和0.5%风味蛋白酶(诺维信公司)55℃下保温3小时,95℃下加热15min灭酶,8000r/min下离心15min,取上清液过200目绢布进行分离,取透过液,得到鸡胸软骨肽液;(3)将鸡胸软骨肽液真空浓缩至固形物约为40%,喷雾干燥得鸡胸软骨肽a(其中包57.46%的ⅱ型胶原蛋白及21.29%的硫酸软骨素)。实施例2一种具有抗关节炎作用的鸡胸软骨肽的制备方法,包括以下步骤:(1)鸡胸软骨洗净后沥干、绞碎;(2)加入3倍水,调节体系ph值至7.0,水浴搅拌加热至55℃,加入鸡胸软骨肉糜质量0.3%的碱性蛋白酶(诺维信公司)和0.3%风味蛋白酶(诺维信公司)55℃下保温4小时,95℃下加热15min灭酶,8000r/min下离心15min,取上清液过200目绢布进行分离,取透过液,得到鸡胸软骨肽液;(3)将鸡胸软骨肽液真空浓缩至固形物约为40%,喷雾干燥得鸡胸软骨肽b(其中包54.83%的ⅱ型胶原蛋白及22.08%的硫酸软骨素)。试验例:一、方法:(1)mmp-1(胶原酶)抑制活性测定试剂配制:磷酸盐缓冲液:称取磷酸氢二钠1.4499g,加入磷酸二氢钠0.1482g,加入去离子水500ml,配置成5mmol/l。胶原酶液:称取30mg胶原酶,加入150ml上述磷酸盐缓冲液。试验方法:取一定量的胶原蛋白(不可溶性)作为底物置于25ml锥形瓶中,加入胶原酶液5ml,0.2mg/ml;加入上述各酶解产物10mg/ml,0.2ml作为酶抑制剂;再加入4.8ml,5mmol/lpbs(ph=7.4)作为缓冲液,于恒温培养箱中(37.0±0.1℃)进行胶原蛋白酶解反应,持续6h,期间不断振荡锥形瓶使其混匀;而后将酶解液迅速过滤得到澄清溶液;取2ml滤液测定其所含羟脯氨酸;计算得到澄清酶解液中所含总羟脯氨酸(hyp总)。以不加入样品组为空白组,测定其澄清酶解液中所含羟脯氨酸为hyp空白;hyp抑制=hyp总-hyp样品式中,hyp样品为鸡软骨各酶解产物中所含羟脯氨酸的量。(2)大鼠功效验证试验(a)大鼠的饲养和管理50只健康雄性wistar大鼠,体重为300g±10.0g,将50只大鼠骨关节炎造模成功后随机分为假手术组(10只)和模型组(10只),a组(10只),b组(10只)。实验室温度20℃~26℃,湿度40%~70%,饲料由广东省医学实验动物中心提供,生产许可证号:scxk(粤)2013-0002,饲料质量合格证号:no.44200300015068。动物饲养于屏障环境实验室,实验动物使用许可证号:syxk(粤)2014-0137。采用经口灌胃方式给予受试物。样品组:a组,100mg/kgbw;b组,100mg/kgbw;假手术组和模型对照组给予同等剂量的纯水。(b)大鼠骨关节炎模型的构建无菌条件下,称取木瓜蛋白酶0.8000g,加生理盐水至16.0ml,配制浓度为5%,采用磁力搅拌器搅拌至溶液呈均匀混悬液(不堵针),4℃储存。实验前4h取出,恢复至常温后待用。模型组动物采用5%木瓜蛋白酶制备骨关节炎模型。试验前,采用3%戊巴比妥钠腹腔注射麻醉大鼠后,首先剃去右侧膝关节腔周边1cm区域的毛发,以75%乙醇消毒后,屈曲45°以髌骨下级的髌腱外边缘为进针点,向髁间窝的方向进针,抵达股骨髁后再回撤2mm,于右侧膝关节腔注入150μl木瓜蛋白酶生理盐水溶液以诱导骨关节炎模型。假手术组注射等量的无菌生理盐水。试验第1d和第5d各注射造模一次。第一次造模后7d,将模型组动物随机分成模型对照组,a组,b组,共3组,每组10只。按照10ml/kg给药体积,各样品组动物按剂量给予相应的药物,假手术组和模型组对照组灌胃给予等量纯水,连续给药30天(唐和斌等,2013)。(c)大鼠血清指标的测定以3%戊巴比妥钠腹腔注射麻醉后,打开腹腔后于腹腔主动脉取血5ml。采血后将血液室温静置2h,以3000r/min转速离心15min,取其上清液为血清,置于-80℃条件下保存。采用luminex试剂盒测试血清中的tnf-α、il-1β、il-10,采用南京建成试剂盒测试血清il-8,武汉华美试剂盒测试血清mmp-13指标。(d)大鼠组织切片病理观察固定:取大鼠左右后肢膝关节,将其切割处理成适宜大小的组织块。而后以4%甲醛溶液固定4h以上。脱钙处理:将固定妥善的大鼠关节放置于脱钙液中浸泡,14h后取出,而后以流动水冲洗其过夜。脱水处理:将脱钙后的大鼠关节梯度浸泡于浓度为80%、95%、100%的酒精中,浸泡时间分别为3h、45min、30min;其中100%浓度酒精浸泡两次,浸泡时间均为30min。而后再两次浸泡于二甲苯中,每次30min。石蜡包埋:先将少量已融化的石蜡倒入包埋模具中,并打开包埋盒,用加热的弯曲钝头镊子夹取已经部分浸蜡的组织块,平整地置于包埋模具底面中央处,而后添加融蜡至覆盖模具。待包埋模具内的融蜡表面凝固后,将其转入冷台加速凝固。最后以刀片或修块仪去除组织块周围的多余石蜡。粗切:将预冷后的蜡块安装在支持器上,刀片安装在持刀座上,调整支持器位置,使蜡块与刀刃接触。而后用匀速旋转切片(15~20μm)修切蜡块表面至组织块完整地全部切到。细切:调节切片机轮厚度(3~5μm),进行切片。将蜡片附着于载玻片上,待其水分留下后置于烤片机上烤干后放入烘箱烘片(60℃,30min),取出后即可准备染色。脱蜡:将切片分别放入二甲苯ⅰ、二甲苯ⅱ内各浸泡5~10min然后再分别放进无水乙醇ⅰ、无水乙醇ⅱ中各浸泡1~3min,随后将切片放入95%乙醇ⅰ、95%乙醇ⅱ内各浸泡1~3min,而后将切片放入80%乙醇内浸泡1min,最后放入蒸馏水内浸泡1min。he染色:先将切片放入苏木素液染色5~10min而后将切片放入蒸馏水内浸泡1min,然后以1%盐酸-乙醇溶液浸泡1~3s,随后将切片放置于蒸馏水中浸泡1~3s,之后将切片放入温水中返蓝5~10min,再以0.1%伊红液染色1~3min,最后以蒸馏水漂洗1~2s后迅速取出。脱水:将切片放入80%乙醇漂洗1~2s后转入95%乙醇ⅰ及95%乙醇ⅱ中各浸泡2~3min,而后将切片取出放入无水乙醇ⅰ及无水乙醇ⅱ中浸泡3~5min。随后将切片转入二甲苯ⅰ,二甲苯ⅱ,二甲苯ⅲ中各浸泡3~5min。中性树胶封固:于组织切片上加一滴中性树胶,而后用镊子轻轻夹住盖玻片的一侧,使得盖玻片可与树胶接触,轻缓放下盖玻片以保证玻片之间无气泡,随后将玻片自然晾干12h即可。(e)软骨组织病理学半定量分级评分:采用国际oa研究学会建立的oochas法对软骨组织病理学进行半定量分级评分:0级,软骨表面平整,软骨完整;1级,软骨表面浅层纤维形成,且不均匀;2级,软骨表面不连续,伴有细胞增殖,在ⅱ~ⅲ层异染物质增加或减少;3级,软骨皲裂扩散至ⅲ层或出现侵蚀;4级,软骨侵蚀加重,关节软骨出现损害;5级,关节软骨剥脱;6级,关节变形统计学处理:所有数据均以表示,采用spss16.0统计软件处理,各组组间差异比较采用t检验方法,p<0.05为差异具有统计学意义。二、结果1、mmp-1抑制活性检测mmp-1又叫胶原蛋白酶,是基质金属蛋白酶的一种,其能够降解关节处的胶原蛋白,导致胶原蛋白的流失和关节炎的恶化,因此通过抑制mmp-1的活性能够有效缓解胶原蛋白的损伤,有助于关节的修复。本发明检测了各实施例制得的鸡胸软骨肽的mmp-1抑制活性,结果如表1。表1各实施例及对mmp-1的体外抑制活性hyp空白(μg)hyp样品(μg)hyp总(μg)mmp-1抑制率(%)鸡胸软骨肽a739.37632.58743.7084.97鸡胸软骨肽b739.37705.33909.5172.38由表1可发现,鸡胸软骨肽a和b均有很好的mmp-1抑制活性,其中以鸡胸软骨肽a效果最佳,达84.97%。2、对关节炎小鼠血清炎症因子水平的影响血清白细胞介素-8(il-8)、白细胞介素-10(il-10)及白细胞介素-1β(il-1β)是骨关节炎患者炎症相关的监测因子,其含量越高表明患病越严重。同时其作为炎症性疾病的重要介质,可以促进炎症细胞趋化和诱导细胞增殖,在抗感染、免疫反应调节以及抗肿瘤方面有重要作用。而tnf-a全称肿瘤坏死因子α,其通过刺激巨噬细胞产生细胞因子,可能会诱导身体炎症的发生。通过检测在关节炎小鼠中炎症因子的表达,可以检测药品的抗炎活性。本发明检测了各实施例制得的鸡胸软骨肽的对关节炎小鼠血清炎症因子水平的影响,结果如表2。表2各实施例鸡胸软骨肽对关节炎小鼠血清炎症因子水平含量的影响(±s)组别il-8(ng/l)il-1β(pg/ml)il-10(pg/ml)tnf-a(pg/ml)正常组222.3±28.1316.326±2.6318.852±1.96142.038±9.052模型组248.75±61.9118.00±1.9720.22±2.41143.27±12.91鸡胸软骨肽a223.74±37.3613.33±0.97**12.36±1.75**131.99±8.66*鸡胸软骨肽b181.94±23.23*14.01±2.17*14.38±1.72**142.25±11.17注:与模型组比较*p<0.05,**p<0.01由表2可以看出,在正常组、鸡胸软骨肽a、b组的骨关节炎小鼠血清中的炎症因子水平均低于模型组,有显著性差异,说明鸡胸软骨肽a、b组具有良好的抗炎作用。3、对大鼠骨关节炎的影响本发明采用大鼠组织病理切片观察,比较各实施例制得的鸡胸软骨肽对大鼠骨关节炎的影响,结果如图1-4。从图1-4的病理分析可以看出,假手术组左侧膝关节和右侧膝关节均未见明显病理异常;模型组、鸡胸软骨肽a、b组三组的右侧膝关节都存在病例异常的情况。模型组的右侧膝关节的病理最复杂,存在软骨面磨损,表面纤维化,软骨细胞排列不规则,关节滑膜组织增生、炎细胞浸润、血管翳形成并深入关节腔内等问题。与模型组相比,鸡胸软骨肽a、b组侧膝关节软骨仅有一些表面浅表磨损外,部分大鼠也存在软骨表面浅层纤维化等现象,但是关节滑膜组织增生、炎细胞浸润、血管翳形成等较模型组有明显改善。综上分析可以发现,本发明所述鸡胸软骨肽a、b均对骨关节炎表现出良好的疗效。上述实施例为本发明较佳的实施方式,但本发明的实施方式并不受上述实施例的限制,其他的任何未背离本发明的精神实质与原理下所作的改变、修饰、替代、组合、简化,均应为等效的置换方式,都包含在本发明的保护范围之内。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1