一种基于改性毛细管的核酸检测微流控芯片及核酸检测系统的制作方法
本发明涉及微流控核酸分析芯片的技术领域,具体涉及一种基于改性毛细管的核酸检测微流控芯片及核酸检测系统。
背景技术:
近年来,全球爆发了数起大规模传染病,比如h1n1、埃博拉病毒和寨卡等,需要通过专业的核酸检测仪器,经过核酸提取和扩增的过程才可检出。通常而言此类仪器具有体积庞大、难以现场部署、造价昂贵且需专人维护等缺点。微流控芯片因其易于集成化、自动化、流体可控以及所需样本量小的特点,广泛用于生化分析领域,比如细菌、病毒及蛋白质检测领域等,一定程度上弥补了专业核酸检测设备难以部署在出入境口岸、野外等非实验室区域的缺陷。
基于微流控芯片的核酸检测方法的核心之一是核酸提取的方法,通常为以下几种方法之一:煮沸法、磁珠法及固相萃取法。为了开发该类型现场快速核酸检测设备,申请人所在的研究团队早已对相关领域进行了一定的研究且有深厚的研究基础,如赵树弥等人在分析化学上发表的《集成核酸提取实时荧光pcr微全分析系统》,此论文报道一种用于检测血液中病毒的微流控芯片及搭配的荧光定量检测装置,但是该论文报道的芯片是采用基于硅胶膜的固相萃取法进行核酸提取,而且针对的样本是血液裂解液,不能对全血进行处理分析。刘映乐等申请的专利《现场快速检测传染病病原体的装置及其方法》中介绍了一种基于沉淀煮沸法的核酸提取装置设计,但是该方法提取的核酸量少且纯度低,难以对rna类病毒等核酸提纯质量要求高的样本进行提纯。邱宪波等在专利《核酸自动提取微流控装置》中介绍了一种基于磁珠法的核酸提取芯片及装置,而磁珠法本身并非是为微流控芯片而设计的方法,相对而言步骤复杂且难以进行自动化集成。thiagowuqingqing等人在analyticalchemistry上发表的<integratedglassmicrodevicefornucleicacidpurification,loop-mediatedisothermalamplification,andonlinedetection>一文中报道了一种基于固相萃取方法的集核酸抽提及扩增的芯片,核酸提取过程中需要额外的核酸洗脱步骤,加大了微流控芯片的集成难度。huijunhou等人在labonachip发表的<multiplexsample-to-answerdetectionofbacteriausingapipette-actuatedcapillaryarraycombwithintegrateddnaextraction,isothermalamplification,andsmartphonedetection>提出了一种基于聚壳糖改性玻璃滤纸吸附核酸的毛细管阵列核酸原位扩增方法,实现了核酸无需经过洗脱步骤即可实现扩增,大大降低了集成难度,但是该论文中提出的方法依然需要依赖人工操作,未能实现核酸“提取——扩增——检测”自动化的过程。
技术实现要素:
本发明解决技术问题:克服上述现有技术缺陷,提供一种基于改性毛细管的核酸检测微流控芯片及核酸检测系统,集成样本裂解、核酸提取、核酸扩增和核酸检测功能,以实现可以部署在非实验室区域并对传染性病原体进行检测。
为了实现上述目的,本发明的技术方案如下:
微流控芯片内部包含一种改性毛细管,用于吸附待测溶液样本中的目标核酸,作为实现核酸吸附、纯化、扩增和检测的自动化实现方式的载体;
所述芯片自下而上分别为基底,液路层基片,弹性薄膜,气路层基片四层结构;液路层基片的上表面嵌有液体流通通道、液体混合通道和液体分流通道,并有穿透孔通往液路层下表面;液路层下表面嵌有裂解腔和毛细管预留腔,后者内部嵌入改性的毛细管,实现核酸样本的吸附及扩增;气路层基片的上表面有多个凸起空心的腔体,用来存储检测样本、裂解液或pcr试剂;下表面含有多个凹陷的气阀,并与上表面通过通孔贯穿,液路层基片的下表面与底部基片键合,其中中间腔体部分与毛细管嵌合,液路层基片的上表面与弹性薄膜下表面键合;上表面和下表面通过微通道和微孔道连接,使得储液腔、裂解腔、毛细管以及出口连通;气路层基片下表面与弹性薄膜上表面键合,构成一块完整的微流控芯片。
所述的基底为玻璃或硅片;液路层基片和气路层基片为pdms、pc、pmma或coc聚合物材料;弹性膜为pdms或tpu的弹性材料;
此外,根据本发明的一个实施例,所述微流控芯片气路层基片上表面还包括三个储液腔,所述储液腔通过穿透气路层基片上下表面的通孔共同连接至位于液路层上表面的蛇形通道,所述蛇形通道连接至用于裂解核酸的裂解腔,所述裂解腔连接至用于嵌合毛细管的腔体。
所述改性毛细管采用的技术方案为:经过表面改性技术使得毛细管表面携带正电荷,样本经过裂解后溶液中的目标核酸可被所述改性毛细管富集,同时被富集的核酸在正常核酸扩增条件下可以自发游离至溶液中;
此外,根据本发明一个实施例,所述的改性毛细管为玻璃、二氧化硅或热塑性塑料中任意一种硬质透明材料制成;
此外,根据本发明的一个实施例,改性毛细管内壁含有末端带氨基结构的官能团或离子的化合物,包括-nh2或[nh4]+结构,主要基于氢键和离子键对核酸进行吸附;
此外,根据本发明一个实施例,所述的改性毛细管通过过盈配合、热粘合或等离子清洗键合固定于微流控芯片液路基片下表面通道内;
此外,根据本发明一个实施例,所述的样本经过裂解后溶液中的目标核酸指处于裂解液环境中的核酸,即无需额外改变裂解液溶液体系;
此外,根据本发明一个实施例,所述的正常核酸扩增条件下主要指无需经过额外的手段,包括改变毛细管内温度、ph值、溶液中其它离子浓度等条件的前提下,被吸附的核酸在核酸扩增反应液体系中自行脱离毛细管壁吸附作用参与核酸扩增反应。
为了实现对上述微流控芯片的自动控制,本发明提供了一种该微流控芯片的配套装置,包含流体驱动控制系统、气阀控制系统、温控系统、光学系统、控制系统以及智能手机,用于实现上述微流控芯片全自动化操作及检测过程。用于实现上述微流控芯片全自动化操作及检测过程,实现“样本进,结果出”的目标。
本发明中微流控芯片采用的技术方案为:采用嵌入芯片内的改性后毛细管吸附并提纯核酸,并集成核酸扩增与检测的微流控芯片;
本发明中微流控芯片的配套装置采用的技术方案为:
所述微流控芯片由气路层基片,弹性薄膜,液路层基片,基底,加热裂解腔,第一储液腔,第二储液腔,第三储液腔,第一注射泵接口,第二注射泵接口,若干弹性薄膜微阀,蛇形液体混合流道,若干改性毛细管预留腔,第一改性毛细管、第二改性毛细管、第三改性毛细管、第四改性毛细管构成;
所述装置包含流体驱动控制系统、气阀控制系统、温控系统、光学系统、控制系统以及智能手机,流体驱动控制系统和气阀控制系统连接芯片气路层基片上表面,温控系统紧贴芯片基底下表面,光学系统置于微流控芯片正上方,智能手机置于光学系统正上方。
所述流体驱动控制系统控制微流控芯片中的流体,所述气阀控制系统操控弹性薄膜微阀开闭,所述温控系统维持核酸扩增所需的温度,所述光学系统提供特定波长的激发光和获得特定波长的发射光,所述控制系统对流体驱动控制系统、温控系统及光学系统实施控制,所述智能手机的图像识别功能对样本进行定性和半定量检测;
此外,根据本发明一个实施例,所述流体驱动控制系统由第一注射泵、第二注射泵构成,注射泵连通微流控芯片上的进出样口,通过正压及负压的方式驱动流体;
此外,根据本发明一个实施例,所述气阀控制系统由气源以及若干电磁阀构成,气源产生持续0.2mpa的正压并与电磁阀连通,电磁阀另一端分别连接至少一个弹性薄膜微阀,通过电磁阀的开闭控弹性薄膜微阀开闭;
此外,根据本发明一个实施例,所述温控系统紧贴微流控芯片的基底,内部包括温度传感器、帕尔帖、热沉、散热鳍片及风扇,温度调节范围为0-100℃,温度调节精度为0.1℃,升降温速度为5℃/s,用于控制微流控芯片内部的毛细管温度,满足核酸扩增需要的温度环境;
此外,根据本发明一个实施例,所述光学系统包括一个激发光源、一个滤光片、一个透镜及一个聚焦镜,主要用于产生特定波长的激发光照射于微流控芯片毛细管表面,并获得特定波长的发射光,实现对毛细管内核酸扩增情况定性和半定量检测;
此外,根据本发明一个实施例,所述控制系统包括一个微处理器以及一处无线通讯接口,微处理器用于操作流体驱动控制系统、光学系统与温控系统,无线通讯接口用于微处理器与智能手机通讯;
此外,根据本发明一个实施例,所述智能手机通过控制微处理器机对流体驱动控制系统、温控系统及光学系统下达命令并获取反馈数据,并通过自带的摄像头检测荧光信号,通过内置的图像处理软件对核酸扩增结果定性或半定量分析。
此外,根据本发明一个实施例,所述微流控芯片进行分析的实现方法步骤如下:
(1)样品加载
核酸分析所需的样本、裂解液和试剂依次加入第一储液腔,第二储液腔,第三储液腔;
(2)样本与裂解液混合
样本与裂解液在注射泵产生的负压的驱动下,经过蛇形液体混合流道的作用混合,并最终混合均匀汇入裂解腔;
(3)样本裂解
通过温控系统对样本与裂解液的混合液于裂解腔内加热,使dna释放至液体中;
(4)核酸吸附
控制驱动力大小,让样本通过改性毛细管,并移除裂解液;
(5)杂质洗脱
注射泵通过位于气路层基片上方的通孔将洗脱液注入第一改性毛细管、第二改性毛细管、第三改性毛细管,然后移除洗脱液,即得核酸样本;
(6)反应液加载
通过外力驱动作用,将位于气路层基片上方的反应液腔体通过分岔流道将反应液装载至第一改性毛细管、第二改性毛细管、第三改性毛细管、第四改性毛细管;
(7)核酸扩增
通过温控系统加热芯片内部的第一改性毛细管、第二改性毛细管、第三改性毛细管、第四改性毛细管,具体核酸扩增所需的温度条件由选用的试剂反应体系所决定;
(8)核酸检测
利用智能手机对改性毛细管定时拍照采集荧光图像,并通过内置的图像识别软件识别及检测改性毛细管荧光强度变化,实现对核酸样本的定性及半定量检测。
本发明的原理在于:
(1)微流控芯片由4层构成,由下自上分别为基底、液路层基片、弹性薄膜和气路层基片,通过外力驱动和弹性薄膜阀的协作,使试剂和样本经过定制的微通道和微孔道进出腔体;此外芯片内部嵌入改的毛细管,核酸在碱性溶液中(ph>7)呈现负电性,从而被毛细管吸附至壁面,实现待测样本的富集,并利用弱碱性溶液洗脱毛细管,从而将多余的杂质去除,而被吸附在改性毛细管内壁的核酸由于管内壁面液体流速较低,相对而言难以被洗脱,从而得到较为纯净的核酸样本。
(2)基于智能手机通过无线通讯的手段发送命令控制各系统,并通过自带的摄像头获取毛细管荧光图像,通过内置的图像识别软件检测毛细管荧光强度变化,从而对扩增结果进行定性和半定量判断。
本发明与现有技术相比有点在于:
(1)相比于传统的核酸提取及检测方法,本发明中的微流控芯片及系统可以实现核酸裂解、核酸吸附、核酸洗脱、核酸扩增及检测的全过程,操作步骤简单,仅需要添加样本即可,全部过程在芯片内实现,完成“样本进——结果出”。
(2)相比于传统的磁珠法和固相萃取法提取核酸的微流控芯片,本发明中含有氨基改性毛细管的微流控芯片,避免了洗脱核酸的步骤,可以减少核酸前处理操作步骤,简化流程;
(3)相比于传统的微流控芯片仪器,本发明基于智能手机实现对样本的检测,降低了设备的制造成本,提高了仪器的便携性和灵活性;
总之,本发明提供一种具有样品前处理、核酸富集与纯化、核酸扩增及检测的多功能核酸分析芯片及配套装置,实现“样品进——结果出”的自动化、全封闭式微流控芯片,适合在难以部署大型仪器设备的场景中应用。
附图说明
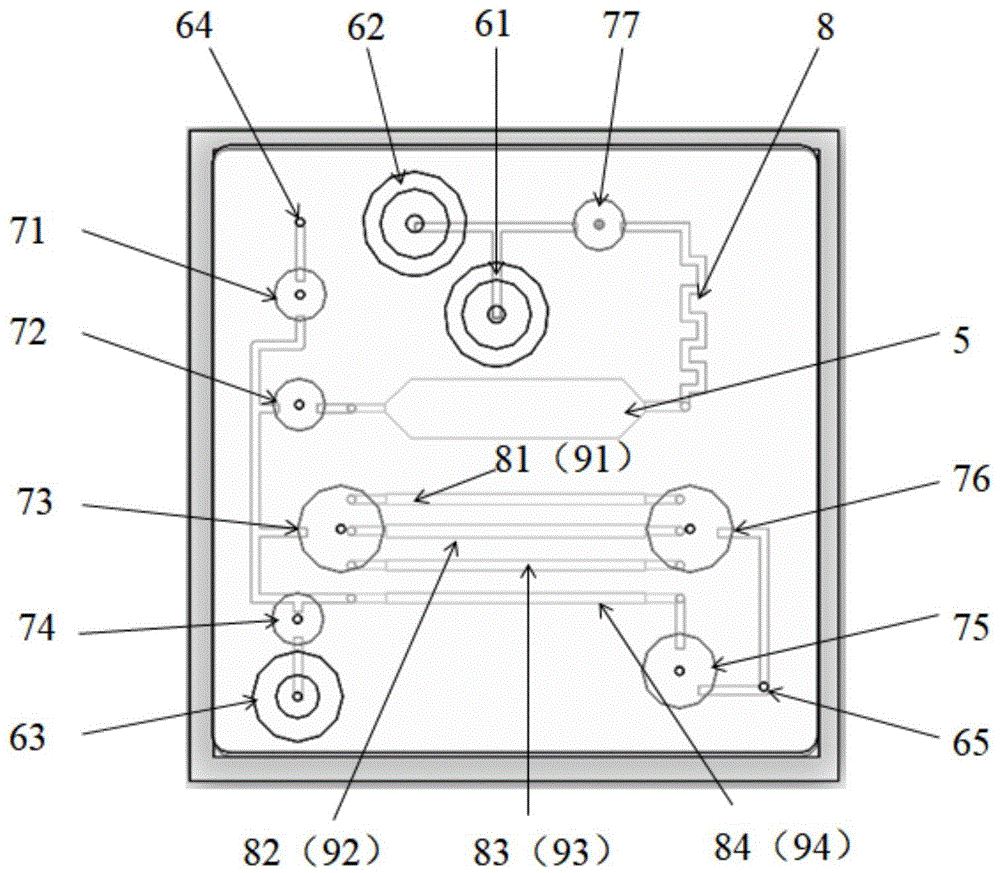
图1为本发明中微流控芯片的俯视图;
图2为本发明中微流控芯片的解析图;
图3为本发明中微流控芯片进样、核酸富集和洗脱过程的装置结构示意图;
图4为本发明中扩增和检测过程的装置结构示意图。
图中,希腊字母编号分别为:微流控芯片i,流体驱动控制系统ii,气阀控制系统iii,控制系统iv,智能手机v,光学系统vi,温控系统vii;阿拉伯数字编号分别为:气路层基片1,弹性薄膜2,液路层基片3,基底4,裂解腔5,第一储液腔61,第二储液腔62,第三储液腔63,第一注射泵接口64,第二注射泵接口65,第一弹性薄膜微阀71,第二弹性薄膜微阀72,第三弹性薄膜微阀73,第四弹性薄膜微阀74,第五弹性薄膜微阀75,第六弹性薄膜微阀76,第七弹性薄膜微阀77,蛇形液体混合流道8,第一改性毛细管预留腔81,第二改性毛细管预留腔82,第三改性毛细管预留腔83,第四改性毛细管预留腔84,第一改性毛细管91,第二改性毛细管92,第三改性毛细管93,第四改性毛细管94,第一电磁阀101,第二电磁阀102,第三电磁阀103,第四电磁阀104,气源11,第一注射泵121,第二注射泵122,透镜13,滤光片14,激发光源15,聚焦镜16,热沉17,散热鳍片18,散热风扇19。
具体实施方式
本发明以下将结合附图和实施例作进一步描述。这些实施例仅用于说明而不限制本发明的应用范围。此外应理解,在阅读本发明讲授的内容之后,本领域的技术人员可对本发明做任何改动和修改,这些等价形式同样落于本申请所附权利要求的范围。
如图1和图2所示,微流控芯片i自上而下为气路层基片1、弹性薄膜2、液路层基片3和基底4。将4根毛细管放入h2so4溶液中浸泡1h,确保毛细管内表面完全被覆盖,以去除毛细管内表面的污渍;再将毛细管取出,用纯水冲洗1h,以去除毛细管内表面的h2so4;最后将毛细管置于末端含有氨基结构的官能团或离子的碱性化合物中,比如-nh2,[nh4]+等结构,此时溶液中的化合物可以与毛细管内壁发生反应,从而将对应的化学基团涂覆在毛细管内壁上,即得第一改性毛细管91、第二改性毛细管92、第三改性毛细管93、第四改性毛细管94。随后将4根改性毛细管分别横置于液路层基片3底部的第一改性毛细管预留腔81、第二改性毛细管预留腔82、第三改性毛细管预留腔83、第四改性毛细管预留腔84内。随后将微流控芯片i按照气路层基片1、弹性薄膜2、液路层基片3和基底4的顺序依次键合,即形成图1和图2所示的微流控芯片i。
图3中iii气阀控制系统包括4个电磁阀,其中第一电磁阀101通过气路密封管道连接图1中的第一弹性薄膜微阀71,第二电磁阀102连接第二弹性薄膜微阀72及第七弹性薄膜微阀77,第三电磁阀103连接第三弹性薄膜微阀73及第六弹性薄膜微阀76,第四电磁阀104连接第四弹性薄膜微阀74及第五弹性薄膜微阀75;电磁阀的另一端与气源11连接,后者提供大小恒定为0.2mpa的气压;通过控制系统iv对电磁阀实施控制,当电磁阀开启时,气源11通入该电磁阀对应的弹性薄膜微阀,导致流道关闭。
如图3和图1所示,图3中流体驱动控制系统ii包括第一注射泵121、第二注射泵122,其中第一注射泵121连接第一注射泵入口64,泵内装有ph为7.0的去离子水;第二注射泵122连接第二注射泵入口65,注射泵内部无装载样本和剩余体积。
如图4和图1所示,图4中微流控芯i片放置于温控系统vii上,并与热沉17紧密相连,热沉17底部为散热鳍片18和风扇19。通过温控系统内置的pid算法控制热沉升降温,并配合散热鳍片18和风扇19,从而维持核酸扩增反应所需的温度;光学系统vi中的滤光片14正对于微流控芯片i第一改性毛细管91、第二改性毛细管92、第三改性毛细管93、第四改性毛细管94的上方,激发光源15照射470nm激发光,经过聚焦镜16以及透镜13反射至第一改性毛细管91、第二改性毛细管92、第三改性毛细管93、第四改性毛细管94,并获得590nm发射光;智能手机摄像头正对于透镜13正上方,拍照采集荧光信号,并通过内置的图像处理软件分析荧光强度。
具体实施方式二,本实施方式为具体实施方式一所述的基于改性毛细管的核酸检测微流控芯片及核酸检测系统应用过程:
步骤1:样本加载。将微流控芯片i底部涂满导热硅脂,并与温控系统vii紧贴。将250μl待测血液样本与500μl裂解液分别置于第一储液腔61、第二储液腔62中,将150μlpcrmix加入第三储液腔63中;将电磁阀和注射泵按照实施方式一中通过密封软管连接至微流控芯片i各弹性薄膜微阀或注射泵接口。
步骤2:样本与裂解液混合。操控手机控制控制系统iv下达命令,启动气源11与电磁阀和注射泵。通过开启和第一电磁阀101和第四电磁阀104,关闭第一弹性薄膜微阀71、第四弹性薄膜微阀74、第五弹性薄膜微阀75使得和第一储液腔61、第二储液腔62和第二注射泵入口65间的液体流路形成通路;通过第二注射泵122拉伸作用使通道内产生负压,驱动样本和解裂解进入裂解腔5,其中二者通过液体混合流道8时,会在蛇形管道内自发混合;当样本填满裂解腔5时,开启第二电磁阀102,使第二弹性薄膜微阀72和第七弹性薄膜微阀77密封。
步骤3:样本裂解。通过智能手机v操控温控系统vii,加热热沉17至95℃,时间为10min,使裂解腔5内的血液样本裂解并释放出待测核酸。
步骤4:核酸吸附。关闭第二电磁阀102,同时控制第二注射泵122继续拉伸,让裂解后的样本缓慢通过经过第一改性毛细管91、第二改性毛细管92、第三改性毛细管93,待测核酸在毛细管表面的电荷吸附作用下固定于表面,最后废液进入第二注射泵122内。
步骤5:杂质洗脱。关闭第一电磁阀101,并开启第二电磁阀102,使得第一注射泵入口64与第二注射泵入口65间的通道连通。通过第一注射泵121驱动去5ml离子水使其缓慢通过第一改性毛细管91、第二改性毛细管92、第三改性毛细管93,将残余的杂质洗脱,而待测核酸在毛细管吸附作用下难以被洗去;同时拉伸第二注射泵122,洗脱后的液体最后进入第二注射泵122内。
步骤6:反应液加载。关闭第一电磁阀101,并开启第四电磁阀104,使得试剂腔63与第二注射泵入口65间的通道连接。通过拉伸第二注射泵122,使得pcrmix进入第一改性毛细管91、第二改性毛细管92、第三改性毛细管93、第四改性毛细管94,待液体同时填满4根毛细管时,开启所有电磁阀,使所有弹性薄膜微阀闭合,以密封所有改性毛细管。
步骤7:核酸扩增。开启温控系统vii,通过热沉的升降温控制样本内核酸扩增,温度参数为:首先95℃持续600s实现taq酶预变性;解旋95℃持续15s,退火62℃持续20s,延伸72℃持续20s,持续35个循环。
步骤8:核酸检测。利用智能手机协调激发光源15和智能手机v,在每个循环的延伸阶段拍照,并利用内部图像处理软件识别毛细管边缘轮廓并获取荧光信号,通过内置的算法获得荧光强度曲线,实现对目标核酸定性及半定量检测。
尽管本发明的实施方案已公开如上,但其并不仅仅限于说明书和实施方式中所列运用,它完全可以被适用于各种适合本发明的领域,对于熟悉本领域的人员而言,可容易地实现另外的修改,因此在不背离权利要求及等同范围所限定的一般概念下,本发明并不限于特定的细节和这里示出与描述的图例。
- 还没有人留言评论。精彩留言会获得点赞!