用于保护肠道菌的冻干保护剂、冻干粉、胶囊及其制备方法与流程
本发明涉及肠道菌群移植领域,特别是涉及一种用于保护肠道菌的冻干保护剂、冻干粉、胶囊及其制备方法。
背景技术:
:肠道菌移植,又称粪菌移植,是将健康人的肠道菌群移植到患者胃肠道内,重塑健康的肠道微生态,实现肠道及肠道外疾病的治疗。我国自古就有用人粪治疗疾病的先例,最早可追溯至东晋时期,葛洪《肘后备急方》记载,用人粪清治疗食物中毒、腹泻、发热并濒临死亡的患者,述“饮粪汁一升,即活”,可见有奇效。长久以来,面对胃肠道功能的紊乱的问题,摄入益生菌被认为是有效改善紊乱的方法,但若肠道环境遭遇破坏性紊乱且导致疾病,益生菌的改善能力有限,而通过移植健康人的肠道菌可以尽可能的重塑患者的肠道环境,从根源上解决或缓解病症。传统的肠道菌移植主要通过胃镜、胃管、空肠管、结肠镜等器械介入的技术进行移植,针对病症严重程度很可能会进行多次移植,每次移植的过程都需要肠道菌群通过导管途经胃,十二指肠,最终注入十二指肠远端,移植过程复杂,患者有一定的痛苦。此外,肠道菌移植的另外一种方式是将肠道菌与冻干保护剂混合后制备成冻干粉,再通过口服摄入人体,但在制备冻干粉的过程中,传统的冻干保护剂对肠道菌的结构、丰度破坏大,无法有效保护肠道菌,最终导致含肠道菌的药剂治疗炎症有关的肠病效果差。技术实现要素:基于此,有必要针对传统的冻干保护剂无法有效保护肠道菌的问题,提供一种有效保护肠道菌的冻干保护剂、冻干粉、胶囊及其制备方法。一种用于保护肠道菌的冻干保护剂,包括如下质量份的原料组分:上述用于保护肠道菌的冻干保护剂的原料各组分相互配合,组分配比合理,可以有效保护肠道菌的菌群结构和丰度,减少冻干过程中造成的菌群损伤,维持肠道菌群的完整性和稳定性。在其中一个实施例中,用于保护肠道菌的冻干保护剂包括如下质量份的原料组分:在其中一个实施例中,所述低聚糖选自低聚半乳糖、低聚木糖和低聚果糖中的一种。本发明还提供一种肠道菌冻干粉,其包括如下原料组分:肠道菌和本发明一实施例所述的用于保护肠道菌的冻干保护剂,其中,所述肠道菌与所述冻干保护剂的质量比为3~5:10。本发明还提供一种包括本发明一实施例所述的肠道菌冻干粉在制备复发性艰难梭菌感染或炎症性肠病治疗药物中的用途。本发明还提供一种含肠道菌冻干粉的胶囊,其包括本发明一实施例所述肠道菌冻干粉和装载所述肠道菌冻干粉的胶囊壳体。在其中一个实施例中,所述胶囊壳体为耐酸的肠溶胶囊壳体。本发明还提供一种含肠道菌冻干粉的胶囊的制备方法,其包括如下步骤:将肠道菌与本发明一实施例中所述的用于保护肠道菌的冻干保护剂按照质量比3~5:10混匀。在其中一个实施例中,所述冷冻的步骤包括:在-18℃~-22℃条件下,预冷冻3.5h~4.5h;之后转移至-78℃~-82℃条件下,冷冻7.5h~8.5h。在其中一个实施例中,所述干燥的条件包括:在真空度6pa~10pa、温度-50℃~-70℃下,干燥24h~48h。附图说明图1为本发明一实施方式中粪菌样本经冻干处理前后的out聚类分析图;图2为图1中粪菌样本经冻干处理前后的属水平的物种丰度图;图3为本发明一实施方式中含肠道菌冻干粉的胶囊中所含活菌的存活率图。具体实施方式为使本发明的上述目的、特征和优点能够更加明显易懂,下面结合附图对本发明的具体实施方式做详细的说明。在下面的描述中阐述了很多具体细节以便于充分理解本发明。但是本发明能够以很多不同于在此描述的其它方式来实施,本领域技术人员可以在不违背本发明内涵的情况下做类似改进,因此本发明不受下面公开的具体实施例的限制。除非另有定义,本文所使用的所有的技术和科学术语与属于本发明的
技术领域:
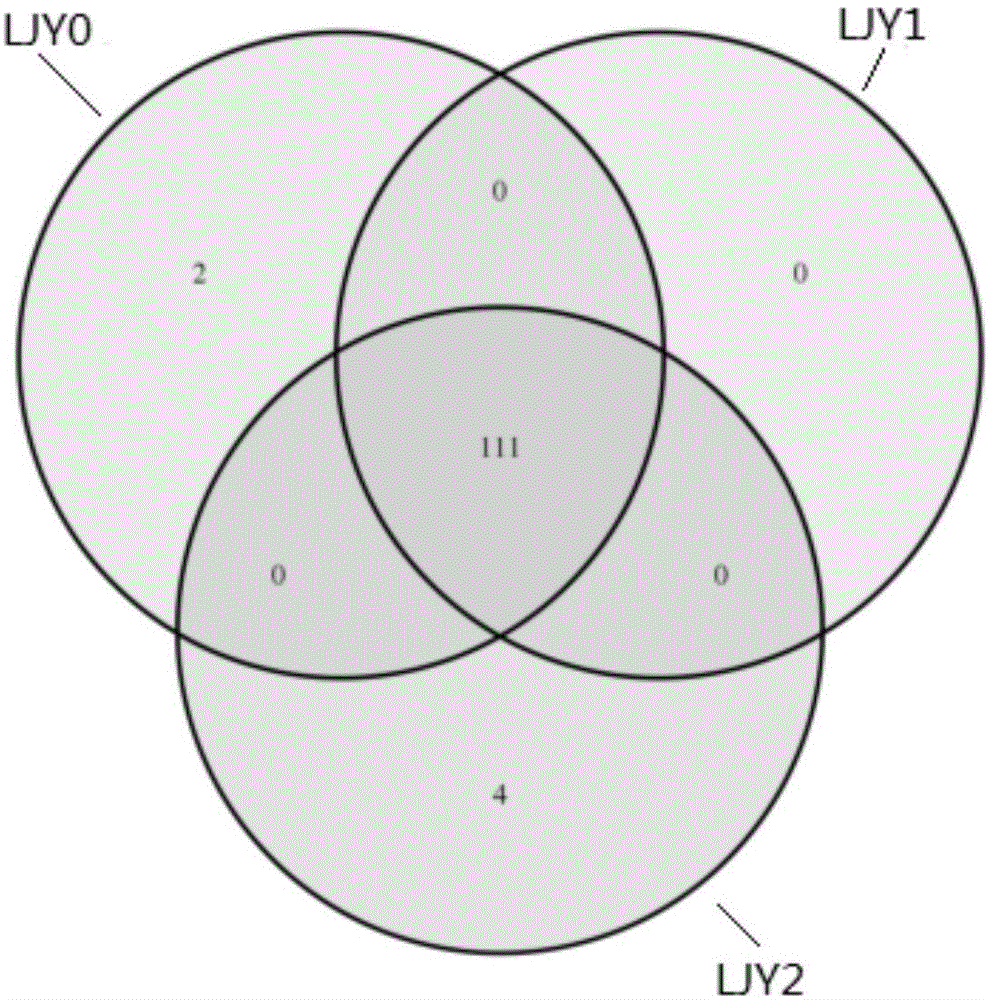
的技术人员通常理解的含义相同。本文中在本发明的说明书中所使用的术语只是为了描述具体的实施例的目的,不是旨在于限制本发明。本文所使用的术语“及/或”包括一个或多个相关的所列项目的任意的和所有的组合。本发明一实施例中提供一种用于保护肠道菌的冻干保护剂,其包括如下质量份的原料组分:其中,甘油具有很强的持水性,在冻干过程中,避免肠道菌的细胞因失水太快,造成细胞蛋白质结构的破坏,进而使肠道菌的菌体受损。其中,水溶性淀粉的主要作用是增加肠道菌的细胞弹性,提高肠道菌的细胞壁的抗压能力,防止肠道菌在冻干过程中菌群结构受到损伤。其中,低聚糖主要作为脱水保护剂,在冻干过程中,低聚糖中的羟基和细胞内大分子形成氢键,取代由水分子和细胞内大分子形成的氢键,使生物体内的蛋白质和其它大分子物质在缺水条件下仍可保持其原有结构,维持生物体活力。其中,甘露醇的作为赋形剂,不仅可以作为优良的骨架剂使用,而且能够兼作蛋白质的保护剂。在其中一个实施例中,所述低聚糖选自低聚半乳糖、低聚木糖和低聚果糖中的一种。进一步地,所述低聚糖选自低聚半乳糖,低聚半乳糖除提供羟基外,还有很强的保护应变功能,对复杂成份的生物制剂有更好的保护效果。在其中一个实施例中,所述水为无菌生理盐水,用无菌生理盐水作为冻干保护剂的溶剂,其与人体肠道的内环境接近,与肠道菌混合后,可以更好的溶解肠道菌,制备得到的冻干粉也容易被肠道吸收。在其中一个实施例中,用于保护肠道菌的冻干保护剂包括如下质量份的原料组分:在其中一个实施例中,用于保护肠道菌的冻干保护剂包括如下质量份的原料组分:在其中一个实施例中,用于保护肠道菌的冻干保护剂包括如下质量份的原料组分:上述用于保护肠道菌的冻干保护剂的原料各组分相互配合,组分配比合理,可以有效保护肠道菌的菌群结构和丰度,减少冻干过程中造成的菌群损伤,维持肠道菌群的完整性和稳定性。本发明还提供一种肠道菌冻干粉,其包括如下原料组分:肠道菌和本发明一实施例所述的用于保护肠道菌的冻干保护剂,其中,所述肠道菌与所述冻干保护剂的质量比为3~5:10。进一步地,所述肠道菌与所述冻干保护剂的质量比为4:10。上述肠道菌冻干粉可以有效保护肠道菌的菌群结构和丰度,减少冻干过程中造成的菌群损伤,维持肠道菌群的稳定性。上述肠道菌冻干粉中的总细菌的活菌存活率、乳杆菌的活菌存活率和双歧杆菌的活菌存活率均在80%以上,对有益菌有很好的保存效果,可以重塑患者健康的肠道微环境,治疗复发性艰难梭菌感染或炎症性肠病有很好的效果。本发明还提供一种包括本发明一实施例中所述的肠道菌冻干粉在制备复发性艰难梭菌感染或炎症性肠病治疗药物中的用途。可以理解,制备复发性艰难梭菌感染或炎症性肠病治疗药物的剂型不做过多限定,可以将本发明一实施例中所述的肠道菌冻干粉加工成片剂、口服液、胶囊等药物剂型。本发明还提供一种含肠道菌冻干粉的胶囊,其包括本发明一实施例所述的肠道菌冻干粉和装载所述肠道菌冻干粉的胶囊壳体。在其中一个实施例中,所述胶囊为耐酸的肠溶胶囊壳体,可以防止肠道冻干粉中的菌被胃酸降解。进一步地,耐酸的肠溶胶囊壳体的材质为羟丙甲基纤维素(hpmc),该材质含水量低,稳定性强,服用安全,无过敏风险。在其中一个实施例中,所述胶囊壳体为双层结构的胶囊壳体,即内层和外层均为羟丙甲基纤维素,可防止含肠道菌冻干粉的胶囊还未达到回肠处就过早崩解,肠道菌冻干粉的治疗功效丧失。上述含肠道菌冻干粉的胶囊可保存方便,可直接服用,无需经器械转入肠道,减少患者痛苦。含肠道菌冻干粉的胶囊对重塑患者健康的肠道微环境,治疗炎症性肠病有很好的效果。本发明还提供一种含肠道菌冻干粉的胶囊的制备方法,其包括如下步骤:将肠道菌与本发明一实施例的用于保护肠道菌的冻干保护剂按照质量比3~5:10混匀,冷冻,干燥得到肠道菌冻干粉;将所述肠道菌冻干粉装入胶囊中即得。在其中一个实施例中,肠道菌的制备方法包括如下步骤:(1)取新鲜粪便样本加入一定体积的无菌生理盐水中进行均质化处理,得到粪便浆体。(2)将粪便浆体过滤除掉大颗粒后,再次均质化处理。(3)将步骤(2)所得的均质化后的样本逐级过滤制得粪便悬液。(4)将粪便悬液低温离心,弃去上层液体制得沉淀物即为肠道菌。在其中一个实施例中,逐级过滤是指依次经50目、100目、200目和300目的无菌滤网。逐级过滤的主要作用是去除未吸收的食物残渣、小颗粒物质及虫卵等物质。在其中一个实施例中,所述冷冻的步骤包括:在-18℃~-22℃条件下,预冷冻3.5h~4.5h;之后转移至-78℃~-82℃条件下,冷冻7.5h~8.5h。在其中一个实施例中,所述干燥的条件包括:在真空度6pa~10pa、温度-50℃~-70℃下,干燥24h~48h。在其中一个实施例中,将所述肠道菌冻干粉装入胶囊中的步骤中是在无菌环境下操作。上述含肠道菌冻干粉的胶囊的制备方法简单,无需经器械转入肠道,减少患者痛苦。为了使本发明的目的及优点更加清楚明白,以下结合实施例对本发明进行进一步详细说明。应当理解,此处所描述的具体实施例仅用以解释本发明,并不用于限定本发明。实施例1一种肠道菌冻干粉的制备方法,其包括如下步骤:称取50g的供体新鲜粪便样本,加入200ml无菌生理盐水中进行均质化处理,得到粪便浆体。之后将粪便浆体逐级经过50目、100目、200目和300目的无菌滤网得到粪便悬液,之后经4000r/min离心20min,弃去上层液体,得到的沉淀物为肠道菌,再将肠道菌按照质量比4:10悬于下表1中用于保护肠道菌的冻干保护剂中,之后冷冻,干燥得到肠道菌冻干粉。其中,冷冻的条件为:先-20℃预冻4h,而后转移至-80℃冷冻8h。干燥的条件为:在真空度为10pa,温度为-60℃下,真空干燥30h,即得肠道菌冻干粉。表1组分含量(g/100ml)甘油0.5水溶性淀粉8.0低聚半乳糖1.0甘露醇0.5无菌生理盐水90实施例2一种肠道菌冻干粉的制备方法,其包括如下步骤:称取50g的供体新鲜粪便样本,加入200ml无菌生理盐水中进行均质化处理,得到粪便浆体。之后将粪便浆体逐级经过50目、100目、200目和300目的无菌滤网得到粪便悬液,之后经4000r/min离心20min,弃去上层液体,得到的沉淀物为肠道菌,再将肠道菌按照质量比3:10悬于下表2中用于保护肠道菌的冻干保护剂中,之后冷冻,干燥得到肠道菌冻干粉。其中,冷冻的条件为:先-20℃预冻4h,而后转移至-80℃冷冻8h。干燥的条件为:在真空度为10pa,温度为-60℃下,真空干燥30h,即得肠道菌冻干粉。表2组分含量(g/100ml)甘油0.5水溶性淀粉8.0低聚木糖1.0甘露醇0.5无菌生理盐水90实施例3一种肠道菌冻干粉的制备方法,其包括如下步骤:称取50g的供体新鲜粪便样本,加入200ml无菌生理盐水中进行均质化处理,得到粪便浆体。之后将粪便浆体逐级经过50目、100目、200目和300目的无菌滤网得到粪便悬液,之后经4000r/min离心20min,弃去上层液体,得到的沉淀物为肠道菌,再将肠道菌按照质量比4:10悬于下表3中用于保护肠道菌的冻干保护剂中,之后冷冻,干燥得到肠道菌冻干粉。其中,冷冻的条件为:先-20℃预冻4h,而后转移至-80℃冷冻8h。干燥的条件为:在真空度为10pa,温度为-60℃下,真空干燥30h,即得肠道菌冻干粉。表3组分含量(g/100ml)甘油1.0水溶性淀粉10低聚半乳糖2.0甘露醇1.0无菌生理盐水86对比例1一种肠道菌冻干粉的制备方法,其大体上与实施例1相同,不同之处在于,不添加本发明实施例中的用于保护肠道菌的冻干保护剂。对比例2一种肠道菌冻干粉的制备方法,其大体上与实施例1相同,不同之处在于,将肠道菌悬于表4中的用于保护肠道菌的冻干保护剂中。表4组分含量(g/100ml)水溶性淀粉8.0低聚半乳糖1.0甘露醇0.5无菌生理盐水90对比例3一种肠道菌冻干粉的制备方法,其大体上与实施例1相同,不同之处在于,将肠道菌悬于表5中的用于保护肠道菌的冻干保护剂中。表5组分含量(g/100ml)甘油0.5低聚半乳糖1.0甘露醇0.5无菌生理盐水90对比例4一种肠道菌冻干粉的制备方法,其大体上与实施例1相同,不同之处在于,将肠道菌悬于表6中的用于保护肠道菌的冻干保护剂中。表6组分含量(g/100ml)甘油0.5水溶性淀粉8.0甘露醇0.5无菌生理盐水90对比例5一种肠道菌冻干粉的制备方法,其大体上与实施例1相同,不同之处在于,将肠道菌悬于表7中的用于保护肠道菌的冻干保护剂中。表7组分含量(g/100ml)甘油2.5水溶性淀粉15.0低聚半乳糖2.5甘露醇2.0无菌生理盐水78效果验证1、活菌计数试验试验方法:倾注平板法进行活菌计数。冻干前的活菌数(冷冻操作前):将待测样本梯度稀释后,培养计数。冻干后的活菌数:向冻干粉中加入无菌生理盐水溶液,补足至冻干前体积,活菌检测方法同上。试验结果见表8:表8组别总细菌存活率乳杆菌存活率双歧杆菌存活率实施例188.3%82.0%85.6%实施例283.2%79.8%84.6%实施例394.2%90.1%92.7%对比例135.5%23.9%31.4%对比例253.7%47.1%58.5%对比例377.4%80.6%73.8%对比例471.1%66.3%65.4%对比例570.2%73.4%80.9%由表8可知,在总细菌存活率、乳杆菌存活率和双歧杆菌存活率三方面,实施例1至实施例3效果明显高于对比例各组,对比例1中不添加冻干保护剂,对比例2至4为缺少用于保护肠道菌的冻干保护剂中的一种重要成分,效果明显比实施例组差。对比例5中虽然不缺少任何一种成分,但是冻干保护剂的组分配比关系与本发明中的用于保护肠道菌的冻干保护剂中的组分配比关系不同。总细菌存活率、乳杆菌存活率和双歧杆菌存活率均较实施例1差。2、菌群结构和丰度测试试验方法:称取50g供体新鲜粪便样本,加入200ml无菌生理盐水中进行均质化处理,得到粪便浆体。之后将粪便浆体逐级经过50目、100目、200目和300目的无菌滤网得到粪便悬液,之后经4000r/min离心20min,弃去上层液体,得到的沉淀物为肠道菌,将肠道菌沉按照质量比4:10重悬于无菌生理盐水中得到肠道菌液,并将肠道菌液均匀分成3等份,分别标记为ljy0、ljy1和ljy2,其中,ljy0不做任何处理,ljy1和ljy2在4000r/min离心20min,弃去上清液,加入实施例3中的用于保护肠道菌的冻干保护剂,将ljy0和ljy1放入-80℃下保存,ljy2按照实施例3的后续步骤进行继续冷冻,干燥得到肠道菌冻干粉。再将得到的冻干粉用生理盐水重悬至冻干前体积,即ljy0为原始菌液,ljy1为加入冻干保护剂处理的菌液,ljy2为进行冻干处理后将冻干粉重悬的菌液,最后,将ljy0,ljy1和ljy2进行高通量测序,试验结果见表9、图1和图2。表9为各样本在不同分类水平下(界、门、纲、目、科、属)物种种类数目统计表:表9样本ljy0ljy1ljy2界111门666纲111111目111112科222122属605859由表9可知,ljy1和ljy2在经过不同处理处理后,样本中的肠道菌的物种种类在不同分类水平(界、门、纲、目、科、属)相差不大,只在科、属水平上有轻微损失。此外,发明人还对ljy0、ljy1和ljy2进行out聚类分析和属水平的丰度测试,参阅图1,图1中三个圆圈相互重叠区域中的数字代表样本共有的out数目,非重叠区域中的数字代表样本特有的out数目(即差异性out),其中,ljy0、ljy1和ljy2三者共有的out数目可达111条,差异性out仅为2条和4条,由此可知,本发明实施例3中的肠道菌冻干粉可以最大程度的保留了肠道菌菌群的物种结构。参阅图2,图2为肠道菌中丰度最高的30个物种的丰度图,虽然有少部分物种的丰度有所损失,但是大部分丰度较高的物种,冻干前后丰度相差不大,这也印证了本发明实施例3中的肠道菌冻干粉可以有效保护肠道菌的菌群结构和丰度,减少冻干过程中造成的菌群损伤,维持肠道菌群的稳定性,进而减少菌群功能的丧失,使肠道菌群整体植入人体肠道,发挥抗炎作用。3、含肠道菌冻干粉的胶囊稳定性试验试验方法:随机抽取3份不同健康供体的新鲜粪便样本,分别采用实施例3的制备方法制得肠道菌冻干粉,在干燥无菌环境下,将肠道菌冻干粉装入羟丙甲基纤维素胶囊中得到含肠道菌冻干粉的胶囊。参照本发明活菌计数试验方法进行活菌计数。试验结果见图3,由图3可知,本发明的肠道菌冻干粉对不同健康供体的粪便样本中的有益菌均有很好的保护效果,试验稳定性好,各测试结果之间无显著差异。以上所述实施例的各技术特征可以进行任意的组合,为使描述简洁,未对上述实施例中的各个技术特征所有可能的组合都进行描述,然而,只要这些技术特征的组合不存在矛盾,都应当认为是本说明书记载的范围。以上所述实施例仅表达了本发明的几种实施方式,其描述较为具体和详细,但并不能因此而理解为对发明专利范围的限制。应当指出的是,对于本领域的普通技术人员来说,在不脱离本发明构思的前提下,还可以做出若干变形和改进,这些都属于本发明的保护范围。因此,本发明专利的保护范围应以所附权利要求为准。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1