一种抗癌药物的制备方法与流程
本发明涉及药物化合物的制备,具体涉及一种抗癌药物的制备方法。
背景技术:
crenolanib,作为一种有效的治疗肿瘤的药物,其结构式如下:
crenolanib是一种有效的、选择性pdgfrα/β抑制剂,能够抑制对imatinib耐药的pdgfrα激酶(d842i,d842v,d842y,d1842-843im,和缺失i843)活性;可用于多种癌症的治疗,包括急性髓性白血病、胃肠道间质瘤、胶质瘤和非小细胞肺癌等方面。
由于该药物有良好的治疗前景,现有技术已对该药物的合成进行了大量研究。其中wo2004/113322中合成该化合物的路线如下:
wo2004/020431的相关合成路线如下:
然而上述路线中存在以下缺陷:
(1)3-甲基-3-氧杂环丁烷甲醇与对甲苯磺酰氯或甲磺酰氯得到相应的磺酸酯,虽然提高了反应活性,但是由于对甲苯磺酰氯或甲磺酰氯为有刺激性的化工原料,而且生成的磺酸酯是药学领域已经验证过的遗传毒性物料,可能会对终产品的质量,带来潜在的隐患;
(2)缩合阶段使用了价格昂贵的三(二亚苄基丙酮)合二钯,且收率并不高;
(3)采用了甲醛与氢氧化钯还原硝基,再用钯碳脱除苄基,步骤相对繁琐;
(4)取代步骤里使用了价格昂贵的4,5-双(二苯基瞵)-9,9-二甲基三环二苯并配体(xantphos),增加了成本,而且导致产品纯度差,收率低;
(5)精制阶段使用了大量的有机混合溶剂,不易回收,产生大量的有机废液,容易给环境带来不必要的污染。
技术实现要素:
针对上述问题,本发明提供一种crenolanib新的制备方法,利用三个关键的中间体,在相对温和的条件下,合成出最终产品。与现有crenolanib生产工艺比较,具有流程简易,纯度高,收率高,流程短,物料易得价廉,成本低,操作安全等特点,更有利于工业化生产。
本发明的技术方案如下:
一种crenolanib的制备方法,包括:以2-氯-8-羟基喹啉为原料,经过三氟甲磺酰氯反应后,缩合、脱水、脱氯化氢、脱保护,即得。
所述制备方法的合成路线为:
进一步地,所述crenolanib的制备方法,包括:
(1)2-氯-8-羟基喹啉与三氟甲磺酰氯在溶剂中反应,得到中间体i(2-氯-8-三氟甲磺酸基喹啉);
(2)中间体i与哌啶-4-基氨基甲酸叔丁酯在溶剂中缩合反应,得到中间体ii(2-氯-8(哌啶-4-基)喹啉氨基甲酸叔丁酯);
(3)3-甲基-3-氧杂环丁烷甲醇与5-羟基苯并咪唑发生脱水反应,得到中间体iii(5-(3-甲基氧杂环丁烷-3-甲氧基)苯并咪唑);
(4)中间体ii与中间体iii在溶剂中发生脱氯化氢反应,生成中间体iv((1-{2-[5-(3-甲基-氧杂环丁烷-3-基甲氧基)-苯并咪唑-1-基]-喹啉-8-基}-哌啶-4-基-氨基甲酸叔丁酯);
(5)中间体iv在乙醇钠作用下发生脱保护,得到目标产物v((1-{2-[5-(3-甲基-氧杂环丁烷-3-基甲氧基)-苯并咪唑-1-基]-喹啉-8-基}-4-氨基哌啶)。
步骤(1)中,所述溶剂为dmf、dmso、乙腈、mdi、六甲基磷酰三胺(hmpa)中的一种或几种混合,优选dmf。所述2-氯-8-羟基喹啉与三氟甲磺酰氯摩尔比为1(1~1.2),以1:1.1为优;所述反应温度为25~30℃,反应时间20~30h。
步骤(1)中,合成路线为:
步骤(2)中,所述2-氯-8-三氟甲磺酸基喹啉与哌啶-4-基氨基甲酸叔丁酯的摩尔比为1:(1~1.2),以1:1.05为优;所述反应溶剂为氯苯、甲苯或二甲苯,以甲苯为优;反应温度为80℃~100℃,反应时间为20~30h。
步骤(2)中,合成路线为:
现有类似步骤(2)的工艺使用了4,5-双(二苯基瞵)-9,9-二甲基三环二苯并配体(xantphos),但是产品纯度较差,收率低,本申请采用了binap为配体催化剂,使得收率进一步提高。
步骤(3)中,所述3-甲基-3-氧杂环丁烷甲醇与5-羟基苯并咪唑摩尔比为1:(1~1.2),以1:1为优;回流温度为60~70℃,优选65-68℃,反应时间为20~24h。
步骤(3)中合成路线为:
本申请利用williamson醚合成法,可以很好地避开使用了有毒性的对甲苯磺酰氯或甲磺酰氯。
步骤(4)中,所述反应溶剂为甲苯、氯苯或二甲苯,优选甲苯;所述反应温度为80~100℃,所述反应时间为24~30h。
步骤(4)合成路线为:
步骤(5)中,所述中间体iv与乙醇钠摩尔比为1:(1.2~2),以1:1.4为优;所述反应温度为78~80℃,反应时间为3~4h。
步骤(5)合成路线为:
本发明所述的crenolanib的制备方法,与原先工艺比较,具有流程简易,纯度高(hplc99.26%),收率高(90.3%),流程短,物料易得价廉,成本低,操作安全等特点,更有利于工业化生产。
附图说明
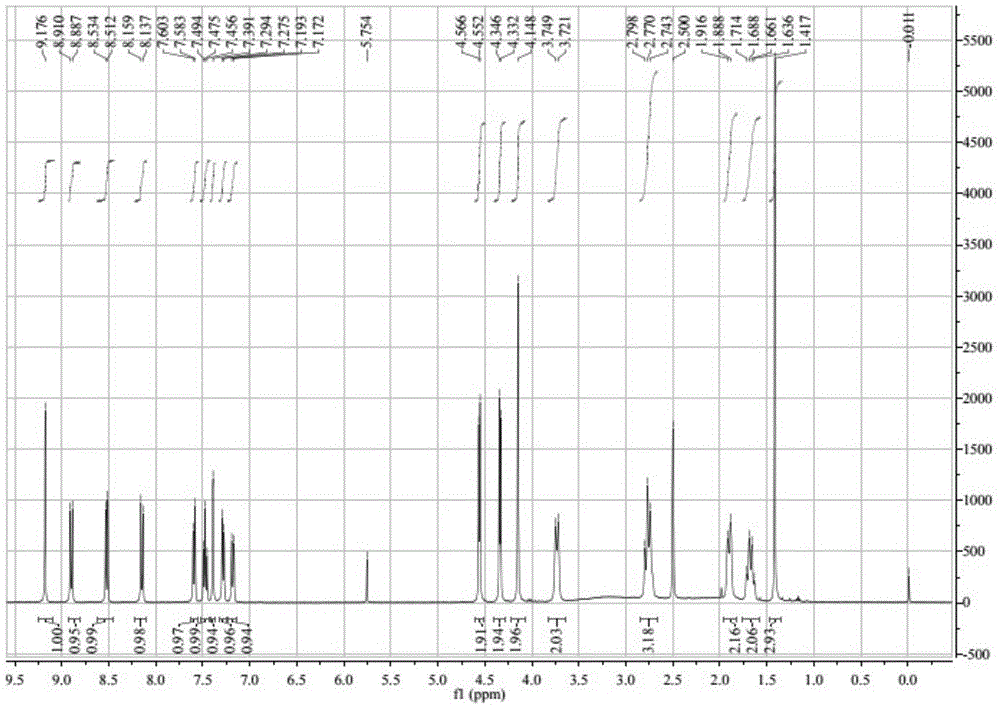
图1为实施例1所得crenolanib的1hnmr。
具体实施方式
以下实施例用于说明本发明,但不用来限制本发明的范围。
实施例1
本实施例提供一种苯并咪唑化合物的制备,包括:
(1)2-氯-8-三氟甲磺酸基喹啉(ι)的合成
将化合物2-氯-8-羟基喹啉50g、dmf150ml、三氟甲磺酰氯53g、三乙胺25g加入到250ml三颈瓶中,搅拌均匀;控温在25~30℃反应20~30h;
反应完全后,过滤析出的固体,滤饼用正己烷20ml×3洗涤,40℃鼓风干燥,所得类白色固体2-氯-8-三氟甲磺酸基苯并咪唑83.39g,收率95.78%;
(2)2-氯-8(哌啶-4基)喹啉氨基甲酸叔丁酯(ⅱ)的合成
向250ml三颈瓶中加入binap0.2g、甲苯70ml,控温在20~25℃搅拌1h;
再向瓶中加入2-氯-8-三氟甲磺酸基喹啉10g、哌啶-4-基氨基甲酸叔丁酯6.41g、碳酸钾7.8g,搅拌下将反应液加热至80℃~100℃,保持此温度反应20~30h;
tlc检测,反应是否完全;反应完全,停止加热;降温至20~30℃,加入二氯乙烷50ml,加硅藻土过滤掉反应液中的固体,滤饼用乙酸乙酯150ml洗涤,20~25℃搅拌8h;过滤掉溶液中析出的固体,滤液用5%磷酸氢二钠溶液2×50ml洗涤;再次将有机相浓缩至干,加入乙腈50ml,20~25℃搅拌析晶10~20h;过滤析出的固体,40℃鼓风干燥得到黄色固体10.69g,2-氯-8(哌啶-4-基)苯并咪唑氨基甲酸叔丁酯,收率92.3%;
(3)5-(3-甲基氧杂环丁烷-3-甲氧基)苯并咪唑(ⅲ)的合成
将化合物3-甲基-3-氧杂环丁烷甲醇30.77g、thf140ml、金属钠6.95g加入到250ml三颈瓶中,搅拌下加热至65~68℃回流4h,冷却至55℃,然后加入5-羟基苯并咪唑40.4g,搅拌下加热回流,反应20~24h;
向反应瓶中加入乙酸乙酯100ml,在30~50℃搅拌0.5h溶解,然后降低至-5℃,滴加正己烷30ml,搅拌1h,抽滤得到浅黄色固体,40℃干燥至恒重,得到56.41克,收率85.8%。
(4)(1-{2-[5-(3-甲基-氧杂环丁烷-3-基甲氧基)-苯并咪唑-1-基]-喹啉-8-基}-哌啶-4-基-氨基甲酸叔丁酯(iv)的合成
ⅱ(50克)、ⅲ(30.14克)、碳酸钾80g、diphos4.3g、甲苯700ml,加入到2l三颈瓶中,加入乙酸钯0.9g,搅拌均匀;搅拌下升温,控温在80~100℃反应24~30h;反应完成后,降温至55℃加入二氯乙烷700ml;搅拌10min,加硅藻土过滤反应液中的固体,滤饼用500ml二氯乙烷冲洗;将滤液浓缩至干,加入乙酸乙酯480ml,加热至回流,降温至20~25℃析晶10~20h;过滤析出的固体,50℃鼓风干燥,得到白色固体,得量70.51g,收率93.90%;
(5)(1-{2-[5-(3-甲基-氧杂环丁烷-3-基甲氧基)-苯并咪唑-1-基]-喹啉-8-基}-4-氨基哌啶(v)的合成
将化合物(1-{2-[5-(3-甲基-氧杂环丁烷-3-基甲氧基)-苯并咪唑-1-基]-喹啉-8-基}-哌啶-4-基-氨基甲酸叔丁酯5g、乙醇钠2.8g、2-甲基四氢呋喃30ml和水0.08ml加入到100ml三颈瓶中,搅拌均匀;将该混合物加热至回流,并在回流下搅拌3~4h;
tlc检测,反应完全;停止加热,加入纯化水60ml,萃取分层;水相用乙酸乙酯2×20ml萃取,合并有机相,用饱和氯化钠溶液20ml洗涤;减压浓缩有机相,向浓缩剩余物中加入30ml乙酸乙酯,在20~25℃搅拌析晶6h;过滤析出的固体,滤液减压浓缩至干;向剩余物中加入24ml乙酸乙酯,在20~25℃搅拌析晶10~12h;过滤析出的固体,干燥得白色固体产品,得量3.68g,收率90.3%,纯度为99.26%。
1hnmr测试,见图1。
(d6-dmso):δ9.176(s,1h),δ8.88-8.91(d,1h,j=8.7hz),δ8.51-8.53(d,1h,j=9.0hz),δ8.13-8.15(d,1h,j=9.0hz),δ7.6(d,1h,j=7.5hz),7.49(t,1h,j=7.9hz),7.39(d,1h,j=2.4hz),7.29(d,1h,j=7.6hz),7.19(dd,1h,j=9.2hz,2.5hz),4.56(d,2h,j=5.6hz),4.34(d,2h,j=5.7hz),4.14(s,2h),3.74(d,2h,j=10.1hz),2.77(m,3h),1.91(d,2h,j=11.1hz),1.68(m,2h),1.41(s,3h).
虽然,上文中已经用一般性说明及具体实施方案对本发明作了详尽的描述,但在本发明基础上,可以对之作一些修改或改进,这对本领域技术人员而言是显而易见的。因此,在不偏离本发明精神的基础上所做的这些修改或改进,均属于本发明要求保护的范围。
- 还没有人留言评论。精彩留言会获得点赞!