金属桥联并具有多维结构的多酸化合物及其应用的制作方法
本发明涉及多酸化合物领域。更具体地说,本发明涉及一种金属桥联并具有多维结构的多酸化合物及其应用。
背景技术:
多酸是无机化学中的重要研究对象,学名为多金属氧酸盐(polyoxometalates,poms)或金属-氧簇(metal-oxygenclusters),其主要是由无机含氧酸根离子缩合而得到的化合物,根据有无杂原子可以分为同多酸化合物(例如六钼酸)和杂多酸化合物(例如磷钨酸)。在多酸化合物中能作为配原子的元素主要包括mo、w、nb等,而可以作为杂原子的元素已接近70种,所以多金属氧酸盐具有种类多和结构比较复杂的特点。近年来,选择合适的配体作为结点将各种多酸建筑块连接为一维、二维或者三维构架结构是多酸化学研究领域的一个热点。特别是由于全无机的多维多酸化合物具有稳定性好和结构多变的优点使其具有很大的应用前景,但是目前只有较少的全无机的多维多酸化合物被报道。在已报道的多维多酸化合物中通常是使用有机配体作为桥联配体来构建的。因此设计和合成全无机的多维多酸化合物仍是多酸化学研究中的一个难题。
技术实现要素:
为了实现以上目的,本发明提供一种金属桥联并具有多维结构的多酸化合物,该多酸化合物由钼酸铵、有机配体以及金属盐在醇溶液作为溶剂中进行热合反应得到;
其中,所述钼酸铵为(nh4)6mo7o24·4h2o;
有机配体为乙二胺/(1r,2r)-1,2-二苯基乙二胺;
金属盐为铜盐。
优选的是,如权利要求1所述的金属桥联并具有多维结构的多酸化合物,所述多酸化合物为化合物1或化合物2;
其中,化合物1的化学式为[cu3(en)6(mo7o24)]·6h2o,en=乙二胺
化合物2的化学式为[cu(dpen)2(mo8o26)0.5]·2h2o,dpen=(1r,2r)-1,2-二苯基乙二胺。
优选的是,如权利要求1所述的金属桥联并具有多维结构的多酸化合物,化合物1为一维链结构。
优选的是,如权利要求1所述的金属桥联并具有多维结构的多酸化合物,化合物2为三维无机有机杂化骨架。
优选的是,如权利要求1所述的金属桥联并具有多维结构的多酸化合物,所述化合物1的合成方法如下:
将cu(no3)2·4h2o、(nh4)6mo7o24·4h2o溶于dmf/正丙醇/h2o混合溶剂中,滴入乙二胺混合,放入小瓶中,并将小瓶放置于烘箱中,80℃反应12h,得到紫色块状晶体,即为目标产物[cu3(en)6(mo7o24)]·6h2o。
优选的是,如权利要求1所述的金属桥联并具有多维结构的多酸化合物,所述化合物2的合成方法如下:
将cu(no3)2·4h2o、(1r,2r)-1,2-二苯基乙二胺和(nh4)6mo7o24·4h2o,溶于dmf/正丙醇/h2o混合溶剂中,置于小瓶中,放入烘箱中,80℃反应3天,得到紫色长条状晶体。
优选的是,如权利要求1所述的金属桥联并具有多维结构的多酸化合物,所述化合物1的合成方法如下:
将0.3mmcu(no3)2·4h2o、0.06mm(nh4)6mo7o24·4h2o溶于dmf/正丙醇/h2o混合溶剂中(三者摩尔比例1:1:1),滴入2滴乙二胺混合,放入小瓶中,并将小瓶放置于烘箱中,80℃反应12h,得到紫色块状晶体,即为目标产物[cu3(en)6(mo7o24)]·6h2o。
优选的是,如权利要求1所述的金属桥联并具有多维结构的多酸化合物,所述化合物2的合成方法如下:
将0.03mmcu(no3)2·4h2o、0.1mm(1r,2r)-1,2-二苯基乙二胺和0.06mm(nh4)6mo7o24·4h2o,溶于dmf/正丙醇/h2o混合溶剂中(三者摩尔比例1:1:1),置于小瓶中,放入烘箱中,80℃反应3天,得到紫色长条状晶体。
一种金属桥联并具有多维结构的多酸化合物作为光催化材料降解有机染料的应用。
一种所述的金属桥联并具有多维结构的多酸化合物作为金属清洗剂的添加剂的应用。
本发明至少包括以下有益效果:本发明提供的金属桥联并具有多维结构的多酸化合物制备方法简单,对有机染料的催化能力强,而且具有很好的去污去锈清洁效果;可作为废水中有机污染物的光降解催化剂,也可作为去污去锈清洗剂。
本发明的其它优点、目标和特征将部分通过下面的说明体现,部分还将通过对本发明的研究和实践而为本领域的技术人员所理解。
附图说明
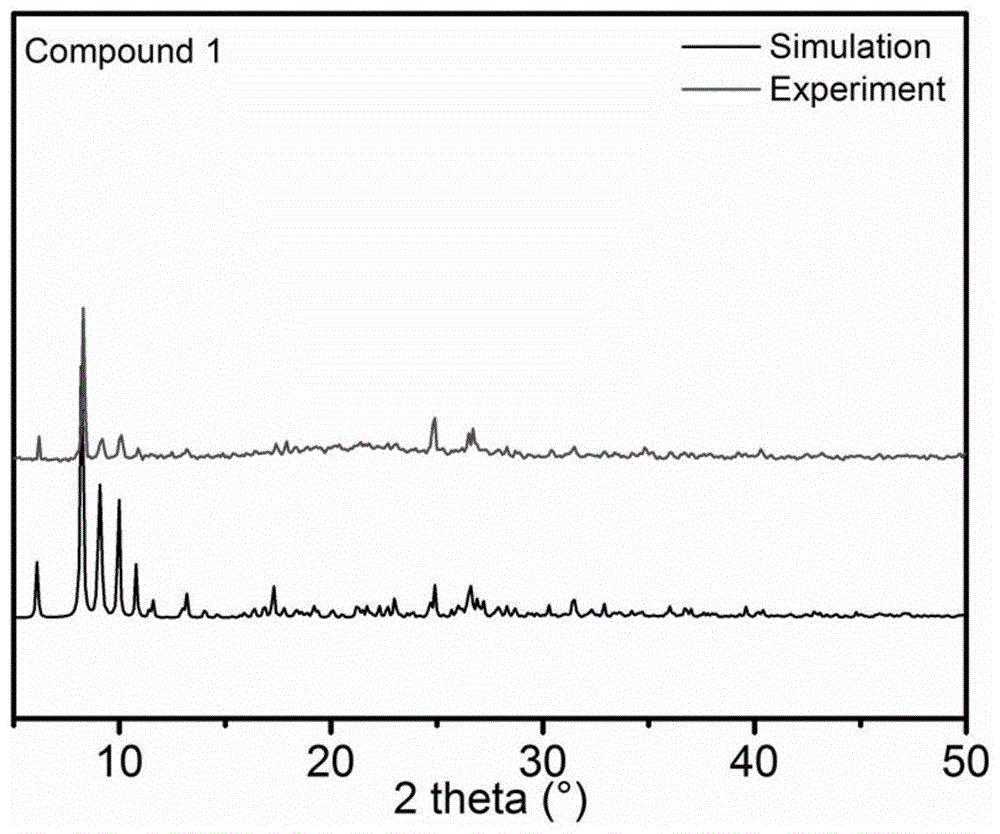
图1为实施例1中化合物1的粉末x-射线衍射图谱;
图2为实施例2中化合物2的粉末x-射线衍射图谱;
图3为实施例1中化合物1的红外光谱分析;
图4为实施例2中化合物2的红外光谱分析;
图5为化合物1的分子结构图;
图6为化合物2的分子结构图;
图7为实施例1中化合物1对于亚甲基蓝的光催化图;
图8为实施例2中化合物2对于亚甲基蓝的光催化图;
图9为实施例1中化合物1对于盐酸副玫瑰苯胺的光催化图;
图10为实施例2中化合物2对于盐酸副玫瑰苯胺的光催化图。
具体实施方式
下面结合附图对本发明做进一步的详细说明,以令本领域技术人员参照说明书文字能够据以实施。
实施例1
化合物1的合成
将0.3mmcu(no3)2·4h2o、0.06mm(nh4)6mo7o24·4h2o溶于dmf/正丙醇/h2o混合溶剂中(三者摩尔比例1:1:1),滴入2滴乙二胺混合,放入小瓶中,并将小瓶放置于烘箱中,80℃反应12h,得到紫色块状晶体,即为目标产物化合物1[cu3(en)6(mo7o24)]·6h2o。
实施例2
化合物2的合成
将0.03mmcu(no3)2·4h2o、0.1mm(1r,2r)-1,2-二苯基乙二胺和0.06mm(nh4)6mo7o24·4h2o,溶于dmf/正丙醇/h2o混合溶剂中(三者摩尔比例1:1:1),置于小瓶中,放入烘箱中,80℃反应3天,得到紫色长条状晶体,即为目标产物化合物2。
其他测试数据
(1)粉末衍射表征相纯度
化合物1的pxrd衍射图如图1所示,实验测得的关键衍射峰位置与理论计算得到的关键衍射峰位置相互匹配,这表明化合物1纯度较高,是单一相。衍射峰强度的不同可能是实验收集数据的过程中粉末择优取向的变化所致。
化合物2的pxrd衍射图如图2所示,实验测得的关键衍射峰位置与理论计算得到的关键衍射峰位置大致一致,这表明化合物2有较高纯度,是单一相。衍射峰强度的不同可能是实验收集数据的过程中粉末择优取向的变化所致。
(2)晶体结构测定
晶体的x-射线衍射数据在oxforddiffractiongeminirultra衍射仪上收集,用经石墨单色器单色化的mo-kα射线
表1化合物1和2的晶体学数据和结构参数
表2化合物1的键长
表3化合物1的键角
表4化合物2的键长
表5.化合物2的键角
(3)晶体结构分析
1、化合物1-[cu3(en)6(mo7o24)]·6h2o的晶体结构
单晶x-射线衍射表明化合物1结晶在单斜晶系p21/n空间群中。化合物1包含三个cu离子,六个en配体,一个同多钼酸盐[mo7o24]6-多阴离子和六个间隙水分子。通过键价计,所有的mo原子都是+vi氧化态,所有的cu原子都是+ii氧化态。化合物1中包含四个晶体学独立的cu(ii)离。cu1位于一个扭曲的八面体几何中,它与来自两个en配体的四个n原子进行配位形成平面单元[cu(en)2],再以一个配位水分子和[mo7o24]6-多阴离子的一个终端o原子作为顶点进行六配位。cu2与两个en分子形成平面单元[cu(en)2],与[mo7o24]6-多阴离子的一个桥连o原子作为顶点进行五配位形成四棱锥几何构型。cu3与两个en分子形成平面单元[cu(en)2],与[mo7o24]6-多阴离子的两个桥连o原子作为顶点进行六配位形成八面体几何构型。同样地,cu4与两个en分子形成平面单元[cu(en)2],与[mo7o24]6-多阴离子的两个终端o原子作为顶点进行六配位形成八面体几何构型。一个[mo7o24]6-多阴离子可以与四个[cu(en)2]平面单元进行配位。cu-o键和cu-n键的键长范围分别在
2、化合物2-[cu(dpen)2(mo8o26)0.5]·2h2o的晶体结构
单晶x-射线衍射表明化合物2结晶在单斜晶系i2/c空间群中。化合物2中包含一个cu离子,两个dpen配体,半个同多钼酸盐[mo8o26]4-多阴离子和两个间隙水分子。通过键价计算,所有的mo原子都是+vi氧化态,所有的cu原子都是+ii氧化态,化合物2中包含两个晶体学独立的cu(ii)离子。cu1位于一个扭曲的八面体几何中,它与来自两个dpen配体的四个n原子进行配位形成平面单元[cu(dpen)2],与两个[mo8o26]4-多阴离子的两个终端o原子作为顶点进行六配位。同样地,cu2与两个dpen分子形成平面单元[cu(dpen)2],与两个[mo8o26]4-多阴离子的两个桥连o原子作为顶点进行六配位形成扭曲八面体几何构型。一个[mo8o26]4-多阴离子可以与四个cu离子进行配位。cu-o键和cu-n键的键长范围分别在
(4)、红外光谱分析
化合物1的红外光谱如图所示,1042cm-1,878cm-1,635cm-1处的振动峰对应为[mo7o24]6-中mo-o的伸缩振动和弯曲振动。1580cm-1处的振动峰属于en配体中-nh2的弯曲振动峰。3300cm-1处的特征峰为水分子中o-h的伸缩振动峰。
化合物2的红外光谱如图所示,在948cm-1和698cm-1处出现的振动峰归属于[mo8o26]4-中mo-o的不对称伸缩振动峰。1648cm-1处的振动峰属于dpen配体中-nh2的弯曲振动峰。912cm-1和845cm-1和698cm-1属于dpen配体中苯环的吸收特征峰。3295cm-1处的特征峰为水分子的o-h的伸缩振动峰。
(5)化合物1、化合物2对亚甲基蓝的光催化性能
称取少量晶体于烧杯中,加入亚甲基蓝(6mg/l-1),再向另一个烧杯中加入亚甲基蓝(6mg/l-1)作为空白对照。将烧杯置于紫外灯照射下的磁力搅拌器上,每隔半小时取出一部分反应溶液进行紫外测定。
如图7~8所示,经紫外测定后分析图可以得到化合物1、2对亚甲基蓝都具有催化降解作用,3小时内,化合物1的催化转化率高达87%,化合物2的催化转化率高达83%。
(6)化合物1、化合物2对盐酸副玫瑰苯胺的光催化性能
称取少量晶体于烧杯中,加入盐酸副玫瑰苯胺(6mg/l-1)),再向另一个烧杯中加入盐酸副玫瑰苯胺(6mg/l-1)作为空白对照。将烧杯置于紫外灯照射下的磁力搅拌器上,每隔半小时取出一部分反应溶液进行紫外测定。
如图9~10所示,经紫外测定后分析图可以得到化合物1、2对盐酸副玫瑰苯胺都具有催化降解作用,3小时内,化合物1的催化转化率高达90%,化合物2的催化转化率高达86%。
(7)化合物1、化合物2作为金属清洗剂的添加剂的应用。
实施例1:金属清洗剂1(包含化合物1)
将3g消泡剂磷酸三丁酯、6g阳离子表面活性剂氯化二硬脂基二甲基铵、5g阴离子表面活性剂甲苯基磺酸钠、10g硅表面活性剂、5g化合物1溶解在50ml水中,搅拌30分钟左右,即得。
实施例2:金属清洗剂2(包含化合物2)
将3g消泡剂磷酸三丁酯、6g阳离子表面活性剂氯化二硬脂基二甲基铵、5g阴离子表面活性剂甲苯基磺酸钠、10g硅表面活性剂、5g化合物2溶解在50ml水中,搅拌30分钟左右,即得。
对比例1:金属清洗剂3(空白对照组)
将3g消泡剂磷酸三丁酯、6g阳离子表面活性剂氯化二硬脂基二甲基铵、5g阴离子表面活性剂甲苯基磺酸钠、10g硅表面活性剂溶解在50ml水中,搅拌30分钟左右,即得。
使用上述金属清洗剂1-4分别清洗金属铝清洗表面油污清洗,结果见表1。
表13种金属清洗剂的性能表征
其中,清洗率=清洗掉的油污重/油污原重;
稳定性:分别将50ml的金属清洗剂1-2在25℃的条件下,放置1个月后,观察其分层情况,稳定为不分层不浑浊,不稳定为分层或浑浊。由表1可知,化合物1-2作为金属清洗剂的添加剂能提高去污能力。
由上表1可知,以本发明的化合物1、化合物2制备得到的金属清洗剂,具有很好的清洗效果,而且性能稳定,具有很好的市场应用前景。
尽管本发明的实施方案已公开如上,但其并不仅仅限于说明书和实施方式中所列运用,它完全可以被适用于各种适合本发明的领域,对于熟悉本领域的人员而言,可容易地实现另外的修改,因此在不背离权利要求及等同范围所限定的一般概念下,本发明并不限于特定的细节和这里示出与描述的图例。
- 还没有人留言评论。精彩留言会获得点赞!