解脲脲原体核酸检测试剂盒的制作方法
本发明涉及检测领域,特别涉及一种解脲脲原体核酸检测试剂盒。
背景技术:
解脲脲原体(Ureaplasma Urealyticum,UU)是人类泌尿生殖道常见的寄生菌之一,在特定环境下可致病。UU结构简单,无细胞壁,其形状呈高度多态性,且营养要求高,生长缓慢。UU在人体定植数量有两次高峰期,即分娩时由母体产道感染新生儿,以后迅速减少,从性生活开始又逐渐增多。UU主要通过性生活传播,亦可以经胎盘垂直传播或由孕妇下生殖道感染上行扩散,引起宫内感染。其感染可导致不孕不育、孕妇流产、早产、胎儿发育迟缓等一系列不良后果。目前病原学检查方法主要有分离培养及分子生物学检测,不同方法各有其特点,寻求快速、简便、准确检测UU的方法对于临床诊治十分必要。
技术实现要素:
本发明的主要目的是提出一种解脲脲原体核酸检测试剂盒,旨在提升解脲脲原体核酸检测的检测精度。
为实现上述目的,本发明提出的解脲脲原体核酸检测试剂盒,包括上游引物、下游引物和探针,所述上游引物的序列如SEQ ID NO:1所示,所述下游引物的序列如SEQ ID NO:2所示;
所述探针为x-CCATCAGGTACTGCTATTCG-MGB;或者,
所述探针为x-CCATCAGGTACTGCTATTCG-y+MGB,所述x为荧光报告基团,所述y为淬灭基团。
可选地,在本实施例中,所述x为FAM基团、VIC基团、TEXAS RED基团中的任意一种。
可选地,所述解脲脲原体核酸检测试剂盒还包括Taq酶、PCR缓冲液、dNTPS以及MgCl2。
可选地,所述解脲脲原体核酸检测试剂盒还包括DNA提取液,所述DNA提取液包括:聚乙二醇6000、氯化钠、十二烷基磺酸钠Tween-20、乙醇和溶剂TE缓冲液。
本发明技术方案采用序列如SEQ ID NO:1所示的上游引物、序列如SEQ ID NO:2所示的下游引物以及所述探针进行解脲脲原体核酸检测,所述上游引物、所述下游引物位于基因保守区域,可以扩增出所有的血清型,具有适用范围广的优点。所述探针为MGB探针,MGB探针的淬灭基团采用非荧光淬灭基团,非荧光淬灭基团本身不产生荧光,可以大大降低本底信号的强度,有利于提升检测时荧光变化的灵敏度,从而提升检测的灵敏度;另一方面,MGB基团可以将探针的Tm值提高10℃左右,有利于以减少非特异性结合,提升检测的精度。所述探针与模板之间只要有一个碱基错配,探针就会检测碱基错配,此时探针将不会与目的片段杂交,从而不产生荧光信号,大大提高了检测的特异性,有利于提升检测的精度。
附图说明
为了更清楚地说明本发明实施例或现有技术中的技术方案,下面将对实施例或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本发明的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图示出的结构获得其他的附图。
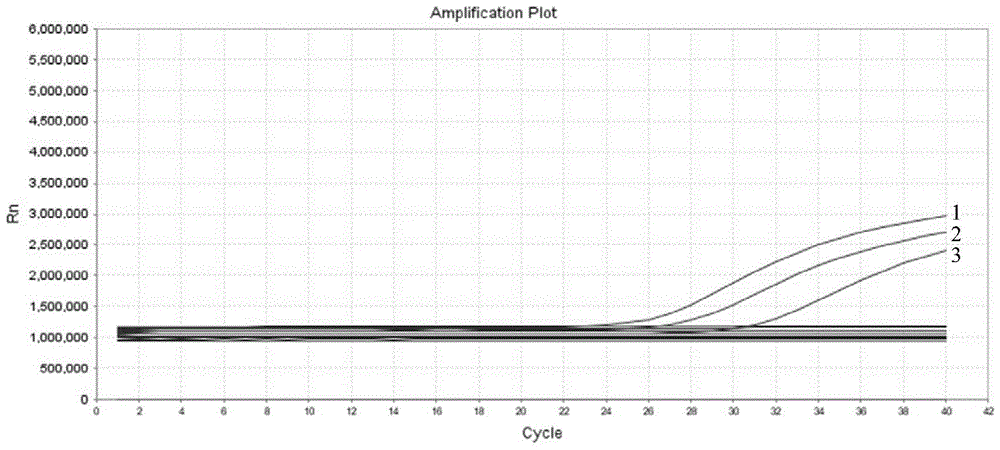
图1是采用本发明所述解脲脲原体核酸检测试剂盒一实施例测试人型支原体、人乳头瘤病毒、沙眼衣原体、淋球菌、巨细胞病毒、肺炎支原体、生殖支原体、单纯疱疹病毒Ⅱ型、大肠埃希菌、解脲脲原体标准株、解脲脲原体临床株以及阳性质控物的荧光强度变化曲线,图1中S型曲线1至3依次分别为解脲脲原体标准株、解脲脲原体临床株和阳性质控物的荧光强度变化曲线;
图2是采用本发明所述解脲脲原体核酸检测试剂盒一实施例测试浓度分别为106copies/μL、105copies/μL、104copies/μL、103copies/μL、102copies/μL、20copies/μL的模板的荧光强度变化曲线,图2中S型曲线4至9依次分别为106copies/μL、105copies/μL、104copies/μL、103copies/μL、102copies/μL、20copies/μL浓度模板的荧光强度变化曲线。
本发明目的的实现、功能特点及优点将结合实施例,参照附图做进一步说明。
具体实施方式
下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明的一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有作出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
需要说明,若本发明实施例中有涉及方向性指示(诸如上、下、左、右、前、后……),则该方向性指示仅用于解释在某一特定姿态(如附图所示)下各部件之间的相对位置关系、运动情况等,如果该特定姿态发生改变时,则该方向性指示也相应地随之改变。
另外,若本发明实施例中有涉及“第一”、“第二”等的描述,则该“第一”、“第二”等的描述仅用于描述目的,而不能理解为指示或暗示其相对重要性或者隐含指明所指示的技术特征的数量。由此,限定有“第一”、“第二”的特征可以明示或者隐含地包括至少一个该特征。另外,各个实施例之间的技术方案可以相互结合,但是必须是以本领域普通技术人员能够实现为基础,当技术方案的结合出现相互矛盾或无法实现时应当认为这种技术方案的结合不存在,也不在本发明要求的保护范围之内。
本发明提出一种解脲脲原体核酸检测试剂盒。
在本发明实施例中,为实现上述目的,本发明提出的解脲脲原体核酸检测试剂盒,包括上游引物、下游引物和探针,所述上游引物的序列如SEQ ID NO:1所示,所述下游引物的序列如SEQ ID NO:2所示;所述探针为x-CCATCAGGTACTGCTATTCG-y+MGB,所述x为荧光报告基团,所述y为淬灭基团。采用所述解脲脲原体核酸检测试剂盒进行测试时,先提取待测物中的DNA,然后采用所述上游引物、所述下游引物以及所述探针测试获得的DNA,然后检测荧光,以得到检测结果。本实施例所述的探针不仅限于上述技术方案,在其他实施例中,也可以是,所述探针为x-CCATCAGGTACTGCTATTCG-MGB,所述x为荧光报告基团。
本发明技术方案采用序列如SEQ ID NO:1所示的上游引物、序列如SEQ ID NO:2所示的下游引物以及所述探针进行解脲脲原体核酸检测,所述上游引物、所述下游引物位于基因保守区域,可以扩增出所有的血清型,具有适用范围广的优点。所述探针为MGB探针,MGB探针的淬灭基团采用非荧光淬灭基团(Non-Fluorescent Quencher),本身不产生荧光,可以大大降低本底信号的强度,有利于提升检测时荧光变化的灵敏度,从而提升检测的灵敏度;另一方面,MGB基团可以将探针的Tm值提高10℃左右,有利于以减少非特异性结合,提升检测的精度。所述探针与模板之间只要有一个碱基错配,探针就会检测碱基错配,此时探针将不会与目的片段杂交,从而不产生荧光信号,大大提高了检测的特异性。
进一步地,在本实施例中,所述x为FAM基团、VIC基团、TEXAS RED基团中的任意一种,具有荧光效果良好的特点。
进一步地,在本实施例中,所述解脲脲原体核酸检测试剂盒还包括Taq酶、PCR缓冲液、dNTPS以及MgCl2。Taq酶为一种耐热性好的DNA聚合酶,Taq酶可以耐受90℃以上的高温而不失活,能够在整个扩增过程中持续使用,使的扩增过程变得非常简捷。所述解脲脲原体核酸检测试剂盒还包括UNG酶。
进一步地,在本实施例中,所述解脲脲原体核酸检测试剂盒还包括DNA提取液,所述DNA提取液包括:聚乙二醇6000、氯化钠、十二烷基磺酸钠Tween-20、乙醇和溶剂TE缓冲液。
本实施例所述的解脲脲原体核酸检测试剂盒的一种使用方法,包括以下步骤:
取200μL分泌物放入到1.5mL离心管中,在12000rpm的转速下离心5分钟,倒除液体,获得底物;
在所述底物中再加入DNA提取液,在100℃下加热10分钟后再次离心,获取上清液,得到所述样本核酸;所述DNA提取液具体包括:50mM/L的聚乙二醇6000、100mM/L的氯化钠,十二烷基磺酸钠0.2wt.%,0.5wt.%的Tween-20,0.1wt.%的乙醇和溶剂TE缓冲液;
将40μL荧光PCR体系加入所述样本核酸中,再以95℃加热3min、95℃加热15秒、52℃加热35秒为一个加热周期,加热40个加热周期;该40μL荧光PCR体系包括1.5U~2U的Taq酶、0.5U的UNG酶、PCR缓冲液、0.2mM dNTPS、2mM MgCl2、0.2μM上游引物、0.2μM下游引物以及0.1μM探针;一个加热周期对应一个PCR反应周期;所述dNTPS中各种成分的摩尔比例为dATP:dCTP:dGTP:dUTP=1:1:1:1。
监测加热周期中的荧光变化,若荧光信号增长,则存在解脲脲原体病毒感染。
人型支原体、人乳头瘤病毒、沙眼衣原体、淋球菌、巨细胞病毒、肺炎支原体、生殖支原体、单纯疱疹病毒Ⅱ型、大肠埃希菌为人体泌尿生殖道常见的病原体或定植菌,为采用试剂盒检测分泌物时,常伴随解脲脲原体核酸出现的病原体或定植菌。为了检测所述解脲脲原体核酸检测试剂盒的特异性,采用上述解脲脲原体核酸检测试剂盒的使用方法,对包括人型支原体、人乳头瘤病毒、沙眼衣原体、淋球菌、巨细胞病毒、肺炎支原体、生殖支原体、单纯疱疹病毒Ⅱ型、大肠埃希菌以及解脲脲原体临床株的目标进行检测,通过荧光PCR仪监测分析荧光进行结果判读,检测得到的荧光强度的变化曲线如图1所示。
图1中显示,在40个PCR反应周期后,脲脲原体临床株的荧光强度大于阳性质控物的荧光强度,小于脲脲原体标准株的荧光强度,所述解脲脲原体核酸检测试剂盒对脲脲原体临床株的检测结果有效。由图1可知,采用本实施例所述解脲脲原体核酸检测试剂盒进行检测时,人型支原体、人乳头瘤病毒、沙眼衣原体、淋球菌、巨细胞病毒、肺炎支原体、生殖支原体、单纯疱疹病毒Ⅱ型和大肠埃希菌都未出现荧光增长,而解脲脲原体临床株出现明显的荧光增长,由此可知所述解脲脲原体核酸检测试剂盒具有良好的特异性。
为了检测所述解脲脲原体核酸检测试剂盒的特异性,采用上述解脲脲原体核酸检测试剂盒的使用方法,对浓度分别为106copies/μL、105copies/μL、104copies/μL、103copies/μL、102copies/μL、20copies/μL的已连接靶基因的质粒的模板进行检测,通过荧光PCR仪监测分析荧光进行结果判读,以荧光分析判读方法的最低检测量作为检测下限,检测得到的荧光强度的变化曲线如图2所示。
由图2可知,浓度为106copies/μL的模板检测得到的曲线在第18个PCR反应周期时开始出现荧光增长,到第20个PCR反应周期时出现明显的荧光增长,因此,在第20个PCR反应周期时,所述解脲脲原体核酸检测试剂盒就能根据荧光增长判定检测结果,因此,所述解脲脲原体核酸检测试剂盒检测解脲脲原体的下限为20个拷贝,该解脲脲原体核酸检测试剂盒具有良好的灵敏性,能有效提升检测的精准度;浓度为106copies/μL、105copies/μL、104copies/μL、103copies/μL、102copies/μL、20copies/μL的所有模板在40个PCR反应周期时均出现明显的荧光增长,可知该解脲脲原体核酸检测试剂盒具有良好的灵敏性;检测的模板的浓度低至20copies/μL也能在第40个PCR反应周期检测出,基于良好的灵敏性,本实施例所述解脲脲原体核酸检测试剂盒具有检测周期数少的优点,能够有效提升检测的效率。
以上所述仅为本发明的优选实施例,并非因此限制本发明的专利范围,凡是在本发明的发明构思下,利用本发明说明书及附图内容所作的等效结构变换,或直接/间接运用在其他相关的技术领域均包括在本发明的专利保护范围内。
SEQUENCE LISTING
<110> 深圳市国赛生物技术有限公司
<120> 一种于解脲脲原体核酸检测试剂盒
<130> QPA1912443CN
<160> 2
<170> PatentIn version 3.3
<210> 1
<211> 20
<212> DNA
<213> 人工序列
<400> 1
cgttgcatta gatggtggta 20
<210> 2
<211> 19
<212> DNA
<213> 人工序列
<400> 2
aggtgaaaca gttgtggct 19
- 还没有人留言评论。精彩留言会获得点赞!