一种N-混杂卟啉光动力治疗剂及其合成方法与流程
本发明涉及有机精细化工技术领域,特别是一种含有n-混杂卟啉光动力治疗剂合成及其应用。
背景技术:
光动力治疗(photodynamictherapy,pdt)是利用光敏剂吸收光能,在体内原位产生活性氧(主要为单线态氧),从而对恶性肿瘤造成氧化性损伤的一种介入性疗法。在众多敏化剂中,卟啉类敏化剂率先被批准做临床研究,是一类极具发展前景的光敏染料之一,已在生命科学、光学药物和材料学等领域中发挥了极其重要的作用。目前,光动力治疗剂存在化合物稳定性差,在水溶液中易团聚,导致其单线态氧产率下降,分布不均匀,而n-混杂卟啉由于单线态氧产率较低,且本身在材料制备过程中合成复杂,难以在光动力治疗剂中应用。因此,对n-混杂卟啉类化合物进行改进是目前科研工作的重点及难点。
技术实现要素:
本发明的主要目的在于提供一种简单合成方法,得到n-混杂卟啉光动力治疗剂及其应用。
本发明的技术方案如下:
一种n-混杂卟啉光动力治疗剂,所述化学结构式为:
合成所述的含有n-混杂卟啉光动力治疗剂的方法,所述方法包括以下合成路径:
所述方法包括以下步骤:
1)在室温下向反应瓶中加入化合物5-卤代-2,3,3-三甲基吲哚(1),5,10,15,20-四苯基-n-混杂卟啉(2)和甲苯,搅拌溶解;
2)将所述步骤1)在冰乙酸催化剂的条件下,升温回流,得到深红色混合液;
3)向所述步骤2)中的固体化合物纯化得到深红色固体化合物3;
完成大共轭二吡咯烯染料的合成。
所述步骤1)化合物1与化合物2的投料比为1.2-5:1。
所述步骤2)化合物1的反应活性较高,在冰乙酸催化剂条件下进行反应。
所述步骤2)冰乙酸与化合物2的投料比为0.2-2:1。
所述步骤2)的回流反应温度为120-125℃,回流反应时间为0.5-3小时所述步骤3)分离方法为利用硅藻土柱层析分离得到目的产物3。
本发明有益效果如下:
1、本发明为以5-卤代-2,3,3-三甲基吲哚与5,10,15,20-四苯基-n-混杂卟啉通过一锅高效得到n-混杂卟啉光动力治疗剂,上述两个底物的反应位点极为活泼,吲哚中亚胺的引入,使得吲哚3位电负性高,在有机弱酸催化下即可发生缩合反应,因此收率高。周环进行修饰引入卤素原子,由于卤原子的重原子效应,使得其单线态氧的产率达到0.5-0.9,在水溶液中,为均匀的分散状态,在光动力治疗过程中减少光损伤。
2、本发明合成了一类n-混杂卟啉光动力治疗剂,该化合物进一步增加了n-混杂卟啉的共轭体系,比单纯的n-混杂卟啉的共轭体系更大,因此,在近红外区有吸收,近红外光对皮肤光损伤小,治疗深度深,对减少病人痛苦。
附图说明
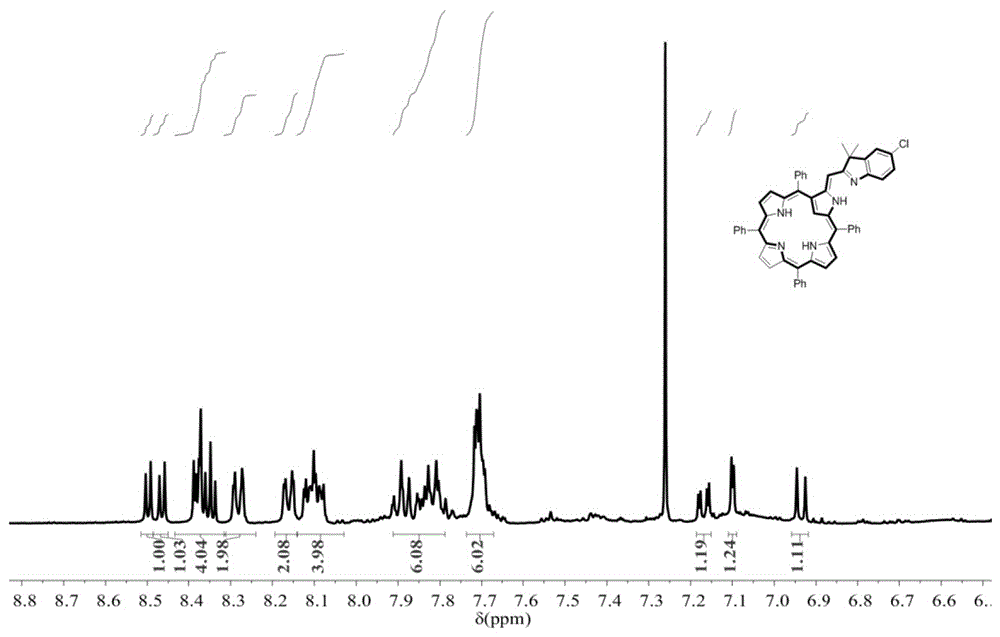
图1为实施例1得到的化合物在cdcl3中的核磁氢谱,x=cl。
图2为实施例1得到的化合物的高分辨质谱,x=cl。
图3为实施例1得到的化合物在thf中的紫外可见吸收光谱,x=cl。
图4为实施例1得到的化合物在thf中的荧光光谱,x=cl。
图5为实施例8得到的化合物在cdcl3中的核磁氢谱,x=br。
图6为实施例8得到的化合物的高分辨质谱,x=br。
图7为实施例8得到的化合物在thf中的紫外可见吸收光谱,x=br。
图8为实施例8得到的化合物在thf中的荧光光谱,x=br。
具体实施方式
下面结合实施例来进一步说明本发明,但本发明要求保护的范围并不局限于实施例表述的范围。
实施例1
取5-氯-2,3,3-三甲基吲哚0.23g(0.12mmol)和5,10,15,20-四苯基-n-混杂卟啉0.61g(0.10mmol)溶于甲苯中,然后加入冰乙酸1.2mg(0.02mmol),搅拌5分钟,于120℃回流0.5小时,反应结束后,旋干后过滤纯化柱层析得到紫色化合物,产率94%,该附图1-4说明能够一步合成得到所需的光动力治疗剂,所述得到的n-混杂卟啉共轭体系可以达到近红外吸收,且单线态氧产率高达0.8-0.9,解决了治疗剂的合成、光吸收范围和单线态氧产率低的难题。
实施例2
取5-氯-2,3,3-三甲基吲哚0.38g(0.2mmol)和5,10,15,20-四苯基-n-混杂卟啉0.61g(0.10mmol)溶于甲苯中,然后加入冰乙酸1.2mg(0.02mmol),搅拌5分钟,于120℃回流0.5小时,反应结束后,旋干后过滤纯化柱层析得到紫色化合物,产率92%。
实施例3
取5-氯-2,3,3-三甲基吲哚0.19g(0.1mmol)和5,10,15,20-四苯基-n-混杂卟啉0.61g(0.10mmol)溶于甲苯中,然后加入冰乙酸3.6mg(0.06mmol),搅拌5分钟,于120℃回流0.5小时,反应结束后,旋干后过滤纯化柱层析得到紫色化合物,产率87%。
实施例4
取5-氯-2,3,3-三甲基吲哚0.19g(0.1mmol)和5,10,15,20-四苯基-n-混杂卟啉0.61g(0.10mmol)溶于甲苯中,然后加入冰乙酸6.0mg(0.10mmol),搅拌5分钟,于120℃回流0.5小时,反应结束后,旋干后过滤纯化柱层析得到紫色化合物,产率85%。
实施例5
取5-氯-2,3,3-三甲基吲哚0.95g(0.5mmol)和5,10,15,20-四苯基-n-混杂卟啉0.61g(0.10mmol)溶于甲苯中,然后加入冰乙酸1.2mg(0.02mmol),搅拌5分钟,于120℃回流0.5小时,反应结束后,旋干后过滤纯化柱层析得到紫色化合物,产率93%。
实施例6
取5-氯-2,3,3-三甲基吲哚0.23g(0.12mmol)和5,10,15,20-四苯基-n-混杂卟啉0.61g(0.10mmol)溶于甲苯中,然后加入冰乙酸1.2mg(0.02mmol),搅拌5分钟,于120℃回流2小时,反应结束后,旋干后过滤纯化柱层析得到紫色化合物,产率86%。
实施例7
取5-氯-2,3,3-三甲基吲哚0.23g(0.12mmol)和5,10,15,20-四苯基-n-混杂卟啉0.61g(0.10mmol)溶于甲苯中,然后加入冰乙酸1.2mg(0.02mmol),搅拌5分钟,于120℃回流3小时,反应结束后,旋干后过滤纯化柱层析得到紫色化合物,产率78%。
实施例8
取5-溴-2,3,3-三甲基吲哚0.25g(0.12mmol)和5,10,15,20-四苯基-n-混杂卟啉0.61g(0.10mmol)溶于甲苯中,然后加入冰乙酸1.2mg(0.02mmol),搅拌5分钟,于120℃回流0.5小时,反应结束后,旋干后过滤纯化柱层析得到紫色化合物,产率97%,该附图5-8说明能够一步合成得到所需的光动力治疗剂,而且较单纯的n-混杂卟啉,其共轭体系更加可以达到近红外吸收,且单线态氧产率高达0.7-0.8,解决了治疗剂的合成、光吸收范围和单线态氧产率低的难题。
实施例9
取5-溴-2,3,3-三甲基吲哚0.48g(0.2mmol)和5,10,15,20-四苯基-n-混杂卟啉0.61g(0.10mmol)溶于甲苯中,然后加入冰乙酸1.2mg(0.02mmol),搅拌5分钟,于120℃回流0.5小时,反应结束后,旋干后过滤纯化柱层析得到紫色化合物,产率94%。
实施例10
称取0.081g实施例1的化合物,将其溶解在10ml四氢呋喃中,配制成10mmol/l的母液,然后取10μl母液稀释成10ml的的染料溶液(10μmol/l),利用紫外可见分光光度计和荧光分光光度计进行测试其紫外可见光光谱和荧光光谱,检测结果如图3、4所示,该化合物具有近红外光吸收,且有一定荧光发射,解决了治疗剂的光吸收范围问题,可以作为光动力治疗剂。
实施例11
称取0.09g实施例8的化合物,将其溶解在10ml四氢呋喃中,配制成10mmol/l的母液,然后取10μl母液稀释成10ml的的染料溶液(10μmol/l),利用紫外可见分光光度计和荧光分光光度计进行测试其紫外可见光光谱和荧光光谱,检测结果如图7、8所示,该化合物具有近红外光吸收,且有交换荧光发射效果,解决了治疗剂的光吸收范围问题,可以作为光动力治疗剂。
- 还没有人留言评论。精彩留言会获得点赞!