用于检测分泌型PD-L1拼接变体的RT-PCR引物、试剂盒及鉴定方法与流程
本发明涉及一种rt-pcr引物、试剂盒及鉴定方法,尤其涉及一种用于检测分泌型pd-l1拼接变体的rt-pcr引物、试剂盒及鉴定方法,特别是用于检测分泌型pd-l1拼接变体存在与肺癌肿瘤、多发性骨髓瘤和淋巴瘤上的rt-pcr引物、试剂盒及鉴定方法,属于生物医学检测技术领域。
背景技术:
肺癌是发病率和死亡率增长最快,对人群健康和生命威胁最大的恶性肿瘤之一,近50年来许多国家都报道肺癌的发病率和死亡率均明显增高,男性肺癌发病率和死亡率均占所有恶性肿瘤的第一位,女性发病率占第二位,死亡率占第二位。
多发性骨髓瘤(mm)是一种恶性浆细胞病,其肿瘤细胞起源于骨髓中的浆细胞,而浆细胞是b淋巴细胞发育到最终功能阶段的细胞,因此多发性骨髓瘤可以归到b淋巴细胞淋巴瘤的范围。目前who将其归为b细胞淋巴瘤的一种,称为浆细胞骨髓瘤/浆细胞瘤,其特征为骨髓浆细胞异常增生伴有单克隆免疫球蛋白或轻链(m蛋白)过度生成,极少数患者可以是不产生m蛋白的未分泌型mm。多发性骨髓瘤常伴有多发性溶骨性损害、高钙血症、贫血、肾脏损害,由于正常免疫球蛋白的生成受抑,因此容易出现各种细菌性感染,其发病率估计为2-3/10万,男女比例为1.6:1,大多患者年龄大于40岁。
淋巴瘤是起源于淋巴造血系统的恶性肿瘤,主要表现为无痛性淋巴结肿大,肝脾肿大,全身各组织器官均可受累,伴发热、盗汗、消瘦、瘙痒等全身症状。
根据瘤细胞分为非霍奇金淋巴瘤(nhl)和霍奇金淋巴瘤(hl)两类。病理学特征在霍奇金淋巴瘤为瘤组织内含有淋巴细胞、嗜酸性粒细胞、浆细胞和特异性的里-斯(reed-steinberg)细胞,hl按照病理类型分为结节性富含淋巴细胞型和经典型,后者包括淋巴细胞为主型、结节硬化型、混合细胞型和淋巴细胞消减型。nhl发病率远高于hl,是具有很强异质性的一组独立疾病的总和,病理上主要是分化程度不同的淋巴细胞、组织细胞或网状细胞,根据nhl的自然病程,可以归为三大临床类型,即高度侵袭性、侵袭性和惰性淋巴瘤。根据不同的淋巴细胞起源,可以分为b细胞、t细胞和nk细胞淋巴瘤。
根据临床症状、体征、影像学检查和组织病理学检查做出诊断,肺癌的早期诊断具有重要意义,只有在病变早期得到诊断和治疗,才能获得较好的疗效。
出现肺癌原发症状或转移症状者及时做胸部x线片检查或胸部ct检查,发现肺部有肿块阴影时,应首先考虑到肺癌的诊断,应作进一步检查,经过组织病理学检查明确诊断;某些慢性疾病(如风湿系统疾病、慢性结核感染、肾病、慢性肝病等)或淋巴瘤等可引起反应性浆细胞增多症和意义未明单克隆丙球蛋白血症(mgus),需要与mm进行鉴别诊断;此外,一些严重骨质疏松或低磷性骨病或转移癌需要与mm的骨质破坏鉴别;淋巴瘤临床表现多样,虽然可以有慢性、进行性、无痛性淋巴结肿大,但也可以表现为其他系统受累或全身症状,临床上怀疑淋巴瘤时,可以做淋巴结或其他受累组织或器官的病理切片检查(活检)以确诊。
pd-1(programmeddeath1)程序性死亡受体1,是一种重要的免疫抑制分子,为免疫球蛋白超家族,是一个268氨基酸残基的膜蛋白,其最初是从凋亡的小鼠t细胞杂交瘤2b4.11克隆出来,以pd-1为靶点的免疫调节对抗肿瘤、抗感染、抗自身免疫性疾病及器官移植存活等均有重要的意义。pd-l1(programmeddeath配体1)是膜蛋白,主要表达在树突状细胞和单核细胞上,它的受体是pd-1,表达在激活的t和b细胞、树突状和单核细胞上。当t细胞识别组织相关抗原,pd-l1与pd-1相互结合抑制t细胞的活化进一步导致免疫功能低下。许多肿瘤都能够表达pd-l1。现有技术中已发现分泌型pd-l1的拼接变体出现在肾癌和皮肤癌中,并与肿瘤的恶化有关联,但对于pd-l1的拼接变体是否存在于其他肿瘤细胞上却没有快速明确的鉴定方法。有鉴与此,发明检测出分泌型pdl1拼接变体存在于肺癌、多发性骨髓瘤和淋巴瘤上的方法是非常必要的。
技术实现要素:
为了解决上述技术问题,本发明提供了一种用于检测分泌型pd-l1拼接变体的rt-pcr引物、试剂盒及鉴定方法,其能够高效的检测出肺癌肿瘤、多发性骨髓瘤和淋巴瘤上的分泌型pd-l1拼接变体,从而为肺癌、多发性骨髓瘤和淋巴瘤的确诊提供一定的临床支撑。
本发明的技术方案是:
本发明公开了一种用于检测分泌型pd-l1拼接变体的rt-pcr引物,该引物由下列引物对组成:
针对肺癌肿瘤的引物对i:
正向引物:ccaaatgaaaggactcacttg;
反向引物:cgtctcctccaaatgtgtatctt;
针对多发性骨髓瘤的引物对ii:
正向引物:aagtcctgagtggagattagatc;
反向引物:cattctcccaagtgagtcc;和
针对淋巴瘤的引物对iii:
正向引物:accagcacactgagaatcaac;
反向引物:cacatccatcattctcccaag。
本发明还公开了一种含上述引物对的用于检测分泌型pd-l1拼接变体的试剂盒,该试剂盒试剂盒包括引物对和cdna模板,其中所述引物对由所述引物对i、引物对ii和引物对iii组成,其中cdna模板是由总rna模板通过反转录酶反转录而成,且所述总rna模板是通过总rna提取试剂盒从肿瘤细胞amo-1、jjn-3、mm.1s、h69、h526、su-dhl-4和su-dhl-6中提取所得。
其进一步的技术方案是:
所述试剂盒还包括双蒸水、pcr反应缓冲液、dntps和热启动高效taq酶。
其更进一步的技术方案是:
所述试剂盒包括2μm引物对i的正向引物1μl、2μm引物对i的反向引物1μl、2μm引物对ii的正向引物1μl、2μm引物对ii的反向引物1μl、2μm引物对iii的正向引物1μl、2μm引物对iii的反向引物1μl、经稀释20倍的cdna模板1μl、双蒸水4.8μl、10×pcr反应缓冲液1μl、2mmeach的dntps1μl、2.5u/μl的热启动高效taq酶0.1μl。
本发明还公开了一种基于上述试剂盒的用于检测分泌型pd-l1拼接变体的rt-pcr鉴定方法,该鉴定方法包括下述步骤:
s1:从患者肿瘤细胞样品中提取总rna,采用反转录酶将该总rna逆转录为cdna,以该cdna为模板利用所述引物对i、引物对ii和引物对iii进行pcr扩增实验,反应结束后进行琼脂糖凝胶电泳实验,得到待测样品结果图;
s2:根据待测样品结果图上显示的扩增出的dna片段大小进行待测样品结果判定。
其进一步的技术方案是:
所述pcr扩增实验中pcr反应程序为:依次进行95℃下预变性3min,94℃变性30s,55℃退火30s,72℃延伸45s,进行45次循环,72℃下延伸10min,最后在4℃下保持1min后结束。
所述琼脂糖凝胶电泳实验结束后,分析样品结果图时,判定依据为所述引物对i、引物对ii和引物对iii分别扩增出的dna片段大小;其中
针对肺癌肿瘤的pd-l1拼接变体pd-l1-1对应的引物对i扩增出的dna片段大小为103bp;
针对多发性骨髓瘤的pd-l1拼接变体pd-l1-3对应的引物对ii扩增出的dna片段大小为104bp;
针对淋巴瘤的pd-l1拼接变体pd-l1-9对应的引物对iii扩增出的dna片段大小为161bp。
本发明的有益技术效果是:本申请设计针对pd-l1的三个拼接变体的特异性引物对,以提取自各肿瘤细胞的总rna经逆转录所形成的cdna作为模板,进行pcr扩增实验,能够准确的检测出pd-l1三个拼接变体是否存在于肺癌肿瘤、多发性骨髓瘤和淋巴瘤上,使用试剂盒配合常规pcr反应,能够有效的缩短检测时间,提高检测鉴定的时间效率,能够为肺癌、多发性骨髓瘤和淋巴瘤的确诊提供一定的临床支撑。
附图说明
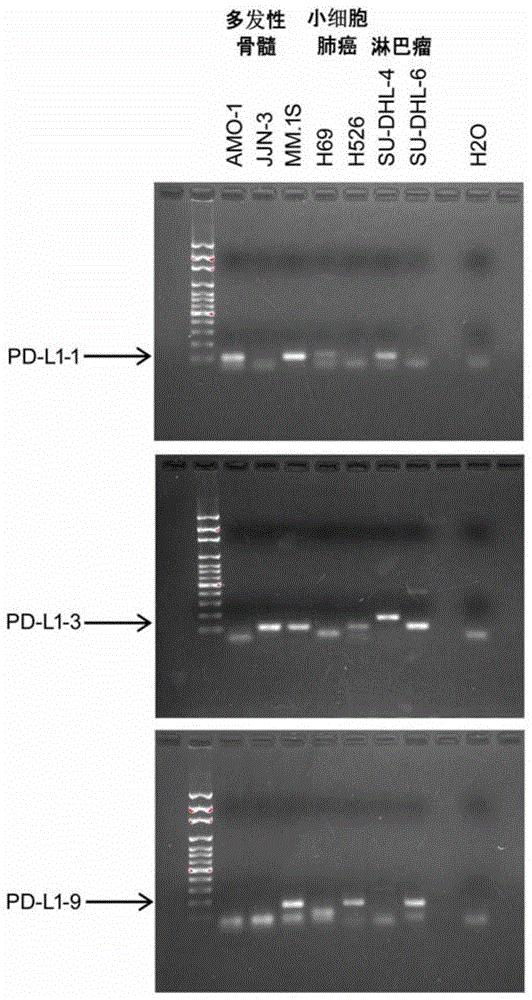
图1是本申请具体实施例待测样品进行pcr扩增所得琼脂糖凝胶电泳实验结果图。
具体实施方式
为了能够更清楚了解本发明的技术手段,并可依照说明书的内容予以实施,下面结合附图和实施例,对本发明的具体实施方式作进一步详细描述,以下实施例用于说明本发明,但不用来限制本发明的范围。
下述具体实施例所采用的材料和试剂:
试剂:总rna提取试剂盒rneasyminikit购自qiagen公司;反转录酶superscript购自lifetechnologies公司;热启动高效taq酶-blendtaq-plus-试剂盒为市售;dna标记物、琼脂糖、dna荧光染料均为市售产品;各引物序列均为合成。
各肿瘤细胞特异性引物的设计
利用美国国立生物技术信息中心(ncbi)核酸序列数据库,针对肺癌肿瘤细胞、多发性骨髓瘤肿瘤细胞和淋巴瘤肿瘤细胞上的分泌型pd-l1拼接变体进行比对分析,设计各特异性引物对。其中:
针对肺癌肿瘤的引物对i:
正向引物:ccaaatgaaaggactcacttg(seqidno.1);
反向引物:cgtctcctccaaatgtgtatctt(seqidno.2);
针对多发性骨髓瘤的引物对ii:
正向引物:aagtcctgagtggagattagatc(seqidno.3);
反向引物:cattctcccaagtgagtcc(seqidno.4);和
针对淋巴瘤的引物对iii:
正向引物:accagcacactgagaatcaac(seqidno.5);
反向引物:cacatccatcattctcccaag(seqidno.6)。
总rna的提取:
利用总rna提取试剂盒rneasyminikit(qiagen)从肿瘤细胞amo-1、jjn-3、mm.1s、h69、h526、su-dhl-4和su-dhl-6(上述肿瘤细胞均为)中提取出标准总rna;利用总rna提取试剂盒从患者肿瘤细胞样品中提取样品总rna。其中提取总rna的方法可参照总rna提取试剂盒操作说明和常规总rna提取操作进行即可,此为本领域技术人员常规操作,本具体实施例中不再赘述。
逆转录过程:
分别将上述标准总rna和样品总rna利用反转录酶superscript(lifetechnologies)逆转录成cdna,将所得逆转录产物cdna置于-20℃下进行保存,该逆转录过程所用实际和操作均为常规逆转录实验,为本领域技术人员所熟知的常规操作,本具体实施例中不再赘述。所得的标准cdna即为试剂盒中的cdna。
利用各引物对进行pcr实验:
分别以上述标准总rna逆转录所得标准cdna和样品总rna逆转录所得样品cdna为模板(经稀释20倍的cdna模板1μl),分别利用试剂盒中的引物对i、引物对ii和引物对iii以及其他试剂,即2μm引物对i的正向引物1μl、2μm引物对i的反向引物1μl、2μm引物对ii的正向引物1μl、2μm引物对ii的反向引物1μl、2μm引物对iii的正向引物1μl、2μm引物对iii的反向引物1μl、双蒸水4.8μl、10×pcr反应缓冲液1μl、2mmeach的dntps1μl、2.5u/μl的热启动高效taq酶0.1μl,进行pcr实验。
其中pcr实验的反应程序为:分别依次进行95℃下预变性3min,94℃变性30s,55℃退火30s,72℃延伸45s,进行45次循环,72℃下延伸10min,最后在4℃下保持1min后结束,得到标准pcr反应产物和样品pcr反应产物。
琼脂糖凝胶电泳实验:
将上述所得标准pcr反应产物和样品pcr反应产物分别进行1.5wt.%琼脂糖凝胶电泳,凝胶中加入gelred进行染色,然后120v电泳30分钟,当溴酚蓝条带迁移至凝胶边缘时停止电泳,则凝胶成像。凝胶成像结果参见图1所示。
结果判定:
分析样品结果图时,判定依据为所述引物对i、引物对ii和引物对iii分别扩增出的dna片段大小。其中
针对肺癌肿瘤的pd-l1拼接变体pd-l1-1对应的引物对i扩增出的dna片段大小为103bp;
针对多发性骨髓瘤的pd-l1拼接变体pd-l1-3对应的引物对ii扩增出的dna片段大小为104bp;
针对淋巴瘤的pd-l1拼接变体pd-l1-9对应的引物对iii扩增出的dna片段大小为161bp。
结合附图1中可以看出,pd-l1的三个拼接变体均能对应的出现在相应的肿瘤细胞中,因此该引物、试剂盒和检测方法能够高效的检测出肺癌肿瘤、多发性骨髓瘤和淋巴瘤上的分泌型pd-l1拼接变体,从而为肺癌、多发性骨髓瘤和淋巴瘤的确诊提供一定的临床支撑。
以上所述仅是本发明的优选实施方式,并不用于限制本发明,应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明技术原理的前提下,还可以做出若干改进和变型,这些改进和变型也应视为本发明的保护范围。
序列表
<110>锋宏生物医药科技(昆山)有限公司
<120>用于检测分泌型pd-l1拼接变体的rt-pcr引物、试剂盒及鉴定方法
<141>2019-06-20
<160>6
<170>siposequencelisting1.0
<210>1
<211>21
<212>dna
<213>人工序列()
<400>1
ccaaatgaaaggactcacttg21
<210>2
<211>23
<212>dna
<213>人工序列()
<400>2
cgtctcctccaaatgtgtatctt23
<210>3
<211>23
<212>dna
<213>人工序列()
<400>3
aagtcctgagtggagattagatc23
<210>4
<211>19
<212>dna
<213>人工序列()
<400>4
cattctcccaagtgagtcc19
<210>5
<211>21
<212>dna
<213>人工序列()
<400>5
accagcacactgagaatcaac21
<210>6
<211>21
<212>dna
<213>人工序列()
<400>6
cacatccatcattctcccaag21
- 还没有人留言评论。精彩留言会获得点赞!