SLIT2-IT1作为新型分子标志物及其定量检测方法和应用与流程
本发明涉及肿瘤分子生物学领域,具体涉及定量检测白血病患者细胞中slit2-it1作为分子标记物的方法及其用途。
背景技术:
随着环境污染的加重和化学制剂的滥用,肿瘤的发病率和死亡率正呈现出逐年增高的趋势,2011年调查揭示我国的肿瘤年发病率达250个/10万人口、死亡率达186个/10万人口;而白血病的死亡率在男性和女性肿瘤患者中分别占第8位和第10位,每年分别达3.46个/10万人口和2.45个/10万人口。包含白血病在内的肿瘤是致国人死亡的第二大原因,在我国已成为威胁公众健康的一个主要问题。
急性髓细胞性白血病(aml)是起源于髓系祖细胞的一类造血系统恶性疾病,其发病涉及细胞分化、增殖、凋亡等多方面的异常改变,非随机性染色体异常、癌基因和抑癌基因突变等在aml发生发展过程中起着重要作用。近二十年的研究结果表明在白血病发生过程中表观遗传学(epigenetics)改变是继染色体异常、基因组改变如杂合性缺失以及基因突变等之外发挥重要作用的又一病理机制。表观遗传学是指在不改变dna序列的前提下,通过某些机制引起可遗传的基因表达或细胞表型的变化,主要包括dna甲基化、组蛋白修饰和非编码rna等。近年来的研究表明,非编码rna与aml的发生、发展密切相关,可以作为有效的分子标志物应用于aml的辅助诊断、预后判断和疾病监测,并且可以为治疗提供更多的靶向分子。临床上期待发现更多特异而敏感的非编码rna,并将其运用于aml的临床诊疗。
slit2蛋白是高度保守的分泌型蛋白,主要通过与跨膜受体robo结合来介导其功能,且slit/robo途径可以通过调控细胞粘附、侵袭、凋亡、周期等参与肿瘤的发生发展和转移;slit2基因启动子cpg岛下游内含子中存在1个非编码rnaslit2-it1,但slit2-it1在白血病的表达状况及其意义亟待发现。
技术实现要素:
针对上述现有技术,本发明的目的在于针对白血病细胞中slit2-it1表达,通过定量pcr技术在急性髓系白血病及正常对照中检测slit2-it1的表达差异,以此作为急性髓系白血病患者的生物标志物,为临床上急性髓系白血病患者的早期发现及预后判断提供支持。
为了实现发明目的,本发明是通过以下技术方案实现的:
本发明的第一个目的是提供一种slit2-it1作为新型生物标记物在制备白血病辅助诊断或者预后判断试剂或药物的应用。
进一步地,所述slit2-it1包含所述如seqidno.1所示的核苷酸序列。
进一步地,所述的白血病辅助诊断或者预后判断试剂为实时定量pcr检测试剂。
进一步地,所述实时定量pcr检测试剂包括如seqidno.2所示的正向引物和如seqidno.3所示的反向引物;以及内参abl1引物,所述内参abl1引物的正向引物如seqidno.4所示,反向引物如seqidno.5所示。
进一步地,所述白血病为急性髓系白血病。
本发明的第二个目的是提供检测人slit2-it1表达的特异性引物,包括一条正向引物和一条反向引物,所述slit2-it1序列如seqidno.1所示,所述引物序列如seqidno.2-3所示。
进一步地,所述定量pcr扩增所使用的引物还包括内参abl1引物,其正向引物如seqidno.4所示,反向引物如seqidno.5所示。
本发明还提供一种用于白血病辅助诊断或者预后判断的试剂盒,所述试剂盒包括如前所述的引物。
本发明的另一目的是提出基于定量pcr检测slit2-it1表达水平的方法,包括如下步骤:
(1)提取人组织或细胞样本总rna并对提取的rna样本进行质量检测;
(2)将步骤(1)总rna逆转录成cdna;
(3)将步骤(2)的cdna分别使用seqidno.2和seqidno.3、seqidno.4和seqidno.5所示的引物对进行扩增,通过定量pcr分析所述样本中slit2-it1的表达水平,得到相关数据。
本发明还提供如前所述的引物、试剂盒在制备白血病辅助诊断或者预后判断用的试剂中的应用。
有益效果:本发明涉及用于检测白血病的基因标志物及其用途,还涉及使用该基因标志物对白血病进行检测的方法。与现有技术相比,本发明用于检测白血病的方法是基于基因标志物slit2-it1的水平,与其他临床指标相结合,为白血病的诊断、治疗与预后提供更准确的判断。本发明提供的引物组是发明人付出创造性劳动进行优化和筛选获得的,其能够高灵敏高特异性的扩增靶基因。
附图说明
为了更清楚地说明本发明实施例的技术方案,下面将对实施例中所需要使用的附图作简单地介绍,应当理解,以下附图仅示出了本发明的某些实施例,因此不应被看作是对范围的限定,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他相关的附图。
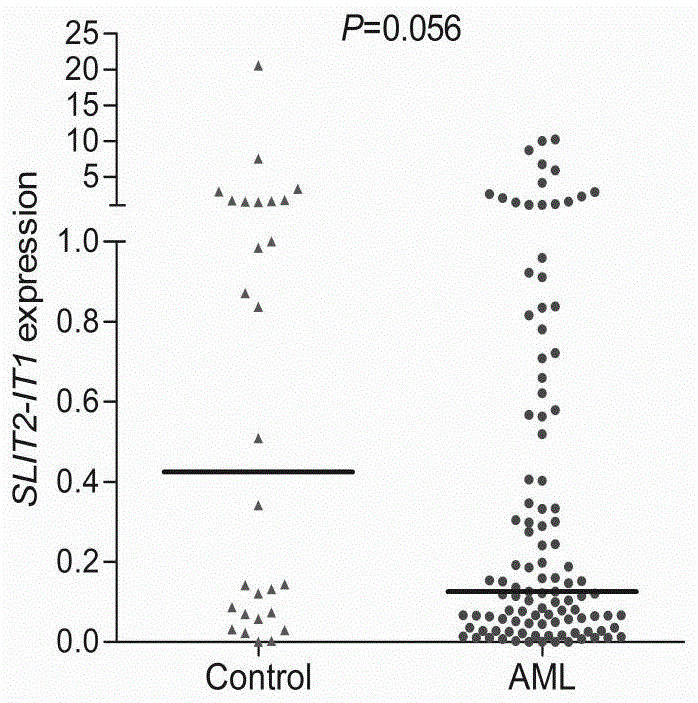
图1为定量pcr检测发现slit2-it1在初诊急性髓系白血病患者中表达下调的示意图。
图2为定量pcr检测发现slit2-it1在缓解后急性髓系白血病患者中表达上调的示意图。
a:对照组、初发aml患者及完全缓解患者中slit2-it1表达;b:6例配对的aml病人初发期与完全缓解期slit2-it1表达。
具体实施方式
下面利用展示实例的方式来具体说明本发明的实施例,应该理解,这些实施例仅用于说明目的,而不用于限制本发明范围。对本发明公开的内容可以同时从材料、方法和反应条件进行改进,所有这些改进,均应落入本发明的精神和范围之内。
实施例1:建立基于定量pcr检测slit2-it1表达水平的方法
(1)总rna提取:
①骨髓单个核细胞分离:将获取的骨髓标本先后加5ml淋巴细胞分离液和红细胞裂解液,上下颠倒混匀,1000×rpm离心5min,弃上清;
②在上述沉淀中加1mltrizol,充分吹打混匀至水样;
③加200μl三氯甲烷,漩涡充分振荡30sec,室温静置5min,12000×rpm离心10min;
④上清加入干净1.5mlep管,同时加入600μl异丙醇,盖紧盖子,上下颠倒混匀50次,室温静置10min后,12000×rpm离心10min,小心弃去上清,ep管底白色沉淀即为rna;
⑤加入1ml70%乙醇,轻弹或颠倒混匀漂洗沉淀,12000×rpm离心5min,小心弃上清;
⑥再加入1ml100%乙醇,轻弹或颠倒混匀漂洗沉淀,12000×rpm离心10min,小心弃上清,并于洁净纸上扣干;
⑦将沉淀rna置于37℃金属浴干燥至沉淀可轻弹起,而后加入适量(10-20μl)depc,于冰上溶解rna;
⑧混匀后取2μlrna,应用nanodrop分光光度计检测所提取样本rna的浓度、纯度,并调整至均一浓度。
(2)cdna逆转录:
①取0.2mlep管,分别依次加入4μl六随机引物、14μldepc水和4μgrna,置于普通pcr仪(37℃,5min);
②将8μl5×buffer、3μldepc水、4μldntp和1μlribolockrnaseinhibitor(thermoscientifictm)加入到上步ep管中,置于普通pcr仪(25℃5min);
③将2μlrevertaidreversetranscriptase(thermoscientifictm)继续加入上步产物中,继续反应(60℃60min),反应结束后将产物cdna保存于-20℃备用。
(3)实时定量pcr检测:
以abl1作为内参,slit2-it1及abl1反应体系为:2×aceqqpcrsybrgreenmastermix(vazyme)10.0μl,表达上游和下游引物各0.8μl,50×roxreferencedye0.4μl,ddh2o6.0μl,2.0μlcdna模板,总反应体积为20μl。特异性检测引物序列见表1。
表1特异性检测引物
slit2-it1反应条件:预变性(95℃、5min),变性(95℃、10sec),退火(58℃、30sec),延伸(72℃、30sec),收集荧光(75℃,30sec),循环数为40循环;abl反应条件:预变性(95℃、5min),变性(95℃、10sec),退火(60℃、30sec),延伸(72℃、30sec),收集荧光(75℃,30sec),循环数为40循环。于abi7300实时荧光定量pcr仪完成检测。
(4)结果定量分析:
slit2-it1基因表达水平通过2-δδct进行计算,具体的计算公式如下:nslit2-it1=(eslit2-it1)△ctslit2-it1(对照-实验)÷(eabl1)△ctabl1(对照-实验)。每个平行实验重复3次。
实施例2:验证正常和急性髓系白血病患者中slit2-it1表达差异
取28例正常人样本和108例急性髓系白血病样本作为分析样本,每一例样本均采用实施例1相同的处理方法进行处理,分别计算每例样本中slit2-it1表达水平。结果如图1所示,相较于正常样本,急性髓系白血病患者样本slit2-it1表达水平明显降低。
实施例3:验证初诊和缓解后急性髓系白血病中slit2-it1表达改变
取72例获得完全缓解的aml样本、6例初诊及缓解后的配对aml样本作为分析样本,每一例样本均采用实施例1相同的处理方法进行处理,分别计算每例样本中slit2-it1表达水平。结果如图2所示,相较于初诊样本,完全缓解后aml患者样本slit2-it1表达水平明显增高。
因此,本发明建立的基于定量pcr检测slit2-it1表达水平的方法,可用于aml及其他肿瘤的辅助诊断、预后判断和疾病监测,具有良好的应用前景。
尽管本发明的实施方案已公开如上,但其并不仅仅限于说明书和实施方式中所列运用。它完全可以被适用于各种适合本发明的领域。对于熟悉本领域的人员而言,可容易地实现另外的修改。因此在不背离权利要求及等同范围所限定的一般概念下,本发明并不限于特定的细节和这里示出与描述的图例。
序列表
<110>镇江市第一人民医院
<120>slit2-it1作为新型分子标志物及其定量检测方法和应用
<160>5
<170>siposequencelisting1.0
<210>1
<211>628
<212>dna
<213>homosapiens
<400>1
agcctattgctcctaggcttcaaacccatacagcatggcactatatggaatactgtaggc60
aattttaacacaatgaatcctgacccttgggaatgggatctggagccagtgggaagcatt120
ctccgaatatgataatgtggttatcttctgacgagtgctggcattatcacttgttgctaa180
aaaaacaccaggcttgttctgaggttcacccgactccactgcatgtattacgtgcatgtg240
taccttggaatggaaaatacatgactaagccctgagacaactctgcactgtatcctgcta300
ttcttccaactgcaggacctcatggagcgagagatccaaacctttctgaagtactttacc360
ttctacctttttcatgctactcaggattgaatcaattggaagccaacaaagccattctgt420
gttactgtgcctcctgactgtcagcacgctgcactgtgcatttagataattctgccagaa480
ggcatttttataaaaacagctttcaaaatctattcttgaaaagacatttgtatactcatt540
atgccattctatcatttatccatagggagttctgtaaataaaacactgaggtctaatact600
aaaaaaaaaaaaaaaaaaaaaaaaaaaa628
<210>2
<211>19
<212>dna
<213>homosapiens
<400>2
gttactgtgcctcctgact19
<210>3
<211>20
<212>dna
<213>homosapiens
<400>3
aactccctatggataaatga20
<210>4
<211>23
<212>dna
<213>homosapiens
<400>4
tcctccagctgttatctggaaga23
<210>5
<211>18
<212>dna
<213>homosapiens
<400>5
tccaacgagcggcttcac18
- 还没有人留言评论。精彩留言会获得点赞!