使用增强的iPSC衍生效应细胞的免疫疗法的制作方法
相关申请
本申请要求于2018年12月2日提交的美国临时申请序列号62/774,278的优先权,所述美国临时申请据此通过引用以其整体并入。
序列表
随附的序列表中的材料据此通过引用以其整体并入。名称为“056932-516001wo_sl_st25”的随附的序列表文件于2019年11月25日创建并且大小为41,518字节。
本公开与现成的免疫细胞产物领域广泛地相关。更具体地说,本公开与研发能够体内递送治疗相关特性的多功能效应细胞的策略相关。根据本公开研发的细胞产物解决了患者来源的细胞疗法的关键限制。
背景技术:
过继性细胞疗法领域目前的重点是使用患者来源的细胞和供体来源的细胞,这使得实现癌症免疫疗法的持续制造以及向所有可能受益的患者递送疗法尤其困难。还需要改善过继转移的淋巴细胞的功效和存留,以促进良好的患者结果。淋巴细胞(例如t细胞和自然杀手(nk)细胞)是有效的抗肿瘤效应子,在先天性和适应性免疫中起重要作用。然而,将这些免疫细胞用于过继性细胞疗法仍然具有挑战性,并且尚未满足改善的需求。因此,在过继性免疫疗法中,仍有大量机会来利用t细胞和nk细胞或其它淋巴细胞的全部潜能。
技术实现要素:
需要在功能上改善的效应细胞,以在以下范围内解决问题:从反应速率、细胞耗竭、输血细胞损失(存活和/或存留)、肿瘤经由标靶损失或谱系转换逃逸、肿瘤靶向精确度、脱靶毒性、肿瘤外效应到针对实体瘤的功效,即肿瘤微环境和相关免疫抑制、募集、运输和浸润。
本发明的一个目的是用以产生由单一细胞衍生诱导性多能干细胞(inducedpluripotentstemcell;ipsc)克隆系分化的衍生非多能细胞的方法和组合物,所述ipsc系包含在其基因组中的一种或几种基因修饰。所述一种或几种基因修饰包括dna插入、缺失和取代,并且所述修饰在分化、扩增、传代和/或移植后在随后衍生细胞中保留并且保持功能性。
本申请的ipsc衍生非多能细胞包括但不限于cd34细胞、生血内皮细胞、hsc(造血干细胞和祖细胞)、造血多能祖细胞、t细胞祖细胞、nk细胞祖细胞、t细胞、nkt细胞、nk细胞和b细胞。本申请的ipsc衍生非多能细胞通过由包含相同基因修饰的ipsc分化在其基因组中包含一种或多种基因修饰。用于获得基因工程化衍生细胞的工程化克隆ipsc分化策略要求ipsc在定向分化中的发育潜能不会受到ipsc中的工程化模式的不利影响,并且也要求工程化模式如预期一般在衍生细胞中起作用。此外,这一策略克服工程化原代淋巴细胞(例如从外周血获得的t细胞或nk细胞)的现有障碍,因此细胞难以工程化,并且对这类细胞进行工程化通常缺乏再现性和均匀性,使得细胞展现伴随高细胞死亡和低细胞扩增的不良细胞存留。此外,这一策略避免产生使用起始时是异源的原代细胞源以其它方式获得的异源效应细胞群。
本发明的一些方面提供使用包含(i)、(ii)或(iii)的方法获得的基因组工程化ipsc,分别反映了在重编程过程之后、同时和之前的基因组工程化策略:
(i):按任何次序利用(i)和(ii)中的一者或两者对ipsc进行基因工程化:(i)将一个或多个构建体引入ipsc中以允许在所选位点进行靶向整合;(ii)(a)使用一种或多种能够进行所选位点识别的核酸内切酶在所选位点将一个或多个双链断裂引入ipsc中;和(b)培养步骤(i)(ii)(a)中的ipsc以允许进行内源性dna修复,从而在所选位点产生靶向插入/缺失;进而获得能够分化成部分或完全分化细胞的基因组工程化ipsc。
(ii):对重编程非多能细胞进行基因工程化,以获得基因组工程化ipsc,所述基因工程化包含:(i)使非多能细胞与一种或多种重编程因子和任选的小分子组合物接触,以启动非多能细胞重编程,所述小分子组合物包含tgfβ受体/alk抑制剂、mek抑制剂、gsk3抑制剂和/或rock抑制剂;和(ii)按任何次序将(a)和(b)中的一者或两者引入步骤(ii)
(i)中的重编程非多能细胞中:(a)一个或多个构建体,以允许在所选位点处进行靶向整合;(b)使用至少一种能够进行所选位点识别的核酸内切酶在所选位点的一个或多个双链断裂,然后培养步骤(ii)(ii)(b)中的细胞以允许进行内源性dna修复,从而在所选位点产生靶向插入/缺失;因此所获基因组工程化ipsc包含至少一种功能性靶向基因组编辑,并且所述基因组工程化ipsc能够分化成部分或完全分化细胞。
(iii):对重编程的非多能细胞进行基因工程化以获得基因组工程化ipsc,所述基因工程化包含(i)和(ii):(i)按任何次序将(a)和(b)中的一者或两者引入非多能细胞中:(a)一个或多个构建体,以允许在一个或多个所选位点处进行靶向整合;(b)使用至少一种能够进行所选位点识别的核酸内切酶在所选位点的一个或多个双链断裂,其中培养步骤(iii)(i)(b)中的细胞以允许进行内源性dna修复,从而在所选位点产生靶向插入/缺失;和(ii)使步骤(iii)(i)中的细胞与一种或多种重编程因子和任选的小分子组合物接触,以获得基因组工程化ipsc,所述小分子组合物包含tgfβ受体/alk抑制剂、mek抑制剂、gsk3抑制剂和/或rock抑制剂,所述ipsc在所选位点包含靶向编辑;进而获得基因组工程化ipsc,其包含至少一种功能性靶向基因组编辑,并且所述基因组工程化ipsc能够分化成部分分化细胞或完全分化细胞。
在上述方法的一个实施例中,在一个或多个所选位点处的至少一种靶向基因组编辑包含一种或多种外源性多核苷酸的插入,所述外源性多核苷酸编码安全开关蛋白质、靶向模式、受体、信号传导分子、转录因子、医药学活性蛋白质和肽、药物标靶候选物或促进基因组工程化ipsc或其衍生细胞移植、运输、归巢、活力、自我更新、存留和/或存活的蛋白质。在一些实施例中,用于插入的外源性多核苷酸与以下可操作地连接:(1)一种或多种外源性启动子,所述一种或多种外源性启动子包括cmv、ef1α、pgk、cag、ubc或其它组成型、诱导性、时间特异性、组织特异性或细胞类型特异性启动子;或者(2)所选位点中包括的一种或多种内源性启动子,所述所选位点包括aavs1、ccr5、rosa26、胶原蛋白、htrp、h11、β-2微球蛋白、gapdh、tcr或runx1或包括以下的其它所选基因座:tap1、tap2、tap相关蛋白、nlrc5、ciita、rfxank、ciita、rfx5、rfxap、tcrα或β恒定区、nkg2a、nkg2d、cd38、cis、cbl-b、socs2、pd1、ctla4、lag3、tim3或tigit。在一些实施例中,使用上述方法产生的基因组工程化ipsc包括一种或多种不同的外源性多核苷酸,所述外源性多核苷酸编码包括胱天蛋白酶、胸苷激酶、胞嘧啶脱氨酶、经过修饰的egfr或b细胞cd20的蛋白质,其中当基因组工程化ipsc包括两种或更多种自杀基因时,所述自杀基因整合在不同的安全港基因座中,所述安全港基因座包括aavs1、ccr5、rosa26、胶原蛋白、htrp、h11、β-2微球蛋白、gapdh、runx1、tap1、tap2、tap相关蛋白、nlrc5、ciita、rfxank、ciita、rfx5、rfxap、tcrα或β恒定区、nkg2a、nkg2d、cd38、cis、cbl-b、socs2、pd1、ctla4、lag3、tim3、tigit或染色体6p21区中的任何基因。在一个实施例中,外源性多核苷酸编码il2、il4、il6、il7、il9、il10、il11、il12、il15、il18、il21和/或其相应受体的部分或全部肽。在一些实施例中,由外源性多核苷酸编码的il2、il4、il6、il7、il9、il10、il11、il12、il15、il18、il21和/或其相应受体的部分或全部肽呈融合蛋白形式。
在一些其它实施例中,使用本文所提供的方法产生的基因组工程化ipsc包含位于一种或多种与以下相关的内源性基因处的插入/缺失:靶向模式、受体、信号传导分子、转录因子、药物标靶候选物、免疫反应调控和调节或抑制ipsc或其衍生细胞移植、运输、归巢、活力、自我更新、存留和/或存活的蛋白质。在一些实施例中,用于破坏的内源性基因包括以下中的至少一种:b2m、tap1、tap2、tap相关蛋白、nlrc5、ciita、rfxank、ciita、rfx5、rfxap、tcrα或β恒定区、nkg2a、nkg2d、cd38、cis、cbl-b、socs2、pd1、ctla4、lag3、tim3、tigit和染色体6p21区中的任何基因中的至少一种的缺失或减少的表达。
在又一些其它实施例中,使用本文所提供的方法产生的基因组工程化ipsc包含位于aavs1基因座的编码胱天蛋白酶的外源性多核苷酸和位于h11基因座的编码胸苷激酶的外源性多核苷酸。
在另外一些其它实施例中,方法(i)、(ii)和/或(iii)进一步包含:使基因组工程化ipsc与包含mek抑制剂、gsk3抑制剂和rock抑制剂的小分子组合物接触,以维持基因组工程化ipsc的多能性。在一个实施例中,包含至少一种靶向基因组编辑的所获得的基因组工程化ipsc具有功能性、能有效分化并且能够分化成包括相同功能性基因组编辑的非多能细胞。
本发明还提供以下内容。
本发明的一方面提供了一种细胞或细胞群体,其中所述细胞是诱导性多能细胞(ipsc)、克隆ipsc或ips细胞系细胞;或者通过分化上文所述ips细胞获得的衍生细胞,并且其中所述细胞包括编码nkg2c的外源性多核苷酸,以及任选地编码cd94的外源性多核苷酸和编码dap12的外源性多核苷酸中的一者或两者。
通过分化包括所述一种或多种外源性多核苷酸的所述ips细胞获得的衍生细胞的各个实施例包含造血细胞,包含但不限于衍生cd34细胞、衍生造血干细胞和祖细胞、衍生造血多能祖细胞、衍生t细胞祖细胞、衍生nk细胞祖细胞、衍生t细胞、衍生nkt细胞、衍生nk细胞或衍生b细胞,其中与衍生细胞的从外周血、脐带血或任何其它供体组织中获得的天然对应细胞相比,所述衍生细胞包括更长的端粒。
在包括所述一个或多个外源性多核苷酸的细胞或细胞群体的一个实施例中,所述细胞进一步包括以下中的一种或多种:(i)bike或trike;(ii)b2m无效或低;(iii)ciita无效或低;(iv)hla-g或不可切割的hla-g的引入的表达;(v)嵌合抗原受体(car);(vi)细胞表面表达的外源性细胞因子或其受体的部分或全部肽;(vii)表1中列出的基因型中的至少一种;(viii)b2m、tap1、tap2、tap相关蛋白、nlrc5、ciita、rfxank、ciita、rfx5、rfxap、tcrα或β恒定区、nkg2a、nkg2d、cd38、cis、cbl-b、socs2、pd1、ctla4、lag3、tim3、tigit或染色体6p21区中的任何基因中的至少一种的缺失或减少的表达;并且(ix)hla-e、41bbl、cd3、cd4、cd8、cd16、cd47、cd113、cd131、cd137、cd80、pdl1、a2ar、fc受体、衔接子或用于与双特异性或多特异性或通用衔接子偶联的表面触发性受体中的至少一种的引入或增加的表达。
在细胞或细胞群体的一些实施例中,所述细胞是衍生nk细胞或衍生t细胞,并且与所述细胞的从外周血、脐带血或任何其它供体组织中获得的天然对应细胞相比具有以下特性中的至少一个特性:(i)改善的肿瘤靶向特异性,(ii)改善的持久性和/或存活率,(iii)对天然免疫细胞的抗性增加,(iv)细胞毒性增加,(v)改善的肿瘤渗透性,(vi)增强或获取的adcc,(vii)将旁观者免疫细胞迁移到肿瘤部位和/或激活或募集所述旁观者免疫细胞的能力增强,(viii)降低肿瘤免疫抑制的能力增强;以及(ix)挽救肿瘤抗原逃逸的能力提高。
在包括bike或trike的细胞或细胞群体的一些实施例中,其中所述bike或所述trike包括用于cd16、cd64或nkg2c结合的第一组分以及用于cd30、cd33、bcma或epcam结合的第二组分。
在trike的细胞或细胞群体的一些实施例中,trike包括用于nkg2c结合的第一组分、用于肿瘤抗原结合的第二组分以及位于所述第一组分与所述第二组分之间的il15接头;其中所述肿瘤抗原是:(i)以下中的至少一种:adgre2、碳酸酐酶ix(calx)、ccri、ccr4、癌胚抗原(cea)、cd3、cd5、cd7、cd8、cd10、cd20、cd22、cd30、cd33、cd34、cd38、cd41、cd44、cd44v6、cd49f、cd56、cd70、cd74、cd99、cd123、cd133、cd138、cds、clec12a、巨细胞病毒(cmv)感染的细胞的抗原、上皮糖蛋白2(egp2)、上皮糖蛋白-40(egp-40)、上皮细胞粘附分子(epcam)、egfrviii、受体酪氨酸-蛋白激酶erb-b2,3,4、egfir、egfr-viii、erbb叶酸结合性蛋白(fbp)、胎儿型乙酰胆碱受体(achr)、叶酸受体a、神经节苷脂g2(gd2)、神经节苷脂g3(gd3)、人表皮生长因子受体2(her-2)、人端粒酶逆转录酶(htert)、icam-1、整合素b7、白细胞介素-13受体亚基α-2(il-13rα2)、κ-轻链、激酶插入结构域受体(kdr)、lewisa(ca19.9)、lewisy(ley)、l1细胞粘附分子(l1-cam)、lilrb2、黑色素瘤抗原家族a1(mage-a1)、mica/b、粘蛋白1(muc-1)、粘蛋白16(muc-16)、间皮素(msln)、nkcsi、nkg2d配体、c-met、癌症-睾丸抗原ny-eso-1、癌胚抗原(h5t4)、prame、前列腺干细胞抗原(psca)、prame前列腺特异性膜抗原(psma)、肿瘤相关糖蛋白72(tag-72)、tim-3、trbci、trbc2、血管内皮生长因子r2(vegf-r2)、威尔姆斯肿瘤蛋白(wilmstumorprotein,wt-1)和病原体抗原。在一个实施例中,trike包括用于nkg2c结合的第一组分和位于所述第一组分与所述第二组分之间的il15接头,所述第二组分与肿瘤抗原cd33结合。
在包括高亲和力不可切割的cd16(hncd16)或其变体的细胞或细胞群体的一些实施例中,所述cd16或其变体包括以下中的至少一种:(a)cd16的胞外结构域中的f176v和s197p;(b)源自cd64的全部或部分胞外结构域;(c)非天然(或非cd16)跨膜结构域;(d)非天然(或非cd16)胞内结构域;(e)非天然(或非cd16)信号传导结构域;(f)非天然刺激性结构域;以及(g)并非源自cd16并且源自相同或不同多肽的跨膜结构域、信号传导结构域和刺激性结构域。
在包括高亲和力不可切割的cd16(hncd16)或其变体的细胞或细胞群体的一些实施例中,所述cd16变体的所述非天然跨膜结构域源自cd3d、cd3e、cd3g、cd3ζ、cd4、cd8、cd8a、cd8b、cd27、cd28、cd40、cd84、cd166、4-1bb、ox40、icos、icam-1、ctla-4、pd-1、lag-3、2b4、btla、cd16、il7、il12、il15、kir2dl4、kir2ds1、nkp30、nkp44、nkp46、nkg2c、nkg2d或t细胞受体(tcr)多肽。在包括高亲和力不可切割的cd16(hncd16)或其变体的细胞或细胞群体的一些实施例中,所述cd16变体的所述非天然刺激性结构域源自cd27、cd28、4-1bb、ox40、icos、pd-1、lag-3、2b4、btla、dap10、dap12、ctla-4或nkg2d多肽。在一些实施例中,所述cd16或其变体的非天然信号传导结构域源自cd3ζ、2b4、dap10、dap12、dnam1、cd137(41bb)、il21、il7、il12、il15、nkp30、nkp44、nkp46、nkg2c或nkg2d多肽。在又一些其它实施例中,所述cd16或其变体包括源自nkg2d的非天然跨膜结构域、源自2b4的非天然刺激性结构域和源自cd3ζ的非天然信号传导结构域。
在所述细胞或细胞群体的一些实施例中,所述细胞进一步包括car,所述car可以具有以下特性中的一个或多个特性:(i)t细胞特异性或nk细胞特异性的;(ii)双特异性抗原结合性car;(iii)可切换的car;(iv)二聚化car;(v)分开的car;(vi)多链car;(vii)诱导性car;(viii)与另一个car共表达;(ix)任选地在单独构建体中或在双顺反子构建体中,与细胞表面表达的外源性细胞因子或其受体的部分或全部肽共表达;(xi)任选地在单独构建体中或在双顺反子构建体中,与检查点抑制剂共表达;(xii)对cd19或bcma具有特异性;和/或(xiii)对以下中的任何一种具有特异性:adgre2、碳酸酐酶ix(calx)、ccri、ccr4、癌胚抗原(cea)、cd3、cd5、cd7、cd8、cd10、cd20、cd22、cd30、cd33、cd34、cd38、cd41、cd44、cd44v6、cd49f、cd56、cd70、cd74、cd99、cd123、cd133、cd138、cds、clec12a、巨细胞病毒(cmv)感染的细胞的抗原、上皮糖蛋白2(egp2)、上皮糖蛋白-40(egp-40)、上皮细胞粘附分子(epcam)、egfrviii、受体酪氨酸-蛋白激酶erb-b2,3,4、egfir、egfr-viii、erbb叶酸结合性蛋白(fbp)、胎儿型乙酰胆碱受体(achr)、叶酸受体a、神经节苷脂g2(gd2)、神经节苷脂g3(gd3)、人表皮生长因子受体2(her-2)、人端粒酶逆转录酶(htert)、icam-1、整合素b7、白细胞介素-13受体亚基α-2(il-13rα2)、κ-轻链、激酶插入结构域受体(kdr)、lewisa(ca19.9)、lewisy(ley)、l1细胞粘附分子(l1-cam)、lilrb2、黑色素瘤抗原家族a1(mage-a1)、mica/b、粘蛋白1(muc-1)、粘蛋白16(muc-16)、间皮素(msln)、nkcsi、nkg2d配体、c-met、癌症-睾丸抗原ny-eso-1、癌胚抗原(h5t4)、prame、前列腺干细胞抗原(psca)、prame前列腺特异性膜抗原(psma)、肿瘤相关糖蛋白72(tag-72)、tim-3、trbci、trbc2、血管内皮生长因子r2(vegf-r2)、威尔姆斯肿瘤蛋白(wt-1)和病原体抗原。在上述car的一些实施例中,所述car可以任选地插入在tcr恒定区处和/或由tcr的内源性启动子驱动,其中所述tcr可以或可以不通过car插入而被敲除。
在细胞或细胞群体的一些实施例中,所述细胞进一步包括细胞表面表达的外源性细胞因子或其受体的部分或全部肽。在一些实施例中,所述外源性细胞因子或其受体包括:(a)il2、il4、il6、il7、il9、il10、il11、il12、il15、il18、il21和其相应受体中的至少一种;或(b)以下中的至少一种:(i)通过使用自切割肽进行il15和il15rα的共表达;(ii)il15和il15rα的融合蛋白;(iii)il15rα的胞内结构域截短的il15/il15rα融合蛋白;(iv)il15和il15rα的结合膜的sushi结构域的融合蛋白;(v)il15和il15rβ的融合蛋白;(vi)il15和共同受体γc的融合蛋白,其中所述共同受体γc是天然的或经过修饰的;以及(vii)il15rβ的同源二聚体;其中(i)-(vii)中的任一项都可以在单独构建体中或在双顺反子构建体中与car共表达。在一些其它实施例中,所述外源性细胞因子或其受体是瞬时表达的。
在细胞或细胞群体的一些实施例中,其中所述细胞是衍生nk,并且衍生nk细胞能够募集t细胞和/或将所述t细胞迁移到肿瘤部位。在细胞或细胞群体的一些实施例中,其中所述细胞是衍生nk细胞或衍生t细胞;其中在存在一种或多种检查点抑制剂的情况下,所述细胞能够降低肿瘤免疫抑制。
在细胞或细胞群体的一些实施例中,所述细胞是在存在检查点抑制剂的情况下,或者所述细胞进一步包括与检查点抑制剂共表达的car,所述检查点抑制剂是针对一种或多种检查点分子的拮抗剂,所述一种或多种检查点分子包括pd-1、pdl-1、tim-3、tigit、lag-3、ctla-4、2b4、4-1bb、4-1bbl、a2ar、bate、btla、cd39、cd47、cd73、cd94、cd96、cd160、cd200、cd200r、cd274、ceacam1、csf-1r、foxpl、garp、hvem、ido、edo、tdo、lair-1、mica/b、nr4a2、mafb、oct-2、rara(视黄酸受体α)、tlr3、vista、nkg2a/hla-e或抑制性kir。在一些其它实施例中,所述检查点抑制剂包括:(a)以下中的一种或多种:阿特珠单抗(atezolizumab)、阿维鲁单抗(avelumab)、度伐单抗(durvalumab)、伊匹单抗(ipilimumab)、iph4102、iph43、iph33、利瑞木单抗(lirimumab)、莫纳利珠单抗(monalizumab)、纳武单抗(nivolumab)、帕博利珠单抗(pembrolizumab)和其衍生物或功能等效物;或(b)阿特珠单抗、纳武单抗和帕博利珠单抗中的至少一种。
在包括编码nkg2c的外源性多核苷酸,以及任选地编码cd94的外源性多核苷酸和编码dap12的外源性多核苷酸中的一者或两者和另外的外源性多核苷酸的细胞或细胞群体的各个实施例中,所述一个或多个外源性多核苷酸整合在至少一个所选基因座或至少两个不同的所选基因座中。在一个实施例中,所述所选基因座包括以下中的至少一种:aavs1、ccr5、rosa26、胶原蛋白、htrp、h11、gapdh、runx1、b2m、tap1、tap2、tap相关蛋白、nlrc5、ciita、rfxank、ciita、rfx5、rfxap、tcrα或β恒定区、nkg2a、nkg2d、cd38、cis、cbl-b、socs2、pd1、ctla4、lag3、tim3、tigit或染色体6p21区中的任何基因。在一个实施例中,所述所选基因座是tcrα的恒定区。
本申请的另一方面提供了一种组合物,所述组合物包括如本文所述的细胞或其群体。在组合物的一些实施例中,所述细胞或其群体包括如本文提供的ipsc的衍生细胞。在包括如本文提供的ipsc的衍生细胞的组合物的一些其它实施例中,所述组合物用于治疗用途,并且可以进一步包括一种或多种治疗剂。在一些实施例中,所述治疗剂包括肽、细胞因子、检查点抑制剂、丝裂原、生长因子、小rna、dsrna(双链rna)、单核血细胞、饲养细胞、饲养细胞组分或其置换因子、包括一种或多种所关注多核酸的载体、抗体、化学治疗剂或放射性部分或免疫调节药物(imid)。
在一些实施例中,在包括如本文提供的ipsc的衍生细胞的治疗组合物中的治疗剂是检查点抑制剂,并且所述检查点抑制剂可以是针对一种或多种检查点分子的拮抗剂,所述一种或多种检查点分子包括pd-1、pdl-1、tim-3、tigit、lag-3、ctla-4、2b4、4-1bb、4-1bbl、a2ar、bate、btla、cd39、cd47、cd73、cd94、cd96、cd160、cd200、cd200r、cd274、ceacam1、csf-1r、foxpl、garp、hvem、ido、edo、tdo、lair-1、mica/b、nr4a2、mafb、oct-2、rara(视黄酸受体α)、tlr3、vista、nkg2a/hla-e或抑制性kir。在一些其它实施例中,所述检查点抑制剂可以是以下中的一种或多种:阿特珠单抗、阿维鲁单抗、度伐单抗、伊匹单抗、iph4102、iph43、iph33、利瑞木单抗、莫纳利珠单抗、纳武单抗、帕博利珠单抗和其衍生物或功能等效物。在又一些其它实施例中,所述检查点抑制剂可以是)阿特珠单抗、纳武单抗和帕博利珠单抗中的至少一种。
在一些实施例中,在包括如本文提供的ipsc的衍生细胞的治疗组合物中的治疗剂是抗体,所述抗体可以是抗cd20、抗her2、抗cd52、抗egfr、抗cd123、抗gd2、抗pdl1和/或抗cd38抗体。在一些其它实施例中,所述抗体可以是以下中的至少一种:雷妥昔单抗(retuximab)、维妥珠单抗(veltuzumab)、奥法木单抗(ofatumumab)、乌布里图昔单抗(ublituximab)、奥卡拉珠单抗(ocaratuzumab)、奥比珠单抗(obinutuzumab)、曲妥珠单抗(trastuzumab)、帕妥珠单抗(pertuzumab)、阿仑单抗(alemtuzumab)、西妥昔单抗(certuximab)、迪努妥昔单抗(dinutuximab)、阿维鲁单抗、达土木单抗(daratumumab)、艾沙妥昔单抗(isatuximab)、mor202、7g3、csl362、埃罗妥珠单抗(elotuzumab)和其人源化或经过fc修饰的变体或片段和其功能等效物和生物仿制药。在一个实施例中,所述抗体是达土木单抗。
本申请的另外的方面提供了一种如上文提供的治疗组合物的治疗用途,所述治疗用途通过将所述治疗组合物引入适于过继性细胞疗法的受试者体内,其中所述受试者患有:自身免疫性病症;血液系统恶性肿瘤;实体瘤;癌症或病毒感染。
本申请的仍另一方面提供了一种制造具有一种或多种期望的外源性多核苷酸的衍生细胞的方法,所述方法包括分化ipsc,其中所述ipsc包括:外源性nkg2c;以及任选地外源性cd94和外源性dap12中的一者或两者;以及任选地以下中的一种或多种:(i)bike或trike;(ii)b2m无效或低;(iii)ciita无效或低;(iv)hla-g或不可切割的hla-g的引入的表达;(v)嵌合抗原受体(car);(vi)细胞表面表达的外源性细胞因子或其受体的部分或全部肽;(vii)表1中列出的基因型中的至少一种;(viii)b2m、tap1、tap2、tap相关蛋白、nlrc5、ciita、rfxank、ciita、rfx5、rfxap、tcrα或β恒定区、nkg2a、nkg2d、cd38、cis、cbl-b、socs2、pd1、ctla4、lag3、tim3、tigit或染色体6p21区中的任何基因中的至少一种的缺失或减少的表达;并且(ix)hla-e、41bbl、cd3、cd4、cd8、cd16、cd47、cd113、cd131、cd137、cd80、pdl1、a2ar、tcr、fc受体、衔接子或用于与双特异性或多特异性或通用衔接子偶联的表面触发性受体中的至少一种的引入或增加的表达。在所述方法的一些实施例中,所述方法进一步包括对ipsc进行基因组工程化以获得具有表1中列出的至少一种基因型的克隆ipsc。在一些实施例中,所述基因组工程化包括靶向编辑。在一些实施例中,所述靶向编辑包括缺失、插入或插入/缺失,并且其中所述靶向编辑通过crispr、zfn、talen、归巢核酸酶、同源重组或这些方法的任何其它功能性变型进行。
本申请的另一方面提供了一种对克隆ipsc进行的crispr介导的编辑,以获得经过编辑的克隆ipsc,所述克隆ipsc包括:外源性nkg2c;以及任选地外源性cd94和外源性dap12中的一者或两者;以及任选地以下中的一种或多种:(i)bike或trike;(ii)高亲和力不可切割的cd16(hncd16)或其变体;以及(iii)嵌合抗原受体(car);或经过编辑的克隆ipsc包括表1中列出的基因型中的至少一种。在其中经过编辑的ipsc包括car的一些实施例中,所述car任选地插入在tcr恒定区处和/或由tcr的内源性启动子驱动,和/或所述tcr通过car插入而被敲除。
本申请的另外的方面提供了一种预防或减少肿瘤抗原逃逸和/或肿瘤复发的方法,并且所述方法包括向处于治疗中的受试者施用效应细胞,所述效应细胞包括:(a)外源性nkg2c;以及任选地外源性cd94和外源性dap12中的一者或两者;以及任选地,以下中的一种或多种:bike或trike;高亲和力不可切割的cd16(hncd16)或其变体;嵌合抗原受体(car);或(b)表1中列出的基因型中的至少一种;以及向所述受试者施用抗原特异性单克隆抗体或人源化或经过fc修饰的变体或片段、其功能等效物和生物仿制药中的任一种,其中所述抗体靶向的抗原不同于由所述car、所述bike或所述trike识别的肿瘤抗原。
通过结合附图进行的以下描述,如本文所提供的组合物和方法的各个目的和优势将变得显而易见,在所述附图中借助于说明和实例阐述本发明的某些实施例。
附图说明
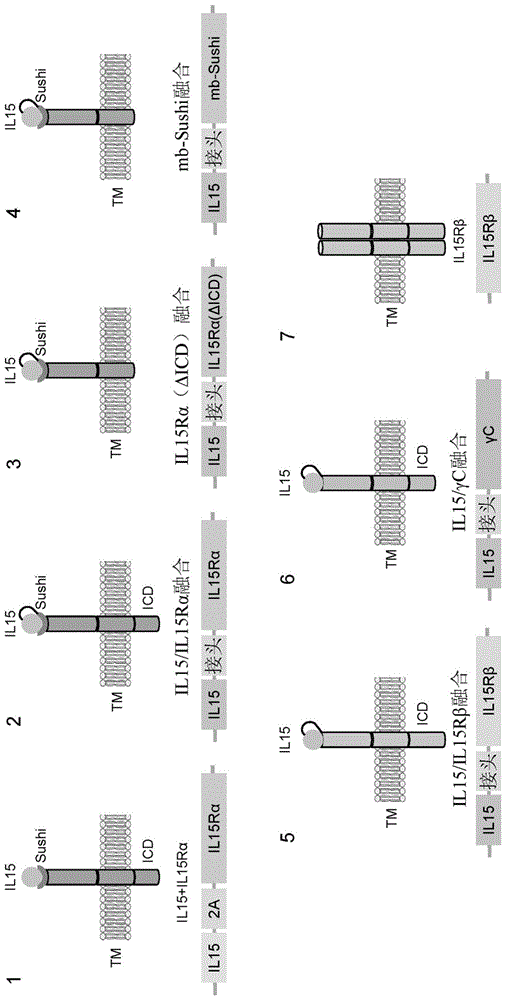
图1是用于ipsc衍生细胞中的细胞表面表达的细胞因子或其受体的若干构建体设计的图示。il15用作说明性实例,其可以用其它所期望的细胞因子置换。
图2示出了含有nkg2c/dap12的ipsc的工程化和分化。(a)ipsc经过工程化以表达nkg2c/dap12;(b)ink细胞分化概况。
图3示出了对在所指示的ink系:未经修饰的ink、nkg2cink和nkg2c/dap12ink中的nkg2c表面表达进行的facs(a)点图和(b)直方图分析。
图4示出了在靶向以所指示浓度包覆有抗nkg2c抗体的p815细胞的重新定向的抗体依赖性细胞毒性(adcc)测定中对在未经修饰的ink、nkg2cink和nkg2c/dap12ink系中脱粒(cd107a表面表达)、ifnγ产生和tnf产生进行的facs分析。
图5是由流式细胞术测定的端粒长度的图示,并且来自ipsc的成熟衍生nk细胞相较于成体外周血nk细胞维持更长的端粒。
具体实施方式
ipsc(诱导性多能干细胞)的基因组修饰包括多核苷酸插入、缺失和取代。基因组工程化ipsc中的外源性基因表达通常遇到问题,例如在初始基因组工程化ipsc长期克隆扩增之后、在细胞分化之后并且在来自衍生自基因组工程化ipsc的细胞的去分化细胞类型中基因沉默或基因表达减少。另一方面,直接工程化例如t细胞或nk细胞的原代免疫细胞具有挑战性,并且对制备和递送用于过继性细胞疗法的工程化免疫细胞存在障碍。本发明提供用于将一种或多种外源性基因(包括自杀基因和其它功能模式)稳定地整合到ipsc衍生细胞中的有效的、可靠的和针对性的方法,所述ipsc衍生细胞通过定向ipsc分化获得,所述一种或多种外源性基因提供与移植、运输、归巢、迁移、细胞毒性、活力、维持、扩增、寿命、自我更新、存留和/或存活有关的有所改善的治疗特性,所述衍生细胞包括但不限于hsc(造血干细胞和祖细胞)、t细胞祖细胞、nk细胞祖细胞、t细胞、nkt细胞、nk细胞。
定义
除非本文中另外定义,否则结合本申请使用的科学与技术术语将具有所属领域的技术人员通常了解的含义。另外,除非上下文另外需要,否则单数术语应包括复数,并且复数术语应包括单数。
应理解,本发明不限于本文所述的特定方法、方案和试剂等,并且因此可变化。本文所用的术语仅仅是出于描述特定实施例的目的,并且并不意欲限制本发明的范围,本发明的范围只由权利要求书来界定。
如本文所用,冠词“一(a/an)”在本文中是指一个(种)或超过一个(种)(即至少一个(种))的所述冠词的语法对象。举例来说,“一个要素”是指一个要素或多于一个要素。
替代方案(例如“或”)的使用应理解为意指替代方案中的任一个、两个或其任何组合。
术语“和/或”应理解为意指替代方案中的一者或两者。
如本文所用,术语“约”或“大约”是指与参考数量、水平、数值、数目、频率、百分比、维度、尺寸、量、重量或长度相比,数量、水平、数值、数目、频率、百分比、维度、尺寸、量、重量或长度变化多达15%、10%、9%、8%、7%、6%、5%、4%、3%、2%或1%。在一个实施例中,术语“约”或“大约”是指关于参考数量、水平、数值、数目、频率、百分比、维度、尺寸、量、重量或长度,数量、水平、数值、数目、频率、百分比、维度、尺寸、量、重量或长度±15%、±10%、±9%、±8%、±7%、±6%、±5%、±4%、±3%、±2%或±1%的范围。
如本文所使用,术语“实质上”或“基本上”是指数量、水平、数值、数目、频率、百分比、维度、尺寸、量、重量或长度为参考数量、水平、数值、数目、频率、百分比、维度、尺寸、量、重量或长度的约90%、91%、92%、93%、94%、95%、96%、97%、98%或99%或更高。在一个实施例中,术语“基本上相同”或“实质上相同”是指与参考数量、水平、数值、数目、频率、百分比、维度、尺寸、量、重量或长度大约相同的数量、水平、数值、数目、频率、百分比、维度、尺寸、量、重量或长度的范围。
如本文所用,术语“实质上不含”与“基本上不含”可互换地使用,并且当用于描述组合物(例如细胞群或培养基)时,是指不含所指定物质或其来源的组合物,例如95%不含、96%不含、97%不含、98%不含、99%不含所指定物质或其来源,或检测不到,如通过常规方式所测量。术语组合物中“不含”或“基本上不含”某种成分或物质也意指(1)所述组合物中不包括任何浓度的这类成分或物质,或(2)所述组合物中包括功能上呈惰性、但呈低浓度的这类成分或物质。类似含义可以应用于术语“缺乏”,其是指组合物中物缺乏特定质或其来源。
在整个本说明书中,除非上下文另外要求,否则词语“包含(comprise/comprises/comprising)”应理解成暗指包括所陈述步骤或要素或一组步骤或要素,但不排除任何其它步骤或要素或一组步骤或要素。在特定实施例中,术语“包括”、“具有”、“含有”和“包含”同义地使用。
“由……组成”打算包括并且限于短语“由……组成”之后的任何事物。因此,短语“由……组成”指示所列要素是需要或必需的,并可能不存在其它要素。
“基本上由……组成”打算包括短语后所列的任何要素,并且限于不干扰或影响本公开中指定的所列要素的活性或作用的其它要素。因此,短语“主要由……组成”指示所列要素是需要或必需的,但其它要素是任选的并且可视其是否影响所列要素的活性或作用而存在或不存在。
在整个本说明书中提及“一个实施例”、“一实施例”、“特定实施例”、“相关实施例”、“某一实施例”、“另外实施例”或“另一实施例”或其组合意指结合实施例描述的特定特点、结构或特征包括于本发明的至少一个实施例中。因此,在整个本说明书中的各处出现的前述短语不一定全部指代同一实施例。此外,在一个或多个实施例中,特定特点、结构或特性可以任何合适方式组合。
术语“离体(exvivo)”通常是指在生物体外发生的活动,如在生物体外的人工环境中的活组织中或上进行的实验或测量,优选地具有最小的自然条件改变。在特定实施例中,“离体”程序涉及从生物体中获取活细胞或组织并且通常在无菌条件下在实验室设备中培养,并且通常培养几小时或长达约24小时,但包括长达48小时或72小时或更长,这视情况而定。在某些实施例中,可以收集和冷冻这类组织或细胞,并且稍后解冻以便进行离体处理。使用活细胞或组织持续时间长于几天的组织培养实验或程序通常被视为“体外”,但在某些实施例中,这个术语可以与离体互换使用。
术语“体内”一般是指在生物体内部进行的活动。
如本文所用,术语“重编程”或“去分化”或“提高细胞效能”或“提高发育效能”是指一种提高细胞效能或使细胞去分化成较低分化状态的方法。举例来说,具有提高的细胞效能的细胞具有与非重编程状态下相同细胞相比更大的发育可塑性(即,可分化成更多细胞类型)。换句话说,重编程细胞是与非重编程状态下相同细胞相比分化状态较低的细胞。
如本文所用,术语“分化”是未特化(“未专门化”)或弱特化细胞借以获得特化细胞(例如血细胞或肌肉细胞)的特点的过程。分化细胞或分化诱导性细胞是已处在细胞谱系内的更特化(“专门化”)位置的细胞。术语“专门化”在应用于分化过程时是指一种细胞,其在分化路径中已经行进到在正常情况下其将继续分化成特定细胞类型或细胞类型的亚群并且在正常情况下其不能分化成不同细胞类型或恢复为更弱分化细胞类型的时刻。如本文所用,术语“多能”是指细胞形成身体或胞体(即,胚胎本身)的所有谱系的能力。举例来说,胚胎干细胞是一种类型多能干细胞,其能够形成三种胚层:外胚层、中胚层和内胚层中的每一种的细胞。多能性是一种连续的发育效能,范围为不能产生完整生物体的不完全或部分多能细胞(例如外胚层干细胞或episc)到能够产生完整生物体的更原始、更多能细胞(例如胚胎干细胞)。
如本文所用,术语“诱导性多能干细胞”或ipsc意指由分化的成体、新生儿或胎儿细胞产生的干细胞,所述干细胞已经诱导或改变,即重编程为能够分化成所有三种胚层或真皮层:中胚层、内胚层和外胚层的组织的细胞。所产生的ipsc并非指如其在自然界中被发现的细胞。
如本文所用,术语“胚胎干细胞”是指胚胎囊胚的内部细胞团块中的天然存在的多能干细胞。胚胎干细胞是多能的并且在发育期间产生三种原代胚层:外胚层、内胚层和中胚层的所有衍生细胞。其对胚胎外膜或胎盘没有贡献,即,并非分化全能的。
如本文所用,术语“多潜能干细胞”是指具有分化成一种或多种胚层(外胚层、中胚层和内胚层)、但非全部三种胚层的细胞的发育潜能的细胞。因此,多潜能细胞也可以称为“部分分化细胞”。多潜能细胞在所属领域中是众所周知的,并且多潜能细胞的实例包括成体干细胞,例如造血干细胞和神经干细胞。“多潜能”表示细胞可以形成指定谱系内的许多类型的细胞,而非其它谱系的细胞。举例来说,多潜能造血细胞能够形成许多不同类型的血细胞(红细胞、白细胞、血小板等),但其不能形成神经元。因此,术语“多潜能性”是指一种细胞状态,其发育潜能的程度低于分化全能和多能。
多能性可部分地通过评定细胞的多能性特性确定。多能性特性包括但不限于:(i)多能干细胞形态;(ii)无限自我更新的潜能;(iii)多能干细胞标记物的表达,所述标记物包括但不限于ssea1(仅小鼠)、ssea3/4、ssea5、tra1-60/81、tra1-85、tra2-54、gctm-2、tg343、tg30、cd9、cd29、cd133/凸素(prominin)、cd140a、cd56、cd73、cd90、cd105、oct4、nanog、sox2、cd30和/或cd50;(iv)分化成所有三种体细胞谱系(外胚层、中胚层和内胚层)的能力;(v)由三种体细胞谱系组成的畸胎瘤形成;以及(vi)由来自三种体细胞谱系的细胞组成的类胚胎体的形成。
先前已描述两种类型的多能性:“激发”或“亚稳定”的多能性状态等效于后期囊胚的外胚层干细胞(episc),并且“初始”或“基础”的多能性状态等效于早期/植入前囊胚的内部细胞团块。尽管两种多能状态都展现如上所述的特性,但所述初始或基础状态进一步展现;(i)雌性细胞中的x染色体的预先失活或再激活;(ii)在单一细胞培养期间,克隆性和存活率改善;(iii)dna甲基化总体减少;(iv)发育调节基因启动子上的h3k27me3抑制性染色质标记沉积减少;以及(v)相对于激发状态的多能细胞,分化标记物的表达减少。通常发现细胞重编程标准方法(其中将外源性多能性基因引入体细胞中,表达,并且然后沉默或从所得多能细胞中去除)具有多能性激发状态的特性。在标准多能细胞培养条件下,除非维持外源性转基因表达(其中观察到基础状态的特性),否则这类细胞保持激发状态。
如本文所用,术语“多能干细胞形态”是指胚胎干细胞的经典形态特点。正常胚胎干细胞形态的特征是小圆形形状,细胞核与细胞质比例高,明显存在核仁,和典型的细胞间间距。
如本文所用,术语“受试者”是指任何动物,优选地是人类患者、牲畜或其它驯养动物。
“多能性因子”或“重编程因子”是指一种试剂,其能够单独或与其它试剂组合来增强细胞的发育效能。多能性因子包括但不限于能够提高细胞发育效能的多核苷酸、多肽和小分子。示例性多能性因子包括例如转录因子和小分子重编程剂。
“培养”或“细胞培养”是指细胞在体外环境中维持、生长和/或分化。“细胞培养基”、“培养基”(在各种情况下,为单数形式“培养基(medium)”)、“补充剂”和“培养基补充剂”是指培育细胞培养物的营养组合物。
“培育”或“维持”是指细胞在组织或身体外部(例如在无菌塑料(或经过涂布的塑料)细胞培养皿或烧瓶中)维持、繁殖(生长)和/或分化。“培育”或“维持”可以使用培养基作为有助于细胞繁殖和/或维持的营养、激素和/或其它因子来源。
如本文所用,术语“中胚层”是指三种胚层之一,其出现于早期胚胎发生期间并且产生各种特化细胞类型,包括循环系统、肌肉、心脏、真皮、骨骼和其它支持和结缔组织的血细胞。
如本文所用,术语“永久性生血内皮细胞”(he)或“多能干细胞衍生永久性生血内皮细胞”(ihe)是指在称为内皮细胞向造血细胞转变的过程中产生造血干细胞和祖细胞的内皮细胞亚群。胚胎中的造血细胞发育依序进行:从侧板中胚层到成血管细胞到永久性生血内皮细胞和造血祖细胞。
术语“造血干细胞和祖细胞”、“造血干细胞”、“造血祖细胞”或“造血前驱细胞”是指向造血谱系专门化、但能够进一步向造血分化的细胞,并且包括多潜能造血干细胞(血胚细胞)、骨髓祖细胞、巨核细胞祖细胞、红细胞祖细胞和淋巴祖细胞。造血干细胞和祖细胞(hsc)是多潜能干细胞,其产生所有血细胞类型,包括骨髓(单核细胞和巨噬细胞、嗜中性粒细胞、嗜碱粒细胞、嗜酸性粒细胞、红细胞、巨核细胞/血小板、树突状细胞)和淋巴谱系(t细胞、b细胞、nk细胞)。如本文所用,术语“永久性造血干细胞”是指cd34+造血细胞,其能够产生成熟骨髓细胞类型和淋巴细胞类型,包括t细胞、nk细胞和b细胞。造血细胞还包括原始造血细胞的多种亚群,其产生原始红细胞、巨核细胞和巨噬细胞。
如本文所用,术语“t淋巴细胞”和“t细胞”可互换地使用并且是指白血细胞的主要类型,其在胸腺中完成成熟并且在免疫系统中具有多种作用,包括鉴别体内的特异性外来抗原和使其它免疫细胞激活和去激活。t细胞可以是任何t细胞,例如培养的t细胞,例如原代t细胞,或来自培养的t细胞系的t细胞,例如jurkat、supt1等,或获自哺乳动物的t细胞。t细胞可以是cd3+细胞。t细胞可以是任何类型的t细胞并且可以处于任何发育阶段,包括但不限于cd4+/cd8+双阳性t细胞、cd4+辅助t细胞(例如th1和th2细胞)、cd8+t细胞(例如细胞毒性t细胞)、外周血单核细胞(pbmc)、外周血白细胞(pbl)、肿瘤浸润性淋巴细胞(til)、记忆t细胞、初始t细胞、调控t细胞、gammadeltat细胞(γδt细胞)等等。其它类型的辅助t细胞包括例如th3(treg)、th17、th9或tfh细胞的细胞。其它类型的记忆t细胞包括例如中枢记忆t细胞(tcm细胞)、效应记忆t细胞(tem细胞和temra细胞)的细胞。t细胞还可以指基因工程化t细胞,例如经过修饰可表达t细胞受体(tcr)或嵌合抗原受体(car)的t细胞。t细胞也可以由干细胞或祖细胞分化。
“cd4+t细胞”是指t细胞的一个亚群,其在其表面上表达cd4并且与细胞介导的免疫反应相关。其特征在于刺激后的分泌概况,其可能包括分泌细胞因子,例如ifn-γ、tnf-α、il2、il4和il10。“cd4”是最初被定义为t淋巴细胞上的分化抗原,但也发现于包括单核细胞/巨噬细胞的其它细胞上的55-kd的糖蛋白。cd4抗原是免疫球蛋白超基因家族成员并且表明为主要组织相容性复合体(majorhistocompatibilitycomplex;mhc)ii类限制的免疫反应中的相关识别元件。在t淋巴细胞上,其界定了辅助/诱导因子亚群。
“cd8+t细胞”是指t细胞的一个亚群,其在其表面上表达cd8,受限于mhci类,并且充当细胞毒性t细胞。“cd8”分子是发现于胸腺细胞上和细胞毒性和抑制性t淋巴细胞上的分化抗原。cd8抗原是免疫球蛋白超基因家族成员并且主要组织相容性复合体i类限制的相互作用中的相关识别元件。
如本文所用,术语“nk细胞”或“自然杀手细胞”是指外周血淋巴细胞的一个亚群,其根据cd56或cd16的表达和t细胞受体(cd3)的缺乏来定义。如本文所用,术语“适应性nk细胞”与“记忆nk细胞”可互换并且是指nk细胞的一个亚群,其表型为cd3-和cd56+,表达nkg2c和cd57和任选的cd16中的至少一种,但缺乏以下一种或多种的表达:plzf、syk、fcerγ和eat-2。在一些实施例中,分离的cd56+nk细胞亚群包含cd16、nkg2c、cd57、nkg2d、ncr配体、nkp30、nkp40、nkp46、激活的和抑制性kir、nkg2a和/或dnam-1的表达。cd56+可以是较弱或较强的表达。
如本文所用,术语“nkt细胞”或“自然杀伤t细胞”是指受限于cd1d的t细胞,其表达t细胞受体(tcr)。不同于常规t细胞检测由常规主要组织相容性(mhc)分子呈递的肽抗原,nkt细胞识别由cd1d(一种非经典mhc分子)呈递的脂质抗原。识别两种类型的nkt细胞。恒定型或i型nkt细胞表达非常有限的tcr谱系:典型α链(人类中为vα24-jα18)与有限光谱的β链(人类中为vβ11)的结合。第二个nkt细胞群,称为非经典或非恒定ii型nkt细胞,显示更不均匀的tcrαβ利用率。i型nkt细胞被认为适于免疫疗法。适应性或恒定(i型)nkt细胞可以根据以下标记物中的至少一种或多种的表达来鉴别:tcrva24-ja18、vb11、cd1d、cd3、cd4、cd8、αgalcer、cd161和cd56。
如本文所用,术语“分离”等是指一种细胞或细胞群,其已与其初始环境中分离,即,分离细胞的环境实质上不含如存在“未分离”参考细胞的环境中所发现的至少一种组分。所述术语包括从一些或所有组分去除的细胞,如同其在其自然环境中发现,例如与组织或活检样品分离。所述术语还包括从至少一种、一些或所有组分中去除的细胞,如同所述细胞在非天然存在的环境中发现,例如与细胞培养物或细胞悬浮液分离。因此,分离细胞部分地或完全地与至少一种组分(包括其它物质、细胞或细胞群)分离,如同其在自然界中发现或如同其在非天然存在的环境中生长、储存或生存。分离细胞的特定实例包括部分纯细胞组合物、实质上纯细胞组合物和非天然存在的培养基中培养的细胞。分离细胞可以通过将所期望的细胞或其群体与环境中的其它物质或细胞分离或通过从环境中去除一个或多个其它细胞群或亚群来获得。
如本文所用,术语“纯化”等是指提高的纯度。举例来说,纯度可以提高到至少50%、60%、70%、80%、90%、95%、99%或100%。
如本文所用,术语“编码”是指多核苷酸中的核苷酸的特异性序列(例如基因、cdna或mrna)的固有特性,以充当生物过程中合成其它聚合物和大分子的模板,所述其它聚合物和大分子具有定义的核苷酸序列(即,rrna、trna和mrna)或定义的氨基酸序列和由其获得的生物特性。因此,如果与一种基因对应的mrna的转录和转译在细胞或其它生物系统中产生一种蛋白质,那么所述基因编码所述蛋白质。编码链(其核苷酸序列与mrna序列一致并且通常提供于序列表中)与非编码链(用作基因或cdna转录的模板)都可以称为编码所述基因或cdna的蛋白质或其它产物。
“构建体”是指包含待体外或体内传递给宿主细胞中的多核苷酸的大分子或分子复合体。如本文所用,“载体”是指能够引导外来遗传物质递送或转移到靶细胞的任何核酸构建体,在靶细胞中,所述核酸构建体能够复制和/或表达。如本文所用,术语“载体”包含待递送的构建体。载体可以是线性或环形分子。载体可以是整合或非整合载体。载体的主要类型包括但不限于质粒、游离型载体、病毒载体、粘粒和人工染色体。病毒载体包括但不限于腺病毒载体、腺相关病毒载体、逆转录病毒载体、慢病毒载体、仙台病毒载体(sendaivirusvector)等。
“整合”意指构建体的一个或多个核苷酸稳定插入细胞基因组中,即,共价连接至细胞染色体dna内的核酸序列。“靶向整合”意指构建体的核苷酸在预选位点或“整合位点”插入细胞染色体或线粒体dna中。如本文所用,术语“整合”进一步是指一种过程,其涉及在内源性序列或核苷酸缺失或不缺失的情况下在整合位点插入构建体的一个或多个外源性序列或核苷酸。在插入位点存在缺失的情况下,“整合”可以进一步包含用一个或多个所插入核苷酸置换缺失的内源性序列或核苷酸。
如本文所用,术语“外源性”旨在意指参考分子或参考活性引入宿主细胞中,或对于宿主细胞是非天然的。所述分子可以通过例如将编码核酸引入宿主遗传物质中来引入,例如整合于宿主染色体中,或作为非染色体遗传物质,例如质粒。因此,所述术语当关于编码核酸的表达使用时是指编码核酸以可表达形式引入细胞中。术语“内源性”是指存在于宿主细胞中的参考分子或活性。类似地,所述术语当关于编码核酸的表达使用时,是指细胞内所含而非外源引入的编码核酸的表达。
如本文所用,“所关注基因”或“所关注多核苷酸序列”是当放置在适当调控序列的控制下时体内转录成rna并且在一些情况下转译成多肽的dna序列。所关注基因或多核苷酸可以包括但不限于原核序列、来自真核mrna的cdna、来自真核(例如哺乳动物)dna的基因组dna序列和合成dna序列。举例来说,所关注基因可以编码mirna、shrna、原生多肽(即自然界中发现的多肽)或其片段;变异多肽(即,与原生多肽具有小于100%的序列一致性的原生多肽的突变体)或其片段;工程化多肽或肽片段、治疗肽或多肽、成像标记物、可选标记物等等。
如本文所用,术语“多核苷酸”是指具有任何长度的核苷酸(脱氧核糖核苷酸或核糖核苷酸)的聚合物形式或其类似物。多核苷酸序列是由四个核苷酸碱基构成:腺嘌呤(a);胞嘧啶(c);鸟嘌呤(g);胸腺嘧啶(t);和尿嘧啶(u)(当多核苷酸是rna时,尿嘧啶代替胸腺嘧啶)。多核苷酸可以包括基因或基因片段(例如探针、引物、est或sage标签)、外显子、内含子、信使rna(mrna)、转移rna、核糖体rna、核酶、cdna、重组多核苷酸、分支链多核苷酸、质粒、载体、任何序列的分离dna、任何序列的分离rna、核酸探针和引物。多核苷酸还指双链和单链分子。
如本文所用,术语“肽”、“多肽”和“蛋白质”可互换地使用并且是指氨基酸残基通过肽键共价连接的分子。多肽必须含有至少两个氨基酸,并且多肽的氨基酸最大数目不受限制。如本文所用,所述术语是指短链(在所属领域中通常也称为例如肽、寡肽和寡聚物)和较长链(在所属领域中通常称为多肽或蛋白质)。“多肽”包括例如生物活性片段、实质上同源多肽、寡肽、同源二聚体、异源二聚体、多肽变体、经过修饰的多肽、衍生物、类似物、融合蛋白以及其它。所述多肽包括自然多肽、重组多肽、合成多肽或其组合。
“可操作地连接”是指单一核酸片段上的核酸序列的结合,以使得一者的功能受另一者影响。举例来说,当启动子能够影响编码序列或功能rna表达(即,所述编码序列或功能rna处于启动子的转录控制下)时,所述启动子与所述编码序列或功能rna可操作地连接。编码序列可以按照有义或反义定向可操作地连接到调控序列。
如本文所用,术语“遗传印记”是指对源细胞或ipsc的优选治疗属性有贡献的遗传或表观遗传信息,并且能保留于源细胞衍生ipsc和/或ipsc衍生造血谱系细胞中。如本文所用,“源细胞”是一种可以用于通过重编程来产生ipsc的非多能细胞,并且源细胞衍生ipsc可以进一步分化成特定细胞类型,包括任何造血谱系细胞。视上下文而定,源细胞衍生ipsc和其分化细胞有时统称为“衍生(derived或derivative)细胞”。举例来说,如在整个本申请中所使用,衍生效应细胞或衍生的nk细胞或衍生t细胞与获自自然/原生来源(例如外周血、脐带血或其它供体组织)的其原代对应细胞相比是由ipsc分化的细胞。如本文所用,赋予优选治疗属性的遗传印记是通过使对供体、疾病或治疗反应具有特异性的所选源细胞重编程或通过使用基因组编辑将基因修饰模式引入ipsc来并入ipsc中。在从特别选择的供体、疾病或治疗背景所获得的源细胞的所述方面中,对优选治疗属性有贡献的遗传印记可以包括任何背景特有的遗传或表观遗传修饰,其显现能保留的表型,即优选的治疗属性,所述表型传递到所选源细胞的衍生细胞,无论潜在分子事件得到鉴别或未得到鉴别。对供体、疾病或治疗反应具有特异性的源细胞可以包含能保留于ipsc和衍生造血谱系细胞中的遗传印记,所述遗传印记包括但不限于预排列的单特异性tcr,例如来自病毒特异性t细胞或恒定型自然杀伤t(inkt)细胞;能追踪和所期望的遗传多态性,例如对编码所选供体中的高亲和力cd16受体的点突变来说为同型;和预定的hla需求,即,所选的hla匹配供体细胞随着群体增大而展现单倍型。如本文所用,优选治疗属性包括衍生细胞的移植、运输、归巢、活力、自更新、存留、免疫反应调控和调节、存活和细胞毒性改善。优先治疗属性还可以与以下有关:抗原靶向受体表达;hla呈递或其缺乏;对肿瘤微环境的抗性;旁观者免疫细胞的诱导和免疫调节;随着肿瘤外效应降低,靶上特异性改善;对例如化学疗法等治疗的抗性。
如本文所用,术语“增强的治疗特性”是指细胞的治疗特性与相同一般细胞类型的典型免疫细胞相比增强。举例来说,与典型的、未修饰的和/或天然存在的nk细胞相比,具有“增强的治疗特性”的nk细胞将具有增强、改善和/或强化的治疗特性。免疫细胞的治疗特性可以包括但不限于细胞移植、运输、归巢、活力、自我更新、存留、免疫反应调控和调节、存活和细胞毒性。免疫细胞的治疗特性也通过以下来体现:靶向抗原的受体表达;hla呈递或其缺乏;对肿瘤微环境的抗性;旁观者免疫细胞的诱导和免疫调节;随着肿瘤外效应降低,靶上特异性改善;对例如化学疗法等治疗的抗性.
如本文所用,术语“衔接子”是指一种分子,例如融合多肽,其能够使免疫细胞(例如t细胞、nk细胞、nkt细胞、b细胞、巨噬细胞、嗜中性粒细胞)与肿瘤细胞之间形成连接;并且激活所述免疫细胞。衔接子的实例包括但不限于双特异性t细胞衔接子(bite)、双特异性杀伤细胞衔接子(bike)、三特异性杀伤细胞衔接子或多特异性杀伤细胞衔接子,或与多种免疫细胞类型相容的通用衔接子。
如本文所用,术语“表面触发性受体”是指一种能够触发或启动免疫反应(例如细胞毒性反应)的受体。表面触发性受体可以加以工程化,并且可以在效应细胞(例如t细胞、nk细胞、nkt细胞、b细胞、巨噬细胞、嗜中性粒细胞)上表达。在一些实施例中,表面触发性受体促进效应细胞与特定靶细胞(例如肿瘤细胞)之间发生双特异性或多特异性抗体接合,不依赖于效应细胞的自然受体和细胞类型。使用这种方法,可以产生包含通用表面触发性受体的ipsc,并且然后使这类ipsc分化成表达所述通用表面触发性受体的各种效应细胞类型的群体。“通用”意指表面触发性受体可表达于任何效应细胞中并且激活任何效应细胞(不论细胞类型)并且表达通用受体的所有效应细胞可与表面触发性受体可识别的具有相同抗原决定基的衔接子偶联或连接(不论衔接子的肿瘤结合特异性)。在一些实施例中,具有相同肿瘤靶向特异性的衔接子用于与通用表面触发性受体偶联。在一些实施例中,具有不同肿瘤靶向特异性的衔接子用于与所述通用表面触发性受体偶联。因而,可使一种或多种效应细胞类型接合,从而在一些情况下杀死一种特定类型的肿瘤细胞并且在一些其它情况下杀死两种或更多种类型的肿瘤。表面触发性受体通常包含用于效应细胞激活的共刺激结构域和对衔接子的抗原决定基具有特异性的抗抗原决定基。双特异性衔接子对位于一端的表面触发性受体的抗抗原决定基具有特异性,并且对位于另一端的肿瘤抗原具有特异性。
如本文所用,术语“安全开关蛋白质”是指一种工程化蛋白质,其经设计以防止细胞疗法的潜在毒性或以其它方式防止副作用。在一些情况下,有条件地控制安全开关蛋白表达,以解决已经将对安全开关蛋白进行编码的基因永久地并入其基因组中的移植的工程细胞的安全问题。这种条件性调控可以是可变的并且可能包括通过小分子介导的转译后激活和组织特异性和/或时间转录调控来进行控制。安全开关可以介导对凋亡的诱导、对蛋白合成或dna复制的抑制、生长阻滞、转录和转录后遗传调节和/或抗体介导的耗竭。在一些情况下,安全开关蛋白由外源性分子例如前药活化,所述外源性分子在被活化时触发了治疗细胞的凋亡和/或细胞死亡。安全开关蛋白的实例包含但不限于自杀基因,如胱天蛋白酶9(或胱天蛋白酶3或7)、胸苷激酶、胞嘧啶脱氨酶、b细胞cd20、经过修饰的egfr和其任何组合。在这种策略中,在发生不良事件时施用的前药由自杀基因产物活化并且杀死转导的细胞。
如本文所用,术语“医药学活性蛋白质或肽”是指能够对生物体实现生物学和/或医药作用的蛋白质或肽。医药学活性蛋白质具有针对疾病的治愈性或姑息性特性,并且可以施用以改善、缓解、减缓、逆转或减轻疾病严重程度。医药学活性蛋白质还具有预防特性并且用于防止疾病发作或减轻这类疾病或病理病况在其显现时的严重强度。医药学活性蛋白质包括完整蛋白质或肽或其医药学活性片段。其还包括所述蛋白质或肽的医药学活性类似物或所述蛋白质或肽的片段的类似物。术语医药学活性蛋白质还指以协作或协同方式发挥作用以提供治疗效益的多种蛋白质或肽。医药学活性蛋白质或肽的实例包括但不限于受体、结合性蛋白、转录和转译因子、肿瘤生长抑制蛋白质、抗体或其片段、生长因子和/或细胞因子。
如本文所用,术语“信号传导分子”是指调节、参与、抑制、激活、减少或增加细胞信号转导的任何分子。信号转导是指分子信号以化学修饰形式传递,其通过沿着最终触发细胞中的生物化学事件的路径募集蛋白质复合体来实现。信号转导路径在所属领域中是众所周知的,并且包括但不限于g蛋白偶联受体信号传导、酪氨酸激酶受体信号传导、整合素信号传导、tg点信号传导、配体门控离子通道信号传导、erk/mapk信号传导路径、wnt信号传导路径、camp依赖性路径和ip3/dag信号传导路径。
如本文所用,术语“靶向模式”是指分子(例如多肽)以遗传方式并入细胞中以促进抗原和/或抗原决定基特异性,其包括但不限于i)抗原特异性(当其涉及独特嵌合抗原受体(car)或t细胞受体(tcr)时);ii)衔接子特异性(当其涉及单克隆抗体或双特异性衔接子时);ⅲ)靶向转化细胞;iv)靶向癌症干细胞,和v)在缺乏特异性抗原或表面分子的情况下的其它靶向策略。
如本文所用,与非特异性或非选择性结合相比,术语“特异性(specific/specificity)”可以用于指分子(例如受体或衔接子)能够选择性地结合到靶分子。
如本文所用,术语“过继性细胞疗法”是指一种基于细胞的免疫疗法,如本文所用,其是指自体或同种异体淋巴细胞的输注,所述淋巴细胞经鉴别为经过遗传修饰或未经遗传修饰的t细胞或b细胞,其在所述输注之前已离体扩增。
如本文所用,“治疗上足够的量”在其含义内包含无毒但足够和/或有效量的其所指代的用于提供期望的治疗效果的特定治疗和/或药物组合物。所需精确量将随各受试者而变化,这取决于例如患者总体健康状况、患者年龄和病况分期和严重强度等因素。在特定实施例中,治疗上足量足以和/或有效地使与所治疗的受试者的疾病或病况相关的至少一种症状改善、减少和/或好转。
多能干细胞的分化需要改变培养系统,例如改变培养基中的刺激剂或细胞的物理状态。大部分常规策略是使用类胚胎体(eb)的形成作为启动谱系特异性分化的共同和关键中间步骤。“类胚胎体”是三维团簇,其已表明可模拟胚胎发育,因为其在其三维区域内产生多种谱系。通过分化过程,通常为几小时到几天,简单的eb(例如经过诱发可分化的聚集多能干细胞)继续成熟并且发育成囊性eb,此时,通常进一步将其处理数日到几周以继续分化。eb形成是通过使多能干细胞彼此紧密接近地形成三维多层细胞团簇来启动,这通常是通过若干种方法之一来实现,所述方法包括允许多能细胞在液滴中沉降、使细胞在“u”形底孔板中沉降或通过机械搅拌。为了促进eb发育,多能干细胞聚集体需要进一步分化提示,原因是多能培养维持性培养基中所维持的聚集体不形成适当eb。因而,多能干细胞聚集体需要转移到分化培养基中,所述分化培养基向所选谱系提供诱发提示。通过在eb细胞团簇内适度增殖,多能干细胞的基于eb的培养通常引起分化细胞群(外胚层、中胚层和内胚层胚层)产生。虽然经证实可促进细胞分化,然而,eb产生了分化状态可变的异质细胞,原因是三维结构中的细胞不一致地暴露于来自环境的分化提示。另外,eb的形成和维持麻烦。此外,通过eb进行的细胞分化伴随适度细胞扩增,这也导致分化效率降低。
相比之下,与“eb形成”不同的“聚集体形成”可以用于扩增多能干细胞衍生细胞群。举例来说,在基于聚集体的多能干细胞扩增期间,选择可维持增殖和多能性的培养基。细胞增殖通常增加聚集体的尺寸,从而形成更大聚集体,这些聚集体可用常规的机械或酶方式解离成更小聚集体,从而维持培养物内的细胞增殖并且增加细胞数目。不同于eb培养,维持培养的聚集体内所培养的细胞维持多能性标记。多能干细胞聚集体需要进一步分化提示来诱导分化。
如本文所用,“单层分化”是关于分化方法的术语,其不同于通过三维多层细胞团簇进行的分化,即,“eb形成”。单层分化以及本文所公开的其它优势避免了分化起始需要eb形成。由于单层培养不模拟胚胎发育,例如eb形成,因此相较于eb中的所有三种胚层分化,向特定谱系的分化被认为是最少的。
如本文所用,“解离”细胞是指已实质上与其它细胞或表面(例如培养板表面)分离或纯化的细胞。举例来说,细胞可通过机械或酶方法从动物或组织中解离。可替代地,在体外聚集的细胞可以彼此解离,如酶促地或机械地解离成簇、单细胞或单细胞和簇的混合物的悬浮液。在又另一个替代实施例中,粘着细胞从培养板或其它表面解离。因此,解离可能涉及破坏与胞外基质(ecm)和衬底(例如培养表面)的细胞相互作用,或破坏细胞之间的ecm。
如本文所用,“饲养细胞”或“饲养层”是描述与第二类型的细胞共培养以提供第二类型的细胞可在其中生长、扩增或分化的环境的一种类型的细胞的术语,因为饲养细胞为支持第二细胞类型提供刺激、生长因子和营养。饲养细胞任选地来自与其支持的细胞不同的物种。举例来说,某些类型的人类细胞,包括干细胞,可以由小鼠胚胎成纤维细胞或永生化小鼠胚胎成纤维细胞的原代培养物支持。在另一个实例中,外周血衍生细胞或转化的白血病细胞支持自然杀伤细胞的扩增和成熟。饲养细胞在与其它细胞共培养时,可以通常通过照射或用抗有丝分裂剂(例如丝裂霉素(mitomycin))处理来失活,以防止其生长超出其支持的细胞。饲养细胞可以包括内皮细胞、基质细胞(例如上皮细胞或成纤维细胞)和白血病细胞。不限于前述,一种特定的饲养细胞类型可以是人类饲养层,例如人类皮肤成纤维细胞。另一饲养细胞类型可以是小鼠胚胎成纤维细胞(mef)。一般来说,多种饲养细胞可部分地用于维持多能性、朝向某一谱系的定向分化,增强增殖能力并且促进向特化细胞类型(例如效应细胞)的成熟。
如本文所用,“无饲养层”(ff)环境是指一种环境,例如培养条件、细胞培养物或培养基,其基本上不含饲养层或基质细胞,和/或尚未通过培育饲养细胞加以预调节。“预调节”培养基是指饲养细胞在培养基内已培育一定时段(例如至少一天)之后所收集的培养基。预调节培养基含有多种介体物质,包括在培养基中培育的饲养细胞所分泌的生长因子和细胞因子。在一些实施例中,无饲料环境不含饲养层或基质细胞,并且也不通过培育饲养细胞进行预调节。
如在ipsc和由其分化的衍生非多能细胞的基因组编辑或修饰或非多能细胞和由其重编程的衍生ipsc的基因组编辑或修饰的背景下所用的“功能”是指(1)在基因层面上成功的敲入、敲除、降低基因表达、转基因或受控基因表达,例如所期望的细胞发育阶段的诱导性或暂时表达,这通过直接的基因组编辑或修饰或通过“传递”、通过最初进行基因组工程化起始细胞的分化或重编程来实现;或(2)在细胞层面成功的去除、添加或改变细胞功能/特性,这通过以下实现:(i)在所述细胞中通过直接的基因组编辑而获得的基因表达变化;(ii)在所述细胞中通过“传递”、通过从最初进行基因组工程化起始细胞的分化或重编程而维持的基因表达变化;(iii)在所述细胞中作为基因表达修饰的结果的下游基因调控,所述基因表达修饰仅出现于所述细胞的较早发育阶段或仅出现于通过分化或重编程而产生所述细胞的起始细胞中;或(iv)成熟细胞产物内所呈现的增强的或新获得的细胞功能或属性,所述成熟细胞产物最初通过对祖细胞或去分化细胞来源的ipsc进行基因组编辑或修饰而获得。
“缺乏hla”,包括缺乏hla-i类,或缺乏hla-ii类,或两者,是指缺乏或不再维持包含hlai类蛋白质异源二聚体和/或hlaii类异源二聚体的完整mhc复合体的表面表达或所述表面表达的水平降低,使得减弱或降低的水平低于被其它细胞天然可检测到的或被合成方法可检测到的水平。
如本文所用,“缺乏hla的已修饰的ipsc”是指缺乏hla的ipsc,其另外通过引入基因表达蛋白质而被修饰,所述蛋白质与以下有关但不限于:改善的分化潜能、抗原靶向、抗原呈递、抗体识别、存留、免疫逃避、抑制抗性、增殖、共刺激、细胞因子刺激、细胞因子产生(自分泌或旁分泌)、趋化性和细胞毒性,例如非经典hlai类蛋白质(例如hla-e和hla-g)、嵌合抗原受体(car)、t细胞受体(tcr)、cd16fc受体、bcl11b、notch、runx1、il15、41bb、dap10、dap12、cd24、cd3z、41bbl、cd47、cd113和pdl1。“缺乏hla的已修饰的”细胞还包含除ipsc之外的细胞。
“fc受体”(缩写为fcr)是基于其识别的抗体类型而分类。举例来说,结合最常见类别的抗体(igg)的受体称为fc-γ受体(fcγr),结合iga的受体称为fc-α受体(fcαr)并且结合ige的受体称为fc-ε受体(fcεr)。fcr的类别也通过表达其(巨噬细胞、粒细胞、自然杀手细胞、t细胞和b细胞)的细胞和每种受体的信号传导特性来区分。fc-γ受体(fcγr)包括若干成员:fcγri(cd64)、fcγriia(cd32)、fcγriib(cd32)、fcγriiia(cd16a)、fcγriiib(cd16b),其因其分子结构不同而对其抗体具有不同亲和力。
「嵌合fc受体」缩写为cfcr,是用于描述其天然跨膜和/或胞内信号传导结构域被非天然跨膜和/或胞内信号传导结构域修饰或置换的工程化fc受体的术语。在嵌合fc受体的一些实施例中,除非天然的跨膜和信号传导结构域中的一者或两者之外,可将一种或多种刺激性结构域引入工程化fc受体的胞内部分中以在触发受体后增强细胞激活、扩增和功能。不同于含有与靶抗原的抗原结合性结构域的嵌合抗原受体(car),嵌合fc受体结合于fc片段、或抗体的fc区、或包含于衔接子或结合性分子中并且在使靶细胞接近或不接近附近的情况下激活细胞功能的fc区。举例来说,可工程化fcγ受体以将所选跨膜、刺激和/或信号传导结构域包含在对在胞外结构域结合igg有反应的胞内区域中,从而产生cfcr。在一个实例中,cfcr由工程化cd16、fcγ受体通过置换其跨膜结构域和/或胞内结构域来产生。为了进一步提高基于cd16的cfcr的结合性亲和力,可合并cd64或cd16的高亲和力变体(例如f176v)的胞外结构域。在涉及高亲和力cd16胞外结构域的cfcr的一些实施例中,位置197处包含丝氨酸的蛋白水解切割位点被消除或置换,使得受体的胞外结构域不可切割,即不经历脱落,从而获得基于hncd16的cfcr。
fcγr受体cd16已鉴别为具有两种异构体:fc受体fcγriiia(cd16a)和fcγriiib(cd16b)。cd16a是由nk细胞表达的跨膜蛋白,其结合附接到靶细胞的单体igg以激活nk细胞和促进抗体依赖性细胞介导的细胞毒性(adcc)。如本文所用,“高亲和力cd16”、“不可切割的cd16”或“高亲和力不可切割的cd16(hncd16)”是指天然或非天然的cd16变体。野生型cd16具有低亲和力并且经历胞外结构域脱落,这是一种蛋白分解切割过程,其在nk细胞激活后调控白细胞上的多种细胞表面分子的细胞表面密度。f176v和f158v是具有高亲和力的示例性cd16多态变体。在接近膜的区域(位置189-212)中改变或消除切割位点(位置195-198)的cd16变体不经历脱落。切割位点和接近膜的区域详细地描述于wo2015148926中,其完整公开内容以引入的方式并入本文中。cd16s197p变体是工程化cd16的不可切割型式。包含f158v和s197p的cd16变体具有高亲和力,并且不可切割。另一示例性高亲和力和不可切割的cd16(hncd16)变体是包含源自cd64胞外结构域的3个外显子中的一个或多个的胞外结构域的工程化cd16。
i.适用于具有增强特性的过继性细胞疗法的细胞和组合物
本文提供一种策略,其系统地工程化克隆ipsc的调控回路,并且不影响ipsc的分化效能以及ipsc和其衍生细胞的细胞发育生物学,同时增强衍生细胞的治疗特性。在ipsc水平上通过基因工程化引入细胞中的选择性模式组合之后,衍生细胞在功能上得到改善,并且适于过继性细胞疗法。不清楚在本发明之前,包含一种或多种所提供的基因编辑的改变的ipsc是否另外具有进入细胞发育和/或使功能分化细胞成熟和产生同时保留调节活性的能力。从ipsc定向细胞分化期间的意外失败归因于包括但不限于以下的方面:发育阶段特定的基因表达或缺乏基因表达、hla复合体呈递的需求、所引入表面表达模式的蛋白质脱落和实现细胞中表型和/或功能变化的分化方案重配置的需要。本申请已展示,如本文所提供的一种或多种所选基因组修饰不会对ipsc分化效能产生负面影响,并且衍生自工程化ipsc的功能效应细胞具有增强的和/或获得的治疗特性,这可归因于在ipsc分化之后保留在效应细胞中的单独的或组合的基因组修饰。
1.nkg2c的过表达
生理学nkg2c表达限于作为巨细胞病毒(cmv)感染的应答而扩增的nk和cd8+t细胞的子集。cd94/nkg2c是异二聚体受体,所述异二聚体受体与hla-e结合并且与dap12相关,所述dap12是一种含有基于免疫受体酪氨酸的活化基序的蛋白质。cd94/nkg2c在细胞表面上的高效表达需要dap12的存在,并且dap12和nkg2c跨膜结构域中的带电氨基酸对这种相互作用进行介导。本文提供了一种用于获得通过对ipsc进行基因工程化来单独地稳定表达nkg2c或与dap12一起稳定表达的效应细胞以向ipsc引入nkg2c以及任选地dap12,并且然后通过定向ipsc分化得到包含nk细胞和t细胞的效应细胞的策略。在一些实施例中,nkg2c进一步与cd94共表达。在本申请之前,尚不清楚在ipsc中过表达nkg2c是否会损害ipsc的分化潜能或生物学,或者在衍生nk细胞中过表达nkg2c是否会赋予记忆细胞(或通常作为nk细胞)的表型和/或功能。也不清楚转基因nkg2c能够与内源性cd94和dap12配对以在细胞表面上形成稳定的结构。
在包括过表达的nkg2c的ipsc或衍生自其的效应细胞中,所述细胞进一步包括过表达的cd94和/或dap12。在一个实施例中,nkg2c和cd94在单独的构建体中表达。在另一个实施例中,nkg2c和cd94在双顺反子构建体中共表达并通过自切割2a编码序列进行连接。如此,在双顺反子构建体中,nkg2c和cd94位于单一开放阅读框(orf)中。在另一个实施例中,nkg2c和dap12在单独的构建体中表达。
2.hncd16敲入
cd16已鉴别为两种异构体:fc受体fcγriiia(cd16a;nm_000569.6)和fcγriiib(cd16b;nm_000570.4)。cd16a是由nk细胞表达的跨膜蛋白,其结合附接到靶细胞的单体igg以激活nk细胞和促进抗体依赖性细胞介导的细胞毒性(adcc)。cd16b仅由人类嗜中性粒细胞表达。如本文所用,“高亲和力cd16”、“不可切割的cd16”或“高亲和力不可切割的cd16”是指各种cd16变体。野生型cd16具有低亲和力并且经历胞外结构域脱落,这是一种蛋白分解切割过程,其在nk细胞激活后调控白细胞上的多种细胞表面分子的细胞表面密度。f176v(在一些公开案中也被称为f158v)是具有高亲和力的例示性cd16多态变体;然而s197p变体是基因工程化cd16的不可切割型式的实例。包含f176v和s197p两者的工程化cd16变体具有高亲和力,并且不可切割,其更详细地描述于wo2015/148926中,并且其完整公开内容以引入的方式并入本文中。另外,cd16的胞外结构域基本上被至少一部分cd64胞外结构域置换的嵌合cd16受体也可实现能够进行adcc的cd16受体的所期望的高亲和力和不可切割特点。在一些实施例中,嵌合cd16的置换胞外结构域包含以下中的一种或多种:cd64的ec1、ec2和ec3外显子(uniprotkb_p12314或其异构体或多态变体)。
因此,高亲和力不可切割的cd16受体(hncd16)在一些实施例中包含f176v和s197p;并且在一些实施例中包含f176v,并且消除了切割区域。在一些其它实施例中,在与各自包括至少一部分cd64胞外结构域的示例性序列seqidno:1-3中的任一个相比时,hncd16包含一致性为至少50%、55%、60%、65%、70%、75%、80%、85%、90%、95%、99%、100%或其间任何百分比的序列。seqidno.1-3通过例示seqidno.4-6分别编码。如本文和整个本申请中所用,考虑需要引入以对两个序列进行最佳比对的间隙数目和每个空隙的长度,两个序列之间的一致性百分比是序列共用的一致位置数目的函数(即,一致性%=一致位置数/位置总数×100)。序列的比较和两个序列之间一致性百分比的确定可以使用所属领域中公认的数学算法实现。
seqidno.1:
mwflttlllwvpvdgqvdttkavitlqppwvsvfqeetvtlhcevlhlpgssstqwflngtatqtstpsyritsasvndsgeyrcqrglsgrsdpiqleihrgwlllqvssrvftegeplalrchawkdklvynvlyyrngkafkffhwnsnltilktnishngtyhcsgmgkhrytsagisvtvkelfpapvlnasvtspllegnlvtlscetklllqrpglqlyfsfymgsktlrgrntsseyqiltarredsglywceaatedgnvlkrspelelqvlglqlptpvwfhyqvsfclvmvllfavdtglyfsvktnirsstrdwkdhkfkwrkdpqdk
(340个氨基酸基于cd64结构域的构造;cd16tm;cd16icd)
seqidno.2
mwflttlllwvpvdgqvdttkavitlqppwvsvfqeetvtlhcevlhlpgssstqwflngtatqtstpsyritsasvndsgeyrcqrglsgrsdpiqleihrgwlllqvssrvftegeplalrchawkdklvynvlyyrngkafkffhwnsnltilktnishngtyhcsgmgkhrytsagisvtvkelfpapvlnasvtspllegnlvtlscetklllqrpglqlyfsfymgsktlrgrntsseyqiltarredsglywceaatedgnvlkrspelelqvlglffppgyqvsfclvmvllfavdtglyfsvktnirsstrdwkdhkfkwrkdpqdk
(336个氨基酸基于cd64外显子的构造;cd16tm;cd16icd)
seqidno.3
mwflttlllwvpvdgqvdttkavitlqppwvsvfqeetvtlhcevlhlpgssstqwflngtatqtstpsyritsasvndsgeyrcqrglsgrsdpiqleihrgwlllqvssrvftegeplalrchawkdklvynvlyyrngkafkffhwnsnltilktnishngtyhcsgmgkhrytsagisvtvkelfpapvlnasvtspllegnlvtlscetklllqrpglqlyfsfymgsktlrgrntsseyqiltarredsglywceaatedgnvlkrspelelqvlgffppgyqvsfclvmvllfavdtglyfsvktnirsstrdwkdhkfkwrkdpqdk
(335个氨基酸基于cd64外显子的构造;cd16tm;cd16icd)
seqidno.4
seqidno.5
seqidno.6
因此,本文提供克隆ipsc,其经过基因工程化以在如本文所涵盖和描述的其它编辑中包含高亲和力不可切割的cd16受体(hncd16),其中基因工程化ipsc能够分化成包含引入ipsc中的hncd16的效应细胞。在一些实施例中,包含hncd16的衍生效应细胞是nk细胞。在一些实施例中,包含hncd16的衍生效应细胞是t细胞。在ipsc或其衍生细胞中表达的外源性hncd16在不仅结合于adcc抗体或其片段,而且结合于识别所述hncd16的cd16或cd64胞外结合性结构域的双特异性、三特异性或多特异性衔接子或结合子中具有高亲和力。双特异性、三特异性或多特异性衔接子或结合子在以下本申请中进一步描述(参见i.6部分)。因此,本申请提供衍生效应细胞或其细胞群,其通过与在衍生效应细胞上表达的hncd16的胞外结构域的高亲和力结合,以对于治疗如以下v部分中进一步详述的病况、疾病或感染的治疗用途足够的量预负载有一种或多种预选adcc抗体,其中所述hncd16包含cd64或具有f176v和s197p的cd16的胞外结合性结构域。
在一些其它实施例中,进一步修饰或置换hncd16的原生cd16跨膜结构域和/或胞内结构域,以使得产生嵌合fc受体(cfcr)以包含非天然跨膜结构域、非天然刺激性结构域和/或非天然信号传导结构域。本文所用的术语“非天然”意指除提供胞外结构域的受体外,跨膜结构域、刺激性结构域或信号传导结构域源自不同受体。在本文的说明中,基于cd16或其变体的cfcr不具有源自cd16的跨膜结构域、刺激性结构域或信号传导结构域。在一些实施例中,基于外源性hncd16的cfcr包含源自以下的非天然跨膜结构域:cd3d、cd3e、cd3g、cd3ζ、cd4、cd8、cd8a、cd8b、cd27、cd28、cd40、cd84、cd166、4-1bb、ox40、icos、icam-1、ctla-4、pd-1、lag-3、2b4、btla、cd16、il7、il12、il15、kir2dl4、kir2ds1、nkp30、nkp44、nkp46、nkg2c、nkg2d、t细胞受体多肽。在一些实施例中,基于外源性hncd16的cfcr包含源自以下的非天然刺激性/抑制性结构域:cd27、cd28、4-1bb、ox40、icos、pd-1、lag-3、2b4、btla、dap10、dap12、ctla-4或nkg2d多肽。在一些实施例中,基于外源性hncd16的cfcr包含源自以下的非天然信号传导结构域:cd3ζ、2b4、dap10、dap12、dnam1、cd137(41bb)、il21、il7、il12、il15、nkp30、nkp44、nkp46、nkg2c或nkg2d多肽。在hncd16的一个实施例中,所提供的嵌合受体包含源自il7、il12、il15、nkp30、nkp44、nkp46、nkg2c和nkg2d多肽中的一种的跨膜结构域和信号传导结构域两者。基于hncd16的嵌合fc受体的一个特定实施例包含nkg2d的跨膜结构域、2b4的刺激性结构域和cd3ζ的信号传导结构域;其中hncd16的胞外结构域源自cd64或cd16的胞外结构域的全长或部分序列,其中cd16的胞外结构域包含f176v和s197p。基于hncd16的嵌合fc受体的另一个实施例包含cd3ζ的跨膜结构域和信号传导结构域;其中hncd16的胞外结构域源自cd64或cd16的胞外结构域的全长或部分序列,其中cd16的胞外结构域包含f176v和s197p。
如上所述的基于hncd16的嵌合fc受体的各种实施例能够以高亲和力结合到抗体或其片段的fc区;或者结合到双特异性、三特异性或多特异性衔接子或结合子的fc区。结合后,嵌合受体的刺激性结构域和/或信号传导结构域实现效应细胞的激活和细胞因子分泌,并且杀死抗体或具有肿瘤抗原结合性组分以及fc区的所述双特异性、三特异性或多特异性衔接子或结合子靶向的肿瘤细胞。在不受理论限制的情况下,通过非天然跨膜结构域、刺激性结构域和/或信号传导结构域,或通过结合于基于hncd16的嵌合fc受体的胞外结构域的衔接子,cfcr可有助于效应细胞的杀伤能力,同时提高效应细胞的增殖和/或扩增潜能。抗体和衔接子可使表达抗原的肿瘤细胞和表达cfcr的效应细胞紧密接近,这也有助于增强肿瘤细胞的杀伤。双特异性、三特异性、多特异性衔接子或结合子的示例性肿瘤抗原包括但不限于b7h3、bcma、cd10、cd19、cd20、cd22、cd24、cd30、cd33、cd34、cd38、cd44、cd79a、cd79b、cd123、cd138、cd179b、cea、clec12a、cs-1、dll3、egfr、egfrviii、epcam、flt-3、folr1、folr3、gd2、gpa33、her2、hm1.24、lgr5、msln、mcsp、mica/b、psma、pama、p-钙粘素和ror1。适于在攻击肿瘤细胞时接合表达基于hncd16的cfcr的效应细胞的一些非限制性例示性双特异性、三特异性、多特异性衔接子或结合子包括cd16(或cd64)-cd30、cd16(或cd64)-bcma、cd16(或cd64)-il15-epcam和cd16(或cd64)-il15-cd33。
不同于nk细胞激活之后从细胞表面切割的原代nk细胞表达的内源性cd16受体,衍生nk中cd16的不可切割型式避免cd16脱落,并且维持恒定表达。在衍生nk细胞中,不可切割的cd16增加tnfα和cd107a的表达,表明细胞功能得到改善。不可切割的cd16还增强了抗体依赖性细胞介导的细胞毒性(adcc)以及双特异性、三特异性或多特异性衔接子的接合。adcc是通过将cd16结合到抗体涂布的靶细胞的nk细胞介导的切割的机制。在向需要细胞疗法的受试者施用细胞之前,衍生nk细胞中引入的hncd16的另外高亲和力特性也允许通过hncd16将adcc抗体体外负载到nk细胞。如所提供,hncd16可在一些实施例中包含f176v和s197p,或可包含源自如由seqidno:1、2或3所例示的cd64的全部或部分胞外结构域,或可进一步包含非天然跨膜结构域、刺激性结构域和信号传导结构域中的至少一种。如所公开,本申请还提供衍生nk细胞或其细胞群,其以对于治疗如以下v部分中进一步详述的病况、疾病或感染的治疗用途足够的量预负载有一种或多种预选adcc抗体。
不同于原代nk细胞,来自原代来源(即,自然/原生来源,例如外周血、脐带血或其它供体组织)的成熟t细胞不表达cd16。出人意料的,包含所表达的外源性不可切割的cd16的ipsc不损害t细胞发育生物学,并且能够分化成功能衍生t细胞,其不仅表达外源性cd16,而且能够通过所获得adcc机制执行功能。衍生t细胞中这一所获adcc可另外用作双靶向和/或挽救伴随car-t细胞疗法常出现的抗原逃逸的方法,其中肿瘤随着靶向car-t的抗原表达或突变抗原表达减少或损失以避免被car(嵌合抗原受体)识别而复发。当所述衍生t细胞通过外源性cd16表达包含所获adcc时,并且当抗体靶向与car靶向的抗原不同的肿瘤抗原时,抗体可用于挽救car-t抗原逃逸并且减少或防止car-t治疗中常见的靶向肿瘤的复发或再现。减少和/或防止抗原逃逸同时实现双靶向的这一策略同样适用于表达一种或多种car的nk细胞。以下进一步叙述可用于这一抗原逃逸减少和防止策略的各种car。
因此,本发明提供包含外源性cd16的衍生t细胞。在一些实施例中,衍生t细胞中包含的hncd16包含f176v和s197p。在一些其它实施例中,衍生t细胞中包含的hncd16包含源自如由seqidno:1、2或3所例示的cd64的全部或部分胞外结构域,或可进一步包含非天然跨膜结构域、刺激性结构域和信号传导结构域中的至少一种。如所解释,这类衍生t细胞具有获得性机制以用由adcc介导的单克隆抗体靶向肿瘤,从而增强抗体的治疗效果。如所公开,本申请还提供衍生t细胞或其细胞群,其以对于治疗如以下v部分中进一步详述的病况、疾病或感染的治疗用途足够的量预负载有一种或多种预选adcc抗体。
3.car表达
适用于基因工程化ipsc和其衍生效应细胞的可以是所属领域中已知的任何car设计。嵌合抗原受体car是融合蛋白,其一般包括包含抗原识别区的胞外结构域、跨膜结构域和内域。在一些实施例中,胞外结构域还可包括信号肽或前导序列和/或间隔子。在一些实施例中,内域可进一步包含信号传导肽,其激活表达car的效应细胞。在一些实施例中,抗原识别结构域可特异性结合抗原。在一些实施例中,抗原识别结构域可特异性结合与疾病或病原体相关的抗原。在一些实施例中,疾病相关的抗原是肿瘤抗原,其中肿瘤可以是液体或实体瘤。在一些实施例中,car适于激活表达所述car的t细胞或nk细胞。在一些实施例中,car是对包含nk特异性信号传导组分具有特异性的nk细胞。在某些实施例中,所述t细胞衍生自表达car的ipsc,并且衍生t细胞可包含t辅助细胞、细胞毒性t细胞、记忆t细胞、调控t细胞、自然杀伤t细胞、αβt细胞、γδt细胞或其组合。在某些实施例中,所述nk细胞衍生自表达car的ipsc。
在某些实施例中,所述抗原识别区包含鼠类抗体、人类抗体、人源化抗体、骆驼ig、只有重链的鲨鱼抗体(vnar)、ignar、嵌合抗体、重组抗体或其抗体片段。抗体片段的非限制性实例包括fab、fab′、f(ab)′2、f(ab)′3、fv、单链抗原结合性片段(scfv)、(scfv)2、二硫键稳定的fv(dsfv)、微型抗体、双功能抗体、三功能抗体、四功能抗体、单域抗原结合性片段(sdab,纳米抗体(nanobody))、只有重链的重组抗体(vhh)和维持全部抗体的结合特异性的其它抗体片段。可由car靶向的抗原的非限制性实例包括adgre2、碳酸酐酶ix(calx)、ccri、ccr4、癌胚抗原(cea)、cd3、cd5、cd7、cd8、cd10、cd19、cd20、cd22、cd30、cd33、cd34、cd38、cd41、cd44、cd44v6、cd49f、cd56、cd70、cd74、cd99、cd123、cd133、cd138、cd269(bcma)、cds、clec12a、巨细胞病毒(cmv)感染的细胞的抗原(例如,细胞表面抗原)、上皮糖蛋白2(egp2)、上皮糖蛋白-40(egp-40)、上皮细胞粘附分子(epcam)、egfrviii、受体酪氨酸-蛋白激酶erb-b2,3,4、egfir、egfr-viii、erbb叶酸结合性蛋白(fbp)、胎儿型乙酰胆碱受体(achr)、叶酸受体a、神经节苷脂g2(gd2)、神经节苷脂g3(gd3)、人类表皮生长因子受体2(her-2)、人类端粒酶逆转录酶(htert)、icam-1、整合素b7、白细胞介素-13受体亚基α-2(il-13rα2)、κ-轻链、激酶插入结构域受体(kdr)、lewisa(ca19.9)、lewisy(ley)、l1细胞粘附分子(l1-cam)、lilrb2、黑色素瘤抗原家族a1(mage-a1)、mica/b、粘蛋白1(muc-1)、粘蛋白16(muc-16)、间皮素(msln)、nkcsi、nkg2d配体、c-met、癌症-睾丸抗原ny-eso-1、癌胚抗原(h5t4)、prame、前列腺干细胞抗原(psca)、prame前列腺特异性膜抗原(psma)、肿瘤相关糖蛋白72(tag-72)、tim-3、trbci、trbc2、血管内皮生长因子r2(vegf-r2)、威尔姆斯肿瘤蛋白(wt-1)和所属领域中已知的各种病原体抗原。病原体的非限制性实例包括能够引起疾病的病毒、细菌、真菌、寄生虫和原虫。
在一些实施例中,car的跨膜结构域包含cd3d、cd3e、cd3g、cd3ζ、cd4、cd8、cd8a、cd8b、cd27、cd28、cd40、cd84、cd166、4-1bb、ox40、icos、icam-1、ctla-4、pd-1、lag-3、2b4、btla、cd16、il7、il12、il15、kir2dl4、kir2ds1、nkp30、nkp44、nkp46、nkg2c、nkg2d、t细胞受体多肽的原生或修饰的跨膜区的全长或至少一部分。
在一些实施例中,内域(或胞内结构域)的信号传导肽包含cd3ζ、2b4、dap10、dap12、dnam1、cd137(41bb)、il21、il7、il12、il15、nkp30、nkp44、nkp46、nkg2c或nkg2d的多肽的全长或至少一部分。在一个实施例中,car的信号传导肽包含与cd3ζ的至少一种基于免疫受体酪氨酸的激活基序(immunoreceptortyrosine-basedactivationmotif;itam)有至少约85%、约90%、约95%、约96%、约97%、约98%或约99%一致性的氨基酸序列。
在某些实施例中,所述内域进一步包含至少一个共刺激信号传导区。所述共刺激信号传导区可包含cd27、cd28、4-1bb、ox40、icos、pd-1、lag-3、2b4、btla、dap10、dap12、ctla-4或nkg2d或其任何组合的多肽的全长或至少一部分。在一个实施例中,适用于本申请中提供的细胞的car包含源自cd28的共刺激性结构域和包括天然或修饰的cd3ζ的itam1的信号传导结构域,所述cd3ζ由与seqidno:7至少约85%、约90%、约95%、约96%、约97%、约98%或约99%一致性的氨基酸序列表示。在另一个实施例中,包含源自cd28和cd3ζ的天然或修饰的itam1的共刺激性结构域的car也包含源自cd28的铰链结构域和跨膜结构域,其中scfv可通过铰链连接到跨膜结构域,并且car包含与seqidno:8至少约85%、约90%、约95%、约96%、约97%、约98%或约99%一致性的氨基酸序列。
seqidno:7
rskrsrllhsdymnmtprrpgptrkhyqpyapprdfaayrsrvkfsrsadapayqqgqnqlynelnlgrreeydvldkrrgrdpemggkprrknpqeglfnelqkdkmaeafseigmkgerrrgkghdglfqglstatkdtfdalhmqalppr
(153个氨基酸的cd28co-stim+cd3ζitam)
seqidno:8
ievmypppyldneksngtiihvkgkhlcpsplfpgpskpfwvlvvvggvlacysllvtvafiifwvrskrsrllhsdymnmtprrpgptrkhyqpyapprdfaayrsrvkfsrsadapayqqgqnqlynelnlgrreeydvldkrrgrdpemggkprrknpqeglfnelqkdkmaeafseigmkgerrrgkghdglfqglstatkdtfdalhmqalppr
(219个氨基酸的cd28铰链+cd28tm+cd28共刺激+cd3ζitam)
在另一个实施例中,适用于本申请中提供的细胞的car包含源自nkg2d的跨膜结构域、源自2b4的共刺激性结构域和包含天然或修饰的cd3ζ的信号传导结构域,所述cd3ζ由与seqidno:9至少约85%、约90%、约95%、约96%、约97%、约98%或约99%一致性的氨基酸序列表示。包含源自nkg2d的跨膜结构域、源自2b4的共刺激性结构域和包含天然或修饰的cd3ζ的信号传导结构域的所述car可进一步包含cd8铰链,其中这类结构的氨基酸序列具有与seqidno:10至少约85%、约90%、约95%、约96%、约97%、约98%或约99%一致性。
seqidno:9
snlfvaswiavmiifrigmavaifccfffpswrrkrkekqsetspkefltiyedvkdlktrrnheqeqtfpgggstiysmiqsqssaptsqepaytlysliqpsrksgsrkrnhspsfnstiyevigksqpkaqnparlsrkelenfdvysrvkfsrsadapaykqgqnqlynelnlgrreeydvldkrrgrdpemggkprrknpqeglynelqkdkmaeayseigmkgerrrgkghdglyqglstatkdtydalhmqalppr
(263个氨基酸nkg2dtm+2b4+cd3ζ)
seqidno:10
tttpaprpptpaptiasqplslrpeacrpaaggavhtrgldfacdsnlfvaswiavmiifrigmavaifccfffpswrrkrkekqsetspkefltiyedvkdlktrrnheqeqtfpgggstiysmiqsqssaptsqepaytlysliqpsrksgsrkrnhspsfnstiyevigksqpkaqnparlsrkelenfdvysrvkfsrsadapaykqgqnqlynelnlgrreeydvldkrrgrdpemggkprrknpqeglynelqkdkmaeayseigmkgerrrgkghdglyqglstatkdtydalhmqalppr
(308个氨基酸cd8铰链+nkg2dtm+2b4+cd3ζ)
非限制性car策略进一步包括:异源二聚体,其通过使一对胞内结构域二聚化而有条件地激活car(参见例如,美国专利第9587020号);分离car,其中同源重组抗原结合、铰链和内域以产生car(参见例如,美国公开案第20170183407号);多链car,其允许分别连接到抗原结合性结构域和信号传导结构域的两个跨膜结构域之间的非共价连接(参见例如,美国公开案第20140134142号);car,其具有双特异性抗原结合性结构域(参见例如,美国专利第9447194号),或具有识别相同或不同抗原或抗原决定基的一对抗原结合性结构域(参见例如,美国专利第8409577号),或串联car(参见例如,hegde等人,《临床研究杂志(jclininvest.)》2016;126(8):3036-3052);诱导性car(参见例如,美国公开案第20160046700号、第20160058857号、第20170166877号);可切换的car(参见例如,美国公开案第20140219975号);和所属领域中已知的任何其它设计。
因此本文所提供的包括获自分化基因组工程化ipsc的衍生细胞,其中ipsc和衍生细胞两者包含一种或多种car以及另外的修饰模式,包括但不限于外源性hncd16的表达。在一个特定实施例中,ipsc和其衍生细胞包含hncd16以及靶向所选肿瘤或病毒抗原的car,其中衍生细胞是nk细胞或t细胞,并且其中衍生细胞可通过hncd16结合与一种或多种adcc抗体或双特异性、三特异性或多特异性衔接子一起使用,所述衔接子靶向与car靶向的抗原不同的肿瘤抗原以避免或减少肿瘤抗原逃逸同时实现相同肿瘤的双靶向。在另一个实施例中,包含car的ipsc和其衍生t细胞具有插入于tcr恒定区的car,引起tcr敲除,并且将car表达置于内源性tcr启动子的控制下。在一些实施例中,衍生自工程化ipsc的衍生tcr剔除型car-t细胞进一步包含具有对于cd16原生的(f176v和/或s197p)或源自cd64的胞外结构域和原生或非天然跨膜结构域、刺激性结构域和信号传导结构域的hncd16。在另一个实施例中,包含car的ipsc和其衍生nk细胞具有插入于nkg2a基因座或nkg2d基因座中的car,引起nkg2a或nkg2d敲除,并且将car置于内源性nkg2a或nkg2d启动子的控制下。
4.外源引入的细胞因子和/或细胞因子信号传导
通过避免全身性高剂量施用临床上相关细胞因子,由于这类实践的剂量限制性毒性的风险降低,同时建立细胞因子介导的细胞自主性。为了实现淋巴细胞自主性而不需要另外施用可溶性细胞因子,将il2、il4、il6、il7、il9、il10、il11、il12、il15、il18、il21和/或其相应受体中的一种或多种的部分或全部肽引入细胞中以在有或无表达细胞因子本身的情况下允许细胞因子信号传导,从而维持或改善细胞生长、增殖、扩增和/或效应功能,并且降低细胞因子毒性的风险。在一些实施例中,在细胞表面上表达用于细胞因子信号传导的所引入细胞因子和/或其相应原生或修饰的受体。在一些实施例中,组成性地激活细胞因子信号传导。在一些实施例中,细胞因子信号传导的激活是可诱导的。在一些实施例中,细胞因子信号传导的激活是瞬时的和/或暂时的。
图1呈现使用il15作为说明性实例的几种构建体设计。图1中的设计中的任一个的跨膜(tm)结构域对于il15受体可以是天然的,或可用任何其它结合膜蛋白的跨膜结构域修饰或置换。
设计1:il15和il15rα通过使用自切割肽共表达,模拟il15的反式呈递而不消除il15的顺式呈递。
设计2:il15rα通过接头在c端与il15融合,模拟反式呈递而不消除il15的顺式呈递并且确保il15膜结合。重组蛋白包含与seqidno:11至少约85%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%一致的氨基酸序列,并且重组蛋白在信号肽下游包含il15肽原。seqidno:12描述编码seqidno:11的氨基酸序列的例示性dna序列。
seqidno:11
mdwtwilflvaaatrvhsgihvfilgcfsaglpkteanwvnvisdlkkiedliqsmhidatlytesdvhpsckvtamkcfllelqvislesgdasihdtvenliilannslssngnvtesgckeceeleeknikeflqsfvhivqmfintssgggsggggsggggsggggsgggslqitcpppmsvehadiwvksyslysreryicnsgfkrkagtssltecvlnkatnvahwttpslkcirdpalvhqrpappstvttagvtpqpeslspsgkepaasspssnntaattaaivpgsqlmpskspstgtteisshesshgtpsqttaknweltasashqppgvypqghsdttvaiststvllcglsavsllacylksrqtpplasvemeamealpvtwgtssrdedlencshhl
(414个氨基酸)
seqidno:12
atggactggacctggattctgttcctggtcgcggctgcaacgcgagtccatagcggtatccatgtttttattcttgggtgtttttctgctgggctgcctaagaccgaggccaactgggtaaatgtcatcagtgacctcaagaaaatagaagaccttatacaaagcatgcacattgatgctactctctacactgagtcagatgtacatccctcatgcaaagtgacggccatgaaatgtttcctcctcgaacttcaagtcatatctctggaaagtggcgacgcgtccatccacgacacggtcgaaaacctgataatactcgctaataatagtctctcttcaaatggtaacgtaaccgagtcaggttgcaaagagtgcgaagagttggaagaaaaaaacataaaggagttcctgcaaagtttcgtgcacattgtgcagatgttcattaatacctctagcggcggaggatcaggtggcggtggaagcggaggtggaggctccggtggaggaggtagtggcggaggttctcttcaaataacttgtcctccaccgatgtccgtagaacatgcggatatttgggtaaaatcctatagcttgtacagccgagagcggtatatctgcaacagcggcttcaagcggaaggccggcacaagcagcctgaccgagtgcgtgctgaacaaggccaccaacgtggcccactggaccacccctagcctgaagtgcatcagagatcccgccctggtgcatcagcggcctgcccctccaagcacagtgacaacagctggcgtgaccccccagcctgagagcctgagcccttctggaaaagagcctgccgccagcagccccagcagcaacaatactgccgccaccacagccgccatcgtgcctggatctcagctgatgcccagcaagagccctagcaccggcaccaccgagatcagcagccacgagtctagccacggcaccccatctcagaccaccgccaagaactgggagctgacagccagcgcctctcaccagcctccaggcgtgtaccctcagggccacagcgataccacagtggccatcagcacctccaccgtgctgctgtgtggactgagcgccgtgtcactgctggcctgctacctgaagtccagacagacccctccactggccagcgtggaaatggaagccatggaagcactgcccgtgacctggggcaccagctccagagatgaggatctggaaaactgctcccaccacctg
(1242个核酸)
设计3:具有截短胞内结构域的il15rα通过接头在c端与il15融合,模拟il15的反式呈递,维持il15膜结合,并且另外消除潜在顺式呈递。这类构建体包含与seqidno:13至少75%、80%、85%、90%、95%或99%一致性的氨基酸序列,其可由seqidno:14表示的例示性核酸序列编码。
seqidno:13
mdwtwilflvaaatrvhsgihvfilgcfsaglpkteanwvnvisdlkkiedliqsmhidatlytesdvhpsckvtamkcfllelqvislesgdasihdtvenliilannslssngnvtesgckeceeleeknikeflqsfvhivqmfintssgggsggggsggggsggggsgggslqitcpppmsvehadiwvksyslysreryicnsgfkrkagtssltecvlnkatnvahwttpslkcirdpalvhqrpappstvttagvtpqpeslspsgkepaasspssnntaattaaivpgsqlmpskspstgtteisshesshgtpsqttaknweltasashqppgvypqghsdttvaiststvllcglsavsllacylksrq
(379个氨基酸;信号传导和接头肽带下划线)
seqidno:14
atggactggacctggattctgttcctggtcgcggctgcaacgcgagtccatagcggtatccatgtttttattcttgggtgtttttctgctgggctgcctaagaccgaggccaactgggtaaatgtcatcagtgacctcaagaaaatagaagaccttatacaaagcatgcacattgatgctactctctacactgagtcagatgtacatccctcatgcaaagtgacggccatgaaatgtttcctcctcgaacttcaagtcatatctctggaaagtggcgacgcgtccatccacgacacggtcgaaaacctgataatactcgctaataatagtctctcttcaaatggtaacgtaaccgagtcaggttgcaaagagtgcgaagagttggaagaaaaaaacataaaggagttcctgcaaagtttcgtgcacattgtgcagatgttcattaatacctctagcggcggaggatcaggtggcggtggaagcggaggtggaggctccggtggaggaggtagtggcggaggttctcttcaaataacttgtcctccaccgatgtccgtagaacatgcggatatttgggtaaaatcctatagcttgtacagccgagagcggtatatctgcaacagcggcttcaagcggaaggccggcacaagcagcctgaccgagtgcgtgctgaacaaggccaccaacgtggcccactggaccacccctagcctgaagtgcatcagagatcccgccctggtgcatcagcggcctgcccctccaagcacagtgacaacagctggcgtgaccccccagcctgagagcctgagcccttctggaaaagagcctgccgccagcagccccagcagcaacaatactgccgccaccacagccgccatcgtgcctggatctcagctgatgcccagcaagagccctagcaccggcaccaccgagatcagcagccacgagtctagccacggcaccccatctcagaccaccgccaagaactgggagctgacagccagcgcctctcaccagcctccaggcgtgtaccctcagggccacagcgataccacagtggccatcagcacctccaccgtgctgctgtgtggactgagcgccgtgtcactgctggcctgctacctgaagtccagacagtga
(1140个核酸)
所属领域的技术人员将理解,上述信号肽和接头序列是说明性的,并且绝不限制适用作信号肽或接头的其变体。存在许多所属领域的技术人员已知和可用的合适信号肽或接头序列。所属领域的普通技术人员理解,信号肽和/或接头序列可以取代另一序列而不改变由信号肽引导或由接头连接的功能肽的活性。
设计4:因为设计3构建体展示在促进效应细胞存活和扩增中具有功能,证明il15rα的细胞质结构域可省略而不会对这类设计中配备有il15的效应细胞的自主构件产生负面影响,设计4是提供设计3的另一起作用的替代方案的构建体,除sushi结构域以外,基本上完整il15rα从所述设计3中去除,在一端与il15融合,并且在另一端与跨膜结构域融合(mb-sushi),任选地利用sushi结构域与跨膜结构域之间的接头。融合il5/mb-sushi通过任何结合膜蛋白的跨膜结构域在细胞表面上表达。在例如设计4的构建体的情况下,在只保留所期望的il15的反式呈递时,消除通过il15rα的不必要的信号传导,包括顺式呈递。在一些实施例中,包含与sushi结构域融合的il15的组分包含与seqidno:15至少75%、80%、85%、90%、95%或99%一致性的氨基酸序列,其可由seqidno:16表示的例示性核酸序列编码。
seqidno:15
mdwtwilflvaaatrvhsgihvfilgcfsaglpkteanwvnvisdlkkiedliqsmhidatlytesdvhpsckvtamkcfllelqvislesgdasihdtvenliilannslssngnvtesgckeceeleeknikeflqsfvhivqmfintssgggsggggsggggsggggsgggslqitcpppmsvehadiwvksyslysreryicnsgfkrkagtssltecvlnkatnvahwttpslkcir
(242个氨基酸;带信号和接头肽的带下划线)
seqidno:16
atggactggacctggattctgttcctggtcgcggctgcaacgcgagtccatagcggtatccatgtttttattcttgggtgtttttctgctgggctgcctaagaccgaggccaactgggtaaatgtcatcagtgacctcaagaaaatagaagaccttatacaaagcatgcacattgatgctactctctacactgagtcagatgtacatccctcatgcaaagtgacggccatgaaatgtttcctcctcgaacttcaagtcatatctctggaaagtggcgacgcgtccatccacgacacggtcgaaaacctgataatactcgctaataatagtctctcttcaaatggtaacgtaaccgagtcaggttgcaaagagtgcgaagagttggaagaaaaaaacataaaggagttcctgcaaagtttcgtgcacattgtgcagatgttcattaatacctctagcggcggaggatcaggtggcggtggaagcggaggtggaggctccggtggaggaggtagtggcggaggttctcttcaaataacttgtcctccaccgatgtccgtagaacatgcggatatttgggtaaaatcctatagcttgtacagccgagagcggtatatctgcaacagcggcttcaagcggaaggccggcacaagcagcctgaccgagtgcgtgctgaacaaggccaccaacgtggcccactggaccacccctagcctgaagtgcatcaga
(726个核酸)
所属领域的技术人员将理解,上述信号肽和接头序列是说明性的,并且绝不限制适用作信号肽或接头的其变体。存在许多所属领域的技术人员已知和可用的合适信号肽或接头序列。所属领域的普通技术人员理解,信号肽和/或接头序列可以取代另一序列而不改变由信号肽引导或由接头连接的功能肽的活性。
设计5:原生或修饰的il15rβ通过接头在c端与il15融合,实现组成性信号传导并且维持il15膜结合和反式重呈递。
设计6:原生或修饰的共同受体γc通过接头在c端与il15融合以用于细胞因子的组成性信号传导和结合膜的反式呈递。共同受体γc也被称为共同γ链或cd132,也称为il2受体亚基γ或il2rg。γc是细胞因子受体亚基,其与受体复合体共用以用于许多白细胞介素受体,包括但不限于il2、il4、il7、il9、il15和il21受体。
设计7:在缺乏il15的情况下形成同源二聚体的工程化il15rβ适用于产生细胞因子的组成性信号传导。
在一些实施例中,可使用图1中的设计中的一种或多种将细胞因子il2、il4、il6、il7、il9、il10、il11、il12、il15、il18和il21和/或其受体中的一种或多种引入ipsc中,并且在ipsc分化后引入其衍生细胞中。在一些实施例中,il2或il15细胞表面表达和信号传导是通过设计1-7中的任一种中所说明的构建体。在一些实施例中,il4、il7、il9或il21细胞表面表达和信号传导是通过设计5、6或7中所说明的构建体,通过使用共同受体或细胞因子特异性受体。图1中的设计中的任一种的跨膜(tm)结构域对于相应细胞因子受体可以是天然的,或可用任何其它结合膜蛋白的跨膜结构域修饰或置换。
在包含car和外源性细胞因子两者和/或细胞因子受体信号传导的ipsc和其衍生细胞中,car和il可在单独构建体中表达,或可在包含car和il两者的双顺反子构建体中共表达。在一些其它实施例中,呈图1中的构建体设计中的任一种表示的形式的il15可通过自切割2a编码序列连接到car表达构建体的5'端或3'端,所述自切割2a编码序列说明为例如car-2a-il15或il15-2a-car。如此,il15和car在单一开放阅读框(orf)中。在一个实施例中,car-2a-il15或il15-2a-car构建体在图1的设计3中包含il15。在另一个实施例中,car-2a-il15或il15-2a-car构建体在图1的设计3中包含il15。在又另一个实施例中,car-2a-il15或il15-2a-car构建体在图1的设计7中包含il15。当表达car-2a-il15或il15-2a-car时,自切割2a肽允许所表达的car和il15解离,并且然后可在细胞表面呈递解离的il15。car-2a-il15或il15-2a-car双顺反子设计在时间和数量上允许配位的car和il15表达,并且在可选择以并入例如诱导性启动子以表达单orf的相同控制机制下。自切割肽发现于小核糖核酸病毒科(picornaviridaevirusfamily)的成员中,包括口疮病毒属(aphthovirus),例如口蹄疫病毒(foot-and-mouthdiseasevirus;fmdv)、马鼻炎a病毒(equinerhinitisavirus;erav)、明脉扁刺蛾病毒(thoseaasignavirus;tav)和猪捷申病毒-1(porcineteschovirus-1;ptv-i)(donnelly,ml,等人,《普通病毒学期刊(j.gen.virol)》,82,1027-101(2001);ryan,md,等人,《普通病毒学期刊》,72,2727-2732(2001));和心病毒属(cardiovirus),例如泰勒病毒(theilovirus)(例如,泰勒鼠类脑脊髓炎)和脑心肌炎病毒。源自fmdv、erav、ptv-i和tav的2a肽有时也分别称为"f2a"、"e2a"、"p2a"和"t2a"。
也涵盖用于il15的如本文所公开的双顺反子car-2a-il15或il15-2a-car实施例以用于表达本文所提供的任何其它细胞因子,例如il2、il4、il6、il7、il9、il10、il11、il12、il18和il21。在一些实施例中,il2细胞表面表达和信号传导是通过设计1-7中的任一种中所说明的构建体。在一些实施例中,il4、il7、il9或il21细胞表面表达和信号传导通过设计5、6或7中所说明的构建体,通过使用共同受体和/或细胞因子特异性受体。
5.hla-i和hla-ii缺乏
必须在同种异体受体中匹配多种hlai类和ii类蛋白,以获得组织相容性,从而避免同种异体排斥反应问题。本文提供一种ipsc细胞系,其具有消除或实质上降低的hlai类和hlaii类蛋白的表达。hlai类缺乏可以通过使hlai类基因座(染色体6p21)的任何区域发生功能缺失或使hlai类相关基因(包括不限于β-2微球蛋白(b2m)基因、tap1基因、tap2基因和tap相关蛋白)缺失或表达水平降低来实现。举例来说,b2m基因编码所有hlai类异源二聚体的细胞表面表达所必要的共同亚单位。b2m剔除型细胞是hla-i缺乏的。hlaii类缺乏可以通过使hla-ii相关基因(包括不限于rfxank、ciita、rfx5和rfxap)发生功能缺失或降低来实现。ciita是转录共激活子,通过ii类蛋白表达所需的转录因子rfx5的激活起作用。ciita剔除型细胞是hla-ii缺乏的。本文提供剔除b2m和ciita两者的ipsc系和其衍生细胞,其中所得衍生效应细胞通过消除mhc(主要组织相容性复合体)匹配的需要允许同种异体细胞疗法,并且通过宿主(同种异体)t细胞避免识别和杀伤。
对于一些细胞类型,i类表达的缺乏引起nk细胞的切割。为解决这一“自我缺失”反应,hla-g可任选地敲入以避免nk细胞识别和杀伤衍生自工程化ipsc的hla-i和hla-ii缺乏的效应细胞。在一个实施例中,hla-i和hla-ii缺乏的ipsc和其衍生细胞进一步包含hncd16,以及任选的car和il中的一种或两种,而不会不利地影响ipsc的分化潜能和包括衍生t细胞和nk细胞的衍生效应细胞的功能。
6.本文提供的基因工程化ipsc系和衍生细胞
鉴于上文,本申请提供至少包括nkg2c过表达的ipsc、ips细胞系细胞或其衍生细胞,其中nkg2c可以与cd94和/或dap12共表达,其中衍生细胞是通过包括nkg2c以及任选地cd94和/或dap12的ipsc的分化获得的功能效应细胞。在一些实施例中,衍生细胞是造血细胞,包括但不限于具有永久性生血内皮细胞(he)潜能的中胚层细胞、永久性he、cd34造血细胞、造血干细胞和祖细胞、造血多能祖细胞(mpp)、t细胞祖细胞、nk细胞祖细胞、骨髓细胞、嗜中性粒细胞祖细胞、t细胞、nkt细胞、nk细胞、b细胞、嗜中性粒细胞、树突状细胞和巨噬细胞。在一些实施例中,功能衍生造血细胞包含效应细胞,例如t细胞、nk细胞和调控细胞。
在一些实施例中,包括至少nkg2c过表达的ipsc、ips细胞系细胞或其衍生细胞,其中所述nkg2c可以与cd94和/或dap12共表达,进一步包括hncd16和car中的一者或两者,由此通过trike(三特异性杀伤衔接子)、adcc抗体和/或car抗原结合来提供肿瘤多靶向策略。在一些实施例中,衍生细胞包括nk细胞或t细胞。可以通过使用设计为使nk细胞上的nkg2c和肿瘤上的抗原与il-15接头结合的trike来增强衍生nk细胞特异性以增强激活、增殖和存活率。均包括nkg2c、hncd16和car中的一种或多种的ipsc衍生nk或t细胞还可用于通过将抗体与car靶向治疗相结合来克服或减少仅在car-t疗法中观察到的与肿瘤抗原逃逸相关的肿瘤复发,前提是抗体和car对肿瘤的不同抗原具有特异性。进一步地,表达hncd16的衍生car-t细胞已获取adcc,除了car靶向外,还为肿瘤杀伤提供另外的机制。在一些实施例中,衍生细胞包括nk细胞。包含nkg2c以及hncd16和car之一或两者的ipsc衍生nk细胞具有增强的细胞毒性,在募集包含t细胞的旁观者细胞以浸润和杀死肿瘤细胞方面有效,并且能够预防或减少肿瘤逃逸和/或复发。
在一些实施例中,至少包括nkg2c过表达的ipsc、ips细胞系细胞或其衍生细胞,其中nkg2c可以与cd94和/或dap12共表达,进一步包括trike。在一些实施例中,表达的trike具有针对以下中的至少一种的肿瘤特异性:b7h3、bcma、cd10、cd19、cd20、cd22、cd24、cd30、cd33、cd34、cd38、cd44、cd79a、cd79b、cd123、cd138、cd179b、cea、clec12a、cs-1、dll3、egfr、egfrviii、epcam、flt-3、folr1、folr3、gd2、gpa33、her2、hm1.24、lgr5、msln、mcsp、mica/b、psma、pama、p-钙粘素和ror1。在一些实施例中,trike结合nkg2c。在一些实施例中,nkg2c结合性trike结合骨髓肿瘤上的cd33。在一些实施例中,nkg2c结合性trike包括il15接头。在一个实施例中,细胞表达的trike包括nkg2c-il15-cd33(“2c1533”)。对于表达包括il15的trike的ipsc或其衍生细胞,所述细胞可能不需要将外源性il15和/或il15受体引入细胞。如此,还提供了包括nkg2c-il15-cd33的ipsc或其衍生细胞的实施例,所述细胞不包括外源性il15和/或il15受体。在另一个实施例中,包括nkg2c-il15-cd33的ipsc或其衍生细胞进一步包括il2、il4、il6、il7、il9、il10、il11、il12、il15、il18和il21中的至少一种的外源性细胞因子和/或细胞因子受体。
另外提供了至少包括nkg2c过表达的ipsc、ips细胞系细胞或其衍生细胞,其中所述nkg2c可以与cd94和/或dap12共表达,可以进一步包括多核苷酸,所述多核苷酸编码至少一种外源性细胞因子和/或其受体(il),以实现细胞因子信号传导有助于细胞激活、存活率、持久性和/或扩增,其中所述ipsc系能够定向分化以产生具有改善的激活、存活率、持久性、扩增和效应细胞功能的功能衍生造血细胞。外源引入的细胞因子信号传导包含il2、il4、il6、il7、il9、il10、il11、il12、il15、il18和il21中的任何一种或两种或更多种的信号传导。在包括包含il15接头的nkg2c过表达和nkg2c结合性trike的ipsc、ips细胞系细胞或其衍生细胞中,一种或多种外源引入的细胞因子信号传导不一定是或不是il15。在一些实施例中,用于细胞因子信号传导的细胞因子和/或其相应受体的所引入部分或全部肽在细胞表面上表达。在一些实施例中,组成性地激活细胞因子信号传导。在一些实施例中,细胞因子信号传导的激活是可诱导的。在一些实施例中,细胞因子信号传导的激活是瞬时的和/或暂时的。在一些实施例中,细胞表面细胞因子/细胞因子受体的瞬时/暂时表达是通过逆转录病毒、仙台病毒、腺病毒、游离基因体、小环或包括mrna的rna。在一些实施例中,包括在nkg2c过表达的ipsc或其衍生细胞中的外源性细胞表面细胞因子和/或受体实现il7信号传导。在一些实施例中,包括在nkg2c过表达的ipsc或其衍生细胞中的外源性细胞表面细胞因子和/或受体实现il10信号传导。在一些实施例中,包括在nkg2c过表达的ipsc或其衍生细胞中的外源性细胞表面细胞因子和/或受体实现il15信号传导。上述实施例的nkg2c/ilipsc和其衍生细胞(无论il是单独表达,还是作为包括在细胞中的nkg2c结合性trike的一部分,还是与引入到细胞的car共表达)能够自主维持或改善细胞生长、增殖、扩增和/或效应功能,而无需在体外或体内接触另外供应的可溶性细胞因子。
还提供了包括过表达的nkg2c、cd94、dap12、bike、trike、hncd16、car、il、b2m敲除和/或ciita敲除的ipsc、ips细胞系细胞或其衍生细胞;以及任选地,编码hla-g的多核苷酸,其中ipsc能够定向分化以产生功能衍生造血细胞。在ipsc和其衍生nk或t细胞的一个实施例中,细胞包括b2m-/-ciita-/-等基因组编辑,并且均为hla-i和hla-ii缺乏的,其中ipsc和其衍生效应细胞具有改善的持久性和/或存活率。在一些实施例中,效应细胞在体内具有增加的存留和/或存活。
如此,本文提供的包含ipsc,所述ipsc包括表达的nkg2c以及任选地,以下中的一种、两种或三种或更多种:cd94、dap12、bike、trike、hncd16、car、外源性细胞因子/受体、b2m敲除和ciita敲除;其中当b2m被敲除时,任选地引入编码hla-g的多核苷酸,并且其中ipsc能够定向分化以产生功能衍生造血细胞。本申请中还包含功能ipsc衍生造血细胞,所述造血细胞包括过表达的nkg2c以及任选地,以下中的一种、两种或三种或更多种:cd94、dap12、bike、trike、hncd16、car、外源性细胞因子/受体、b2m敲除和ciita敲除;其中当b2m被敲除时,任选地引入编码hla-g的多核苷酸,并且其中衍生造血细胞包含但不限于具有永久性生血内皮细胞(he)潜能的中胚层细胞、永久性he、cd34造血细胞、造血干细胞和祖细胞、造血多能祖细胞(mpp)、t细胞祖细胞、nk细胞祖细胞、骨髓细胞、嗜中性粒细胞祖细胞、t细胞、nkt细胞、nk细胞、b细胞、嗜中性粒细胞、树突状细胞和巨噬细胞。
鉴于上述内容,本申请提供了ipsc和其功能衍生造血细胞,所述ipsc和其功能衍生造血细胞包括表1中的以下基因型中的任一种。如所提供,视选择哪种特异性细胞因子/受体表达而定,“il”表示il2、il4、il6、il7、il9、il10、il11、il12、il15、il18和il21中的一种。进一步地,“2c1533”代表nkg2c-il15-cd33trike。当ipsc和其功能衍生造血细胞具有包括nkg2c和cd94两者的基因型时,nkg2c和cd94包括在双顺反子表达盒中,所述双顺反子表达盒包括2a序列。相比之下,在一些其它实施例中,nkg2c和cd94位于包括在ipsc和其功能衍生造血细胞中的单独的表达盒中。在一些实施例中,其中ipsc和其功能衍生效应细胞表达2c1533和il两者,il不是il15。在一些其它实施例中,其中ipsc和其功能衍生效应细胞表达car和外源性il两者,il构建体包括在具有或与car分开的表达盒中。在一些实施例中,其中ipsc和其功能衍生效应细胞过表达nkg2c,所述细胞可以进一步包括过表达的cd94。在一些实施例中,其中ipsc和其功能衍生效应细胞包括b2m和ciita敲除,所述细胞可以进一步包括hla-g。
表1:提供的细胞的适用基因型:
7.另外修饰
在一些实施例中,包括表1中的基因型中的任一种的ipsc和其衍生效应细胞可以另外地包括tap1、tap2、tap相关蛋白、nlrc5、pd1、lag3、tim3、rfxank、rfx5、rfxap、染色体6p21区域中的任何基因中的至少一种的缺失或减少的表达;或hla-e、41bbl、cd3、cd4、cd8、cd47、cd113、cd131、cd137、cd80、pdl1、a2ar、tcr、fc受体、(双特异性、多特异性、或通用)衔接子和用于与衔接子偶联的表面触发性受体中至少一种的引入或增加的表达。
在一些实施例中,用于双特异性或多特异性衔接子的表面触发性受体对于效应细胞可以是内源的,有时视细胞类型而定。在一些其它实施例中,可使用本文所提供的方法和组合物将一种或多种外源性表面触发性受体引入效应细胞中,即通过另外工程化包含表1中所列的基因型的ipsc,然后将ipsc的分化引向t细胞、nk细胞或任何其它效应细胞,其包含相同基因型和表面触发性受体作为源ipsc。
双特异性或多特异性衔接子是由两个或更多个不同抗体的单链可变片段(scfv)组成的融合蛋白,其中至少一个scfv结合于效应细胞表面分子,并且至少另一个经由肿瘤特异性表面分子结合于肿瘤细胞。可用于双特异性或多特异性衔接子识别或偶联的例示性效应细胞表面分子或表面触发性受体包括但不限于cd3、cd28、cd5、cd16、nkg2d、cd64、cd32、cd89、nkg2c和如本文所公开的嵌合fc受体。在一些实施例中,在效应细胞的表面上表达的cd16可以用于衔接子识别。在一些实施例中,cd16是hncd16或其变体,包括cd16(含有f176v和任选地s197p)或cd64胞外结构域。在一些其它实施例中,如本文提供的过表达的nkg2c用于衔接子识别。在其它实施例中,基于nkg2c的嵌合fc受体(cfcr)用于衔接子识别,其中基于nkg2c的cfcr包括非天然跨膜结构域、刺激/抑制结构域和/或信号传导结构域。本文所用的术语“非天然”意指除提供胞外结构域的受体外,跨膜结构域、刺激性结构域或信号传导结构域源自不同受体。在一些实施例中,基于nkg2c的cfcr包括源自以下的非天然跨膜结构域:cd3d、cd3e、cd3g、cd3ζ、cd4、cd8、cd8a、cd8b、cd16、cd27、cd28、cd40、cd84、cd166、4-1bb、ox40、icos、icam-1、ctla-4、pd-1、lag-3、2b4、btla、cd16、il7、il12、il15、kir2dl4、kir2ds1、nkp30、nkp44、nkp46、nkg2d、t细胞受体多肽。在一些实施例中,基于nkg2c的cfcr包括源自以下的非天然刺激/抑制结构域:cd27、cd28、4-1bb、ox40、icos、pd-1、lag-3、2b4、btla、dap10、dap12、ctla-4或nkg2d多肽。在一些实施例中,基于nkg2c的cfcr包括源自以下的非天然信号传导结构域:cd3ζ、2b4、dap10、dap12、dnam1、cd137(41bb)、il21、il7、il12、il15、nkp30、nkp44、nkp46或nkg2d多肽。在基于nkg2c的cfcr的一个实施例中,所提供的嵌合受体包括两者均源自以下之一的跨膜结构域和信号传导结构域:il7、il12、il15、nkp30、nkp44、nkp46和nkg2d多肽。在一些实施例中,基于nkg2c的cfcr包括胞外结构域,所述胞外结构域源自nkg2c的胞外结构域、nkg2d的跨膜结构域、2b4的刺激性结构域和cd3ζ的信号传导结构域的全长或部分序列。用于双特异性或多特异性衔接子识别的示例性肿瘤细胞表面分子包括但不限于b7h3、bcma、cd10、cd19、cd20、cd22、cd24、cd30、cd33、cd34、cd38、cd44、cd79a、cd79b、cd123、cd138、cd179b、cea、clec12a、cs-1、dll3、egfr、egfrviii、epcam、flt-3、folr1、folr3、gd2、gpa33、her2、hm1.24、lgr5、msln、mcsp、mica/b、psma、pama、p-钙粘素、ror1。在一个实施例中,衔接子是接合hncd16或其变体的双特异性抗体,其中衔接子是cd16-cd30或cd64-cd30;cd16-bcma或cd64-bcma。在另一个实施例中,用于nkg2c识别的双特异性抗体或衔接子是nkg2c-cd33。在另一个实施例中,用于nkg2c识别的双特异性抗体或衔接子是nkg2c-cd30。在又另一个实施例中,双特异性抗体或衔接子包括位于效应细胞与肿瘤细胞抗原结合性结构域之间的接头,例如,作为效应nk细胞的接头(在一些出版物中被称为trike或三特异性杀伤衔接子)以促进效应细胞扩增的经修饰il15。在一个实施例中,trike是cd16-il15-epcam或cd64-il15-epcam。在另一个实施例中,trike是cd16-il15-cd33或cd64-il15-cd33。在又另一个实施例中,trike是nkg2c-il15-cd33。在包括nkg2c和任选的dap12的ipsc或其衍生细胞的另一个实施例中,细胞进一步包括cfcr,和任选的识别在细胞中表达的cfcr的bike或trike。
8.用于免疫疗法的抗体
在一些实施例中,除如本文所提供的基因组工程化效应细胞之外,包含靶向与病况、疾病或适应症相关的抗原的抗体或抗体片段的另外治疗剂可在组合疗法中与这些效应细胞一起使用。在一些实施例中,抗体是一种单克隆抗体。在一些实施例中,抗体是人源化抗体、人源化单克隆抗体或嵌合抗体。在一些实施例中,抗体或抗体片段特异性结合于病毒抗原。在其它实施例中,抗体或抗体片段特异性结合于肿瘤抗原。在一些实施例中,肿瘤或病毒特异性抗原激活所施用的ipsc衍生效应细胞以增强其杀伤能力。在一些实施例中,适用于作为另外治疗剂与所施用的ipsc衍生效应细胞的组合治疗的抗体包括但不限于抗cd20(利妥昔单抗、维妥珠单抗、奥法木单抗、乌布里图昔单抗、奥卡拉珠单抗、奥比珠单抗)、抗her2(曲妥珠单抗、帕妥珠单抗)、抗cd52(阿仑单抗)、抗egfr(西妥昔单抗)、抗gd2(迪努妥昔单抗)、抗pdl1(阿维鲁单抗)、抗cd38(达土木单抗、艾沙妥昔单抗、mor202)、抗cd123(7g3、csl362)、抗slamf7(埃罗妥珠单抗);和其人源化或fc修饰的变体或片段或其功能等效物和生物仿制药。在一些实施例中,ipsc衍生效应细胞包含造血谱系细胞,其包含表1中所列的基因型。在一些实施例中,ipsc衍生效应细胞包含nk细胞,其包含表1中列出的基因型。在一些实施例中,ipsc衍生效应细胞包含t细胞,其包含表1中所列的基因型。在适用于治疗液体或实体瘤的组合物的一些实施例中,组合物包含ipsc衍生nk细胞或t细胞,其包含hncd16和car以及具有与car不同的抗原特异性的抗体。在一些其它实施例中,包含于表达衍生nk细胞或t细胞的hncd16中的car靶向以下中的任一种:cd19、bcma、cd20、cd22、cd123、her2、cd52、egfr、gd2和pdl1;和细胞可以与靶向与car识别的抗原不同的抗原以减少或防止肿瘤抗原从car靶向逃逸的任何抗体一起使用。举例来说,如果在一个实施例中,也表达hncd16的衍生nk细胞或t细胞的car靶向cd123,那么与细胞组合使用的抗体不是抗cd123抗体。在一些其它实施例中,组合治疗中所用的ipsc衍生nk细胞或t细胞包含hncd16、il15和car;其中il15与car共表达或分开表达;并且il15呈图1的构建体1到7中呈现的形式中的任一种;并且其中组合治疗包含靶向相较于car不同的抗原的抗体。在一些特定实施例中,当il15与car共表达或分开表达时,其呈构建体3、4或7的形式。
9.检查点抑制剂
检查点是细胞分子,通常是细胞表面分子,在不被抑制时能够抑制或下调免疫反应。现在清楚的是,肿瘤选择某些免疫检查点途径作为免疫抗性的主要机制,尤其是针对对肿瘤抗原具有特异性的t细胞。检查点抑制剂(ci)是能够减少检查点基因表达或基因产物,或降低检查点分子的活性,从而阻断抑制性检查点,恢复免疫系统功能的拮抗剂。检查点抑制剂靶向pd1/pdl1或ctla4的发展转变了肿瘤学前景,这些试剂提供多种适应症的长期缓解。但是,许多肿瘤亚型对检查点阻断疗法具有抗性,并且复发仍然是一个大问题。本申请的一个方面提供了一种通过包括如在与ci的组合疗法中所提供的基因组工程化功能衍生细胞来克服ci抗性的治疗方法。在组合疗法的一个实施例中,衍生细胞是nk细胞。在组合疗法的另一个实施例中,衍生细胞是t细胞。除了表现出直接的抗肿瘤能力外,本文提供的衍生nk细胞还显示出抵抗pdl1-pd1介导的抑制作用,并且具有增强t细胞迁移、将t细胞募集到肿瘤微环境并且增强肿瘤部位处的t细胞激活的能力。因此,由功能上有效的基因组工程化衍生nk细胞促进的t细胞的肿瘤浸润表明,所述nk细胞能够与t细胞靶向的免疫疗法(包括检查点抑制剂)协同作用,以缓解局部免疫抑制并且减少肿瘤负荷。
因此,在一个实施例中,用于检查点抑制剂组合疗法的衍生nk细胞包括过表达的nkg2c以及任选地以下中的一种、两种或三种或更多种:cd94、dap12、bike、trike、hncd16、car、b2m敲除、ciita敲除和外源性细胞表面细胞因子和/或受体表达;其中当敲除b2m时,任选地包含编码hla-g的多核苷酸。在一些实施例中,衍生nk细胞包含表1中所列的基因型中的任一种。在一些实施例中,上述衍生nk细胞另外包含:tap1、tap2、tap相关蛋白、nlrc5、pd1、lag3、tim3、rfxank、rfx5、rfxap以及染色体6p21区域中的任何基因中的至少一种的缺失或减少的表达;或hla-e、41bbl、cd3、cd4、cd8、cd47、cd113、cd131、cd137、cd80、pdl1、a2ar、car、tcr、fc受体、衔接子和用于与双特异性、多特异性或通用衔接子偶联的表面触发性受体中的至少一种的引入或增加的表达。
在另一个实施例中,用于检查点抑制剂组合疗法的衍生t细胞包括过表达的nkg2c以及任选地以下中的一种、两种或三种或更多种:cd94、dap12、bike、trike、hncd16、car、b2m敲除、ciita敲除和外源性细胞表面细胞因子和/或受体表达;其中当敲除b2m时,任选地包含编码hla-g的多核苷酸。在一些实施例中,衍生t细胞包含表1中所列的基因型中的任一种。在一些实施例中,上述衍生t细胞另外包含:tap1、tap2、tap相关蛋白、nlrc5、pd1、lag3、tim3、rfxank、rfx5、rfxap以及染色体6p21区域中的任何基因中的至少一种的缺失或减少的表达;或hla-e、41bbl、cd3、cd4、cd8、cd47、cd113、cd131、cd137、cd80、pdl1、a2ar、car、tcr、fc受体、衔接子和用于与双特异性、多特异性或通用衔接子偶联的表面触发性受体中的至少一种的引入或增加的表达。
上文所述的衍生nk细胞或t细胞通过分化ipsc克隆系获得,所述ipsc克隆系包括过表达的nkg2c以及任选地以下中的一种、两种或三种或更多种:cd94、dap12、bike、trike、hncd16、car、b2m敲除、ciita敲除和外源性细胞表面细胞因子和/或受体表达;其中当b2m在ipsc中敲除时,任选地引入编码hla-g的多核苷酸。在一些实施例中,上文所述ipsc克隆系进一步包含:tap1、tap2、tap相关蛋白、nlrc5、pd1、lag3、tim3、rfxank、rfx5、rfxap以及染色体6p21区域中的任何基因中的至少一种的缺失或减少的表达;或hla-e、41bbl、cd3、cd4、cd8、cd47、cd113、cd131、cd137、cd80、pdl1、a2ar、car、tcr、fc受体、衔接子和用于与双特异性、多特异性或通用衔接子偶联的表面触发性受体中的至少一种的引入或增加的表达。
适用于与如本文所提供的衍生nk细胞或t细胞的组合疗法的检查点抑制剂包括但不限于pd-1(pdcdl、cd279)、pdl-1(cd274)、tim-3(havcr2)、tigit(wucam和vstm3)、lag-3(lag3、cd223)、ctla-4(ctla4、cd152)、2b4(cd244)、4-1bb(cd137)、4-1bbl(cd137l)、a2ar、bate、btla、cd39(entpdl)、cd47、cd73(nt5e)、cd94、cd96、cd160、cd200、cd200r、cd274、ceacam1、csf-1r、foxpl、garp、hvem、ido、edo、tdo、lair-1、mica/b、nr4a2、mafb、oct-2(pou2f2)、视黄酸受体α(rara)、tlr3、vista、nkg2a/hla-e和抑制性kir(例如2dl1、2dl2、2dl3、3dl1和3dl2)的拮抗剂。
在一些实施例中,抑制以上检查点分子中的任一种的拮抗剂是抗体。在一些实施例中,检查点抑制性抗体可以是鼠类抗体、人类抗体、人源化抗体、骆驼ig、只有重链的鲨鱼抗体(vnar)、ignar、嵌合抗体、重组抗体或其抗体片段。抗体片段的非限制性实例包括f(ab)′2、f(ab)′3、fv、单链抗原结合性片段(scfv)、(scfv)2、二硫键稳定的fv(dsfv)、微型抗体、双功能抗体、三功能抗体、四功能抗体、单域抗原结合性片段(sdab,纳米抗体)、只有重链的重组抗体(vhh)和维持全部抗体的结合特异性的其它抗体片段,其比起全部抗体可以更有成本效益地产生、更易于使用或更敏感。在一些实施例中,一种、或两种、或三种、或更多种检查点抑制剂包含以下中的至少一种:阿特珠单抗(抗pdl1mab)、阿维鲁单抗(抗pdl1mab)、度伐单抗(抗pdl1mab)、曲美木单抗(tremelimumab)(抗ctla4mab)、伊匹单抗(抗ctla4mab)、iph4102(抗kir)、iph43(抗mica)、iph33(抗tlr3)、利瑞木单抗(抗kir)、莫纳利珠单抗(抗nkg2a)、纳武单抗(抗pd1mab)、帕博利珠单抗(抗pd1mab)和其任何衍生物、功能等效物或生物仿制药。
在一些实施例中,抑制以上检查点分子中的任一种的拮抗剂是基于微rna的,因为发现许多mirna作为控制免疫检查点的表达的调控因子(dragomir等人,《癌症生物医学(cancerbiolmed.)》2018,15(2):103-115)。在一些实施例中,检查点拮抗性mirna包括但不限于mir-28、mir-15/16、mir-138、mir-342、mir-20b、mir-21、mir-130b、mir-34a、mir-197、mir-200c、mir-200、mir-17-5p、mir-570、mir-424、mir-155、mir-574-3p、mir-513和mir-29c。
与所提供的衍生nk细胞或t细胞的组合疗法的一些实施例包含至少一种检查点抑制剂以靶向至少一种检查点分子;其中衍生细胞具有表1中所列的基因型。具有所提供的衍生nk细胞或t细胞的组合疗法的一些其它实施例包含两种、三种或更多种检查点抑制剂,使得靶向两种、三种或更多种检查点分子。在包含至少一种检查点抑制剂和具有表1中所列的基因型的衍生细胞的组合疗法的一些实施例中,所述检查点抑制剂是抗体、或人源化或fc修饰的变体或片段、或其功能等效物或生物仿制药,并且所述检查点抑制剂通过表达编码所述抗体或其片段或变体的外源性多核苷酸序列由衍生细胞产生。在一些实施例中,编码抑制检查点的抗体或其片段或变体的外源性多核苷酸序列在单独构建体中或在包含car和编码抗体或其片段的序列两者的双顺反子构建体中与car共表达。在一些其它实施例中,编码抗体或其片段的序列可通过自切割2a编码序列连接到car表达构建体的5'端或3'端,所述自切割2a编码序列说明为例如car-2a-ci或ci-2a-car。因此,检查点抑制剂和car的编码序列在单一开放阅读框(orf)中。当通过能够浸润肿瘤微环境(tme)的衍生效应细胞将检查点抑制剂递送、表达和分泌为有效负载时,其在接合tme后抵消抑制性检查点分子,允许通过例如car或激活受体的激活模式激活效应细胞。在一些实施例中,与car共表达的检查点抑制剂抑制以下检查点分子中的至少一种:pd-1、pdl-1、tim-3、tigit、lag-3、ctla-4、2b4、4-1bb、4-1bbl、a2ar、bate、btla、cd39(entpdl)、cd47、cd73(nt5e)、cd94、cd96、cd160、cd200、cd200r、cd274、ceacam1、csf-1r、foxpl、garp、hvem、ido、edo、tdo、lair-1、mica/b、nr4a2、mafb、oct-2(pou2f2)、视黄酸受体α(rara)、tlr3、vista、nkg2a/hla-e和抑制性kir。在一些实施例中,在具有表1中所列的基因型的衍生细胞中与car共表达的检查点抑制剂选自包含以下的群组:阿特珠单抗、阿维鲁单抗、度伐单抗、曲美木单抗、伊匹单抗、iph4102、iph43、iph33、利瑞木单抗、莫纳利珠单抗、纳武单抗、帕博利珠单抗和其人源化或fc修饰的变体、片段和其功能等效物或生物仿制药。在一些实施例中,与car共表达的检查点抑制剂是阿特珠单抗或其人源化或fc修饰的变体、片段或其功能等效物或生物仿制药。在一些其它实施例中,与car共表达的检查点抑制剂是纳武单抗或其人源化或fc修饰的变体、片段或其功能等效物或生物仿制药。在一些其它实施例中,与car共表达的检查点抑制剂是帕博利珠单抗或其人源化或fc修饰的变体、片段或其功能等效物或生物仿制药。
在包含本文所提供的衍生细胞和至少一种抑制检查点分子的抗体的组合疗法的一些其它实施例中,所述抗体不由衍生细胞或在衍生细胞中产生,并且在施用具有表1中所列的基因型的衍生细胞之前、同时或之后另外施用。在一些实施例中,在与所提供的衍生nk细胞或t细胞的组合疗法中施用一种、两种、三种或更多种检查点抑制剂是同时或依序的。在包含具有表1中所列的基因型的衍生nk细胞或t细胞的组合治疗的一个实施例中,治疗中包括的检查点抑制剂是阿特珠单抗、阿维鲁单抗、度伐单抗、曲美木单抗、伊匹单抗、iph4102、iph43、iph33、利瑞木单抗、莫纳利珠单抗、纳武单抗、帕博利珠单抗和其人源化或fc修饰的变体、片段和其功能等效物或生物仿制药中的一种或多种。在包含具有表1中所列的基因型的衍生nk细胞或t细胞的组合治疗的一些实施例中,治疗中包括的检查点抑制剂是阿特珠单抗或其人源化或fc修饰的变体、片段和其功能等效物或生物仿制药。在包含具有表1中所列的基因型的衍生nk细胞或t细胞的组合治疗的一些实施例中,治疗中包括的检查点抑制剂是纳武单抗或其人源化或fc修饰的变体、片段或其功能等效物或生物仿制药。在包含具有表1中所列的基因型的衍生nk细胞或t细胞的组合治疗的一些实施例中,治疗中包括的检查点抑制剂是帕博利珠单抗或其人源化或fc修饰的变体、片段和其功能等效物或生物仿制药。
ii.在ipsc中选定基因座处进行靶向基因组编辑的方法
如本文中可互换使用,基因组编辑或基因编辑是一种类型的基因工程,其中在靶细胞的基因组中进行dna插入、缺失和/或置换。靶向基因组编辑(可与“靶向基因组编辑”或“靶向基因编辑”互换)能够在基因组中的预选位点实现插入、缺失和/或取代。当在靶向编辑期间使内源性序列在插入位点缺失时,可以敲除包含受影响序列的内源性基因或因序列缺失而降低。因此,靶向编辑还可以用于精确地中断内源性基因表达。本文中类似地使用术语“靶向整合”,其是指一种涉及在使内源性序列在插入位点缺失或不缺失的情况下插入一个或多个外源性序列的方法。相比之下,随机整合的基因经历位置效应和静默,以致其表达不可靠并且不可预测。举例来说,着丝点和亚端粒区域特别容易发生转基因沉默。相反,新整合的基因可以影响周围内源性基因和染色质,潜在地改变细胞特性或有利于细胞转化。因此,将外源性dna插入预选基因座(例如安全港基因座或基因组安全港(gsh))对于安全、效率、拷贝数控制以及可靠的基因反应控制来说是重要的。
靶向编辑可以通过核酸酶非依赖性方法或通过核酸酶依赖性方法实现。在核酸酶非依赖性靶向编辑方法中,同源重组是通过宿主细胞的酶机制、通过同源序列侧接待插入的外源性多核苷酸而引导。
可替代地,靶向编辑可以借助于通过特异性稀有切割核酸内切酶来特异性引入双链断裂(dsb)以更高频率来实现。这类核酸酶依赖性靶向编辑是利用dna修复机制,包括非同源末端连接(nhej),其响应于dsb而发生。不使用含有外源性遗传物质的供体载体,nhej通常引起少量的内源性核苷酸的随机插入或缺失(插入/缺失)。相比之下,当存在含有位于一对同源臂两侧的外源性遗传物质的供体载体时,可以在同源指导修复(hdr)期间通过同源重组将外源性遗传物质引入基因组中,从而导致“靶向整合”。在一些实施例中,靶向的整合位点旨在位于所选基因的编码区内,并且因此靶向整合可能破坏基因表达,从而在一个单一编辑步骤中同时敲入和敲除(ki/ko)。
根据一些实施例,可以实现在所关注基因座(goi)中将一个或多个转基因插入在所选位置处以同时敲除所述基因。适于同时敲入和敲除(ki/ko)的基因位点包含但不限于b2m、tap1、tap2、tap相关蛋白、nlrc5、ciita、rfxank、ciita、rfx5、rfxap、tcrα或β恒定区、nkg2a、nkg2d、cd38、cis、cbl-b、socs2、pd1、ctla4、lag3、tim3和tigit。利用用于位置选择性插入的相应的位点特异性靶向同源臂,一个或多个转基因可以在内源性启动子下,在所述位点处表达,或在包括在构建体中的外源性启动子下表达。当将两个或更多个转基因插入在cd38基因座中的所选位置处时,可以将接头序列(例如,2a接头或ires)放置在任何两个转基因之间。2a接头编码源自fmdv、erav、ptv-i和tav的自切割肽(分别称为“f2a”、“e2a”、“p2a”和“t2a”),使得可由单次转译产生单独的蛋白质。在一些实施例中,构建体中包括绝缘子以降低转基因和/或外源性启动子沉默的风险。外源性启动子可以是cag或其它组成性、诱导性、时间特异性、组织特异性和/或细胞类型特异性的启动子,包括但不限于cmv、ef1α、pgk和ubc。
能够引入特异性和靶向dsb的可用核酸内切酶包括但不限于锌指核酸酶(zfn)、转录激活子样效应物核酸酶(talen)、rna引导的crispr(簇聚的规则间隔的短回文重复序列)系统。另外,利用phic31和bxb1整合酶的dice(双整合酶盒交换)系统也是靶向整合的一种有前景的工具。
zfn是靶向核酸酶,其包含与锌指dna结合性结构域融合的核酸酶。“锌指dna结合性结构域”或“zfbd”意指按照序列特异性方式、通过一个或多个锌指结合dna的多肽结构域。锌指是锌指结合性结构域内的约30个氨基酸的结构域,其结构通过锌离子的配位而稳定化。锌指实例包括但不限于c2h2锌指、c3h锌指和c4锌指。“设计”的锌指结构域是一种不存在于自然界中的结构域,其设计/组成主要来源于合理准则,例如应用取代规则和计算机化算法来处理存储现有zfp设计和结合数据信息的数据库中的信息。参见例如,美国专利第6,140,081号;6,453,242;和第6,534,261号;还参见wo98/53058;wo98/53059;wo98/53060;wo02/016536和wo03/016496。“所选”锌指结构域是一种在自然界中未发现的结构域,其产生主要来源于经验方法,例如噬菌体呈现、相互作用截留或杂交选择。zfn更详细地描述于美国专利第7,888,121号和美国专利第7,972,854号中,其完整公开内容以引入的方式并入本文中。zfn在所属领域中的最公认实例是foki核酸酶与锌指dna结合性结构域的融合物。
talen是一种靶向核酸酶,其包含与tal效应子dna结合性结构域融合的核酸酶。“转录激活子样效应子dna结合性结构域”、“tal效应子dna结合性结构域”或“taledna结合性结构域”意指负责tal效应蛋白结合到dna的tal效应蛋白的多肽结构域。tal效应蛋白由黄单胞菌属(xanthomonas)植物病原体在感染期间分泌。这些蛋白质进入植物细胞的核,通过其dna结合性结构域结合效应子特异性dna序列,并且通过其反式激活结构域在这些序列处激活基因转录。tal效应子dna结合性结构域特异性取决于不完美的34个氨基酸重复的效应子可变数目,其包含所选重复位置处的多态性,称为重复可变双残基(rvd)。talen更详细地描述于美国专利申请第2011/0145940号,所述申请以引用的方式并入本文中。talen在所属领域中的最公认实例是foki核酸酶与tal效应子dna结合性结构域的融合多肽。
用于本发明方法中的靶向核酸酶的另一实例是靶向spo11核酸酶,一种包括spo11多肽的多肽,所述多肽具有与dna结合性结构域(例如对所关注dna序列具有特异性的锌指dna结合性结构域、tal效应子dna结合性结构域等)融合的核酸酶活性。参见例如美国申请第61/555,857号,其公开内容以引入的方式并入本文中。
适用于本发明的靶向核酸酶的其它实例包括但不限于bxb1、phic31、r4、phibt1和wβ/spbc/tp901-1,不论单独地或组合地使用。
靶向核酸酶的其它非限制性实例包括天然存在的核酸酶和重组核酸酶;来自包括以下的家族的crispr相关核酸酶:cas、cpf、cse、csy、csn、csd、cst、csh、csa、csm和cmr;限制性核酸内切酶;大范围核酸酶;归巢核酸内切酶等。
作为一示例性实例,crispr/cas9需要两种主要组分:(1)cas9核酸内切酶和(2)crrna-tracrrna复合体。共表达时,所述两种组分形成募集到标靶dna序列的复合体,包含pam和靠近pam的接种区域。crrna与tracrrna可以组合而形成嵌合向导rna(grna)以引导cas9靶向所选序列。这两种组分然后可以通过转染或转导递送到哺乳动物细胞。
dice介导的插入是利用一对重组酶(例如phic31和bxb1)来提供外源性dna的单向整合,其严格局限于每种酶自身的小attb和attp识别位点。由于这些att靶点并非天然存在于哺乳动物基因组中,因此必须首先将其引入基因组中的所期望整合位点。参见例如美国申请公开第2015/0140665号,其公开内容以引入的方式并入本文中。
本发明的一个方面提供一种构建体,其包含一个或多个用于靶向基因组整合的外源性多核苷酸。在一个实施例中,所述构建体进一步包含对所期望的整合位点具有特异性的一对同源臂,并且所述靶向整合方法包含将所述构建体引入细胞中以允许细胞宿主酶机制实现定点同源重组。在另一个实施例中,在细胞中实现靶向整合的方法包含将包含一个或多个外源性多核苷酸的构建体引入细胞中,和将包含对所期望的整合位点具有特异性的dna结合性结构域的zfn表达盒引入细胞中以实现zfn介导的插入。在又另一个实施例中,在细胞中实现靶向整合的方法包含将包含一个或多个外源性多核苷酸的构建体引入细胞中,和将包含对所期望的整合位点具有特异性的dna结合性结构域的talen表达盒引入细胞中以实现talen介导的插入。在另一个实施例中,在细胞中实现靶向整合的方法包含将包含一个或多个外源性多核苷酸的构建体引入细胞中、将cas9表达盒和包含对所期望的整合位点具有特异性的向导序列的grna引入细胞中以实现cas9介导的插入。在再另一个实施例中,在细胞中实现靶向整合的方法包含将包含一对dice重组酶的一个或多个att位点的构建体引入细胞中的所期望的整合位点、将包含一个或多个外源性多核苷酸的构建体引入细胞中,和将dice重组酶的表达盒引入以实现dice介导的靶向整合。
有望用于靶向整合的位点包括但不限于安全港基因座或基因组安全港(gsh),其是人类基因组的基因内或基因外区域,在理论上,其能够容纳新整合的dna的可预测表达而不会对宿主细胞或生物体产生不利影响。适用的安全港必须允许转基因表达足以产生由载体编码的蛋白质或非编码rna的所期望水平。安全港还不得使细胞容易发生恶性转化,也不得改变细胞功能。如果整合位点是潜在的安全港基因座,那么理想的是需要满足包括但不限于以下的准则:如通过序列注释所判断,调控元件或基因没有中断;是基因密集区域中的基因间区域,或沿相反方向转录的两种基因之间的汇聚位置;保持距离以使载体编码的转录激活子与相邻基因(特别是癌症相关和微rna基因)的启动子之间的长程相互作用的可能性最小化;并且具有明显普遍存在的转录活性,如通过按较宽空间和时间表达的序列标签(est)表达谱所反映,其指示普遍存在的转录活性。这个后一特点在干细胞中特别重要,其中在分化期间,染色质重塑通常引起一些基因座的沉默和其它基因座的潜在激活。在适于外源插入的区域内,选用于插入的确切基因座应所述不含重复元件和保守序列并且可以针对其容易地设计出用于扩增同源臂的引物。
适用于人类基因组编辑或具体地说靶向整合的位点包括但不限于腺相关病毒位点1(aavs1)、趋化因子(cc基元)受体5(ccr5)基因座和小鼠rosa26基因座的人类直系同源物。另外,小鼠h11基因座的人类直系同源物也可以是使用本文所公开的靶向整合组合物和方法进行插入的合适位点。另外,也可以使用胶原蛋白和htrp基因座作为靶向整合的安全港。然而,每个所选位点的验证已表明是必需的,特别是在特异性整合事件的干细胞中,并且通常需要优化插入策略,包括启动子选择、外源性基因序列和配置,以及构建体设计。
用于靶向插入/缺失的编辑位点通常包含于其表达和/或功能旨在是中断的内源性基因中。在一个实施例中,包含靶向插入/缺失的内源性基因与免疫反应调控和调节相关。在一些其它实施例中,包含靶向插入/缺失的内源性基因与以下相关:靶向模式、受体、信号传导分子、转录因子、药物标靶候选物、免疫反应调控和调节,或抑制干细胞和/或祖细胞和其衍生细胞移植、运输、归巢、活力、自我更新、存留和/或存活的蛋白质。
因而,本发明的一个方面提供一种在所选基因座中进行靶向整合的方法,所选基因座包括基因组安全港或已知或证实安全的预选基因座并且经充分调控以实现连续或暂时基因表达,例如如本文所提供的b2m、tap1、tap2或tap相关蛋白基因座。在一个实施例中,靶向整合方法用的基因组安全港包含一个或多个所期望的整合位点,包含aavs1、ccr5、rosa26、胶原蛋白、htrp、h11、β-2微球蛋白、gapdh、tcr或runx1,或满足基因组安全港准则的其它基因座。在一些实施例中,靶向整合位于期望作为整合的结果的基因敲减或敲除的基因位点之一,其中此类基因位点包含但不限于tap1、tap2、tap相关蛋白、nlrc5、ciita、rfxank、ciita、rfx5、rfxap、tcrα或β恒定区、nkg2a、nkg2d、cd38、cis、cbl-b、socs2、pd1、ctla4、lag3、tim3和tigit。
在一个实施例中,细胞中的靶向整合的方法包括向细胞引入包括一种或多种外源性多核苷酸的构建体,以及引入包括对期望整合位点具有特异性的一对同源臂的一个或多个同源序列的构建体,以通过细胞宿主酶机制实现位点特异性同源重组,其中期望的整合位点包括aavs1、ccr5、rosa26、胶原蛋白、htrp、h11、gapdh、runx1、b2m、tap1、tap2、tap相关蛋白、nlrc5、ciita、rfxank、ciita、rfx5、rfxap、tcrα或β恒定区、nkg2a、nkg2d、cd38、cd38、cis、cbl-b、socs2、pd1、ctla4、lag3、tim3或tigit。
在另一个实施例中,细胞中的靶向整合的方法包括向细胞引入包括一种或多种外源性多核苷酸的构建体,以及向细胞引入包括对期望整合位点具有特异性的dna结合性结构域的zfn表达盒,以实现zfn介导的插入,其中期望的整合位点包括aavs1、ccr5、rosa26、胶原蛋白、htrp、h11、gapdh、runx1、b2m、tap1、tap2、tap相关蛋白、nlrc5、ciita、rfxank、ciita、rfx5、rfxap、tcrα或β恒定区、nkg2a、nkg2d、cd38、cis、cbl-b、socs2、pd1、ctla4、lag3、tim3或tigit。在又另一个实施例中,细胞中的靶向整合的方法包括向细胞引入包括一种或多种外源性多核苷酸的构建体,以及向细胞引入包括对期望整合位点具有特异性的dna结合性结构域的talen表达盒,以实现talen介导的插入,其中期望的整合位点包括aavs1、ccr5、rosa26、胶原蛋白、htrp、h11、gapdh、runx1、b2m、tap1、tap2、tap相关蛋白、nlrc5、ciita、rfxank、ciita、rfx5、rfxap、tcrα或β恒定区、nkg2a、nkg2d、cd38、cis、cbl-b、socs2、pd1、ctla4、lag3、tim3或tigit。在另一个实施例中,细胞中的靶向整合的方法包括向细胞引入包括一种或多种外源性多核苷酸的构建体,向细胞引入cas9表达盒以及包括对期望整合位点具有特异性的引导序列的grna,以实现cas9介导的插入,其中期望的整合位点包括aavs1、ccr5、rosa26、胶原蛋白、htrp、h11、gapdh、runx1、b2m、tap1、tap2、tap相关蛋白、nlrc5、ciita、rfxank、ciita、rfx5、rfxap、tcrα或β恒定区、nkg2a、nkg2d、cd38、cis、cbl-b、socs2、pd1、ctla4、lag3、tim3或tigit。在仍另一个实施例中,细胞中的靶向整合的方法包括向细胞中的期望整合位点引入包括一对dice重组酶的一个或多个att位点,向细胞引入包括一个或多个外源性多核苷酸的构建体,以及引入dice重组酶的表达盒,以实现dice介导的靶向整合,其中期望的整合位点包括aavs1、ccr5、rosa26、胶原蛋白、htrp、h11、gapdh、runx1、b2m、tap1、tap2、tap相关蛋白、nlrc5、ciita、rfxank、ciita、rfx5、rfxap、tcrα或β恒定区、nkg2a、nkg2d、cd38、cis、cbl-b、socs2、pd1、ctla4、lag3、tim3或tigit。
另外,如本文所提供,用于靶向整合于安全港的上述方法是用于插入所关注的任何多核苷酸,例如编码以下的多核苷酸:安全开关蛋白质、靶向模式、受体、信号传导分子、转录因子、医药学活性蛋白质和肽、药物标靶候选物,和促进干细胞和/或祖细胞移植、运输、归巢、活力、自我更新、存留和/或存活的蛋白质。在一些其它实施例中,包含一个或多个外源性多核苷酸的构建体进一步包含一个或多个标记物基因。在一个实施例中,本发明的构建体中的外源性多核苷酸是编码安全开关蛋白质的自杀基因。适用于诱导细胞死亡的自杀基因系统包括但不限于胱天蛋白酶9(或胱天蛋白酶3或7)和ap1903;胸苷激酶(tk)和苷昔洛韦(ganciclovir,gcv);胞嘧啶脱氨酶(cd)和5-氟胞嘧啶(5-fc)。另外,一些自杀基因系统对细胞类型具有特异性,例如使用b细胞分子cd20对t淋巴细胞进行基因修饰允许其在施用mab利妥昔单抗后消除。另外,当基因工程化细胞暴露于西妥昔单抗(cetuximab)时,含有被西妥昔单抗识别的抗原决定基的修饰的egfr可以用于耗尽所述细胞。因而,本发明的一个方面提供一种靶向整合一个或多个编码安全开关蛋白质的自杀基因的方法,所述安全开关蛋白质选自胱天蛋白酶9(胱天蛋白酶3或7)、胸苷激酶、胞嘧啶脱氨酶、修饰的egfr和b细胞cd20。
在一些实施例中,通过本文中的方法整合的一个或多个外源性多核苷酸是通过用于靶向整合的构建体中包含的可操作连接的外源性启动子驱动。所述启动子可以是可诱导的或结构性的,并且可以是时间特异性、组织特异性或细胞类型特异性的。适用于本发明方法的结构性启动子包括但不限于巨细胞病毒(cmv)、延伸因子1α(ef1α)、磷酸甘油酸激酶(pgk)、杂交cmv增强子/鸡肉β-肌动蛋白(cag)和泛素c(ubc)启动子。在一个实施例中,外源性启动子是cag。
通过本文中的方法整合的外源性多核苷酸可以通过宿主基因组中的内源性启动子在整合位点驱动。在一个实施例中,本发明的方法是用于使一个或多个外源性多核苷酸靶向整合于细胞基因组中的aavs1基因座。在一个实施例中,至少一种整合的多核苷酸是由内源性aavs1启动子驱动。在另一个实施例中,本发明的方法是用于靶向整合于细胞基因组中的rosa26基因座。在一个实施例中,至少一种整合的多核苷酸是由内源性rosa26启动子驱动。在再另一个实施例中,本发明的方法是用于靶向整合于细胞基因组中的h11基因座。在一个实施例中,至少一种整合的多核苷酸是由内源性h11启动子驱动。在另一个实施例中,本发明的方法是用于靶向整合于细胞基因组中的胶原蛋白基因座。在一个实施例中,至少一种整合的多核苷酸是由内源性胶原蛋白启动子驱动。在再另一个实施例中,本发明的方法是用于靶向整合于细胞基因组中的htrp基因座。在一个实施例中,至少一种整合的多核苷酸是由内源性htrp启动子驱动。理论上,只有正确插入所期望位置才能实现由内源性启动子驱动的外源性基因的基因表达。
在一些实施例中,靶向整合方法用的构建体中包含的一个或多个外源性多核苷酸是由一个启动子驱动。在一些实施例中,所述构建体包含一个或多个位于由同一个启动子驱动的两个相邻多核苷酸之间的接头序列,以使得各部分之间的物理间距更大并且使酶机制可行性最大化。接头序列的接头肽可以由为了使各部分(外源性多核苷酸,和/或由其编码的蛋白质或肽)之间产生物理间距而选择的氨基酸组成,视相关功能而定,其较柔软或较硬。接头序列可以通过蛋白酶切割或以化学方式切割以产生单独的部分。接头中的酶切割位点实例包括蛋白水解酶(例如肠激酶、因子xa、胰蛋白酶、胶原蛋白酶和凝血酶)的切割位点。在一些实施例中,所述蛋白酶是由宿主天然产生的蛋白酶或其通过外源引入。可替代地,接头中的切割位点可以是在暴露于所选化学物质(例如溴化氰、羟胺或低ph)后能够切割的位点。任选存在的接头序列可以服务于除提供切割位点之外的目的。接头序列应所述允许所述部分相对于另一相邻部分有效定位,以便所述部分正确地发挥功能。接头还可以是长度足以防止所述部分之间出现任何空间位阻的简单氨基酸序列。另外,所述接头序列可以实现转译后修饰,包括但不限于例如磷酸化位点、生物素化位点、硫酸化位点、γ-羧基化位点等等。在一些实施例中,接头序列是柔软的,以便使生物活性肽不能保持单一非期望的构形。接头可以主要包含具有小侧链的氨基酸,例如甘氨酸、丙氨酸和丝氨酸,以提供柔性。在一些实施例中,接头序列中的约80或90%或更多包含甘氨酸、丙氨酸或丝氨酸残基,尤其是甘氨酸和丝氨酸残基。在若干实施例中,g4s接头肽将融合蛋白的末端处理域和核酸内切酶结构域分隔。在其它实施例中,2a接头序列允许单次转译产生两种单独的蛋白质。合适的接头序列能容易凭经验鉴别。另外,接头序列的合适尺寸和序列也能通过常规计算机建模技术确定。在一个实施例中,接头序列编码自切割肽。在一个实施例中,自切割肽是2a。在一些其它实施例中,接头序列提供内部核糖体入口序列(ires)。在一些实施例中,任何两个相邻的接头序列是不同的。
将包含待靶向整合的外源性多核苷酸的构建体引入细胞中的方法可以使用本来已知的将基因转移到细胞的方法实现。在一个实施例中,所述构建体包含病毒载体,例如腺病毒载体、腺相关病毒载体、逆转录病毒载体、慢病毒载体、仙台病毒载体的骨架。在一些实施例中,质粒载体用于将外源性多核苷酸递送到靶细胞中和/或使外源性多核苷酸在靶细胞中表达(例如pal-11、pxtl、prc/cmv、prc/rsv、pcdnai/neo)等等。在一些其它实施例中,游离型载体用于将外源性多核苷酸递送到靶细胞。在一些实施例中,重组腺相关病毒(raav)可用于基因工程以通过同源重组来引入插入、缺失或取代。不同于慢病毒,raav不整合到宿主基因组中。另外,游离型raav载体介导同源定向的基因,其相较于常规靶向质粒的转染以高得多的比例靶向。在一些实施例中,aav6或aav2载体用于在ipsc的基因组中的标靶位点引入插入、缺失或取代。在一些实施例中,使用本文中的方法和组合物获得的基因组修饰的ipsc和其衍生细胞包含表1中所列的至少一种基因型。
iii.获取和维持基因组工程化ipsc的方法
本发明提供一种获得和维持基因组工程化ipsc的方法,所述方法包含在一个或多个所期望的位点进行的一个或多个靶向编辑,其中所述靶向编辑在扩增的基因组工程化ipsc或ipsc衍生非多能细胞中、在相应所选编辑位点处保持完整和功能。所述靶向编辑将ipsc和其衍生细胞插入、缺失和/或取代引入基因组中,即,在所选位点引入靶向整合和/或插入/缺失。与直接工程化患者源的外周血起源原代效应细胞相比,通过编辑和分化如本文所提供的ipsc获得基因组工程化衍生细胞的许多益处包括但不限于:工程化效应细胞的来源不受限制;无需重复操纵效应细胞,尤其在涉及多种工程化模式时;所获效应细胞因具有伸长端粒和经历较少耗竭而再生;效应细胞群关于编辑位点、拷贝数和缺乏等位基因变体、随机突变和表达杂色是均匀的,主要是由于如本文所提供的工程化ipsc中能够进行克隆选择。
在特定实施例中,包含在一个或多个所选位点进行一个或多个靶向编辑的基因组工程化ipsc作为单一细胞在表2所示的作为命运维持培养基(fmm)的细胞培养基中长期维持、传代和扩增,其中所述ipsc在所选位点保留靶向编辑和功能修饰。培养基的组分可以表2中所示的最优范围内的量存在于培养基中。fmm中所培养的ipsc已表明继续维持其未分化和基础或初始轮廓;基因组稳定性,而不需要培养物清洗或选择;并且通过体外类胚胎体或单层分化(不形成类胚胎体);和体内畸胎瘤形成的分化容易产生所有三种体细胞谱系。参见例如美国申请第61/947,979号,其公开内容以引入的方式并入本文中。
表2:用于ipsc重编程和维持的例示性培养基
在一些实施例中,包含一个或多个靶向整合和/或插入/缺失的基因组工程化ipsc是在包含meki、gski和rocki并且不含或基本上不含tgfβ受体/alk5抑制剂的培养基中维持、传代和扩增,其中所述ipsc在所选位点保留完整和功能靶向编辑。
本发明的另一方面提供一种产生基因组工程化ipsc的方法,其通过ipsc的靶向编辑;或者首先通过靶向编辑来产生基因组工程化非多能细胞,并且然后将所选/分离的基因组工程化非多能细胞重编程,以获得包含与非多能细胞相同的靶向编辑的ipsc。本发明的另一个方面提供基因组工程化非多能细胞,其通过将靶向整合和/或靶向插入/缺失引入细胞中而同时经历重编程,其中所接触的非多能细胞处于足以用于重编程的条件下,并且其中重编程条件包含使非多能细胞与一种或多种重编程因子和小分子接触。在同时进行基因组工程化和重编程的方法的各种实施例中,可以在启动重编程之前或基本上同时,通过使非多能细胞与一种或多种重编程因子和小分子接触而将靶向整合和/或靶向插入/缺失引入非多能细胞中。
在一些实施例中,为了对非多能细胞同时进行基因组工程化和重编程,还可以在通过使非多能细胞与一种或多种重编程因子和小分子接触而启动多日重编程工艺之后,将靶向整合和/或插入/缺失引入非多能细胞中,并且其中携带构建体的载体是在重编程细胞呈现一种或多种内源性多能基因(包括但不限于ssea4、tra181和cd30)的稳定表达之前引入。
在一些实施例中,重编程是通过使非多能细胞与至少一种重编程因子和任选存在的tgfβ受体/alk抑制剂、mek抑制剂、gsk3抑制剂与rock抑制剂的组合(frm;表2)接触来启动。在一些实施例中,通过上述任何方法实现的基因组工程化ipsc进一步使用包含mek抑制剂、gsk3抑制剂和rock抑制剂的组合的混合物(fmm;表2)来维持和扩增。
在产生基因组工程化ipsc的方法的一些实施例中,所述方法包含:对ipsc进行基因组工程化,其通过将一个或多个靶向整合和/或插入/缺失引入ipsc中以获得具有至少一种表1中所列的基因型的基因组工程化ipsc。可替代地,产生基因组工程化ipsc的方法包含:(a)将一个或多个靶向编辑引入非多能细胞中,以获得包含位于所选位点的靶向整合和/或插入/缺失的基因组工程化非多能细胞,和(b)使基因组工程化非多能细胞与一种或多种重编程因子和任选存在的小分子组合物接触,以获得包含位于所选位点的靶向整合和/或插入/缺失的基因组工程化ipsc,所述小分子组合物包含tgfβ受体/alk抑制剂、mek抑制剂、gsk3抑制剂和/或rock抑制剂。可替代地,产生基因组工程化ipsc的方法包含:(a)使非多能细胞与一种或多种重编程因子和任选存在的小分子组合物接触,以启动非多能细胞的重编程,所述小分子组合物包含tgfβ受体/alk抑制剂、mek抑制剂、gsk3抑制剂和/或rock抑制剂;(b)将一种或多种靶向整合和/或插入/缺失引入用于基因组工程化重编程非多能细胞中;和(c)获得包含位于所选位点的靶向整合和/或插入/缺失的基因组工程化克隆ipsc。
重编程因子选自由以下组成的群组:oct4、sox2、nanog、klf4、lin28、c-myc、ecat1、utf1、esrrb、sv40lt、hesrg、cdh1、tdgf1、dppa4、dnmt3b、zic3、l1td1和其任何组合,如pct/us2015/018801和pct/us16/57136中所公开,其公开内容以引入的方式并入本文中。一种或多种重编程因子可以呈多肽形式。重编程因子也可以呈多核苷酸形式,并且从而通过载体(例如逆转录病毒、仙台病毒、腺病毒、游离基因体、质粒和小环)引入非多能细胞中。在特定实施例中,通过慢病毒载体引入编码至少一种重编程因子的一种或多种多核苷酸。在一些实施例中,通过游离型载体引入一种或多种多核苷酸。在各种其它实施例中,通过仙台病毒载体引入一种或多种多核苷酸。在一些实施例中,通过质粒的组合引入一种或多种多核苷酸。参见例如美国申请第62/571,105号,其公开内容以引入的方式并入本文中。
在一些实施例中,非多能细胞是利用包含不同外源性多核苷酸和/或不同启动子的多种构建体、通过用于在相同或不同所选位点进行靶向整合的多种载体转移。这些外源性多核苷酸可以包含自杀基因,或编码靶向模式、受体、信号传导分子、转录因子、医药学活性蛋白质和肽、药物标靶候选物的基因,或编码蛋白质的基因,所述蛋白质促进ipsc或其衍生细胞移植、运输、归巢、活力、自我更新、存留和/或存活。在一些实施例中,外源性多核苷酸编码rna,包括但不限于sirna、shrna、mirna和反义核酸。这些外源性多核苷酸可以由一个或多个启动子驱动,所述启动子选自由以下组成的群组:组成性启动子、诱导性启动子、时间特异性启动子和组织或细胞类型特异性启动子。因此,当在例如在诱导剂存在下或在特定分化细胞类型中激活启动子的条件下时,多核苷酸是可表达的。在一些实施例中,多核苷酸在ipsc中和/或在由ipsc分化的细胞中表达。在一个实施例中,一个或多个自杀基因由组成性启动子驱动,例如capase-9由cag驱动。可以同时或连续将包含不同外源性多核苷酸和/或不同启动子的这些构建体转移到非多能细胞中。经历多个构建体的靶向整合的非多能细胞可同时接触一个或多个重编程因子以与基因工程化同时启动重编程,从而获得在同一细胞池中包含多个靶向整合的基因组工程化ipsc。因此,这一稳固方法实现同时重编程和工程化策略,从而得到具有整合到一个或多个所选靶向位点的多种模式的克隆的基因组工程化hipsc。在一些实施例中,使用本文中的方法和组合物获得的基因组修饰的ipsc和其衍生细胞包含表1中所列的至少一种基因型。
iv.通过分化基因组工程化ipsc获得基因工程化非多能细胞的方法
本发明的另一方面提供一种通过畸胎瘤形成体内分化基因组工程化ipsc的方法,其中通过基因组工程化ipsc体内得到的分化细胞保留完整和功能性靶向编辑,其包括在所期望的位点处的靶向整合和/或插入/缺失。在一些实施例中,基因组工程化ipsc经由畸胎瘤体内得到的分化细胞包含在一个或多个所期望的位点整合的一个或多个诱导性自杀基因,所述位点包含aavs1、ccr5、rosa26、胶原蛋白、htrp、h11、β-2微球蛋白、gapdh、tcr或runx1,或满足基因组安全港准则的其它基因座。在一些其它实施例中,基因组工程化ipsc经由畸胎瘤体内得到的分化细胞包含编码靶向模式或编码促进干细胞和/或祖细胞的运输、归巢、活力、自我更新、存留和/或存活的蛋白质的多核苷酸。在一些实施例中,基因组工程化ipsc经由畸胎瘤体内得到的分化细胞包含一个或多个诱导性自杀基因,在与免疫反应调控和介导相关的内源性基因中进一步包含一个或多个插入/缺失。在一些实施例中,插入/缺失包含在一个或多个内源性检查点基因中。在一些实施例中,插入/缺失包含在一个或多个内源性t细胞受体基因中。在一些实施例中,插入/缺失包含在一个或多个内源性mhci类抑制基因中。在一些实施例中,插入/缺失包含在与主要组织相容性复合体相关的一个或多个内源性基因中。在一些实施例中,插入/缺失包括在一个或多个内源性基因中,所述一个或多个内源性基因包含但不限于gapdh、runx1、b2m、tap1、tap2、tap相关蛋白、nlrc5、ciita、rfxank、ciita、rfx5、rfxap、tcrα或β恒定区、nkg2a、nkg2d、cd38、cis、cbl-b、socs2、pd1、ctla4、lag3、tim3或tigit。在一个实施例中,在所选位点包含一个或多个外源性多核苷酸的基因组工程化ipsc在b2m(β-2-微球蛋白)编码基因中进一步包含靶向编辑。
在特定实施例中,包含如本文所提供的一种或多种基因修饰的基因组工程化ipsc用于体外得到造血细胞谱系或任何其它特定细胞类型,其中衍生非多能细胞保留功能性基因修饰,包括在所选位点处的靶向编辑。在一个实施例中,基因组工程化ipsc衍生细胞包括但不限于具有永久性生血内皮细胞(he)潜能的中胚层细胞、永久性he、cd34造血细胞、造血干细胞和祖细胞、造血多能祖细胞(mpp)、t细胞祖细胞、nk细胞祖细胞、骨髓细胞、嗜中性粒细胞祖细胞、t细胞、nkt细胞、nk细胞、b细胞、嗜中性粒细胞、树突状细胞和巨噬细胞,其中衍生自基因组工程化ipsc的这些细胞保留功能性基因修饰,包括在所期望的位点处的靶向编辑。
适用于获得ipsc衍生造血细胞谱系的分化方法和组合物包括例如国际申请第pct/us2016/044122号中描绘的分化方法和组合物,所述申请的公开内容以引入的方式并入本文中。如所提供,用于产生造血细胞谱系的方法和组合物是在无血清、无饲养层和/或无基质的条件下并且在可扩展和单层培养平台中在无需eb形成的情况下通过衍生自多能干细胞(包括hipsc)的永久性生血内皮细胞(he)。可以根据所提供的方法分化的细胞的范围是多能干细胞到专门化为特定末端分化细胞和转分化细胞的祖细胞、和直接转向造血命运而不经历多能中间体的多种谱系细胞。类似地,干细胞分化而产生的细胞的范围是多潜能干细胞或祖细胞到末端分化细胞,和所有中间造血细胞谱系。
用于在单层培养中分化和扩增来自多能干细胞的造血谱系细胞的方法包含使多能干细胞与bmp路径活化剂和任选的bfgf接触。如所提供,无需由多能干细胞形成类胚胎体便获得并且扩增多能干细胞衍生中胚层细胞。然后使中胚层细胞与bmp路径活化剂、bfgf和wnt路径活化剂接触,以获得具有永久性生血内皮细胞(he)潜能的扩增中胚层细胞,而无需由多能干细胞形成类胚胎体。通过随后与bfgf和任选存在的rock抑制剂和/或wnt路径活化剂接触,具有永久性he潜能的中胚层细胞分化成永久性he细胞,在分化期间,所述永久性he细胞还得以扩增。
本文所提供的用于获得造血谱系细胞的方法优于eb介导的多能干细胞分化,原因在于:eb形成产生了适度到最低限度的细胞扩增;不允许单层培养,而单层培养对于需要所述细胞在群体中均匀扩增和均匀分化的许多应用来说是重要的;并且费力并且效率低。
所提供的单层分化平台促进向永久性生血内皮细胞分化,从而得到造血干细胞和分化后代,例如t细胞、b细胞、nkt细胞和nk细胞。单层分化策略实现了增强的分化效率与大规模扩增的组合,从而能够在不同治疗应用中递送治疗上相关数目个多能干细胞衍生造血细胞。此外,使用本文所提供的方法进行的单层培养产生了功能造血谱系细胞,其实现了全范围的试管内分化、体外调节和体内长期造血自我更新、重构和移植。如所提供,ipsc衍生造血谱系细胞包括但不限于永久性生血内皮细胞、造血多能祖细胞、造血干细胞和祖细胞、t细胞祖细胞、nk细胞祖细胞、t细胞、nk细胞、nkt细胞、b细胞、巨噬细胞和嗜中性粒细胞。
用于引导多能干细胞分化成永久性造血谱系细胞的方法,其中所述方法包含:(i)使多能干细胞与包含bmp活化剂和任选存在的bfgf的组合物接触,以启动多能干细胞分化成和扩增中胚层细胞;(ii)使所述中胚层细胞与包含bmp活化剂、bfgf和gsk3抑制剂的组合物接触,以启动中胚层细胞分化成和扩增具有永久性he潜能的中胚层细胞,其中所述组合物任选地不含tgfβ受体/alk抑制剂;(iii)使具有永久性he潜能的所述中胚层细胞与组合物接触,以启动具有永久性生血内皮细胞潜能的多能干细胞衍生中胚层细胞分化成和扩增永久性生血内皮细胞,所述组合物包含rock抑制剂、一个或多个生长因子和细胞因子和任选存在的wnt路径活化剂,所述细胞因子选自由以下组成的群组:bfgf、vegf、scf、igf、epo、il6和il11,其中所述组合物任选地不含tgfβ受体/alk抑制剂。
在一些实施例中,所述方法进一步包含:使多能干细胞与包含mek抑制剂、gsk3抑制剂和rock抑制剂的组合物接触,以接种和扩增多能干细胞,其中组合物不含tgfβ受体/alk抑制剂。在一些实施例中,多能干细胞是ipsc、或初始ipsc、或包含一种或多种遗传印记的ipsc;并且ipsc中所包含的一种或多种遗传印记保留于自其分化的造血细胞中。在用于引导多能干细胞分化成造血谱系细胞的一些实施例中,多能干细胞分化成造血谱系细胞缺乏产生类胚胎体,并且呈单层培养形式。
在上述方法的一些实施例中,所得多能干细胞衍生永久性生血内皮细胞是cd34+。在一些实施例中,所得永久性生血内皮细胞是cd34+cd43-。在一些实施例中,永久性生血内皮细胞是cd34+cd43-cxcr4-cd73-。在一些实施例中,永久性生血内皮细胞是cd34+cxcr4-cd73-。在一些实施例中,永久性生血内皮细胞是cd34+cd43-cd93-。在一些实施例中,永久性生血内皮细胞是cd34+cd93-。
在上述方法的一些实施例中,所述方法进一步包含(i)使多能干细胞衍生永久性生血内皮细胞与组合物接触以启动所述永久性生血内皮细胞分化成前t细胞祖细胞,所述组合物包含rock抑制剂、一种或多种生长因子和细胞因子和任选存在的bmp活化剂,所述细胞因子选自由以下组成的组:vegf、bfgf、scf、flt3l、tpo和il7;(ii)使所述前t细胞祖细胞与组合物接触以启动所述前t细胞祖细胞分化成t细胞祖细胞或t细胞,所述组合物包含一种或多种生长因子和选自由scf、flt3l和il7组成的群组的细胞因子,但不含vegf、bfgf、tpo、bmp活化剂和rock抑制剂中的一种或多种。在所述方法的一些实施例中,所述多能干细胞衍生t细胞祖细胞是cd34+cd45+cd7+。在所述方法的一些实施例中,所述多能干细胞衍生t细胞祖细胞是cd45+cd7+。
在用于引导多能干细胞分化成造血谱系细胞的上述方法的又一些实施例中,所述方法进一步包含:(i)使多能干细胞衍生永久性生血内皮细胞与组合物接触,以启动所述永久性生血内皮细胞分化成前nk细胞祖细胞,所述组合物包含rock抑制剂、一种或多种生长因子和细胞因子以及任选存在的bmp活化剂,所述细胞因子选自由以下组成的组:vegf、bfgf、scf、flt3l、tpo、il3、il7和il15;和任选地,(ii)使多能干细胞衍生前nk细胞祖细胞与包含一种或多种生长因子和细胞因子的组合物接触,以启动所述前nk祖细胞分化成nk细胞祖细胞或nk细胞,所述细胞因子选自由以下组成的群组:scf、flt3l、il3、il7和il15,其中所述培养基不含vegf、bfgf、tpo、bmp活化剂和rock抑制剂中的一种或多种。在一些实施例中,所述多能干细胞衍生nk祖细胞是cd3-cd45+cd56+cd7+。在一些实施例中,所述多能干细胞衍生nk细胞是cd3-cd45+cd56+,以及任选地进一步由nkp46+、cd57+和cd16+定义。
因此,使用上述分化方法可以获得一种或多种ipsc衍生造血细胞群:(i)cd34+he细胞(icd34),使用一种或多种选自impp-a、itc-a2、itc-b2、ink-a2和ink-b2的培养基;(ii)永久性生血内皮细胞(ihe),使用一种或多种选自impp-a、itc-a2、itc-b2、ink-a2和ink-b2的培养基;(iii)永久性hsc,使用一种或多种选自impp-a、itc-a2、itc-b2、ink-a2和ink-b2的培养基;(iv)多潜能祖细胞(impp),使用impp-a;(v)t细胞祖细胞(ipro-t),使用一种或多种选自itc-a2和itc-b2的培养基;(vi)t细胞(itc),使用itc-b2;(vii)nk细胞祖细胞(ipro-nk),使用一种或多种选自ink-a2和ink-b2的培养基;和/或(viii)nk细胞(ink),和ink-b2。在一些实施例中,所述培养基:
a.icd34-c包含rock抑制剂、一种或多种生长因子和选自由bfgf、vegf、scf、il6、il11、igf和epo组成的群组的细胞因子,和任选存在的wnt路径活化剂;并且不含tgfβ受体/alk抑制剂;
b.impp-a包含bmp活化剂、rock抑制剂和一种或多种生长因子和选自由tpo、il3、gmcsf、epo、bfgf、vegf、scf、il6、flt3l和il11组成的群组的细胞因子;
c.itc-a2包含rock抑制剂、一种或多种生长因子和选自由scf、flt3l、tpo和il7组成的群组的细胞因子;和任选存在的bmp活化剂;
d.itc-b2包含一种或多种生长因子和选自由scf、flt3l和il7组成的群组的细胞因子;
e.ink-a2包括rock抑制剂和选自由以下组成的组的一种或多种生长因子和细胞因子:scf、flt3l、tpo、il3、il7和il15;以及任选地,bmp活化剂,和
f.ink-b2包括选自由scf、flt3l、il7和il15组成的组的一种或多种生长因子和细胞因子。
在一些实施例中,通过以上方法获得的基因组工程化ipsc衍生细胞包括在一个或多个期望整合位点处整合的一个或多个诱导性自杀基因,所述一个或多个期望整合位点包括aavs1、ccr5、rosa26、胶原蛋白、htrp、h11、gapdh、runx1、b2m、tap1、tap2、tap相关蛋白、nlrc5、ciita、rfxank、ciita、rfx5、rfxap、tcrα或β恒定区、nkg2a、nkg2d、cd38、cis、cbl-b、socs2、pd1、ctla4、lag3、tim3或tigit。在一些其它实施例中,基因组工程化ipsc衍生细胞包含编码以下的多核苷酸:安全开关蛋白质、靶向模式、受体、信号传导分子、转录因子、医药学活性蛋白质和肽、药物标靶候选物或促进干细胞和/或祖细胞的运输、归巢、活力、自我更新、存留和/或存活的蛋白质。在一些实施例中,包含一个或多个自杀基因的基因组工程化ipsc衍生细胞进一步包含一个或多个内源性基因中所包含的一种或多种插入/缺失,所述内源性基因与免疫反应调控和介导相关,包括但不限于检查点基因、内源性t细胞受体基因和mhci类抑制基因。在一个实施例中,包含一个或多个自杀基因的基因组工程化ipsc衍生细胞在b2m基因中进一步包含插入/缺失,其中敲除b2m。
另外,可应用于获得第一命运的基因组工程化造血细胞到第二命运的基因组工程化造血细胞的去分化方法和组合物包括例如国际公开案第wo2011/159726号中所描绘的方法和组合物,其公开内容以引入的方式并入本文中。其中提供的方法和组合物允许部分地将起始非多能细胞重编程为非多能中间细胞,这是通过在重编程期间限制内源性nanog基因表达以及使所述非多能中间细胞经历用于使中间细胞分化成所期望细胞类型的条件来实现。在一些实施例中,使用本文中的方法和组合物获得的基因组修饰的ipsc和其衍生细胞包含表1中所列的至少一种基因型。
v.具有由基因工程化ipsc分化的功能模式的衍生免疫细胞的治疗用途
在一些实施例中,本发明提供一种组合物,其包含功能上增强的衍生免疫细胞的分离的群体或亚群,所述免疫细胞使用所公开的方法和组合物由基因组工程化ipsc分化。在一些实施例中,ipsc包含一种或多种靶向基因编辑,其能在ipsc衍生免疫细胞中保留,其中基因工程化ipsc和其衍生细胞适于基于细胞的过继性疗法。在一个实施例中,基因工程化免疫细胞的分离的群体或亚群包含ipsc衍生cd34细胞。在一个实施例中,基因工程化免疫细胞的分离的群体或亚群包含ipsc衍生hsc细胞。在一个实施例中,基因工程化免疫细胞的分离的群体或亚群包含ipsc衍生prot细胞或t细胞。在一个实施例中,基因工程化免疫细胞的分离的群体或亚群包含ipsc衍生pronk细胞或nk细胞。在一个实施例中,基因工程化免疫细胞的分离的群体或亚群包含ipsc衍生免疫调控细胞或骨髓衍生抑制性细胞(mdsc)。在一些实施例中,ipsc衍生基因工程化免疫细胞进一步离体调节以改善治疗潜能。在一个实施例中,已衍生自ipsc的基因工程化免疫细胞的分离的群体或亚群包含增加的数目或比例的初始t细胞、干细胞记忆t细胞和/或中枢记忆t细胞。在一个实施例中,已衍生自ipsc的基因工程化免疫细胞的分离的群体或亚群包含增加的数目或比例的i型nkt细胞。在另一个实施例中,已衍生自ipsc的基因工程化免疫细胞的分离的群体或亚群包含增加的数目或比例的适应性nk细胞。在一些实施例中,衍生自ipsc的基因工程化cd34细胞、hsc细胞、t细胞、nk细胞或骨髓衍生抑制性细胞的分离群体或亚群是同种异体的。在一些其它实施例中,衍生自ipsc的基因工程化cd34细胞、hsc细胞、t细胞、nk细胞或mdsc的分离的群体或亚群是自体的。
在一些实施例中,用于分化的ipsc包含被选择以在效应细胞中传达所期望的治疗属性的遗传印记,其限制条件为分化期间的细胞发育生物学不中断,并且其限制条件为遗传印记在衍生自所述ipsc的分化的造血细胞中保留并且起作用。
在一些实施例中,多能干细胞中的遗传印记包含(i)在将非多能细胞重编程为ipsc期间或之后通过在多能细胞基因组中进行基因组插入、缺失或取代而获得的一种或多种基因修饰模式;或者(ii)对供体、疾病或治疗反应具有特异性的来源特异性免疫细胞的一种或多种能保留治疗属性,并且其中所述多能细胞是由来源特异性免疫细胞重编程,其中所述ipsc保留来源治疗属性,ipsc衍生造血谱系细胞中也包含所述来源治疗属性。
在一些实施例中,基因修饰模式包含以下中的一种或多种:安全开关蛋白质、靶向模式、受体、信号传导分子、转录因子、医药学活性蛋白质和肽、药物标靶候选物;或者促进ipsc或其衍生细胞移植、运输、归巢、活力、自我更新、存留、免疫反应调控和调节和/或存活的蛋白质。在一些实施例中,基因修饰的ipsc和其衍生细胞包含表1中所列的基因型。在一些其它实施例中,包括表1中列出的基因型的经基因修饰的ipsc和其衍生细胞进一步包括另外的经过基因修饰的模式,所述另外的经过基因修饰的模式包括(1)以下的缺失或减少的表达的一种或多种:gapdh、runx1、b2m、tap1、tap2、tap相关蛋白、nlrc5、ciita、rfxank、ciita、rfx5、rfxap、tcrα或β恒定区、nkg2a、nkg2d、cd38、cis、cbl-b、socs2、pd1、ctla4、lag3、tim3或tigit;和(2)hla-e、41bbl、cd3、cd4、cd8、cd47、cd113、cd131、cd137、cd80、pdl1、a2ar、car、tcr、fc受体或用于与双特异性或多特异性或通用衔接子偶联的表面触发性受体的引入或增加的表达。
在再一些其它实施例中,造血谱系细胞包含与以下中的至少两种的组合有关的来源特异性免疫细胞的治疗属性:(i)一种或多种靶向抗原的受体表达;(ii)修饰的hla;(iii)对肿瘤微环境的抗性;(iv)旁观者免疫细胞的募集和免疫调节;(iv)随着肿瘤外效应降低,靶上特异性改善;和(v)归巢、存留、细胞毒性或抗原逃逸拯救改善。
在一些实施例中,ipsc衍生造血细胞包含表1中所列的基因型,并且所述细胞表达至少一种细胞因子和/或其受体,包含il2、il4、il6、il7、il9、il10、il11、il12、il15、il18或il21或其任何被修饰的蛋白质,并且至少表达car和hncd16。在一些实施例中,细胞因子和car的工程化表达具有nk细胞特异性。在一些其它实施例中,细胞因子和car的工程化表达具有t细胞特异性。在一个实施例中,衍生造血细胞的car包含识别cd19、bcma、cd20、cd22、cd123、her2、cd52、egfr、gd2和pdl1抗原中的任一种的结合性结构域。在一些实施例中,抗原特异性衍生效应细胞靶向液体肿瘤。在一些实施例中,抗原特异性衍生效应细胞靶向实体瘤。在一些实施例中,抗原特异性ipsc衍生效应细胞能够挽救肿瘤抗原逃逸。
多种疾病可以通过向适合于过继性细胞疗法的受试者引入本发明的免疫细胞而得到改善。在一些实施例中,所提供的ipsc衍生造血细胞用于同种异体过继性细胞疗法。另外,在一些实施例中,本发明提供上述治疗性组合物通过将所述组合物引入适于过继性细胞疗法的受试者来实现的治疗用途,其中所述受试者患有:自身免疫病症;血液系统恶性肿瘤;实体瘤;或与hiv、rsv、ebv、cmv、腺病毒或bk多瘤病毒相关的感染。
血液系统恶性病的实例包括但不限于急性和慢性白血病(急性骨髓白血病(aml)、急性成淋巴细胞性白血病(all)、慢性骨髓性白血病(cml))、淋巴瘤、非霍奇金氏淋巴瘤(non-hodgkinlymphoma;nhl)、霍奇金氏病、多发性骨髓瘤和骨髓增生异常综合症。实体癌的实例包括但不限于脑癌、前列腺癌、乳腺癌、肺癌、结肠癌、子宫癌、皮肤癌、肝癌、骨癌、胰腺癌、卵巢癌、睾丸癌、膀胱癌、肾癌、头癌、颈癌、胃癌、子宫颈癌、直肠癌、喉癌和食道癌。多种自身免疫病症的实例包括但不限于斑秃、自身免疫性溶血性贫血、自身免疫性肝炎、皮肌炎、糖尿病(1型)、幼年型特发性关节炎的一些形式、肾小球肾炎、格雷夫斯病(graves'disease)、吉兰-巴雷综合症(guillain-barrésyndrome)、特发性血小板减少性紫癜、重症肌无力、心肌炎的一些形式、多发性硬化症、天疱疮/类天疱疮、恶性贫血、结节性多动脉炎、多发性肌炎、原发性胆汁性肝硬化、牛皮癣、类风湿性关节炎、硬皮病/全身性硬化症、薛格连氏综合症(
使用本文所公开的实施例的衍生造血谱系细胞的治疗可在症状后进行或用于防止复发。术语“治疗(treatment、treating)”等在本文中一般用于意指获得所期望的药理学和/或生理学作用。对于疾病和/或可归因于所述疾病的不良作用,所述作用就完全或部分预防疾病来说,可以是防治性的,和/或就部分或完全治愈来说,可以是治疗性的。如本文所用,“治疗”涵盖对受试者疾病的任何干预,并且包括:防止可能易患所述疾病、但尚未被诊断患有其的受试者出现所述疾病;抑制所述疾病,即,阻滞其发展;或缓解所述疾病,即,引起所述疾病消退。可以在疾病或损伤发作之前、期间或之后施用治疗剂或组合物。发展中的疾病的治疗也是备受关注的,其中治疗稳定或减少患者的不期望的临床症状。在特定实施例中,需要治疗的受试者患有可以通过细胞疗法使至少一种相关症状得以含有、改善和/或好转的疾病、病况和/或损伤。某些实施例预期需要细胞疗法的受试者包括但不限于骨髓或干细胞移植候选者、已接受化学疗法或照射疗法的受试者、患有或处于产生过度增殖病症或癌症(例如过度增殖病症或造血系统癌症)的风险下的受试者、患有肿瘤(例如实体瘤)或处于罹患肿瘤的风险下的受试者、患有病毒感染或与病毒感染相关的疾病或处于患有病毒感染或与病毒感染相关的疾病的风险下的受试者。
在评估对包含本文中所公开的实施例的衍生造血谱系细胞的治疗的反应性时,反应可由包含以下中的至少一种的准则来测量:临床效益率、直到死亡的存活期、病理性完全反应、病理性反应的半定量测量、临床完全缓解、临床部分缓解、临床稳定疾病、无再现存活、无转移存活、无疾病存活、循环肿瘤细胞减少、循环标记物反应和实体瘤的反应评估准则(responseevaluationcriteriainsolidtumors;recist)。
可以在其它治疗之前、期间和/或之后在受试者中施用包含如所公开的衍生造血谱系细胞的治疗组合物。因此,组合疗法的方法可涉及在使用另外治疗剂之前、期间和/或之后施用或制备ipsc衍生免疫细胞。如上文所提供,一种或多种另外治疗剂包含肽、细胞因子、检查点抑制剂、丝裂原、生长因子、小rna、dsrna(双链rna)、单核血细胞、饲养细胞、饲养细胞组分或其置换因子、包含一种或多种所关注多核酸的载体、抗体、化学治疗剂或放射性部分或免疫调节药物(imid)。施用ipsc衍生免疫细胞与施用另外治疗剂可以在时间是间隔几小时、几天或甚至几周。另外地或可替代地,施用可与其它生物活性剂或模式组合,所述生物活性剂或模式例如但不限于抗肿瘤剂、非药物疗法,例如手术。
在组合细胞疗法的一些实施例中,治疗组合包含本文所提供的ipsc衍生造血谱系细胞和另外治疗剂,所述另外治疗剂是抗体或抗体片段。在一些实施例中,抗体是一种单克隆抗体。在一些实施例中,抗体可以是人源化抗体、人源化单克隆抗体或嵌合抗体。在一些实施例中,抗体或抗体片段特异性结合于病毒抗原。在其它实施例中,抗体或抗体片段特异性结合于肿瘤抗原。在一些实施例中,肿瘤或病毒特异性抗原激活所施用的ipsc衍生造血谱系细胞以增强其杀伤能力。在一些实施例中,适用于作为另外治疗剂与所施用的ipsc衍生造血谱系细胞的组合治疗的抗体包括但不限于抗cd20(例如利妥昔单抗、维妥珠单抗、奥法木单抗、乌布里图昔单抗、奥卡拉珠单抗、奥比珠单抗)、抗her2(例如曲妥珠单抗、帕妥珠单抗)、抗cd52(阿仑单抗)、抗egfr(例如西妥昔单抗)、抗gd2(例如迪努妥昔单抗)、抗pdl1(例如阿维鲁单抗)、抗cd38(例如达土木单抗、艾沙妥昔单抗、mor202)、抗cd123(例如7g3、csl362)、抗slamf7(埃罗妥珠单抗)和其人源化或fc修饰的变体或片段或其功能等效物和生物仿制药。
在一些实施例中,另外治疗剂包含一种或多种检查点抑制剂。检查点是指细胞分子,通常是细胞表面分子,在不被抑制时能够抑制或下调免疫反应。检查点抑制剂是能够减少检查点基因表达或基因产物或降低检查点分子活性的拮抗剂。适用于与如本文所提供的衍生效应细胞(包括nk细胞或t细胞)的组合疗法的检查点抑制剂包括但不限于pd-1(pdcdl、cd279)、pdl-1(cd274)、tim-3(havcr2)、tigit(wucam和vstm3)、lag-3(lag3、cd223)、ctla-4(ctla4、cd152)、2b4(cd244)、4-1bb(cd137)、4-1bbl(cd137l)、a2ar、bate、btla、cd39(entpdl)、cd47、cd73(nt5e)、cd94、cd96、cd160、cd200、cd200r、cd274、ceacam1、csf-1r、foxpl、garp、hvem、ido、edo、tdo、lair-1、mica/b、nr4a2、mafb、oct-2(pou2f2)、视黄酸受体α(rara)、tlr3、vista、nkg2a/hla-e和抑制性kir(例如2dl1、2dl2、2dl3、3dl1和3dl2)的拮抗剂。
包含所提供的衍生效应细胞的组合疗法的一些实施例进一步包含至少一种靶向检查点分子的抑制剂。具有所提供的衍生效应细胞的组合疗法的一些其它实施例包含两种、三种或更多种抑制剂,以使得靶向两种、三种或更多种检查点分子。在一些实施例中,用于如本文所述的组合疗法的效应细胞是如所提供的衍生nk细胞。在一些实施例中,用于如本文所述的组合疗法的效应细胞是衍生t细胞。在一些实施例中,如本文所提供,用于组合疗法的衍生nk细胞或t细胞在功能上增强。在一些实施例中,两种、三种或更多种检查点抑制剂可以在施用衍生效应细胞同时、之前或之后在组合疗法中施用。在一些实施例中,两种或更多种检查点抑制剂同时或一次一个地(依序)施用。
在一些实施例中,抑制以上检查点分子中的任一种的拮抗剂是抗体。在一些实施例中,检查点抑制性抗体可以是鼠类抗体、人类抗体、人源化抗体、骆驼ig、只有重链的鲨鱼抗体(vnar)、ignar、嵌合抗体、重组抗体或其抗体片段。抗体片段的非限制性实例包括f(ab)′2、f(ab)′3、fv、单链抗原结合性片段(scfv)、(scfv)2、二硫键稳定的fv(dsfv)、微型抗体、双功能抗体、三功能抗体、四功能抗体、单域抗原结合性片段(sdab,纳米抗体)、只有重链的重组抗体(vhh)和维持全部抗体的结合特异性的其它抗体片段,其比起全部抗体可以更有成本效益地产生、更易于使用或更敏感。在一些实施例中,一种、或两种、或三种、或更多种检查点抑制剂包含阿特珠单抗、阿维鲁单抗、度伐单抗、伊匹单抗、iph4102、iph43、iph33、利瑞木单抗、莫纳利珠单抗、纳武单抗、帕博利珠单抗和其衍生物或功能等效物中的至少一种。
包含衍生效应细胞和一种或多种检查抑制剂的组合疗法适用于治疗液体和实体癌,其包括但不限于皮肤t细胞淋巴瘤、非霍奇金氏淋巴瘤(nhl)、蕈样真菌病(mycosisfungoide)、变形性骨炎网状细胞增生症(pagetoidreticulosis)、塞氏综合症(sezarysyndrome)、肉芽肿性皮肤松弛、淋巴瘤样丘疹病、慢性苔癣样糠疹(pityriasislichenoideschronica)、急性苔癣痘疹样糠疹(pityriasislichenoidesetvarioliformisacuta)、cd30+皮肤t细胞淋巴瘤、继发性皮肤cd30+大细胞淋巴瘤、非蕈样真菌病cd30皮肤大t细胞淋巴瘤、多形性t细胞淋巴瘤、伦纳特淋巴瘤(lennertlymphoma)、皮下t细胞淋巴瘤、血管中心性淋巴瘤(angiocentriclymphoma)、母细胞nk细胞淋巴瘤(blasticnk-celllymphoma)、b细胞淋巴瘤、霍奇金氏淋巴瘤(hl)、头颈部肿瘤;鳞状细胞癌、横纹肌肉瘤(rhabdomyocarcoma)、路易斯肺癌(lewislungcarcinoma,llc)、非小细胞肺癌、食管鳞状细胞癌、食道腺癌、肾细胞癌(rcc)、结肠直肠癌(crc)、急性骨髓白血病(aml)、乳腺癌、胃癌、前列腺小细胞神经内分泌癌瘤(scnc)、肝癌、神经胶母细胞瘤、肝癌、口腔鳞状细胞癌、胰腺癌、甲状腺乳头状癌、肝内胆管细胞癌、肝细胞癌瘤、骨癌、癌转移和鼻咽癌。
在一些实施例中,除如本文所提供的衍生效应细胞外,用于治疗用途的组合包含一种或多种另外治疗剂,其包含化学治疗剂或放射性部分。化学治疗剂是指细胞毒性抗肿瘤剂,即优先杀死肿瘤细胞或中断快速增殖细胞的细胞循环,或发现其根除癌症干细胞并且在治疗上使用其以预防或减少肿瘤细胞生长的化学试剂。化学治疗剂有时也被称作抗肿瘤或细胞毒性药物或药剂,并且在所属领域中是众所周知的。
在一些实施例中,化学治疗剂包含蒽环霉素、烷基化剂、烷基磺酸盐、氮丙啶、乙烯亚胺、甲基三聚氰胺、氮芥、亚硝基脲、抗生素、抗代谢物、叶酸类似物、嘌呤类似物、嘧啶类似物、酶、鬼臼毒素(podophyllotoxin)、含铂剂、干扰素和白细胞介素。示例性化学治疗剂包括但不限于烷基化剂(环磷酰胺、二氯甲二乙胺、马法兰(mephalin)、苯丁酸氮芥(chlorambucil)、六甲基三聚氰胺、噻替派(thiotepa)、白消安(busulfan)、卡莫司汀(carmustine)、洛莫司汀(lomustine)、司莫司汀(semustine))、抗代谢物(甲胺喋呤、氟尿嘧啶、氟尿苷、阿糖胞苷、6-巯基嘌呤、硫鸟嘌呤、喷司他汀(pentostatin))、长春花生物碱(vincaalkaloid)(长春新碱(vincristine)、长春碱(vinblastine)、长春地辛(vindesine))、表鬼臼毒素(依托泊苷(etoposide)、依托泊苷邻苯醌(etoposideorthoquinone)和替尼泊苷(teniposide))、抗生素(道诺霉素(daunorubicin)、小红莓(doxorubicin)、米托蒽醌(mitoxantrone)、双蒽、放线菌素d、普卡霉素(plicamycin)、嘌呤霉素(puromycin)和短杆菌肽d(gramicidined))、太平洋紫杉醇(paclitaxel)、秋水仙碱(colchicine)、细胞松弛素b(cytochalasinb)、吐根素(emetine)、美登素(maytansine)和安吖啶(amsacrine)。另外药剂包括氨苯乙哌啶酮(gminoglutethimide)、顺铂(cisplatin)、卡铂(carboplatin)、丝裂霉素、六甲蜜胺(altretamine)、环磷酰胺、洛莫司汀(ccnu)、卡莫司汀(bcnu)、伊立替康(cpt-11)、阿仑单抗、六甲蜜胺、阿那曲唑(anastrozole)、l-天冬酰胺酶、阿扎胞苷(azacitidine)、贝伐单抗(bevacizumab)、贝瑟罗汀(bexarotene)、博莱霉素(bleomycin)、硼替佐米(bortezomib)、白消安、二甲睾酮calusterone)、卡培他滨(capecitabine)、塞内昔布(celecoxib)、西妥昔单抗、克拉屈滨(clofurabine)、阿糖胞苷、达卡巴嗪(dacarbazine)、地尼白介素(denileukindiftitox)、己烯雌酚(diethlstilbestrol)、多西他赛(docetaxel)、甲雄烷醇酮(dromostanolone)、表柔比星(epirubicin)、埃罗替尼(erlotinib)、雌莫司汀(estramustine)、依托泊苷、乙炔基雌二醇、依西美坦(exemestane)、氟尿苷(floxuridine)、5-氟尿嘧啶、氟达拉滨(fludarabine)、氟他胺(flutamide)、氟维司群(fulvestrant)、吉非替尼(gefitinib)、吉西他滨(gemcitabine)、戈舍瑞林(goserelin)、羟基脲、异贝莫单抗(ibritumomab)、艾达霉素(idarubicin)、异环磷酰胺(ifosfamide)、伊马替尼(imatinib)、干扰素α(2a、2b)、伊立替康、来曲唑(letrozole)、甲酰四氢叶酸(leucovorin)、亮丙立德(leuprolide)、左旋咪唑(levamisole)、氮芥、甲地孕酮(megestrol)、马法兰、巯基嘌呤、甲胺喋呤、甲氧呋豆素(methoxsalen)、丝裂霉素c、米托坦(mitotane)、米托蒽醌、诺龙(nandrolone)、诺非单抗(nofetumomab)、奥沙利铂(oxaliplatin)、太平洋紫杉醇、帕米膦酸盐(pamidronate)、培美曲塞(pemetrexed)、培加酶(pegademase)、培门冬酶(pegasparagase)、喷司他汀(pentostatin)、哌泊溴烷(pipobroman)、普卡霉素(plicamycin)、聚苯丙生(polifeprosan)、卟吩姆(porfimer)、丙卡巴肼(procarbazine)、奎纳克林(quinacrine)、利妥昔单抗(rituximab)、沙格司亭(sargramostim)、链脲菌素(streptozocin)、他莫昔芬(tamoxifen)、替莫唑胺(temozolomide)、替尼泊苷(teniposide)、睾内酯(testolactone)、硫鸟嘌呤(thioguanine)、噻替派、拓扑替康(topetecan)、托瑞米芬(toremifene)、托西莫单抗(tositumomab)、曲妥珠单抗(trastuzumab)、维甲酸(tretinoin)、尿嘧啶芥(uracilmustard)、伐柔比星(valrubicin)、长春瑞宾(vinorelbine)和唑来膦酸盐(zoledronate)。其它合适药剂是批准用于人类用途的药剂,包括将批准作为化学治疗剂或放射治疗剂并且所属领域中已知的药剂。这类药剂可由多个标准医师和肿瘤学家参考文献(例如《古德曼和吉尔曼治疗学的药理学基础(goodman&gilman'sthepharmacologicalbasisoftherapeutics)》,第9版,mcgraw-hill,n.y.,1995)中的任一种或由国家癌症研究所网站(fda.gov/cder/cancer/druglistfrarne.htm)引用,两者都会不时更新。
例如沙立度胺(thalidomide)、来那度胺(lenalidomide)和泊马度胺(pomalidomide)的免疫调节药物(imid)刺激nk细胞和t细胞两者。如本文所提供,imid可与ipsc衍生治疗性免疫细胞一起用于癌症治疗。
除治疗性组合物中包括的ipsc衍生造血谱系细胞的分离的群体外,适于向患者施用的组合物还可包括一种或多种医药学上可接受的载体(添加剂)和/或稀释剂(例如,药物学上可接受的培养基,例如细胞培养基)或其它药物学上可接受的组分。医药学上可接受的载体和/或稀释剂部分地由所施用的特定组合物以及用于施用治疗组合物的特定方法决定。因此,本发明的治疗组合物存在多种合适的配方(参见例如《雷明顿氏医药科学(remington'spharmaceuticalsciences)》第17版,1985,其公开内容以全文引用的方式并入本文中)。
在一个实施例中,治疗组合物包含利用本文中所公开的方法和组合物制造的多能细胞衍生t细胞。在一个实施例中,治疗组合物包含利用本文中所公开的方法和组合物制造的多能细胞衍生nk细胞。在一个实施例中,治疗组合物包含利用本文中所公开的方法和组合物制造的多能细胞衍生cd34+he细胞。在一个实施例中,治疗组合物包含利用本文中所公开的方法和组合物制造的多能细胞衍生hsc。在一个实施例中,治疗组合物包含利用本文中所公开的方法和组合物制造的多能细胞衍生mdsc。可以通过静脉内、腹膜内、肠内或气管施用方法分开施用或与其它合适的化合物组合施用包含如本文所公开的ipsc衍生造血谱系细胞的群体的治疗组合物以实现所期望的治疗目标。
这些医药学上可接受的载体和/或稀释剂可以按照足以使治疗组合物的ph维持在约3与约10之间的量存在。因而,缓冲剂可以占总组合物的高达约5%(重量/重量)。治疗组合物中还可以包括电解质,例如但不限于氯化钠和氯化钾。在一个方面中,治疗组合物的ph在约4到约10的范围内。可替代地,治疗组合物的ph在约5到约9的范围内、在约6到约9的范围内或在约6.5到约8的范围内。在另一个实施例中,治疗组合物包括ph在所述ph范围中的一种的缓冲液。在另一个实施例中,治疗组合物的ph是约7。可替代地,治疗组合物的ph在约6.8到约7.4的范围内。在再另一个实施例中,治疗组合物的ph是约7.4。
本发明还部分地提供医药学上可接受的细胞培养基在本发明的特定组合物和/或培养物中的用途。这类组合物适于向人类受试者施用。一般来说,支持根据本发明的实施例的ipsc衍生免疫细胞的维持、生长和/或健康的任何培养基适用作医药学细胞培养基。在特定实施例中,医药学上可接受的细胞培养基是无血清和/或无饲养层的培养基。在各种实施例中,无血清培养基是无动物成分的,并且可以任选地是无蛋白质的。任选地,所述培养基可以含有生物医药学上可接受的重组蛋白。无动物成分培养基是指其中所述组分来源于非动物来源的培养基。重组蛋白置换无动物成分培养基中的原生动物蛋白质并且营养是从合成、植物或微生物来源获得。相比之下,无蛋白质培养基定义为实质上不含蛋白质。所属领域的技术人员将了解,上述培养基实例具有说明性并且决不限制适用于本发明的培养基配方,存在许多已知的且可供所属领域的技术人员使用的合适培养基。
分离的多能干细胞衍生造血谱系细胞可具有至少50%、60%、70%、80%、90%、95%、98%或99%的t细胞、nk细胞、nkt细胞、prot细胞、pronk细胞、cd34+he细胞、hsc、b细胞、骨髓衍生抑制细胞(mdsc)、调控巨噬细胞、调控树突状细胞或间充质基质细胞。在一些实施例中,分离的多能干细胞衍生造血谱系细胞具有约95%到约100%的t细胞、nk细胞、prot细胞、pronk细胞、cd34+he细胞或骨髓衍生抑制细胞(mdsc)。在一些实施例中,本发明提供具有经纯化的t细胞或nk细胞的治疗组合物,例如具有约95%的t细胞、nk细胞、prot细胞、pronk细胞、cd34+he细胞或骨髓衍生抑制细胞(mdsc)的分离群体的组合物以治疗需要细胞疗法的受试者。
在一个实施例中,组合细胞疗法包括治疗抗体或其片段以及衍生自包括表1中列出的基因型的基因组工程化ipsc的nk细胞群体,其中衍生nk细胞包括hncd16。在另一个实施例中,组合细胞疗法包括治疗抗体或其片段以及衍生自包括表1中列出的基因型的基因组工程化ipsc的t细胞群体,其中衍生t细胞包括hncd16。在一些实施例中,组合细胞疗法包括以下中的至少一种:利妥昔单抗、维妥珠单抗、奥法木单抗、乌布里图昔单抗、奥卡拉珠单抗、奥比珠单抗、曲妥珠单抗、帕妥珠单抗、阿仑单抗、西妥昔单抗、迪努妥昔单抗、阿维鲁单抗、达土木单抗、艾沙妥昔单抗、mor202、7g3、csl362和埃罗妥珠单抗;和衍生自包含表1中列出的基因型的基因组工程化ipsc的nk细胞或t细胞群体,其中衍生nk细胞或t细胞包括hncd16。在又一些其它实施例中,组合细胞疗法包含埃罗妥珠单抗以及衍生自包含表1中所列的基因型的基因组工程化ipsc的nk细胞或t细胞的群体,其中衍生nk细胞或t细胞包含hncd16和靶向cd19、bcma、cd38、cd20、cd22或cd123的car。在另外一些另外实施例中,组合细胞疗法包含利妥昔单抗以及衍生自包含表1中所列的基因型的基因组工程化ipsc的nk细胞或t细胞的群体,其中衍生nk细胞或t细胞包含hncd16和car以及一种或多种外源性细胞因子。
如所属领域的普通技术人员将理解,基于本文中的方法和组合物的衍生自ipsc的自体和同种异体造血谱系细胞两者可在如上所述的细胞疗法中使用。对于自体移植来说,衍生造血谱系细胞的分离群体相对于患者是完全或部分hla匹配的。在另一个实施例中,衍生造血谱系细胞不与受试者hla匹配,其中衍生造血谱系细胞是hlai和hlaii剔除型的nk细胞或t细胞。
在一些实施例中,治疗组合物中衍生造血谱系细胞的数目是每剂量至少0.1×105个细胞、至少1×105个细胞、至少5×105个细胞、至少1×106个细胞、至少5×106个细胞、至少1×107个细胞、至少5×107个细胞、至少1×108个细胞、至少5×108个细胞、至少1×109个细胞或至少5×109个细胞。在一些实施例中,治疗组合物中衍生造血谱系细胞的数目是每剂量约0.1×105个细胞到约1×106个细胞;每剂量约0.5×106个细胞到约1×107个细胞;每剂量约0.5×107个细胞到约1×108个细胞;每剂量约0.5×108个细胞到约1×109个细胞;每剂量约1×109个细胞到约5×109个细胞;每剂量约0.5×109个细胞到约8×109个细胞;每剂量约3×109个细胞到约3×1010个细胞或其间任何范围。一般来说,1×108个细胞/剂量转化为对于60kg的患者1.67×106个细胞/千克。
在一个实施例中,治疗组合物中衍生造血谱系细胞的数目是部分或单一脐带血中的免疫细胞数目,或是至少0.1×105个细胞/千克体重、至少0.5×105个细胞/千克体重、至少1×105个细胞/千克体重、至少5×105个细胞/千克体重、至少10×105个细胞/千克体重、至少0.75×106个细胞/千克体重、至少1.25×106个细胞/千克体重、至少1.5×106个细胞/千克体重、至少1.75×106个细胞/千克体重、至少2×106个细胞/千克体重、至少2.5×106个细胞/千克体重、至少3×106个细胞/千克体重、至少4×106个细胞/千克体重、至少5×106个细胞/千克体重、至少10×106个细胞/千克体重、至少15×106个细胞/千克体重、至少20×106个细胞/千克体重、至少25×106个细胞/千克体重、至少30×106个细胞/千克体重、1×108个细胞/千克体重、5×108个细胞/千克体重或1×109个细胞/千克体重。
在一个实施例中,向受试者递送一定剂量的衍生造血谱系细胞。在一个说明性实施例中,向受试者提供的细胞的有效量是至少2×106个细胞/千克、至少3×106个细胞/千克、至少4×106个细胞/千克、至少5×106个细胞/千克、至少6×106个细胞/千克、至少7×106个细胞/千克、至少8×106个细胞/千克、至少9×106个细胞/千克或至少10×106个细胞/千克或更多个细胞/千克,包括所有介于中间的细胞剂量。
在另一个说明性实施例中,向受试者提供的细胞的有效量是约2×106个细胞/千克、约3×106个细胞/千克、约4×106个细胞/千克、约5×106个细胞/千克、约6×106个细胞/千克、约7×106个细胞/千克、约8×106个细胞/千克、约9×106个细胞/千克或约10×106个细胞/千克或更多个细胞/千克,包括所有介于中间的细胞剂量。
在另一说明性实施例中,向受试者提供的细胞的有效量是约2×106个细胞/千克到约10×106个细胞/千克、约3×106个细胞/千克到约10×106个细胞/千克、约4×106个细胞/千克到约10×106个细胞/千克、约5×106个细胞/千克到约10×106个细胞/千克、2×106个细胞/千克到约6×106个细胞/千克、2×106个细胞/千克到约7×106个细胞/千克、2×106个细胞/千克到约8×106个细胞/千克、3×106个细胞/千克到约6×106个细胞/千克、3×106个细胞/千克到约7×106个细胞/千克、3×106个细胞/千克到约8×106个细胞/千克、4×106个细胞/千克到约6×106个细胞/千克、4×106个细胞/千克到约7×106个细胞/千克、4×106个细胞/千克到约8×106个细胞/千克、5×106个细胞/千克到约6×106个细胞/千克、5×106个细胞/千克到约7×106个细胞/千克、5×106个细胞/千克到约8×106个细胞/千克或6×106个细胞/千克到约8×106个细胞/千克,包括所有介于中间的细胞剂量。
在一些实施例中,衍生造血谱系细胞的治疗用途是单剂量治疗。在一些实施例中,衍生造血谱系细胞的治疗用途是多剂量治疗。在一些实施例中,多剂量治疗是每天、每3天、每7天、每10天、每15天、每20天、每25天、每30天、每35天、每40天、每45天或每50天或期间任何天数一次剂量。
包含本发明的衍生造血谱系细胞群的组合物可以是无菌的,并且可以适于施用和备好施用(即,可以在不进行任何进一步处理的情况下施用)给人类患者。准备好用于施用的基于细胞的组合物意指所述组合物在移植或施用到受试者之前不需要任何另外的加工或操纵。在其它实施例中,本发明提供在与一种或多种药剂一起施用之前扩增和/或调节的衍生造血谱系细胞的分离群体。对于被基因工程化以表达重组tcr或car的衍生造血谱系细胞,可使用如例如美国专利6,352,694中所述的方法激活和扩增细胞。
在某些实施例中,可以利用不同方案向衍生造血谱系细胞提供主要刺激信号和共刺激信号。举例来说,提供每种信号的试剂可以存在于溶液中或与表面偶联。与表面偶联时,所述试剂可以与相同表面(即,“顺式”形式)或个别表面(即,“反式”形式)偶联。可替代地,一种试剂可以与表面偶联并且另一种试剂存在于溶液中。在一个实施例中,提供共刺激信号的试剂可以结合到细胞表面并且提供主要激活信号的试剂存在于溶液中或与表面偶联。在某些实施例中,两种试剂都可以存在于溶液中。在另一个实施例中,试剂可呈可溶形式,并且然后交联到表面,例如表达fc受体的细胞或抗体或其它粘合剂,其将结合于例如美国专利申请公开案第20040101519号和第20060034810号中所公开的试剂以用于人工抗原呈递细胞(aapc),其预期在本发明的实施例中用于激活和扩增t淋巴细胞。
剂量、频率和方案必然会出现一些变化,这取决于所治疗受试者的病况。负责施用的人员将在任何情况下确定单独的受试者的合适剂量、频率和方案。
实例
以下实例是为了说明,而非为了限制而提供。
实例1——材料和方法
为了在与不同安全港基因座整合策略组合的不同启动子的控制下有效选择和测试自杀系统,使用本申请人的一种专用的hipsc平台,其能够完成单一细胞传代和高通量的基于96孔板的流式细胞术分选,以便得到具有单一或多种基因调节的克隆hipsc。
hipsc在小分子培养物中的维持:hipsc按常规方式,在培养物融合度达到75%-90%后,即作为单一细胞传代。单一细胞解离时,hipsc用pbs(mediatech)洗涤一次并且在37℃下用阿库酶(accutase)(millipore)处理3-5分钟,随后移液以确保单一细胞解离。然后将单一细胞悬浮液与传统培养基等体积混合,在225×g下离心4分钟,再悬浮于fmm中并且接种于基质胶涂布的表面上。传代数通常为1:6-1:8,转移预先涂有基质胶的组织培养板在37℃下维持2-4小时并且每2-3天用fmm饲养。细胞培养物在设定为37℃和5%co2的增湿培育箱中维持。
用zfn、crispr进行人类ipsc工程化以靶向编辑相关模式:使用rosa26靶向插入作为实例,对于zfn介导的基因组编辑,两百万个ipsc用2.5μgzfn-l(ftv893)、2.5μgzfn-r(ftv894)和5μg供体构建体的混合物转染以进行aavs1靶向插入。对于crispr介导的基因组编辑,用5μgrosa26-grna/cas9(ftv922)和5μg供体构建体的混合物转染两百万个ipsc以进行rosa26靶向插入。使用neon转染系统(生命技术公司(lifetechnologies))、使用参数1500v、10ms、3个脉冲进行转染。转染后第2天或第3天,如果所述质粒含有人工启动子驱动gfp和/或rfp表达盒,那么利用流式细胞术测量转染效率。转染后第4天,将嘌呤霉素按照开始7天0.1μg/ml和随后7天0.2μg/ml的浓度添加到培养基中以选择靶细胞。在嘌呤霉素选择期间,在第10天将细胞传代到基质胶涂布的新制孔上。在嘌呤霉素选择的第16天或更晚,通过流式细胞术分析存活细胞的gfp+ips细胞百分比。
基因组编辑的ipsc的批量分选和克隆分选:嘌呤霉素选择20天之后,对使用zfn或crispr-cas9进行基因组靶向编辑的ipsc进行gfp+ssea4+tra181+ipsc的批量分选和克隆分选。将单一细胞解离的靶向ipsc池再悬浮于冷却的染色缓冲液中,所述缓冲液含有汉克氏平衡盐溶液(hanks'balancedsaltsolution)(mediatech)、4%胎牛血清(invitrogen)、1×青霉素/链霉素(mediatech)和10mmhepes(mediatech);新鲜制备以达到最优效能。向细胞溶液中添加所结合的一级抗体,包括ssea4-pe、tra181-alexafluor-647(bdbiosciences),并且在冰上培育15分钟。所有抗体都以每百万个细胞7μl/100μl染色缓冲液使用。所述溶液在染色缓冲液中洗涤一次,在225g下离心4分钟并且再悬浮于含有10μm噻唑维的染色缓冲液中并且在冰上维持以供流式细胞术分选。对facsariaii(bdbiosciences)进行流式细胞术分选。批量分选时,将gfp+ssea4+tra181+细胞门控和分选到装填有7mlfmm的15ml标准管中。对于克隆分选,使用100μm喷嘴,按照每孔3个事件的浓度,将分选出的细胞直接喷射到96孔板中。每个孔预装填有200μlfmm,所述fmm补充有5μg/ml纤维结合蛋白和1x青霉素/链霉素(mediatech)并且预先经5x基质胶涂布整夜。5x基质胶预涂布包括将一个基质胶等分试样添加到5mldmem/f12中,然后在4℃下培育整夜以允许适当再悬浮并且最终以每孔50μl添加到96孔板中,随后在37℃下培育整夜。紧接在将培养基添加到各孔之前抽吸5x基质胶。完成分选后,在培育之前,96孔板在225g下离心1到2分钟。培养板保持不受干扰七天。第七天,从每个孔中去除150μl培养基并且用100μlfmm置换。分选后第10天,孔中再进料到另外100μlfmm中。早在第2天就检测出群落形成并且大部分群落在分选后第7天到第10天之间扩增。在第一次传代中,各孔用pbs洗涤且在37℃下用30μl阿库酶解离约10分钟。需要延长阿库酶处理反映了长期培养中已闲置的群落的紧密性。发现细胞解离之后,将200μlfmm添加到每个孔中并且吸移若干次以使群落破碎。将解离的菌落转移到此前涂布有5x基质胶的96孔培养板的另一孔,并且随后在培育之前在225g下离心2分钟。扩增之前,进行这种1:1传代以扩展早期群落。后续传代按常规方式用阿库酶处理3-5分钟并且在fmm中、在预先涂有1x基质胶的较大孔中达到75-90%融合度后以1:4-1:8扩增。分析每种克隆细胞系的gfp荧光水平和tra1-81表达水平。选择近似100%gfp+和tra1-81+的克隆系用于进一步pcr筛检和分析。在guavaeasycyte8ht(millipore)上进行流式细胞术分析并且使用flowjo(flowjo,llc)分析。
实例2——自主衍生细胞的细胞表面表达的细胞因子的构建体和设计
在本申请案中,展示置换外源性可溶性重组细胞因子不仅支持来自ipsc的造血细胞的体外得到而且支持衍生效应细胞的体内存留和存活。通过避免全身性高剂量施用临床上相关细胞因子,由于这类实践的剂量限制性毒性的风险降低,同时建立细胞因子介导的细胞自主性。图1呈现使用il15作为说明性实例的几种构建体设计。特定来说,设计3证实具有截短胞内结构域的il15rα通过接头在c端与il15融合,模拟il15的反式呈递,并且维持il15膜结合,并且另外消除潜在顺式呈递。作为设计3的替代方案,除胞外sushi结构域以外,设计4基本上去除了完整的il15rα,所述胞外sushi结构域在一端与il15融合,并且在另一端与跨膜结构域(mb-sushi)融合,任选地与位于suchi结构域与跨膜结构域之间的接头融合。融合il5/mb-sushi通过任何结合膜蛋白的跨膜结构域在细胞表面上表达。在例如设计3或4的构建体的情况下,在只保留期望的il15的反式呈递时,消除通过il15rα的不必要的信号传导,包含顺式呈递。
实例3——ipsc的逐步工程化和修饰的衍生nk细胞的验证
使用示例性nkg2c-p2a-cd94-t2a-dap12构建体,对诱导性多能干细胞(ipsc)进行工程化以获得nkg2c、cd94和dap12表达,所述构建体具有由seqidno:17表示的氨基序列。
seqidno:17
mnkqrgtfsevslaqdpkrqqrkpkgnkssisgteqeifqvelnlqnpslnhqgidkiydcqgllpppekltaevlgiicivlmatvlktivlipfleqnnfspntrtqkarhcghcpeewitysnscyyigkerrtweesllactsknssllsidneeemkflasilpsswigvfrnsshhpwvtinglafkhkikdsdnaelncavlqvnrlksaqcgssmiyhckhklgsgatnfsllkqagdveenpgpmavfkttlwrlisgtlgiiclslmstlgillknsftklsiepaftpgpnielqkdsdccscqekwvgyrcncyfisseqktwnesrhlcasqkssllqlqntdeldfmsssqqfywiglsyseehtawlwengsalsqylfpsfetfntknciaynpngnaldescedknryickqqligsgegrgslltcgdveenpgpmgglepcsrllllplllavsglrpvqaqaqsdcscstvspgvlagivmgdlvltvlialavyflgrlvprgrgaaeaatrkqritetespyqelqgqrsdvysdlntqrpyyk
(氨基酸序列:nkg2c-p2a-cd94-t2a-dap12)
在工程化步骤之后,针对期望的表型对ipsc进行分类。图2a示出了在工程化ipsc中nkg2c的细胞表面表达。工程化ipsc分化为cd34+造血祖细胞,并且随后使用逐步分化和扩增策略分化为cd56+nk细胞(ink细胞)。如通过facs确定的,在未经修饰的ink细胞上,表面nkg2c表达很低(约5-10%)。观察到仅衍生自nkg2c的ipsc系的ink细胞表面上的nkg2c的水平较高(40-60%)(图3a),这证明转基因nkg2c可以与内源性cd94和dap12配对以在细胞表面上形成稳定的结构。重要的是,表面nkg2c表达在衍生自nkg2c/dap12系的ink细胞上最高(70-85%),这证明用nkg2a和dap12组分两者对系进行工程化的重要性。图3bmfi在nkg2c/dap12ink系中也较高,这表明阳性细胞中nkg2c的表面水平较高。
为了通过nkg2c在ink细胞上的接合来验证功能,使用重定向抗体依赖性细胞毒性(adcc)测定,其中p815细胞(其与抗体的fc部分结合)包覆有处于一定浓度范围(0.01-10μg/ml)的单克隆抗nkg2c激动剂抗体,并且与未经修饰的ink细胞、nkg2cink细胞或nkg2c/dap12ink细胞共培养。据发现在所有测试浓度下,nkg2c/dap12ink细胞表现出最强的功能应答,如通过表面cd107a表达、干扰素γ(ifnγ)产生和肿瘤坏死因子(tnf)产生的频率所测量,其中nkg2cink细胞表现出中等功能应答(图4)。
先前已经示出了ipsc含有高亲和力不可切割的cd16(hncd16)表达、car、通过敲除b2m基因的hla-i丢失、通过敲除ciita的hla-ii丢失、非经典hla分子hla-g的过表达和连接的il15/il15rα构建体的表达,因此在pct申请号:pct/us2018/067289中也示出了衍生nk或t细胞的表型和相关功能,所述申请的完整公开内容通过引用并入本文。
实例4——具有增强的功能和留存的ipsc衍生自然杀手(nk)细胞
端粒随着细胞老化而缩短并且与干细胞功能障碍和细胞衰老相关。本文中展示,通过定向分化ipsc获得的成熟ink细胞含有相较于成体外周血nk细胞更长的端粒。在针对g0/1细胞的dna指数进行校正的情况下使用1301个t细胞白血病系作为对照(100%),通过流式细胞术来测定ipsc、成体外周血nk细胞和ipsc衍生nk细胞的端粒长度。如图5中所示,当与成体外周血nk细胞(p=.105,anova)相比,ipsc衍生nk细胞维持显著更长的端粒长度,这表示ipsc衍生nk细胞中更大的增殖率、存活率和持久性潜能。
所属领域技术人员将容易地了解,本文所描述的方法、组合物和产物代表示例性实施例,并且不预期限制本发明的范围。对于所属领域的技术人员显而易见的是,可以对本文所公开的本公开进行各种取代和修改而不脱离本发明的范围和精神。
本说明书中提到的所有专利和公开案都指示本公开所属领域的技术人员的技能水平。所有专利和公开案以引用的方式并入,其程度如同每一个别公开案专门并且单独指定为以引用的方式并入。
本文说明性描述的本公开可以在本文未特别公开的任何成分、限制不存在的情况下适当地实施。因此,例如,在本文中的每一种情况下,术语“包含”、“主要由……组成”和“由……组成”中的任一个可由其它两个术语中的任一个替换。已使用的术语和表述是作为描述而非限制的术语使用,并且使用这类术语和表述时,不希望排除所示和所述特点的任何等效物或其一部分,而是应认识到,在所要求的本公开的范围内可以存在各种修改。因此,应理解,虽然本公开已通过优选实施例和任选存在的特点进行特别地公开,但所属领域的技术人员可以对本文中所公开的观点进行修改和变化形式,且这类修改和变化形式被视为属于如所附权利要求书限定的本发明范围内。
序列表
<110>菲特治疗公司
b·瓦拉梅尔
r·比乔戴尔
t·t·李
<120>使用增强的ipsc衍生效应细胞的免疫疗法
<130>056932-516001wo
<150>62/774,278
<151>2018-12-02
<160>17
<170>patentin版本3.5
<210>1
<211>340
<212>prt
<213>人工序列(artificialsequence)
<220>
<223>合成多肽
<220>
<221>misc_feature
<223>340个氨基酸的基于cd64结构域的构造,cd16tm,cd16icd
<400>1
mettrppheleuthrthrleuleuleutrpvalprovalaspglygln
151015
valaspthrthrlysalavalilethrleuglnproprotrpvalser
202530
valpheglnglugluthrvalthrleuhiscysgluvalleuhisleu
354045
proglyserserserthrglntrppheleuasnglythralathrgln
505560
thrserthrprosertyrargilethrseralaservalasnaspser
65707580
glyglutyrargcysglnargglyleuserglyargseraspproile
859095
glnleugluilehisargglytrpleuleuleuglnvalserserarg
100105110
valphethrgluglygluproleualaleuargcyshisalatrplys
115120125
asplysleuvaltyrasnvalleutyrtyrargasnglylysalaphe
130135140
lysphephehistrpasnserasnleuthrileleulysthrasnile
145150155160
serhisasnglythrtyrhiscysserglymetglylyshisargtyr
165170175
thrseralaglyileservalthrvallysgluleupheproalapro
180185190
valleuasnalaservalthrserproleuleugluglyasnleuval
195200205
thrleusercysgluthrlysleuleuleuglnargproglyleugln
210215220
leutyrpheserphetyrmetglyserlysthrleuargglyargasn
225230235240
thrserserglutyrglnileleuthralaargarggluaspsergly
245250255
leutyrtrpcysglualaalathrgluaspglyasnvalleulysarg
260265270
serprogluleugluleuglnvalleuglyleuglnleuprothrpro
275280285
valtrpphehistyrglnvalserphecysleuvalmetvalleuleu
290295300
phealavalaspthrglyleutyrpheservallysthrasnilearg
305310315320
serserthrargasptrplysasphislysphelystrparglysasp
325330335
proglnasplys
340
<210>2
<211>336
<212>prt
<213>人工序列(artificialsequence)
<220>
<223>合成多肽
<220>
<221>misc_feature
<223>336个氨基酸的基于cd64外显子的构造,cd16tm,cd16icd
<400>2
mettrppheleuthrthrleuleuleutrpvalprovalaspglygln
151015
valaspthrthrlysalavalilethrleuglnproprotrpvalser
202530
valpheglnglugluthrvalthrleuhiscysgluvalleuhisleu
354045
proglyserserserthrglntrppheleuasnglythralathrgln
505560
thrserthrprosertyrargilethrseralaservalasnaspser
65707580
glyglutyrargcysglnargglyleuserglyargseraspproile
859095
glnleugluilehisargglytrpleuleuleuglnvalserserarg
100105110
valphethrgluglygluproleualaleuargcyshisalatrplys
115120125
asplysleuvaltyrasnvalleutyrtyrargasnglylysalaphe
130135140
lysphephehistrpasnserasnleuthrileleulysthrasnile
145150155160
serhisasnglythrtyrhiscysserglymetglylyshisargtyr
165170175
thrseralaglyileservalthrvallysgluleupheproalapro
180185190
valleuasnalaservalthrserproleuleugluglyasnleuval
195200205
thrleusercysgluthrlysleuleuleuglnargproglyleugln
210215220
leutyrpheserphetyrmetglyserlysthrleuargglyargasn
225230235240
thrserserglutyrglnileleuthralaargarggluaspsergly
245250255
leutyrtrpcysglualaalathrgluaspglyasnvalleulysarg
260265270
serprogluleugluleuglnvalleuglyleuphepheproprogly
275280285
tyrglnvalserphecysleuvalmetvalleuleuphealavalasp
290295300
thrglyleutyrpheservallysthrasnileargserserthrarg
305310315320
asptrplysasphislysphelystrparglysaspproglnasplys
325330335
<210>3
<211>335
<212>prt
<213>人工序列(artificialsequence)
<220>
<223>合成多肽
<220>
<221>misc_feature
<223>335个氨基酸的基于cd64外显子的构造,cd16tm,cd16icd
<400>3
mettrppheleuthrthrleuleuleutrpvalprovalaspglygln
151015
valaspthrthrlysalavalilethrleuglnproprotrpvalser
202530
valpheglnglugluthrvalthrleuhiscysgluvalleuhisleu
354045
proglyserserserthrglntrppheleuasnglythralathrgln
505560
thrserthrprosertyrargilethrseralaservalasnaspser
65707580
glyglutyrargcysglnargglyleuserglyargseraspproile
859095
glnleugluilehisargglytrpleuleuleuglnvalserserarg
100105110
valphethrgluglygluproleualaleuargcyshisalatrplys
115120125
asplysleuvaltyrasnvalleutyrtyrargasnglylysalaphe
130135140
lysphephehistrpasnserasnleuthrileleulysthrasnile
145150155160
serhisasnglythrtyrhiscysserglymetglylyshisargtyr
165170175
thrseralaglyileservalthrvallysgluleupheproalapro
180185190
valleuasnalaservalthrserproleuleugluglyasnleuval
195200205
thrleusercysgluthrlysleuleuleuglnargproglyleugln
210215220
leutyrpheserphetyrmetglyserlysthrleuargglyargasn
225230235240
thrserserglutyrglnileleuthralaargarggluaspsergly
245250255
leutyrtrpcysglualaalathrgluaspglyasnvalleulysarg
260265270
serprogluleugluleuglnvalleuglyphepheproproglytyr
275280285
glnvalserphecysleuvalmetvalleuleuphealavalaspthr
290295300
glyleutyrpheservallysthrasnileargserserthrargasp
305310315320
trplysasphislysphelystrparglysaspproglnasplys
325330335
<210>4
<211>1032
<212>dna
<213>人工序列(artificialsequence)
<220>
<223>合成多核苷酸
<400>4
cttggagacaacatgtggttcttgacaactctgctcctttgggttccagttgatgggcaa60
gtggacaccacaaaggcagtgatcactttgcagcctccatgggtcagcgtgttccaagag120
gaaaccgtaaccttgcattgtgaggtgctccatctgcctgggagcagctctacacagtgg180
tttctcaatggcacagccactcagacctcgacccccagctacagaatcacctctgccagt240
gtcaatgacagtggtgaatacaggtgccagagaggtctctcagggcgaagtgaccccata300
cagctggaaatccacagaggctggctactactgcaggtctccagcagagtcttcacggaa360
ggagaacctctggccttgaggtgtcatgcgtggaaggataagctggtgtacaatgtgctt420
tactatcgaaatggcaaagcctttaagtttttccactggaattctaacctcaccattctg480
aaaaccaacataagtcacaatggcacctaccattgctcaggcatgggaaagcatcgctac540
acatcagcaggaatatctgtcactgtgaaagagctatttccagctccagtgctgaatgca600
tctgtgacatccccactcctggaggggaatctggtcaccctgagctgtgaaacaaagttg660
ctcttgcagaggcctggtttgcagctttacttctccttctacatgggcagcaagaccctg720
cgaggcaggaacacatcctctgaataccaaatactaactgctagaagagaagactctggg780
ttatactggtgcgaggctgccacagaggatggaaatgtccttaagcgcagccctgagttg840
gagcttcaagtgcttggcctccagttaccaactcctgtctggtttcattaccaagtctct900
ttctgcttggtgatggtactcctttttgcagtggacacaggactatatttctctgtgaag960
acaaacattcgaagctcaacaagagactggaaggaccataaatttaaatggagaaaggac1020
cctcaagacaaa1032
<210>5
<211>1020
<212>dna
<213>人工序列(artificialsequence)
<220>
<223>合成多核苷酸
<400>5
cttggagacaacatgtggttcttgacaactctgctcctttgggttccagttgatgggcaa60
gtggacaccacaaaggcagtgatcactttgcagcctccatgggtcagcgtgttccaagag120
gaaaccgtaaccttgcattgtgaggtgctccatctgcctgggagcagctctacacagtgg180
tttctcaatggcacagccactcagacctcgacccccagctacagaatcacctctgccagt240
gtcaatgacagtggtgaatacaggtgccagagaggtctctcagggcgaagtgaccccata300
cagctggaaatccacagaggctggctactactgcaggtctccagcagagtcttcacggaa360
ggagaacctctggccttgaggtgtcatgcgtggaaggataagctggtgtacaatgtgctt420
tactatcgaaatggcaaagcctttaagtttttccactggaattctaacctcaccattctg480
aaaaccaacataagtcacaatggcacctaccattgctcaggcatgggaaagcatcgctac540
acatcagcaggaatatctgtcactgtgaaagagctatttccagctccagtgctgaatgca600
tctgtgacatccccactcctggaggggaatctggtcaccctgagctgtgaaacaaagttg660
ctcttgcagaggcctggtttgcagctttacttctccttctacatgggcagcaagaccctg720
cgaggcaggaacacatcctctgaataccaaatactaactgctagaagagaagactctggg780
ttatactggtgcgaggctgccacagaggatggaaatgtccttaagcgcagccctgagttg840
gagcttcaagtgcttggtttgttctttccacctgggtaccaagtctctttctgcttggtg900
atggtactcctttttgcagtggacacaggactatatttctctgtgaagacaaacattcga960
agctcaacaagagactggaaggaccataaatttaaatggagaaaggaccctcaagacaaa1020
<210>6
<211>1005
<212>dna
<213>人工序列(artificialsequence)
<220>
<223>合成多核苷酸
<400>6
atgtggttcttgacaactctgctcctttgggttccagttgatgggcaagtggacaccaca60
aaggcagtgatcactttgcagcctccatgggtcagcgtgttccaagaggaaaccgtaacc120
ttgcactgtgaggtgctccatctgcctgggagcagctctacacagtggtttctcaatggc180
acagccactcagacctcgacccccagctacagaatcacctctgccagtgtcaatgacagt240
ggtgaatacaggtgccagagaggtctctcagggcgaagtgaccccatacagctggaaatc300
cacagaggctggctactactgcaggtctccagcagagtcttcacggaaggagaacctctg360
gccttgaggtgtcatgcgtggaaggataagctggtgtacaatgtgctttactatcgaaat420
ggcaaagcctttaagtttttccactggaactctaacctcaccattctgaaaaccaacata480
agtcacaatggcacctaccattgctcaggcatgggaaagcatcgctacacatcagcagga540
atatctgtcactgtgaaagagctatttccagctccagtgctgaatgcatctgtgacatcc600
ccactcctggaggggaatctggtcaccctgagctgtgaaacaaagttgctcttgcagagg660
cctggtttgcagctttacttctccttctacatgggcagcaagaccctgcgaggcaggaac720
acatcctctgaataccaaatactaactgctagaagagaagactctgggttatactggtgc780
gaggctgccacagaggatggaaatgtccttaagcgcagccctgagttggagcttcaagtg840
cttggcttctttccacctgggtaccaagtctctttctgcttggtgatggtactccttttt900
gcagtggacacaggactatatttctctgtgaagacaaacattcgaagctcaacaagagac960
tggaaggaccataaatttaaatggagaaaggaccctcaagacaaa1005
<210>7
<211>153
<212>prt
<213>人工序列(artificialsequence)
<220>
<223>合成多肽
<220>
<221>misc_feature
<223>153个氨基酸的cd28共刺激加cd3-ζ-itam
<400>7
argserlysargserargleuleuhisserasptyrmetasnmetthr
151015
proargargproglyprothrarglyshistyrglnprotyralapro
202530
proargaspphealaalatyrargserargvallyspheserargser
354045
alaaspalaproalatyrglnglnglyglnasnglnleutyrasnglu
505560
leuasnleuglyargarggluglutyraspvalleuasplysargarg
65707580
glyargaspproglumetglyglylysproargarglysasnprogln
859095
gluglyleupheasngluleuglnlysasplysmetalaglualaphe
100105110
sergluileglymetlysglygluargargargglylysglyhisasp
115120125
glyleupheglnglyleuserthralathrlysaspthrpheaspala
130135140
leuhismetglnalaleuproproarg
145150
<210>8
<211>219
<212>prt
<213>人工序列(artificialsequence)
<220>
<223>合成多肽
<220>
<221>misc_feature
<223>219个氨基酸的cd28铰链加cd28tm加cd28共刺激加cd3-ζ-itam
<400>8
ilegluvalmettyrproproprotyrleuaspasnglulysserasn
151015
glythrileilehisvallysglylyshisleucysproserproleu
202530
pheproglyproserlysprophetrpvalleuvalvalvalglygly
354045
valleualacystyrserleuleuvalthrvalalapheileilephe
505560
trpvalargserlysargserargleuleuhisserasptyrmetasn
65707580
metthrproargargproglyprothrarglyshistyrglnprotyr
859095
alaproproargaspphealaalatyrargserargvallyspheser
100105110
argseralaaspalaproalatyrglnglnglyglnasnglnleutyr
115120125
asngluleuasnleuglyargarggluglutyraspvalleuasplys
130135140
argargglyargaspproglumetglyglylysproargarglysasn
145150155160
proglngluglyleupheasngluleuglnlysasplysmetalaglu
165170175
alaphesergluileglymetlysglygluargargargglylysgly
180185190
hisaspglyleupheglnglyleuserthralathrlysaspthrphe
195200205
aspalaleuhismetglnalaleuproproarg
210215
<210>9
<211>263
<212>prt
<213>人工序列(artificialsequence)
<220>
<223>合成多肽
<220>
<221>misc_feature
<223>263个氨基酸的nkg2dtm加2b4加cd3-ζ
<400>9
serasnleuphevalalasertrpilealavalmetileilephearg
151015
ileglymetalavalalailephecyscysphephepheprosertrp
202530
argarglysarglysglulysglnsergluthrserprolysgluphe
354045
leuthriletyrgluaspvallysaspleulysthrargargasnhis
505560
gluglngluglnthrpheproglyglyglyserthriletyrsermet
65707580
ileglnserglnserseralaprothrserglngluproalatyrthr
859095
leutyrserleuileglnproserarglysserglyserarglysarg
100105110
asnhisserproserpheasnserthriletyrgluvalileglylys
115120125
serglnprolysalaglnasnproalaargleuserarglysgluleu
130135140
gluasnpheaspvaltyrserargvallyspheserargseralaasp
145150155160
alaproalatyrlysglnglyglnasnglnleutyrasngluleuasn
165170175
leuglyargarggluglutyraspvalleuasplysargargglyarg
180185190
aspproglumetglyglylysproargarglysasnproglnglugly
195200205
leutyrasngluleuglnlysasplysmetalaglualatyrserglu
210215220
ileglymetlysglygluargargargglylysglyhisaspglyleu
225230235240
tyrglnglyleuserthralathrlysaspthrtyraspalaleuhis
245250255
metglnalaleuproproarg
260
<210>10
<211>308
<212>prt
<213>人工序列(artificialsequence)
<220>
<223>合成多肽
<220>
<221>misc_feature
<223>308个氨基酸的cd8铰链加nkg2dtm加2b4加cd3-ζ
<400>10
thrthrthrproalaproargproprothrproalaprothrileala
151015
serglnproleuserleuargproglualacysargproalaalagly
202530
glyalavalhisthrargglyleuaspphealacysaspserasnleu
354045
phevalalasertrpilealavalmetileilepheargileglymet
505560
alavalalailephecyscysphephepheprosertrpargarglys
65707580
arglysglulysglnsergluthrserprolysglupheleuthrile
859095
tyrgluaspvallysaspleulysthrargargasnhisgluglnglu
100105110
glnthrpheproglyglyglyserthriletyrsermetileglnser
115120125
glnserseralaprothrserglngluproalatyrthrleutyrser
130135140
leuileglnproserarglysserglyserarglysargasnhisser
145150155160
proserpheasnserthriletyrgluvalileglylysserglnpro
165170175
lysalaglnasnproalaargleuserarglysgluleugluasnphe
180185190
aspvaltyrserargvallyspheserargseralaaspalaproala
195200205
tyrlysglnglyglnasnglnleutyrasngluleuasnleuglyarg
210215220
arggluglutyraspvalleuasplysargargglyargaspproglu
225230235240
metglyglylysproargarglysasnproglngluglyleutyrasn
245250255
gluleuglnlysasplysmetalaglualatyrsergluileglymet
260265270
lysglygluargargargglylysglyhisaspglyleutyrglngly
275280285
leuserthralathrlysaspthrtyraspalaleuhismetglnala
290295300
leuproproarg
305
<210>11
<211>414
<212>prt
<213>人工序列(artificialsequence)
<220>
<223>合成多肽
<400>11
metasptrpthrtrpileleupheleuvalalaalaalathrargval
151015
hisserglyilehisvalpheileleuglycyspheseralaglyleu
202530
prolysthrglualaasntrpvalasnvalileseraspleulyslys
354045
ilegluaspleuileglnsermethisileaspalathrleutyrthr
505560
gluseraspvalhisprosercyslysvalthralametlyscysphe
65707580
leuleugluleuglnvalileserleugluserglyaspalaserile
859095
hisaspthrvalgluasnleuileileleualaasnasnserleuser
100105110
serasnglyasnvalthrgluserglycyslysglucysglugluleu
115120125
gluglulysasnilelysglupheleuglnserphevalhisileval
130135140
glnmetpheileasnthrserserglyglyglyserglyglyglygly
145150155160
serglyglyglyglyserglyglyglyglyserglyglyglyserleu
165170175
glnilethrcysproproprometservalgluhisalaaspiletrp
180185190
vallyssertyrserleutyrserarggluargtyrilecysasnser
195200205
glyphelysarglysalaglythrserserleuthrglucysvalleu
210215220
asnlysalathrasnvalalahistrpthrthrproserleulyscys
225230235240
ileargaspproalaleuvalhisglnargproalaproproserthr
245250255
valthrthralaglyvalthrproglnprogluserleuserproser
260265270
glylysgluproalaalaserserproserserasnasnthralaala
275280285
thrthralaalailevalproglyserglnleumetproserlysser
290295300
proserthrglythrthrgluileserserhisgluserserhisgly
305310315320
thrproserglnthrthralalysasntrpgluleuthralaserala
325330335
serhisglnproproglyvaltyrproglnglyhisseraspthrthr
340345350
valalaileserthrserthrvalleuleucysglyleuseralaval
355360365
serleuleualacystyrleulysserargglnthrproproleuala
370375380
servalglumetglualametglualaleuprovalthrtrpglythr
385390395400
serserargaspgluaspleugluasncysserhishisleu
405410
<210>12
<211>1242
<212>dna
<213>人工序列(artificialsequence)
<220>
<223>合成多核苷酸
<400>12
atggactggacctggattctgttcctggtcgcggctgcaacgcgagtccatagcggtatc60
catgtttttattcttgggtgtttttctgctgggctgcctaagaccgaggccaactgggta120
aatgtcatcagtgacctcaagaaaatagaagaccttatacaaagcatgcacattgatgct180
actctctacactgagtcagatgtacatccctcatgcaaagtgacggccatgaaatgtttc240
ctcctcgaacttcaagtcatatctctggaaagtggcgacgcgtccatccacgacacggtc300
gaaaacctgataatactcgctaataatagtctctcttcaaatggtaacgtaaccgagtca360
ggttgcaaagagtgcgaagagttggaagaaaaaaacataaaggagttcctgcaaagtttc420
gtgcacattgtgcagatgttcattaatacctctagcggcggaggatcaggtggcggtgga480
agcggaggtggaggctccggtggaggaggtagtggcggaggttctcttcaaataacttgt540
cctccaccgatgtccgtagaacatgcggatatttgggtaaaatcctatagcttgtacagc600
cgagagcggtatatctgcaacagcggcttcaagcggaaggccggcacaagcagcctgacc660
gagtgcgtgctgaacaaggccaccaacgtggcccactggaccacccctagcctgaagtgc720
atcagagatcccgccctggtgcatcagcggcctgcccctccaagcacagtgacaacagct780
ggcgtgaccccccagcctgagagcctgagcccttctggaaaagagcctgccgccagcagc840
cccagcagcaacaatactgccgccaccacagccgccatcgtgcctggatctcagctgatg900
cccagcaagagccctagcaccggcaccaccgagatcagcagccacgagtctagccacggc960
accccatctcagaccaccgccaagaactgggagctgacagccagcgcctctcaccagcct1020
ccaggcgtgtaccctcagggccacagcgataccacagtggccatcagcacctccaccgtg1080
ctgctgtgtggactgagcgccgtgtcactgctggcctgctacctgaagtccagacagacc1140
cctccactggccagcgtggaaatggaagccatggaagcactgcccgtgacctggggcacc1200
agctccagagatgaggatctggaaaactgctcccaccacctg1242
<210>13
<211>379
<212>prt
<213>人工序列(artificialsequence)
<220>
<223>合成多肽
<400>13
metasptrpthrtrpileleupheleuvalalaalaalathrargval
151015
hisserglyilehisvalpheileleuglycyspheseralaglyleu
202530
prolysthrglualaasntrpvalasnvalileseraspleulyslys
354045
ilegluaspleuileglnsermethisileaspalathrleutyrthr
505560
gluseraspvalhisprosercyslysvalthralametlyscysphe
65707580
leuleugluleuglnvalileserleugluserglyaspalaserile
859095
hisaspthrvalgluasnleuileileleualaasnasnserleuser
100105110
serasnglyasnvalthrgluserglycyslysglucysglugluleu
115120125
gluglulysasnilelysglupheleuglnserphevalhisileval
130135140
glnmetpheileasnthrserserglyglyglyserglyglyglygly
145150155160
serglyglyglyglyserglyglyglyglyserglyglyglyserleu
165170175
glnilethrcysproproprometservalgluhisalaaspiletrp
180185190
vallyssertyrserleutyrserarggluargtyrilecysasnser
195200205
glyphelysarglysalaglythrserserleuthrglucysvalleu
210215220
asnlysalathrasnvalalahistrpthrthrproserleulyscys
225230235240
ileargaspproalaleuvalhisglnargproalaproproserthr
245250255
valthrthralaglyvalthrproglnprogluserleuserproser
260265270
glylysgluproalaalaserserproserserasnasnthralaala
275280285
thrthralaalailevalproglyserglnleumetproserlysser
290295300
proserthrglythrthrgluileserserhisgluserserhisgly
305310315320
thrproserglnthrthralalysasntrpgluleuthralaserala
325330335
serhisglnproproglyvaltyrproglnglyhisseraspthrthr
340345350
valalaileserthrserthrvalleuleucysglyleuseralaval
355360365
serleuleualacystyrleulysserarggln
370375
<210>14
<211>1140
<212>dna
<213>人工序列(artificialsequence)
<220>
<223>合成多核苷酸
<400>14
atggactggacctggattctgttcctggtcgcggctgcaacgcgagtccatagcggtatc60
catgtttttattcttgggtgtttttctgctgggctgcctaagaccgaggccaactgggta120
aatgtcatcagtgacctcaagaaaatagaagaccttatacaaagcatgcacattgatgct180
actctctacactgagtcagatgtacatccctcatgcaaagtgacggccatgaaatgtttc240
ctcctcgaacttcaagtcatatctctggaaagtggcgacgcgtccatccacgacacggtc300
gaaaacctgataatactcgctaataatagtctctcttcaaatggtaacgtaaccgagtca360
ggttgcaaagagtgcgaagagttggaagaaaaaaacataaaggagttcctgcaaagtttc420
gtgcacattgtgcagatgttcattaatacctctagcggcggaggatcaggtggcggtgga480
agcggaggtggaggctccggtggaggaggtagtggcggaggttctcttcaaataacttgt540
cctccaccgatgtccgtagaacatgcggatatttgggtaaaatcctatagcttgtacagc600
cgagagcggtatatctgcaacagcggcttcaagcggaaggccggcacaagcagcctgacc660
gagtgcgtgctgaacaaggccaccaacgtggcccactggaccacccctagcctgaagtgc720
atcagagatcccgccctggtgcatcagcggcctgcccctccaagcacagtgacaacagct780
ggcgtgaccccccagcctgagagcctgagcccttctggaaaagagcctgccgccagcagc840
cccagcagcaacaatactgccgccaccacagccgccatcgtgcctggatctcagctgatg900
cccagcaagagccctagcaccggcaccaccgagatcagcagccacgagtctagccacggc960
accccatctcagaccaccgccaagaactgggagctgacagccagcgcctctcaccagcct1020
ccaggcgtgtaccctcagggccacagcgataccacagtggccatcagcacctccaccgtg1080
ctgctgtgtggactgagcgccgtgtcactgctggcctgctacctgaagtccagacagtga1140
<210>15
<211>242
<212>prt
<213>人工序列(artificialsequence)
<220>
<223>合成多肽
<400>15
metasptrpthrtrpileleupheleuvalalaalaalathrargval
151015
hisserglyilehisvalpheileleuglycyspheseralaglyleu
202530
prolysthrglualaasntrpvalasnvalileseraspleulyslys
354045
ilegluaspleuileglnsermethisileaspalathrleutyrthr
505560
gluseraspvalhisprosercyslysvalthralametlyscysphe
65707580
leuleugluleuglnvalileserleugluserglyaspalaserile
859095
hisaspthrvalgluasnleuileileleualaasnasnserleuser
100105110
serasnglyasnvalthrgluserglycyslysglucysglugluleu
115120125
gluglulysasnilelysglupheleuglnserphevalhisileval
130135140
glnmetpheileasnthrserserglyglyglyserglyglyglygly
145150155160
serglyglyglyglyserglyglyglyglyserglyglyglyserleu
165170175
glnilethrcysproproprometservalgluhisalaaspiletrp
180185190
vallyssertyrserleutyrserarggluargtyrilecysasnser
195200205
glyphelysarglysalaglythrserserleuthrglucysvalleu
210215220
asnlysalathrasnvalalahistrpthrthrproserleulyscys
225230235240
ilearg
<210>16
<211>726
<212>dna
<213>人工序列(artificialsequence)
<220>
<223>合成多核苷酸
<400>16
atggactggacctggattctgttcctggtcgcggctgcaacgcgagtccatagcggtatc60
catgtttttattcttgggtgtttttctgctgggctgcctaagaccgaggccaactgggta120
aatgtcatcagtgacctcaagaaaatagaagaccttatacaaagcatgcacattgatgct180
actctctacactgagtcagatgtacatccctcatgcaaagtgacggccatgaaatgtttc240
ctcctcgaacttcaagtcatatctctggaaagtggcgacgcgtccatccacgacacggtc300
gaaaacctgataatactcgctaataatagtctctcttcaaatggtaacgtaaccgagtca360
ggttgcaaagagtgcgaagagttggaagaaaaaaacataaaggagttcctgcaaagtttc420
gtgcacattgtgcagatgttcattaatacctctagcggcggaggatcaggtggcggtgga480
agcggaggtggaggctccggtggaggaggtagtggcggaggttctcttcaaataacttgt540
cctccaccgatgtccgtagaacatgcggatatttgggtaaaatcctatagcttgtacagc600
cgagagcggtatatctgcaacagcggcttcaagcggaaggccggcacaagcagcctgacc660
gagtgcgtgctgaacaaggccaccaacgtggcccactggaccacccctagcctgaagtgc720
atcaga726
<210>17
<211>566
<212>prt
<213>人工序列(artificialsequence)
<220>
<223>合成多肽
<220>
<221>misc_feature
<223>566个氨基酸的序列nkg2c-p2a-cd94-t2a-dap12
<400>17
metasnlysglnargglythrphesergluvalserleualaglnasp
151015
prolysargglnglnarglysprolysglyasnlysserserileser
202530
glythrgluglngluilepheglnvalgluleuasnleuglnasnpro
354045
serleuasnhisglnglyileasplysiletyraspcysglnglyleu
505560
leuproproproglulysleuthralagluvalleuglyileilecys
65707580
ilevalleumetalathrvalleulysthrilevalleuileprophe
859095
leugluglnasnasnpheserproasnthrargthrglnlysalaarg
100105110
hiscysglyhiscysprogluglutrpilethrtyrserasnsercys
115120125
tyrtyrileglylysgluargargthrtrpglugluserleuleuala
130135140
cysthrserlysasnserserleuleuserileaspasnglugluglu
145150155160
metlyspheleualaserileleuprosersertrpileglyvalphe
165170175
argasnserserhishisprotrpvalthrileasnglyleualaphe
180185190
lyshislysilelysaspseraspasnalagluleuasncysalaval
195200205
leuglnvalasnargleulysseralaglncysglysersermetile
210215220
tyrhiscyslyshislysleuglyserglyalathrasnpheserleu
225230235240
leulysglnalaglyaspvalglugluasnproglyprometalaval
245250255
phelysthrthrleutrpargleuileserglythrleuglyileile
260265270
cysleuserleumetserthrleuglyileleuleulysasnserphe
275280285
thrlysleuserilegluproalaphethrproglyproasnileglu
290295300
leuglnlysaspseraspcyscyssercysglnglulystrpvalgly
305310315320
tyrargcysasncystyrpheilesersergluglnlysthrtrpasn
325330335
gluserarghisleucysalaserglnlysserserleuleuglnleu
340345350
glnasnthraspgluleuaspphemetserserserglnglnphetyr
355360365
trpileglyleusertyrserglugluhisthralatrpleutrpglu
370375380
asnglyseralaleuserglntyrleupheproserphegluthrphe
385390395400
asnthrlysasncysilealatyrasnproasnglyasnalaleuasp
405410415
glusercysgluasplysasnargtyrilecyslysglnglnleuile
420425430
glyserglygluglyargglyserleuleuthrcysglyaspvalglu
435440445
gluasnproglyprometglyglyleugluprocysserargleuleu
450455460
leuleuproleuleuleualavalserglyleuargprovalglnala
465470475480
glnalaglnseraspcyssercysserthrvalserproglyvalleu
485490495
alaglyilevalmetglyaspleuvalleuthrvalleuilealaleu
500505510
alavaltyrpheleuglyargleuvalproargglyargglyalaala
515520525
glualaalathrarglysglnargilethrgluthrgluserprotyr
530535540
glngluleuglnglyglnargseraspvaltyrseraspleuasnthr
545550555560
glnargprotyrtyrlys
565
- 还没有人留言评论。精彩留言会获得点赞!