检测9种转基因大豆品系的核酸组合物及其应用的制作方法
本发明属于基因检测技术,具体涉及检测9种转基因大豆品系的核酸组合物及其应用。
背景技术:
中国是大豆和大豆产品进口国,国内需求量不断增加引起转基因大豆进口量屡创新高。在还不能确定转基因作物及其产品对人类健康和生态环境是否存在潜在的不利影响之前,对其检测及标识对消费者非常重要。挪威是首个对转基因食品实行明确含量标识的国家。2002年农业部颁布了有关农业转基因生物的安全评价、进口、标识等管理办法和管理程序,要求对5类转基因生物所涉及的17种转基因产品进行标识,其中包括转基因大豆。目前我国已批准进口共16个品系的转基因大豆,为避免转基因大豆的非法种植和销售,必须加强对相关环节的检测力度。
目前转基因成分检测主要包括蛋白质和核酸水平上的检测,而核酸水平上的检测方法又分为定性pcr检测、实时荧光定量pcr检测、基因芯片检测等多种方法。近年来国内外基于核酸检测转基因的方法主要是普通pcr,多重pcr,多重巢氏pcr,实时荧光定量pcr,环介导等温扩增技术(lamp)等。普通pcr检测一般采用凝胶电泳分析,具有一定的局限性,只能检测到10ng以上的dna条带,因此在目的片段产量较低时无法检测到。实时荧光定量pcr通过检测荧光信号的强弱从而实时检测pcr产物扩增量,可以对转基因成分进行定量分析,但是只能做单重或最高3-4重,无法提高其通量。
技术实现要素:
本发明公开了一种检测9种转基因大豆品系的核酸组合物,可以通过一次pcr准确的检测出9种转基因大豆品系a2704-12,a5547-127,dp356043,mon87705,mon87701,dp305423,fg72,cv127-9,das-68416-4,实现了检测过程简单、灵敏度高、检测结果准确的效果。
本发明采用如下技术方案:
检测9种转基因大豆品系的核酸组合物,包括a2704-12引物对、a5547-127引物对、dp356043引物对、mon87705引物对、mon87701引物对、dp305423引物对、fg72引物对、cv127-9引物对、das-68416-4引物对中的一组或多组。
检测9种转基因大豆品系的试剂盒,包括核酸组合物、膜芯片;所述核酸组合物包括a2704-12引物对、a5547-127引物对、dp356043引物对、mon87705引物对、mon87701引物对、dp305423引物对、fg72引物对、cv127-9引物对、das-68416-4引物对中的一组或多组;所述膜芯片包括支持膜与检测探针。
本发明还公开了上述检测9种转基因大豆品系的核酸组合物或者检测9种转基因大豆品系的试剂盒在检测转基因大豆品系中的应用,尤其是在利用一次pcr检测2~9种转基因大豆品系中的应用。
一种检测转基因大豆品系的方法,包括以下步骤,以待测大豆样品的总dna为模板,以核酸组合物为引物进行pcr扩增,然后将pcr扩增产物在膜芯片上显色,实现转基因大豆品系的检测;所述核酸组合物包括a2704-12引物对、a5547-127引物对、dp356043引物对、mon87705引物对、mon87701引物对、dp305423引物对、fg72引物对、cv127-9引物对、das-68416-4引物对中的一组或多组;所述膜芯片包括支持膜与检测探针。
本发明中,核酸组合物还包括lectin引物对,具体为seqidno:1、seqidno:2;优选的,a2704-12引物对为seqidno:3、seqidno:4,a5547-127引物对为seqidno:5、seqidno:6,dp356043引物对为seqidno:7、seqidno:8,mon87705引物对为seqidno:9、seqidno:10、mon87701引物对为seqidno:11、seqidno:12,dp305423引物对为seqidno:13、seqidno:14,fg72引物对为seqidno:15、seqidno:16,cv127-9引物对为seqidno:17、seqidno:18,das-68416-4引物对为seqidno:19、seqidno:20。本发明采用与现有技术不同的各基因的引物对,实现了检测过程简单、灵敏度高、检测结果准确的效果,这是软件常规设计无法预期的。
本发明中,核酸组合物中,反向引物5’端带生物素标记,即每一对引物中其反向引物5’端带生物素标记;生物素与亲和素的结合具有专一、迅速和稳定的特点,并且这些结合只需要生物素的脲基环部分,因此可将其戊酸侧链通过酰胺键与核酸分子相连,构成生物素标记的引物,具体为常规技术。
本发明中,膜芯片包括支持膜和负载于支持膜上的检测探针;支持膜包括硝酸纤维素膜、尼龙膜或具有三维孔径结构的薄膜中的一种,将探针负载于支持膜上,探针与pcr扩增产物杂交,然后通过探针和引物上标记的标记分子(生物素)显色,通过显色反应(产物序列与探针序列进行杂交,产物序列上的生物素与酶标液中的链霉亲和素(碱性磷酸酶标记的链霉亲和素)结合,最终通过显色底物与碱性磷酸酶的化学反应,出现蓝色络合物而呈现肉眼可见的斑点),可以直接肉眼判定实验结果,方法简单易行,避免了其他检测方法带来的操作复杂的问题。检测探针包括a2704-12检测探针、a5547-127检测探针、dp356043检测探针、mon87705检测探针、mon87701检测探针、dp305423检测探针、fg72检测探针、cv127-9检测探针、das-68416-4检测探针中的一组或多组,进一步包括lectin检测探针;优选的,lectin检测探针为seqidno:21,a2704-12检测探针为seqidno:22,a5547-127检测探针为seqidno:23,dp356043检测探针为seqidno:24,mon87705检测探针为seqidno:25、mon87701检测探针为seqidno:26,dp305423检测探针为seqidno:27,fg72检测探针为seqidno:28,cv127-9检测探针为seqidno:29,das-68416-4检测探针为seqidno:30。
具体实施例中,选用硝酸纤维素膜、尼龙膜或具有三维孔径结构的薄膜中的一种作为支持膜,方便将探针负载于膜上;如具有三维孔径结构的薄膜可以方便的将探针分子吸附固定在薄膜上,便于后续的反应的进行。
利用本发明检测9种转基因大豆品系的试剂盒检测转基因大豆品系时,以待测大豆样品的总dna为模板,以核酸组合物进行pcr扩增,引物组合中有5’端带生物素标记(biotin)的引物;同时将各探针点在尼龙膜上,最后将扩增产物与探针杂交后使用显色液显色,并通过肉眼观察检测结果;核酸组合物可以为lectin引物对以及a2704-12引物对、a5547-127引物对、dp356043引物对、mon87705引物对、mon87701引物对、dp305423引物对、fg72引物对、cv127-9引物对、das-68416-4引物对中的一组或多组,各对引物的目标序列分别为大豆内源基因序列lectin,转基因大豆品系a2704-12、a5547-127、dp356043、mon87705、mon87701、dp305423、fg72、cv127-9、das-68416-4特异靶序列。本发明在同一pcr体系中进行多重pcr扩增,采用不同转基因大豆品系特异性模板进行pcr,利用引物及探针特异性实现高达9种转基因大豆品系的检测。
本发明中,检测9种转基因大豆品系的试剂盒还包括pcr反应组分、配液等常规组份,还可以包括阳性对照探针和/或阴性对照探针,这都是本领域常规技术,本发明的创造性在于提供可同时检测9种转基因大豆品系的核酸组合物以及检测探针,从而可以在不需要公共引物的情况下,实现了检测过程简单、灵敏度高、检测结果准确的效果,这是现有技术无法预期的。
本发明中,pcr反应组分包括dntps、taqdna聚合酶、mg2+和pcr缓冲液中的至少一种。dntps作为pcr反应的原料,应用于以原dna为模板合成新的dna序列;通过taqdna聚合酶的作用,dna链更容易打开,使反应更容易进行;mg2+作为taqdna聚合酶的活化剂,可以激活taqdna聚合酶的功能;pcr反应缓冲液,使反应在一个稳定的环境中反应,避免影响taqdna聚合酶的活性,进而影响反应的进行;pcr反应缓冲液使得反应顺利的进行。
配液包括去活化液、去活化清洗液、杂交液、杂交清洗液、酶标液、酶标清洗液1、酶标清洗液2、显色液和显色清洗液。比如,去活化液包括100mmol/l的naoh,去活化清洗液包括2×sspe和0.1%sds;杂交液包括2×sspe和0.1%sds;杂交清洗液包括2×sspe和0.5%sds;酶标液包括2×sspe和0.5%sds;酶标清洗液1包括2×sspe和0.5%sds;酶标清洗液2包括1mtris-hcl,ph9.5,5mnacl,1mmgcl2。sspe(salinesodiumphosphateedta,sspe)缓冲液是一种常见的核酸杂交缓冲液;sspe缓冲液包括nacl、nah2po4•h2o(或nah2po4•2h2o)和edta-na2。配制1l的sspe缓冲液,包括将17.53g的nacl,27.6g的nah2po4•h2o(或31.2g的nah2po4•2h2o)和7.4g的edta-na2,然后用10m的naoh大约6ml调节ph值至7.4,然后定容至1l,过滤后高压蒸汽灭菌。通过上述的各种配液,清除杂质,排除干扰,使结果更准确、清晰可靠。显色液为碱性磷酸酶化学显色底物nbt/bcip,含0.15mg/mlbcip,0.30mg/mlnbt,100mmol/ltris-hcl,5mmol/lmgcl2,ph9.5);显色清洗液为双蒸水。生物素与链霉亲和素(streptavidin,sa)具有极高的亲和力,反应呈高度专一性。每个链霉亲和素分子具有4个生物素分子结合位点,因此,链霉亲和素可同时以多价形式结合生物素。生物素标记的引物与碱性磷酸酶标记的链霉亲和素联合使用,将检测信号级联放大,最后通过显色反应或化学发光可检测。
利用本发明检测9种转基因大豆品系的试剂盒检测转基因大豆品系时,将提取后的dna进行多重pcr扩增,并进行杂交反应,检测样品所含转基因大豆成分。通过市场采样,对不同样品进行dna提取,通过多重pcr扩增,得到pcr产物;将pcr产物与负载于支持膜上的探针分别反应结合;然后通过显色反应,显示出检测的结果,通过显色的情况判断出样品为何种转基因大豆品系,达到品系鉴定的目的。
附图说明
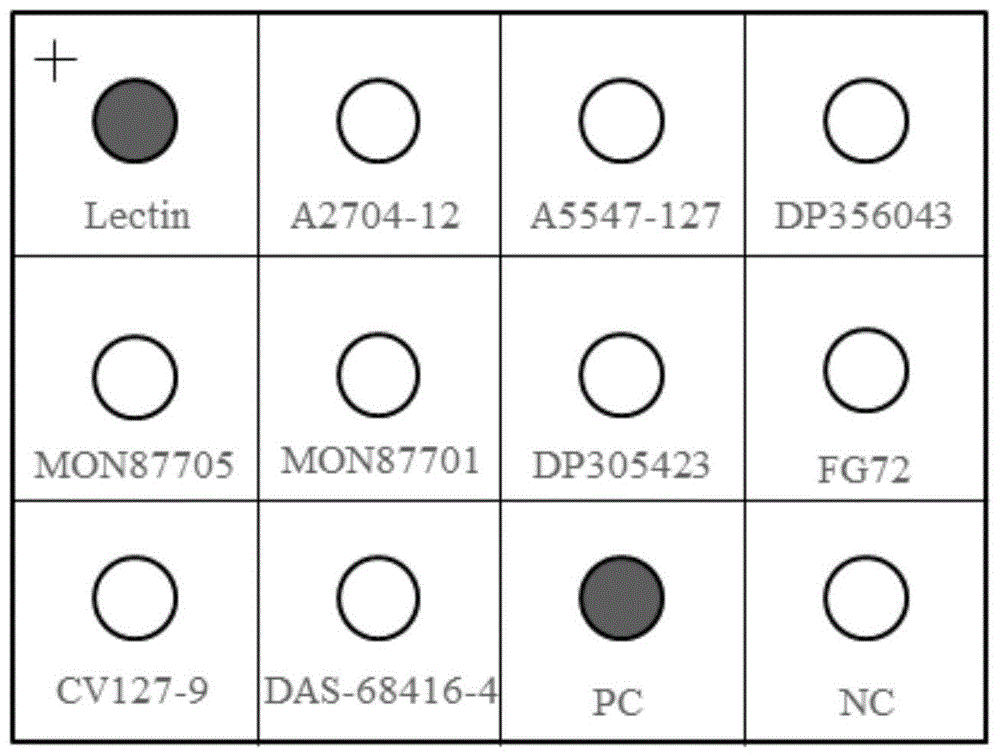
图1为检测9种转基因大豆品系的核酸组合物芯片点阵图;
图2为实施例1结果;
图3为实施例2结果;
图4为实施例3结果;
图5为实施例4结果;
图6为实施例5结果;
图7为实施例6结果;
图8为不同引物对比检测结果
图9为不同探针对比检测结果。
具体实施方式
本发明公开了核酸组合物,具体为a2704-12引物对、a5547-127引物对、dp356043引物对、mon87705引物对、mon87701引物对、dp305423引物对、fg72引物对、cv127-9引物对、das-68416-4引物对中的一组或多组,以及lectin引物对,进一步的,引物组合中各对引物的碱基序列5’-3’如下:
lectin
正向引物(seqidno:1):gacagtgaaacaggcaaggt
反向引物(seqidno:2):gagtcactattgaaaagacca
a2704-12
正向引物(seqidno:3):tcgggggcgttcgtagt
反向引物(seqidno:4):gcgagttctgttaggtcctcta
a5547-127
正向引物(seqidno:5):ccattccgccacgatcatta
反向引物(seqidno:6):ttatcccgtattgacgccgg
dp356043
正向引物(seqidno:7):cttttgcccgaggtcgttag
反向引物(seqidno:8):gccctttggtcttctgagactg
mon87705
正向引物(seqidno:9):gtagacacgtcgaaataaaga
反向引物(seqidno:10):gcagtgataacaacaccctga
mon87701
正向引物(seqidno:11):cacgcttagtgtgtgtgtcaaac
反向引物(seqidno:12):gatccgtcgacctgacggttaac
dp305423
正向引物(seqidno:13):aggaataaaggaagtacagtaga
反向引物(seqidno:14):cctaaaggatgcgtatagagtaa
fg72
正向引物(seqidno:15):ggctgcaggaattaatgtgg
反向引物(seqidno:16):tggagcaataaacatgtgatagc
cv127-9
正向引物(seqidno:17):cgccgtttagtgtataggaa
反向引物(seqidno:18):caggttcgtttaaggatgaaaatt
das-68416-4
正向引物(seqidno:19):attaataacgtccgcaatgtgt
反向引物(seqidno:20):tagttcttacagtttattgttag
本发明公开了检测9种转基因大豆品系的试剂盒,包括上述核酸组合物、膜芯片以及常规pcr反应组分、配液、阳性对照探针、阴性对照探针,其中膜芯片包括支持膜和负载于支持膜上的检测探针,进一步的,检测探针如下:
lectin探针(seqidno:21):caatccaaaggagggttccttgg
a2704-12探针(seqidno:22):agccaagcattctattcttcttatgtcgg
a5547-127探针(seqidno:23):caagtcattctgagaatagtgtatgcg
dp356043探针(seqidno:24):cgttaggtcgaataggctaggttta
mon87705探针(seqidno:25):ttgaccatcatactcattgctgatcc
mon87701探针(seqidno:26):aaacactgatagtttaaactgaaggc
dp305423探针(seqidno:27):gtgtcaatagtttgtgttatgtattcattgg
fg72探针(seqidno:28):taatgcggtcatcaatacgtgcctcaa
cv127-9探针(seqidno:29):atttatattcctcaaataaaacccaatt
das-6841-4探针(seqidno:30):tattaagttgtctaagcgtcaatatt
阳性对照探针(seqidno:31):gcatccagatcagaagcaataatgagcagtgc
阴性对照探针(seqidno:32):ccctcgggttaatgcgcgattgtcaccacacg
以上核酸组合物以及探针用于以下实施例,其中核酸组合物中,反向引物在5`端标记生物素,具体为常规技术,在合成引物时一并制备;探针带有nh2-c6,可与支持膜结合,具体为常规技术,在探针合成时一并制备。
实验中,将带有生物素标记的产物与探针进行杂交,利用碱基互补配对原理将扩增产物与膜芯片上的探针杂交后,通过生物素-链霉亲和素亲和系统的共价结合及多级级联放大效应提高系统检测灵敏度,最终通过化学显色(碱性磷酸酶对显色底物bcip/nbt)直观显示检测结果,实现多种基因的检测。体系中含有能与阳性探针杂交的单链寡核苷酸dna,其5‘端带有生物素标记,序列如下(seqidno:33):gcactgctcattattgcttctgatctggatgc。
膜芯片的制备
用打印机在市购膜上打印出表格后把膜浸泡于50ml含有3%(体积分数)戊二醛的pbs溶液中,摇床缓慢摆动孵育2小时;随后在pbs中洗膜4次,一次50ml,每次5分钟;最后将膜放在空气中干燥并密封保存。
用0.5mnahco3,ph8.4调整检测探针浓度至10μm,将阳性对照探针和阴性对照探针分别稀释到5μm;并将各检测探针、阳性对照探针和阴性对照探针依次点样在尼龙膜上。点好探针的膜芯片放入烘箱中,80℃烘烤2小时备用。
膜芯片的模式图如图1所示,lectin表示大豆内源基因;a2704-12,a5547-127,dp356043,mon87705,mon87701,dp305423,fg72,cv127-9,das-68416-4分别表示不同的转基因大豆品系,pc表示阳性对照(positivecontrol);nc表示阴性对照(negativecontrol)。
以下实施例、对比例中,去活化液包括100mmol/l的naoh,去活化清洗液包括2×sspe和0.1%sds;杂交液包括2×sspe和0.1%sds;杂交清洗液包括2×sspe和0.5%sds;酶标液包括2×sspe和0.5%sds(使用前按1∶2000的比例加入碱性磷酸酶标记的链霉亲和素母液(浓度为1mg/ml));酶标清洗液1包括2×sspe和0.5%sds;酶标清洗液2包括1mtris-hcl,ph9.5,5mnacl,1mmgcl2。sspe(salinesodiumphosphateedta,sspe)缓冲液是一种常见的核酸杂交缓冲液;sspe缓冲液包括nacl、nah2po4•h2o(或nah2po4•2h2o)和edta-na2。配制1l的sspe缓冲液,包括将17.53g的nacl,27.6g的nah2po4•h2o(或31.2g的nah2po4•2h2o)和7.4g的edta-na2,然后用10m的naoh大约6ml调节ph值至7.4,然后定容至1l,过滤后高压蒸汽灭菌。通过上述的各种配液,清除杂质,排除干扰,使结果更准确、清晰可靠。显色液为碱性磷酸酶化学显色底物nbt/bcip,含0.15mg/mlbcip,0.30mg/mlnbt,100mmol/ltris-hcl,5mmol/lmgcl2,ph9.5);显色清洗液为双蒸水。
实施例1
核酸组合物为seqidno:1至seqidno:20;检测探针为seqidno:21至seqidno:30;支持膜为市购尼龙膜;同时还包括阳性对照探针(seqidno:31)、阴性对照探针(seqidno:32)以及能与阳性对照探针杂交的单链寡核苷酸dna(seqidno:33);核酸组合物反向引物以及单链寡核苷酸dna的5‘端带有生物素标记,探针带有nh2-c6,合成引物或者探针时根据常规方法制备。其余实施例与此一样。
按照天根生化科技(北京)有限公司植物基因组dna提取试剂盒(货号:dp305)的说明分别提取转基因大豆品系dp356043,dp305423,a2704-12,a5547-127,fg72,cv127-9,mon87701,mon87705,das-68416-4标准样品基因组dna。提取后的dna用超微量分光光度计(nanodrop2000)测定浓度及质量后分别进行pcr加样及扩增,pcr扩增的反应体系如下所示:
引物mix:10μl;
10×pcr缓冲液(+mg2+):2.5μl;
taqdna聚合酶:0.5μl(50u/μl)
dntps(10mm):2μl;
单链寡核苷酸dna(20μm):0.01μl;
提取的样品基因组dna(10ng/μl):1μl;
ddh2o:补足至总体积25μl。
反应体系中,a2704-12引物对、a5547-127引物对、dp356043引物对、mon87705引物对、mon87701引物对、dp305423引物对、fg72引物对、cv127-9引物对、das-68416-4、lectin引物对等量混合成引物mix,然后用灭菌ddh2o补足体积(pcr反应体系中生物素修饰引物终浓度为0.3μm,非修饰引物终浓度为0.2μm)。
对上述各转基因品系pcr扩增反应体系进行同样的pcr扩增,扩增条件如下所示,反应过程由taqdna聚合酶反应,经过预变性、变性、退火和延伸,条件分别为:
预变性:温度95℃,时间3分钟;pcr循环:35个循环组成:变性:温度95℃,时间15秒;退火:温度55℃,时间30秒;延伸:温度72℃,时间15秒;最后延伸:温度72℃,时间3分钟;保存:温度4℃。
膜芯片杂交
将上述pcr产物放入pcr仪,95℃热变性5分钟,然后置于冰上降温,备用。取冷却后的pcr产物25μl加入杂交液中混匀,然后加在经过去活化、去活化清洗的膜芯片上(以下实施例操作步骤一样),再依次经过杂交、杂交清洗、酶标、酶标清洗、显色、显色清洗等步骤,完成杂交过程,杂交程序如表1所示,具体步骤为常规操作。
杂交完成后,根据杂交点显色情况参照图1进行结果判读,结果如图2所示。判读结果为样品均为大豆,从左至右,由上到下分别含转基因大豆品系a2704-12,a5547-127,dp356043,mon87705,mon87701,dp305423,fg72,cv127-9,das-68416-4特异成分。
实施例2
按照天根生化科技(北京)有限公司植物基因组dna提取试剂盒(货号:dp305)的说明提取混合样品基因组dna(已知)。提取后的dna用超微量分光光度计(nanodrop2000)测定浓度及质量后进行pcr加样。
pcr扩增的反应体系如下所示:
引物mix:10μl;
10×pcr缓冲液(+mg2+):2.5μl;
taqdna聚合酶:0.5μl(50u/μl)
dntps(10mm):2μl;
单链寡核苷酸dna(20μm):0.01μl;
提取的样品基因组dna(100ng/μl):2μl;
ddh2o:补足至总体积25μl。
反应体系中,a2704-12引物对、a5547-127引物对、dp356043引物对、mon87705引物对、mon87701引物对、dp305423引物对、fg72引物对、cv127-9引物对、das-68416-4、lectin引物对等量混合成引物mix(浓度与实施例1一致),对上述pcr反应体系(1组,混合样品基因组dna)进行扩增,扩增条件如下所示,反应过程由taqdna聚合酶反应,经过预变性、变性、退火和延伸,条件分别为:
预变性:温度95℃,时间3分钟;pcr循环:35个循环组成:变性:温度95℃,时间15秒;退火:温度55℃,时间30秒;延伸:温度72℃,时间15秒;最后延伸:温度72℃,时间3分钟;保存:温度4℃。
膜芯片杂交
将pcr产物放入pcr仪,95℃热变性5分钟,然后置于冰上降温,备用。取冷却后的pcr产物25μl加入杂交液中,依次完成去活化、去活化清洗、杂交、杂交清洗、酶标、酶标清洗、显色、显色清洗等步骤,完成杂交过程,杂交程序如表1所示。
实验完成后,根据杂交点显色情况参照图1进行结果判读,结果如图3所示。判读结果为该样品为大豆,并且含有转基因大豆品系a2704-12,a5547-127、dp356043、mon87701、dp305423等成分,与混合样品实际组成一致。
实施例3
按照天根生化科技(北京)有限公司植物基因组dna提取试剂盒(货号:dp305)的说明提取玉米基因组dna。提取后的dna用超微量分光光度计(nanodrop2000)测定浓度及质量后进行pcr加样。
pcr扩增的反应体系如下所示:
引物mix:10μl;
10×pcr缓冲液(+mg2+):2.5μl;
taqdna聚合酶:0.5μl(50u/μl)
dntps(10mm):2μl;
单链寡核苷酸dna(20μm):0.01μl;
提取的样品基因组dna(100ng/μl):2μl;
ddh2o:补足至总体积25μl。
反应体系中,上述10引物对等量混合成引物mix(浓度与实施例1一致),对上述反应体系进行pcr循环扩增,pcr循环条件如下所示,反应过程由taqdna聚合酶反应,经过预变性、变性、退火和延伸,条件分别为:
预变性:温度95℃,时间3分钟;pcr循环:35个循环组成:变性:温度95℃,时间15秒;退火:温度55℃,时间30秒;延伸:温度72℃,时间15秒;最后延伸:温度72℃,时间3分钟;保存:温度4℃。
膜芯片杂交
将pcr产物放入pcr仪,95℃热变性5分钟,然后置于冰上降温,备用。取冷却后的pcr产物25μl加入杂交液中,依次完成去活化、去活化清洗、杂交、杂交清洗、酶标、酶标清洗、显色、显色清洗等步骤,完成杂交过程,杂交程序如表1所示。
实验完成后,根据杂交点显色情况参照图1进行结果判读,结果如图4所示。判读结果为该样品不含有大豆内参及相应转基因大豆品系成分。
实施例4
按照天根生化科技(北京)有限公司植物基因组dna提取试剂盒(货号:dp305)的说明提取1%cv127-9的基因组dna。提取后的dna用超微量分光光度计(nanodrop2000)测定浓度及质量后进行pcr加样;1%cv127-9即质量分数为1%的cv127-9,以已知的野生型大豆(非转基因大豆)粉末为基质,如,向49.5g野生型大豆粉末中加入0.5g纯的cv127-9转基因大豆粉末充分混匀,即配制成1%的cv127-9样品。
pcr扩增的反应体系如下所示:
引物mix:10μl;
10×pcr缓冲液(+mg2+):2.5μl;
taqdna聚合酶:0.5μl(50u/μl)
dntps(10mm):2μl;
单链寡核苷酸dna(20μm):0.01μl;
提取的样品基因组dna(10ng/μl):1μl;
ddh2o:补足至总体积25μl。
反应体系中,上述10引物对等量混合成引物mix(浓度与实施例1一致),对上述反应体系进行pcr循环扩增,pcr循环条件如下所示,反应过程由taqdna聚合酶反应,经过预变性、变性、退火和延伸,条件分别为:
预变性:温度95℃,时间3分钟;pcr循环:35个循环组成:变性:温度95℃,时间15秒;退火:温度55℃,时间30秒;延伸:温度72℃,时间15秒;最后延伸:温度72℃,时间3分钟;保存:温度4℃。
膜芯片杂交
将pcr产物放入pcr仪,95℃热变性5分钟,然后置于冰上降温,备用。取冷却后的pcr产物25μl加入杂交液中,依次完成去活化、去活化清洗、杂交、杂交清洗、酶标、酶标清洗、显色、显色清洗等步骤,完成杂交过程,杂交程序如表1所示。
实验完成后,根据杂交点显色情况参照图1进行结果判读,结果如图5所示。判读结果为在转基因含量为1%时能检测到样品中含有大豆内参和转基因大豆品系cv127-9成分,判断该样品为转基因大豆品系cv127-9。
实施例5
按照天根生化科技(北京)有限公司植物基因组dna提取试剂盒(货号:dp305)的说明提取未知样品d1-d6基因组dna。提取后的dna用超微量分光光度计(nanodrop2000)测定浓度及质量后进行pcr加样。
pcr扩增的反应体系如下所示:
引物mix:10μl;
10×pcr缓冲液(+mg2+):2.5μl;
taqdna聚合酶:0.5μl(50u/μl)
dntps(10mm):2μl;
单链寡核苷酸dna(20μm):0.01μl;
提取的样品基因组dna(100ng/μl):2μl;
ddh2o:补足至总体积25μl。
反应体系中,上述10引物对等量混合成引物mix(浓度与实施例1一致),对上述六组反应体系分别进行pcr循环扩增,pcr循环条件如下所示,反应过程由taqdna聚合酶反应,经过预变性、变性、退火和延伸,条件分别为:
预变性:温度95℃,时间3分钟;pcr循环:35个循环组成:变性:温度95℃,时间15秒;退火:温度55℃,时间30秒;延伸:温度72℃,时间15秒;最后延伸:温度72℃,时间3分钟;保存:温度4℃。
膜芯片杂交
将pcr产物放入pcr仪,95℃热变性5分钟,然后置于冰上降温,备用。取冷却后的pcr产物25μl加入杂交液中,依次完成去活化、去活化清洗、杂交、杂交清洗、酶标、酶标清洗、显色、显色清洗等步骤,完成杂交过程,杂交程序如表1所示。
实验完成后,根据杂交点显色情况参照图1进行结果判读,结果如图6a所示。判读结果为样品d2中含有大豆内参、mon87705和fg72,d6中含有大豆内参、a2704和fg72成分;d2和d6中转基因成分分别用现有标准中的引物进行验证,结果如图6b所示(说明:mon87705按照农业部2122号公告-4-2014检测,产物长度为318bp;fg72按照农业部2259号公告-8-2015检测,产物长度为150bp;a2704-12按照农业部1485号公告-7-2010检测,产物长度为239bp),如结果所示,膜芯片检测结果与相关标准中引物检测结果完全一致,由左至右依次为对照、d2-87705、d2fg72、d6fg72、d62704。
实施例6
按照天根生化科技(北京)有限公司植物基因组dna提取试剂盒(货号:dp305)的说明提取野生型大豆基因组dna。提取后的dna用超微量分光光度计(nanodrop2000)测定浓度及质量后进行pcr加样。
pcr扩增的反应体系如下所示:
引物mix:10μl;
10×pcr缓冲液(+mg2+):2.5μl;
taqdna聚合酶:0.5μl(50u/μl)
dntps(10mm):2μl;
单链寡核苷酸dna(20μm):0.01μl;
提取的样品基因组dna(10ng/μl):1μl;
ddh2o:补足至总体积25μl。
反应体系中,上述10引物对等量混合成引物mix(浓度与实施例1一致),对上述反应体系进行pcr循环扩增,pcr循环条件如下所示,反应过程由taqdna聚合酶反应,经过预变性、变性、退火和延伸,条件分别为:
预变性:温度95℃,时间3分钟;pcr循环:35个循环组成:变性:温度95℃,时间15秒;退火:温度55℃,时间30秒;延伸:温度72℃,时间15秒;最后延伸:温度72℃,时间3分钟;保存:温度4℃。
膜芯片杂交
将pcr产物放入pcr仪,95℃热变性5分钟,然后置于冰上降温,备用。取冷却后的pcr产物25μl加入杂交液中,依次完成去活化、去活化清洗、杂交、杂交清洗、酶标、酶标清洗、显色、显色清洗等步骤,完成杂交过程,杂交程序如表1所示。
实验完成后,根据杂交点显色情况参照图1进行结果判读,结果如图7所示。判读结果为该样品为野生型大豆,无本芯片所列转基因大豆品系成分,与预期结果相符。
对比例
将针对fg72的引物更换为软件自动设计的如下序列:
fg72f1:cgggctgcaggaattaatg
fg72r1:tttggagcaataaacatgtg
反向引物5`端带有生物素标记,通过常规方法制备,与实施例一致。
其余不变,根据实施例1的方法,对fg72转基因大豆品系核酸进行检测,结果无靶点显色,见图8(显色情况参照图1),即该引物对没能检测出fg72转基因大豆品系的特异性基因/片段;说明引物的设计对检测结果具有决定影响。
为了进一步说明引物的重要性,将针对mon87701的引物更换为软件自动设计的如下序列:
mon87701f3:gcttagtgtgtgtgtcaaacactg
mon87701r3:gttaacgcggccgctctagaac
反向引物5`端带有生物素标记,通过常规方法制备,与实施例一致。
其余不变,根据实施例1的方法,对mon87701转基因大豆品系核酸进行检测,结果无靶点显色,即该引物对没能检测出mon87701转基因大豆品系的特异性基因/片段;说明引物的设计对检测结果具有决定影响。
探针的设计对检测结果也有影响,将fg72探针更换为软件自动设计的如下序列:ctccctatatttttgcttgttgg,探针带有nh2-c6,为常规制备,与实施例一样,其余不变,根据实施例1的方法,对fg72转基因大豆品系进行核酸检测,结果无靶点显色,即该探针没能检测出fg72转基因大豆品系的fg72特异性基因/片段;本发明设计的fg72探针可以有效显色,见图2。
将mon87701探针更换为软件自动设计的如下序列:ccactagttctagagcggccgcgtt(对比探针),探针带有nh2-c6,为常规制备,与实施例一样,其余不变,根据实施例1的方法,对mon87701转基因大豆品系进行核酸检测,靶点显色非常浅,见图9,其中a为检测结果、b为点阵设计,其中mon87701p1为本发明设计的探针,mon87701p3为对比探针,其他基因的探针都为本发明上述设计的探针,即该对比探针不能有效检测出mon87701转基因大豆品系的mon87701特异性基因/片段;给出本发明设计的mon87701探针作比较。
现有技术中,定性pcr检测一般采用凝胶电泳分析,具有一定的局限性,只能检测到10ng以上的dna条带,因此在目的片段产量较低时无法检测到。实时荧光定量pcr通过检测荧光信号的强弱从而实时检测pcr产物扩增量,可以对转基因成分进行定量分析,但是只能做单重或最高3-4重,无法提高其通量。本发明将多重pcr与膜芯片杂交技术结合,利用10对特异引物对,可同时对多达10种特异基因/片段进行检测,并通过pcr产物与膜芯片上探针的杂交进一步保证检测结果的特异性与准确率,较普通定性pcr和荧光定量pcr的检测效率和准确性有所提高,本发明灵敏度可达1%,并且基因芯片检测通量高,可以同时进行多指标的筛检。膜芯片杂交中使用的反向斑点杂交技术,可使pcr产物与膜芯片上探针的杂交特异性的结合,而生物素的酶联放大作用则大大提高了pcr产物的检测灵敏度。膜芯片技术最后通过碱性磷酸酶与bcip/nbt的显色作用,将杂交结果直观的显示在膜芯片上,不需借助额外的仪器,肉眼即可判断检测结果,大大简化了检测步骤。
综上所述,本发明可对9种转基因大豆品系同时检测,并且检测灵敏度和检测通量高,结果直观可见,可大大提高检测效率,用于同时检测国家允许进口和不允许进口的转基因大豆品系,增加对非法进口的打击力度。
序列表
<110>苏州市食品检验检测中心
<120>检测9种转基因大豆品系的核酸组合物及其应用
<160>39
<170>siposequencelisting1.0
<210>1
<211>20
<212>dna
<213>人工序列(artificialsequence)
<400>1
gacagtgaaacaggcaaggt20
<210>2
<211>21
<212>dna
<213>人工序列(artificialsequence)
<400>2
gagtcactattgaaaagacca21
<210>3
<211>17
<212>dna
<213>人工序列(artificialsequence)
<400>3
tcgggggcgttcgtagt17
<210>4
<211>22
<212>dna
<213>人工序列(artificialsequence)
<400>4
gcgagttctgttaggtcctcta22
<210>5
<211>20
<212>dna
<213>人工序列(artificialsequence)
<400>5
ccattccgccacgatcatta20
<210>6
<211>20
<212>dna
<213>人工序列(artificialsequence)
<400>6
ttatcccgtattgacgccgg20
<210>7
<211>20
<212>dna
<213>人工序列(artificialsequence)
<400>7
cttttgcccgaggtcgttag20
<210>8
<211>22
<212>dna
<213>人工序列(artificialsequence)
<400>8
gccctttggtcttctgagactg22
<210>9
<211>21
<212>dna
<213>人工序列(artificialsequence)
<400>9
gtagacacgtcgaaataaaga21
<210>10
<211>21
<212>dna
<213>人工序列(artificialsequence)
<400>10
gcagtgataacaacaccctga21
<210>11
<211>23
<212>dna
<213>人工序列(artificialsequence)
<400>11
cacgcttagtgtgtgtgtcaaac23
<210>12
<211>23
<212>dna
<213>人工序列(artificialsequence)
<400>12
gatccgtcgacctgacggttaac23
<210>13
<211>23
<212>dna
<213>人工序列(artificialsequence)
<400>13
aggaataaaggaagtacagtaga23
<210>14
<211>23
<212>dna
<213>人工序列(artificialsequence)
<400>14
cctaaaggatgcgtatagagtaa23
<210>15
<211>20
<212>dna
<213>人工序列(artificialsequence)
<400>15
ggctgcaggaattaatgtgg20
<210>16
<211>23
<212>dna
<213>人工序列(artificialsequence)
<400>16
tggagcaataaacatgtgatagc23
<210>17
<211>20
<212>dna
<213>人工序列(artificialsequence)
<400>17
cgccgtttagtgtataggaa20
<210>18
<211>24
<212>dna
<213>人工序列(artificialsequence)
<400>18
caggttcgtttaaggatgaaaatt24
<210>19
<211>22
<212>dna
<213>人工序列(artificialsequence)
<400>19
attaataacgtccgcaatgtgt22
<210>20
<211>23
<212>dna
<213>人工序列(artificialsequence)
<400>20
tagttcttacagtttattgttag23
<210>21
<211>23
<212>dna
<213>人工序列(artificialsequence)
<400>21
caatccaaaggagggttccttgg23
<210>22
<211>29
<212>dna
<213>人工序列(artificialsequence)
<400>22
agccaagcattctattcttcttatgtcgg29
<210>23
<211>27
<212>dna
<213>人工序列(artificialsequence)
<400>23
caagtcattctgagaatagtgtatgcg27
<210>24
<211>25
<212>dna
<213>人工序列(artificialsequence)
<400>24
cgttaggtcgaataggctaggttta25
<210>25
<211>26
<212>dna
<213>人工序列(artificialsequence)
<400>25
ttgaccatcatactcattgctgatcc26
<210>26
<211>26
<212>dna
<213>人工序列(artificialsequence)
<400>26
aaacactgatagtttaaactgaaggc26
<210>27
<211>31
<212>dna
<213>人工序列(artificialsequence)
<400>27
gtgtcaatagtttgtgttatgtattcattgg31
<210>28
<211>27
<212>dna
<213>人工序列(artificialsequence)
<400>28
taatgcggtcatcaatacgtgcctcaa27
<210>29
<211>28
<212>dna
<213>人工序列(artificialsequence)
<400>29
atttatattcctcaaataaaacccaatt28
<210>30
<211>26
<212>dna
<213>人工序列(artificialsequence)
<400>30
tattaagttgtctaagcgtcaatatt26
<210>31
<211>32
<212>dna
<213>人工序列(artificialsequence)
<400>31
gcatccagatcagaagcaataatgagcagtgc32
<210>32
<211>32
<212>dna
<213>人工序列(artificialsequence)
<400>32
ccctcgggttaatgcgcgattgtcaccacacg32
<210>33
<211>32
<212>dna
<213>人工序列(artificialsequence)
<400>33
gcactgctcattattgcttctgatctggatgc32
<210>34
<211>19
<212>dna
<213>人工序列(artificialsequence)
<400>34
cgggctgcaggaattaatg19
<210>35
<211>20
<212>dna
<213>人工序列(artificialsequence)
<400>35
tttggagcaataaacatgtg20
<210>36
<211>24
<212>dna
<213>人工序列(artificialsequence)
<400>36
gcttagtgtgtgtgtcaaacactg24
<210>37
<211>22
<212>dna
<213>人工序列(artificialsequence)
<400>37
gttaacgcggccgctctagaac22
<210>38
<211>23
<212>dna
<213>人工序列(artificialsequence)
<400>38
ctccctatatttttgcttgttgg23
<210>39
<211>25
<212>dna
<213>人工序列(artificialsequence)
<400>39
ccactagttctagagcggccgcgtt25
- 还没有人留言评论。精彩留言会获得点赞!