一种快速识别羟基自由基的荧光探针及其制备方法和应用
1.本发明涉及一种快速识别羟基自由基的荧光探针及其制备方法和应用,属于有机小分子荧光探针领域。
背景技术:
2.适量的生物活性物种(ros,包括o2·
、h2o2、hocl,1o2,
·
oh、hobr等)对于维持细胞内稳态非常重要,并在许多生理过程中起着至关重要的作用,如病原体的防御、信号转导和细胞分化。但是,ros的过度产生会导致氧化应激的发生,引起器官系统功能衰退甚至是一系列疾病。
3.羟基自由基是目前已知活性氧中对生物体毒性最强、危害最大的一种自由基,它能够造成细胞中dna、脂质、糖类、蛋白质等分子过度氧化,而造成细胞伤害。有研究表明,这些损伤可进一步造成多种退化性疾病、老化、突变以及癌症的形成。
4.羟基自由基的寿命短,含量低,对其的检测是化学分析和生命科学分析领域最困难的问题之一。传统的羟基自由基的检测方法主要有:自旋捕集-电子自旋磁共振法、高效液相法、电化学检测法、分光光度法和荧光光度法等。而近年来随着有机小分子荧光探针的不断发展逐渐显现出特有的性质,比如:灵敏度高、操作简便、重现性好、膜透性好、原位检测、选择性好等众多优点,使得有机小分子荧光探针已被越来越多地应用于多种复杂生物、环境样品中的羟基自由基检测及成像分析。因此,设计开发有效的并能够用于生物体系中羟基自由基检测的方法具有非常重要的意义。
技术实现要素:
5.本发明的目的之一是提供一种对细胞渗透性好,毒副作用小,适用于生物体内羟基自由基检测的荧光探针。
6.本发明的目的之二是提供一种工艺简单的该荧光探针的合成方法。
7.本发明的目的之三是提供该荧光探针的用途。
8.本发明采用以下技术方案:
9.一种快速识别羟基自由基的荧光探针,其特征在于,该探针化学结构式如式(i)所示:
10.11.一种上述快速识别羟基自由基的荧光探针的制备方法,其特征在于,它包括以下步骤:
12.在氮气环境下,将(9-乙基-9h-咔唑-3-基)硼酸、7-溴-2,3-二氢噻吩并[3,4-b][1,4]二恶烷-5-甲醛、pd(pph3)4和k2co3溶于有机溶剂和水中,将反应物回流过夜。冷却至室温将反应后的产物倒入水中,用ch2cl2萃取并用无水硫酸镁干燥,柱层析分离得到黄色中间体1。
[0013][0014]
在氩气环境中,将中间体1和1-丁基-4-甲基吡啶溴化物加入到干燥乙醇中,在几滴哌啶的催化下回流过夜。冷却至室温后,减压蒸发除去溶剂。柱层析分离得到红黑色产物ctop。
[0015][0016]
本发明的快速识别羟基自由基的荧光探针的应用:该荧光探针可以应用于生物体和水环境中羟基自由基的含量传感检测;所述的传感检测主要为荧光检测。
[0017]
本发明的优点在于:(1)探针的合成只需要两步,并且后处理过程相对简单,易于操作;(2)本发明发射波长在近红外区,可以有效降低生物组织自发荧光的干扰;(3)本发明实现了羟基自由基的快速检测。在一般紫外灯(365nm)下,即可观察到与羟基自由基作用前后颜色发生明显的变化(红色到澄清),该试剂可实现关节炎小鼠的活体成像,在生物分子检测领域具有广阔的应用前景。
附图说明
[0018]
为了更清楚地说明本发明实施实例中的技术方案,下面将对实施例描述中所需要的附图做简单的介绍:
[0019]
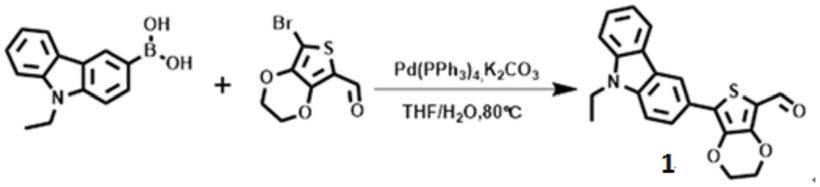
图1是本发明实施例所得荧光探针1的合成路线图。
[0020]
图2是本发明实施例所得荧光探针ctop的合成路线图。
[0021]
图3是本发明实施例所得荧光探针1的1h-nmr谱图。
[0022]
图4是本发明实施例所得荧光探针ctop的1h-nmr谱图。
[0023]
图5是本发明实施例所得荧光探针ctop与羟基自由基作用前后的光谱图,其中波峰高的线表示羟基自由基(0当量)。
[0024]
图6是本发明实施例所得荧光探针ctop应用于生物体系中,对其生物毒性进行测试。
具体实施方式
[0025]
以下将结合附图及实施例来详细说明本发明的实施方式,借此对本发明如何应用技术手段来解决技术问题,并达成技术效果的实现过程能充分理解并据以实施。需要说明的是,只要不构成冲突,本发明中的各个实施例中的各个特征可以相互结合,形成的技术方案均在本发明的保护范围之内。
[0026]
本发明公开一种快速识别羟基自由基的荧光探针,其特征在于,该探针化学结构式如式(i)所示:
[0027][0028]
实施例1:荧光探针1的合成
[0029]
合成路线如下:
[0030][0031]
在氮气环境下,向(9-乙基-9h-咔唑-3-基)硼酸(478mg,2mmol)、7-溴-2,3-二氢噻吩并[3,4-b][1,4]二恶烷-5-甲醛(498mg,2mmol)、pd(pph3)4(84mg,0.073mmol)和甲苯(20ml)的混合物中加入k2co3(2.0m,1.5ml)的水溶液,将反应物回流过夜。反应结束冷却至室温后将反应后的产物倒入水中,用ch2cl2萃取并用无水硫酸镁干燥。粗品经硅胶柱层析(石油醚/dcm=1/2)纯化,得到黄色中间体1粉末(493mg,产率为68%),黄色中间体的全称为7-(9-乙基-9h-咔唑-3-基)-2,3-二氢噻吩并[3,4-b][1,4]二恶英-5-甲醛。1h nmr(600mhz,dmso-d6)δ9.88(s,1h),8.59(d,j=1.8hz,1h),8.24(d,j=7.7hz,1h),7.91(dd,j=8.6,1.8hz,1h),7.71(d,j=8.6hz,1h),7.65(d,j=8.2hz,1h),7.52
–
7.48(m,1h),7.25(t,j=7.4hz,1h),4.55
–
4.45(m,6h),1.33(t,j=7.1hz,3h)。
[0032][0033]
在氩气环境中,将中间体1(363mg,1mmol)和1-丁基-4-甲基吡啶溴化物(230mg,1mmol))加入到干燥乙醇中,在几滴哌啶的催化下回流过夜。冷却至室温后,减压蒸发除去
溶剂。用al2o3柱层析法纯化残余物,用dcm和甲醇混合物(90:1v/v)作为洗脱溶剂,得到红黑色的ctop粉末(333mg,产率为58%)。1h nmr(600mhz,dmso-d6)δ8.81(d,j=6.7hz,2h),8.52(d,j=1.8hz,1h),8.19(dd,j=13.7,7.3hz,3h),8.03(d,j=15.8hz,1h),7.87(dd,j=8.6,1.9hz,1h),7.71(d,j=8.7hz,1h),7.66(d,j=8.2hz,1h),7.51(ddd,j=8.2,7.0,1.2hz,1h),7.25(t,j=7.4hz,1h),7.02(d,j=15.8hz,1h),4.52
–
4.48(m,4h),4.43(t,j=7.4hz,2h),1.87(tt,j=9.1,6.6hz,2h),1.36
–
1.31(m,4h),1.26
–
1.22(m,3h),0.92(t,j=7.4hz,3h)。
[0034]
ctop全称为:(e)-1-丁基-4-(2-(7-(9-乙基-9h-咔唑-3-基)-2,3-二氢噻吩[3,4-b][1,4]二恶英-5-基)乙烯基)吡啶-1-氨基溴盐。
[0035]
实施例2:探针ctop随
·
oh的加入荧光谱图的变化
[0036]
取实施例1制备的ctop荧光探针溶于dmf中,制成1mmol/l储备液。从储备液中取出30μl加入到5ml离心管当中,加入100当量
·
oh标准溶液,用dmf/pbs(1:1,v/v)稀释至3ml(10μm),测量其荧光性质。荧光光谱如图5所示,由图5可见,ctop随
·
oh加入荧光强度下降,这是由于产活性氧五中可以对探针进行漂白。
[0037]
实施例3:ctop探针生物兼容性实验
[0038]
在37℃下将细胞用含有不同浓度探针的细胞培养液培养24h和48h,用酶标仪测定活细胞百分比,所得实验结果如图6所示,可见与空白细胞相比,加入不同浓度的探针培养24h和48h后,活细胞数量均大于90%,可知该探针具有良好的生物兼容性和低的生物毒性。
[0039]
以上列出的数值均为示意性举例,本领域技术人员根据本技术的教导可以选用其他合适的比例,这也在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1