一种深色有隔内生真菌干粉菌剂的制备方法与流程
本发明涉及微生物领域中,一种深色有隔内生真菌干粉菌剂的制备方法。
背景技术:
深色有隔内生真菌(darkseptateendophyte,dse)泛指一群定居于植物根内,并能形成典型的有隔菌丝和微菌核等结构但对宿主无致病性的小型土壤内生真菌。
研究表明,深色有隔内生真菌可促进植物生长、提高植物抗逆性及改善土壤理化性质。中国专利申请201910505641.5公开了深色有隔内生真菌针a2-1(中国微生物菌种保藏管理委员会普通微生物中心保藏编号为cgmccno.17465的菌株)可以促进根的生长。随着深色有隔内生真菌的生态作用逐渐被揭示,深色有隔内生真菌菌剂的研发也逐渐成为研究的热点与难点。
目前深色有隔内生真菌菌剂培养时要经过2次活化,每次7-10天,制作过程缓慢,而且转接过程中容易污染而染上杂菌。另外,随着深色有隔内生真菌应用逐渐由室内走向野外,而实验室规模下的液体菌剂存在性能不稳定、运输不便等问题,因此急需探索一种易运输、易贮存、可量化生产的固体菌剂制作的方法。
技术实现要素:
本发明的目的是提供一种深色有隔内生真菌干粉菌剂的制备方法,具体为针a2-1干粉菌剂的制备方法。
本发明提供的针a2-1干粉菌剂的制备方法,包括:将针a2-1在60℃下干燥,所得干燥的真菌即为针a2-1菌剂;所述针a2-1为在中国微生物菌种保藏管理委员会普通微生物中心保藏编号为cgmccno.17465的菌株。
所述干燥的时间可小于等于42小时。
上述方法中,所述干燥的真菌的含水量可为2%-3%,如3%。
上述方法中,所述将针a2-1在60℃下干燥可包括:将所述针a2-1的菌丝在60℃下干燥。
上述方法还可包括将干燥的真菌进行粉碎,所得粉碎后的真菌即为针a2-1菌剂。
上述方法还可包括将所述粉碎后的真菌过孔径小于等于0.5mm的筛子,得到的粒径小于等于0.5mm的粉末状物质即为针a2-1菌剂。
所述方法在制备促进植物生长或提高植物抗逆性或改善土壤理化性质产品中的应用,也属于本发明的保护范围。
本发明的针a2-1干粉菌剂的制备方法,通过将针a2-1菌丝在60℃下烘干至含水量在3%获得针a2-1干粉菌剂,该方法具有如下优势:制备菌剂简单快速,在42小时内即可完成;对菌的活性无明显的影响,菌的活性与干燥前无显著差异;所得菌剂可长时间保存,在常温保存20天仍具有很好的活性,易贮存;所得菌剂与传统液体菌剂相比,还有效克服了其运输不便、易污染等问题;利用本发明的方法所得菌剂,粒径小于等于0.5mm,进一步提高了菌剂利用效率。本发明的方法不仅可用于批量化生产针a2-1菌剂,对于菌剂的进一步推广使用起着至关重要的作用,更为土地的可持续发展奠定重要基础,具有很好的应用前景。
生物材料保藏说明
生物材料的分类命名:darksideasp.
生物材料的菌株编号:针a2-1
生物材料的保藏单位名称:中国微生物菌种保藏管理委员会普通微生物中心
生物材料的保藏单位简称:cgmcc
生物材料的保藏单位地址:北京市朝阳区北辰西路1号院3号,中国科学院微生物研究所,邮政编码:100101
生物材料的保藏日期:2019年4月8日
生物材料的保藏中心登记入册编号:cgmccno.17465
生物材料保藏说明
生物材料的分类命名:darksideasp.
生物材料的菌株编号:针a2-7
生物材料的保藏单位名称:中国微生物菌种保藏管理委员会普通微生物中心
生物材料的保藏单位简称:cgmcc
生物材料的保藏单位地址:北京市朝阳区北辰西路1号院3号,中国科学院微生物研究所,邮政编码:100101
生物材料的保藏日期:2019年11月19日
生物材料的保藏中心登记入册编号:cgmccno.18811
生物材料保藏说明
生物材料的分类命名:格孢菌(pleosporalessp.)
生物材料的菌株编号:针a2-8
生物材料的保藏单位名称:中国微生物菌种保藏管理委员会普通微生物中心
生物材料的保藏单位简称:cgmcc
生物材料的保藏单位地址:北京市朝阳区北辰西路1号院3号,中国科学院微生物研究所,邮政编码:100101
生物材料的保藏日期:2019年11月19日
生物材料的保藏中心登记入册编号:cgmccno.18812
附图说明
图1为针a2-1的形态照片。
图2为针a2-7的形态照片。
图3为针a2-8的形态照片。
图4为干粉菌剂大小对菌剂生长的影响。
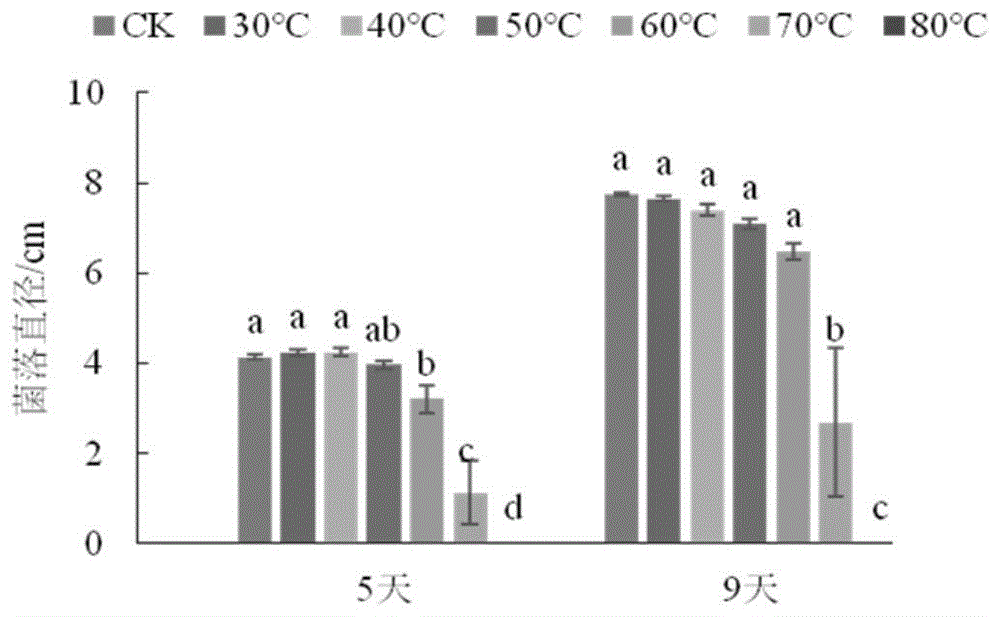
图5为烘干温度对菌剂生长的影响。同一培养时间下,从左至右依次为湿菌剂对照、烘干温度为30、40、50、60、70、80℃时制备的干粉菌剂。
具体实施方式
下面结合具体实施方式对本发明进行进一步的详细描述,给出的实施例仅为了阐明本发明,而不是为了限制本发明的范围。下述实施例中的实验方法,如无特殊说明,均为常规方法。下述实施例中所用的材料、试剂、仪器等,如无特殊说明,均可从商业途径得到。以下实施例中的定量试验,均设置三次重复实验,结果取平均值。下述实施例中,如无特殊说明,序列表中各核苷酸序列的第1位均为相应dna/rna的5′末端核苷酸,末位均为相应dna/rna的3′末端核苷酸。
实施例中所述操作均为无菌操作台中进行,试验操作前,先用紫外照射工作台20min。实施例中所有试剂与用具均为无菌试剂与用具。
液体mmn培养基(ph5.5):将cacl20.05g、mgso40.15g、nacl0.025g、fecl30.01g、kh2po40.5g、vitaminb1(硫胺素)0.0001g、(nh4)2hpo40.25g、葡萄糖10g、柠檬酸0.2g和maltextract(麦芽提取物)10g混合,得到混合物,然后加入蒸馏水并定容至1l,分装,121℃高压灭菌15min。
固体pda培养基:取去皮马铃薯200g,切成小块,加入1l蒸馏水,煮沸30min;纱布过滤后收集滤液,向滤液中加入葡萄糖20.0g、kh2po43.0g、mgso47h2o1.5g、维生素b110μg和琼脂15.0g,调ph值至6.0并用蒸馏水定容至1.0l,然后115℃灭菌15min。
实施例1、菌液的制备
所用菌株为针a2-1、针a2-7和针a2-8,均由发明人从内蒙古自治区锡林郭勒盟锡林浩特市北电胜利矿区的针茅根系中分离纯化所得。
检测针a2-1的its序列,其序列为序列表中序列1,鉴定为深色有隔内生真菌(dse)(darksideasp.),该菌株已于2019年4月8日保藏于中国微生物菌种保藏管理委员会普通微生物中心(简称cgmcc,地址为:北京市朝阳区北辰西路1号院3号),保藏编号为cgmccno.17465。深色有隔内生真菌的形态特征:黑色或深褐色,菌丝在根系内呈深色,有明显的横隔。针a2-1在根系内的形态照片见图1。
检测针a2-7的its序列,如序列表中序列2所示,鉴定为深色有隔内生真菌(dse)(darksideasp.)。针a2-7已于2019年11月19日保藏于中国微生物菌种保藏管理委员会普通微生物中心,保藏编号为cgmccno.18811。深色有隔内生真菌的形态特征:黑色或深褐色,菌丝在根系内呈深色,有明显的横隔。针a2-7在根系内的形态照片见图2。
检测针a2-8的its序列,如序列表中序列3所示,鉴定为深色有隔内生真菌(dse)格孢菌(pleosporalessp.)。针a2-8已于2019年11月19日保藏于中国微生物菌种保藏管理委员会普通微生物中心,保藏编号为cgmccno.18812。格孢菌(pleosporalessp.)的形态特征:黑色或深褐色,菌丝在根系内呈深色,有明显的横隔。针a2-8在根系内的形态照片见图3。
每种菌株均按照如下步骤制备菌液:
1、菌株的培养
将菌株进行活化,即在操作台内将使用无菌接种针挑取菌株边缘菌丝,接种到新的固体pda培养基进行培养。待其长出新菌落后,根据菌落颜色和形态等特征再次挑取边缘菌丝,接种到新的固体pda培养基进行培养。反复进行上述步骤,直至培养基中的菌落均匀一致。
2、菌液的制备
完成步骤1后,用无菌打孔器打取5mm×5mm菌饼,将2个菌饼置于装有150ml液体mmn培养基的250ml锥形瓶中,黑暗条件下、27℃、170r/min振荡培养,共培养24瓶。
步骤2完成后分别得到针a2-1菌液、针a2-7菌液和针a2-8菌液。
实施例2、含水率对菌剂的影响
所用菌液为实施例1的针a2-1菌液,将各菌液分别按照如下步骤进行操作制备菌剂:
将菌液于单层纱布下过滤,收集新鲜菌丝混匀。取15g新鲜菌丝于120℃下烘干12小时,计算出其含水率。将其余新鲜菌丝分随机为等量6份,置于洁净烘箱中,30℃烘干至其含水率分别为4-6%(不包括4%,包括6%)、3-4%(不包括3%,包括4%)、2-3%(不包括2%,包括3%)、1-2%(不包括1%,包括2%)、0-1%(不包括0,包括1%)及0,得到不同含水率的固体菌丝。
将不同含水率固体菌丝分别于超净工作台中接种于pda固体培养基中(培养皿大小为9mm×9mm),于28℃恒温培养箱中黑暗培养,每个培养皿中含有1个大小相同的菌片,每种范围含水率重复5个,将接种当天记为接种第0天。采用十字交叉法,于接种第2、5及9天测量菌落直径。对照组采用大小相同新鲜菌饼代替,重复5个。
结果(表1)表明,对于针a2-1,相同培养天数,菌落直径随着含水率呈现先不变后降低的趋势,临界含水率值为2-3%,因此在制作固体干燥菌剂时,其含水率不应低于2%。
表1、不同菌剂的菌落直径(cm)
注:表1中,ck表示湿菌剂对照;4-6%,不包括4%,包括6%;3-4%,不包括3%,包括4%;2-3%,不包括2%,包括3%;1-2%,不包括1%,包括2%;0-1%,不包括0,包括1%。同一列中,标有相同字母的数据间差异不显著,标有不同字母的数据间具有显著差异。
实施例3、粉末粒径对干粉菌剂的影响
按照实施例2的方法制备针a2-1的在30℃下含水率为3%的固体菌丝,将所得固体菌丝研磨后,分别过孔径为5mm、1mm及0.5mm筛子,分别得到粒径大于5mm、0.5-1mm(不包括1mm,包括0.5mm)及小于0.5mm干粉菌剂。
将不同粒径大小的干粉菌剂接种于pda培养基中,于28℃恒温培养箱中黑暗培养,每个培养皿中含有1种粒径大小的菌剂,每种菌剂重复5个,将接种当天记为接种第0天。采用十字交叉法,于接种第2、5及9天测量菌落直径。对照组采用相同大小新鲜菌饼代替,重复5个。
以培养天数为横坐标,菌落直径为纵坐标作柱形图,见图4。培养第2天时,随着菌剂粉末大小逐渐增大,菌落直径逐渐增大;随着培养时间的逐渐增长至第9天,菌剂粉末大小对菌落直径无显著影响。因此说明在一定范围内,菌剂粉末大小对菌剂生长无显著影响。由于菌剂粉末越小,相同质量下菌剂粉末数量越多,菌剂利用效率越高,因此制备干粉菌剂时,其粒径可小于0.5mm。
实施例4、烘干温度对菌剂生长的影响
所用菌液为实施例1的针a2-1菌液,按照如下步骤制备菌剂:
将针a2-1菌液于单层纱布下过滤,收集新鲜菌丝混匀。将新鲜菌丝随机分为等量7份,每份30g,将其中6份菌丝分别于30℃、40℃、50℃、60℃、70℃及80℃条件下烘干至含水率为3%,得到固体菌丝,并记录烘干时间。将不同条件下烘干的固体菌丝分别研磨充分,过筛(0.5mm),得到6种粒径小于0.5mm的干粉菌剂,将所得各干粉菌剂全部分别于超净工作台中接种于pda固体培养基中(培养皿大小为9mm×9mm)于28℃恒温培养箱中黑暗培养,每个培养皿中含有1种菌剂,每个处理重复5个,将接种当天记为接种第0天。采用十字交叉法,在接种第5、9天测量菌落直径。利用另外1份未烘干的新鲜菌丝作为湿菌剂对照进行接种,重复5个。
统计不同烘干温度下所需的烘干时间,烘干温度为30℃、40℃、50℃、60℃、70℃及80℃条件所需的烘干时间分别为96、84、66、42、24及18h。
接种不同时间各菌剂的菌落直径如表2所示,培养第5和9天时,随着烘干温度的增加,菌落直径均呈现先不变后变小的趋势,临界温度为60℃,图5。因此,针a2-1干粉菌剂制作的最佳烘干温度为60℃,在该温度下制备菌剂不仅保证了干粉菌剂的活性,也缩短了烘干所用时间,大大提高了其制作效率。
将实施例1的针a2-7菌液和针a2-8菌液分别替换上述步骤中的针a2-1菌液,并将烘干温度定为60℃,分别得到针a2-7干粉菌剂和针a2-8干粉菌剂,并分别利用针a2-7和针a2-8的未烘干的新鲜菌丝作为湿菌剂对照。将所得菌剂按照针a2-1菌剂的培养方法进行培养,接种不同时间各菌剂的菌落直径如表2所示。
在烘干温度为60℃时,所得针a2-1干粉菌剂接种第5天和第9天,菌落直径分别为湿菌剂对照的77.5%和83.7%,而所得针a2-7干粉菌剂接种第5天和第9天的菌落直径分别为湿菌剂对照的39.8%和58.2%,所得针a2-8干粉菌剂接种第5天和第9天的菌落直径分别为湿菌剂对照的35.1%和50.5%。说明,针a2-7与针a2-8不适于在烘干温度为60℃时制备干粉菌剂。
表2、不同菌剂的菌落直径(cm)
注:表2中,ck表示湿菌剂对照,同种菌的相同培养时间下的数据,标有不同字母表示差异显著,标有相同字母表示差异不显著。
实施例5、干粉菌剂的保存
按照实施例4的方法制备针a2-1菌株在烘干温度为60℃下的干粉菌剂,将制备好的菌剂置于洁净自封袋中,于室温(20℃)下分别保存10天和20天,再将菌剂接种于pda培养基中于28℃恒温培养箱中黑暗培养,观察其是否仍然具有活性。
结果发现,针a2-1干粉菌剂仍然可以于培养基中生长,说明针a2-1干粉菌剂于室温下最少可以保存20天。
<110>中国矿业大学(北京)、北京合生元生态环境工程技术有限公司
<120>一种深色有隔内生真菌干粉菌剂的制备方法
<160>3
<170>patentinversion3.5
<210>1
<211>589
<212>dna
<213>darksideasp.
<400>1
cttccgtaggtgaacctgcggaaggatcattacctggccttgggccgctcgcgggagcta60
gtcgcttgcgacgacgctaccgagggcgcttagcccttgactatcaccttgactacgtgc120
accttttgttgtttcctcggcaggtcacctgccgccaggaaccccctaaaccttttgtaa180
tagcatccaaacttctgaaaacaaaccaaattatttacaacttttaacaatggatctctt240
ggttctggcatcgatgaagaacgcagcgaaatgcgataagtagtgtgaattgcagaattc300
agtgaatcatcgaatctttgaacgcacattgcgccccatggtattccgtggggcatgcct360
gttcgagcgtcatttaccccctcaagctccgcttggtgttgggcgtctgtcccgcttcgc420
gcgcggactcgccccaaaggtattggcagcggtcgtgccagcttctcgcgcagcacattg480
cgcttctcgaggcaccggcgggcccgcgtccatcaagctcaccccccagtttgacctcgg540
atcaggtagggatacccgctgaacttaagcatatcaataagcggaggaa589
<210>2
<211>589
<212>dna
<213>darksideasp.
<400>2
cttccgtaggtgaacctgcggaaggatcattacctggccttgggccgctcgcgggagcta60
gtcgcttgcgacgacgctaccgagggcgcttagcccttgactatcaccttgactacgtgc120
accttttgttgtttcctcggcaggtcacctgccgccaggaaccccctaaaccttttgtaa180
tagcatccaaacttctgaaaacaaaccaaattatttacaacttttaacaatggatctctt240
ggttctggcatcgatgaagaacgcagcgaaatgcgataagtagtgtgaattgcagaattc300
agtgaatcatcgaatctttgaacgcacattgcgccccatggtattccgtggggcatgcct360
gttcgagcgtcatttaccccctcaagctccgcttggtgttgggcgtctgtcccgcttcgc420
gcgcggactcgccccaaaggtattggcagcggtcgtgccagcttctcgcgcagcacattg480
cgcttctcgaggcaccggcgggcccgcgtccatcaagctcaccccccagtttgacctcgg540
atcaggtagggatacccgctgaacttaagcatatcaataagcggaggaa589
<210>3
<211>593
<212>dna
<213>格孢菌(pleosporalessp.)
<400>3
cttccgtaggtgaacctgcggaaggatcattacctggccttgggccgctcgggggagcca60
gtcgctcgcgacggcgctgccttgggcgcttagcccttgactatcaccttgactacgtgc120
accttttgttgtttcctcggcaggtcctctgccgccaggaaccccctaaacctttttgca180
atagcatccaaacttctgaaaacaaaccaaatcatttacaacttttaacaatggatctct240
tggttctggcatcgatgaagaacgcagcgaaatgcgatatgtagtgtgaattgcagaatt300
cagtgaatcatcgaatctttgaacgcacattgcgccccatggtattccgtggggcatgcc360
tgttcgagcgtcatttaccccctcaagctccgcttggtgttgggcgtctgtcccgcttcg420
cgcgcggactcgccccaaaggtattggcagcggtcatgccagcttctcgcgcagcacatt480
gcgcttctcgaggcaccggcgggcccgcgtccatcaagctctcacccccccagtttgacc540
tcggatcaggtagggatacccgctgaacttaagcatatcaataagcggaggaa593
- 还没有人留言评论。精彩留言会获得点赞!