一种动物体内新型冠状病毒的荧光PT-PCR检测方法及试剂盒与流程
一种动物体内新型冠状病毒的荧光pt
‑
pcr检测方法及试剂盒
技术领域
1.本发明属于病毒检测技术领域,具体涉及一种动物体内新型冠 状病毒的荧光rt
‑
pcr检测方法及试剂盒。
背景技术:
2.申请号为cn202010096344.2公开了一种新型冠状病毒 2019
‑
ncov核酸检测技术,步骤包括样品制备及rna提取、反应体 系配置和pcr扩增、质量控制和结果分析与判定。操作简便、特异 性强、准确度高且可重复性强。
[0003][0004]
申请号为cn202010306852.9公开了一种具有抗突变性能的新型 冠状病毒核酸检测引物对、试剂盒及其应用,通过优选设计使得引物 对具有优异的抗突变性能,从而可以有效避免因新冠病毒基因突变导 致的检测灵敏度降低甚至假阴性现象的产生,从而实现对新型冠状病 毒sars
‑
cov
‑
2快速的、高敏感度和高准确性的实时荧光定量pcr 检测。
[0005]
申请号为cn202010060229.x公开了一种新型冠状病毒 2019
‑
ncov双通道实时荧光定量pcr检测引物和探针、试剂盒和方 法,采用单管双荧光通道同时检测新型冠状病毒2019
‑
ncov和内参 基因rnase p的存在,能检测肺泡灌洗液、鼻咽拭子、全血、血清、 粪便和组织等标本中新型冠状病毒2019
‑
ncov rna的存在。
技术实现要素:
[0006]
本发明的目的在于解决现有技术中用于动物体内新型冠状病毒检 测检测灵敏度不高的技术问题,提供一种动物体内新型冠状病毒的荧 光rt
‑
pcr检测方法及试剂盒,其检测限可达1拷贝/μl。
[0007]
本发明提供一种动物体内新型冠状病毒的荧光pt
‑
pcr检测方法, 包括以下步骤:
[0008]
s1、样本采集:从动物体内采集待检测样本,在2~8℃下保存12h;
[0009]
s2、核酸提取:在待检测样本中加入内标rna control,使用核 酸提取试剂盒提取待检测样本中的rna,得到样本并将样本冷冻保 存;
[0010]
s3、pcr试剂准备:在试剂盒中按体积比4:1量取pcr反应液a 和pcr反应液b置于离心管中震荡混匀后离心2~10s,按15μl/管分 装至pcr反应管中,得到pcr试剂;
[0011]
s4、pcr扩增检测:将样本、阴性对照、阳性对照各15μl分别 加入pcr试剂,震荡混匀后离心2~10s,在荧光pcr仪上进行扩增 检测;
[0012]
s5、质量判断:根据以下条件判断实验结果是否有效,
[0013]
判断条件一:阴性对照的结果为阴性;
[0014]
判断条件二:阳性对照的结果为阳性;
[0015]
当同时满足上述两个判断条件时,实验结果判断为是,进入步骤 s6;当上述两个判断条件有任意一条不满足时,实验结果判断为是, 返回步骤s3;
[0016]
s6、结果判定:
[0017]
阳性判断条件:fam通道ct值<38且有扩增曲线;
[0018]
阴性判断条件:fam通道ct值≥38无扩增曲线,且rox通道 ct值≤36有明显扩增曲线。fam为新型冠状病毒扩增信号,rox为 内标扩增信号。
[0019]
本发明所述的一种动物体内新型冠状病毒的荧光pt
‑
pcr检测方 法,作为优选方式,步骤s1中所述待检测样本为血液样本。
[0020]
本发明所述的一种动物体内新型冠状病毒的荧光pt
‑
pcr检测方 法,作为优选方式,包括以下步骤:
[0021]
s1、样本采集:从动物体内采集待检测样本,在2~8℃下保存12h;
[0022]
s2、样本处理:将待检测样本置于研磨管中研磨后加入pbs缓冲 液混合均匀,在5000r/min下离心5min后取上清液;
[0023]
s3、核酸提取:在上清液中加入内标rna control,使用核酸提 取试剂盒提取待检测样本中的rna,得到样本并将样本冷冻保存;
[0024]
s4、pcr试剂准备:在试剂盒中按体积比4:1量取pcr反应液a 和pcr反应液b置于离心管中震荡混匀后离心2~10s,按15μl/管分 装至pcr反应管中,得到pcr试剂;
[0025]
s5、pcr扩增检测:将样本、阴性对照、阳性对照各15μl分别 加入pcr试剂,震荡混匀后离心2~10s,在荧光pcr仪上进行扩增 检测;
[0026]
s6、质量判断:根据以下条件判断实验结果是否有效,
[0027]
判断条件一:阴性对照的结果为阴性;
[0028]
判断条件二:阳性对照的结果为阳性;
[0029]
当同时满足上述两个判断条件时,实验结果判断为是,进入步骤 s7;当上述两个判断条件有任意一条不满足时,实验结果判断为是, 返回步骤s4;
[0030]
s7、结果判定:
[0031]
阳性判断条件:fam通道ct值<38且有扩增曲线;
[0032]
阴性判断条件:fam通道ct值≥38无扩增曲线,且rox通道 ct值≤36有明显扩增曲线。
[0033]
本发明所述的一种动物体内新型冠状病毒的荧光pt
‑
pcr检测方 法,作为优选方式,步骤s1中所述待检测样本为组织样本。组织样 本可以为肺、扁桃体、淋巴结、肌肉等组织样本。
[0034]
本发明所述的一种动物体内新型冠状病毒的荧光pt
‑
pcr检测方 法,作为优选方式,pcr反应液a由引物、探针、5
×
neoscript rtpremix buffer、25
×
rox primer probe mix、rnase
‑
free te缓冲液组 成,所述pcr反应液b由25
×
neoscript rtase mix、rnase
‑
free te 缓冲液组成,阴性对照为rnase
‑
free te缓冲液,阳性对照包括 rnase
‑
free te缓冲液、pmd19
‑
t
‑
ncov
‑
o质粒原液。
[0035]
本发明所述的一种动物体内新型冠状病毒的荧光pt
‑
pcr检测方 法,作为优选方式,引物包括:
[0036]
上游引物:5
′‑
gcactcaatttgcttttgcttgt
‑3′
[0037]
下游引物:5
′‑
ggtgaaactgatctggcacgtaa
‑3′
;
[0038]
探针为
[0039]
5'
‑
fam
‑
ctgacggcgtaaaacacgtctatcagt
‑
bhq1
‑
3'。
[0040]
本发明所述的一种动物体内新型冠状病毒的荧光pt
‑
pcr检测方 法,作为优选方式,阴性对照结果为阴性时ct值≥38或无ct值,内 标结果为阳性时ct值≤36,阳性对照为阳性时ct值<38。
[0041]
本发明所述的一种动物体内新型冠状病毒的荧光pt
‑
pcr检测方 法,作为优选方式,扩增检测的靶区域为新型冠状病毒核壳蛋白基因 区域的高度保守区,即该基因片段与其它物种无交叉反应且基因稳定 不易发生变异。
[0042]
本发明所述的一种动物体内新型冠状病毒的荧光pt
‑
pcr检测方 法,作为优选方式,试剂盒包括盒体、设置在盒体上的盒盖和设置在 盒体内的试剂管、离心管,试剂管包括pcr反应液a试剂管、pcr 反应液b试剂管、内标试剂管、阳性对照试剂管和阴性对照试剂管。
[0043]
本发明的有益效果是:
[0044]
(1)可用于多种动物的新型冠状病毒核酸检测;
[0045]
(2)灵敏度高,检测限可达1拷贝/μl;
[0046]
(3)特异性强,与犬、猫、猪、禽等多种动物的多种病毒无交 叉反应,实现对新冠病毒的特异性检测。
附图说明
[0047]
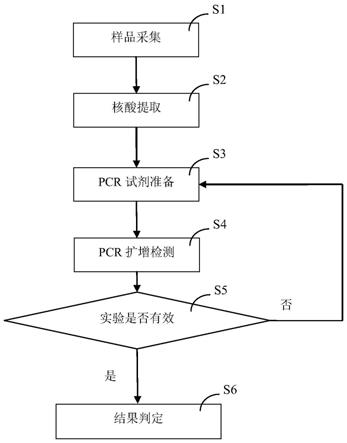
图1为一种动物体内新型冠状病毒的荧光pt
‑
pcr检测方法流程 图;
[0048]
图2为实施例2流程图;
具体实施方式
[0049]
下面将结合本发明实施例中的附图,对本发明实施例中的技术方 案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部 分实施例,而不是全部的实施例。
[0050]
如图1所示,一种动物体内新型冠状病毒的荧光pt
‑
pcr检测方 法,包括以下步骤:
[0051]
s1、样本采集:使用无菌注射器从动物体内采集血液样本,在2~8℃ 下保存12h;
[0052]
s2、核酸提取:在每份血液样本中加入2μl内标rna control, 使用核酸提取试剂盒提取待检测样本中的rna,得到样本并将样本 冷冻保存,并在2h内完成pcr扩增检测;
[0053]
s3、pcr试剂准备:根据pcr反应管数n,在试剂盒中取n
×ꢀ
12μlpcr反应液a和n
×
3μlpcr反应液b置于离心管中震荡混匀 后离心2~10s,以15μl/管分装至pcr反应管中,得到pcr试剂;其 中,pcr反应液a由引物、探针、5
×
neoscript rt premix buffer、25
×ꢀ
rox primer probe mix、rnase
‑
free te缓冲液组成,pcr反应液b 由25
×
neoscript rtase mix、rnase
‑
free te缓冲液组成,阴性对照为 rnase
‑
free te缓冲液,阳性对照包括rnase
‑
free te缓冲液、 pmd19
‑
t
‑
ncov
‑
o质粒原液;
[0054]
引物包括:浓度为0.4μmol/l
[0055]
上游引物:5
′‑
gcactcaatttgcttttgcttgt
‑3′
[0056]
下游引物:5
′‑
ggtgaaactgatctggcacgtaa
‑3′
;
[0057]
探针:浓度为0.2μmol/l
[0058]
5'
‑
fam
‑
ctgacggcgtaaaacacgtctatcagt
‑
bhq1
‑
3';
[0059]
s4、pcr扩增检测:用带滤芯的吸头分别取样本、阴性对照、阳 性对照各15μl装入pcr试剂管中,震荡混匀后离心2~10s,在荧光 pcr仪上进行扩增检测;
[0060]
pcr扩增检测的循环参数设定如下:
[0061][0062][0063]
s5、质量判断:根据以下条件判断实验结果是否有效,
[0064]
判断条件一:阴性对照的结果为阴性;
[0065]
判断条件二:阳性对照的结果为阳性;
[0066]
当同时满足上述两个判断条件时,实验结果判断为是,进入步骤 s6;当上述两个判断条件有任意一条不满足时,实验结果判断为是, 返回步骤s3;
[0067]
s6、结果判定:
[0068]
阳性判断条件:fam通道ct值<38且有扩增曲线;
[0069]
阴性判断条件:fam通道ct值≥38无扩增曲线,且rox通道 ct值≤36有明显扩增曲线。
[0070]
实施例2
[0071]
如图2所示,一种动物体内新型冠状病毒的荧光pt
‑
pcr检测方 法,包括以下步骤:
[0072]
s1、样本采集:使用清洁器材从动物体内采集肺、扁桃体、淋巴 结、肌肉等组织样本,在2~8℃下保存12h;
[0073]
s2、样本处理:将0.2g组织样本置于研磨管中研磨后加入1ml pbs缓冲液混合均匀,在5000r/min下离心5min后取上清液;
[0074]
s3、核酸提取:在每份血液样本中加入2μl内标rna control, 使用核酸提取试剂盒提取待检测样本中的rna,得到样本并将样本 冷冻保存,并在2h内完成pcr扩增检测;
[0075]
s4、pcr试剂准备:根据pcr反应管数n,在试剂盒中取n
×ꢀ
12μlpcr反应液a和n
×
3μlpcr反应液b置于离心管中震荡混匀 后离心2~10s,以15μl/管分装至pcr反应管中,得到pcr试剂;
[0076]
其中,pcr反应液a由引物、探针、5
×
neoscript rt premix buffer、 25
×
rox primer probe mix、rnase
‑
free te缓冲液组成,pcr反应 液b由25
×
neoscript rtase mix、rnase
‑
free te缓冲液组成,阴性 对照为rnase
‑
free te缓冲液,阳性对照包括rnase
‑
free te缓冲液、 pmd19
‑
t
‑
ncov
‑
o质粒原液;
[0077]
引物包括:
[0078]
上游引物:5
′‑
gcactcaatttgcttttgcttgt
‑3′
[0079]
下游引物:5
′‑
ggtgaaactgatctggcacgtaa
‑3′
;
[0080]
探针为
[0081]
5'
‑
fam
‑
ctgacggcgtaaaacacgtctatcagt
‑
bhq1
‑
3';
[0082]
s5、pcr扩增检测:用带滤芯的吸头分别取样本、阴性对照、阳 性对照各15μl装入
pcr试剂管中,震荡混匀后离心2~10s,在荧光 pcr仪上进行扩增检测;
[0083]
pcr扩增检测的循环参数设定如下:
[0084][0085]
s6、质量判断:根据以下条件判断实验结果是否有效,
[0086]
判断条件一:阴性对照的结果为阴性;
[0087]
判断条件二:阳性对照的结果为阳性;
[0088]
当同时满足上述两个判断条件时,实验结果判断为是,进入步骤 s7;当上述两个判断条件有任意一条不满足时,实验结果判断为是, 返回步骤s4;
[0089]
s7、结果判定:
[0090]
阳性判断条件:fam通道ct值<38且有扩增曲线;
[0091]
阴性判断条件:fam通道ct值≥38无扩增曲线,且rox通道 ct值≤36有明显扩增曲线。
[0092]
以上所述,仅为本发明较佳的具体实施方式,但本发明的保护范 围并不局限于此,任何熟悉本技术领域的技术人员在本发明揭露的技 术范围内,根据本发明的技术方案及其发明构思加以等同替换或改变, 都应涵盖在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1