同时检测次氯酸和过氧化亚硝基阴离子的荧光探针及其合成方法和应用与流程
[0001]
本发明涉及生物检测技术及临床医学检测领域,尤其是涉及一种同时检测次氯酸和过氧化亚硝基阴离子的荧光探针及其合成方法。
背景技术:
[0002]
次氯酸根作为活性氧物种的一种,在免疫抵抗微生物感染和炎症过程中发挥着极其重要的作用。在生物体中h2o2和氯离子在髓过氧化物酶的催化作用下产生次氯酸根,这是内因性次氯酸根的主要来源。保持适当的次氯酸根浓度对许多细胞功能至关重要,然而研究结果表明,一旦细胞内的次氯酸根水平不能保持在正常的生理水平范围内,将可能会导致多种疾病,例如动脉粥样硬化、关节炎、类风湿性关节炎甚至肿瘤,所以生物体内次氯酸的实时监测十分必要。
[0003]
过氧亚硝基是生物体内非常重要的一种活性氧物质,它是由一氧化氮和超氧自由基快速反应而生成,且在一些生理和病理过程中具有很高的活性。一方面,过量的过氧化亚硝酰会氧化或硝化细胞内的一些生物分子,如含有酪氨酸残基或硫醇的蛋白质、dna、含不饱和脂肪酸的脂滴等,使得这些生物分子遭到伤害,从而导致一系列疾病,包括癌症、糖尿病、阿尔兹海默症、帕金森氏症、亨廷顿舞蹈症和炎性疾病等。另一方面,已有研究表明,过氧化亚硝酰还参与了细胞的信号传导和细胞凋亡过程。
[0004]
近些年来,荧光生物成像技术因为具有深的组织穿透性、低背景荧光干扰、最小生物样本光损伤、检测灵敏度高等优点引起人们越来越多的关注。该技术为活体组织和细胞中超氧离子自由基(包括次氯酸和过氧化亚硝基阴离子等)的“实时、可视、定量”检测提供了途径,一系列近红外荧光探针设计合成,并用于动态观测研究活细胞和组织内活性氧自由基的产生、代谢、相互转化及其动态损伤生物机体的过程。
[0005]
然而,已报道的这些探针只是针对hocl或onoo-的单一识别,忽略了肿瘤等疾病的发生、发展是细胞内多种超氧化物交互作用的结果,不能反映出细胞内hocl和onoo-水平实时、动态的量变规律,而且反复、分步测试的准确度较低,系统误差较高。单独检测一种标志物并不能确定是否有该症状发生,并可能会造成误诊。
技术实现要素:
[0006]
本发明的目的就是为了克服上述现有技术存在的缺陷而提供一种同时检测次氯酸和过氧化亚硝基阴离子的荧光探针及其合成方法,该近红外荧光探针组织穿透性强、背景荧光干扰小、生物样本光损伤小,适用于细胞内次氯酸和过氧化亚硝基阴离子同时检测成像,从而能够减少使用多个探针造成的相互干扰或影响;该近红外荧光探针的合成方法工艺简单、成本低、操作方便、探针具有大的斯托克斯位移,响应灵敏度高,选择性好等优势。
[0007]
本发明的目的可以通过以下技术方案来实现:
[0008]
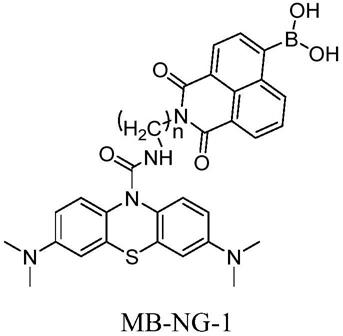
本发明中同时检测次氯酸和过氧化亚硝基阴离子的荧光探针,其特征在于,所述荧光探针的结构式如下:
[0009][0010]
其中n=0-10。
[0011]
本荧光探针中探针的主体结构为亚甲基蓝荧光团和萘酰亚胺荧光团。
[0012]
其中萘酰亚胺部分中4位联接的是硼酸和硼酸酯的结构。
[0013]
进一步地,所述荧光探针通过化合物4和化合物2在乙醇溶剂中回流反应,之后将反应产物柱层析分离,得淡黄色固体纯品,即为检测次氯酸和过氧化亚硝基阴离子的荧光探针;
[0014]
所述化合物4和化合物2之间的摩尔量为1:1.1,回流反应时间为18h。
[0015][0016]
进一步地,所述化合物2的制备过程为,将化合物1:醋酸铵:高碘酸钾按照摩尔量1:1.5-4:1.5-4溶解在乙醇溶液中,反应12h,过滤,萃取保留有机相并旋干,得到化合物2。
[0017][0018]
进一步地,所述化合物1的制备过程为,按照4-溴-1,8-萘二甲酸酐:联硼酸频哪醇酯:醋酸钾:钯催化剂=1:0.7-1.3:1-4:0.01-0.2的摩尔当量比依次取4-溴-1,8-萘二甲酸酐、联硼酸频哪醇酯、醋酸钾、钯催化剂进行混合,反应得到化合物1。
[0019]
进一步地,所述化合物4的制备过程为,把化合物3溶解到二氯甲烷中,把烷基二胺
用少量二氯甲烷稀释后恒压滴加到化合物3中,搅拌体系8h,反应完成后柱层析法得化合物4;
[0020]
所述化合物3的制备过程为:
[0021]
将亚甲基蓝盐酸盐和na2co3加入两口烧瓶中,并溶解在溶剂体积比为水:二氯甲烷=2:1的混合溶液中;
[0022]
之后将该混合物在30℃下搅拌,之后采用惰性气体保护,滴加用水溶解的连二亚硫酸钠;
[0023]
滴加完毕后,将混合物继续反应,向其中滴加用二氯甲烷溶解的双(三氯甲基)碳酸酯;
[0024]
滴加完毕后,将混合物再搅拌1-3小时,反应完毕后萃取,干燥有机相,旋干,得到化合物3。
[0025][0026]
作为本技术方案的另一种实施方式,所述荧光探针由化合物3和化合物8在1,4-二氧六环中回流反应所得。
[0027][0028]
进一步地,所述化合物8的制备过程为:
[0029]
将化合物2匀速滴加至烷基二胺和无水乙醇的混合溶液中,100℃回流20h,并在反应过程中采用氮气保护,反应完成后抽滤得到化合物8。
[0030]
作为本技术方案的另一种实施方式,所述化合物8的制备过程为:
[0031]
将化合物7在稀盐酸中乙醇溶液中进行水解反应2h,使得叔丁氧羰基脱保护,之后柱层析得到化合物8。
[0032][0033]
进一步地,所述化合物7的制备过程为:
[0034]
将化合物6、醋酸铵、高碘酸钾溶解在适量丙酮和水的混合溶液中,反应12h,过滤体系、萃取保留有机相并旋干得到化合物7;
[0035]
[0036]
进一步地,所述化合物6是由化合物5、联硼酸频哪醇酯、醋酸钾、钯催化剂在乙醇溶剂中反应得到,反应过程通过氮气保护,反应条件为110℃回流12h,反应结束后经过过滤,柱层析后得到化合物6;
[0037][0038]
进一步地,所述化合物5是由市售4-溴-1,8-萘二甲酸酐和boc-烷基二胺在1,4-二氧六环20ml中反应得到,反应过程通过氮气保护,反应条件为110℃回流12h,反应结束后经过过滤,柱层析后得到化合物5。
[0039]
本技术方案中涉及的烷基二胺为
[0040]
本发明中检测次氯酸和过氧化亚硝基阴离子在荧光生物成像中具有优异的应用,该近红外荧光探针由亚甲基蓝染料和萘酰亚胺构成,激发发射波长分别在蓝光450nm激发,560nm发射;或者808nm激发,560nm发射(萘酰亚胺的双光子激发)和红光620nm激发,680nm发射。两者的激发波长和发射波长有很大的斯托克斯位移,两者之间几乎无任何干扰,能够提高检测方法的灵敏度,降低测试方法的检测限。有望实现细胞内hocl和onoo-的差异化同时定量检测,对于动态观测研究细胞内活性氧自由基的产生、代谢、相互转化及其动态损伤生物机体的过程通路及机制,具有一定的理论意义;也为包括细胞活性、细胞毒性、细胞凋亡、细胞膜电位以及细胞周期等细胞功能方面的指标检测,提供一种有用的工具。
[0041]
与现有技术相比,本发明具有以下技术优势:
[0042]
1、本发明的荧光探针具有较好的化学、光稳定性,较好的溶解性,较高的次氯酸和过氧亚硝基选择性,不受其他活性氧和活性氮等物种的干扰。激光共聚焦成像实验表明这类探针具有较好的细胞通透性,对细胞和生物体毒副作用小。
[0043]
2、本发明探针分子激发和发射光谱在近红外区,属于近红外荧光探针,对过氧亚硝基响应的萘酰亚胺激发位于450nm(双光子萘酰亚胺激发808nm,发射在560nm),对次氯酸响应的亚甲基蓝激发在620nm发射在680nm,可以有效避免细胞自发荧光的干扰,提高检测方法的选择性和灵敏度。
附图说明
[0044]
图1是实施例1制备的mb-ng-1对水溶液中的次氯酸的荧光响应曲线。
[0045]
图2是实施例1制备的mb-ng-1对水溶液中的过氧亚硝基的荧光响应曲线。
[0046]
图3是实施例1制备的mb-ng-1荧光探针对水溶液的次氯酸对其他活性氧和活性氮的选择性。
[0047]
图4是实施例1制备的mb-ng-1荧光探针对水溶液的过氧亚硝基对其他活性氧和活性氮的选择性。
[0048]
图5是实施例1制备的mb-ng-1荧光探针对细胞内中次氯酸和过氧亚硝基的响应机理。
具体实施方式
[0049]
下面结合附图和具体实施例对本发明进行详细说明。
[0050]
实施例1
[0051]
本实施例中同时检测次氯酸和过氧化亚硝基阴离子的近红外荧光探针的合成方法,该合成方法包括如下步骤:
[0052]
步骤一、将市售4-溴-1,8-萘二甲酸酐(6g,21.74mmol)和联硼酸频哪醇酯(6.631g,26.1mmol)和醋酸钾(2.13g,21.74mmol):钯催化剂(10g,10.87mmol)加入到250ml的圆底烧瓶中,向混合物中添加其质量为10-20倍的1,4-二氧六环,氮气保护,110℃回流12h,过滤,柱层析后得化合物1备用(产率89%)。
[0053]
步骤二、将化合物1(2g,6.2mmol)、醋酸铵(1.4g,18.6mmol)、高碘酸钾(2.7g,12.4mmol)溶解在适量丙酮和水的混合溶液中,反应12h,过滤体系、萃取保留有机相并旋干有机相得化合物2备用(产率53%)。
[0054]
步骤三、将亚甲基蓝盐酸盐(10g,26.8mmol)和na2co3(2.85g,26.8mmol)加入1000ml的两口烧瓶中并溶解在水:二氯甲烷=2:1(溶剂体积比)中,并将该混合物在30℃下搅拌。惰性气体保护,滴加用水(20ml)溶解的连二亚硫酸钠(9.34g,53.6mmol)。滴加完毕后,将混合物继续反应,向其中滴加用二氯甲烷(50ml)溶解的双(三氯甲基)碳酸酯。滴加完毕后,将混合物再搅拌1-3小时。反应完毕后萃取。干燥有机相,旋干的化合物3备用(产率94%)。
[0055]
步骤四、将化合物3(3.5g,10mmol)和乙二胺(1.8g,30mmol,2ml)溶解在30ml二氯甲烷的100ml的圆底烧瓶中,反应6h后柱色谱得化合物4备用(产率75%)。
[0056]
步骤五、将化合物4(1.5g,6.2mmol)和化合物2(2.8g,7.5mmol)在适量的乙醇溶剂中回流18h后柱层析得橙黄色固体纯品,即为同时检测次氯酸和过氧化亚硝基阴离子的荧光探针。
[0057][0058]
1.荧光探针对次氯酸的荧光应答
[0059]
测试利用本发明合成方法合成的荧光探针在模拟生物体条件下(tris-hcl缓冲溶液,ph 7.4,终浓度5mm),5μm分子探针分别与不同浓度的次氯酸响应和探针空白的荧光发射光谱。体系中没有次氯酸存在时,在680nm处几乎无荧光。当次氯酸存在时,随着次氯酸浓度的增加探针在680nm处达到80倍的荧光增强。
[0060]
2.近红外荧光探针对onoo-的荧光应答
[0061]
测试利用本发明合成方法合成的近红外荧光探针在模拟生物体条件下(tris-hcl缓冲溶液,ph 7.4,终浓度5mm),5μm分子探针与不同浓度的onoo-作用及探针空白的荧光发射光谱。体系中没有onoo-存在时,没有绿色荧光。当onoo-存在时,560nm处荧光强度随着过氧亚硝基的浓度增加而可达到120倍的荧光增强。
[0062]
3.近红外荧光探针对次氯酸和过氧亚硝基的双重应答
[0063]
测试利用本发明合成方法合成的近红外荧光探针在模拟生物体条件下(tris-hcl缓冲溶液,ph 7.4,终浓度20mm),5μm分子探针与不同浓度的次氯酸和过氧亚硝基探针荧光光谱。体系中没有次氯酸和过氧亚硝基存在时,560nm和680nm处都没有荧光。当次氯酸和过氧亚硝基同时存在时,560nm和680nm处都有荧光。
[0064]
实施例2
[0065]
本实施例中同时检测次氯酸和过氧化亚硝基阴离子的近红外荧光探针的合成方法,该合成方法包括如下步骤:
[0066]
步骤一、将市售4-溴-1,8-萘二甲酸酐(6g,21.74mmol)和boc-烷基二胺(4g,25mmol)加入50ml的圆底烧瓶中,加入1,4-二氧六环20ml,氮气保护,110℃回流12h,过滤,柱层析后得化合物5备用(产率92%);
[0067]
步骤二、将所得化合物5(8.3g,20mmol)和联硼酸频哪醇酯(6.631g,26.1mmol)醋酸钾(2.13g,21.74mmol):钯催化剂(10g,10.87mmol)加入到250ml的圆底烧瓶中,加入适量乙醇作溶剂,氮气保护,110℃回流12h,过滤,柱层析后得化合物6备用(产率87%)。
[0068]
步骤三、将化合物6(9.4g,20mmol)在醋酸铵(4.2g,56mmol)、高碘酸钾(8.1g,37mmol)溶解在适量丙酮和水的混合溶液中,反应12h,过滤体系、萃取保留有机相并旋干有机相得化合物7备用(产率53%)。
[0069]
步骤四、将化合物7(9.4g,20mmol)在稀盐酸中乙醇溶液中水解boc脱保护搅拌2h,柱层析法得化合物8(产率93%)。
[0070]
步骤五、将亚甲基蓝盐酸盐(10g,26.8mmol)和na2co3(2.85g,26.8mmol)加入1000ml的两口烧瓶中并溶解在水:二氯甲烷=2:1(溶剂体积比)中,并将该混合物在30℃下搅拌。惰性气体保护,滴加用水(20ml)溶解的连二亚硫酸钠(9.34g,53.6mmol)。滴加完毕后,将混合物继续反应,向其中滴加用二氯甲烷(50ml)溶解的双(三氯甲基)碳酸酯。滴加完毕后,将混合物再搅拌1-3小时。反应完毕后萃取。干燥有机相,旋干的化合物3备用(产率94%)。
[0071]
步骤六、将化合物3(5.8g,20mmol)和化合物8(7.8g,23mmol)加入250ml的圆底烧瓶中,加入50ml 1,4-二氧六环100℃回流12h,色谱柱层析得橙黄色固体纯品,即为可以同时检测次氯酸和过氧化亚硝基阴离子的荧光探针。
[0072]
具体的反应结构式如下:
[0073][0074]
实施例3
[0075]
本实施例中同时检测次氯酸和过氧化亚硝基阴离子的近红外荧光探针的合成方法,该合成方法包括如下步骤:
[0076]
步骤一、将市售4-溴-1,8-萘二甲酸酐(6g,21.74mmol)和联硼酸频哪醇酯(6.631g,26.1mmol)和醋酸钾(2.13g,21.74mmol):钯催化剂(10g,10.87mmol)加入到250ml的圆底烧瓶中,加入50ml无水乙醇做溶剂,向混合物中添加其质量为10-20倍的1,4-二氧六环,氮气保护,110℃回流12h,过滤,柱层析后得化合物1备用(产率89%)。
[0077]
步骤二、将化合物1(2g,6.2mmol)、醋酸铵(1.4g,18.6mmol)、高碘酸钾(2.7g,12.4mmol)溶解在适量丙酮和水的混合溶液中,反应12h,过滤体系、萃取保留有机相并旋干有机相得化合物2备用(产率53%)。
[0078]
步骤三、将烷基二胺(1.8g,30mmol,2ml)加到在30ml无水乙醇的100ml的圆底烧瓶中,置换氮气,把化合物2(3.5g,10mmol)匀速滴加到体系中,100℃回流20h,反应完成后抽滤得化合物8(产率84%)。
[0079]
步骤四、将亚甲基蓝盐酸盐(10g,26.8mmol)和na2co3(2.85g,26.8mmol)加入1000ml的两口烧瓶中并溶解在水:二氯甲烷=2:1(溶剂体积比)中,并将该混合物在30℃下搅拌。惰性气体保护,滴加用水(20ml)溶解的连二亚硫酸钠(9.34g,53.6mmol)。滴加完毕后,将混合物继续反应,向其中滴加用二氯甲烷(50ml)溶解的双(三氯甲基)碳酸酯。滴加完毕后,将混合物再搅拌1-3小时。反应完毕后萃取。干燥有机相,旋干的化合物4备用(产率94%)。
[0080]
步骤五、将化合物3(1.5g,6.2mmol)和化合物8(2.8g,7.5mmol)在适量的乙醇溶剂中回流18h后柱色谱纯化硅胶柱层析分离得橙黄色固体纯品,即为可以同时检测次氯酸和过氧化亚硝基阴离子的荧光探针。
[0081]
具体的反应结构式如下:
[0082][0083]
实施例4
[0084]
本实施例中同时检测次氯酸和过氧化亚硝基阴离子的近红外荧光探针的合成方法,该合成方法包括如下步骤:
[0085]
步骤一、将市售4-溴-1,8-萘二甲酸酐(6g,21.74mmol)和联硼酸频哪醇酯(6.631g,26.1mmol)和醋酸钾(2.13g,21.74mmol):钯催化剂(10g,10.87mmol)加入到250ml的圆底烧瓶中,向混合物中添加其质量为10-20倍的1,4-二氧六环,氮气保护,110℃回流12h,过滤,柱层析后得化合物1备用(产率89%);
[0086]
步骤二、将亚甲基蓝盐酸盐(10g 26.8mmol)和na2co3(2.85g,26.8mmol),加入1000ml的两口烧瓶中并溶解在水:二氯甲烷=2:1(溶剂体积比)中,并将该混合物在30℃下搅拌。惰性气体保护,滴加用水(20ml)溶解的连二亚硫酸钠(9.34g,53.6mmol)。滴加完毕后,将混合物继续反应,向其中滴加用二氯甲烷(50ml)溶解的双(三氯甲基)碳酸酯。滴加完毕后,将混合物再搅拌1-3小时。反应完毕后萃取。干燥有机相,旋干的化合物3备用(产率94%)。
[0087]
步骤三、将化合物3(3.5g,10mmol)和烷基二胺(1.8g,30mmol,2ml)溶解在30ml二氯甲烷的100ml的圆底烧瓶中,反应6h后柱色谱得化合物备用(产率75%)。
[0088]
步骤四、将化合物1(1.5g,6.2mmol)和化合物4(2.8g,7.5mmol)在适量的乙醇溶剂中回流18h后柱色谱纯化硅胶柱层析分离所得化合物9
[0089]
步骤五:将化合物9(4.2g,6mmol,1eq)、醋酸铵(1.4g,18.6mmol)、高碘酸钾(2.7g,12.4mmol)溶解在适量丙酮和水的混合溶液中,反应12h,过滤体系、萃取保留有机相并旋干有机相得化合物mb-ni-1,即为同时检测次氯酸和过氧化亚硝基阴离子的荧光探针。
[0090]
具体的反应结构式下
[0091][0092]
上述的对实施例的描述是为便于该技术领域的普通技术人员能理解和使用发明。熟悉本领域技术的人员显然可以容易地对这些实施例做出各种修改,并把在此说明的一般原理应用到其他实施例中而不必经过创造性的劳动。因此,本发明不限于上述实施例,本领域技术人员根据本发明的揭示,不脱离本发明范畴所做出的改进和修改都应该在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1