一种高通量测序方法和试剂盒与流程
一种高通量测序方法和试剂盒
发明领域
1.本发明属于诊断和测序技术领域,并且涉及一种高通量测序方法和包含用于执行该方法的工具的试剂盒,其通过切换检测步骤结合捕获和扩增,优选所谓的“通过加尾和切换的捕获和扩增(capture and amplification by tailing andswitching)”(cats)和测序技术,优选所谓的“纳米球测序(nanobal1s sequencing)”技术。
2.发明背景
3.通过切换的捕获和扩增技术,尤其是所谓的“通过加尾和切换的捕获和扩增”(cats)技术,是一种产生dna文库的无连接酶的方法,用于从rna或dna进一步测序,并在国际专利申请wo2015/173402-a1中描述。
4.需要改进rna测序(或rna-seq),其使用下一代测序(ngs)技术来揭示给定时刻生物样品中rna的存在和数量,分析不断变化的细胞转录组。通过切换的捕获和扩增方案,尤其是cats方案,比使用连接酶通过在cdna合成过程中在单个反应管中加入衔接子的方案更有效地创建rna-seq文库。特别是,cats技术允许对敏感的、降解的、无细胞rna(cfrna)序列、血浆来源的rna序列、非编码rna(ncras)序列诸如mirna序列或长非编码rna(incrna序列))、外泌体rna序列、稀有且低输入的rna样本进行优化测序,它们是不同疾病诸如癌症的有效标志物。
5.改进的测序方案,尤其是drmanac等人(science 327:5961,78-81页(2010))公开的“纳米球测序”技术需要基因组dna的片段化,其中单个片段用于产生环状dna,其中平台特异性寡核苷酸衔接子将基因组dna序列分开。
6.获得的环状dna被扩增以有利地产生单链多联体(dna纳米球(dnb),具有大小为约300纳米),其可以在特定位置处固定化在基底上并保持彼此分离,因为它们在图案化基底上带负电荷,该图案化基底包含多达30亿个点,每个点包含一个(且仅一个)dna纳米球。
7.发明目的
8.本发明旨在提供一种新的检测和测序方法以及用于执行这种方法的工具,其不存在现有技术的方法和试剂盒的缺点。
9.本发明的第一目的是获得一种方法和用于执行该方法的工具,以改进核酸文库的产生和测序,尤其是敏感的、降解的、化学修饰的、无细胞核酸序列,尤其是所有种类的rna序列(编码或非编码rna序列、mirna、miscrna、pirna、rrna、sirna、snrna、snorna、trna
……
),无论从单个池中可能获得的掺入如何。
10.本发明的另一目的是获得这样的方法和用于执行该方法的工具,它们易于使用,并具有最少的实践时间;它们还是稳健的,并呈现改进的灵敏度和出色的重现性。
11.定义
12.本技术中引用的所有文献和类似材料,包括但不限于专利、专利申请、科学文章、书籍和网页,均通过援引以其整体明确并入本发明的说明书中。
13.除非另有定义,否则用于公开本发明的所有术语,包括技术和科学术语,均具有本发明领域中本领域普通技术人员通常理解的含义。
14.在本说明书和权利要求书中使用的单数形式“一个”、“一种”和“该/所述”包括单数和复数指示对象,除非说明书的内容另有明确规定。
15.术语“包含”、“包含”和“组成为”与“包括”或“含有”同义,并且是包括性的且非开放式的,并且不排除任何额外的、未列举的成员、要素或方法步骤。
16.术语“一个或多个”或“至少一个”本身是明确的,并且涵盖对这些成员中的任何的引用,其意指任何两个或多个成员且直至所有成员。
17.如本文所用的术语“约”,当提及可测量值,诸如化合物的量、剂量、时间等时,意在涵盖10%、9%、8%、7%、6%、5%、4%、3%、2%、1%、0.5%或甚至0.1%的指定量或值。
18.如在说明书和权利要求书中使用的,术语“核酸”包括聚合和寡聚大分子,由称为核苷酸的dna(脱氧核糖核酸)和rna(核糖核酸)组成,包含选自由以下组成的组的碱基:腺嘌呤(a)、胸腺嘧啶(t)、胞嘧啶(c)、鸟嘌呤(g)和尿嘧啶(u)。
19.术语“单链核酸”(ss核酸)是指仅由一条多核苷酸或寡核苷酸链组成的核酸。相反,“双链核酸”(ds核酸)由两条多核苷酸或寡核苷酸链组成,其中大部分核苷酸根据已知配对规则配对。
20.术语“基因扩增”是分子生物学中多年来使用的一种通过引物序列进行扩增的生化技术,一段或一部分dna的单个或几个拷贝通过跨越几个数量级的复制和拷贝,产生数千至数百万个特定dna序列的拷贝。最著名的基因扩增技术是所谓的“聚合酶链式反应或pcr”,如美国专利4,683,195-b2和4,683,202-b2中所描述的,使用引物序列和热稳定dna聚合酶,诸如从细菌水生栖热菌(bacteriumthermus aquatic)获得的taq聚合酶,允许热循环。
21.术语“引物”是指寡核苷酸序列,通常包含约12个核苷酸至约25个核苷酸,与感兴趣并且用作底物的靶序列特异性杂交,核苷酸可通过聚合酶聚合到该底物上。
22.术语“模板切换寡核苷酸”或tso是指在逆转录过程中与通过逆转录酶添加的非模板c核苷酸杂交的寡核苷酸。
技术实现要素:
23.本发明涉及核酸链序列的高通量(检测和)测序方法以及用于执行该方法的工具(优选包括在试剂盒中),该(检测和测序)方法至少包括以下步骤(或由以下步骤组成),优选连续的步骤:
[0024]-提供样品,尤其是液体或固体活检,诸如血液样品(优选血浆)、组织样品、化石、单细胞样品或甚至细胞的靶向区室(细胞核、内质网......),该样品包含天然单链核酸序列或天然双链核酸序列,
[0025]-可能地将天然单链核酸序列或天然双链核酸序列片段化成更小的核酸序列片段
[0026]-可能地使天然双链核酸序列变性
[0027]-可能地末端修复天然核酸序列
[0028]-可能地向天然单链或天然双链核酸序列或其片段的3-末端添加至少5个连续核苷酸,
[0029]-杂交与添加的核苷酸序列互补的引发寡核苷酸(priming oligonucleotide)序列,并用模板依赖性dna聚合酶合成cdna序列以获得双链核酸序列,
[0030]-将模板切换寡核苷酸(tso)与该生成的双链核酸序列杂交,
[0031]-延伸cdna链的3
′
末端以合成双链核酸序列,其中核酸序列的一条链包含引发寡核苷酸和与单链核酸序列以及模板切换寡核苷酸序列互补的cdna序列。当逆转录酶到达核酸序列的5
′
末端时,它会切换模板并在模板切换寡核苷酸(tso)上继续dna合成。含有三个3
′‑
末端核糖核苷酸x(rx)的tso有助于模板切换并携带衔接子序列,
[0032]-可能地添加夹板寡核苷酸序列(splint o1igo sequence),与衔接子dna序列杂交,连接形成环,并添加外切核酸酶以去除所有剩余的单链和双链dna产物以仅收集环状dna模板,
[0033]-通过对合成的链状核酸序列进行滚环复制来获得dna纳米球(dnb),
[0034]-将dna纳米球(dnb)固定在图案化阵列流动池上,
[0035]-进行碱基测序,优选地,该碱基测序通过选自由合成、连接酶碱基测序或焦磷酸测序组成的组的方法获得,以及
[0036]-获得对天然核酸序列的每个核苷酸的鉴定,优选通过纳米孔测序或成像,更优选在高分辨率ccd相机上。
[0037]
在本发明的方法中,合成的双链核酸序列呈现优选包含在约200和约500个核苷酸之间的长度。
[0038]
根据本发明,天然单链核酸序列或天然双链核酸序列优选地选自由片段化和/或亚硫酸氢盐转化的dna序列、mrna序列、mirna序列、小rna序列、pirna序列、亚硫酸氢盐转化的rna或其混合物组成的组。
[0039]
在根据本发明的方法中,至少5个连续的相同核苷酸优选地选自由a、t、c、g或u的核糖、脱氧核糖核苷酸或双脱氧核糖核苷酸组成的组,它们优选地通过选自由poly(a)-聚合酶、poly(u)-聚合酶、poly(g)-聚合酶、末端转移酶、dna连接酶、rna连接酶以及二核苷酸和三核苷酸rna连接酶组成的组的酶添加。
[0040]
本发明的另一方面涉及用于执行本发明的方法的装置或测序试剂盒,该试剂盒或装置包含存在于合适小瓶中的以下试剂或由以下试剂组成
[0041]-能够将核苷酸添加到单链核酸的3末端的试剂,
[0042]-用于基因扩增的试剂,优选用于进行逆转录酶pcr扩增的试剂,
[0043]-引发寡核苷酸,
[0044]-模板切换寡核苷酸,
[0045]-滚环复制酶,优选phi29dna聚合酶
[0046]-可能的环化试剂,
[0047]-可能的图案化流动池,和
[0048]-可能的不依赖模板的dna或rna聚合酶和阻断核苷酸,诸如3d-ntp、3-me-ntp和ddntp,以及
[0049]-可能的用于执行本发明的方法步骤的(书面)说明书。
[0050]
在根据本发明的方法、装置和试剂盒中,引发寡核苷酸优选地包含在wo2015/173402的权利要求9至12以及权利要求19和20中公开的核苷酸序列,其通过援引并入本文。
[0051]
有利地,在根据本发明的方法、装置和试剂盒中,滚环扩增是通过添加足量的phi 29dna聚合酶获得的,允许将多联体或dna纳米球(dnb)生产成包含环状模板的几个头对尾
拷贝的长单链dna序列,其中所得纳米颗粒自组装成紧密的dna球。
[0052]
该聚合酶复制环形dna,并且当它完成一个环时,它不会停止,而是通过剥离其先前复制的dna来继续复制。这种复制过程一遍又一遍地继续,形成了dna纳米球,将要测序的大量重复dna全部连接在一起。
[0053]
优选地,在根据本发明的方法、装置和试剂盒中,图案化阵列流动池是涂覆有二氧化硅、钛、六甲基二硅氮烷(hdms)和光刻胶材料的硅片,并且每个dna纳米球根据图案选择性地结合到带正电的氨基硅烷上。
[0054]
有利地,在本发明的方法中,通过添加由聚合酶并入的dntp来获得连接酶碱基测序,每个dntp优选地与特定标记缀合或包含允许在未来通过与一种或多种标记抗体结合而对它们进行检测的修饰(技术提高了灵敏度并降低了获得更准确和更长读段的成本),优选地标记是荧光团或染料并且可能地包含阻断添加延伸的终止子,其中未并入的dntp被洗去,其中图像被捕获,其中染料和终止子优选地被切割,并且其中重复这些步骤直到完成测序。
[0055]
coolngs技术基于使用附着在抗体上的多个荧光染料分子,提供更高的信噪比并减少昂贵材料的消耗,同时并入天然碱基,在测序循环之间没有干扰。
[0056]
此外,在本发明的方法中,添加的荧光团被激光激发,该激光激发特定波长的光,并且来自每个dna纳米球的荧光发射被高分辨率ccd相机捕获,并且其中每个dna纳米球的颜色对应于询问位置的碱基,并且其中计算机记录碱基位置信息。
[0057]
本发明的最后方面涉及根据前述权利要求中任一项的装置、试剂盒或方法的用途。优选的用途被提议用于测序或表达分析,用于克隆标记,用于基因或突变的鉴定,用于人类或动物疾病或法医学的检测,用于传染病和病毒、细菌、真菌、动物或植物(包括它们的衍生细胞)的基因组的分析,用于植物、水果的表征,植物或水果疾病的育种检查检测。
[0058]
本发明将在以下实施例中描述,其作为本发明的非限制性优选实施方式呈现。
实施例
[0059]
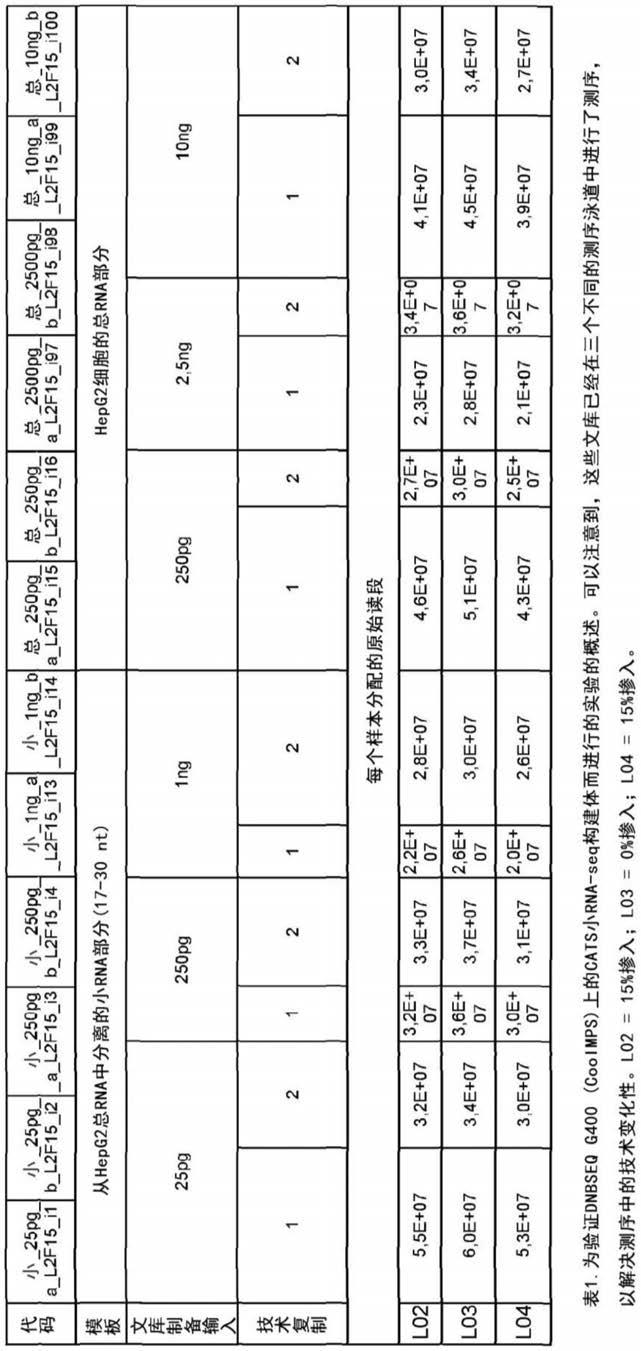
下表1示出了为验证本发明的方法而进行的实验的概述,通过切换检测,诸如在dnbseq-g400(用于“纳米球测序”的cooimps系统(来自mgi))上的cats小rna-seq构建体,进行捕获和扩增。
[0060]
在表1中,l02=15%掺入;l03=0%掺入以及l05=15%掺入。这些文库已经在三个不同的测序泳道中进行了测序,以解决测序中的技术变化性。
[0061]
申请人获得了泳道03中测序的样品的平均每碱基序列分布。这种分布显示了典型的通过切换检测构建体即cats小rna-seq构建体的捕获和扩增,具有与测序的rna(小的非编码rna)的性质相符的短插入短插入大小(short insertshort insert size),并且也显示了在小rna读段后在文库制备过程中合成的预期的poly(a)尾部。
[0062]
n含量是非空的,但足够低,不会在以后的数据分析过程中引起问题。前(1-3)个测序循环中不存在模板切换基序(模板切换寡核苷酸tso),因为这些循环的测序是在暗循环模式下完成的。
[0063]
申请人还获得了在泳道03中测序的dnb的平均质量分布。由于获得的1a03中的绝大多数dnb(>85%)呈现的质量得分高于30(图2的下部),这使得在dnbseq-g400系统上
cats小rna文库的测序是一种高效且高质量的测序系统。
[0064]
使用本发明的方法,申请人选择了在不同测序泳道中每样品分配的读段(#指数n
°
),以及在不同测序泳道中样品的平均q30%。获得的结果表明,无论掺入如何,文库都能够正常测序,并产生高质量的读段(q30>85%)。
[0065]
此外,对于不同泳道中的不同样品,获得了修整读段中的映射读段的相对比例(%)。过滤和修整之后的大多数读段都映射(star)到参考基因组(hg19)到cats小rna文库的预期百分比。测序方法在不同的泳道中执行,无论掺入含量如何,都不会影响映射统计。这意味着根据本发明的测序方法和系统可跨泳道重现。
[0066]
通过使用ensembl注释获得了在泳道03中测序的文库的在tpm高于或等于2下的完整多样性生物分型。大多数文库内容被注释为非编码rna,即使某些部分来自蛋白质编码转录物,构成降解的产物,其在文库制备过程中被捕获。这种生物分型表示出乎意料地完全符合通过现有技术方法和系统,尤其是所谓的illumina(ilmn)测序方法和系统获得的文库表示。
[0067]
通过使用ensembl注释获得了在泳道03中测序的文库的在tpm高于或等于2下的小的非编码rna多样性生物分型。通过本发明的方法和系统鉴定的非编码rna跨越了从mirna到snorna的范围的广泛多样的小的非编码rna。因此,根据本发明要求保护的方法和系统与现有技术的已知方法和系统,尤其是所谓的illumina(ilmn)测序方法和系统一样有效。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1