人源化抗Claudin18.2(CLDN18.2)抗体的制作方法
no:59;(vii)vl结构域,其包含seq id no:56;和/或vh结构域,其包含seq id no:60;(viii)vl结构域,其包含seq id no:56;和/ 或vh结构域,其包含seq id no:61;(ix)vl结构域,其包含seq idno:56;和/或vh结构域,其包含seq id no:62;(x)vl结构域,其包含seq id no:56;和/或vh结构域,其包含seq id no:63;(xi) vl结构域,其包含seq id no:57;和/或vh结构域,其包含seq id no: 59;(xii)vl结构域,其包含seq id no:57;和/或vh结构域,其包含seq id no:60;(xiii)vl结构域,其包含seq id no:57;和/或vh结构域,其包含seq id no:61;(xiv)vl结构域,其包含seq id no:57;和/或vh结构域,其包含seq id no:62;(xv)vl结构域,其包含seqid no:57;和/或vh结构域,其包含seq id no:63;(xvi)vl结构域,其包含seq id no:58;和/或vh结构域,其包含seq id no:59;(xvii) vl结构域,其包含seq id no:58;和/或vh结构域,其包含seq id no: 60;(xviii)vl结构域,其包含seq id no:58;和/或vh结构域,其包含seq id no:61;(xix)vl结构域,其包含seq id no:58;和/或vh 结构域,其包含seq id no:62;(xx)vl结构域,其包含seq id no: 58;和/或vh结构域,其包含seq id no:63;(xxi)vl结构域,其包含 seq id no:55;和/或vh结构域,其包含seq id no:64;(xxii)vl 结构域,其包含seq id no:56;和/或vh结构域,其包含seq id no: 64;(xxiii)vl结构域,其包含seq id no:57;和/或vh结构域,其包含seq id no:64;(xxiv)vl结构域,其包含seq id no:58;和/或 vh结构域,其包含seq id no:64;(xxv)vl结构域,其包含seq id no: 55;和/或vh结构域,其包含seq id no:65;(xxvi)vl结构域,其包含seq id no:56;和/或vh结构域,其包含seq id no:65;(xxvii) vl结构域,其包含seq id no:57;和/或vh结构域,其包含seq id no: 65;或(xxviii)vl结构域,其包含seq id no:58;和/或vh结构域,其包含seq id no:65。
8.在一些实施方案中,本技术提供抗cldn18.2抗体或其抗原结合片段,其包含轻链可变结构域(vl)和重链可变结构域(vh),其中vl 结构域包含:(i)框架区1(fw1),其包含seq id no:34、37、39或20); (ii)框架区2(fw2),其包含seq id no:35、38或40;(iii)框架区3 (fw3),其包含seq id no:36或22;以及(iv)框架区4(fw4),其包含seq id no:19;和/或其中vh包含:(i)框架区1(fw1),其包含 seq id no:41、44、46或49;(ii)框架区2(fw2),其包含seq id no: 42、47、50或52;(iii)框架区3(fw3),其包含seq id no:43、45、48或51;以及(iv)框架区4(fw4),其包含seq id no:26或30。在一些实施方案中,vl包含:(i)fw1,其包含seq id no:34;fw2,其包含seq id no:35;fw3,其包含seq id no:36;和fw4,其包含 seq id no:19;(ii)fw1,其包含seq id no:37;fw2,其包含seq idno:38;fw3,其包含seq id no:36;和fw4,其包含seq id no: 19;(iii)fw1,其包含seq id no:39;fw2,其包含seq id no:40; fw3,其包含seq id no:22;和fw4,其包含seq id no:19;或(iv) fw1,其包含seq id no:20;fw2,其包含seq id no:40;fw3,其包含seq id no:22;和fw4,其包含seq id no:19;和/或vh包含: fw1,其包含seq id no:41;fw2,其包含seq id no:42;fw3,其包含seq id no:43;和fw4,其包含seq id no:26;(ii)fw1,其包含seq id no:44;fw2,其包含seq id no:42;fw3,其包含seq idno:45;和fw4,其包含seq id no:26;(iii)fw1,其包含seq id no: 46;fw2,其包含seq id no:47;fw3,其包含seq id no:48;和fw4,其包含seq id no:30;(iv)fw1,其包含seq id no:49;fw2,其包含seq id no:50;fw3,其包含seq id no:51;和fw4,其包含seqid no:26;(v)fw1,其包含seq id no:49;fw2,其包含seq id no: 52;fw3,其包含seq id no:51;和fw4,其包含seq id no:26;(vi) fw1,其包含seq id no:
49;fw2,其包含seqidno:50;fw3,其包含seqidno:51;和fw4,其包含seqidno:26;或(vii)fw1,其包含seqidno:49;fw2,其包含seqidno:52;fw3,其包含seqidno:51;和fw4,其包含seqidno:26;在一些实施方案中,(a)所述vl包含:fw1,其包含seqidno:34;fw2,其包含seqidno:35;fw3,其包含seqidno:36;和fw4,其包含:seqidno:19;并且所述vh包含:fw1,其包含seqidno:41;fw2,其包含seqidno:42;fw3,其包含seqidno:43;和fw4,其包含seqidno:26;(b)所述vl包含:fw1,其包含seqidno:34;fw2,其包含seqidno:35;fw3,其包含seqidno:36;和fw4,其包含:seqidno:19;并且所述vh包含:fw1,其包含seqidno:44;fw2,其包含seqidno:42;fw3,其包含seqidno:45;和fw4,其包含seqidno:26;(c)所述vl包含:fw1,其包含seqidno:34;fw2,其包含seqidno:35;fw3,其包含seqidno:36;和fw4,其包含:seqidno:19;并且所述vh包含:fw1,其包含seqidno:46;fw2,其包含seqidno:47;fw3,其包含seqidno:48;和fw4,其包含seqidno:30;(d)所述vl包含:fw1,其包含seqidno:34;fw2,其包含seqidno:35;fw3,其包含seqidno:36;和fw4,其包含:seqidno:19;并且所述vh包含:fw1,其包含seqidno:49;fw2,其包含seqidno:50;fw3,其包含seqidno:51;和fw4,其包含seqidno:26;(e)所述vl包含:fw1,其包含seqidno:34;fw2,其包含seqidno:35;fw3,其包含seqidno:36;和fw4,其包含:seqidno:19;并且所述vh包含:fw1,其包含seqidno:49;fw2,其包含seqidno:52;fw3,其包含seqidno:51;和fw4,其包含seqidno:26;(f)所述vl包含:fw1,其包含seqidno:37;fw2,其包含seqidno:38;fw3,其包含seqidno:36;和fw4,其包含:seqidno:19;并且所述vh包含:fw1,其包含seqidno:41;fw2,其包含seqidno:42;fw3,其包含seqidno:43;和fw4,其包含seqidno:26;(g)所述vl包含:fw1,其包含seqidno:37;fw2,其包含seqidno:38;fw3,其包含seqidno:36;和fw4,其包含:seqidno:19;并且所述vh包含:fw1,其包含seqidno:44;fw2,其包含seqidno:42;fw3,其包含seqidno:45;和fw4,其包含seqidno:26;(h)所述vl包含:fw1,其包含seqidno:37;fw2,其包含seqidno:38;fw3,其包含seqidno:36;和fw4,其包含:seqidno:19;并且所述vh包含:fw1,其包含seqidno:46;fw2,其包含seqidno:47;fw3,其包含seqidno:48;和fw4,其包含seqidno:30;(i)所述vl包含:fw1,其包含seqidno:37;fw2,其包含seqidno:38;fw3,其包含seqidno:36;和fw4,其包含:seqidno:19;并且所述vh包含:fw1,其包含seqidno:49;fw2,其包含seqidno:50;fw3,其包含seqidno:51;和fw4,其包含seqidno:26;(j)所述vl包含:fw1,其包含seqidno:37;fw2,其包含seqidno:38;fw3,其包含seqidno:36;和fw4,其包含:seqidno:19;并且所述vh包含:fw1,其包含seqidno:49;fw2,其包含seqidno:52;fw3,其包含seqidno:51;和fw4,其包含seqidno:26;(k)所述vl包含:fw1,其包含seqidno:39;fw2,其包含seqidno:40;fw3,其包含seqidno:22;和fw4,其包含:seqidno:19;并且所述vh包含:fw1,其包含seqidno:41;fw2,其包含seqidno:42;fw3,其包含seqidno:43;和fw4,其包含seqidno:26;(l)所述vl包含:fw1,其包含seqidno:39;fw2,其包含seqidno:40;fw3,其包含seqidno:22;和fw4,其包含:seqidno:19;并且所述vh包含:fw1,其包含seqidno:44;fw2,其包含seqidno:42;fw3,其包含seqidno:45;和fw4,其包含seqidno:26;(m)所述vl包含:fw1,其包含seqidno:39;fw2,其包含seqidno:40;fw3,其包含seqidno:22;和fw4,其包含:seqidno:19;并且所述vh包含:fw1,其包含
seqidno:46;fw2,其包含seqidno:47;fw3,其包含seqidno:48;和fw4,其包含seqidno:30;(n)所述vl包含:fw1,其包含seqidno:39;fw2,其包含seqidno:40;fw3,其包含seqidno:22;和fw4,其包含:seqidno:19;并且所述vh包含:fw1,其包含seqidno:49;fw2,其包含seqidno:50;fw3,其包含seqidno:51;和fw4,其包含seqidno:26;(o)所述vl包含:fw1,其包含seqidno:39;fw2,其包含seqidno:40;fw3,其包含seqidno:22;和fw4,其包含:seqidno:19;并且所述vh包含:fw1,其包含seqidno:49;fw2,其包含seqidno:52;fw3,其包含seqidno:51;和fw4,其包含seqidno:26;(p)所述vl包含:fw1,其包含seqidno:20;fw2,其包含seqidno:40;fw3,其包含seqidno:22;和fw4,其包含:seqidno:19;并且所述vh包含:fw1,其包含seqidno:41;fw2,其包含seqidno:42;fw3,其包含seqidno:43;和fw4,其包含seqidno:26;(q)所述vl包含:fw1,其包含seqidno:20;fw2,其包含seqidno:40;fw3,其包含seqidno:22;和fw4,其包含:seqidno:19;并且所述vh包含:fw1,其包含seqidno:44;fw2,其包含seqidno:42;fw3,其包含seqidno:45;和fw4,其包含seqidno:26;(r)所述vl包含:fw1,其包含seqidno:20;fw2,其包含seqidno:40;fw3,其包含seqidno:22;和fw4,其包含:seqidno:19;并且所述vh包含:fw1,其包含seqidno:46;fw2,其包含seqidno:47;fw3,其包含seqidno:48;和fw4,其包含seqidno:30;(s)所述vl包含:fw1,其包含seqidno:20;fw2,其包含seqidno:40;fw3,其包含seqidno:22;和fw4,其包含:seqidno:19;并且所述vh包含:fw1,其包含seqidno:49;fw2,其包含seqidno:50;fw3,其包含seqidno:51;和fw4,其包含seqidno:26;(t)所述vl包含:fw1,其包含seqidno:20;fw2,其包含seqidno:40;fw3,其包含seqidno:22;和fw4,其包含:seqidno:19;并且所述vh包含:fw1,其包含seqidno:49;fw2,其包含seqidno:52;fw3,其包含seqidno:51;和fw4,其包含seqidno:26;(u)所述vl包含:fw1,其包含seqidno:34;fw2,其包含seqidno:35;fw3,其包含seqidno:36;和fw4,其包含:seqidno:19;并且所述vh包含:fw1,其包含seqidno:49;fw2,其包含seqidno:50;fw3,其包含seqidno:51;和fw4,其包含seqidno:26;(v)所述vl包含:fw1,其包含seqidno:37;fw2,其包含seqidno:38;fw3,其包含seqidno:36;和fw4,其包含:seqidno:19;并且所述vh包含:fw1,其包含seqidno:49;fw2,其包含seqidno:50;fw3,其包含seqidno:51;和fw4,其包含seqidno:26;(w)所述vl包含:fw1,其包含seqidno:39;fw2,其包含seqidno:40;fw3,其包含seqidno:22;和fw4,其包含:seqidno:19;并且所述vh包含:fw1,其包含seqidno:49;fw2,其包含seqidno:50;fw3,其包含seqidno:51;和fw4,其包含seqidno:26;(x)所述vl包含:fw1,其包含seqidno:20;fw2,其包含seqidno:40;fw3,其包含seqidno:22;和fw4,其包含:seqidno:19;并且所述vh包含:fw1,其包含seqidno:49;fw2,其包含seqidno:50;fw3,其包含seqidno:51;和fw4,其包含seqidno:26;(y)所述vl包含:fw1,其包含seqidno:34;fw2,其包含seqidno:35;fw3,其包含seqidno:36;和fw4,其包含:seqidno:19;并且所述vh包含:fw1,其包含seqidno:49;fw2,其包含seqidno:52;fw3,其包含seqidno:51;和fw4,其包含seqidno:26;(z)所述vl包含:fw1,其包含seqidno:37;fw2,其包含seqidno:38;fw3,其包含seqidno:36;和fw4,其包含:seqidno:19;并且所述vh包含:fw1,其包含seqidno:49;fw2,其包含seqidno:52;fw3,其包含seqidno:51;和fw4,其包含seqidno:26;(aa)所述vl包含:fw1,其包含
seq id no:39;fw2,其包含seqid no:40;fw3,其包含seq id no:22;和fw4,其包含:seq id no: 19;并且所述vh包含:fw1,其包含seq id no:49;fw2,其包含seqid no:52;fw3,其包含seq id no:51;和fw4,其包含seq id no: 26;或(bb)所述vl包含:fw1,其包含seq id no:20;fw2,其包含seq id no:40;fw3,其包含seq id no:22;和fw4,其包含:seqid no:19;并且所述vh包含:fw1,其包含seq id no:49;fw2,其包含seq id no:52;fw3,其包含seq id no:51;和fw4,其包含 seq id no:26。在一些实施方案中,抗cldn18.2抗体或其抗原结合片段还包含例如描述于pct/cn2019/078150中的抗cdln抗体的6个互补性决定区(cdr),所述文献的内容通过引用整体并入本技术。
9.在一些实施方案中,抗cldn18.2抗体或其抗原结合片段包含人 igg的fc序列。在一些实施方案中,人igg是igg1、igg2、igg3或igg4。在一些实施方案中,抗cldn18.2抗体或其抗原结合片段包含fc结构域,所述fc结构域包含seq id no:109、seq id no:110或seq id no: 111的氨基酸序列。在一些实施方案中,抗体是人源化抗体。在一些实施方案中,本文提供的抗cldn18.2抗体的抗原结合片段选自由以下组成的组: fab、fab’、f(ab)’2、单链fv(scfv)、fv片段、双抗和线性抗体。在一些实施方案中,抗体是多特异性抗体。在一些实施方案中,通过本技术提供的抗体或其抗原结合片段结合的cldn18.2是人cldn18.2。在一些实施方案中,抗cldn18.2抗体或抗原结合片段与治疗剂缀合。在一些实施方案中,抗cldn18.2抗体或抗原结合片段与标记物缀合。在一些实施方案中,标记物选自由以下组成的组:放射性同位素、荧光染料和酶。
10.在一些实施方案中,提供了编码本技术提供的抗cldn18.2抗体或其抗原结合片段的分离的核酸分子。在一些实施方案中,提供了编码核酸分子的表达载体。在一些实施方案中,提供了包含核酸分子或表达载体的宿主细胞。在一些实施方案中,提供了产生抗cldn18.2抗体的方法,包含培养宿主细胞和从细胞培养物中回收抗体。
11.在一些实施方案中,提供了包含本技术所述的抗cldn18.2抗体或其抗原结合片段以及药学上可接受的载体的组合物。
12.在一些实施方案中,提供了检测来自患者的样品中的cldn18.2 蛋白的方法,其通过使本技术所述的抗cldn18.2抗体或其抗原结合片段与样品接触并检测与cldn18.2蛋白结合的抗cldn18.2抗体(或片段) 来进行。在一些实施方案中,用于该方法的抗cldn18.2抗体或其抗原结合片段与标记(例如,放射性同位素、荧光染料和酶)缀合。在一些实施方案中,所述方法包含免疫组织化学测定(ihc)或elisa测定。
13.在一些实施方案中,提供了治疗受试者的癌症的方法,包含施用有效量的包含本技术所述的抗cldn18.2抗体或其抗原结合片段以及药学上可接受的载体的组合物。在一些实施方案中,癌症选自实体瘤、胃癌、食管癌、胃食管交界癌、胰腺癌、胆管癌、肺癌、卵巢癌、结肠癌、肝癌、头颈癌、胆囊癌。在一些实施方案中,向受试者进一步施用选自由以下组成的组的治疗剂:抗肿瘤剂、化疗剂、生长抑制剂和细胞毒性剂。
附图说明
14.图1a显示了自制嵌合抗hcldn18.2抗体和下列纯化的 hucldn18.2抗体:v.13、v.1、v.2、v.6、v.7、v.8、v.9、v.10、v.17和v.19 的非还原性sds page(十二烷基硫酸钠-聚丙烯酰胺凝胶电泳)分析。
15.图1b显示了自制嵌合抗hcldn18.2抗体和下列纯化的 hucldn18.2抗体:v.13、v.1、v.2、v.6、v.7、v.8、v.9、v.10、v.17和v.19 的还原性sds page分析。
16.图1c显示了自制嵌合抗hcldn18.2抗体和下列纯化的 hucldn18.2抗体:v.11、v.12、v.13、v.14、v.15、v.16、v.18和v.20的非还原性sds page分析。
17.图1d显示了自制嵌合抗hcldn18.2抗体和下列纯化的 hucldn18.2抗体:v.11、v.12、v.13、v.14、v.15、v.16、v.18和v.20的还原性sds page分析。
18.图1e显示了下列纯化的hucldn18.2抗体:v.22、v.23、v.24、 v.26和v.27的还原性sds page分析,和下列纯化的hucldn18.2抗体: v.22、v.23、v.24、v.26、v.27和v.28的非还原性sds-page分析。
19.图1f显示了下列纯化的hucldn18.2抗体:v.19和v.28的还原性sds-page分析和非还原sds-page分析。
20.图2a提供了实验结果,进行该实验用于评价与自制嵌合抗 cldn18.2抗体和参照抗cldn18.2抗体imab362相比,人源化抗cldn18.2抗体v.1、v.2、v.6、v.8、v.9、v.10、v.17和v.19与在 hek293-cldn18.2细胞表面表达的cldn18.2的结合。
21.图2b提供了实验结果,进行该实验用于评价与自制嵌合抗 cldn18.2抗体和参照抗cldn18.2抗体imab362相比,人源化抗cldn18.2抗体v.11、v.12、v.13、v.14、v.15、v.16、v.18和v.20与在 hek293-cldn18.2细胞表面表达的cldn18.2的结合。
22.图3提供了实验结果,进行该实验用于评价与自制嵌合抗 cldn18.2抗体和参照抗cldn18.2抗体imab362相比,人源化抗 cldn18.2抗体v.1、v.2、v.11、v.14、v.15、v.16、v.19和v.20与在kato iii 人胃癌细胞表面表达的cldn18.2的结合。
23.图4提供了实验结果,进行该实验用于评价与自制嵌合抗 cldn18.2抗体和参照抗cldn18.2抗体imab362相比,人源化抗 cldn18.2抗体v.22、v.23、v.24、v.26、v.27和v.28与在hek293-cldn18.2 细胞表面表达的cldn18.2的结合。
24.图5提供了实验结果,进行该实验用于评价与自制嵌合抗 cldn18.2抗体和参照抗cldn18.2抗体imab362相比,人源化抗 cldn18.2抗体v.23、v.24、v.27和v.28与在kato iii人胃癌细胞表面表达的cldn18.2的结合。
25.图6提供了实验结果,进行该实验用于评价人源化抗cldn18.2 抗体v.1、v.2、v.6、v.8、v.9、v.10、v.11、v.12、v.13、v.14、v.15、v.16、 v.17、v.18、v.19、v.20、v.22、v.23、v.24、v.26、v.27和v.28与cldn18.1 的结合。
26.图7a提供了实验结果,进行该实验用于评价人源化抗 cldn18.2抗体v.1、v.2、v.6、v.8、v.9、v.10、v.11、v.12、v.13、v.14、v.15、 v.16、v.17、v.18、v.19、v.20、v.22、v.23、v.24、v.26、v.27和v.28与肽2c 的结合。
27.图7b提供了实验结果,进行该实验用于评价人源化抗cldn18.2 抗体v.1、v.2、v.6、v.8、v.9、v.10、v.11、v.12、v.13、v.14、v.15、v.16、v.17、v.18、v.19、v.20、v.22、v.23、v.24、v.26、v.27和v.28与肽3c的结合。
28.图8提供了实验结果,进行该实验用于评价与包含野生型人igg1 fc结构域的人源化抗cldn18.2 v.19抗体相比人源化抗cldn18.2抗体 v.19_fc变体1、v.19_fc变体2和v.19_fc变体3的adcc活性。
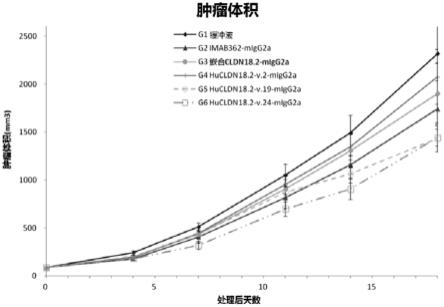
29.图9提供了在小鼠中同基因mc38-hucldn18.2肿瘤异种移植实验的结果,进行这些
实验以评价抗体hucldn18.2-v2、hucldn18.2-v19、hucldn18.2-v24、自制嵌合抗cldn18.2抗体和参考抗体imab362在抑制肿瘤生长中的体内功效。
具体实施方式
30.以下描述阐述了示例性方法,参数等。然而,应当认识到,这样的描述并非旨在作为对本技术的保护范围的限制,而是作为对示例性实施方案的描述来提供。定义
31.在详细描述所公开的实施方案之前,应当理解,本技术不限于特定的组合物或生物系统,其当然可以变化。还应当理解,本技术使用的术语仅出于描述特定实施方案的目的,而并不意图进行限制。
32.如本说明书和所附权利要求中所使用的,单数形式“一”、“一个”和“该”包括复数个对象,除非上下文另外明确指出。因此,例如,提及“一种分子”任选地包括两种或更多种这样的分子的组合,等等。
33.本技术所使用的术语“约”是指本技术领域的技术人员容易知道的各个值的通常误差范围。本文中提及“约”一个值或参数包括(并描述)涉及该值或参数本身的实施方案。
34.应当理解,本技术的各方面和各实施方案包括“包含(comprising)”、“由
…
组成(consisting)”以及“基本上由
…
组成(consistingessentiallyof)”方面和实施方案。
35.术语“claudin18”或“cldn18”优选是指人cldn18并且包括cldn18的任何剪接变体,诸如cldn18.1和cldn18.2。cldn18.1和cldn18.2的不同在于包含第一跨膜(tm)区和环1的n-末端部分,而c-末端的一级蛋白序列是相同的。
36.术语“cldn18.1”优选涉及人cldn18.1,且特别涉及一种蛋白质,所述蛋白质包含氨基酸序列mstttcqvvafllsilglagciaatgmdmwstqdlydnpvtsvfqyeglwrscvrqssgftecrpyftilglpamlqavralmivgivlgaigllvsifalkcirigsmedsakanmtltsgimfivsglcaiagvsvfanmlvtnfwmstanmytgmggmvqtvqtrytfgaalfvgwvaggltliggvmmciacrglapeetnykavsyhasghsvaykpggfkastgfgsntknkkiydggartedevqsypskhdyv(seqidno:106)或所述氨基酸序列的变体
37.术语“cldn18.2”优选涉及人cldn18.2,且特别是涉及一种蛋白质,所述蛋白质包含氨基酸序列mavtacqglgfvvsligiagiiaatcmdqwstqdlynnpvtavfnyqglwrscvressgftecrgyftllglpamlqavralmivgivlgaigllvsifalkcirigsmedsakanmtltsgimfivsglcaiagvsvfanmlvtnfwmstanmytgmggmvqtvqtrytfgaalfvgwvaggltliggvmmciacrglapeetnykavsyhasghsvaykpggfkastgfgsntknkkiydggartedevqsypskhdyv(seqidno:107)或所述氨基酸序列的变体。
38.术语“cldn”、“cldn18”、“cldn18.1”和“cldn18.2”是指任何翻译后修饰的变体和构象变体。
39.如本技术所用,术语“抗体”可以指完整的(全长)抗体;抗体片段(包括但不限于
fab、f(ab')2、fab'-sh、fv、双抗、scfv、scfv-fc、单结构域抗体、单重链抗体和单轻链抗体),只要它们表现出所需的生物学活性(例如表位结合);单克隆抗体;多克隆抗体;单特异性抗体;多特异性抗体(例如双特异性抗体);抗体样蛋白,包括但不限于例如融合蛋白、半胱氨酸工程抗体,共价修饰的抗体和抗体缀合物(诸如抗体-药物缀合物或与可检测标记物缀合的抗体)。
[0040]“分离的”抗体可以指已从其天然环境的组分(例如,宿主细胞或生物体)分离和/或回收的抗体。在一些实施方案中,将抗体纯化至期望的重量纯度(例如,至少95%);和/或通过sds-page使用例如银染色、考马斯(coomassie)染色等进行均质化。在一些实施方案中,在一个或多个纯化步骤后获得分离的抗体。
[0041]
如本领域已知的,“天然”抗体通常指包括两条相同的轻(l)链和两条相同的重(h)链的异源四聚体复合物。可变数目的二硫键连接两条重链,除了链内二硫键外,一个二硫键还将每条轻链连接至重链。重链包括:可变结构域(vh),其后(n端至c端)是三个或四个恒定域。轻链包括可变结构域(vl),其后是恒定结构域(cl)。通常,基于氨基酸序列,哺乳动物轻链分为两类之一:κ和λ。
[0042]“恒定结构域”可以指抗体或片段的更保守部分,例如在可变结构域的外部。该术语可以包括cl结构域以及重链恒定结构域ch1、ch2、ch3和任选的ch4。
[0043]
重链的恒定结构域可指定为5种主要类型之一:iga、igd、ige、igg和igm。这些主要类型中的许多存在若干亚型。不同类别免疫球蛋白的亚型结构和三维构型是熟知的,并且通常描述于例如abbasetal.cellularandmol.immunology,4thed.(w.b.saunders,co.,2000)。
[0044]
如本技术所用,术语“抗体可变结构域”是指抗体的轻链和重链的部分,包括互补决定区(cdrs,例如cdrl1、cdrl2、cdrl3、cdrh1、cdrh2和cdrh3)和框架区(frs)。
[0045]
术语“可变”是指抗体之间的可变结构域的子序列在序列上实质上不同并且对于特定抗体针对其抗原的结合特异性起到关键作用的事实。可变性集中在vh和vl结构域中的三个“高变区”(hvrs)或“互补性决定区”(cdrs)(术语“hvr”和“cdr”在本文中可互换使用)。可变区的更保守的部分称为框架区(“fr”或“fw”),cdrs散布在其中。天然重链和轻链的可变结构域各自包含由形成环的三个cdrs连接的四个fr区(参见kabatetal.,sequencesofproteinsofimmunologicalinterest,fifthedition,nationalinstituteofhealth,bethesda,md.(1991))。
[0046]
术语“高变区(hvr)”或“互补性决定区(cdr)”可以指vh和vl结构域的以增强的序列可变性和/或限定环的形成为特征的子区。这些包括在vh结构域中的三个cdr(h1、h2和h3)和在vl结构域中的三个cdr(l1、l2和l3)。认为h3在赋予良好的结合特异性中是关键的,其中l3和h3显示最高水平的多样性。参见johnson和wu,在分子生物学方法(methodsinmolecularbiology)248:1-25中所述(lo,ed.,humanpress,totowa,n.j.,2003)。
[0047]
许多cdr/hvr描绘是已知的。kabat互补性决定区(cdr)是基于序列可变性的,并且是最常用的(kabatetal.,sequencesofproteinsofimmunologicalinterest,5thed.publichealthservice,nationalinstitutesofhealth,bethesda,md.(1991))。而chothia是指结构环的位置(chothiaandleskj.mol.biol.196:901-917(1987))。“martin”(增强型chothia)方案还考虑了框架区中indel(插入缺失)的结构正确位置。因
antibodies),第113卷,rosenburg和moore编辑,(springer-verlag,newyork,1994),pp.269-315。在一些实施方案中,scfv融合至抗体fc结构域(例如,scfv-fc)。虽然六个hvrs通常包含抗原结合位点,但是具有三个hvrs的单个可变结构域仍然能够结合抗原,尽管亲和力较低。参见hamers-castermanetal.,nature363:446-448(1993);sheriffetal.,naturestruct.biol.3:733-736(1996)。单个结构域抗体(例如,骆驼抗体)通常包括用于抗原结合的单个单体可变结构域。单重链(vhh)和单轻链抗体也是已知的。fab'片段通常在c-末端包括比fab片段多几个残基。fab
’‑
sh包括具有游离巯基的半胱氨酸残基。抗体片段的各种化学偶联是本领域已知的。
[0052]“双抗体”包括具有两个抗原结合位点的抗体片段。这些包括通过接头连接的vh和vl结构域,其通常太短而不能促进相同链中的结构域的配对。双抗可以是二价的或双特异性的。三抗和四抗,或其它数目的vh/vl结构域是已知的。参见hudsonetal.,nat.med.9:129-134(2003)。
[0053]
如本技术所用,“单克隆”抗体是指从基本上均一的抗体群获得的抗体,抗体群例如是基本上相同但允许较低水平的背景突变和/或修饰的抗体群。“单克隆”表示抗体的基本上均一的特性,并且不需要通过任何特定的方法产生抗体。在一些实施方案中,单克隆抗体通过其hvr、vh和/或vl序列和/或结合特性来选择,例如选自克隆(例如,重组体、杂交瘤或噬菌体衍生物)的集合。可以将单克隆抗体工程化以包括一个或多个突变,例如以影响抗体的结合亲和力或其它性质,产生人源化或嵌合抗体,改善抗体产生和/或均一性,设计多特异性抗体,其产生的抗体仍然被认为是天然单克隆的。单克隆抗体群可以与多克隆抗体区分开,因为群的单个单克隆抗体识别相同的抗原位点。生产单克隆抗体的各种技术是已知的;参见,例如,杂交瘤方法(例如,kohlerandmilstein,nature,256:495-97(1975);hongoetal.,hybridoma,14(3):253-260(1995),harlowetal.,antibodies:alaboratorymanual,(coldspringharborlaboratorypress,2nded.1988);hammerling等,在单克隆抗体和t-细胞杂交瘤(monoclonalantibodiesandt-cellhybridomas)563-681(elsevier,n.y.,1981)),重组dna方法(参见,例如美国专利no.4,816,567),噬菌体展示技术(参见,例如clacksonetal.,nature,352:624-628(1991);marksetal.,j.mol.biol.222:581-597(1992);sidhuetal.,j.mol.biol.338(2):299-310(2004);leeetal.,j.mol.biol.340(5):1073-1093(2004);fellouse,proc.natl.acad.sci.usa101(34):12467-12472(2004);以及leeetal.,j.immunol.methods284(1-2):119-132(2004),以及用于在具有编码人免疫球蛋白序列的人免疫球蛋白基因座或基因的部分或全部的动物中产生人或类人抗体的技术(参见,例如,wo1998/24893;wo1996/34096;wo1996/33735;wo1991/10741;jakobovitsetal.,proc.natl.acad.sci.usa90:2551(1993);jakobovitsetal.,nature362:255-258(1993);bruggemannetal.,yearinimmunol.7:33(1993);美国专利no.5,545,807;5,545,806;5,569,825;5,625,126;5,633,425;和5,661,016;marksetal.,bio/technology10:779-783(1992);lonbergetal.,nature368:856-859(1994);morrison,nature368:812-813(1994);fishwildetal.,naturebiotechnol.14:845-851(1996);neuberger,naturebiotechnol.14:826(1996);和lonbergandhuszar,intern.rev.immunol.13:65-93(1995)。
[0054]“嵌合”抗体可以指具有来自特定同种型、类别或有机体的重链和/或轻链的一部分和来自另一同种型、类别或有机体的另一部分的抗体。在一些实施方案中,可变区来自一个来源或有机体,且恒定区来自另一个来源或有机体。
[0055]“人源化抗体”可以指具有主要为人的序列和最少量的非人(例如,小鼠或鸡)序列的抗体。在一些实施方案中,人源化抗体具有来自移植到人受体抗体框架“fr”或“fw”上的非人(例如,鼠或鸡)生物体的抗体的一个或多个hvr序列(具有感兴趣的结合特异性)。在一些实施方案中,将非人残基进一步移植到人框架(不论是源抗体还是受体抗体都不存在)上,例如,以改善抗体性质。通常,人源化抗体将包含至少一个,且通常两个,可变区的基本上全部,其中高变环的全部或基本上全部对应于非人免疫球蛋白的那些序列,并且frs的全部或基本上全部是人免疫球蛋白序列的那些序列。人源化抗体任选地还包含(通常是人免疫球蛋白的) 免疫球蛋白恒定区(fc)的至少一部分。参见jones et al.,nature 321:522-525 (1986);riechmann et al.,nature 332:323-329(1988);和presta, curr.op.struct.biol.2:593-596(1992)。
[0056]“人”抗体可以指具有与人产生的抗体的氨基酸序列相对应的氨基酸序列的抗体和/或使用本技术公开的用于制备人抗体的任何技术制备的抗体。人抗体可以使用本领域已知的各种技术产生,包括噬菌体展示文库。hoogenboom and winter,j.mol.biol.,227:381(1991);marks et al.,j. mol.biol.,222:581(1991);如以下中描述的人单克隆抗体的制备:cole et al., monoclonal antibodies and cancer therapy,alan r.liss,p.77(1985); boerner et al.,j.immunol.,147(1):86-95(1991);和通过将抗原向已被修饰以响应抗原攻击而产生此类抗体但其内源性基因座已被禁用的转基因动物施用,例如免疫的异种移植小鼠(xenomice)(参见例如关于xenomousetm 技术的美国专利no.6,075,181和6,150,584)或具有人免疫球蛋白序列的鸡 (参见例如wo2012162422、wo2011019844和wo2013059159)。
[0057]
本技术所用的术语“细胞毒性剂”可以指抑制细胞增殖或诱导细胞死亡的任何试剂。细胞毒性剂包括但不限于化疗剂;放射性同位素;生长抑制剂;和毒素,如小分子毒素或酶活性毒素,包括其片段和/或变体。示例性细胞毒性剂包括但不限于代谢抑制剂、抗微管剂、含铂化合物、烷化剂、蛋白酶体抑制剂、拓扑异构酶ii抑制剂、抗代谢物、拓扑异构酶i 抑制剂、信号转导通路抑制剂、非受体酪氨酸激酶血管生成抑制剂、激素和激素类似物、促凋亡剂、ldh-a的抑制剂、细胞周期抑制剂、hdac抑制剂和抗生素剂。
[0058]
如本技术所使用,“标记”可包括例如充当本技术的经标记抗体与大分子或细胞之间的结合的检测剂的任何部分。示例性标记包括但不限于荧光(例如,化合物或蛋白质)、放射性或酶部分,以及亲和纯化标签。
[0059]
术语“检测”旨在包括确定物质的存在或不存在,或定量物质(诸如cldn18.2)的量。因此,该术语是指本发明的材料、组合物和方法用于定性和定量测定的用途。通常,用于检测的特定技术对于本发明的实施不是关键的。
[0060]
例如,根据本发明的“检测”可包括:观察cldn18.2多肽的 cldn18.2基因产物的存在或缺失;结合至靶标的cldn18.2多肽的水平或量的变化;cldn18.2多肽的生物学功能/活性的改变。在一些实施方案中,“检测”可包括检测野生型cldn18.2水平(例如,多肽水平)。检测可以包括当与对照相比时定量10%至90%之间的任何值、或30%至60%之间的任何
值、或超过100%的变化(增加或减少)。检测可以包括量化在2倍至 10倍或更多(例如100倍)之间的任何值的变化。
[0061]
如本技术所用,抗体可以说以足以使抗体用于体外和/或体内操纵抗原的亲和力“结合”抗原。
[0062]
如本技术所用,术语“亲和力”或“结合亲和力”是指两个分子之间的结合相互作用的强度。通常,结合亲和力是指分子与其结合配偶体 (如高亲和力sirp-αd1变体和cd47)之间的非共价相互作用的总和的强度。除非另外指明,否则结合亲和力是指固有结合亲和力,其反映结合对的成员之间的1:1相互作用。两种分子间的结合亲和力通常用解离常数(kd) 或缔合常数(ka)来描述。彼此具有低结合亲和力的两个分子通常结合缓慢,易于解离,并且表现出大的kd。彼此具有高亲和力的两个分子通常容易结合,趋于更长久地保持结合,并且表现出小的kd。在一些实施方案中,使用已知的方法和技术测定两种相互作用分子的kd,例如,表面等离子体共振(spr)。kd可以作为koff/kon的比率计算。
[0063]
如本技术所用,术语“小于...的k
d”是指数值上较小的kd值和相对于所列举的kd值增加的结合亲和力。如本技术所用,术语“大于...的k
d”是指数值上较大的kd值和相对于所列举的kd值降低的结合亲和力。
[0064]
如本技术所用,“治疗”可指分子、化合物、制剂、组合物等的治疗性施用,以获得有益的或期望的治疗结果,包括临床结果。出于本发明的目的,有益的或期望的临床结果包括但不限于以下中的一种或多种:减轻由疾病引起的一种或多种症状,减少疾病的程度,稳定疾病(例如,防止或延迟疾病的恶化),防止或延迟疾病的传播(例如,转移),预防或延迟疾病的复发,延迟或减缓疾病的进展,改善疾病状态,提供疾病的缓解(部分或全部),减少治疗疾病所需的一种或多种其它药物的剂量,减轻病理症状或疾病状态,增加或改善生存质量,防止过度体重减轻,改善预后,实现疾病缓解和/或延长存活。“治疗”还包括减少癌症的病理结果(诸如,举例而言肿瘤体积增加)。本技术提供的方法考虑了治疗的这些方面中的任何一个或多个。
[0065]
如本技术所用,疾病的“延迟进展”可以指减缓、延迟、延缓、推迟疾病的发展,稳定或以其他方式阻碍疾病的病理过程。在一些实施方案中,该术语可以指有效地涵盖预防(例如足以在预防个体疾病发展中) 的延迟。在一些实施方案中,例如,对于晚期癌症来说,延迟进展可以包括延迟转移。本领域技术人员将理解,延迟的精确长度可取决于例如具体疾病、个体状况等。
[0066]
术语“再发(recurrence)”或“复发(relapse/relapsed)”是指以经临床评价疾病消失后以异常的cldn18.2表达或异常的cldn18.2活性为特征的疾病或病症的复发(例如,癌症,诸如胃癌、食管癌、胃食管交界癌、胰腺癌、胆管癌、肺癌、卵巢癌、结肠癌、肝癌、头颈癌、胆囊癌等)。
[0067]
术语“难治的(refractory)”或“抗性的(resistant)”是指尚未对使用特定药剂或药剂组合的治疗作出应答、以异常的cldn18.2表达或异常的cldn18.2活性为特征的疾病或病症(例如,癌症,诸如胃癌、食管癌、胃食管交界癌、胰腺癌、胆管癌、肺癌、卵巢癌、结肠癌、肝癌、头颈癌、胆囊癌等)。
[0068]
如本技术所用,术语“有效量”可以指本技术的抗体或含有本技术的抗体的药物组合物足以且有效地实现治疗或延迟患有疾病的患者的进展的期望治疗效果的量,疾病诸如
为表达cldn18.2的肿瘤或以异常 cldn18.2表达或活性为特征的癌症,例如胃癌、食管癌、胃食管交界癌、胰腺癌、胆管癌、肺癌、卵巢癌、结肠癌、肝癌、头颈癌、胆囊癌等。在一些实施方案中,治疗有效量将避免不良副作用,和/或这种副作用将被有益效果抵消。有效量可取决于所治疗的个体(例如,年龄、体重、性别、疾病状态)以及药剂产生所需应答的能力。可以一次或多次施用来施用有效量。如在临床环境中,药物、化合物或药物组合物的有效量可以或可以不与另一种药物、化合物或药物组合物(例如另一种治疗剂)联合实现。因此,“有效量”也可以在施用一种或多种另外的治疗剂的环境中考虑,并且如果单一药剂与一种或多种其它药剂联合可以得到或实现期望的结果,则可以认为以有效量施用。
[0069]
术语“治疗有效量”是指如本技术所公开的人源化抗cldn18.2 抗体(或其片段)或组合物有效“治疗”哺乳动物(例如患者或受试者) 中的疾病或病症的量。在癌症的情况下,治疗有效量的本技术公开的人源化抗cldn18.2抗体(或其片段)或组合物可以减少癌细胞的数量;减小肿瘤大小或重量;抑制(即,在一定程度上减慢并且优选地停止)癌细胞浸润到周围器官中;抑制(即,在一定程度上减慢并且优选地停止)肿瘤转移;在一定程度上抑制肿瘤生长;和/或在一定程度上减轻与癌症相关的一种或多种症状。就如本技术所公开的人源化抗cldn18.2抗体(或其片段)或组合物可以防止现存癌细胞生长和/或杀死现存癌细胞而言,其可以是细胞抑制性的和/或细胞毒性的。在一个实施方案中,治疗有效量是生长抑制量。在另一个实施方案中,治疗有效量是延长患者存活的量。在另一个实施方案中,治疗有效量是改善患者的无进展存活的量。
[0070]
如本技术所用,术语“药物组合物”可以指包括活性成分以及赋形剂或稀释剂(或赋形剂和稀释剂两者)并且使得活性成分能够通过合适的施用方法施用的药用或药物制剂。在一些实施方案中,本技术公开的药物组合物包括与本技术的一种或多种抗体相容的药学上可接受的组分。在一些实施方案中,药物组合物是用于口服施用的片剂或胶囊形式或用于静脉内或皮下施用(例如通过注射)的水性形式。
[0071]
如本技术所用,“药学上可接受的”或“药理学上相容的”是指不是生物学上或其它方面不期望的材料,例如,所述材料可并入向患者施用的药物组合物中,而不引起任何显著不期望的生物效应或以有害方式与含有所述材料的组合物的任何其它组分的相互作用。药学上可接受的载体或赋形剂优选满足毒理学和制造测试的所需标准和/或包括在美国食品和药物管理局编写的《非活性成分指南(inactive ingredient guide)》中。
[0072]
如本技术所用,术语“受试者”、“个体”和“患者”可互换使用,是指脊椎动物,例如哺乳动物。哺乳动物包括但不限于鼠、猿、人、农场动物、运动动物和宠物。
[0073]
关于本技术鉴定的多肽和抗体序列的“氨基酸序列同一性百分比 (%)”或“同源性”定义为在将考虑任何保守取代作为序列同一性的一部分的序列比对后,候选序列中与被比较多肽中的氨基酸残基相同的氨基酸残基的百分比。用于确定氨基酸序列同一性百分比的比对可通过本领域技术人员已知的各种方法实现,例如,使用公众可获得的计算机软件,诸如 blast、blast-2、align或megalign(dnastar)软件。本领域技术人员可以确定用于测量比对的适当参数,包括在所比较的全长序列上实现最大比对所需的任何算法。然而,出于本技术的目的,使用序列比较计算机程序align-2产生%氨基酸序列同一性值。align-2序列比较计算机程序由genentech公司编写,其源代码已在20559华盛顿特区的美国版权局中与用户文档一起提交,以美国版权注册号no.txu510087登记。align-2 程序可通过加利
福尼亚州南旧金山genentech公司公开获得。应编译 align-2程序以在unix操作系统上使用,优选在数字unix v4.0d上使用。所有序列比较参数均由align-2程序设定且不更改。
[0074]
本文引用的所有参考文献,包括专利申请和出版物,均通过引用整体并入本文。人源化抗claudin 18.2(cldn18.2)抗体
[0075]
本技术基于结合claudin 18.2(cldn18.2)的人源化抗体的鉴定。本技术提供的人源化抗cldn18.2抗体可用于多种治疗和诊断方法。例如,人源化抗cldn18.2抗体可单独使用或与其它药剂组合使用以治疗以异常 cldn18.2表达或异常cldn18.2活性为特征的疾病或病症,包括但不限于实体瘤或癌症,例如,胃癌、食管癌、胃食管交界癌、胰腺癌、胆管癌、肺癌、卵巢癌、结肠癌、肝癌、头颈癌、胆囊癌等。本技术所提供的人源化抗体可以用来检测患者(如人类患者)或患者样品中的cldn18.2,例如通过向患者施用人源化抗cldn18.2抗体并检测与cldn18.2结合的人源化抗cldn18.2抗体(例如,体内或离体),或者,例如通过使来自患者的样品与人源化抗cldn18.2抗体接触,并定性或定量地检测与cldn18.2 蛋白结合的人源化抗cldn18.2抗体。
[0076]
人源化抗cldn18.2抗体是以足够的亲和力和特异性结合 cldn18.2的抗体。例如,本技术提供的人源化抗cldn18.2抗体(或其生物活性片段)可用作靶向和干扰与畸变/异常cldn18.2表达和/或活性相关的疾病或病症的治疗剂。在一些实施方案中,人源化抗cldn18.2抗体是单克隆抗体。在一些实施方案中,所述人源化抗cldn18.2抗体包含本技术公开的抗体的至少一个cdr、重链可变结构域(vh)和/或轻链可变结构域(vl)。
[0077]
在一些实施方案中,本技术提供的抗cldn18.2抗体(诸如人源化抗体)(或其抗原结合片段)包含cdr-h2,所述cdr-h2包含iiiggiyt (seq id no:6)。
[0078]
在一些实施方案中,抗cldn18.2抗体(诸如人源化抗体)或其抗原结合片段进一步包含:(a)cdr-l1,其包含seq id no:1和85-93 中的任一个;(b)cdr-l2,其包含seq id no:2或94;(c)cdr-l3,其包含seq id no:3和95-105中的任一个;(d)cdr-h1,其包含seq idno:4和66-74的任一个;和(e)cdr-h3,其包含seq id no:7、75-84 和108中的任一个。
[0079]
在一些实施方案中,抗cldn18.2抗体(诸如人源化抗体)或其抗原结合片段包含(a)cdr-l1,其包含qsllnsgnqkny(seq id no: 1);(b)cdr-l2,其包含was(seq id no:2);(c)cdr-l3,其包含 qnnyiypft(seq id no:3);(d)cdr-h1,其包含gftfsnya(seqid no:4);(e)cdr-h2,其包含iiiggtyt(seq id no:5)或iiiggiyt (seq id no:6);和(e)cdr-h3,其包含arqvygnsfay(seq id no: 7)。在一些实施方案中,抗cldn18.2抗体(诸如人源化抗体)或其抗原结合片段包含(a)cdr-l1,其包含qsllnsgnqkny(seq id no:1); (b)cdr-l2,其包含was(seq id no:2);(c)cdr-l3,其包含 qnnyiypft(seq id no:3);(d)cdr-h1,其包含gftfsnya(seqid no:4);(e)cdr-h2,其包含iiiggtyt(seq id no:5);和(e) cdr-h3,其包含arqvygnsfay(seq id no:7)。在一些实施方案中,抗cldn18.2抗体(诸如人源化抗体)或其抗原结合片段包含(a)cdr-l1,其包含qsllnsgnqkny(seq id no:1);(b)cdr-l2,其包含was (seq id no:2);(c)cdr-l3,其包含qnnyiypft(seq id no:3); (d)cdr-h1,其包含gftfsnya(seq id no:4);(e)cdr-h2,其 iiiggiyt(seq id no:6);和(e)cdr-h3,其包含arqvygnsfay (seq id no:7)。在一些实施方案中,cdrs根据imgt cdr编号方案定义,如在 www(dot)imgt(dot)org/imgtscientificchart/nomenclature/imgt-frcdrdefinition(dot)html中所描述。seq id no:1-7的氨基酸序列提供于下表1中。
表1.
[0080]
在一些实施方案中,抗cldn18.2抗体(诸如人源化抗体)或其抗原结合片段包含:轻链可变结构域(vl),所述轻链可变结构域(vl) 包含(诸如由其组成):在seq id no:55-58中的任一个的氨基酸序列;和/或重链可变结构域(vh),所述重链可变结构域(vh)包含seq id no: 59-65中的任一个的氨基酸序列。seq id no:55-65的氨基酸序列提供于下表2中:表2.
[0081]
在一些实施方案中,抗cldn18.2抗体(诸如人源化抗体)或其抗原结合片段包含:轻链可变结构域(vl)的一个、两个或三个cdr,所述轻链可变结构域(vl)包含(诸如由其组成):在seq id no:55-58中的任一个的氨基酸序列;或重链可变结构域(vh)的一个、两个或三个 cdr,所述重链可变结构域(vh)包含seq id no:59-65中的任一个的氨基酸序列。在一些实施方案中,抗cldn18.2抗体(诸如人源化抗体) 或其抗原结合片段包含:轻链可变结构域(vl)的一个、两个或三个cdr,所述轻链可变结构域(vl)包含(诸如由其组成):在seq id no:55-58 中的任一个的氨基酸序列;和重链可变结构域(vh)的一个、两个或三个 cdr,所述重链可变结构域(vh)包含seq id no:59-65中的任一个的氨基酸序列。
[0082]
在一些实施方案中,抗cldn18.2抗体(诸如人源化抗体)或其抗原结合片段包含:vl结构域,其包含(诸如由以下组成)seq id no: 55的氨基酸序列;和/或vh结构域,其包含(诸如由以下组成)seq id no:59的氨基酸序列。在一些实施方案中,抗cldn18.2抗体(诸如人源化抗体)或其抗原结合片段包含:vl结构域的3个cdr,所述vl结构域包含 seq id no:55;和/或vh结构域的3个cdr,所述vh结构域包含seqid no:59。在一些实施方案中,cdr根据imgt编号方案、chothia编号方案、kabat编号方案、martin(增强型chothia)编号方案、abm编号方案或aho编号方案定义。在一些实施方案中,抗cldn18.2抗体(或其抗原结合片段)包含:vl结构域,其包含(诸如由以下组成)seq id no: 55;和vh结构域,其包含(诸如由以下组成)seq id no:59。
[0083]
在一些实施方案中,抗cldn18.2抗体(诸如人源化抗体)或其抗原结合片段包含:vl结构域,其包含(诸如由以下组成)seq id no: 55的氨基酸序列;和/或vh结构域,其包含(诸如由以下组成)seq id no: 60的氨基酸序列。在一些实施方案中,抗cldn18.2抗体(诸
如人源化抗体)或其抗原结合片段包含:vl结构域的3个cdr,所述vl结构域包含 seq id no:55;和/或vh结构域的3个cdr,所述vh结构域包含seqid no:60。在一些实施方案中,cdr根据imgt编号方案、chothia编号方案、kabat编号方案、martin(增强型chothia)编号方案、abm编号方案或aho编号方案定义。在一些实施方案中,抗cldn18.2抗体(或其抗原结合片段)包含:vl结构域,其包含(诸如由以下组成)seq id no: 55;和vh结构域,其包含(诸如由以下组成)seq id no:60。
[0084]
在一些实施方案中,抗cldn18.2抗体(诸如人源化抗体)或其抗原结合片段包含:vl结构域,其包含(诸如由以下组成)seq id no: 55的氨基酸序列;和/或vh结构域,其包含(诸如由以下组成)seq id no: 61的氨基酸序列。在一些实施方案中,抗cldn18.2抗体(诸如人源化抗体)或其抗原结合片段包含:vl结构域的3个cdr,所述vl结构域包含 seq id no:55;和/或vh结构域的3个cdr,所述vh结构域包含seqid no:61。在一些实施方案中,cdr根据imgt编号方案、chothia编号方案、kabat编号方案、martin(增强型chothia)编号方案、abm编号方案或aho编号方案定义。在一些实施方案中,抗cldn18.2抗体(或其抗原结合片段)包含:vl结构域,其包含(诸如由以下组成)seq id no: 55;和vh结构域,其包含(诸如由以下组成)seq id no:61。
[0085]
在一些实施方案中,抗cldn18.2抗体(诸如人源化抗体)或其抗原结合片段包含:vl结构域,其包含(诸如由以下组成)seq id no: 55的氨基酸序列;和/或vh结构域,其包含(诸如由以下组成)seq id no: 62的氨基酸序列。在一些实施方案中,抗cldn18.2抗体(诸如人源化抗体)或其抗原结合片段包含:vl结构域的3个cdr,所述vl结构域包含 seq id no:55;和/或vh结构域的3个cdr,所述vh结构域包含seqid no:62。在一些实施方案中,cdr根据imgt编号方案、chothia编号方案、kabat编号方案、martin(增强型chothia)编号方案、abm编号方案或aho编号方案定义。在一些实施方案中,抗cldn18.2抗体(或其抗原结合片段)包含:vl结构域,其包含(诸如由以下组成)seq id no: 55;和vh结构域,其包含(诸如由以下组成)seq id no:62。
[0086]
在一些实施方案中,抗cldn18.2抗体(诸如人源化抗体)或其抗原结合片段包含:vl结构域,其包含(诸如由以下组成)seq id no: 55的氨基酸序列;和/或vh结构域,其包含(诸如由以下组成)seq id no: 63的氨基酸序列。在一些实施方案中,抗cldn18.2抗体(诸如人源化抗体)或其抗原结合片段包含:vl结构域的3个cdr,所述vl结构域包含 seq id no:55;和/或vh结构域的3个cdr,所述vh结构域包含seqid no:63。在一些实施方案中,cdr根据imgt编号方案、chothia编号方案、kabat编号方案、martin(增强型chothia)编号方案、abm编号方案或aho编号方案定义。在一些实施方案中,抗cldn18.2抗体(或其抗原结合片段)包含:vl结构域,其包含(诸如由以下组成)seq id no: 55;和vh结构域,其包含(诸如由以下组成)seq id no:63。
[0087]
在一些实施方案中,抗cldn18.2抗体(诸如人源化抗体)或其抗原结合片段包含:vl结构域,其包含(诸如由以下组成)seq id no:56的氨基酸序列;和/或vh结构域,其包含(诸如由以下组成)seq id no: 59的氨基酸序列。在一些实施方案中,抗cldn18.2抗体(诸如人源化抗体)或其抗原结合片段包含:vl结构域的3个cdr,所述vl结构域包含 seq id no:56;和/或vh结构域的3个cdr,所述vh结构域包含seqid no:59。在一些实施方案中,cdr根据imgt编号方案、chothia编号方案、kabat编号方案、martin(增强型chothia)编号方案、
abm编号方案或aho编号方案定义。在一些实施方案中,抗cldn18.2抗体(或其抗原结合片段)包含:vl结构域,其包含(诸如由以下组成)seqidno:56;和vh结构域,其包含(诸如由以下组成)seqidno:59。
[0088]
在一些实施方案中,抗cldn18.2抗体(诸如人源化抗体)或其抗原结合片段包含:vl(结构域),其包含(诸如由以下组成)seqidno:56的氨基酸序列;和/或vh结构域,其包含(诸如由以下组成)seqidno:60的氨基酸序列。在一些实施方案中,抗cldn18.2抗体(诸如人源化抗体)或其抗原结合片段包含:vl结构域的3个cdr,所述vl结构域包含seqidno:56;和/或vh结构域的3个cdr,所述vh结构域包含seqidno:60。在一些实施方案中,cdr根据imgt编号方案、chothia编号方案、kabat编号方案、martin(增强型chothia)编号方案、abm编号方案或aho编号方案定义。在一些实施方案中,抗cldn18.2抗体(或其抗原结合片段)包含:vl结构域,其包含(诸如由以下组成)seqidno:56;和vh结构域,其包含(诸如由以下组成)seqidno:60。
[0089]
在一些实施方案中,抗cldn18.2抗体(诸如人源化抗体)或其抗原结合片段包含:vl结构域,其包含(诸如由以下组成)seqidno:56的氨基酸序列;和/或vh结构域,其包含(诸如由以下组成)seqidno:61的氨基酸序列。在一些实施方案中,抗cldn18.2抗体(诸如人源化抗体)或其抗原结合片段包含:vl结构域的3个cdr,所述vl结构域包含seqidno:56;和/或vh结构域的3个cdr,所述vh结构域包含seqidno:61。在一些实施方案中,cdr根据imgt编号方案、chothia编号方案、kabat编号方案、martin(增强型chothia)编号方案、abm编号方案或aho编号方案定义。在一些实施方案中,抗cldn18.2抗体(或其抗原结合片段)包含:vl结构域,其包含(诸如由以下组成)seqidno:56;和vh结构域,其包含(诸如由以下组成)seqidno:61。
[0090]
在一些实施方案中,抗cldn18.2抗体(诸如人源化抗体)或其抗原结合片段包含:vl结构域,其包含(诸如由以下组成)seqidno:56的氨基酸序列;和/或vh结构域,其包含(诸如由以下组成)seqidno:62的氨基酸序列。在一些实施方案中,抗cldn18.2抗体(诸如人源化抗体)或其抗原结合片段包含:vl结构域的3个cdr,所述vl结构域包含seqidno:56;和/或vh结构域的3个cdr,所述vh结构域包含seqidno:62。在一些实施方案中,cdr根据imgt编号方案、chothia编号方案、kabat编号方案、martin(增强型chothia)编号方案、abm编号方案或aho编号方案定义。在一些实施方案中,抗cldn18.2抗体(或其抗原结合片段)包含:vl结构域,其包含(诸如由以下组成)seqidno:56;和vh结构域,其包含(诸如由以下组成)seqidno:62。
[0091]
在一些实施方案中,抗cldn18.2抗体(诸如人源化抗体)或其抗原结合片段包含:vl结构域,其包含(诸如由以下组成)seqidno:56的氨基酸序列;和/或vh结构域,其包含(诸如由以下组成)seqidno:63的氨基酸序列。在一些实施方案中,抗cldn18.2抗体(诸如人源化抗体)或其抗原结合片段包含:vl结构域的3个cdr,所述vl结构域包含seqidno:56;和/或vh结构域的3个cdr,所述vh结构域包含seqidno:63。在一些实施方案中,cdr根据imgt编号方案、chothia编号方案、kabat编号方案、martin(增强型chothia)编号方案、abm编号方案或aho编号方案定义。在一些实施方案中,抗cldn18.2抗体(或其抗原结合片段)包含:vl结构域,其包含(诸如由以下组成)seqidno:56;和vh结构域,其包含(诸如由以下组成)seqidno:63。
[0092]
在一些实施方案中,抗cldn18.2抗体(诸如人源化抗体)或其抗原结合片段包含:vl结构域,其包含(诸如由以下组成)seq id no: 57的氨基酸序列;和/或vh结构域,其包含(诸如由以下组成)seq id no: 59的氨基酸序列。在一些实施方案中,抗cldn18.2抗体(诸如人源化抗体)或其抗原结合片段包含:vl结构域的3个cdr,所述vl结构域包含 seq id no:57;和/或vh结构域的3个cdr,所述vh结构域包含seqid no:59。在一些实施方案中,cdr根据imgt编号方案、chothia编号方案、kabat编号方案、martin(增强型chothia)编号方案、abm编号方案或aho编号方案定义。在一些实施方案中,抗cldn18.2抗体(或其抗原结合片段)包含:vl结构域,其包含(诸如由以下组成)seq id no: 57;和vh结构域,其包含(诸如由以下组成)seq id no:59。
[0093]
在一些实施方案中,抗cldn18.2抗体(诸如人源化抗体)或其抗原结合片段包含:vl结构域,其包含(诸如由以下组成)seq id no: 57的氨基酸序列;和/或vh结构域,其包含(诸如由以下组成)seq id no: 60的氨基酸序列。在一些实施方案中,抗cldn18.2抗体(诸如人源化抗体)或其抗原结合片段包含:vl结构域的3个cdr,所述vl结构域包含 seq id no:57;和/或vh结构域的3个cdr,所述vh结构域包含seqid no:60。在一些实施方案中,cdr根据imgt编号方案、chothia编号方案、kabat编号方案、martin(增强型chothia)编号方案、abm编号方案或aho编号方案定义。在一些实施方案中,抗cldn18.2抗体(或其抗原结合片段)包含:vl结构域,其包含(诸如由以下组成)seq id no: 57;和vh结构域,其包含(诸如由以下组成)seq id no:60。
[0094]
在一些实施方案中,抗cldn18.2抗体(诸如人源化抗体)或其抗原结合片段包含:vl结构域,其包含(诸如由以下组成)seq id no: 57的氨基酸序列;和/或vh结构域,其包含(诸如由以下组成)seq id no: 61的氨基酸序列。在一些实施方案中,抗cldn18.2抗体(诸如人源化抗体)或其抗原结合片段包含:vl结构域的3个cdr,所述vl结构域包含seq id no:57;和/或vh结构域的3个cdr,所述vh结构域包含seqid no:61。在一些实施方案中,cdr根据imgt编号方案、chothia编号方案、kabat编号方案、martin(增强型chothia)编号方案、abm编号方案或aho编号方案定义。在一些实施方案中,抗cldn18.2抗体(或其抗原结合片段)包含:vl结构域,其包含(诸如由以下组成)seq id no: 57;和vh结构域,其包含(诸如由以下组成)seq id no:61。
[0095]
在一些实施方案中,抗cldn18.2抗体(诸如人源化抗体)或其抗原结合片段包含:vl结构域,其包含(诸如由以下组成)seq id no: 57的氨基酸序列;和/或vh结构域,其包含(诸如由以下组成)seq id no: 62的氨基酸序列。在一些实施方案中,抗cldn18.2抗体(诸如人源化抗体)或其抗原结合片段包含:vl结构域的3个cdr,所述vl结构域包含 seq id no:57;和/或vh结构域的3个cdr,所述vh结构域包含seqid no:62。在一些实施方案中,cdr根据imgt编号方案、chothia编号方案、kabat编号方案、martin(增强型chothia)编号方案、abm编号方案或aho编号方案定义。在一些实施方案中,抗cldn18.2抗体(或其抗原结合片段)包含:vl结构域,其包含(诸如由以下组成)seq id no: 57;和vh结构域,其包含(诸如由以下组成)seq id no:62。
[0096]
在一些实施方案中,抗cldn18.2抗体(诸如人源化抗体)或其抗原结合片段包含:vl结构域,其包含(诸如由以下组成)seq id no: 57的氨基酸序列;和/或vh结构域,其包含(诸如由以下组成)seq id no: 63的氨基酸序列。在一些实施方案中,抗cldn18.2抗体(诸
如人源化抗体)或其抗原结合片段包含:vl结构域的3个cdr,所述vl结构域包含 seq id no:57;和/或vh结构域的3个cdr,所述vh结构域包含seqid no:63。在一些实施方案中,cdr根据imgt编号方案、chothia编号方案、kabat编号方案、martin(增强型chothia)编号方案、abm编号方案或aho编号方案定义。在一些实施方案中,抗cldn18.2抗体(或其抗原结合片段)包含:vl结构域,其包含(诸如由以下组成)seq id no: 57;和vh结构域,其包含(诸如由以下组成)seq id no:63。
[0097]
在一些实施方案中,抗cldn18.2抗体(诸如人源化抗体)或其抗原结合片段包含:vl(结构域),其包含(诸如由以下组成)seq id no: 58的氨基酸序列;和/或vh结构域,其包含(诸如由以下组成)seq id no: 59的氨基酸序列。在一些实施方案中,抗cldn18.2抗体(诸如人源化抗体)或其抗原结合片段包含:vl结构域的3个cdr,所述vl结构域包含 seq id no:58;和/或vh结构域的3个cdr,所述vh结构域包含seqid no:59。在一些实施方案中,cdr根据imgt编号方案、chothia编号方案、kabat编号方案、martin(增强型chothia)编号方案、abm编号方案或aho编号方案定义。在一些实施方案中,抗cldn18.2抗体(或其抗原结合片段)包含:vl结构域,其包含(诸如由以下组成)seq id no: 58;和vh结构域,其包含(诸如由以下组成)seq id no:59。
[0098]
在一些实施方案中,抗cldn18.2抗体(诸如人源化抗体)或其抗原结合片段包含:vl结构域,其包含(诸如由以下组成)seq id no: 58的氨基酸序列;和/或vh结构域,其包含(诸如由以下组成)seq id no: 60的氨基酸序列。在一些实施方案中,抗cldn18.2抗体(诸如人源化抗体)或其抗原结合片段包含:vl结构域的3个cdr,所述vl结构域包含 seq id no:58;和/或vh结构域的3个cdr,所述vh结构域包含seqid no:60。在一些实施方案中,cdr根据imgt编号方案、chothia编号方案、kabat编号方案、martin(增强型chothia)编号方案、abm编号方案或aho编号方案定义。在一些实施方案中,抗cldn18.2抗体(或其抗原结合片段)包含:vl结构域,其包含(诸如由以下组成)seq id no: 58;和vh结构域,其包含(诸如由以下组成)seq id no:60。
[0099]
在一些实施方案中,抗cldn18.2抗体(诸如人源化抗体)或其抗原结合片段包含:vl结构域,其包含(诸如由以下组成)seq id no: 58的氨基酸序列;和/或vh结构域,其包含(诸如由以下组成)seq id no:61的氨基酸序列。在一些实施方案中,抗cldn18.2抗体(诸如人源化抗体)或其抗原结合片段包含:vl结构域的3个cdr,所述vl结构域包含 seq id no:58;和/或vh结构域的3个cdr,所述vh结构域包含seqid no:61。在一些实施方案中,cdr根据imgt编号方案、chothia编号方案、kabat编号方案、martin(增强型chothia)编号方案、abm编号方案或aho编号方案定义。在一些实施方案中,抗cldn18.2抗体(或其抗原结合片段)包含:vl结构域,其包含(诸如由以下组成)seq id no: 58;和vh结构域,其包含(诸如由以下组成)seq id no:61。
[0100]
在一些实施方案中,抗cldn18.2抗体(诸如人源化抗体)或其抗原结合片段包含:vl结构域,其包含(诸如由以下组成)seq id no: 58的氨基酸序列;和/或vh结构域,其包含(诸如由以下组成)seq id no: 62的氨基酸序列。在一些实施方案中,抗cldn18.2抗体(诸如人源化抗体)或其抗原结合片段包含:vl结构域的3个cdr,所述vl结构域包含 seq id no:58;和/或vh结构域的3个cdr,所述vh结构域包含seqid no:62。在一些实施方案中,cdr根据imgt编号方案、chothia编号方案、kabat编号方案、martin(增强型chothia)编号方案、
abm编号方案或aho编号方案定义。在一些实施方案中,抗cldn18.2抗体(或其抗原结合片段)包含:vl结构域,其包含(诸如由以下组成)seq id no: 58;和vh结构域,其包含(诸如由以下组成)seq id no:62。
[0101]
在一些实施方案中,抗cldn18.2抗体(诸如人源化抗体)或其抗原结合片段包含:vl结构域,其包含(诸如由以下组成)seq id no:58的氨基酸序列;和/或vh结构域,其包含(诸如由以下组成)seq id no: 63的氨基酸序列。在一些实施方案中,抗cldn18.2抗体(诸如人源化抗体)或其抗原结合片段包含:vl结构域的3个cdr,所述vl结构域包含 seq id no:58;和/或vh结构域的3个cdr,所述vh结构域包含seqid no:63。在一些实施方案中,cdr根据imgt编号方案、chothia编号方案、kabat编号方案、martin(增强型chothia)编号方案、abm编号方案或aho编号方案定义。在一些实施方案中,抗cldn18.2抗体(或其抗原结合片段)包含:vl结构域,其包含(诸如由以下组成)seq id no: 58;和vh结构域,其包含(诸如由以下组成)seq id no:63。
[0102]
在一些实施方案中,抗cldn18.2抗体(诸如人源化抗体)或其抗原结合片段包含:vl结构域,其包含(诸如由以下组成)seq id no: 55的氨基酸序列;和/或vh(结构域),其包含(诸如由以下组成)seq id no: 59的氨基酸序列。在一些实施方案中,抗cldn18.2抗体(诸如人源化抗体)或其抗原结合片段包含:vl结构域的3个cdr,所述vl结构域包含 seq id no:55;和/或vh结构域的3个cdr,所述vh结构域包含seqid no:59。在一些实施方案中,cdr根据imgt编号方案、chothia编号方案、kabat编号方案、martin(增强型chothia)编号方案、abm编号方案或aho编号方案定义。在一些实施方案中,抗cldn18.2抗体(或其抗原结合片段)包含:vl结构域,其包含(诸如由以下组成)seq id no: 55;和vh结构域,其包含(诸如由以下组成)seq id no:64。
[0103]
在一些实施方案中,抗cldn18.2抗体(诸如人源化抗体)或其抗原结合片段包含:vl结构域,其包含(诸如由以下组成)seq id no: 56的氨基酸序列;和/或vh结构域,其包含(诸如由以下组成)seq id no: 60的氨基酸序列。在一些实施方案中,抗cldn18.2抗体(诸如人源化抗体)或其抗原结合片段包含:vl结构域的3个cdr,所述vl结构域包含 seq id no:56;和/或vh结构域的3个cdr,所述vh结构域包含seqid no:60。在一些实施方案中,cdr根据imgt编号方案、chothia编号方案、kabat编号方案、martin(增强型chothia)编号方案、abm编号方案或aho编号方案定义。在一些实施方案中,抗cldn18.2抗体(或其抗原结合片段)包含:vl结构域,其包含(诸如由以下组成)seq id no: 56;和vh结构域,其包含(诸如由以下组成)seq id no:64。
[0104]
在一些实施方案中,抗cldn18.2抗体(诸如人源化抗体)或其抗原结合片段包含:vl结构域,其包含(诸如由以下组成)seq id no:57的氨基酸序列;和/或vh结构域,其包含(诸如由以下组成)seq id no: 61的氨基酸序列。在一些实施方案中,抗cldn18.2抗体(诸如人源化抗体)或其抗原结合片段包含:vl结构域的3个cdr,所述vl结构域包含 seq id no:57;和/或vh结构域的3个cdr,所述vh结构域包含seqid no:61。在一些实施方案中,cdr根据imgt编号方案、chothia编号方案、kabat编号方案、martin(增强型chothia)编号方案、abm编号方案或aho编号方案定义。在一些实施方案中,抗cldn18.2抗体(或其抗原结合片段)包含:vl结构域,其包含(诸如由以下组成)seq id no: 57;和vh结构域,其包含(诸如由以下组成)seq id no:64。
[0105]
在一些实施方案中,抗cldn18.2抗体(诸如人源化抗体)或其抗原结合片段包含:vl结构域,其包含(诸如由以下组成)seqidno:58的氨基酸序列;和/或vh结构域,其包含(诸如由以下组成)seqidno:62的氨基酸序列。在一些实施方案中,抗cldn18.2抗体(诸如人源化抗体)或其抗原结合片段包含:vl结构域的3个cdr,所述vl结构域包含seqidno:58;和/或vh结构域的3个cdr,所述vh结构域包含seqidno:62。在一些实施方案中,cdr根据imgt编号方案、chothia编号方案、kabat编号方案、martin(增强型chothia)编号方案、abm编号方案或aho编号方案定义。在一些实施方案中,抗cldn18.2抗体(或其抗原结合片段)包含:vl结构域,其包含(诸如由以下组成)seqidno:58;和vh结构域,其包含(诸如由以下组成)seqidno:64。
[0106]
在一些实施方案中,抗cldn18.2抗体(诸如人源化抗体)或其抗原结合片段包含:vl结构域,其包含(诸如由以下组成)seqidno:55的氨基酸序列;和/或vh结构域,其包含(诸如由以下组成)seqidno:59的氨基酸序列。在一些实施方案中,抗cldn18.2抗体(诸如人源化抗体)或其抗原结合片段包含:vl结构域的3个cdr,所述vl结构域包含seqidno:55;和/或vh结构域的3个cdr,所述vh结构域包含seqidno:59。在一些实施方案中,cdr根据imgt编号方案、chothia编号方案、kabat编号方案、martin(增强型chothia)编号方案、abm编号方案或aho编号方案定义。在一些实施方案中,抗cldn18.2抗体(或其抗原结合片段)包含:vl结构域,其包含(诸如由以下组成)seqidno:55;和vh结构域,其包含(诸如由以下组成)seqidno:65。
[0107]
在一些实施方案中,抗cldn18.2抗体(诸如人源化抗体)或其抗原结合片段包含:vl结构域,其包含(诸如由以下组成)seqidno:56的氨基酸序列;和/或vh结构域,其包含(诸如由以下组成)seqidno:60的氨基酸序列。在一些实施方案中,抗cldn18.2抗体(诸如人源化抗体)或其抗原结合片段包含:vl结构域的3个cdr,所述vl结构域包含seqidno:56;和/或vh结构域的3个cdr,所述vh结构域包含seqidno:60。在一些实施方案中,cdr根据imgt编号方案、chothia编号方案、kabat编号方案、martin(增强型chothia)编号方案、abm编号方案或aho编号方案定义。在一些实施方案中,抗cldn18.2抗体(或其抗原结合片段)包含:vl结构域,其包含(诸如由以下组成)seqidno:56;和vh结构域,其包含(诸如由以下组成)seqidno:65。
[0108]
在一些实施方案中,抗cldn18.2抗体(诸如人源化抗体)或其抗原结合片段包含:vl结构域,其包含(诸如由以下组成)seqidno:57的氨基酸序列;和/或vh结构域,其包含(诸如由以下组成)seqidno:61的氨基酸序列。在一些实施方案中,抗cldn18.2抗体(诸如人源化抗体)或其抗原结合片段包含:vl结构域的3个cdr,所述vl结构域包含seqidno:57;和/或vh结构域的3个cdr,所述vh结构域包含seqidno:61。在一些实施方案中,cdr根据imgt编号方案、chothia编号方案、kabat编号方案、martin(增强型chothia)编号方案、abm编号方案或aho编号方案定义。在一些实施方案中,抗cldn18.2抗体(或其抗原结合片段)包含:vl结构域,其包含(诸如由以下组成)seqidno:57;和vh结构域,其包含(诸如由以下组成)seqidno:65。
[0109]
在一些实施方案中,抗cldn18.2抗体(诸如人源化抗体)或其抗原结合片段包含:vl结构域,其包含(诸如由以下组成)seqidno:58的氨基酸序列;和/或vh结构域,其包含(诸如由以下组成)seqidno:62的氨基酸序列。在一些实施方案中,抗cldn18.2抗体(诸
如人源化抗体)或其抗原结合片段包含:vl结构域的3个cdr,所述vl结构域包含 seq id no:58;和/或vh结构域的3个cdr,所述vh结构域包含seqid no:62。在一些实施方案中,cdr根据imgt编号方案、chothia编号方案、kabat编号方案、martin(增强型chothia)编号方案、abm编号方案或aho编号方案定义。在一些实施方案中,抗cldn18.2抗体(或其抗原结合片段)包含:vl结构域,其包含(诸如由以下组成)seq id no: 58;和vh结构域,其包含(诸如由以下组成)seq id no:65。
[0110]
在一些实施方案中,本技术提供抗cldn18.2抗体(诸如人源化抗体)或其抗原结合片段,其包含轻链可变结构域(vl)和重链可变结构域(vh),其中vl结构域包含(i)框架区1(fw1),其包含seq id no: 34、37、39或20;(ii)框架区2(fw2),其包含seq id no:35、38或 40;(iii)框架区3(fw3),其包含seq id no:36或22;以及(iv)框架区4(fw4),其包含seq id no:19;并且其中vh包含:(i)框架区 1(fw1),其包含seq id no:41、44、46或49;(ii)框架区2(fw2),其包含seq id no:42、47、50或52;(iii)框架区3(fw3),其包含seqid no:43、45、48或51;以及(iv)框架区4(fw4),其包含seq id no: 26或30。
[0111]
seq id no:19、20、22、26、30和34-52的氨基酸序列提供于实施例1的表a-c中,其再现如下:表a.全鼠和全人可变区的非cdr序列。
表b.人源化回复突变轻链(lc)可变区的非cdr序列
粗体和下划线氨基酸表示鼠序列的回复突变表c.人源化回复突变重链(hc)可变区的非cdr序列
粗体和下划线氨基酸表示鼠序列的回复突变
[0112]
在一些实施方案中,抗cldn18.2抗体(诸如人源化抗体)或其抗原结合片段包含vl,所述vl包含:(i)fw1,其包含seqidno:34;fw2,其包含seqidno:35;fw3,其包含seqidno:36;和fw4,其包含seqidno:19;(ii)fw1,其包含seqidno:37;fw2,其包含seqidno:38;fw3,其包含seqidno:36;和fw4,其包含seqidno:19;(iii)fw1,其包含seqidno:39;fw2,其包含seqidno:40;fw3,其包含seqidno:22;和fw4,其包含seqidno:19;或(iv)fw1,其包含seqidno:20;fw2,其包含seqidno:40;fw3,其包含seqidno:22;和fw4,其包含seqidno:19。另外或可选地,在一些实施方案中,抗cldn18.2抗体(诸如人源化抗体)或其抗原结合片段包含vh,所述vh包含:(i)fw1,其包含seqidno:41;fw2,其包含seqidno:42;fw3,其包含seqidno:43;和fw4,其包含seqidno:26;(ii)fw1,其包含seqidno:44;fw2,其包含seqidno:42;fw3,其包含seqidno:45;和fw4,其包含seqidno:26;(iii)fw1,其包含seqidno:46;fw2,其包含seqidno:47;fw3,其包含seqidno:48;和fw4,其包含seqidno:30;(iv)fw1,其包含seqidno:49;fw2,其包含seqidno:50;fw3,其包含seqidno:51;和fw4,其包含seqidno:26;(v)fw1,其包含seqidno:49;fw2,其包含seqidno:52;fw3,其包含seqidno:51;和fw4,其包含seqidno:26;(vi)fw1,其包含seqidno:49;fw2,其包含seqidno:50;fw3,其包含seqidno:51;和fw4,其包含seqidno:26;或(vii)fw1,其包含seqidno:49;fw2,其包含seqidno:52;fw3,其包含seqidno:51;和fw4,其包含seqidno:26;
[0113]
在一些实施方案中,抗cldn18.2抗体(诸如人源化抗体)或其抗原结合片段包含:vl,所述vl包含:fw1,其包含seqidno:34,fw2,其包含seqidno:35,fw3,其包含seqidno:36,和fw4,其包含:seqidno:19;和vh,所述vh包含:fw1,其包含seqidno:41,fw2,其包含seqidno:42,fw3,其包含seqidno:43,和fw4,其包含seqidno:26。在一些实施方案中,抗cldn18.2抗体(诸如人源化抗体)或其抗原结合片段包含:vl,所述vl包含:fw1,其包含seqidno:34,fw2,其包含seqidno:35,fw3,其包含seqidno:36,和fw4,其包含:seqidno:19;和vh,所述vh包含:fw1,其包含seqidno:44,fw2,其包含seqidno:42,fw3,其包含seqidno:45,和fw4,其包含seqidno:26。在一些实施方案中,抗cldn18.2抗体(诸如人源化抗体)或其抗原结合片段包含:vl,所述vl包含:fw1,其包含seqidno:34,fw2,其包含seqidno:35,fw3,其包含seqidno:36,和fw4,其包含:seqidno:19;和vh,所述vh包含:fw1,其包含seqidno:46,fw2,其包含seqidno:47,fw3,其包
含seqidno:48,和fw4,其包含seqidno:30。在一些实施方案中,抗cldn18.2抗体(诸如人源化抗体)或其抗原结合片段包含:vl,所述vl包含:fw1,其包含seqidno:34,fw2,其包含seqidno:35,fw3,其包含seqidno:36,和fw4,其包含:seqidno:19;和vh,所述vh包含:fw1,其包含seqidno:49,fw2,其包含seqidno:50,fw3,其包含seqidno:51,和fw4,其包含seqidno:26。在一些实施方案中,抗cldn18.2抗体(诸如人源化抗体)或其抗原结合片段包含:vl,所述vl包含:fw1,其包含seqidno:34,fw2,其包含seqidno:35,fw3,其包含seqidno:36,和fw4,其包含:seqidno:19;和vh,所述vh包含:fw1,其包含seqidno:49,fw2,其包含seqidno:52,fw3,其包含seqidno:51,和fw4,其包含seqidno:26。在一些实施方案中,抗cldn18.2抗体(诸如人源化抗体)或其抗原结合片段包含:vl,所述vl包含:fw1,其包含seqidno:37,fw2,其包含seqidno:38,fw3,其包含seqidno:36,和fw4,其包含:seqidno:19;和vh,所述vh包含:fw1,其包含seqidno:41,fw2,其包含seqidno:42,fw3,其包含seqidno:43,和fw4,其包含seqidno:26。在一些实施方案中,抗cldn18.2抗体(诸如人源化抗体)或其抗原结合片段包含:vl,所述vl包含:fw1,其包含seqidno:37,fw2,其包含seqidno:38,fw3,其包含seqidno:36,和fw4,其包含:seqidno:19;和vh,所述vh包含:fw1,其包含seqidno:44,fw2,其包含seqidno:42,fw3,其包含seqidno:45,和fw4,其包含seqidno:26。(在一些实施方案中,抗cldn18.2抗体(诸如人源化抗体)或其抗原结合片段包含:vl,所述vl包含:fw1,其包含seqidno:37,fw2,其包含seqidno:38,fw3,其包含seqidno:36,和fw4,其包含:seqidno:19;和vh,所述vh包含:fw1,其包含seqidno:46,fw2,其包含seqidno:47,fw3,其包含seqidno:48,和fw4,其包含seqidno:30。在一些实施方案中,抗cldn18.2抗体(诸如人源化抗体)或其抗原结合片段包含:vl,所述vl包含:fw1,其包含seqidno:37,fw2,其包含seqidno:38,fw3,其包含seqidno:36,和fw4,其包含:seqidno:19;和vh,所述vh包含:fw1,其包含seqidno:49,fw2,其包含seqidno:50,fw3,其包含seqidno:51,和fw4,其包含seqidno:26。在一些实施方案中,抗cldn18.2抗体(诸如人源化抗体)或其抗原结合片段包含:vl,所述vl包含:fw1,其包含seqidno:37,fw2,其包含seqidno:38,fw3,其包含seqidno:36,和fw4,其包含:seqidno:19;和vh,所述vh包含:fw1,其包含seqidno:49,fw2,其包含seqidno:52,fw3,其包含seqidno:51,和fw4,其包含seqidno:26。在一些实施方案中,抗cldn18.2抗体(诸如人源化抗体)或其抗原结合片段包含:vl,所述vl包含:fw1,其包含seqidno:39,fw2,其包含seqidno:40,fw3,其包含seqidno:22,和fw4,其包含:seqidno:19;且vh包含:fw1,其包含seqidno:41,fw2,其包含seqidno:42,fw3,其包含seqidno:43,和fw4,其包含seqidno:26。在一些实施方案中,抗cldn18.2抗体(诸如人源化抗体)或其抗原结合片段包含:vl,所述vl包含:fw1,其包含seqidno:39,fw2,其包含seqidno:40,fw3,其包含seqidno:22,和fw4,其包含:seqidno:19;和vh,所述vh包含:fw1,其包含seqidno:44,fw2,其包含seqidno:42,fw3,其包含seqidno:45,和fw4,其包含seqidno:26。在一些实施方案中,抗cldn18.2抗体(诸如人源化抗体)或其抗原结合片段包含:vl,所述vl包含:fw1,其包含seqidno:39,fw2,其包含seqidno:40,fw3,其包含seqidno:22,和fw4,其包含:seqidno:19;和vh,所述vh包含:fw1,其包含seqidno:46,fw2,其包含seqidno:47,fw3,其包含seqidno:48,和fw4,其包含seqidno:30。在一些实施方案中,抗cldn18.2抗体(诸如人源化
抗体)或其抗原结合片段包含:vl,所述vl包含:fw1,其包含seqidno:39,fw2,其包含seqidno:40,fw3,其包含seqidno:22,和fw4,其包含:seqidno:19;和vh,所述vh包含:fw1,其包含seqidno:49,fw2,其包含seqidno:50,fw3,其包含seqidno:51,和fw4,其包含seqidno:26。在一些实施方案中,抗cldn18.2抗体(诸如人源化抗体)或其抗原结合片段包含:vl,所述vl包含:fw1,其包含seqidno:39,fw2,其包含seqidno:40,fw3,其包含seqidno:22,和fw4,其包含:seqidno:19;和vh,所述vh包含:fw1,其包含seqidno:49,fw2,其包含seqidno:52,fw3,其包含seqidno:51,和fw4,其包含seqidno:26。在一些实施方案中,抗cldn18.2抗体(诸如人源化抗体)或其抗原结合片段包含:vl,所述vl包含:fw1,其包含seqidno:20,fw2,其包含seqidno:40,fw3,其包含seqidno:22,和fw4,其包含:seqidno:19;和vh,所述vh包含:fw1,其包含seqidno:41,fw2,其包含seqidno:42,fw3,其包含seqidno:43,和fw4,其包含seqidno:26。在一些实施方案中,抗cldn18.2抗体(诸如人源化抗体)或其抗原结合片段包含:vl,所述vl包含:fw1,其包含seqidno:20,fw2,其包含seqidno:40,fw3,其包含seqidno:22,和fw4,其包含:seqidno:19;和vh,所述vh包含:fw1,其包含seqidno:44,fw2,其包含seqidno:42,fw3,其包含seqidno:45,和fw4,其包含seqidno:26。在一些实施方案中,抗cldn18.2抗体(诸如人源化抗体)或其抗原结合片段包含:vl,所述vl包含:fw1,其包含seqidno:20,fw2,其包含seqidno:40,fw3,其包含seqidno:22,和fw4,其包含:seqidno:19;和vh,所述vh包含:fw1,其包含seqidno:46,fw2,其包含seqidno:47,fw3,其包含seqidno:48,和fw4,其包含seqidno:30。在一些实施方案中,抗cldn18.2抗体(诸如人源化抗体)或其抗原结合片段包含:vl,所述vl包含:fw1,其包含seqidno:20,fw2,其包含seqidno:40,fw3,其包含seqidno:22,和fw4,其包含:seqidno:19;和vh,所述vh包含:fw1,其包含seqidno:49,fw2,其包含seqidno:50,fw3,其包含seqidno:51,和fw4,其包含seqidno:26。在一些实施方案中,抗cldn18.2抗体(诸如人源化抗体)或其抗原结合片段包含:vl,所述vl包含:fw1,其包含seqidno:20,fw2,其包含seqidno:40,fw3,其包含seqidno:22,和fw4,其包含:seqidno:19;和vh,所述vh包含:fw1,其包含seqidno:49,fw2,其包含seqidno:52,fw3,其包含seqidno:51,和fw4,其包含seqidno:26。在一些实施方案中,抗cldn18.2抗体(诸如人源化抗体)或其抗原结合片段包含:vl,所述vl包含:fw1,其包含seqidno:34,fw2,其包含seqidno:35,fw3,其包含seqidno:36,和fw4,其包含:seqidno:19;和vh,所述vh包含:fw1,其包含seqidno:49,fw2,其包含seqidno:50,fw3,其包含seqidno:51,和fw4,其包含seqidno:26。在一些实施方案中,抗cldn18.2抗体(诸如人源化抗体)或其抗原结合片段包含:vl,所述vl包含:fw1,其包含seqidno:37,fw2,其包含seqidno:38,fw3,其包含seqidno:36,和fw4,其包含:seqidno:19;和vh,所述vh包含:fw1,其包含seqidno:49,fw2,其包含seqidno:50,fw3,其包含seqidno:51,和fw4,其包含seqidno:26。在一些实施方案中,抗cldn18.2抗体(诸如人源化抗体)或其抗原结合片段包含:vl,所述vl包含:fw1,其包含seqidno:39,fw2,其包含seqidno:40,fw3,其包含seqidno:22,和fw4,其包含:seqidno:19;和vh,所述vh包含:fw1,其包含seqidno:49,fw2,其包含seqidno:50,fw3,其包含seqidno:51,和fw4,其包含seqidno:26。在一些实施方案中,抗cldn18.2抗体(诸如人源化抗体)或其抗原结合片段包含:vl,所述vl包含:fw1,其包含seqidno:20,fw2,其包含seqid
no:40,fw3,其包含seqidno:22,和fw4,其包含:seqidno:19;和vh,所述vh包含:fw1,其包含seqidno:49,fw2,其包含seqidno:50,fw3,其包含seqidno:51,和fw4,其包含seqidno:26。在一些实施方案中,抗cldn18.2抗体(诸如人源化抗体)或其抗原结合片段包含:vl,所述vl包含:fw1,其包含seqidno:34,fw2,其包含seqidno:35,fw3,其包含seqidno:36,和fw4,其包含:seqidno:19;和vh,所述vh包含:fw1,其包含seqidno:49,fw2,其包含seqidno:52,fw3,其包含seqidno:51,和fw4,其包含seqidno:26。在一些实施方案中,抗cldn18.2抗体(例如人源化抗体)或其抗原结合片段包含:vl,所述vl包含:fw1,其包含seqidno:37,fw2,其包含seqidno:38,fw3,其包含seqidno:36,和fw4,其包含:seqidno:19;和vh,所述vh包含:fw1,其包含seqidno:49,fw2,其包含seqidno:52,fw3,其包含seqidno:51,和fw4,其包含seqidno:26。在一些实施方案中,抗cldn18.2抗体(诸如人源化抗体)或其抗原结合片段包含:vl,所述vl包含:fw1,其包含seqidno:39,fw2,其包含seqidno:40,fw3,其包含seqidno:22,和fw4,其包含:seqidno:19;和vh,所述vh包含:fw1,其包含seqidno:49,fw2,其包含seqidno:52,fw3,其包含seqidno:51,和fw4,其包含seqidno:26。在一些实施方案中,抗cldn18.2抗体(诸如人源化抗体)或其抗原结合片段包含:vl,所述vl包含:fw1,其包含seqidno:20,fw2,其包含seqidno:40,fw3,其包含seqidno:22,和fw4,其包含:seqidno:19;和vh,所述vh包含:fw1,其包含seqidno:49,fw2,其包含seqidno:52,fw3,其包含seqidno:51,和fw4,其包含seqidno:26。
[0114]
在一些实施方案中,抗cldn抗体(诸如人源化抗体)或其抗原结合片段包含:vl,其包含本技术所述的fw1、fw2、fw3和fw4序列;和vh,其包含本技术所述的fw1、fw2、fw3,和fw4序列;还包含例如在pct/cn2019/078150中描述的抗cdln抗体的6个互补性决定区(cdr),所述文献的内容通过引用整体并入本技术。
[0115]
在一些实施方案中,提供了本技术所述的抗cldn18.2抗体(诸如人源化抗体)或其片段的氨基酸序列变体(“抗cldn18.2抗体变体”)。例如,可能需要改善抗cldn18.2抗体的结合亲和力和/或其它生物学特性。抗cldn18.2抗体的氨基酸序列变体可通过在编码抗体试剂的核苷酸序列中引入适当的修饰或通过肽合成来制备。这样的修饰包括例如抗体试剂的氨基酸序列内的残基的删除和/或插入和/或取代。可以进行删除、插入和取代的任何组合以获得最终构建体,条件是最终构建体具有所需的特征,例如抗原结合。
[0116]
在一些实施方案中,提供了具有一个或多个氨基酸取代的抗cldn18.2抗体变体。用于取代诱变的目标位点包括hvr和fr。可以将氨基酸取代引入到感兴趣的抗体试剂中,并筛选具有期望活性的产物,例如保留的/改善的抗原结合,降低的免疫原性或改善的adcc或cdc。
[0117]
示例性的取代变体是亲和力成熟的抗体试剂,其可以例如使用基于噬菌体展示的亲和力成熟技术来方便地产生。简单地说,使一个或多个cdr残基突变,并且在噬菌体上展示变体抗体部分,并且针对特定的生物活性(例如,结合亲和力)进行筛选。可以在hvr中进行改变(例如取代)以改善抗体亲和力。这样的改变可以在hvr“热点”中进行,即,在由在体细胞成熟过程中以高频率经历突变的密码子编码的残基中进行(参见,例如,see,e.g.,chowdhury,methodsmol.biol.207:179-196(2008)),和/或在特异性确定残基(sdr)中进行,测试所得变体vh或v
l
的结合亲和力。例如,methodsinmolecularbiology178:1-37
(o'brienetal.,ed.,humanpress,totowa,nj,(2001))中已经描述了通过从二级文库构建和重新选择的亲和力成熟。
[0118]
在亲和力成熟的一些实施方案中,通过多种方法(例如易错pcr、链重排或寡核苷酸定向诱变)中的任一种将多样性引入用于成熟选择的可变基因中。然后创建二级文库。然后筛选文库以鉴定具有期望亲和力的任何抗体试剂变体。引入多样性的另一种方法涉及hvr-定向途径,其中将若干hvr残基(例如,一次4-6个残基)随机化。涉及抗原结合的hvr残基,可以例如使用丙氨酸扫描诱变或建模,被特异性地鉴定。通常特定地靶向cdr-h3和cdr-l3。
[0119]
在一些实施方案中,取代、插入或删除可以发生在一个或多个hvr内,只要这样的改变基本上不降低抗体试剂与抗原结合的能力。例如,可以在hvr中进行基本上不降低结合亲和力的保守改变(例如,本技术提供的保守取代)。这些改变可以在hvr“热点”或sdr之外。在以上提供的变体vh和vl序列的一些实施方案中,每个hvr或者是未改变的,或者含有不超过一个、两个或三个氨基酸取代。
[0120]
如cunninghamandwells(1989)science,244:1081-1085所述,鉴定可靶向突变的抗体试剂的残基或区域的有用方法称为“丙氨酸扫描突变”。在该方法中,鉴定一个残基或一组靶残基(例如,带电残基,诸如arg、asp、his、lys和glu),并用中性或带负电荷的氨基酸(例如,丙氨酸或聚丙氨酸)取代,以确定抗体试剂与抗原的相互作用是否受影响。可以在氨基酸位置引入进一步的取代,表明对初始取代的功能敏感性。可选地或另外,可测定抗原-抗体试剂复合物的晶体结构以鉴定抗体试剂和抗原之间的接触点。这样的接触残基和相邻残基可以作为用于取代的候选物被靶向或消除。可以筛选变体以确定它们是否含有期望的特性。
[0121]
氨基酸序列插入包括在长度上从一个残基到含有一百个或更多个残基的多肽的氨基和/或羧基末端融合,以及单个或多个氨基酸残基的序列内插入。末端插入的实例包括具有n-末端甲硫氨酰基残基的抗体试剂。抗体试剂分子的其它插入变体包括抗体试剂的n-或c-末端与酶(例如用于adept)或增加抗体试剂的血清半衰期的多肽的融合。
[0122]
在某些实施方案中,抗cldn抗体变体中的氨基酸取代是保守氨基酸取代。在某些实施方案中,抗cldn抗体变体中的氨基酸取代是非保守氨基酸取代。在某些实施方案中,氨基酸取代基本上不降低抗体与抗原结合的能力。例如,可以进行基本上不降低cldn18.2结合亲和力的保守改变(例如,本技术提供的保守取代)。抗cldn18.2抗体对cldn18.2的结合亲和力可使用以下实施例中所述的方法评估。
[0123]
保守取代示于表3中“保守取代”的标题下。在表3的“示例性取代”标题下提供了更实质性的改变,以及如以下关于氨基酸侧链类别的进一步描述。可以将氨基酸取代引入兴趣抗体中,并筛选具有期望活性的产物,例如保留的/改善的cldn18.2结合。表3:氨基酸取代
[0124]
非保守取代需要将这些类别之一的成员替换为另一类别。示例性替代变体是亲和力成熟的抗体,其可以例如使用基于噬菌体展示的亲和力成熟技术(例如本技术所述的那些技术)方便地产生。简单地说,使一个或多个cdr残基突变,并且在噬菌体上展示变体抗体,并且针对特定的生物活性(例如,结合亲和力)进行筛选。可以在hvr中进行改变(例如取代)以改善抗体亲和力。这样的改变可以在hvr“热点”中进行,即,在由在体细胞成熟过程中以高频率经历突变的密码子编码的残基中进行(参见,例如,see,e.g.,chowdhury,methods mol.biol.207:179-196(2008)),和/ 或在sdr中进行,测试所得变体vh或vl的结合亲和力。例如,methodsin molecular biology 178:1-37(o'brien et al.,ed.,human press,totowa,nj, (2001)中已经描述了通过从二级文库构建和重新选择的亲和力成熟)。
[0125]
在一些实施方案中,抗cldn18.2抗体与cldn18.2蛋白(或其片段)的至少一种等位基因变体交叉反应。在一些实施方案中,当与天然存在的cldn18.2(或其片段)相比时,等位
00/42072和shields et al.j biol.chem.9(2):6591-6604(2001)描述了与fcr的结合改善或减弱的抗体变体。这些出版物的内容在本技术特别引入作为参考。抗体可以是fab、fab’、f(ab)’2、单链fv(scfv)、fv片段;双抗和线性抗体。此外,抗体可以是与cldn18.2结合但也与一种或多种其它靶标结合并抑制其功能的多特异性抗体。所述抗体可以与治疗剂 (例如,细胞毒性剂、放射性同位素和化疗剂)或用于通过成像(例如,放射性同位素、荧光染料和酶)在患者样品或体内检测cldn18.2的标记缀合。其它修饰包括毒素与本技术提供的抗cldn18.2抗体的缀合。编码人源化抗claudin 18.2抗体的核酸
[0132]
还考虑了编码本技术所述的人源化抗cldn18.2抗体的核酸分子。在一些实施方案中,提供了编码人源化抗cldn18.2抗体(包括本技术所述的人源化抗cldn18.2抗体的任一个)的核酸(或一组核酸)。在一些实施方案中,本技术描述的编码人源化抗cldn18.2抗体的核酸(或一组核酸)可进一步包含编码肽标签(诸如蛋白质纯化标签,例如his标签、 ha标签)。
[0133]
这里还考虑了分离的宿主细胞,其包含:人源化的抗cldn18.2 抗体;分离的核酸,其编码人源化的抗cldn18.2抗体的多肽组分;以及载体,其包含编码本技术所述的人源化抗cldn18.2抗体的多肽组分的核酸。
[0134]
本技术还包括这些核酸序列的变体。例如,变体包括在至少中等严格的杂交条件下与编码本技术所述的人源化抗cldn18.2抗体的核酸序列杂交的核苷酸序列。
[0135]
本发明还提供了其中插入了本技术的核酸的载体。
[0136]
简而言之,编码人源化抗cldn18.2抗体的天然或合成核酸对人源化抗cldn18.2抗体的表达可以通过将核酸插入合适的表达载体来实现,使得核酸可操作地连接至与5'和3'调节元件,包括例如启动子(例如,淋巴细胞特异性启动子)和3'非翻译区(utr)。该载体可适用于真核宿主细胞的复制和整合。典型的克隆和表达载体含有转录和翻译终止子、起始序列和用于调节期望核酸序列表达的启动子。
[0137]
使用标准基因递送方案,本技术的核酸也可用于核酸免疫和基因治疗。基因转运的方法是本领域熟知的。参见,例如,美国专利no.5,399,346、 5,580,859、5,589,466,通过引用将其整体并入本文。在一些实施方案中,本发明提供了一种基因治疗载体。
[0138]
可将核酸克隆到多种类型的载体中。例如,可以将核酸克隆到载体中,所述载体包括但不限于质粒、噬菌粒、噬菌体衍生物、动物病毒和粘粒。特别感兴趣的载体包括表达载体、复制载体、探针产生载体和测序载体。
[0139]
此外,所述表达载体可以病毒载体的形式提供给细胞。病毒载体技术在本领域中是众所周知的,并且已被描述于例如sambrook et al.(2001, molecular cloning:a laboratory manual,cold spring harbor laboratory,newyork),以及其他病毒学和分子生物学手册。可用作载体的病毒包括但不限于逆转录病毒、腺病毒、腺相关病毒、疱疹病毒和慢病毒。通常,合适的载体包含在至少一个生物体中有功能的复制起点、启动子序列、方便的限制性内切核酸酶位点和一个或多个可选择标记(参见,例如,wo 01/96584; wo 01/29058;和美国专利no.6,326,193)。
[0140]
已经开发了许多基于病毒的系统用于将基因转移到哺乳动物细胞中。例如,逆转录病毒为基因递送系统提供了方便的平台。可以使用本领域已知的技术将选择的基因插入
载体并包装在逆转录病毒颗粒中。然后可以分离重组病毒并在体内或离体递送至受试者的细胞。许多逆转录病毒系统是本领域已知的。在一些实施方案中,使用腺病毒载体。许多腺病毒载体是本领域已知的。在一些实施方案中,使用慢病毒载体。衍生自诸如慢病毒的逆转录病毒的载体是实现长期基因转移的合适工具,因为它们允许转基因的长期、稳定的整合及其在子细胞中的增殖。慢病毒载体相对于衍生自诸如鼠白血病病毒的瘤逆转录病毒的载体具有额外的优点,因为它们可以转导非增殖细胞,诸如肝细胞。它们还具有低免疫原性的附加优点。
[0141]
另外的启动子元件,例如增强子,调节转录起始的频率。通常,它们位于起始位点上游30-110bp的区域,尽管最近已经显示许多启动子也含有起始位点下游的功能元件。启动子元件之间的间隔经常是柔性的,使得当元件相对于彼此倒置或移动时保持启动子功能。在胸苷激酶(tk)启动子中,启动子元件之间的间隔可以增加至相距50bp,之后活性开始下降。
[0142]
合适的启动子的一个实例是立即早期巨细胞病毒(cmv)启动子序列。该启动子序列是能够驱动与其可操作连接的任何多核苷酸序列的高水平表达的强组成型启动子序列。合适的促进剂的另一个实例是延长生长因子-1α(ef-1α)。然而,也可以使用其它组成型启动子序列,包括但不限于猿猴病毒40(sv40)早期启动子、小鼠乳腺肿瘤病毒(mmtv)、人免疫缺陷病毒(hiv)长末端重复(ltr)启动子、莫洛尼(momulv) 启动子、鸟白血病病毒启动子,埃巴(eb)病毒立即早期启动子、劳斯(rous) 肉瘤病毒启动子以及人基因启动子,诸如但不限于肌动蛋白启动子、肌球蛋白启动子、血红蛋白启动子和肌酸激酶启动子。此外,本发明不应限于使用组成型启动子。诱导型启动子也被考虑作为本发明的一部分。使用诱导型启动子提供了分子开关,当期望这种表达时,该分子开关能够接通与其可操作连接的多核苷酸序列的表达,或者当不期望表达时关闭该表达。诱导型启动子的实例包括但不限于金属硫蛋白启动子、糖皮质激素启动子、孕酮启动子和四环素启动子。
[0143]
在一些实施方案中,所述人源化抗cldn18.2抗体试剂的表达是诱导型的。在一些实施方案中,编码抗cldn18.2抗体试剂的核酸序列可操作地连接至诱导型启动子,包括本文所述的任何诱导型启动子。抗体生产方法
[0144]
本技术的抗体可以通过本领域已知的任何方法产生。下面描述用于抗体生产的示例性技术;然而,这些示例性技术仅仅是为了说明的目的而提供的,并不旨在是限制性的。此外,进一步描述了预期与本技术所述抗体一起使用的示例性抗体特性。
[0145]
为了制备抗原,可以纯化抗原或者从天然来源获得抗原,或者可以使用重组技术表达抗原。在一些实施方案中,抗原可用作可溶性蛋白质。在一些实施方案中,抗原可以缀合至另一多肽或其它部分,例如,以增加其免疫原性。例如,本文所述的抗原可以与fc区偶联。在一些实施方案中,在其细胞表面上表达抗原的细胞可用作抗原。
[0146]
可以通过多次皮下(sc)或腹膜内(ip)注射抗原和佐剂在动物中产生多克隆抗体。例如,本技术描述了鸡免疫的描述。在一些实施方案中,使用双功能或衍生化试剂使抗原与免疫原性蛋白质缀合,所述免疫原性蛋白质例如是钥孔血蓝蛋白、血清白蛋白、牛甲状腺球蛋白或大豆胰蛋白酶抑制剂。本技术提供了用于鸡免疫的示例性方法。适用于诸如哺乳动物的各种其它生物体的相关方法是本领域熟知的。
[0147]
如上所述,单克隆抗体可通过多种方法产生。在一些实施方案中,本技术的单克隆抗体使用杂交瘤方法制备,该方法首次描述于kohleretal.,nature,256:495(1975),并且在hongoetal.,hybridoma,14(3):253-260(1995);harlowetal.,antibodies:alaboratorymanual,(coldspringharborlaboratorypress,2nded.1988);以及hammerling等人,在monoclonalantibodiesandt-cellhybridomas563-681(elsevier,n.y.,1981)中进一步描述。人杂交瘤技术(triomatechnology)描述于vollmersandbrandlein,histologyandhistopathology,20(3):927-937(2005)和vollmersandbrandlein,methodsandfindingsinexperimentalandclinicalpharmacology,27(3):185-91(2005)。可以例如通过体外结合测定、免疫沉淀、elisa、ria等在其中生长有杂交瘤细胞的培养基中筛选兴趣抗体的存在,且结合亲和力可以通过例如scatchard分析来确定。产生具有期望结合特性的抗体的杂交瘤可以使用已知的培养技术进行亚克隆和生长,在动物中作为腹水肿瘤进行体内生长等。
[0148]
在一些实施方案中,使用诸如噬菌体展示文库的文库方法来制备单克隆抗体。参见,例如,hoogenboom等人,在methodsinmolecularbiology178:1-37(o’brienetal.,ed.,humanpress,totowa,nj,2001)中所描述。在一些实施方案中,通过聚合酶链反应(pcr)克隆vh和vl基因的所有组成成分,并在噬菌体文库中随机重组,然后筛选抗原结合的噬菌体,例如,如winter等人,在jwinteretal.,ann.rev.immunol.,12:433-455(1994)中所描述。噬菌体通常展示抗体片段,作为单链fv(scfv)片段或作为fab片段。或者,可克隆(例如,来自人)所有幼稚组成成分,以提供针对广泛的非自身以及自身抗原的单一抗体来源,而无需如griffiths等人,在emboj,12:725-734(1993)中所述的任何免疫。最后,如hoogenboomandwinter,j.mol.biol.,227:381-388(1992)所述,通过从干细胞克隆未重排的v-基因片段,并使用含有随机序列的pcr引物来编码高度可变的cdr3区并在体外完成重排,也可以合成地制备天然文库。
[0149]
在一些实施方案中,本技术的抗体是鸡抗体。可以使用本领域已知的各种技术生产鸡抗体;参见,例如,美国专利no.6,143,559;8,592,644;和9,380,769。
[0150]
在一些实施方案中,本技术的抗体是嵌合抗体。参见,例如,美国专利no.4,816,567和morrisonetal.,proc.natl.acad.sci.usa,81:6851-6855(1984)。在一些实施方案中,嵌合抗体包含非人可变区(例如,来自鸡、小鼠、大鼠、仓鼠、兔或诸如猴的非人灵长类动物的可变区)和人恒定区。在一些实施方案中,嵌合抗体是“类别转换的”抗体,其中类别或亚类已经从亲本抗体的类别或亚类改变。嵌合抗体包括其抗原结合片段。
[0151]
在一些实施方案中,嵌合抗体是人源化抗体。可以将非人抗体人源化以降低对人的免疫原性,同时保持亲代非人抗体的特异性和亲和力。通常,人源化抗体包含一个或多个可变结构域,其中,hvr,例如cdr(或其部分),衍生自非-人抗体(例如鸡抗体),并且fr(或其部分)衍生自人抗体序列。人源化抗体任选地还包含人恒定区的至少一部分。在一些实施方案中,人源化抗体中的一些fr残基用来自非人抗体(例如,衍生自所述抗体的hvr或cdr残基)的相应残基取代,例如以恢复或改善抗体特异性或亲和力。在almagro和fransson,front.biosci.13:1619-1633(2008)中综述了人源化抗体及其制备方法。例如,在wo2005014653中还描述了将鸡抗体人源化的方法。
[0152]
对于人源化有用的人框架区包括但不限于:使用“最佳匹配”方法选择的框架区
域;来自轻或重链可变区的特定亚组的人抗体的共有序列的框架区;人体细胞突变框架区或人种系框架区;和衍生自筛选fr库的框架区。参见,例如,simsetal.j.immunol.151:2296(1993);carteretal.proc.natl.acad.sci.usa,89:4285(1992);prestaetal.j.immunol.,151:2623(1993);almagroandfransson,front.biosci.13:1619-1633(2008);和bacaetal.,j.biol.chem.272:10678-10684(1997)。
[0153]
在一些实施方案中,本技术的抗体是人抗体。人抗体可以使用本领域已知的各种技术产生。在一些实施方案中,人抗体由非人动物产生,诸如基因工程鸡(参见例如美国专利no8,592,644和9,380,769)和/或本技术所述的小鼠产生。人抗体一般描述于lonberg,curr.opin.immunol.20:450-459(2008)。
[0154]
在一些实施方案中,本技术的抗体是抗体片段,包括但不限于fab、f(ab’)2、fab
’‑
sh、fv或scfv片段、或单结构域、单重链或单轻链抗体。抗体片段可以例如通过酶消化或重组技术产生。在一些实施方案中,使用完整抗体的蛋白水解消化来产生抗体片段,例如,如在morimotoetal.,journalofbiochemicalandbiophysicalmethods24:107-117(1992)和brennanetal.,science,229:81(1985)中所述。在一些实施方案中,通过重组宿主细胞产生抗体片段。例如,fab、fv和scfv抗体片段由大肠杆菌表达并从大肠杆菌分泌。或者可从抗体噬菌体文库中分离抗体片段。
[0155]
可以从大肠杆菌中直接回收fab'-sh片段并化学偶联以形成f(ab')2片段。参见carteretal.,bio/technology10:163-167(1992)。f(ab')2片段也可以直接从重组宿主细胞培养物中分离。具有增加的体内半衰期、包含挽救受体结合表位残基的fab和f(ab')2片段描述于美国专利no.5,869,046。
[0156]
在一些实施方案中,抗体是单链fv片段(scfv)。参见wo93/16185和美国专利no.5,571,894和5,587,458。可以构建scfv融合蛋白以在scfv的氨基或羧基末端产生效应蛋白的融合体。抗体片段还可以是“线性抗体”,例如,如美国专利no.5,641,870。这样的线性抗体可以是单特异性的或双特异性的。
[0157]
在一些实施方案中,本技术的抗体是多特异性抗体。多特异性抗体具有针对多于一种抗原的结合特异性(例如,具有两种、三种或更多种结合特异性的抗体)。在一些实施方案中,抗体是双特异性抗体。在一些实施方案中,双特异性抗体包含针对同一抗原的两种不同的结合特异性(例如,针对同一抗原具有不同的结合亲和力和/或特异性表位)。在一些实施方案中,双特异性抗体包含对两种不同抗原的结合特异性。在一些实施方案中,双特异性抗体是全长或完整抗体。在一些实施方案中,双特异性抗体是本技术的抗体片段。
[0158]
用于产生和纯化双特异性抗体的各种方法是本领域已知的。已经描述了许多方法。一种途径是“杵臼”或“突起-进入-空腔”途径(参见,例如,美国专利no.5,731,168)。在一些实施方案中,fc结构域单体的异二聚化通过在两个fc结构域单体中引入不同的但相容的取代来促进,诸如“杵臼”残基对和电荷残基对。杵和臼相互作用有利于异二聚体的形成,而杵-杵和臼-臼相互作用由于有利相互作用的空间碰撞和缺失而阻碍同二聚体的形成。臼是指当蛋白质中的原始氨基酸被具有较小侧链体积的不同氨基酸替代时产生的空隙。杵是指当蛋白质中的原始氨基酸被具有较大侧链体积的不同氨基酸替代时产生的凸起。例如,在一些实施方案中,被置换的氨基酸在fc结构域单体的ch3抗体恒定结构域中并且参与两个fc结构域单体的二聚化。在一些实施方案中,在一个ch3抗体恒定结构域中产生臼以容纳
另一个ch3抗体恒定结构域中的杵,使得杵和臼氨基酸起到促进或有利于两个fc结构域单体的异源二聚化的作用。在一些实施方案中,在一个ch3抗体恒定结构域中产生臼以更好地容纳另一个ch3抗体恒定结构域中的原始氨基酸。在一些实施方案中,一个ch3抗体恒定结构域中产生杵以与另一个ch3抗体恒定结构域中的原始氨基酸形成额外的相互作用。
[0159]
在一些实施方案中,通过用具有较小侧链的氨基酸(例如丙氨酸、缬氨酸或苏氨酸)置换具有较大侧链的氨基酸(例如酪氨酸或色氨酸)来构建臼,例如在ch3抗体恒定结构域中的y407v突变。类似地,在一些实施方案中,通过用具有较大侧链的氨基酸置换具有较小侧链的氨基酸来构建杵,例如在ch3抗体恒定结构域中的t366w突变。在一些实施方案中,一个fc结构域单体包含杵突变t366w,并且另一个fc结构域单体包含臼突变t366s、l358a和y407v。杵-臼氨基酸对的实例包括但不限于表 4中所示的那些。表4.杵-臼氨基酸突变
[0160]
另一种途径使用具有期望结合特异性(抗体-抗原结合位点)的抗体可变区,其与免疫球蛋白恒定结构域序列融合,例如与包含铰链区ch2 区和ch3区的至少一部分的免疫球蛋白重链恒定结构域融合。在一些实施方案中,双特异性抗体具有在一个臂中具有第一结合特异性的杂合免疫球蛋白重链和在另一个臂中具有杂合免疫球蛋白重链-轻链对(提供第二结合特异性)。参见wo 94/04690。另一种方法使用交联(参见,例如,美国专利no.4,676,980)以产生异源缀合抗体。在一些实施方案中,双特异性抗体可以使用化学连接(参见,例如,brennan et al.,science,229:81(1985))来制备,以蛋白水解地将完整抗体裂解成f(ab')2片段,所述片段在二硫醇络合剂的存在下被还原并转化为硫代硝基苯甲酸酯(tnb)衍生物,其中一种通过还原重新转化为fab
’‑
硫醇并与另一种fab
’‑
tnb衍生物混合以形成双特异性抗体。在一些实施方案中,fab
’‑
sh片段被化学偶联。在一些实施方案中,使用亮氨酸拉链在细胞培养物中产生双特异性抗体片段,如 kostelny et al.,j.immunol.,
148(5):1547-1553(1992)所述。对于其它双特异性抗体形式,参见,例如,spiess,c.et al.(2015)mol.immunol.67:95-106。
[0161]
在一些实施方案中,本技术的抗体是双抗,参见,例如hollinger etal.,proc.natl.acad.sci.usa,90:6444-6448(1993);在双抗中,一个片段的 vh和v
l
结构域与另一片段的互补v
l
和vh结构域配对,从而形成两个抗原结合位点。还已经报道了通过使用单链fv(sfv)二聚体制备双特异性抗体片段的另一种策略。参见gruber et al,j.immunol,152:5368(1994)。
[0162]
在一些实施方案中,本技术的抗体是单结构域抗体。单结构域抗体是指包含抗体的全部或部分重链可变结构域或全部或部分轻链可变结构域的单个多肽链。在某些实施方案中,单结构域抗体是人单结构域抗体(参见,例如,美国专利no.6,248,516b1)。在一个实施方案中,单结构域抗体包括抗体的重链可变结构域的全部或一部分。骆驼科动物抗体也是已知的。
[0163]
可以使用重组方法产生抗体。为了重组产生抗抗原抗体,将编码抗体的核酸分离并插入可复制载体中用于进一步克隆(dna扩增)或用于表达。使用常规步骤(例如,通过使用能够与编码抗体重链和轻链的基因特异性结合的寡核苷酸探针),可以容易地分离和测序编码抗体的dna。许多载体是可用的。载体组件通常包括但不限于以下的一种或多种:信号传导序列、复制起点、一个或多个标记基因、增强子元件、启动子和转录终止序列。
[0164]
本技术的抗体可以作为融合多肽与异源多肽(例如,信号传导序列或在成熟蛋白质或多肽的n末端具有特异性切割位点的其他多肽)重组产生。所选择的异源信号传导序列可以是被宿主细胞识别和加工(例如,通过信号肽酶切割)的信号传导序列。对于不识别和处理天然抗体信号传导序列的原核宿主细胞而言,所述信号传导序列被选自例如碱性磷酸酶、青霉素酶、lpp或热稳定肠毒素ii前导序列的原核信号传导序列取代。对于酵母分泌,天然信号传导序列可被例如以下取代:酵母转化酶前导序列、因子前导序列(包括酵母属(saccharomyces)和克鲁维酵母属 (kluyveromyces)α-因子前导序列)或酸性磷酸酶前导序列、白色念珠菌 (c.albicans)葡糖淀粉酶前导序列等。在哺乳动物细胞表达中,可获得哺乳动物信号传导序列以及病毒分泌前导序列,例如单纯疱疹gd信号。
[0165]
表达和克隆载体都含有使载体能够在一个或多个选定的宿主细胞中复制的核酸序列,以例如允许载体独立于宿主染色体dna进行复制。该序列可以包括复制起点或自主复制序列。这些序列对于各种细菌、酵母和病毒是熟知的。通常,哺乳动物表达载体不需要复制起点组件(可以使用sv40起点,因为它含有早期启动子。
[0166]
表达和克隆载体可以含有选择基因或可选择标志物。典型的选择基因编码蛋白质,该蛋白质(a)赋予对抗生素或其它毒素的抗性,例如,氨苄青霉素、新霉素、氨甲喋呤或四环素,(b)补充营养缺陷型缺陷,或 (c)提供不能从复合培养基获得的关键营养物。优选实例使用新霉素、霉酚酸和潮霉素。用于哺乳动物细胞的合适的可选择标志物的另一个实例是能够鉴定有能力吸收抗体编码的核酸的细胞的那些标志物,诸如dhfr、谷氨酰胺合成酶(gs)、胸苷激酶、金属硫蛋白-i和-ii,优选灵长类金属硫蛋白基因、腺苷脱氨酶、鸟氨酸脱羧酶等。例如,通过在含有dhfr的竞争性拮抗剂甲氨蝶呤(mtx)的培养基中培养转化体,鉴定了用dhfr基因转化的缺乏内源dhfr活性的中国仓鼠卵巢(cho)细胞系。
[0167]
或者,用编码兴趣抗体的dna序列、野生型dhfr基因和诸如氨基糖苷3-磷酸转移酶
(aph)的另一可选择标志物转化或共转化的宿主细胞(特别是含有内源性dhfr的野生型宿主)可以通过细胞在含有用于可选择标志物(诸如氨基糖苷抗生素,例如卡那霉素、新霉素或g418)的选择试剂的培养基中生长来选择。
[0168]
表达和克隆载体通常含有被宿主生物体识别并与编码抗体的核酸可操作连接的启动子。适用于原核宿主的启动子包括phoa启动子、β
‑ꢀ
内酰胺酶和乳糖启动子系统、碱性磷酸酶启动子、色氨酸(trp)启动子系统和杂合启动子,如tac启动子。然而,其它已知的细菌启动子也是合适的。已知用于真核的启动子序列。酵母启动子是本领域熟知的,并且可以包括由生长条件调节的诱导型启动子/增强子。几乎所有真核基因都具有富at 的区域,该区域位于转录起始位点上游约25-30个碱基处。实例包括但不限于3-磷酸甘油酸激酶或其它糖酵解酶的启动子,例如烯醇化酶、甘油醛
ꢀ‑
3-磷酸脱氢酶、己糖激酶、丙酮酸脱羧酶、磷酸果糖激酶、葡萄糖-6-磷酸异构酶、3-磷酸甘油酸变位酶、丙酮酸激酶、丙糖磷酸异构酶、磷酸葡萄糖异构酶和葡萄糖激酶。来自哺乳动物宿主细胞中的载体的抗体转录可以例如通过从病毒基因组获得的启动子来控制。sv40病毒的早期和晚期启动子方便地作为也含有sv40病毒复制起点的sv40限制性片段获得。人巨细胞病毒的立即早期启动子方便地作为hindiii e限制性片段获得。或者,rous 肉瘤病毒长末端重复可用作启动子。
[0169]
编码本发明抗体的dna在高等真核生物中的转录通常通过将增强子序列插入到载体中来增加。现在已知许多来自哺乳动物基因(珠蛋白、弹性蛋白酶、白蛋白、α-甲胎蛋白和胰岛素等)的增强子序列。然而,通常使用真核细胞病毒的增强子。
[0170]
用于真核宿主细胞(酵母、真菌、昆虫、植物、动物、人或其它多细胞生物的有核细胞)的表达载体也将含有转录终止和稳定mrna所需的序列。
[0171]
用于在本技术的载体中克隆或表达dna的合适的宿主细胞是上述原核生物、酵母或高等真核生物细胞。为此目的合适的原核生物包括真细菌,诸如革兰氏阴性或革兰氏阳性生物体,例如肠杆菌科 (enterobacteriaceae),诸如埃希氏杆菌属(escherichia),例如大肠杆菌(e. coli),肠杆菌(enterobacter),欧文氏菌(erwinia),克雷伯菌(klebsiella),变形杆菌(proteus),沙门氏菌(salmonella),例如鼠伤寒沙门氏菌 (salmonella typhimurium),沙雷氏菌(serratia),例如粘质沙雷氏菌 (serratia marcescans)和志贺氏菌(shigella)等,除原核生物外,诸如丝状真菌或酵母菌的真核微生物也是编码抗体的载体的合适克隆或表达宿主。酿酒酵母(saccharomyces cerevisiae)或普通面包酵母在低等真核宿主微生物中是最常用的。可以选择某些真菌和酵母菌株,其中糖基化通路已经被“人源化”从而导致产生具有部分或完全人糖基化模式的抗体。参见,例如,li et al.,nat.biotech.24:210-215(2006)。
[0172]
棉花、玉米、马铃薯、大豆、矮牵牛、番茄、浮萍(leninaceae)、苜蓿(m.truncatula)和烟草的植物细胞培养物可以用作宿主。
[0173]
用于表达糖基化抗体的合适的宿主细胞也衍生自多细胞生物体(无脊椎动物和脊椎动物)。无脊椎动物细胞的实例包括植物和昆虫细胞。已经鉴定了许多杆状病毒株和变体,以及来自诸如草地贪夜蛾(spodopterafrugiperda)、埃及伊蚊(aedes aegypti)、白纹伊蚊(aedes albopictus)、黑腹果蝇(drosophila melanogaster)、和家蚕(bombyxmori)的宿主的相应受纳昆虫宿主细胞。
[0174]
脊椎动物细胞可用作宿主、脊椎动物细胞在培养(组织培养)中的增殖已成为常规
步骤。有用的哺乳动物宿主细胞系的实例是:通过sv40转化的猴肾cv1系(cos-7,atcccrl1651);人胚肾系(293或用于在悬浮培养中生长的亚克隆293细胞,grahametal.,j.genvirol.36:59(1977));幼仓鼠肾细胞(bhk,atccccl10);小鼠塞尔托利氏(sertoli)细胞(tm4,mather,biol.reprod.23:243-251(1980));猴肾细胞(cv1atccccl70);非洲绿猴肾细胞(vero-76,atcccrl-1587);人宫颈癌细胞(hela,atccccl2);犬肾细胞(mdck,atccccl34);水牛大鼠肝细胞(brl3a,atcccrl1442);人肺细胞(w138,atccccl75);人肝细胞(hepg2,hb8065);小鼠乳腺肿瘤(mmt060562,atccccl51);tri细胞(matheretal.,annalsn.y.acad.sci.383:44-68(1982));mrc5细胞;fs4细胞;和人肝癌细胞系(hepg2)。其它有用的哺乳动物宿主细胞系包括中国仓鼠卵巢(cho)细胞,包括dhfr-cho细胞(urlaubetal.,proc.natl.acad.sci.usa77:4216(1980));和骨髓瘤细胞系,诸如ns0和sp2/0。对于某些适于产生抗体的哺乳动物宿主细胞系的综述,参见,例如,yazaki和wu,《分子生物学方法》(methodsinmolecularbiology),第248卷(b.k.c.lo,ed.,humanapress,totowa,n.j.,2003),第255-268页。
[0175]
本技术的宿主细胞可以在多种培养基中培养。市售培养基,诸如ham'sf10(sigma)、最小必需培养基((mem),sigma)、rpmi-1640(sigma)和杜氏改良伊戈尔培养基((dmem),sigma)适于培养宿主细胞。另外,在hametal.,meth.enz.58:44(1979)、barnesetal.,anal.biochem.102:255(1980)、美国专利no.4,767,704;4,657,866;4,927,762;4,560,655;或5,122,469;wo90/03430;wo87/00195或u.s.pat.re.30,985中描述的培养基的任一个均可用作宿主细胞的培养基。这些培养基中的任一种可根据需要补充激素和/或其它生长因子(诸如胰岛素、转铁蛋白或表皮生长因子),盐(诸如氯化钠、钙、镁、和磷酸盐),缓冲液(诸如hepes)、核苷酸(诸如腺苷和胸苷),抗生素(诸如gentamycin
tm
药物),微量元素(定义为通常以微摩尔范围内的终浓度存在的无机化合物)和葡萄糖或等同的能量源。还可以包括本领域技术人员已知的适当浓度的任何其它必要补充剂。培养条件,诸如温度、ph等,是先前选择用于表达的宿主细胞使用的那些,并且对于本领域技术人员是显而易见的。
[0176]
当使用重组技术时,抗体可以在胞内、周质空间中产生,或直接分泌到培养基中。如果抗体在胞内产生,则作为第一步骤,通过例如离心或超滤除去宿主细胞或裂解片段的颗粒碎片。carteretal.,bio/technology10:163-167(1992)描述了对分泌到大肠杆菌周质空间的抗体进行分离的步骤。
[0177]
可以使用例如羟基磷灰石层析、疏水作用层析、凝胶电泳、透析和亲和层析来纯化从细胞制备的抗体组合物,其中亲和层析是通常优选的纯化步骤之一。糖基化变体
[0178]
在一些实施方案中,改变本技术提供的人源化抗cldn18.2抗体以增加或降低抗cldn18.2抗体糖基化的程度。通过改变人源化抗cldn18.2抗体或其多肽部分的氨基酸序列,使得产生或除去一个或多个糖基化位点,可以方便地完成向人源化抗cldn18.2抗体添加或删除糖基化位点。
[0179]
当人源化抗cldn18.2抗体包含fc区时,与其连接的碳水化合物可以更改。由哺乳动物细胞产生的天然抗体通常包含通常通过n-连接与fc区ch2结构域的asn297连接的分支,双触角寡糖。参见,例如wrightetal.,tibtech15:26-32(1997)。所述低聚糖可包括
各种碳水化合物,例如甘露糖、n-乙酰葡糖胺(glcnac)、半乳糖和唾液酸,以及在双触角低聚糖结构的“茎”中与glcnac连接的岩藻糖。在一些实施方案中,可以对本发明的人源化抗cldn18.2抗体中的寡糖进行修饰,以产生具有某些改善性质的人源化抗cldn18.2抗体变体。
[0180]
与fc的ch2结构域连接的n-聚糖是异质的。在cho细胞中产生的抗体或fc融合蛋白通过岩藻糖基转移酶活性被岩藻糖基化。参见 shoji-hosaka et al.,j.biochem.2006,140:777-83。通常,可以在人血清中检测到小百分比的天然存在的无岩藻糖基化iggs。fc的n-糖基化对于结合 fcγr是重要的;并且n-聚糖的岩藻糖基化增加fc’对fcγriiia的结合能力。增加的fcγriiia结合可以增强adcc,这在期望细胞毒性的某些抗体试剂治疗应用中是有利的。
[0181]
在一些实施方案中,当fc介导的细胞毒性是不期望的时,增强的效应子功能可能是有害的。在一些实施方案中,fc片段或ch2结构域未被糖基化。在一些实施方案中,使ch2结构域中的n-糖基化位点突变以防止糖基化。
[0182]
在一些实施方案中,提供了包含fc区的人源化抗cldn18.2抗体变体,其中附着于fc区的碳水化合物结构具有减少的岩藻糖或缺乏岩藻糖,这可以改善adcc功能。具体地,本技术考虑了人源化抗cldn18.2 抗体,其相对于在野生型cho细胞中产生的相同人源化抗cldn18.2抗体上的岩藻糖的量具有降低的岩藻糖。就是说,它们的特征在于其岩藻糖的量比天然cho细胞(例如,产生天然糖基化模式的cho细胞,诸如含有天然fut8基因的cho细胞)产生的岩藻糖的含量低。在一些实施方案中,所述人源化抗cldn18.2抗体是其上少于约50%、40%、30%、20%、10%或5%的n-联聚糖包含岩藻糖的抗体。例如,在这种人源化抗cldn18.2 抗体中岩藻糖的量可以为1%至80%、1%至65%、5%至65%或20%至40%。在一些实施方案中,所述人源化抗cldn18.2抗体是其上没有n-联聚糖包含岩藻糖的抗体,即,其中人源化抗cldn18.2抗体完全不带有岩藻糖或没有岩藻糖或无岩藻糖基化。岩藻糖的量是通过相对于通过maldi-tof 质谱法测得的与asn 297附着的所有糖结构(例如,复杂、杂合和高甘露糖结构)的总和计算asn297糖链中岩藻糖的平均量来确定的,例如,如 wo 2008/077546中所述。asn297是指位于fc区中约297位的天冬酰胺残基(fc区残基的eu编号);然而,由于抗体中的微小序列变化,asn297 也可位于位置297上游或下游约
±
3个氨基酸,即在位置294和300之间。这样的岩藻糖基化变体可以具有改善的adcc功能。参见,例如,美国专利公开no.us 2003/0157108(presta,l.);us 2004/0093621(kyowa hakkokogyo株式会社)。涉及“去岩藻糖基化的”或“岩藻糖缺乏型”抗体试剂变体的出版物的实例包括:us 2003/0157108;wo 2000/61739;wo2001/29246;us 2003/0115614;us 2002/0164328;us 2004/0093621;us2004/0132140;us 2004/0110704;us 2004/0110282;us 2004/0109865; wo 2003/085119;wo 2003/084570;wo 2005/035586;wo 2005/035778; wo2005/053742;wo2002/031140;okazaki et al.j.mol.biol.336:1239-1249 (2004);yamane-ohnuki et al.biotech.bioeng.87:614(2004)。能够产生脱岩藻糖基化抗体的细胞系的实例包括缺乏蛋白质岩藻糖基化的lec13 cho细胞(ripka et al.arch.biochem.biophys.249:533-545(1986);美国专利申请 no us 2003/0157108 a1,presta,l;和wo 2004/056312 a1,adams等,特别是实施例11),和敲除细胞系,诸如α-1,6-岩藻糖基转移酶基因、fut8、敲除cho细胞(参见例如,yamane-ohnuki et al.biotech.bioeng.87:614 (2004);kanda,y.et al.,
biotechnol.bioeng.,94(4):680-688(2006);andwo2003/085107)。
[0183]
进一步为人源化抗cldn18.2抗体变体提供等分寡糖,例如其中连接于人源化抗cldn18.2抗体fc区的双触角寡糖被glcnac等分。这种人源化抗cldn18.2抗体变体可以具有减少的岩藻糖基化和/或改善的adcc功能。此类抗体试剂变体的实例描述于例如wo2003/011878(jean-mairet等人);美国专利no.6,602,684(umana等人);us2005/0123546(umana等),和ferraraetal.,biotechnologyandbioengineering,93(5):851-861(2006)。还提供了在附着于fc区的寡糖中具有至少一个半乳糖残基的人源化抗cldn18.2抗体变体。这种人源化抗cldn18.2抗体变体可以具有改善的cdc功能。这样的抗体试剂变体例如描述于wo1997/30087(pateletal.);wo1998/58964(raju,s.);和wo1999/22764(raju,s.)。
[0184]
在一些实施方案中,包含fc区的人源化抗cldn18.2抗体变体能够结合fcγriii。在一些实施方案中,与包含人野生型igg1fc区的其它相同的人源化抗cldn18.2抗体相比,包含fc区的人源化抗cldn18.2抗体变体在人效应细胞(例如,t细胞)存在下具有adcc活性或在人效应细胞存在下具有增加的adcc活性。在一些实施方案中,本技术提供的抗cldn18.2抗体包含seqidno:109、seqidno:110或seqidno:111的氨基酸序列。astkgpsvfplapsskstsggtaalgclvkdyfpepvtvswnsgaltsgvhtfpavlqssglyslssvvtvpssslgtqtyicnvnhkpsntkvdkkvepkscdkthtcppcpapellggpdvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalplpeektiskakgqprepqvytlppsrdeltknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspg(seqidno:109)astkgpsvfplapsskstsggtaalgclvkdyfpepvtvswnsgaltsgvhtfpavlqssglyslssvvtvpssslgtqtyicnvnhkpsntkvdkkvepkscdkthtcppcpapellggpsvfllppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkppeeqynstlrvvsiltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppsrdeltknqvsltclvkgfypsdiavewesngqpennykttplvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspg(seqidno:110)astkgpsvfplapsskstsggtaalgclvkdyfpepvtvswnsgaltsgvhtfpavlqssglyslssvvtvpssslgtqtyicnvnhkpsntkvdkkvepkscdkthtcppcpapellggpsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynatyrvvsvltvlhqdwlngkeykckvsnkalpapiaatiskakgqprepqvytlppsrdeltknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspg(seqidno:111)半胱氨酸工程变体
[0185]
在一些实施方案中,可能需要产生半胱氨酸工程化人源化抗cldn18.2抗体,其中一个或多个氨基酸残基被半胱氨酸残基取代。在一些实施方案中,取代的残基出现在人源化抗cldn18.2抗体的可接近位点。通过用半胱氨酸取代那些残基,反应性巯基由此位于人源化抗cldn18.2抗体的可接近位点,并可用于将人源化抗cldn18.2抗体与诸如药物部分或接头-药物部分的其它部分缀合,以产生如本技术进一步描述的人源化抗cldn18.2免疫
缀合物。半胱氨酸改造的人源化抗cldn18.2抗体可以如例如描述于美国专利no.7,521,541来完成。效应子功能工程
[0186]
可能需要在效应子功能方面修饰本技术提供的人源化抗 cldn18.2抗体,以增强(例如)抗体在治疗癌症中的有效性。例如,可将半胱氨酸残基引入fc区中,从而允许在该区中形成链间二硫键。如此产生的同二聚体抗体可具有提高的内化能力和/或增加的补体介导的细胞杀伤和抗体依赖性细胞毒性(adcc)。参见caron et al.,j.exp.med.,176: 1191-1195(1992)and shapes,j.immunol.,148:2918-2922(1992)。具有增强的抗肿瘤活性的同型二聚体抗体也可以使用异双功能交联剂制备,如wolffet al.,cancer research,53:2560-2565(1993)中所述。或者,可将抗体工程化以包含通常的fc区,并由此可具有增强的补体裂解和adcc能力。参见, stevenson et al.,anti-cancer drug design3:219-230(1989)。
[0187]
可在fc区序列中进行突变或改变以改善fcr结合(例如,与fcγr、 fcrn的结合)。在一些实施方案中,与天然igg或亲本抗体相比,本技术提供的人源化抗cldn18.2抗体包含至少一种改变的效应子功能,例如,改变的adcc、cdc和/或fcrn结合。在一些实施方案中,包含突变或改变的抗体的效应子功能相对于亲本抗体增加。在一些实施方案中,包含突变或改变的抗体的效应子功能相对于亲本抗体降低。几种有用的特异性突变的实例描述于,例如,shields,rl et al.(2001)jbc 276(6)6591-6604;presta, l.g.,(2002)biochemical society transactions 30(4):487-490;和wo 00/42072。
[0188]
在一些实施方案中,本技术提供的人源化抗cldn18.2抗体包含野生型fc结构域,例如,野生型igga、igd、ige、igg(包括igg1、igg2、 igg3或igg4)或igm fc结构域。在一些实施方案中,本技术提供的人源化抗cldn18.2抗体包含fc结构域变体,所述fc结构域变体包含突变,例如fc结构域的至少一个位置上的取代突变。可以对fc结构域中的氨基酸位置进行这样的取代突变,所述氨基酸位置包括但不限于,例如,238、 239、246、248、249、252、254、255、256、258、265、267、268、269、 270、272、276、278、280、283、285、286、289、290、292、293、294、 295、296、298、301、303、305、307、309、312、315、320、322、324、 326、327、329、330、331、332、333、334、335、337、338、340、360、 373、376、378、382、388、389、398、414、416、419、430、434、435、 437、438或439,其中fc区中残基的编号是根据eu编号系统。在一些实施方案中,fc受体突变是d265a取代。在一些实施方案中,fc受体突变是n297a取代。其他合适的突变是本领域众所周知的。示例性突变在例如美国专利no.7,332,581中所述。免疫偶联物和共价修饰
[0189]
本发明还涉及包含与第二部分缀合的抗体的免疫缀合物。在一些实施方案中,第二部分是细胞毒性剂,诸如化疗剂、毒素(例如细菌、真菌、植物或动物来源的酶活性毒素,或其片段)或放射性同位素(即放射性缀合物)。
[0190]
可使用的酶活性毒素及其片段包括白喉毒素a链,白喉毒素的非结合活性片段,外毒素a链(来自铜绿假单胞菌(pseudomonas aeruginosa)、蓖麻毒素a链、相思豆毒素a链、modeccin a链、α-sarcin、油桐(aleuritesfordii)蛋白、香石竹蛋白、美洲商陆(phytolaca americana)蛋白(papi、 papii和pap-s)、苦瓜(phytolaca americana)抑制剂、麻疯树毒蛋白、巴豆毒蛋白、肥皂草(sapaonaria officinalis)抑制剂、白树毒素、丝裂
霉素 (mitogellin)、局限曲菌素(restrictocin)、酚霉素、依诺霉素和单端孢菌素 (tricothecenes)。各种放射性核素可用于制备放射性缀合的抗体。实例包括
212
bi、
131
i、
131
in、
90
y和
186
re。用于产生此类免疫缀合物的示例性化疗剂在本技术别处描述。
[0191]
在某些实施方案中,本技术提供的人源化抗cldn18.2抗体(或其抗原结合片段)与美登素(maytansine)、美登木素生物碱(maytansinoid) 或加利车霉素(calicheamicin)缀合。在某些实施方案中,本技术提供的人源化抗cldn18.2抗体(或其抗原结合片段)与美登木素生物碱dm1缀合。
[0192]
抗体和细胞毒性剂的缀合物使用多种双功能蛋白质-偶联剂制备,所述双功能蛋白质-偶联剂诸如n-琥珀酰亚胺基-3-(2-吡啶基二硫基)丙酸酯 (spdp)、亚氨基硫杂环戊烷(it)、亚氨酸酯的双功能衍生物(诸如己二酰亚氨酸二甲酯盐酸盐)、活性酯(诸如辛二酸二琥珀酰亚胺酯)、醛(诸如戊二醛)、双叠氮基化合物(诸如双(对-叠氮基苯甲酰基)己二胺)、双重氮衍生物(诸如双(对-重氮基苯甲酰基)-乙二胺)、二异氰酸酯(诸如甲苯 2,6-二异氰酸酯)和双活性氟化合物(诸如1,5-二氟-2,4-二硝基苯)。例如,蓖麻毒蛋白免疫毒素可以如vitetta et al.,science,238:1098(1987)中所述制备。碳-14-标记的1-异硫氰酰苄基-3-甲基二亚乙基三胺五乙酸(mx-dtpa) 是用于将放射性核苷酸与抗体缀合的示例性螯合剂。参见wo 94/11026。
[0193]
在另一个实施方案中,抗体可以与“受体”(诸如链霉素亲和素) 缀合,用于肿瘤预靶向,其中向患者施用抗体-受体缀合物,然后使用清除剂从循环中除去未结合的缀合物,然后施用与细胞毒性剂(例如放射性核苷酸)缀合的“配体”(例如亲和素)。
[0194]
还提供了包含与至少一种其它抗体共价连接的本技术所述的人源化抗cldn18.2抗体的异源缀合物抗体。例如,已经提出异源缀合物抗体将免疫系统细胞靶向不需要的细胞(美国专利no.4,676,980),并用于治疗hiv感染。包含本技术所述的人源化抗cldn18.2抗体的异源缀合物抗体可以使用合成蛋白质化学中已知的方法体外制备,包括涉及交联剂的那些方法。例如,可以使用二硫化物交换反应或通过形成硫醚键构建免疫毒素。用于此目的的合适试剂的实例包括亚氨基硫醇盐和4-巯基丁酰亚胺酸甲酯以及例如在美国专利no.4,676,980中公开的那些。
[0195]
还提供了包含至少一种共价修饰的人源化抗cldn18.2抗体。一种类型的共价修饰包括将人源化抗cldn18.2的靶向氨基酸残基与能够与抗体的选定侧链或n-或c-末端残基反应的有机衍生剂反应。常用的交联剂包括但不限于,例如,1,1-双(重氮乙酰基)-2-苯基乙烷;戊二醛;n-羟基琥珀酰亚胺酯,例如,与4-叠氮基水杨酸的酯;高双官能亚氨酸酯,包括二琥珀酰亚胺酯,诸如3,3
’‑
二硫代双(琥珀酰亚胺基-丙酸酯);双官能马来酰亚胺,诸如双-n-马来酰亚胺-1,8-辛烷;和试剂,诸如3-[(对-叠氮基苯基)
‑ꢀ
二硫]丙亚氨酸甲酯。
[0196]
其它修饰包括谷氨酰胺酰基和天冬酰胺酰基残基分别脱酰胺为相应的谷氨酰和天冬氨酰残基,脯氨酸和赖氨酸的羟基化,丝氨酰基或苏氨酰基残基的羟基的磷酸化,赖氨酸、精氨酸和组氨酸侧链的α-氨基的甲基化[t.e.creighton,proteins:structure and molecular properties,w.h. freeman&co.,san francisco,pp.79-86(1983)],n-末端胺的乙酰化和任何 c-末端羧基的酰胺化。
[0197]
共价修饰的另一种类型包括,以美国专利no.4,640,835、4,496,689、 4,301,144、4,670,417、4,791,192或4,179,337中阐述的方式,将本技术提供的人源化抗cldn18.2抗体
(或其抗原结合片段)连接至多种非蛋白质聚合物中的一种,例如聚乙二醇(peg)、聚丙二醇或聚氧化烯。嵌合分子
[0198]
本技术提供的人源化抗cldn18.2抗体(或其抗原结合片段)也可以由嵌合分子修饰,所述嵌合分子包含与另一种异源多肽或氨基酸序列融合的抗体。
[0199]
在一个实施方案中,这样的嵌合分子包含本技术提供的人源化抗cldn18.2抗体(或其抗原结合片段)与蛋白转导结构域的融合物,所述蛋白转导结构域使用例如人免疫缺陷病毒tat蛋白的蛋白转导结构域靶向多肽以递送至各种组织,更特别地穿过脑血屏障(schwarzeetal.,1999,science285:1569-72)。
[0200]
在另一个实施方案中,这样的嵌合分子包含本技术提供的人源化抗cldn18.2抗体(或其抗原结合片段)与标签多肽的融合物,所述标签多肽提供抗标签抗体可以选择性结合的表位。表位标签通常位于多肽的氨基或羧基末端。可使用抗标记多肽的抗体来检测本技术提供的人源化抗cldn18.2抗体(或其抗原结合片段)的此类表位标记形式的存在。各种标记多肽和它们各自的抗体是本领域已知的。实例包括聚组氨酸(poly-his)或聚组氨酸-甘氨酸(poly-his-gly)标签;fluha标签多肽及其抗体12ca5[fieldetal.,mol.cell.biol.,8:2159-2165(1988)];c-myc标签和其上的8f9、3c7、6e10、g4、b7和9e10抗体[evanetal.,molecularandcellularbiology,5:3610-3616(1985)];和单纯疱疹病毒糖蛋白d(gd)标签及其抗体[paborskyetal.,proteinengineering,3(6):547-553(1990)]。其它标签多肽包括flag-肽[hoppetal.,biotechnology,6:1204-1210(1988)];kt3表位肽[martinetal.,science,255:192-194(1992)];α-微管蛋白表位肽生物[skinneretal.,j.biol.chem.,266:15163-15166(1991)];和t7基因10蛋白肽标签[lutz-freyermuthetal.,proc.natl.acad.sci.usa,87:6393-6397(1990)]。嵌合抗原受体(car)和car效应细胞
[0201]
在一些实施方案中,人源化抗cldn18.2抗体或其片段(称为“抗cldn18.2部分”)是抗cldn18.2构建体的一部分。一些实施方案中的抗cldn18.2构建体是包含抗cldn18.2抗体部分(在本技术中也称为“抗cldn18.2car”)的嵌合抗原受体(car)。还提供了包含car的car效应细胞(例如,t细胞、nk细胞或巨噬细胞),所述car包含抗cldn18.2抗体部分。此类细胞在本技术中也称为“抗cldn18.2car效应细胞”,例如,“抗cldn18.2cart细胞”、“抗cldn18.2carnk细胞”或“抗cldn18.2car巨噬细胞”。
[0202]
一些实施方案中的抗cldn18.2car)包含a)包含与cldn18.2特异性结合的人源化抗cldn18.2抗体部分的细胞外结构域,和b)胞内信号传导结构域。跨膜结构域可以存在于胞外结构域和胞内结构域之间。
[0203]
在抗cldn18.2car的胞外结构域和跨膜结构域之间,或者在抗cldn18.2car的胞内结构域和跨膜结构域之间,可以存在间隔区结构域。间隔区结构域可以是任何寡肽或多肽,其功能是将跨膜结构域连接到多肽链中的细胞外结构域或胞内结构域。间隔区结构域可包含至多约300个氨基酸,包括例如约10个至约100个、或约25个至约50个氨基酸。
[0204]
跨膜结构域可以衍生自天然或合成来源。当来源是天然的时,结构域可以衍生自任何膜结合或跨膜蛋白。在本发明中特别使用的跨膜区可以衍生自(即至少包含下述的跨膜区)t细胞受体cd28、cd3ε、cd3ζ、cd45、cd4、cd5、cd8、cd9、cd16、cd22、cd33、cd37、cd64、
cd80、cd86、cd134、cd137或cd154的α、β、δ或γ链。在一些实施方案中,跨膜结构域可以是合成的,在这种情况下它可以主要包含疏水残基,诸如亮氨酸和缬氨酸。在一些实施方案中,苯丙氨酸、色氨酸和缬氨酸的三联体可以在合成的跨膜结构域的每一端找到。在一些实施方案中,短的寡聚(?)或长度例如在约2至约10个氨基酸之间(例如约2、3、4、5、6、7、8、9或10中的任何一个)的多肽接头可形成抗cldn18.2 car 的跨膜结构域和胞内信号传导结构域之间的连接。在一些实施方案中,接头是甘氨酸-丝氨酸双联体。
[0205]
在一些实施例中,使用与抗cldn18.2 car的胞内结构域中的序列中的一个天然相关联的跨膜结构域(例如,如果抗cldn18.2 car的胞内结构域包含4-1bb共刺激序列,那么使用抗cldn18.2 car的跨膜结构域衍生自4-1bb跨膜结构域)。
[0206]
抗cldn18.2 car的胞内信号传导结构域负责激活已放置抗 cldn18.2 car的免疫细胞的正常效应子功能的至少一种。例如,t细胞、 nk细胞或巨噬细胞的效应子功能可以是溶细胞活性或辅助活性,包括细胞因子的分泌。因此,术语“胞内信号传导结构域”是指转导效应子功能信号并指导细胞执行特定功能的蛋白质的部分。虽然通常可以使用整个胞内信号传导结构域,但在许多情况下不必使用整条链。就使用胞内信号传导结构域的截短部分而言,可使用此类截短部分代替完整链,只要其转导效应子功能信号即可。术语“胞内信号传导序列”因此意指包括足以转导效应子功能信号的胞内信号传导结构域的任何截短部分。
[0207]
用于本发明的抗cldn18.2 car的胞内信号传导结构域的实例包括:t细胞受体(tcr)和共同受体的细胞质序列,其在抗原受体接合后共同作用以启动信号转导;以及这些序列的任何衍生物或变体和具有相同功能能力的任何合成序列。
[0208]
t细胞激活可由两类不同的胞内信号传导序列介导:通过tcr 启动抗原依赖性初级激活的那些(初级信号传导序列)和以抗原非依赖性方式起作用以提供次级或共刺激信号的那些(共刺激信号传导序列)。本技术所述的抗cldn18.2 car可包含一个或两个信号传导序列。
[0209]
初级信号传导序列以刺激方式或以抑制方式调节tcr复合物的初级激活。以刺激方式起作用的初级信号传导序列可以含有信号传导基序,其被称为基于免疫受体酪氨酸的激活基序或itam。在一些实施方案中,所述抗cldn18.2 car构建体包含一种或多种itam。在本发明中特别使用的含有初级信号传导序列的itam的实例包括衍生自tcrζ、fcrγ、fcr β、cd3γ、cd3δ、cd3ε、cd5、cd22、cd79a、cd79b和cd66d的那些。
[0210]
在一些实施方案中,抗cldn18.2 car包含衍生自cd3ζ的初级信号传导序列。例如,car的胞内信号传导结构域可以包含cd3ζ胞内信号传导序列本身或与在本发明的抗cldn18.2 car的上下文中有用的任何其它期望的胞内信号传导序列组合。
[0211]
本技术描述的共刺激信号传导序列可以是共刺激分子的胞内结构域的一部分,所述共刺激分子包括,例如,cd27、cd28、4-1bb(cd137)、 ox40、cd30、cd40、pd-1、icos、淋巴细胞功能相关抗原-1(lfa-1)、 cd2、cd7、light、nkg2c、b7-h3、与cd83特异性结合的配体等。
[0212]
在一些实施方案中,抗cldn18.2 car的胞内信号传导结构域包含cd3ζ的胞内信号传导序列和cd28的胞内信号传导序列。在一些实施方案中,抗cldn18.2 car的胞内信号传导结构域包含cd3ζ的胞内信号传导序列和4-1bb的胞内信号传导序列。在一些实施方案中,抗 cldn18.2 car的胞内信号传导结构域包含cd3ζ的胞内信号传导序列和 cd28和4-1bb或
其它共刺激分子的胞内信号传导序列。
[0213]
因此,例如,在一些实施方案中,提供了抗cldn18.2 car,其包含a)包含与cldn18.2特异性结合的抗cldn18.2抗体部分的细胞外结构域(诸如人源化抗cldn18.2抗体或其片段(例如,scfv、scfv)中的任一个),b)跨膜结构域,和c)胞内信号传导结构域。在一些实施方案中,所述胞内信号传导结构域能够激活免疫细胞。在一些实施方案中,所述胞内信号传导结构域包含初级信号传导序列和共刺激信号传导序列。在一些实施方案中,所述初级信号传导序列包含cd3ζ胞内信号传导序列。在一些实施方案中,共刺激信号传导序列包含cd28和/或4-1bb胞内信号传导序列。在一些实施方案中,所述胞内结构域包含cd3ζ胞内信号传导序列和cd28和/或-1bb胞内信号传导序列。在一些实施方案中,所述胞内结构域包含cd3ζ胞内信号传导序列和cd28和/或-1bb胞内信号传导序列以及单独的细胞因子转基因,如car-诱导型白介素-12(iil-12)盒。
[0214]
本技术还提供了表达抗cldn18.2 car的效应细胞(诸如,t 细胞、nk细胞和/或巨噬细胞)。
[0215]
还提供了产生表达抗cldn18.2 car的效应细胞的方法,所述方法包含将编码抗cldn18.2 car的核酸引入效应细胞。在一些实施方案中,所述方法包含例如通过转导、转染或电穿孔将包含编码抗cldn18.2 car的核酸的载体引入效应细胞中。在一些实施方案中,所述方法包含通过病毒转导引入包含编码抗cldn18.2 car的核酸序列的载体。在一些实施方案中,所述方法包含通过转座子引入包含编码抗cldn18.2 car的核酸的载体。在一些实施方案中,所述方法包含通过crispr/cas9引入包含编码抗cldn18.2 car的核酸序列的载体。在一些实施方案中,所述方法包含,通过非病毒转移,例如质粒dna的电穿孔或体外转录的mrna (ivt-mrna)的电穿孔,引入包含编码抗cldn18.2 car的核酸序列的载体。可以使用本领域已知的任何方法将载体或mrna转导、转染或电穿孔到效应细胞中。治疗方法
[0216]
可将本技术所述的人源化抗cldn18.2抗体(或其抗原结合片段) 施用于受试者(例如哺乳动物,诸如人)以治疗或延缓涉及异常cldn18.2 活性或表达的疾病或病症的进展,所述疾病或病症包括例如实体瘤或癌症 (诸如胃癌,食管癌,胃食管交界癌,胰腺癌、胆管癌,肺癌,卵巢癌,结肠癌,肝癌,头颈癌,胆囊癌等)。在某些实施方案中,提供了本技术所述的人源化抗cldn18.2抗体(或其抗原结合片段)在制备药物的用途,所述药物用于在受试者(诸如哺乳动物,例如人)中治疗实体瘤或癌症(例如胃癌、食管癌、胃食管交界癌、胰腺癌、胆管癌、肺癌、卵巢癌、结肠癌、肝癌、头颈癌、胆囊癌等)。在某些实施方案中,提供了本技术所述的人源化抗cldn18.2抗体(或其抗原结合片段)用于在受试者(诸如哺乳动物,例如人)中治疗实体瘤或癌症(例如胃癌、食管癌、胃食管交界癌、胰腺癌、胆管癌、肺癌、卵巢癌、结肠癌、肝癌、头颈癌、胆囊癌等)的用途。在某些实施方案中,提供了包含本技术所述的人源化抗cldn18.2 抗体(或其抗原结合片段)的药物组合物用于在受试者(诸如哺乳动物,例如人)中治疗实体瘤或癌症(例如胃癌、食管癌、胃食管交界癌、胰腺癌、胆管癌、肺癌、卵巢癌、结肠癌、肝癌、头颈癌、胆囊癌等)的用途。在一些实施方案中,治疗表达cdln 18.2的肿瘤。
[0217]
在某些实施方案中,待治疗的受试者是哺乳动物(例如人、非人灵长类动物、大鼠、小鼠、母牛、马、猪、绵羊、山羊、狗、猫等)。在某些实施方式中,受试者是人。在某些实施方案
中,受试者是临床患者、临床试验志愿者、实验动物等。在某些实施例中,受试者被怀疑患有或有风险患有表达cdln 18.2的肿瘤(诸如实体瘤)或癌(例如胃癌、食管癌、胃食管交界癌、胰腺癌、胆管癌、肺癌、卵巢癌、结肠癌、肝癌、头颈癌、胆囊癌等)。在某些实施例中,受试者已被诊断为患有表达cdln 18.2的肿瘤(例如实体瘤)或癌(例如胃癌、食管癌、胃食管交界癌、胰腺癌、胆管癌、肺癌、卵巢癌、结肠癌、肝癌、头颈癌、胆囊癌等),和/或与异常 cldn18.2表达或活性相关的疾病。在某些实施方案中,施用本技术所述的人源化抗cldn18.2抗体(或其抗原结合片段)的受试者对克劳地单抗 (claudiximab)(imab362)或其生物相似药具有抗性。在某些实施方案中,施用本技术所述的人源化抗cldn18.2抗体(或其抗原结合片段)的受试者针对claudiximab(imab362)或其生物类似物已经是进展性的。在某些实施方案中,施用本技术所述的人源化抗cldn18.2抗体(或其抗原结合片段)的受试者对claudiximab(imab362)或其生物相似药具有耐性。
[0218]
对于表达cdln 18.2的肿瘤(例如实体瘤)或癌(例如胃癌、食管癌、胃食管交界癌、胰腺癌、胆管癌、肺癌、卵巢癌、结肠癌、肝癌、头颈癌、胆囊癌等)或与异常cldn18.2活性相关的其它疾病和那些疾病的临床描述是本领域已知的。这些方法包括,但不限于例如免疫组织化学、 pcr、荧光原位杂交(fish)。关于这种用于评估异常cldn18.2活性或表达的诊断方法的其它细节描述于,例如,gupta et al.(2009)mod pathol.22(1): 128-133;lopez-rios et al.(2013)j clin pathol.66(5):381-385;ellison etal.(2013)j clin pathol 66(2):79-89;和guha et al.(2013)plos one 8(6): e67782。
[0219]
本技术所述的人源化抗cldn18.2抗体(或其抗原结合片段)可以使用任何合适的途径施用,包括例如静脉内、肌内或皮下。在一些实施方案中,本技术提供的人源化抗cldn18.2抗体(或其抗原结合片段)与第二、第三或第四试剂(包括例如抗肿瘤剂、生长抑制剂、细胞毒性剂或化疗剂)组合施用以治疗与异常cldn18.2活性相关的疾病或病症。这类药剂包括但不限于例如多西他赛、吉非替尼、folfiri(伊立替康、5-氟尿嘧啶和亚叶酸)、伊立替康、顺铂、卡铂、紫杉醇、贝伐单抗(bevacizumab) (抗vegf抗体)、folfox-4(输注氟尿嘧啶、亚叶酸和奥沙利铂、阿法替尼、吉西他滨、卡培他滨、培美曲塞、伐替尼、依维莫司、cpg-odn、雷帕霉素、来那度胺、维罗非尼、内皮抑素、拉帕替尼、px-866、imprimepgg和伊洛替尼(irlotinibm))。在一些实施方案中,本技术提供的人源化抗cldn18.2抗体(或其抗原结合片段)与抗肿瘤剂、生长抑制剂、细胞毒性剂或化疗剂缀合。
[0220]
在某些实施方案中,本技术提供的人源化抗cldn18.2抗体(或其抗原结合片段)与一种或多种另外的疗法例(诸如放射疗法、手术、化学疗法和/或靶向疗法)组合施用。在某些实施方案中,本技术提供的人源化抗cldn18.2抗体(或其抗原结合片段)与化学疗法联合施用。在某些实施例中,该化学疗法包含eox(即,表柔比星、奥沙利铂和卡培他滨)。在某些实施方案中,化疗包含唑来膦酸和白介素-2。
[0221]
取决于待治疗的适应症和与本领域技术人员熟悉的剂量相关的因素,本技术提供的抗体将以有效治疗该适应症同时使毒副作用最小化的剂量施用。对于表达cdln 18.2的肿瘤(例如实体瘤)或癌(例如胃癌、食管癌、胃食管交界癌、胰腺癌、胆管癌、肺癌、卵巢癌、结肠癌、肝癌、头颈癌、胆囊癌等)的治疗,典型的剂量可以是例如:0.001-1000μg的范围;然而,低于或高于该示例性范围的剂量在本技术所述的治疗方法的范围内。该剂量可以是约0.1μg/kg至约100mg/kg总体重(例如,约5μg/kg、约10μg/kg、约100μg/kg、约500μg/kg、约
1mg/kg、约50mg/kg或由前述值中的任何两个限定的范围,包括前述值之间的任何范围)。在一些实施方案中,典型剂量可以是,例如,在10mg/m2和1500mg/m2之间;然而,低于或高于该示例性范围的剂量在本技术所述的治疗方法的范围内。剂量可以是约25mg/m2至约1000mg/m2(例如,约25mg/m2、约100mg/m2、约250mg/m2、约500mg/m2、约750mg/m2或由前述值中的任何两个限定的范围,包括前述值之间的任何范围)。在一些实施方案中,剂量为约300 mg/m2、600mg/m2、800mg/m2或1000mg/m2中的任一个。
[0222]
本技术提供的人源化抗cldn18.2抗体(或其抗原结合片段)可以以单次日剂量施用,或总日剂量可以以每日两、三或四次的分剂量施用。或者,人源化抗cldn18.2抗体(或其抗原结合片段)可以低于每天的频率施用,例如每周六次、每周五次、每周四次、每周三次、每周两次、每周一次、每两周一次、每三周一次、每四周一次、每月一次、每两月一次、每三月一次、或每六月一次。
[0223]
在一些实施方案中,在第一周期期间以800mg/m2的剂量施用一次本技术提供的人源化抗cldn18.2抗体(或其抗原结合片段),之后每三周或之后21天以600mg/m2的剂量施用一次。在一些实施方案中,本技术提供的人源化抗cldn18.2抗体(或其抗原结合片段)以1000mg/m2的剂量每三周或21天施用一次。在一些实施方案中,在周期1的第1天以800 mg/m2的剂量施用本技术提供的人源化抗cldn18.2抗体(或其抗原结合片段),之后在每隔一个后续周期的第1天以600mg/m2的剂量施用。
[0224]
治疗或预防功效可以通过对接受治疗的受试者进行定期评估来监测。对于几天或更长时间的重复给药,根据情况,重复治疗直至出现期望的疾病症状抑制。然而,其他剂量方案可能是有用的并且在本发明的范围内。期望剂量可通过单次推注施用本技术提供的人源化抗cldn18.2抗体(或其抗原结合片段)、通过多次推注施用本技术提供的人源化抗 cldn18.2抗体(或其抗原结合片段)、或通过连续输注施用本技术提供的人源化抗cldn18.2抗体(或其抗原结合片段)来递送。
[0225]
可通过例如但不限于以下评价癌症治疗:肿瘤消退、肿瘤重量或尺寸缩小、进展时间、缓解率、生存期、无进展存活、总应答率、总存活、应答持续时间、疾病控制率、临床受益率、生活质量、cldn18.2表达的量或水平、和/或cldn18.2活性的水平。可以使用确定疗效的途径,包括例如通过例如recist(实体瘤疗效评价评估)标准的反应测量(参见例如, eisenhauer et al.(2009)“new response evaluation in solid tumors:revisedrecist guideline(version 1.1).”eur j.cancer.45:228-247)。抗cldn18.2 car效应细胞疗法
[0226]
本发明还提供了在个体中刺激对包含cldn18.2呈递细胞的靶细胞群或组织的效应细胞介导的应答(诸如t细胞、nk细胞或巨噬细胞介导的免疫应答)的方法,包含向个体施用表达抗cldn18.2 car的效应细胞(诸如t细胞)的步骤。在一些实施方案中,所述个体是人类个体。
[0227]
可将表达抗cldn18.2 car的抗cldn18.2 car效应细胞(诸如t细胞、nk细胞和/或巨噬细胞)输注至有需要的接受者。在一些实施方案中,抗cldn18.2 car效应细胞(诸如t细胞、nk细胞和/或巨噬细胞)能够在体内复制,导致可导致持续肿瘤控制的长期持久性。在一些实施方案中,抗cldn18.2 car效应细胞可经历稳健的体内t细胞扩增并持续延长的时间量。在一些实施方案中,本发明的抗cldn18.2 car t细胞发育成特异性记忆t细胞,其可被
1bb胞内信号传导序列的胞内信号传导结构域。在一些实施方案中,所述个体对cldn18.2呈阳性。在一些实施方案中,与患者群体中的中等水平相比,所述个体表达高水平的clnd18.2。在一些实施方案中,所述施用经由静脉内、腹膜内或肿瘤内途径。在一些实施方案中,所述施用经由静脉内途径。在一些实施方案中,所述施用经由瘤内途径。在一些实施方案中,所述个体是人。
[0234]
在一些实施方案中,提供了在个体中引发t细胞的方法,包含向所述个体施用有效量的组合物,所述组合物包含表达根据上述任一种抗 cldn18.2 car的抗-cldn18.2 car效应细胞(诸如t细胞)。在一些实施方案中,个体患有癌症。在一些实施方案中,所述施用经由静脉内、腹膜内或肿瘤内途径。在一些实施方案中,所述施用经由静脉内途径。在一些实施方案中,所述施用经由瘤内途径。在一些实施方案中,所述个体是人。药物制剂
[0235]
本技术提供的人源化抗cldn18.2抗体(或其片段)可以与药学上可接受的载体或赋形剂一起配制,使得它们适于向有需要的受试者(例如,哺乳动物,诸如人)施用。通过将具有期望纯度的抗体(或其片段) 与任选的药学上可接受的载体、赋形剂或稳定剂(remington's pharmaceutical sciences 16th edition,osol,a.ed.(1980))混合来获得合适的抗体制剂,以冻干制剂或水溶液的形式。药学上可接受的载体、赋形剂或稳定剂在所采用的剂量和浓度下对接受者是无毒的,并且包括:缓冲剂,诸如磷酸盐、柠檬酸盐和其他有机酸;抗氧化剂,包括抗坏血酸和甲硫氨酸;防腐剂(诸如十八烷基二甲基苄基氯化铵;氯化六甲氧铵;苯扎氯铵、苄索氯铵;苯酚,丁醇或苯甲醇;对羟基苯甲酸烷基酯,诸如羟基苯甲酸甲酯或对羟基苯甲酸丙酯;儿茶酚;间苯二酚;环己醇;3-戊醇;和间甲酚);低分子量(少于约10个残基)多肽;蛋白质,诸如血清白蛋白、明胶或免疫球蛋白;亲水性聚合物,诸如聚乙烯吡咯烷酮;氨基酸,诸如甘氨酸,谷氨酰胺,天冬酰胺,组氨酸,精氨酸或赖氨酸;单糖、二糖和其它碳水化合物,包括葡萄糖、甘露糖或糊精;螯合剂,诸如edta;糖,诸如蔗糖、甘露醇、海藻糖或山梨糖醇;成盐抗衡离子,诸如钠;金属配合物(例如锌-蛋白复合物;和/或非离子表面活性剂,例如,或tween
tm
、 pluronics
tm
或聚乙二醇(peg)。
[0236]
本技术公开的抗体也可以配制成免疫脂质体。含有所述抗体的脂质体通过本领域已知的方法制备,诸如描述于epstein et al.,pnas usa,82: 3688(1985);hwang et al.,pnas usa,77:4030(1980);和美国专利 no.4,485,045或4,544,545。美国专利no.5,013,556公开了循环时间延长的脂质体。
[0237]
特别有用的脂质体可以通过反相蒸发方法用包含磷脂酰胆碱、胆固醇和peg衍生的磷脂酰乙醇胺(peg-pe)的脂质组合物产生。脂质体通过限定孔径的滤器挤出以产生具有期望直径的脂质体。如martinet al.,j. biol.chem.,257:286-288(1982)中所述,本发明抗体的fab'片段可以经由二硫化物交换反应与脂质体缀合。脂质体内任选还包含抗肿瘤剂、生长抑制剂或化疗剂(诸如多柔比星)。参见gabizon et al.,j.national cancer inst., 81(19):1484(1989)。
[0238]
包含本技术所述的人源化抗cldn18.2抗体的药物制剂还可以含有一种以上的活性化合物,这对于所治疗的特定适应症是必需的,优选那些具有互补活性但不会彼此不利影响的活性化合物。例如,可能需要提供除本技术所述的人源化抗cldn18.2抗体之外的抗肿瘤剂、生长抑制剂、细胞毒性剂或化疗剂。这类分子合适地以对预期目的有效的量而组合
存在。此类其它试剂的有效量取决于制剂中存在的抗体的量、疾病或病症或治疗的类型和上文讨论的其它因素。此类其它试剂的有效量取决于制剂中存在的抗体的量、疾病或病症或治疗的类型和上文讨论的其它因素。这些通常以与本技术所述相同的剂量和施用途径使用,或为迄今使用的剂量的约1 至99%。
[0239]
在一些实施方案中,本技术的抗体是冻干的。这样的冻干制剂可以用合适的稀释剂重构为高蛋白浓度,并且重构的制剂可以施用于哺乳动物(诸如人)。
[0240]
在某些实施方案中,用于体内施用的药物制剂是无菌的。这可通过(例如)通过无菌过滤膜过滤包含本技术所述的人源化抗cldn18.2抗体的溶液而容易地实现。使用抗claudin 18.2抗体的诊断和成像方法
[0241]
与cldn18.2多肽特异性结合的经标记的人源化抗cldn18.2抗体、其片段及其衍生物和类似物可用于诊断目的以检测、诊断或监测与 cldn18.2的表达、异常表达和/或活性相关的疾病和/或病症。例如,本技术提供的人源化抗cldn18.2抗体(或其片段)可用于原位、体内、离体和体外诊断测定或成像测定。用于检测cldn18.2多肽的表达的方法,其包含(a)使用一种或多种本发明的抗体测定所述多肽在个体的细胞(例如组织)或体液中的表达,和(b)将基因表达水平与标准基因表达水平进行比较,其中与标准表达水平相比,所测定的基因表达水平的增加或降低指示异常表达。这样的测定可以在体内或离体(例如使用从患者获得的样品) 进行。
[0242]
本技术还提供了诊断与动物(例如,哺乳动物,诸如人类)中的 cldn18.2的表达或异常表达相关的疾病或病症的方法。在一些实施方案中,所述方法包含检测哺乳动物中的cldn18.2多肽。在某些实施方案中,诊断包含:(a)向哺乳动物施用有效量的标记的人源化抗cldn18.2抗体(或其片段);(b)等待施用步骤后的时间间隔,以允许标记的人源化抗 cldn18.2抗体(或其片段)优先在受试者中表达cldn18.2的位点浓缩(和 /或对于未结合的标记分子,以清除至背景水平);(d)检测受试者中标记的人源化抗cldn18.2抗体的量或水平;和(e)将受试者中标记的人源化抗cldn18.2抗体的量或水平与健康对照受试者中的人源化抗cldn18.2 抗体的水平或量进行比较。如果受试者中标记的人源化抗cldn18.2抗体的量或水平超过健康对照受试者中人源化抗cldn18.2抗体的量或水平,则这可以指示受试者具有与cldn18.2的表达或异常表达相关的疾病或病症。
[0243]
使用本领域技术人员已知的经典免疫组织学方法,本技术提供的人源化抗cldn18.2抗体(或其片段)可用于分析生物样品中cldn18.2的量或水平(例如参见jalkanen,et al.,j.cell.biol.101:976-985(1985); jalkanen,et al.,j.cell.biol.105:3087-3096(1987))。用于检测cldn18.2表达的其它基于抗体的方法包括免疫测定,诸如酶联免疫吸附测定(elisa) 和放射免疫测定(ria)。合适的抗体测定标记是本领域已知的,并且包括酶标记,诸如葡萄糖氧化酶;放射性同位素,例如碘(
131
i、
125
i、
123
i、
121
i), 碳(
14
c),硫(
35
s),氚(3h),铟(
115m
in、
113m
in、
112
in、
111
in)和锝(
99
tc、
99m
tc),铊(
201
ti),镓(
68
ga、
67
ga),钯(
103
pd),钼(
99
mo),氙(
133
xe),氟 (
18
f),
153
sm、
177
lu、
159
gd、
149
pm、
140
la、
175
yb、
166
ho、
90
y、
47
sc、
186 re、
188
re、
142
pr、
105
rh、
97
ru;鲁米诺(luminol);荧光标记,诸如荧光素、罗丹明和生物素。
[0244]
本领域已知的技术可应用于本技术提供的标记抗体(或其片段)。这类技术包括但不限于使用双官能缀合剂(参见例如,美国专利 no.5,756,065;5,714,631;5,696,239;5,
652,361;5,505,931;5,489,425; 5,435,990;5,428,139;5,342,604;5,274,119;4,994,560;和5,808,003)。
[0245]
在一些实施方案中,通过确定诸如血清的生物体液中脱落的抗原的量来测量cldn18.2过表达,例如通过使用基于抗体的测定法(还参见例如1990年6月12日公布的美国专利no.4,933,294;1991年4月18日公开的w091/05264;1995年3月28日公布的美国专利5,401,638;和sias etal.,j.immunol.methods 132:73-80(1990))。除了上述测定法之外,本领域技术人员可以获得各种体内和离体测定法。例如,可以将哺乳动物体内的细胞暴露于抗体,所述抗体任选地用可检测标记物(例如放射性同位素) 标记,并且可以例如通过体外扫描放射性或通过分析取自先前暴露于抗体的哺乳动物的样品(例如活组织检查或其他生物样品)来评估抗体的结合。car效应细胞制备
[0246]
在一个方面,本发明提供表达抗cldn18.2 car的效应细胞(诸如t细胞、nk细胞和/或巨噬细胞)。本技术提供了制备表达抗cldn18.2 car的效应细胞(诸如t细胞、nk细胞和/或巨噬细胞)(抗cldn18.2 car 效应细胞,诸如抗cldn18.2 car t细胞、抗cldn18.2 car nk细胞和/ 或抗cldn18.2 car巨噬细胞)的示例性方法。
[0247]
在一些实施方案中,抗cldn18.2 car效应细胞(诸如t细胞、 nk细胞或巨噬细胞)可通过将包含抗cldn18.2 car(例如下述一种car, 其包含抗cldn18.2抗体部分、4-1bb共刺激序列和cd3ζ初级信号传导序列或其它序列,诸如能够延长car细胞存活的il-2、il15或能够消除 car细胞的序列)的载体(包括例如慢病毒载体)引入效应细胞(诸如t 细胞、nk细胞或巨噬细胞)来产生。在一些实施例中,本发明的抗cldn18.2 car效应细胞(诸如t细胞、nk细胞和/或巨噬细胞)能够在体内复制。在一些实施方案中,抗cldn18.2 car效应细胞(诸如t细胞,nk细胞或巨噬细胞)可通过将编码抗cldn18.2 car(诸如包含抗cldn18.2抗体部分、4-1bb共刺激序列和cd3ζ初级信号传导序列的car)的mrna 引入效应细胞(诸如t细胞、nk细胞和/或巨噬细胞活动。
[0248]
本发明的抗cldn18.2 car t细胞可以经历稳健的体内t细胞扩增并且可以建立在血液和骨髓中以高水平持续延长的时间量的 cldn18.2特异性记忆细胞。在一些实施方案中,注入患者的本发明的抗 cldn18.2 car t细胞可以在患有疾病(例如以高cldn18.2表达为特征的疾病)的患者体内消除cldn18.2-呈递细胞,诸如cldn18.2-呈递癌细胞。
[0249]
在t细胞、nk细胞或巨噬细胞的扩增和遗传修饰之前,从受试者获得t细胞、nk细胞或巨噬细胞的来源。例如,t细胞可以从许多来源获得,包括外周血单核细胞、骨髓、淋巴结组织、脐带血、胸腺组织、来自感染部位的组织、腹水、胸腔积液、脾组织和肿瘤。在本发明的一些实施方案中,可以使用本领域可获得的任何数量的t细胞、nk细胞和/或巨噬细胞系。在本发明的一些实施方案中,可以使用本领域技术人员已知的任何数量的技术,例如ficoll
tm
分离,从收集自受试者的血液单位获得t细胞。在一些实施方案中,通过单采血液成分术获得来自个体的循环血液的细胞。单采血液成分术产物通常含有淋巴细胞,包括t细胞、单核细胞、粒细胞、b细胞,其它有核白细胞、红细胞和血小板。在一些实施方案中,可以洗涤通过单采血液成分术收集的细胞以除去血浆部分并将细胞置于合适的缓冲液或培养基中以用于随后的处理步骤。在一些实施方案中,用磷酸盐缓冲盐水 (pbs)洗涤细胞。在一些实施方案中,洗涤溶液缺乏钙并且可能缺乏镁或可能缺乏许多(如果不是全部的话)二价阳离子。
如本领域普通技术人员将容易理解的,洗涤步骤可以通过本领域技术人员已知的方法完成,例如根据制造商的说明书通过使用半自动“流通式”离心机(例如cobe 2991 细胞处理器、baxter细胞器或haemonetics cell saver 5)进行。洗涤后,可以将细胞重悬于各种生物相容性缓冲液中,诸如不含ca
2+
、不含mg
2+
的pbs、 plasmalyte a或其它含或不含缓冲液的盐水溶液。或者,可除去单采血液成分术样品中不需要的成分,并将细胞直接重悬于培养基中。
[0250]
在一些实施方案中,通过裂解红细胞并耗竭单核细胞,例如,通过percoll
tm
密度梯度离心或通过逆流离心淘析,从外周血淋巴细胞分离t 细胞。可以通过阳性或阴性选择技术进一步分离t细胞的特定亚群,诸如 cd3
+
、cd28
+
、cd4+、cd8
+
、cd45ra
+
和cd45ro
+
t细胞。可以使用多轮选择。
[0251]
通过负选择富集t细胞群可以用针对负选择细胞所特有的表面标志物的抗体的组合来实现。一种方法是通过负磁性免疫粘附或流式细胞术进行细胞分选和/或选择,所述负磁性免疫粘附或流式细胞术使用针对负选择的细胞上存在的细胞表面标志物的单克隆抗体的混合物。制品和试剂盒
[0252]
提供了包含用于治疗表达cdln 18.2的肿瘤(诸如实体瘤)或癌(例如胃癌、食管癌、胃食管交界癌、胰腺癌、胆管癌、肺癌、卵巢癌、结肠癌、肝癌、头颈癌、胆囊癌等)的材料的制品。
[0253]
在某些实施方案中,所述制品或试剂盒包含含有一种或多种本技术所述的人源化抗cldn18.2抗体或组合物的容器。在某些实施方案中,制品或试剂盒包括含有编码一种(或多种)本技术所述的人源化抗cldn18.2 抗体或组合物的核酸的容器。在一些实施方案中,试剂盒包括产生如本技术所述的抗cldn18.2抗体的细胞系的细胞。在一些实施方案中,试剂盒包括一种或多种阳性对照,例如cldn18.2(或其片段)或cldn18.2
+
细胞。在一些实施方案中,试剂盒包括阴性对照,例如基本上不含cldn18.2的表面或溶液。
[0254]
在某些实施方案中,制品或试剂盒包括容器和在容器上或与容器相关的标签或包装插页。合适的容器包括例如瓶、小瓶、注射器、iv溶液袋等。这些容器可以由多种材料形成,诸如玻璃或塑料。该容器容纳一种组合物,该组合物单独的或与有效治疗、预防和/或诊断表达cdln 18.2的肿瘤(诸如实体瘤)或癌(例如胃癌、食管癌、胃食管交界癌、胰腺癌、胆管癌、肺癌、卵巢癌、结肠癌、肝癌、头颈癌、胆囊癌等)的另一种组合物组合,并且可以具有无菌进入端口(例如容器可以是静脉内溶液袋或具有可由皮下注射针刺穿的塞子的小瓶)。组合物中的至少一种试剂是本技术所述的人源化抗cldn18.2抗体。标签或包装插页表明该组合物用于治疗表达cdln 18.2的肿瘤(诸如实体瘤)或癌(例如胃癌、食管癌、胃食管交界癌、胰腺癌、胆管癌、肺癌、卵巢癌、结肠癌、肝癌、头颈癌、胆囊癌等)。
[0255]
此外,所述制品或试剂盒可包含(a)其中含有组合物的第一容器,其中所述组合物包含本技术所述的人源化抗cldn18.2抗体;和(b) 其中含有组合物的第二容器,其中所述组合物包含另外的细胞毒性剂或其它治疗剂。在一些实施方案中,所述治疗剂是免疫治疗剂,如本技术所述。另外,所述制品还可包含另外的容器,所述容器包含药学上可接受的缓冲液,诸如抑菌注射用水(bwfi)、磷酸盐缓冲盐水、林格氏(ringer)溶液和右旋糖溶液。它可以进一步包括从商业和使用者的观点所期望的其他材料,包括其他缓冲剂、稀释剂、过滤
器、针和注射器。
[0256]
应理解,任何上述制品或试剂盒可包括本技术所述的免疫缀合物代替人源化抗cldn18.2抗体(或除人源化抗cldn18.2抗体外,还包括本技术所述的免疫缀合物)。
[0257]
还提供了可用于各种目的的试剂盒,例如任选地与制品组合用于分离或检测患者中的cldn18.2。对于cldn18.2的分离和纯化,试剂盒可以含有本技术提供的与珠粒(例如琼脂糖珠粒)偶联的人源化抗cldn18.2抗体(或其片段)。可以提供试剂盒,其包含用于在体外例如在elisa或蛋白质印迹中检测和定量cldn18.2的抗体(或其片段)。就像该制品一样,试剂盒包含容器和在容器上或与容器相关的标签或包装插页。例如,所述容器容纳包含至少一种本技术提供的人源化抗cldn18.2抗体的组合物。可以包括另外的容器,其例如包含稀释剂和缓冲液、对照抗体。标签或包装插页可提供组合物的描述以及用于预期体外或诊断用途的说明书。实施例
[0258]
通过参考以下实施例将更全面地理解本技术。然而,这些实施例不应被解释为限制本技术的范围。应理解,本技术所述的实施例和实施方案仅用于说明目的,并且根据其的各种修改或变化将被建议给本领域技术人员,并且将包括在本技术的精神和范围以及所附权利要求的范围内。实施例1:鼠抗人cldn18.2抗体的人源化cdr移植抗体可变区序列的设计
[0259]
使用两种不同的途径,即基于结构的途径和基于序列同源性的途径,来使鼠抗人cldn18.2抗体人源化。
[0260]
在基于结构的途径中,使用suite生成鼠抗人cldn18.2抗体的cdr环结构模型,并且然后使用所建模的鼠cdr环搜索人抗体的晶体结构数据库(可从获得)。然后选择来自最接近匹配的人抗体结构的框架作为鼠cdr移植的受体框架。
[0261]
在基于序列同源性的途径中,针对imgt人抗体种系基因数据库(即国际免疫遗传学信息系统在www(dot)imgt(dot)org上可获得),使用imgt的domaingapalign程序(在www(dot)imgt(dot)org/3dstructure-db/cgi/domaingapalign(dot)cgi上可获得),分别对鼠重链和轻链序列的可变区进行序列同源性检索。选择最接近匹配的人抗体种系基因作为鼠cdr移植的受体框架。人源化回复突变重链和轻链变体的设计
[0262]
在将鼠cdr移植到所选择的人种系基因框架上之后(如上文所述),将人源化框架的氨基酸序列与鼠框架序列进行比较。如padlanea(1994)molimmunol.31(3)169-217andfooteandwinter(1992)j.mol.biol.224:487-499中所述,将以前显示在cdr-框架相互作用和重链-轻链相互作用中起作用的人源化框架中的关键残基被靶向回复为鼠残基突变以保持人源化抗体对hcldn18.2的亲和力。通过改变回复突变的数目和被鉴定为对于恢复原始鼠抗体的抗原结合亲和力可能关键的回复突变残基的位置,设计了一系列重链和轻链变体。参见下表a、b、c和d。表a.全鼠和全人可变区的非cdr序列。
表b.人源化回复突变轻链(lc)可变区的非cdr序列
粗体和下划线氨基酸表示鼠序列的回复突变表c.人源化回复突变重链(hc)可变区的非cdr序列
粗体和下划线氨基酸表示向鼠序列的回复突变表d.人源化回复突变cldn18.2抗体轻链变体和重链变体的可变区的氨基酸序列*
*cdr序列为粗体并带有下划线cdr移植和回复突变变体的构建:
[0263]
如以上表d所示,设计了总共4个轻链变体和7个重链变体。它们的dna序列合成、克隆并表达为人igg1,用于结合亲和力表征。这 4个轻链和7个重链变体的完整交叉配对产生了28个重链/轻链组合,即hucldn18.2-v.1至v.28。参见表e:表e.重/轻链组合和变体版本id
实施例2:hucldn18.2抗体的质粒构建,表达和纯化
[0264]
合成编码表d所示vh和vk变体的dna片段。编码vh结构域的 dna片段分别与人igg1恒定区符合读框地克隆到pcdna3.4中,编码vk 结构域的dna片段分别与人ig kappa恒定区符合读框地克隆到pcdna3.4 中。将编码重链和轻链dna的质粒使用expifectamine
tm 293(thermofisher scientific)转染试剂转染(转染的hc:lc质粒=1:1)至6孔板中的2 ml expi293f中。转染20小时后将expifectamine
tm 293转染增强子1 和2加入孔中。于37℃、在提供有5%co2的75%湿度的潮湿孵育箱中孵育培养物。转染后6天,通过在4℃、13,200rpm离心20分钟来收获转染的培养物。使用蛋白质a hp spintrap
tm
柱(ge healthcare)通过将上清液和树脂在室温下孵育4分钟来纯化hucldn18.2抗体。该柱用ph 7.2的磷酸钠缓冲液洗涤,然后用ph 2.9的100mm甘氨酸-hcl洗脱。洗脱液用 ph 9.0的1.0m tris-hcl中和。纯化的抗体在ph 7.2的pbs缓冲液中透析,并通过0.2μm膜无菌过滤。表f中总结了来自2ml培养物的hucldn18.2-v.1-hucldn18.2-v.20的每一个的纯化收率。表g总结了来自2ml培养物的hucldn18.2-v.21-hucldn18.2-v.28的每一个的纯化收率。hucldn18.2-v.3、hucldn18.2-v.4、hucldn18.2-v.5、 hucldn18.2-v.21和hucldn18.2-v.25不表达。抗体的sds-page分析,如图1a-1f所示,证明所有hucldn18.2抗体(除了hucldn18.2-v.3、 hucldn18.2-v.4、hucldn18.2-v.5、hucldn18.2-v.21和 hucldn18.2-v.25)都纯化至接近90%的纯度。表f.2ml expi293f培养物中hucldn18.2-v.1-hucldn18.2-v.20 的纯化收率
*hucldn18.2-v.7在用ph 2.9的100mm甘氨酸-hcl洗脱以及透析过程后在用ph 9.0的1m tris-hcl中和的步骤中沉淀。因此,未回收 hucldn18.2-v.7抗体。表g.2ml expi293f培养物中hucldn18.2-v.21-hucldn18.2-v.28 的纯化收率抗体纯化收率hucldn18.2-v.21无表达hucldn18.2-v.22193μg
hucldn18.2-v.23190μghucldn18.2-v.24256μghucldn18.2-v.25无表达hucldn18.2-v.26189μghucldn18.2-v.27188μghucldn18.2-v.28181μg实施例3a.流式细胞术分析hucldn18.2抗体与表达cldn18.2的细胞的结合
[0265]
使用hek293-cldn18.2细胞(即,表达人cldn18.2的稳定的 hek293细胞系)和kato-iii(htb-103
tm
)(即cldn18.2
+
人胃癌细胞系)经由facs评估图1a-1d所示的纯化的hucldn18.2抗体与细胞表面表达的人cldn18.2的相互作用。facs试验按如下进行:制备每种抗体的系列稀释液,在冰上用hek293-cldn18.2或kato-iii细胞染色一小时,抗体终浓度为20μg/ml、10μg/ml、5μg/ml、2.5μg/ml、1.25μg/ml、 0.63μg/ml、0.31μg/ml、0.16μg/ml、0.08μg/ml、0.04μg/ml、0.02μg/ml 和0.01μg/ml。用染色缓冲液(pbs+2%胎牛血清)洗涤细胞以除去游离抗体,并进一步用alexa fluor(荧光染料缀合的抗人igg抗体) 在冰上染色30分钟。洗涤细胞并通过facs分析。人源化抗体的结合曲线和ec
50
值总结在图2a-2b和图3中。
[0266]
如图2a和2b所示,在使用hek293-cldn18.2细胞、 hucldn18.2-v.1、v.2、v.11、v.14、v.15、v.16、v.19和v.20的试验中,证明了与自制嵌合抗cldn18.2抗体和参照抗cldn18.2抗体imab362相当的ec
50
值。还测试了人源化抗体与kato iii细胞的结合。如图3中所示,发现hucldn18.2-v.14、v.15、v.19和v.20的ec
50
值和最大结合值与自制嵌合抗cldn18.2抗体相当。此外,发现hucldn18.2-v.1、v.2、v.11和v.16 的ec
50
值和最大结合值与参照抗cldn18.2抗体imab362的那些相当。实施例3b.流式细胞术分析hucldn18.2抗体与表达cldn18.2的细胞的结合
[0267]
使用hek293-cldn18.2细胞(即,表达人cldn18.2的稳定的 hek293细胞系)和kato-iii(htb-103
tm
)(即cldn18.2
+
人胃癌细胞系)经由facs评估图1e-1f所示的纯化的hucldn18.2抗体与细胞表面表达的人cldn18.2的相互作用。facs试验按如下进行:制备每种抗体的系列稀释液,在冰上用hek293-cldn18.2或kato-iii细胞染色一小时,抗体终浓度为20μg/ml、10μg/ml、5μg/ml、2.5μg/ml、1.25μg/ml、0.63 μg/ml、0.31μg/ml、0.16μg/ml、0.08μg/ml、0.04μg/ml、0.02μg/ml和0.01 μg/ml。用染色缓冲液(pbs+2%胎牛血清)洗涤细胞以除去游离抗体,并进一步用alexa fluor(荧光染料缀合的抗人igg抗体)在冰上染色30分钟。洗涤细胞并通过facs分析。人源化抗体的结合曲线和ec
50
值总结在图4和图5中。
[0268]
如图4中所示,在使用hek293-cldn18.2细胞、 hucldn18.2-v.23、v.24、v.27和v.28的试验中,显示了与自制嵌合抗 cldn18.2抗体和参照抗cldn18.2抗体imab362相当的ec
50
值。还测试了人源化抗体与kato iii细胞的结合。如图5中所示,发现 hucldn18.2-v.23、v.24、v.27和v.28的ec
50
值和最大结合值与自制嵌合抗 cldn18.2抗体相当。实施例4:hucldn18.2抗体的结合特异性
[0269]
使用hek293-cldn18.1细胞(即表达人cldn18.1的稳定的 hek293细胞系)经由facs评估图1a-1f中所示的纯化的hucldn18.2 抗体与细胞表面表达的人cldn18.1的结合。
还使用hek293-cldn18.2细胞(即表达人cldn18.2的稳定的hek293细胞系)作为对照,经由facs评估图1a-1f中所示的纯化的hucldn18.2抗体与细胞表面表达的人cldn18.2的结合。facs试验按如下进行:制备20μg/ml的每一种hucldn18.2抗体并在冰上用hek293-cldn18.2或hek293-cldn18.1细胞染色一小时。用染色缓冲液(pbs+2%胎牛血清)洗涤细胞以除去游离抗体,并进一步用alexafluor(荧光染料缀合的抗人igg抗体)在冰上染色30分钟。洗涤细胞并通过facs分析。人源化抗体的结合总结在图6中。
[0270]
如图6中所示,未检测到hucldn18.2抗体与hek293-cldn18.1细胞结合。因此,所有hucldn18.2抗体均显示对hek293-cldn18.2的特异性结合。实施例5:评估抗cldn18.2抗体与imab362特异性肽的结合
[0271]
imab362(也称为zolbetuximab或claudiximab)是对cldn18.2有特异性的嵌合igg1抗体。预先通过噬菌体展示开发了两种小环化肽(即,肽2c和肽3c),然后经由肽微阵列技术优化以结合imab362,用于通过elisa在临床组织样品中检测血清imab362(参见daneschdaretal.(2014)jptpeptidetechnologies,volmerstrasse5,12489)。daneschdar和同事们通过elisa显示imab362以亚纳摩尔亲和力与肽2c和肽3c结合。通过elisa评估图1a-1f中所示的抗体和参考抗体imab362结合肽2c和肽3c的能力。
[0272]
如图7a和图7b所示,仅发现参考抗体imab362结合肽2c和3c。相反,没有发现测试的hucldn18.2抗体可检测地结合任一肽。这些结果表明,所有hucldn18.2抗体与cldn18.2的表位结合、与imab362结合的表位不同。实施例6:评价fc突变对hucldn18.2-v.19的adcc活性的影响
[0273]
hucldn18.2-v.19的fc结构域是野生型人igg1。对包含hucldn18.2-v.19可变结构域和以下所列的变体fc结构域之一的氨基酸序列的抗体进行构建、表达和纯化。每个fc变体结构域中的突变用粗体和下划线表示。fc结构域变体1:astkgpsvfplapsskstsggtaalgclvkdyfpepvtvswnsgaltsgvhtfpavlqssglyslssvvtvpssslgtqtyicnvnhkpsntkvdkkvepkscdkthtcppcpapellggpdvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalplpeektiskakgqprepqvytlppsrdeltknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspg(seqidno:109)fc结构域变体2:
fc结构域变体3:fc结构域变体3:
[0274]
如下制备用于adcc测定的试剂:将纯化的抗体在adcc测定培养基(99.5%rpmi 1640+0.5%fbs)中稀释至20μg/ml的浓度。进行5 倍连续稀释以产生10种另外的工作液(即,4μg/ml、0.8μg/ml、160ng/ml、32ng/ml、6.4ng/ml、1.28ng/ml、256pg/ml、51.2pg/ml、10.24pg/ml和2.048 pg/ml用于adcc测定。分别培养adcc效应细胞(adcc fcγriiia(158v) jurkat效应细胞系克隆,genomeditech,cat#gm-c01620)和靶细胞 (kato-iii-hclaudin18.2细胞系,由beijing xuanyi pharmatech公司开发),直到adcc效应细胞和靶细胞的细胞密度达到1.2
×
106/ml。两种培养物的细胞活力均大于90%。将效应细胞培养物和靶细胞培养物以1000 rpm离心5分钟。弃去上清液,然后将效应细胞和靶细胞各自重悬于adcc 测定培养基中至终密度为6.0
×
106/ml(效应细胞)和4.0
×
105/ml(靶细胞)。
[0275]
为了准备测定,将25μl每种hucldn18.2-v.19抗体变体的每种工作溶液加入到微量滴定盘的单独孔中。接着,向各孔中依次加入25μl 靶细胞和25μl效应细胞。效应细胞与靶细胞的比例为15:1。在单独的孔中平行制备以下对照:(1)75μl的adcc测定培养基(背景对照);和(2) 25μl的adcc测定培养基,25μl效应细胞和25μl靶细胞(阴性对照)。在向含有hucldn18.2-v.19抗体变体的各孔中添加效应细胞和靶细胞后,将微量滴定板于37℃和5%co2下孵育6小时。孵育后,将微量滴定板冷却至室温15分钟。接着,向各孔中加入75μl bio-glo
tm
荧光素酶试剂 (promega catalog#g7940),并将微量滴定板在室温下孵育5分钟。每个孔中产生的信号由spectra max 微板读数器读取。发光值由 spectra max微板读数器以全长波读取模型获得。对于相对发光单位(rlu)分析,将发光值直接输出至
graphpad prism以计算ec
50
并进行曲线拟合分析。对于诱导倍数(fi)分析,通过下式计算fi值:fi=(exp_rlu
ꢀ‑
b_rlu)/(ck_rlu-b_rlu),其中exp_rlu是实验样品的rlu,b_rlu 是背景的rlu,且ck_rlu是rlu的阴性对照。将计算的fi值输出至 graphpad prism以计算ec
50
并进行曲线拟合分析。
[0276]
如图8中所示,hucldn18.2-v.19_变体1抗体的ec
50
和 hucldn18.2-v.19_变体2抗体的ec
50
均比包含wt人igg1 fc的 hucldn18.2的ec
50
高约100倍。hucldn18.2-v.19_变体3的ec
50
比包含 wt人igg1 fc的hucldn18.2高大约~30倍。实施例7:小鼠模型中所选hucldn18.2抗体的体内功效研究
[0277]
在同系mc38-hucldn18.2异种移植小鼠模型中评价了 hucldn18.2-v.2-migg2a、hucldn18.2-v.19-migg2a和 hucldn18.2-v.24-migg2a的抗肿瘤活性。mc38-hucldn18.2细胞系是已被工程化以表达人claudin 18.2的鼠claudin18.2-/-小鼠结肠癌细胞系。用 mc38-hcldn18.2肿瘤细胞在右前肋区皮下接种六组c57bl/6n小鼠(7只小鼠/组)。一旦平均肿瘤体积约为87mm3,则如表h所示进行处理。小鼠通过i.v.给药每周处理两次。表h:不同处理组的携带mc38-hucldn18.2结肠癌细胞小鼠的平均肿瘤生长抑制(tgi)(tgi)
[0278]
如图9和表h所示,施用后第18天,用hucldn18.2-v.19-migg2a (1433
±
363mm3)或hucldn18.2-v.24-migg2a(1442
±
2318mm3)处理的小鼠的平均肿瘤体积小于用缓冲液对照
(2318
±
750mm3)处理的小鼠的平均肿瘤体积(hucldn18.2-v.19-migg2a与缓冲液:p《.05; hucldn18.2-v.24-migg2a与缓冲液:p《.05)。hucldn18.2-v.19-migg2a 或hucldn18.2-v.24-migg2a(1442
±
2318mm3)处理的小鼠的平均肿瘤体积小于imab362-migg2a处理的小鼠的平均肿瘤体积。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1