用于治疗的组合物和方法
1.本公开涉及用于治疗和预防以tdp-43病理学为特征或与tdp-43病理学相关的神经退行性疾病的组合物和方法。本公开还涉及适合治疗和预防所述神经退行性疾病的分离的肽和嵌合分子,以及编码所述肽和嵌合分子的核酸和基因构建体。
背景技术:
2.肌萎缩侧索硬化(als)是一种运动神经元疾病,其影响脑和脊髓二者中的运动神经元。als是一种致命疾病,其特征是大脑运动皮层中的锥体细胞、脊髓前运动神经元和脑干运动神经元丢失,导致肌无力和萎缩。als通常在发病后迅速恶化,通常会在几年内导致死亡。
3.额颞叶痴呆(ftd)的特征是对脑额叶和/或颞叶的进行性损伤并且与决策能力、行为和语言控制的进行性恶化有关。ftd是早老性痴呆的最常见形式之一,诊断后的中位预期寿命不到15年。
4.als和ftd二者是快速进展且致命的神经退行性疾病,具有显著的临床、遗传和病理重叠。als和ftd通常分为家族性(约10%的病例,其中涉及一个或多个明确的基因突变)或散发性(约90%的病例,其中病因学通常不太了解)。这些疾病的家族性和散发性形式在临床上难以区分。als和ftd的神经病理学特征是tdp-43在神经元中的沉积。目前的研究表明,核tdp-43错误定位到细胞质会引发毒性事件,包括tdp-43的异常磷酸化和片段化(shenouda等人,2018,adv neurobiol 20:239-263)。然而,在mrna加工过程中调节tdp-43的生理性核质穿梭和在疾病中驱动细胞质积累的分子机制仍然未知。
5.没有治愈als或ftd的方法。预后差并且治疗有限。显然需要开发治疗这些使人衰弱的疾病的新方法。
技术实现要素:
6.本公开基于发明人将14-3-3θ鉴定为促进tdp-43的异常细胞质定位并促进als和ftd发病机制的tdp-43的新的相互作用配偶体。发明人发现,使用衍生自14-3-3θ的特定肽可以靶向和清除病理性tdp-43,从而逆转与als和ftd相关的功能缺陷。
7.本公开的第一方面提供了一种用于治疗或预防与tdp-43病理学相关的神经退行性疾病或改善其至少一种症状的方法,所述方法包括向有此需要的受试者施用有效量的包含seq id no:1的氨基酸序列或其保守变体或由其组成的肽,或编码所述肽的核酸分子。
8.在一个具体的实施方案中,神经退行性疾病选自肌萎缩侧索硬化(als)和额颞叶痴呆(ftd)。als可以是家族性als或散发性als。ftd可以是家族性ftd或散发性ftd。至少一种症状可以包括,例如,去抑制、多动、运动缺陷或肌肉力量降低。
9.seq id no:1的氨基酸序列可以提供在更大的连续肽或多肽序列内。在一个示例性实施方案中,肽序列可以包含seq id no:2的氨基酸序列、其保守变体或与seq id no:2的序列具有至少约75%同一性的序列,或由其组成。
10.编码seq id no:1的肽或其保守变体的核酸分子可以包含seq id no:4的核苷酸序列或与seq id no:4的序列具有至少约70%同一性的核苷酸序列。
11.编码seq id no:2的肽、其保守变体或与其具有至少约75%同一性的序列的核酸分子可以包含seq id no:5的核苷酸序列或与seq id no:5的序列具有至少约70%同一性的核苷酸序列。
12.在一个具体的实施方案中,肽包含或连接至蛋白质去稳定结构域序列。在一个示例性实施方案中,蛋白质去稳定结构域序列包含雷帕霉素结合蛋白fkbp12。
13.因此,在一个实施方案中,所述方法包括向受试者施用编码包含seq id no:1的序列或其保守变体或由其组成的肽的基因构建体,所述肽可操纵地连接至编码蛋白质去稳定结构域的核苷酸序列。
14.本公开的第二方面提供了包含seq id no:1的氨基酸序列或其保守变体或由其组成的肽或编码所述肽的核酸分子在制造用于治疗或预防与tdp-43病理学相关的神经退行性疾病或改善其至少一种症状的药物中的用途。
15.本公开的第三方面提供了一种分离的肽,包含seq id no:1的氨基酸序列或其保守变体或由其组成。
16.肽可以包含seq id no:2的氨基酸序列、其保守变体或与seq id no:2的序列具有至少约75%同一性的序列,或由其组成。
17.本公开的第四方面提供了分离的编码第三方面的肽的多核苷酸。
18.多核苷酸可以包含seq id no:4或seq id no:5的序列或与seq id no:4或seq id no:5的序列具有至少约70%同一性的多核苷酸,或由其组成。
19.在第三和第四方面的示例性实施方案中,肽或多核苷酸用于在治疗或预防与tdp-43病理学相关的神经退行性疾病或改善其至少一种症状中使用。
20.本公开的第五方面提供了一种嵌合分子,包含连接至蛋白质去稳定结构域序列的包含seq id no:1的氨基酸序列或其保守变体或由其组成的肽。
21.本公开的第六方面提供了分离的编码第五方面的嵌合分子的多核苷酸。
22.在第五和第六方面的示例性实施方案中,嵌合分子或多核苷酸用于在治疗或预防与tdp-43病理学相关的神经退行性疾病或改善其至少一种症状中使用。
23.本公开的第七方面提供了包含第四或第六方面的多核苷酸序列的载体。
24.载体可以是病毒载体。病毒载体可以是aav载体。通常,载体用于向受试者施用以治疗或预防与tdp-43病理学相关的神经退行性疾病或改善其至少一种症状。
25.载体可以设计为用于引入神经元或脑细胞中并指导或促进编码的肽或嵌合分子在神经元或脑细胞中的表达。
附图说明
26.本文仅通过非限制性实例的方式参考以下附图描述了本公开的方面和实施方案。
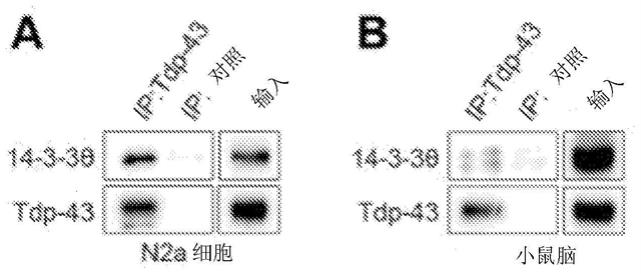
27.图1.14-3-3θ与tdp-43相互作用。来自n2a细胞(a)和小鼠脑(b)的14-3-3θ/tdp-43复合物的免疫沉淀(ip)。对照(ctr)ip确认不存在非特异性结合。
28.图2.共表达显示与其非突变形式相比,具有致病突变的tdp-43的14-3-3θ免疫沉淀(ip)显著增强(n=3)。***p《0.001;**p《0.01;*p《0.05。误差线表示sem。
29.图3.(a)a315t突变体tdp-43,当单独表达时,定位于细胞核(+mock;箭头),但当与14-3-3θ一起表达时,a315t-tdp-43共定位于细胞质(空心箭头)。(b)共表达显示与其非突变形式相比,缺少(δ)nls或nes的tdp-43与14-3-3θ的ip显著增强(n=3)。****p《0.0001;*p《0.05。误差线表示sem。(c)14-3-3θ的共表达赋予δnes tdp-43的细胞质定位(空心箭头),后者通常定位于细胞核(实心箭头)。作为比较,δnls tdp-43的细胞质定位和非突变tdp-43的核定位没有被14-3-3θ改变。
30.图4.除非去除α-螺旋6(δf),否则14-3-3θ的n-和c-末端截短变体与tdp-43免疫沉淀。注意在没有α-螺旋7-9(δg)的情况下14-3-3θ/tdp-43免疫沉淀增强。
31.图5.与14-3-3θ的gδ变体类似,单独14-3-3θα-螺旋6(14-3-3θ-fx-v5)与tdp-43免疫沉淀的共表达。
32.图6.对应于14-3-3θ-fx的14-3-3同种型的α-螺旋6的比对。红框,14-3-3θ特有的11个氨基酸的序列。
33.图7.(a)aav介导的14-3-3θ-v5在海马中的表达分别导致对照(ctr)和itdp-43
a315t
小鼠中tdp-43的不溶性和片段化(箭头)。来自独立实验(n=6)的tdp-43片段水平的量化。***p《0.001;*p《0.05。误差线表示sem。(b)aav-vec(载体)和aav-14-3-3θ-v5注射的itdp-43
a315t
小鼠的海马ca1区域中表达htdp-43的神经元的量化。**p《0.01。误差线表示sem。
34.图8.(a)具有c-末端降解结构域(dd)和n-末端v5标签的14-3-3θ的氨基酸135-164(dd-θfx)当在原代神经元中表达时自发降解,除非用shield1处理而稳定。(b)dd-θfx降低了原代神经元中共表达的a315t突变人(h)tdp-43的水平(n=4)。图:左侧柱,tdp-43;右侧柱,tdp-43+dd-θfx。**,p《0.01。误差线表示sem。
35.图9.(a)vec注射的itdp-43
a315t
小鼠皮层中主要的核htdp-43在表达dd-θfx的神经元中显著减少。(b)从出生起表达dd-θfx的itdp-43
a315t
脑中tdp-43水平减少(n=3)。mcherry和v5证实了aav介导的表达。请注意,dd-θfx在itdp-43
a315t
中的表达高于对照小鼠。图:左侧柱,p0:itdp-43+vec;右侧柱,p0:itdp-43+dd-θfx。*,p《0.05。误差线表示sem。
36.图10.(a)vec处理的itdp-43
a315t
小鼠的去抑制(如通过高架十字迷宫中增加的开放臂活动时间所反映)在dd-θfx表达时显著降低(n=8)。(b)vec处理的itdp-43
a315t
小鼠的增加的活动(如通过开阔场地中行进更远距离所反映)在dd-θfx表达时显著降低(n=8)。(c)vec处理的itdp-43
a315t
小鼠的降低的运动能力(如通过跌落旋转杆的短时间所反映)在dd-θfx表达时与ctr小鼠相当(n=8)。(d)vec处理的itdp-43
a315t
小鼠的减小的握力在dd-θfx表达时显著更大(n=8)。对于(a)
–
(d):第一个柱,p0:ctr+vec;第二个柱,p0:ctr+dd-θfx;第三个柱,p0:itdp-43+vec;第四个柱,p0:itdp-43+dd-θfx。vec=载体。ctr=对照。***p《0.001;**p《0.01;*p《0.05;ns,不显著。误差线表示sem。
37.图11.(a)与mcherry相比,表达dd-θfx-v5的itdp-43
a315t
小鼠中转基因htdp-43水平降低(n=3)。图:左侧柱,i.v.:itdp-43+vec;右侧柱,i.v.:itdp-43+dd-θfx。vec=载体。*p《0.05。误差线表示sem。(b)表达vec和表达dd-θfx的小鼠的脑染色显示海马中htdp-43阳性细胞的数量减少(n=6)。图:左侧柱,i.v.:itdp-43+vec;右侧柱,i.v.:itdp-43+dd-θfx。vec=载体。**p《0.01。误差线表示sem。
38.图12.vec处理的itdp-43
a315t
小鼠的去抑制在dd-θfx表达时显著改善(n=6)。第一
个柱,i.v.:ctr+vec;第二个柱,i.v.:ctr+dd-θfx;第三个柱,i.v.:itdp-43+vec;第四个柱,i.v.:itdp-43+dd-θfx。vec=载体。ctr=对照。***p《0.001;**p《0.01;*p《0.05。误差线表示sem。
39.图13.与aav-dd-θfx注射的aav-htdp小鼠和对照相当,vec处理的aav-htdp-43小鼠中通过减少的倒置丝线(inverted wire)时间(a)和相应的线性回归斜率差异(b)所反映的体力逐渐下降(n=10)。b:第一个柱,aav-vec+aav-vec;第二个柱,aav-vec+aav-dd-θfx;第三个柱,aav-htdp-43+aav-vec;第四个柱,aav-htdp-43+aav-dd-θfx。*p《0.05,***p《0.001。误差线表示sem。
40.图14.与aav-dd-θfx注射的aav-htdp-43小鼠相比,aav-vec处理的aav-htdp-43小鼠的握力降低(n=7)。第一个柱,aav-htdp-43+aav-vec雌性小鼠;第二个柱,aav-htdp-43+aav-dd-θfx雌性小鼠;第三个柱,aav-htdp-43+aav-vec雄性小鼠;第四个柱,aav-htdp-43+aav-dd-θfx雄性小鼠。*p《0.05。误差线表示sem。
41.图15.与aav-dd-θfx注射的aav-htdp小鼠相当,雌性和雄性vec处理的aav-htdp-43小鼠中通过重量减轻表示的胫骨前肌(ta)肌肉萎缩(n=3-7)。对于雌性和雄性小鼠:第一个柱,aav-vec+aav-vec;第二个柱,aav-vec+aav-dd-θfx;第三个柱,aav-htdp-43+aav-vec;第四个柱,aav-htdp-43+aav-dd-θfx。*p《0.05,***p《0.001。误差线表示sem。
42.氨基酸和核苷酸序列由序列标识符号(seq id no)指代。序列在序列表中提供。seq id no:1中所示的氨基酸序列代表来自人14-3-3θ的α螺旋6(αf)的11个氨基酸的基序,编码该基序的dna序列在seq id no:4中示出。seq id no:2中所示的氨基酸序列代表来自人14-3-3θ的αf的30个氨基酸的区域,编码该区域的dna序列在seq id no:5中示出。人14-3-3θ的氨基酸序列在seq id no:3中示出。在实施例中描述的研究中使用的其它核苷酸序列,包括引物序列,在seq id no:6至20中示出。
具体实施方式
43.除非另外定义,否则本文使用的所有技术和科学术语具有与本公开所属领域的技术人员通常理解的相同含义。除非另有说明,否则在整个公开中提及的所有专利、专利申请、公布的申请和出版物、数据库、网站和其它公布的材料都通过引用整体并入。在术语的定义有多种的情况下,以本节中的那些为准。在提及url或其它这样的标识符或地址的情况下,应理解这样的标识符可能会发生变化,并且互联网上的特定信息可以来来去去,但可以通过搜索互联网找到等效信息。对标识符的引用证明了这样的信息的可用性和公开传播。
44.本文中使用的未用数量词限定的名词是指一个或多于一个(即,至少一个)指示对象。举例来说,“元件”是指一个元件或多于一个元件。
45.在本说明书的上下文中,术语“约”被理解为是指本领域技术人员认为等同于在实现相同功能或结果的上下文中列举的值的数字范围。
46.在整个本说明书和所附权利要求书中,除非上下文另有要求,否则词语“包括”和诸如“包含”或“含有”的变体将被理解为暗示包含阐述的整数或步骤或者整数或步骤的组,但不排除任何其它整数或步骤或者整数或步骤的组。
47.如本文所用,术语“可操纵地连接”是指两个元件之间的功能连接,无论两个元件之间的方向或距离如何,使得一个元件的功能受另一个元件控制或影响。例如,关于启动子
和核酸序列的可操纵连接是指核酸序列的转录和表达在启动子的控制下或由启动子驱动。在本公开内容的另一个例子中,两个核苷酸序列之间的可操纵连接可以导致所表达的编码肽或多肽之间的物理连接或偶联,从而形成嵌合分子。
48.术语“任选地”在本文中用于表示随后描述的特征可能存在或可能不存在,或者随后描述的事件或情况可能发生或可能不发生。因此,本说明书将被理解为包括并涵盖其中存在特征的实施方案和不存在特征的实施方案,以及事件或情况发生的实施方案和事件或情况不发生的实施方案。
49.术语“肽”是指由通过肽键连接在一起的氨基酸组成的聚合物。术语“多肽”也可用于指代这样的聚合物,尽管在某些情况下多肽可能比肽更长(即由更多氨基酸残基组成)。尽管如此,术语“肽”和“多肽”在本文中可以互换使用。
50.如本文所用,术语“治疗(treating)”、“治疗(treatment)”、“预防(preventing)”、“预防(prevention)”和语法等同物是指补救所述的神经退行性疾病,预防、延缓或延迟疾病形成,或以其它方式预防、阻碍、延缓或逆转疾病的进展的任何和所有用途。因此,术语“治疗”和“预防”等应在其最广泛的上下文中考虑。例如,治疗并不一定意味着治疗患者直到完全康复。在疾病表现出多种症状或以多种症状为特征的情况下,治疗或预防不一定需要补救、预防、阻碍、延缓或逆转所有所述症状,而是可以预防、阻碍、延缓或逆转所述症状中的一种或多种。
51.如本文所用,术语“有效量”在其含义内包括无毒但足以提供期望效果的试剂或化合物的量或剂量。所需的确切量或剂量将因受试者而异,这取决于以下因素,例如所治疗的物种,受试者的年龄、尺寸、体重和一般状况,所治疗的疾病或病症的严重程度,所施用的特定药剂以及施用方式等。因此,不可能指定准确的“有效量”。然而,对于任何给定的情况,合适的“有效量”可以由本领域普通技术人员仅使用常规实验来确定。
52.如本文所用,术语“受试者”是指哺乳动物,并且包括人、灵长类动物、家畜(例如羊、猪、牛、马、驴)、实验室试验动物(例如小鼠、兔、大鼠、豚鼠)、表演和展示动物(例如马、家畜、狗、猫)、伴侣动物(例如狗、猫)和圈养的野生动物。优选地,哺乳动物是人或实验室试验动物。甚至更优选地,哺乳动物是人。
53.tdp-43是由tardbp基因编码的多功能rna/dna结合蛋白。其具有两个rna识别基序和介导蛋白质-蛋白质相互作用的大的c末端富含甘氨酸的结构域(grd)。富含g的结构域包含家族性als中绝大多数的致病性tardbp突变。然而,在本发明之前,关于tdp-43相互作用在生理学和疾病中的功能作用知之甚少。
54.如本文所例示,发明人已将蛋白质14-3-3θ鉴定为tdp-43的新的相互作用配偶体。tdp-43的致病性变体表现出与14-3-3θ的相互作用增加,导致tdp-43的细胞质积累、不溶性、磷酸化和片段化,类似于疾病的病理变化。不希望受理论束缚,发明人提出与14-3-3θ的瞬时相互作用可以稳定tdp-43,同时其在rna穿梭期间驻留在细胞质中。本发明人进一步提出14-3-3θ与异常的tdp-43构象相互作用并使它们易于发生病理性修饰。
55.如本文所例示,发明人证明使用源自14-3-3θ的独特肽序列介导从小鼠脑中去除病理性tdp-43,并逆转和预防als和ftd相关症状。尽管本文在与蛋白质去稳定结构域缀合的该肽序列的上下文中例示,但本公开考虑了在不存在蛋白质去稳定结构域的情况下使用肽。不希望受理论束缚,发明人提出肽干扰14-3-3θ和tdp-43之间的生理和/或病理相互作
用,从而防止14-3-3θ/tdp-43复合物的毒性下游效应。
56.在一个方面,本公开提供了一种用于治疗或预防与tdp-43病理学相关的神经退行性疾病或改善其至少一种症状的方法,所述方法包括向有此需要的受试者施用包含seq id no:1的氨基酸序列或其保守变体或由其组成的肽,或编码所述肽的核酸分子。
57.本公开的实施方案适合治疗或预防以tdp-43病理学为特征或以其它方式与tdp-43病理学相关的任何神经退行性疾病。通常,这样的疾病以核tdp-43的细胞质积累以及tdp-43的异常磷酸化和片段化为特征,或与之相关。在具体实施方案中,该疾病是肌萎缩侧索硬化(als)或额颞叶痴呆(ftd)。als可以是家族性或散发性als。ftd可以是家族性或散发性ftd。
58.神经退行性疾病的症状包括疾病特征性的或与疾病相关的行为和身体缺陷。因此,根据本公开,肽或编码所述肽的核酸分子的施用可以改善以神经退行性疾病为特征或与神经退行性疾病相关的一种或多种行为或身体缺陷。这样的行为和身体缺陷包括去抑制、多动、运动缺陷和肌肉力量降低。
59.已知tdp-43的许多致病性变体与散发性或家族性als和ftd相关,包括例如a315t、n345k、m337v、g294a、a382t和g287s突变。然而,本领域技术人员将认识到本公开的范围不限于治疗或预防携带一种或多种这些突变的个体的神经退行性疾病。
60.用于根据本公开的方面和实施方案使用的肽rkqtidnsqga(seq id no:1)是存在于人14-3-3θ的α螺旋6(αf)内的11个氨基酸的基序(对应于如seq id no:3所示的野生型人14-3-3θ的氨基酸残基138-148)。
61.本文还考虑了seq id no:1的肽的保守变体。保守变体包含一个或多个保守氨基酸置换,即用一个氨基酸置换或替换具有相似性质的另一个氨基酸,如本领域技术人员将充分理解的。例如,中性氨基酸丝氨酸(s)对相似的中性氨基酸苏氨酸(t)的置换将是保守氨基酸置换。本领域技术人员将能够确定不消除肽在tdp-43相互作用方面的功能特性的合适的保守氨基酸置换。
62.因此,本文还提供了一种分离的肽,包含seq id no:1的氨基酸序列或其保守变体或由其组成。在本文中,术语“分离的”是指如本文所用,关于核酸分子的“分离的”是指肽基本上不含来自该肽所源自的细胞的细胞物质或其它污染蛋白质(因此从其天然状态改变),或在化学合成时基本上不含化学前体或其它化学品,因此从其天然状态改变。
63.seq id no:1的肽或其保守变体可以提供在更大的连续肽或多肽序列内。包含seq id no:1序列的肽序列可包含例如约12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30、31、32、33、34、35、36、37、38、39、40、41、42、43、44、45、46、47、48、49、50、55、60、65、70、75、80、85、90、95或100个残基,通常作为连续序列。举例来说,根据本公开使用的seq id no:1的肽可以作为14-3-3θ的αf螺旋序列的一部分提供,例如包含人14-3-3θ(seq id no:3)的氨基酸135至164(seq id no:2)或其一部分的序列,或与其具有至少约75%同一性的序列。例如,包含seq id no:1序列的αf螺旋的序列的长度可以是12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30个或更多个氨基酸。
64.在一个实施方案中,肽可以包含seq id no:2的氨基酸序列、其保守变体或与seq id no:2的序列具有至少约75%同一性的序列,或由其组成。该序列可以与seq id no:2的序列具有约75%、80%、85%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%同
一性。因此,本文还提供了一种分离的肽,其包含seq id no:2的氨基酸序列、其保守变体或与seq id no:2的序列具有至少约75%同一性的序列,或由其组成。
65.包含seq id no:1的序列或其保守变体或由其组成的肽可以包含或连接至一个或多个其它部分以促进例如转运、细胞识别、靶向或其它功能,例如蛋白质去稳定或降解。例如,肽可以连接至或包含细胞靶向部分,该部分有助于将肽靶向至一种或多种特定类型,例如中枢神经系统的神经元或其它细胞。还举例来说,如下文进一步描述的,肽可以包含或连接至蛋白质去稳定或降解信号或结构域以破坏稳定性和/或诱导体内降解。通过本领域已知的任何方法(包括任何化学或重组方法)可以将肽连接至一个或多个其它部分,合适时,导致在分子和一个或多个其它部分之间形成共价和/或非共价键。这些部分可以是肽、多肽或蛋白质部分。因此,本公开进一步提供了包含与异源肽、多肽或蛋白质缀合的序列rkqtidnsqga(seq id no:1)或其保守变体的嵌合肽、多肽和蛋白质。这样的嵌合肽、多肽或蛋白质可以具有例如多至约15、20、25、30、35、40、45、50、55、60、65、70、75、80、85、90、95、100、110、120、130、140、150、160、170、180、190、200、250、300、350、400、450、500、600、700、800、900、1000、1500或2000个或更多个残基的长度。
66.seq id no:1的肽或保守变体可以缀合至附加肽、多肽或蛋白质部分的c-末端或n-末端。组分分子可以使用例如标准化学偶联技术如mbs、戊二醛、edc或bdb偶联缀合,或者可以通过本领域技术人员已知的肽合成方法或重组方法连接。
67.在本公开的具体实施方案中,包含seq id no:1的序列或其保守变体的肽缀合至或包含提供蛋白质去稳定或降解信号的部分。在示例性实施方案中,蛋白质去稳定或降解信号由蛋白质去稳定或降解结构域(本文为方便起见称为“去稳定结构域”)提供。“去稳定结构域”是指蛋白质、多肽或氨基酸序列,当其功能性偶联至感兴趣的肽、多肽或蛋白质时,其能够破坏感兴趣的肽、多肽或蛋白质的稳定性并任选地诱导降解。本领域技术人员熟知的去稳定结构域的实例包括泛素、pest序列(富含脯氨酸、谷氨酸、丝氨酸和苏氨酸的序列)、细胞周期蛋白破坏盒、氨基酸的疏水性延伸片段和雷帕霉素结合蛋白fkbp12(例如在ptuner质粒中发现的,clontech)。可以将合适的去稳定结构域引入本公开的肽序列中,或在有或没有接头的情况下与肽的n-或c-末端缀合。对于希望包括去稳定结构域的实施方案,本领域技术人员将理解可以采用任何合适的去稳定结构域,并且本公开的范围不限于参考任何特定的去稳定结构域。
68.本文还提供了包含与蛋白质去稳定结构域序列缀合的seq id no:1的肽或其保守变体的嵌合肽、多肽和蛋白质。本文还提供了包含与蛋白质去稳定结构域序列缀合的seq id no:2的肽、其保守变体或与seq id no:2的序列具有至少约75%同一性的序列的嵌合肽、多肽和蛋白质。
69.本文公开的肽和多肽可以使用本领域已知的任何方法产生,包括化学合成技术、核酸合成技术、肽合成技术和/或重组技术。在一个实例中,使用固相肽合成的fmoc-聚酰胺模式合成肽,例如seq id no:1的肽。其它合成方法包括固相t-boc合成和液相合成。纯化可以通过任何一种技术或其组合进行,例如重结晶、尺寸排阻色谱、离子交换色谱、疏水相互作用色谱和反相高效液相色谱,使用例如乙腈/水梯度分离。
70.或者,可以使用本领域熟知的重组方法来生产肽和多肽。编码肽和多肽的核酸可以通过任何合适的方法获得,例如rt-pcr或编码本发明多肽的寡核苷酸的合成。因此,如下
文进一步描述的,本文还提供了编码肽和多肽(包括本文公开的嵌合肽和多肽)的核酸分子。设计编码肽和多肽(包括本文公开的嵌合肽和多肽)的核酸分子完全在本领域技术人员的技能范围内。
71.本公开还考虑和涵盖了本文公开的肽序列的肽模拟物。如本文所用,术语“肽模拟物”是指肽样分子,其具有结构上所基于的肽与tdp-43相互作用的能力。这样的肽模拟物包括化学修饰的肽、含有非天然存在的氨基酸的肽样分子,以及类肽(参见,例如,goodman and ro,peptidomimetics for drug design,在"burger's medicinal chemistry and drug discovery"第1卷(编辑m.e.wolff;john wiley&sons 1995),第803-861页)。本领域已知多种肽模拟物,包括例如含有受限氨基酸(例如,α-甲基化氨基酸、α,α-二烷基甘氨酸、α-、β-或γ-氨基环烷羧酸、α,β-不饱和氨基酸、β,β-二甲基或β-甲基氨基酸或其它氨基酸模拟物)的肽样分子,模拟肽二级结构的非肽组分(例如非肽3-转角模拟物、γ-转角模拟物、β折叠结构模拟物或螺旋结构模拟物),或酰胺键等排体(例如,还原的酰胺键、亚甲基醚键、乙烯键、硫代酰胺键或其它酰胺等排体)。用于鉴定肽模拟物的方法在本领域中也是众所周知的并且包括例如筛选包含潜在肽模拟物文库的数据库。
72.本公开还提供了分离的编码如本文所述的肽和嵌合肽的核酸分子,以及将所述核酸分子(通常作为载体或类似基因构建体的一部分)施用于有此需要的受试者的方法。
73.例如,编码seq id no:1的肽或其保守变体的核酸分子可以包含如seq id no:4所示的核苷酸序列或与如seq id no:4所示的序列具有至少或约70%、75%、80%、81%、82%、83%、84%、85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的序列。例如,编码seq id no:2的肽、其保守变体或与seq id no:2的序列具有至少约75%同一性的序列的核酸分子可以包含如seq id no:5所示的核苷酸序列或与如seq id no:5所示的序列具有至少或约70%、75%、80%、81%、82%、83%、84%、85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的序列。核酸分子还可包含与上述核苷酸序列可操纵地连接的选定蛋白质去稳定结构域的核苷酸序列,从而表达嵌合肽或多肽。
74.本公开还提供了包含本文所述的一种或多种核苷酸序列的载体。通常,核苷酸序列可操纵地连接至启动子以允许肽或多肽的表达。载体可以是附加型载体(即不整合到宿主细胞基因组中),或者可以是整合到宿主细胞基因组中的载体。载体可能具有复制能力或复制缺陷。示例性载体包括但不限于质粒、粘粒和病毒载体,例如腺相关病毒(aav)载体、慢病毒、逆转录病毒、腺病毒、疱疹病毒、细小病毒和肝炎病毒载体。合适载体的选择和设计在本领域普通技术人员的能力和判断范围内。
75.本文提供了包含表达盒或表达构建体的多核苷酸,所述表达盒或表达构建体可用于在合适的载体中表达本文所述的肽、多肽或嵌合肽或多肽,用于基因治疗。因此,在具体实施方案中,本公开的方法包括向有需要的受试者施用载体,该载体包含编码本文公开的肽和多肽的核苷酸序列,通常可操纵地连接至异源启动子,使得感兴趣的肽、多肽或嵌合肽或多肽在体内表达。在具体的示例性实施方案中,载体是病毒载体。如本文所用,术语“病毒载体”是指源自任何病毒的载体并且通常包括至少一个起点元件并且具有被包装成重组病毒或病毒体的能力。病毒载体可以具有载体所来源的病毒的一个或多个野生型基因的全部或部分缺失,但保留功能性侧翼itr序列,这是病毒体的拯救、复制和包装所必需的。因此,
病毒载体通常至少包含病毒复制和包装所需的顺式序列(例如,功能性itr)。itr不必是野生型核苷酸序列,并且可以改变,例如,通过核苷酸的插入、缺失或替换,只要该序列提供功能性拯救、复制和包装即可。载体和/或病毒体可用于将异源序列转移到体外或体内细胞中。
76.在具体实施方案中,载体是aav载体,即源自腺相关病毒的载体,包括但不限于aav1、aav2、aav3、aav4、aav5、aav6、aav7、aav8、aav9、aav10、aav11、aav12或aav13,或使用合成或修饰的aav衣壳蛋白,例如为有效体内转导(例如中枢神经系统)而优化的那些。重组aav载体描述了复制缺陷型病毒,其包括包裹aav基因组的aav衣壳。通常,一种或多种野生型aav基因已从基因组中全部或部分缺失,优选rep和/或cap基因。功能性itr序列对于将载体基因组拯救、复制和包装到raav病毒体中是必需的。
77.aav itr可以源自几种aav血清型中的任一种,包括但不限于aav1、aav2、aav3、aav4、aav5、aav6、aav7、aav8、aav9、aav10、aav11、aav12、aav13等,或者可以是合成的。技术人员可以在没有过度实验的情况下进行选择。aav itr的长度通常为约145个核苷酸,尽管不需要具有野生型核苷酸序列,即可以通过核苷酸的插入、缺失和/或替换而改变,只要它们是功能性的即可。此外,多核苷酸中的itr不必相同或源自相同的aav血清型或分离株,只要它们按预期发挥作用,即有助于拯救、复制和包装转基因即可。aav itr的核苷酸序列是本领域众所周知的。
78.根据本公开使用的载体还可以包含转录增强子、翻译信号以及转录和翻译终止信号。转录终止信号的实例包括但不限于多腺苷酸化信号序列,例如牛生长激素(bgh)poly(a)、sv40晚期poly(a)、兔β-珠蛋白(rbg)poly(a)、胸苷激酶(tk)poly(a)序列及其任何变体。在一些实施方案中,转录终止区位于转录后调控元件的下游。在一些实施方案中,转录终止区是多腺苷酸化信号序列。
79.根据本公开使用的载体还可以包含各种转录后调控元件。在一些实施方案中,转录后调控元件可以是病毒转录后调控元件。病毒转录后调控元件的非限制性实例包括土拨鼠肝炎病毒转录后调控元件(wpre)、乙型肝炎病毒转录后调控元件(hbvpre)、rna转运元件及其任何变体。
80.本公开考虑通过任何合适的方式将肽、多肽、多核苷酸和载体递送至需要治疗的受试者,并且通常以药物组合物的形式,该药物组合物可以包含一种或多种药学上可接受的载体、赋形剂或稀释剂。这样的组合物可以通过任何方便或合适的途径施用,例如通过肠胃外(例如腹膜内、皮下、动脉内、静脉内、肌肉内)、口服(包括舌下)、鼻或局部途径。在需要将适当浓度的分子直接递送至体内待治疗部位的情况下,施用可以是区域性的而不是全身性的。区域施用提供了将非常高的局部浓度的分子递送到所需部位的能力,因此适合实现期望的治疗或预防效果,同时避免身体的其它器官暴露于载体和分子,从而潜在地减少副作用。
81.应当理解,本发明的组合物对任何特定受试者的具体剂量水平将取决于多种因素,包括例如所使用的具体药剂的活性,待治疗的个体的年龄、体重、一般健康状况和饮食,施用时间、排泄频率以及与任何其它治疗或疗法的组合。可以进行单次或多次施用,剂量水平和模式由治疗医师选择。可以应用广泛的剂量范围。考虑到患者,例如,每天每千克体重可以施用约0.1mg至约1mg的药剂。可以调整剂量方案以提供最佳治疗反应。例如,可以每
天、每周、每月或其它合适的时间间隔施用几个分开的剂量,或者可以根据情况的紧急情况按比例减少剂量。
82.药学上可接受的载体或稀释剂的实例是软化水或蒸馏水;生理盐水;植物油,例如花生油(peanut oil)、红花油、橄榄油、棉籽油、玉米油、芝麻油、花生油(arachis oil)或椰子油;硅油,包括聚硅氧烷,例如甲基聚硅氧烷、苯基聚硅氧烷和甲基苯基聚硅氧烷;挥发性有机硅;矿物油,例如液体石蜡、软石蜡或角鲨烷;纤维素衍生物,例如甲基纤维素、乙基纤维素、羧甲基纤维素、羧甲基纤维素钠或羟丙基甲基纤维素;低级烷醇,例如乙醇或异丙醇;低级芳烷醇;低级聚亚烷基二醇或低级亚烷基二醇,例如聚乙二醇、聚丙二醇、乙二醇、丙二醇、1,3-丁二醇或甘油;脂肪酸酯,例如棕榈酸异丙酯、肉豆蔻酸异丙酯或油酸乙酯;聚乙烯吡咯烷酮;琼脂;角叉菜胶;黄蓍胶或阿拉伯树胶和凡士林。通常,一种或多种载体将形成组合物重量的10%至99.9%。
83.本发明考虑了联合疗法,其中将如本文所述的肽、多肽、多核苷酸和载体与可促进期望治疗或预防结果的其它合适药剂共施用。“共施用”是指以相同的制剂或以两种不同的制剂通过相同或不同的途径同时施用或通过相同或不同的途径顺序施用。“顺序”施用是指药剂施用之间的数秒、数分钟、数小时或数天的时间差。施用可以按任何顺序进行。
84.本说明书中对任何先前出版物(或从其来源的信息)或任何已知事项的引用不是也不应被视为认同或承认或任何形式的暗示该先前出版物(或从其来源的信息)或已知事项构成本说明书所涉及的努力领域的公知常识的一部分。
85.现在将参考以下具体实施例来描述本公开,不应将其解释为以任何方式限制本公开的范围。
86.实施例
87.以下实施例是对本公开的说明,并且不应被解释为以任何方式限制整个说明书中描述的公开的一般性质。
88.一般方法
89.细菌双杂交筛选。bacteriomatch ii双杂交系统按照制造商的说明(chem-agilent)进行。简而言之,将人tdp-43的羧基末端部分(对应于uniprot登录号q13148的人tdp-43序列的氨基酸259-415)克隆到pbt(诱饵)载体中,并用于从人脑cdna ptrg质粒文库中鉴定相互作用配偶体。蛋白质-蛋白质相互作用配偶体的检测基于his3报告基因的转录激活,并且阳性通过二次链霉素抗性报告子进一步验证。所有的增殖和转化都是使用试剂盒中提供的化学感受态细胞完成的。通过在37℃将生长板与2%ttc/pbs(sigma)孵育10分钟,使菌落可视化以获取图像。
90.克隆。点突变和截短变体通过标准定点诱变产生(ittner等人,2005,biochemistry 44:5749-5754)。使用具有序列ccggcagttgcttagagacaacctactcgagtaggttgtctctaagcaactgtttttg(seq id no:6)的14-3-3θmission shrna慢病毒(sigma-aldich)进行14-3-3θ的敲低。使用慢病毒(克隆载体plenti6/ubc;life technologies)实现了sh-sy5y细胞中14-3-3θ(c末端v5-标签)的稳定过表达。将所有14-3-3同种型都与c末端myc标签一起克隆到pcdna3.1/myc(life technologies)中,并且将tdp-43野生型/突变体与c末端v5标签一起克隆到pcdna3.1/v5(life technologies)中用于免疫沉淀。
91.腺相关病毒。使用质粒paav-hsyn-egfp(addgene,#50465)作为骨架并去除egfp,
将14-3-3θ(具有v5标签)在人突触蛋白启动子下克隆到raav载体中。用于mcherry表达的相同载体或变体用作对照。使用衣壳aav9.php.b(deverman等人,2016,nat biotechnol 34:204-209)如先前所述(bi等人,2017,nat commun 8:473)进行raav9载体的包装。将2μl raav(1
×
10
13
病毒基因组/ml)注射到3月龄的野生型或itdp-43
a315t
小鼠的海马(从λ的-1.94mm ap,1.6mm ml,1.8mm dv)(ke等人,2015,acta neuropathol 130:661-678)。对于脊髓注射,将1μl raav(1
×
10
13
病毒基因组/ml)直接注射到冷冻麻醉的新生幼崽(p0-2)的脊髓中。所有动物实验均已获得麦考瑞大学动物伦理委员会(macquarie university animal ethics committee)的批准。
92.免疫沉淀。如先前所述进行免疫沉淀(ittner等人,2009,j biol chem 284:20909-20916)。简而言之,将293t hek细胞用pcdna3.1/v5中的tdp-43变体和/或14-3-3同种型/变体共转染。将细胞在ripa缓冲液中裂解。将等量的蛋白质与1μl v5抗体(life technologies)一起孵育过夜,并使用磁性蛋白g珠(life technologies)沉淀。通过使用myc抗体的蛋白质印迹进一步证实免疫共沉淀。
93.蛋白质印迹。如先前所述进行蛋白质印迹(ke等人,2012,plos one 7:e35678)。用于免疫印迹的一抗是人tdp-43、c-末端tdp-43、pan-tdp-43(proteintech)、14-3-3θ(abcam)、v5、myc(life technologies)、磷酸化-tdp-43s409/410(cosmobio)、gapdh(merck-millipore)。
94.细胞培养和染色。所有免疫沉淀实验均在293t hek细胞中进行。根据标准方案,将细胞维持在含有10%胎牛血清(fbs)的dmem中。将sh-sy5y细胞维持在含有10%fbs的dmem/f-12中,并用于14-3-3θ过表达或敲低。通过慢病毒转导实现了14-3-3θ的稳定过表达和敲低。对于免疫细胞化学,将细胞固定在4%pfa中并用3%热灭活山羊血清/2%bsa封闭。使用抗体v5(sigma)、myc(life technologies)和二抗alexa fluor 488、555(life technologies)。盖玻片在immun-mount(southern biotech)中固定。
95.显微镜检查。所有细胞培养荧光图像均使用bx51落射荧光或共聚焦fv10i显微镜(olympus)拍摄。
96.体外复合物测定。hek293t细胞用全长野生型tdp-43或具有f147l/f149l双突变(均具有c末端v5标签)的tdp-43或14-3-3θ(具有多组氨酸-标签)转染。用tdp-43构建体转染的细胞在补充有不含edta的完全蛋白酶抑制剂混合物(roche)的免疫沉淀缓冲液(ipb)(20mm tris-hcl(ph 7.8)、150mm nacl、0.1%(v/v)np-40)中裂解,并且具有v5标签的tdp-43用小鼠抗v5抗体(life technologies)进行ip(如上)。随后,将裂解物用ipb洗涤两次,用dnase/rnase缓冲液(drb)(10mm tris-hcl(ph 7.6)、2.5mm mgcl2和0.5mm cacl2)洗涤两次,并在drb中重构。14-3-3θ-his转染的细胞在ipb中裂解并通过talon树脂(clontech laboratories)进行纯化。简而言之,将裂解物与talon树脂在4℃下孵育2小时,用ipb洗涤三次并在体外相互作用缓冲液(ivib)(20mm tris-hcl(ph 7.8)、0.1m nacl、20%(v/v)甘油、5mm mgcl2、5mm cacl2、0.1%(v/v)np-40、1mm edta、0.1mm dtt和0.2mm pmsf)中洗脱。对于rna和dna消化,将含有结合有v5标签的tdp-43的磁珠悬液与dnase、rnase或缓冲液(对照)在37℃孵育10分钟。消化后,将所有反应混合物用冰冷的ipb洗涤一次并重悬在ivib中。随后将纯化的tdp-43和14-3-3θ在4℃孵育2小时以进行体外相互作用。按照常规ip洗涤反应,并在4x样品缓冲液中洗脱用于蛋白质印迹。
97.定量pcr。如前所述进行rna纯化和定量pcr(bi等人,2017,nat commun 8:473)。简而言之,按照制造商的说明,使用rneasy mini kit(qiagen)从小鼠皮质脑组织中提取rna。为了去除污染的基因组dna,使用不含rnase的dnase i(qiagen)进行柱上dna消化。使用第二链cdna合成试剂盒(invitrogen)从2.5μg总rna合成cdna。使用快速sybr绿色反应混合物(invitrogen)和基因特异性引物对,使用mx3000实时pcr循环仪(stratagene),通过定量pcr测定mrna水平。水平表示为持家基因gapdh的倍数变化,并转换为相对于对照组织的倍数差异。使用了这些引物(5’至3’):
98.14-3-3θ
99.(f):gctaaaacggcttttgatgagg(seq id no:7);
100.(r):gtgccctggatgcctttagtt(seq id no:8)
101.14-3-3β
102.(f):ctccagtcctccgcgaaaat(seq id no:9);
103.(r):gagagttcgtgtccctgctc(seq id no:10)
104.14-3-3γ
105.(f):ggcggtcttcggtttccttc(seq id no:11);
106.(r):gttcagctcggtcacgttctt(seq id no:12)
107.14-3-3ε
108.(f):cgcaccccattcgtttagg(seq id no:13);
109.(r):attctgctcttcaccatcacc(seq id no:14)
110.14-3-3ζ
111.(f):ctacgatcacgtccaacccg(seq id no:15);
112.(r):gtcaaacgcttctggctgc(seq id no:16)
113.14-3-3σ
114.(f):acaacctgacactgtggacg(seq id no:17);
115.(r):cctttggagcaagaacagcg(seq id no:18)
116.gapdh
117.(f):gtgaaggtcggtgtgaac(seq id no:19);
118.(r):atctccactttgccactgcaa(seq id no:20)
119.小鼠。先前已经描述了itdp-43
a315t
小鼠(ke等人,2015,acta neuropathol 130:661-678)。这些小鼠在cns神经元中在多西环素可控(tet-off)启动子的控制下组成性地表达人a315t突变体tdp-43。将小鼠分组饲养在12小时光照/黑暗循环中,自由获取食物和水。时间匹配的c57bl/6小鼠获自arc perth。所有动物实验均已获得麦考瑞大学动物伦理委员会的批准。
120.运动测试——如前所述进行丝线测试(van hummel等人,2018,am j pathol 188:1447-1456)。简而言之,将小鼠放在金属丝网上并让其倒挂,记录掉落潜伏期。如先前所述(am j pathol 188,1447-1456)使用握力计测量峰值前臂力量(chatillon,ametek)得到握力。
121.免疫组织化学。先前已经描述了石蜡组织切片的染色,包括抗原修复(van eersel等人,2015,neuropathology and applied neurobiology 41:906-925)。用于染色的一抗
是针对人tdp-43、pan-tdp-43(proteintech).neun、mcherry、egfp(abcam)、v5(sigma)。使用的二抗是alexa-fluo偶联488、555和647(life technologies)。
122.统计分析。使用graphpad prism 6.0进行统计分析。学生t检验用于比较两个组,anova用于多组比较。
123.实施例1
–
tdp-43的新的相互作用配偶体的鉴定
124.为了鉴定tdp-43的c末端富含甘氨酸的结构域(grd)的新的相互作用配偶体,发明人进行了如上所述的细菌双杂交筛选。确定的最佳候选者(65个命中物中的11个)是14-3-3θ(由ywhaq基因编码),它是14-3-3支架蛋白家族的成员。来自鼠n2a细胞和小鼠脑的免疫共沉淀证实了内源性14-3-3θ和tdp-43之间的相互作用(图1)。
125.为了测试14-3-3θ/tdp-43相互作用是否与疾病相关,发明人在293t hek细胞中表达了14-3-3θ和tdp-43突变体。令人惊讶的是,14-3-3θ与携带致病突变的tdp-43变体的相互作用明显更多,tdp-43的致病突变包括a315t突变,这样的tdp-43变体是与家族性als和ftd相关的致病变体(见图2)。14-3-3θ与tdp-43-a315t的共表达导致显著的细胞质共定位(图3a)。核定位(nls)和核输出(nes)序列介导tdp-43的主要核定位。有趣的是,14-3-3θ表现出与tdp-43的nes缺失(δnes)变体和nls缺失(δnls)变体二者的强烈相互作用(图3b)。虽然tdp-43-δnls的细胞质定位和非突变tdp-43的核定位没有被14-3-3θ改变,但是严格定位于细胞核并在细胞中表达时形成核聚集体的tdp-43-δnes(winton等人,2008,j biol chem 283:13302-13309)被发现当与14-3-3θ共转染时几乎只存在于细胞质中(图3c)。
126.上述发现表明,发明人已经确定了14-3-3θ和tdp-43之间的新的相互作用,具有驱动tdp-43变体(包括致病变体)的细胞质定位的增强的复合物形成。
127.然后,发明人通过免疫共沉淀测试了所有14-3-3同种型与tdp-43的潜在相互作用。与14-3-3θ相比,tdp-43显示更强地与14-3-3η、14-3-3γ和14-3-3σ同种型相互作用,但与14-3-3ε、14-3-3ζ和14-3-3β没有明显相互作用(数据未示出)。14-3-3σ和14-3-3ζ同种型在神经元中并不富集。更重要的是,与野生型tdp-43相比,仅14-3-3θ显示出与tdp-43-a315t,特别是tdp-43-δnes变体的明显更强的相互作用,而其它相互作用的同种型没有显示出增强的相互作用(事实上14-3-3σ与tdp-43-δnes较少相互作用)(数据未示出)。因此,仅与14-3-3θ的相互作用会随着tdp-43的致病变体而改变。
128.实施例2
–
14-3-3θ中介导与tdp-43结合的相互作用基序
129.14-3-3二聚体通常与其相互作用配偶体的磷酸化形式相互作用。然而相比之下,在tdp-43的情况下,发明人发现tdp-43的磷酸化模拟变体较少与14-3-3θ相互作用,支持非规范类型的相互作用(数据未示出)。
130.在结构上,14-3-3θ含有九个α-螺旋(参见图4),其中螺旋αc、αe、αg和αi有助于14-3-3θ二聚体的典型配偶体结合。为了鉴定14-3-3θ中介导tdp-43结合的相互作用基序,发明人逐步截短14-3-3θ,揭示相互作用是由14-3-3θ的第六个α-螺旋(αf)介导的(图4)。
131.发明人生产了仅包含14-3-3θ的α-螺旋6(αf)(seq id no:2中所示的30个氨基酸的序列;对应于野生型人tdp-43序列的氨基酸135-164)的构建体,将此构建体称为“fx”。表达fx使tdp-43共沉淀(图5),但未能拉下已知的14-3-3θ相互作用配偶体yes相关蛋白(yap)和foxo1(数据未示出),进一步支持14-3-3θ和tdp-43之间的非规范相互作用。14-3-3θ的α-螺旋6(αf)具有10个氨基酸的基序,该基序是14-3-3θ与其它14-3-3同种型相比是独特的
43
a315t
小鼠的确定的功能缺陷。该数据表明,可以使用特定的相互作用肽靶向和清除病理性tdp-43,类似于治疗als和ftd的潜在新途径。
138.实施例5
–
dd-θfx阻止了小鼠中由人野生型tdp-43的表达诱导的缺陷
139.然后,发明人基于cns神经元中aav介导的非突变htdp-43的表达,研究了dd-θfx表达在散发性als小鼠模型中的影响。发明人使用嗜神经性aav9血清型aav.php.b,通过在幼稚的新生c57bl/6小鼠中的颞静脉注射实现全身递送和在cns神经元中的均匀表达(deverman等人,2016,nat biotechnol 34:204-209)。通过在注射天然htdp-43(aav-htdp-43)或单独aav载体(aav-ctr)的小鼠中出生时的共注射(aav-dd-θfx)研究了dd-θfx的作用。
140.直到10周龄,aav-htdp-43和aav-ctr在每两周的倒置丝线测试中显示出相当的性能(图13),表明力量相当。此后,在施用aav-htdp-43的小鼠中,倒置丝线测试的性能逐渐下降,但当小鼠在出生时用aav-dd-θfx共治疗时,这种情况完全被阻止(图13)。握力的直接评估证实了这一结果,与aav-ctr小鼠相比,雄性aav-htdp-43小鼠的握力显著降低,并且通过dd-θfx共治疗得到了预防(图14)。在雌性小鼠中观察到可比较的趋势。此外,与各自的对照相比,19周龄雌性和雄性aav-htdp-43小鼠的胫骨前肌重量显著降低(图15)。这些结果表明,dd-θfx防止了小鼠中由非突变tdp-43表达引起的缺陷。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1