C(sp3)-H活化与DNA编码的合并
c(sp3)-h活化与dna编码的合并
1.相关申请的交叉引用
2.本技术要求于2019年11月25日提交的美国申请序列号no.62/940,063的优先权,其公开内容通过引用并入本文。
背景技术:
3.brenner和lerner1最初提出了在裂池合成(split-pool synthesis)期间的每个反应步骤中使用dna序列编码每个单一试剂的概念。将数百万或数十亿个del分子与同一混合物中的固定靶蛋白一起孵育的情况下,现在可在工作台上进行针对靶蛋白的dna编码文库(dna-encoded library,del)亲和力选择2。del技术的应用导致了用于药物发现的先导化合物的快速鉴定3。
4.目前,提高命中率以及改进先导化合物的类药性(drug-like)性质是用于构建优异del的主要关注点。在这种情况下,建立多种类型的与del技术相容的有机转化(水作为溶剂,存在dna,dna底物的浓度为1mm)是至关重要的4。on-dna反应的发展面临多种不同的挑战。dna骨架降解可在常规反应条件下发生;金属催化剂可被寡核苷酸毒化;溶解dna标记的底物需要至少20%的水作为共溶剂。
5.在过去十年中,dna相容反应的进展集中在亲核芳族取代(snar)、交联、环加成和点击化学以构建c(sp2)-c(sp2)5、c-n6、c-o7、s-x键8和杂环9。考虑到并入c(sp3)碳中心以构建c(sp2)-c(sp3)键
10
并避免高分子量和亲脂性的公知趋势,将简单脂肪酸和酮的c(sp3)-h键与dna编码杂芳基偶联将是高度期望的。多种羧酸和酮的多个c-h键的可用性为扩展用于del的可接近化学空间提供了独特的机会。
6.本发明人及其同事们最近对β-c-h键的广泛转化的开发表明了用于从简单性中产生前所未有的多样性的潜力
11
,如在图1a的图中示意性地示出的。使用羧酸来源底物的c-h芳基化构建dna编码文库的吸引力从最近的研究中显而易见,在该研究中,在有机溶剂中进行c-h活化反应并且随后单独附加dna标签。然而,这种方法不允许在裂池合成期间的每个反应步骤中编码每个单一试剂,因此限制了可用构建单元(building block)的数目,并从而限制了文库的大小
12
(图1b)。
7.相反,使用c-h活化作为on-dna的偶联步骤允许构建大得多的文库。值得注意的是,尽管使用了非常强有力的定向基团(directing group),但迄今为止在存在dna的情况下c(sp3)-h活化反应尚未取得成功
13
。本文考虑了开发不同类别底物的on-dna c(sp3)-h活化,其可顺序地用于构建具有富集的c(sp3)特征、手性中心、小环和杂环的del,如在图1c中示意性地示出的,并在下文中具体示例。
技术实现要素:
8.本发明考虑了用于制备包含具有多个不同双官能分子的文库的水性组合物的方法以及文库本身。所考虑的方法考虑了以下步骤:使存在于水性组合物的一个或更多个等分试样中的具有根据式a'-b-c'的末端a'和c'的双官能化接头分子b反应。末端c'包含不含
仲环氮原子的键合的(系的(tethered))经碘取代芳族环部分,并且末端a'包含标识符核苷酸序列前体z'。接头末端c'经碘取代芳族环部分在一种或更多种反应物c
4-c
16
脂族羧酸、甲酰胺或掩蔽酮单元x'的β-c(sp3)-h或γ-c(sp3)-h位置通过钯催化芳基化进行反应。不同的x'在每个等分试样中反应,不同的核苷酸标识符序列前体z'也是如此与接头的末端a'反应,以形成包含具有式(i)z
nα-a-b-c-x
nα
的双官能分子的水性组合物。
9.在式(i)中,n是x和z的位置标识符并且为1至10的整数,优选1至约6,并且更优选2至约5,使得当n为1时,x和z位于最接近接头b的位置,并且“α”标识一种或更多种特定的反应的c
4-c
16
脂族羧酸、甲酰胺或掩蔽酮单元x和由此形成的双官能分子中相应的一种或更多种标识成对dna序列z。每个z'或z分别与特定的x'或x成对并将其标识。任选地,将如此形成的包含大致等量双官能分子的反应的水性等分试样组合物混合以形成包含大致等数目(量)的双官能分子混合物的单一组合物。
10.使存在于一种或更多种包含式(i)的双官能分子的水性组合物的一个或更多个等分试样中的羧酸、甲酰胺或掩蔽酮官能团x
nα
与一种或更多种不含仲环氮原子的经碘取代芳族环部分(本文所用的每个其他的经碘取代芳族环部分也是如此,并且与在末端c'处存在的相同或不同)w'反应。使一种或更多种前体核苷酸序列标识符y'与z
nα
反应以形成一种或更多种包含具有式(ii)y
nβ-z
nα-a-b-c-x
nα-w
nβ
的双官能分子的水性组合物。“β”标识式(ii)的双官能分子中的一种或更多种特定的反应化学基团w和相应的一种或更多种成对dna序列标识符y。
11.任选地将如此形成的包含大致等量双官能分子的反应的水性等分试样组合物混合以形成包含大致等同双官能分子混合物的单一组合物。每个y'或y分别与特定的w'或w成对并将其标识。
12.使存在于包含式(ii)的双官能分子的水性组合物或其等分试样中的一种或更多种经碘取代芳族环部分w
nβ
在与先前反应的相同或不同的一种或更多种c
4-c
16
脂族羧酸、甲酰胺或掩蔽酮单元v'的β-c(sp3)-h或γ-c(sp3)-h位置通过钯催化芳基化进行反应。使一种或更多种前体核苷酸序列标识符t'与y
nγ
反应以形成一种或更多种包含式(iii)t
nγ-y
nβ-z
nα-a-b-c-x
nα-w
nβ-v
nγ
的双官能分子的组合物。
13.每个t'或t分别与特定的v'或v成对并将其标识。另外,γ标识双官能分子中的一种或更多种特定的c
4-c
16
脂族羧酸、甲酰胺或掩蔽酮单元v和相应的一种或更多种标识成对dna序列y。
14.关于上述概述的反应序列,应当理解至少一组反应步骤包括使包含双官能分子的水性组合物的多个等分试样单独与不同于在该步骤的另一个等分试样中的双官能分子反应的反应物进行反应,随后将所产生的等分试样组合以形成包含多个构成水性组合物中的所述双官能分子的文库的不同双官能分子的混合物的水性组合物。
15.提及反应物或双官能分子,还应当理解z、a、c、x、y、w、t和v是相应的z'、a'、c'、x'、y'、w'、t'和v'的反应形式。
16.将包含式iii双官能分子的两个或更多个等分试样组合以形成包含双官能分子混合物的水性组合物,从而形成包含文库的水性组合物。如此形成的文库可通过从水性组合物分离如通过冻干、用有机溶剂沉淀、色谱法以及技术人员公知的其他方法来分离。
17.还应当注意的是,所考虑的双官能分子文库的合成不需要在如上所示的三个反应
步骤循环之后停止,而是可继续进行另外数个遵循以上所述模式的反应循环。优选2个循环至约7个,更优选3个至约5个反应循环。
18.还考虑了具有多个不同双官能分子的文库,所述双官能分子具有式(iii)、z、a、c、x、y、w、t和v的式(iii)双官能分子。在式iii官能分子的文库中,z、a、c、x、y、w、t和v具有与先前提供的相同的含义,下标符号nγ、nβ和nα也是如此。因此,t
nγ-y
nβ-z
nα-a是多核苷酸序列的混合物,其中特定标识符标识反应的经碘取代芳族环部分和c
4-c
16
脂族羧酸、甲酰胺或掩蔽酮单元,它们构成文库的双官能分子混合物中的反应构建单元c-x
nα-w
nβ-v
nγ
。
19.优选地,接头b包含足够长以成为用于重复聚合酶链反应(polymerase chain reaction,pcr)的引物的寡核苷酸序列(约18至22个碱基对(base pair,bp)),并且还包含允许切割t
ni-y
ni-z
n-a标识符的多核苷酸序列的预定限制性内切核酸酶的识别序列。还优选的是,每个标识符寡核苷酸序列是双链dna并且特定标识符t
ni-y
ni-z
n-a多核苷酸序列也是双链dna。
20.还优选的是,每个特定标识符双链dna寡核苷酸包含两个限制性内切核酸酶识别位点,一个识别位点位于用于合成的反应物的特定标识符核苷酸序列的任一侧。如果相同的核酸内切酶识别位点位于双官能分子的给定位置处存在的所有寡核苷酸的任一侧,则用该核酸内切酶切割提供许多可以使用质谱分析进行分离和标识的标识符dna寡聚物。
21.技术人员还可将靶组合蛋白与双官能分子文库或子文库混合,捕获那些结合的文库分子,并且然后对任何靶结合的双官能分子进行pcr反应,随后对经复制的dna进行测序。
22.还优选的是,在一些实施方案中,每个芳族环部分包含六元环,而在另一些实施方案中优选的是,每个芳族环部分包含五元环。在另一些实施方案中,5元和6元芳族环部分都存在于双官能分子文库中。在一些优选实施方案中,每个芳族环部分是碳环的,而在另一些优选实施方案中,每个芳族环部分是杂环的。在另外的一些优选实施方案中,至少一个芳族环部分是碳环的并且至少一个芳族环部分是杂环的。
23.在更进一步的优选中,c
4-c
16
脂族羧酸、甲酰胺或掩蔽酮中的至少一个包含与羰基碳原子键合的3元或4元环,并且反应的3元或4元环在形成芳基化键的位置处包含β-c(sp3)-h。
24.下文还公开了在c
4-c
16
脂族羧酸、甲酰胺或掩蔽酮羰基碳原子位置的β位或γ位进行羧酸、甲酰胺或掩蔽酮的水性芳基化反应的方法。
附图说明
25.在形成本公开内容的一部分的附图中,
26.图1a、1b和1c示出了c-h活化的多样性在dna编码文库(del)中的利用。图1a示出了通过顺序c-h活化合成组合化学文库
11
的示意图,图1b是用于获得del
12
的off-dna c-h活化的示意图,以及图1c示意性地示出了用于获得如本文所述的del的顺序的on-dna c-h活化。星号指示在原子处存在手性中心。tbhp,叔丁基过氧化氢;boc,叔丁氧羰基基因;dg,定向基团;以及表示包含键合的dna序列和键的接头。
27.图2a和2b示出了多个c-h活化在del合成中的效用,示出了进一步添加化合物1(其本身是通过c-h活化形成的)以形成化合物1'。图2b示出了在dna键合的接头基团胺与芳族羧酸之间的酰胺形成反应,其示出了本发明on-dna c-h反应的可靠性。
28.图3a和3b示出了在与经碘取代芳族环部分键合的胺封端的系链接头(dna-nh-)与c
4-c
16
羧酸、甲酰胺或掩蔽酮的β-c(sp3)-h之间获得水性芳基化产物和产率。提供进行图3a和3b的反应的标准条件的一般的反应、反应物、催化剂、氧化剂及其浓度以及反应的温度和持续时间在表1中示出。除非另有说明,否则表1中条目1的条件被用作其产率在图3a和图3b二者中示出的反应的标准条件。图3a示出了与胺封端接头(dna-nh-)键合的单个经碘取代芳族环部分与数种不同的甲酰胺活化的c
4-c
16
羧酸的反应的产物和产率,该羧酸各自具有相对于甲酰胺羰基碳原子的β-c(sp3)-h且具有在相对于甲酰胺基氮原子和羧基碳原子二者的α位的取代基r。表1中所示的手性配体l1存在于其产率在图3a中示出的反应中,而不存在于其产率在图3b中示出的反应中。图3b示出了新戊酸或1-丁基环丙烷-1-羧酸a23与数种不同的经碘取代芳族环部分(具有不同的芳族环结构和不同的碘取代基位置)的反应产物和产率。例外:化合物2:相应的a,500mm;对于化合物3至13、18、19和39至45:agtfa,300mm;相应的a,300mm;36小时;对于化合物15:ag3po4,200mm;相应的a,300mm;36小时;对于化合物21:相应的a,300mm;36小时;对于化合物16:agotf,300mm;相应的a,300mm;36小时;对于化合物17:h2o/dma(6/1)。
29.图4a、4b和4c示出了在系链经碘取代芳族环部分的胺封端接头(dna-nh-)与c
4-c
16
羧酸的β-c(sp3)-h之间获得的水性芳基化产物和产率。图4a示出了提供进行图4b和4c的反应的标准条件的反应、反应物、催化剂、氧化剂及其浓度以及反应的温度和持续时间。图4b示出了与胺封端接头(dna-nh-)键合的单个经碘取代芳族环部分与数种不同的c
4-c
16
羧酸反应的产物和产率,该羧酸各自具有β-c(sp3)-h并且在相对于羧基碳原子和甲酰胺基氮原子二者的α位具有取代基r。图4c示出了产物芳基化dna-系链芳族部分、图4b中所示的化合物68和在ph 5.5缓冲液中的甘氨酸甲酯在室温下持续约16至18小时(过夜)的酰胺化以形成化合物73。dmtmm=氯化4-(4,6-二甲氧基-1,3,5三嗪-2-基)-4-甲基吗啉盐酸盐。
30.图5a至5d示出了dna系链的经碘取代芳族部分与包含β-c(sp3)-h和γ-c(sp3)-h基团的掩蔽酮的芳基化反应的结果。除了以下针对特定编号的化合物所说明的以外,使用下文在表3中所示的标准条件进行反应。更特别地,图5a示出了在相对于先前且可逆地被掩蔽为肟(其羟基与两个示例性定向基团dg1和dg2中的任一个键合)的掩蔽酮羰基碳原子的β位获得的水性芳基化产物产率。图5b示出了在相对于类似的掩蔽酮羰基碳原子(其与在不同的环位置具有碘基基团的多种不同的系链的经碘取代芳族环部分反应)的β-位获得的水性芳基化产物产率。图5c示出了从化合物83去除dg1酮羰基封闭基团以形成化合物103的去封闭反应。图5d示出了涉及多个c-h活化反应以通过多个c-h活化和反应构建del多样性的所考虑的合成过程的示意性流程图。图5e示出了化合物106的代表性合成,其中步骤[a)、b)、c)
…
等]的条件如下:
[0031]
a)a1(1000当量),pd(oac)2(10当量),l1(20当量),ag2co3(300当量),naoac(150当量),h2o/dma/hfip(8/1/1),80℃,16小时;b)4-碘苄胺(300当量),
dmtmm(300当量),磷酸盐缓冲液(ph 5.5),室温16小时;c)c10(300当量),pd(oac)2(40当量),l8(40当量),agtfa(500当量),naoac(150当量),h2o/dma(9/1),80℃,20小时;d)苯胺(500当量),丙酮(300当量),磷酸盐缓冲液(ph 6.5),50℃,24小时。
具体实施方式
[0032]
本发明考虑了用于制备包含具有多个不同双官能分子的文库的水性组合物的方法以及文库本身及其制备方法。用于制备所考虑的文库的主要反应是在水性介质中进行的钯(ii)催化芳基化反应。所考虑的芳基化反应在反应底物与芳族或杂芳族碘化物之间形成碳-碳(c-c)键。
[0033]
在所考虑的反应中,不含仲环氮原子的经碘取代芳族环部分的碘基基团被c
4-c
16
脂族羧酸、甲酰胺或掩蔽酮单元的先前β-c(sp3)-h或γ-c(sp3)-h位置的键替代,从而形成新的c-c键。在文献中已报道了在类似反应物之间的钯催化芳基化反应,但其在没有添加水的有机溶剂中进行。认为这是在水性介质中进行这样的反应的首次报道,也是在制备双官能分子和包含其的文库中使用这样的反应的首次报道。
[0034]
方法考虑了以下步骤:使存在于水性组合物的一个或更多个等分试样中的具有根据式a'-b-c'的末端a'和c'的双官能化接头分子b反应。末端c'包含不含仲环氮原子的键合的(系链的)经碘取代芳族环部分,并且末端a'包含标识符核苷酸序列前体z'。接头末端c'经碘取代芳族环部分在一种或更多种反应物c
4-c
16
脂族羧酸、甲酰胺或掩蔽酮单元x'的β-c(sp3)-h或γ-c(sp3)-h位置通过钯催化芳基化进行反应。不同的x'在每个等分试样中反应,不同的核苷酸标识符序列前体z'也是如此与接头的末端a'反应,以形成包含具有式(i)z
nα-a-b-c-x
nα
的双官能分子的水性组合物。
[0035]
在式(i)中,n是x和z的位置标识符并且为1至10的整数,优选1至约6,并且更优选2至约5,使得当n为1时,x和z位于最接近接头b的位置,并且“α”标识一种或更多种特定的反应的c
4-c
16
脂族羧酸、甲酰胺或掩蔽酮单元x和由此形成的双官能分子中相应的一种或更多种标识成对dna序列z。每个z'或z分别与特定的x'或x成对并将其标识。任选地,将如此形成的包含大致等量双官能分子的反应的水性等分试样组合物混合以形成包含大致等同双官能分子混合物的单一组合物。
[0036]
所考虑的掩蔽酮是其羰基基团被保护而在芳基化期间不反应但可容易地去保护以再次提供羰基基团的化合物。示例性的掩蔽羰基基团包括肟、腙和缩酮。当用作肟时,羟基基团本身如通过形成醚键而被保护不发生反应,如下文所示。
[0037]
可用的pd(ii)催化剂在本领域中是公知的。示例性催化剂包括pdcl2、pd(tfa)2、pd(piv)2、[pdcl(c3h5)]2、pdcl2(pph3)2、pd(pph3)4、pd2(dba)3、[pdcl2(mecn)2]、[pd(otf)2·
4mecn]和[pd(bf4)2·
4mecn]。在这些催化剂中,目前优选pd(tea)2、pd(piv)2和pd(oac)2。所考虑的催化剂以催化量使用。基于反应底物的摩尔数,该量通常为约5至约40摩尔百分比,
并且更优选约10至约20摩尔百分比。
[0038]
示例性碱性盐包括naoac、na2co3、nahco3、na2hpo4、na2hpo4、nah2po4、na3po4、khco3、koac、k2co3、k3po4、k2hpo4·
3h2o、li2co3和cs2co3。在这些盐中,naoac和li2co3通常提供最高产率并且是优选的。
[0039]
在芳基化反应完成之后,通常向反应混合物添加清除剂例如二乙基二硫代氨基甲酸钠三水合物以帮助回收钯催化剂。每当量的系链的经碘取代芳族环部分使用约70至约90当量的清除剂实现了钯的回收和初始dna存在的最大量。
[0040]
所考虑的反应介质任选地但优选地包括可促进c-h裂解和后续的官能化步骤二者的配体。有效的c-h官能化通常需要配体和与金属中心配位的底物之间的协同关系。
[0041]
尽管一些反应通常不需要进行,但配体分子的存在通常会提高期望产物的产率。配体通常以基于底物摩尔的约10至约30摩尔百分比存在于反应组合物中。优选地,配体以约20摩尔百分比存在。作为替代,配体以所述钯(ii)催化剂的摩尔量的约1.5至约4倍的量存在。
[0042]
所考虑的钯催化芳基化反应混合物被保持在约70℃至约100℃的温度下持续足以进行亲电插入并形成芳基化反应产物的时间段。更优选地,该温度为约75℃至约90℃。反应时间通常为约15至约30小时,约18至约25小时的时间是常见的。
[0043]
使存在于一种或更多种包含式(i)的双官能分子的水性组合物的一个或更多个等分试样中的羧酸、甲酰胺或掩蔽酮官能团x
nα
与一种或更多种不含仲环氮原子的经碘取代芳族环部分w'(其与在末端c'处存在的相同或不同)反应。一种或更多种前体核苷酸序列标识符y'与z
nα
以形成一种或更多种包含具有式(ii)y
nβ-z
nα-a-b-c-x
nα-w
nβ
的双官能分子的水性组合物。将如此形成的包含大致等量双官能分子的反应的水性等分试样组合物任选地混合以形成包含大致等同双官能分子混合物的单一组合物。每个y'或y分别与特定的w'或w成对并将其标识。“β”标识式(ii)的双官能分子中的一种或更多种特定的反应化学基团w和相应的一种或更多种成对dna序列标识符y。
[0044]
使存在于包含式(ii)的双官能分子的水性组合物或其等分试样中的一种或更多种经碘取代芳族环部分w
nβ
在与先前反应的相同或不同的一种或更多种c
4-c
16
脂族羧酸、甲酰胺或掩蔽酮单元v'的β-c(sp3)-h或γ-c(sp3)-h位置通过钯催化芳基化进行反应。使一种或更多种前体核苷酸序列标识符t'与y
nγ
反应以形成一种或更多种包含式(iii)t
nγ-y
nβ-z
nα-a-b-c-x
nα-w
nβ-v
nγ
的双官能分子的组合物。
[0045]
每个t'或t分别与特定的v'或v成对并将其标识。另外,γ标识双官能分子中的一种或更多种特定的c
4-c
16
脂族羧酸、甲酰胺或掩蔽酮单元v和相应的一种或更多种标识成对dna序列y。
[0046]
关于上述概述的反应序列,应当理解至少一组反应步骤包括使包含双官能分子的水性组合物的多个等分试样单独与不同于在该步骤的另一个等分试样中反应的反应物进行反应,随后将所产生的等分试样组合以形成包含多个构成水性组合物中的所述双官能分子的文库的不同双官能分子的混合物的水性组合物。
[0047]
接头在本文中也称为“头基”。以下示出了本文所用的示例性的头基,以及本文经常使用的其两个缩写和dna-nh2:
[0048][0049]
所示的胺基-nh2是可用于与经碘取代芳族部分反应并将其系链至头基的其余部分的官能团,而dna序列通过公知的寡核苷酸合成方法容易被扩展。
[0050]
优选的双链寡核苷酸标识符z'的核苷酸序列被用于标识在添加至接头上的有机残基“串(string)”中下标“n”位置处芳基化的特定x'。伴随每个下标“n”的下标希腊字母代表1种多至40种不同的化学结构和标识那些结构中的每个结构的相应的寡核苷酸序列。在优选的实践中,在每个位置“n”处使用了1至约20种不同的化学结构以及相同数目的在线性双官能分子另一侧相对于b的相同位置“n”处的标识dna序列。更优选地,使用1至约10种不同的化学结构以及相同数目的存在于双官能分子中的每个位置处的标识dna序列。
[0051]
在一个优选实施方案中,限制性内切核酸酶的核苷酸序列位于x'标识序列的上游和下游二者的侧翼以便由内切核酸酶标识的位置标识符可被容易地去除以标识其一种或更多种反应物-标识核苷酸序列。优选地,相同的内切核酸酶序列存在于标识序列的两侧,因此只需要一种酶来消除双官能分子中给定位置处的标识符序列。
[0052]
应注意的是,每个水性芳基化优选地在相对于羧酸、甲酰胺或掩蔽酮单元的羰基碳的β-c(sp3)-h位置处进行。
[0053]
在式iii的双官能分子中,每个t'或t分别与特定的v'或v成对并将其标识,而y
ni
、zn、a、b、c、xn和w
ni
如前所定义。
[0054]
将包含式iii的双官能分子的两个或更多个等分试样组合以形成包含双官能分子的混合物的水性组合物,从而形成包含文库的水性组合物。如此形成的文库可通过从水性组合物分离如通过冻干、用有机溶剂沉淀和技术人员公知的其他方式来分离。
[0055]
还应注意的是,所考虑的双官能分子文库的合成不需要在如上所示的三个反应步骤循环之后停止,而是可继续进行另外数个遵循以上所述模式的反应循环。优选2个循环至约7个,更优选3个至约5个反应循环。
[0056]
当期望在序列中给定位置处有多个不同的残基时,将包含双官能分子的水性组合物分成至少与期望添加的不同反应物以及每个反应物的标识dna序列以及侧翼位置标识符(如果期望的话)的数目一样多的等分试样。
[0057]
如果期望下一个相邻的位置被混合物占据的话,则将每个反应的等分试样再次分成至少在该步骤使用的反应物的数目。在每个新分的等分试样中,使下一反应物组的成员单独与增长的双官能分子反应,下一个标识每一个的dna序列以及标识特定位置的侧翼限制性位点序列(如果期望的话)也是如此。
[0058]
在以下中使用不同的合成说明了上述变体和其他平行合成(其产物被合并然后划分):
[0059]
brenner and lerner,proc natl acad sci,usa 89:5381-5383(june 1992),美国专利no.5,573,905,no.5,723,598和6,060,596,以及houghten,proc natl acad sci,usa 82:5131-5135(1985),houghten et al.,biotechniques,4(6):522-528(1986),美国专利no.4,631,211和no.5,763,193
[0060]
,其公开内容各自通过引用并入。
[0061]
如果不期望下一个可能的位置是混合物,则将所有先前反应的等分试样组合来提供包含混合的双官能分子的单一组合物。然后那些混合的双官能分子可与单个反应物反应,无需进一步反应即可使用或回收以备后用。
[0062]
因此,t
nγ-y
nβ-z
nα-a是多核苷酸序列,其中特定标识符标识文库的双官能分子中构成c-x
nα-w
nβ-v
nγ
的反应构建单元的反应的芳族环部分和c
4-c
16
脂羧酸、甲酰胺或掩蔽酮单元。优选地,接头b包含寡核苷酸序列,其包含预定的限制性内切核酸酶的识别序列,该酶允许切割t
nγ-y
nβ-z
nα-a标识符的多核苷酸序列。
[0063]
还优选的是,每个标识符寡核苷酸序列为双链dna以及特定标识符t
nγ-y
nβ-z
nα-a多核苷酸序列也为双链dna。还优选地,每个特定标识符双链dna寡核苷酸包含两个限制性内切核酸酶识别位点,一个识别位点在用于合成的反应物的特定标识符核苷酸序列的任一侧。另一个优选的是,与芳族环部分芳基化键合的c
4-c
16
脂族羧酸、甲酰胺或掩蔽酮通过先前存在的相对于该羧酸、甲酰胺或掩蔽酮的羰基基团的β-c(sp3)-h位置而键合。
[0064]
在一些实施方案中还优选的是,每个芳族环部分包含六元环,而在另一些实施方案中优选的是,每个芳族环部分包含五元环。在另一些实施方案中,5元和6元芳族环部分都存在于双官能分子的文库中。在一些优选实施方案中,每个芳族环部分是碳环的,而在另一些优选实施方案中,每个芳族环部分是杂环的。在另外的一些优选实施方案中,至少一个芳族环部分是碳环的并且至少一个芳族环部分是杂环的。
[0065]
在仍进一步的优选中,c
4-c
16
脂族羧酸、碳酰胺或掩蔽酮中的至少一个包含与羰基碳原子键合的3元或4元环,并且反应的3元或4元环在形成芳基化键的位置处包含β-c(sp3)-h。
[0066]
以下还公开了在羧酸、甲酰胺或掩蔽酮羰基碳原子位置的β位或γ位进行c
4-c
16
脂族羧酸、甲酰胺或掩蔽酮的水性芳基化反应的方法。
[0067]
使不含仲环氮原子的经碘取代芳族环部分、包含β-c(sp3)-h或γ-c(sp3)-h的反应物(即c
4-c
16
脂族羧酸、甲酰胺或掩蔽酮)、催化量的钯(ii)催化剂、银盐、碱性碱金属盐以及任选存在的与水性介质中的pd
2+
离子相互作用的配体在水性介质中溶解或分散以形成水性反应介质。使水性反应介质在约室温(约20℃)至约100℃并且优选在约70℃至约100℃的温度下维持约15至约30小时的时间段,以提供产物不含仲环氮原子的芳族环部分,所述仲环氮原子键合在由碘取代基正式占据的环位置与由c
4-c
16
脂族羧酸、甲酰胺或掩蔽酮的β-c(sp3)-h或γ-c(sp3)-h占据的先前位置之间。
[0068]
在一个优选实施方案中,包含β-c(sp3)-h或γ-c(sp3)-h的c
4-c
16
脂族羧酸、甲酰胺或掩蔽酮以相对于经碘取代芳族部分10:1至约1200:1的摩尔过量存在于水性反应介质中。在另一个优选实施方案中,银盐和碱性碱金属盐以约2:1至约4:1的摩尔比存在于水性反应介质中,并且银盐与经碘取代芳族部分的摩尔比为约100:1至约400:1。
[0069]
在另一个优选实施方案中,配体以钯(ii)催化剂的摩尔量的约1.5至约4倍的量存在。优选的配体选自以下中的一种或更多种:
[0070][0071]
在另一个优选实施方案中,不含仲环氮原子的经碘取代芳族环部分包含单个5元或6元芳族环、自身与描述为“dna
‑”
的含dna接头连接并且选自以下中的一种或更多种:
[0072][0073]
在一些优选实施方案中,包含β-c(sp3)-h或γ-c(sp3)-h的掩蔽酮选自以下中的一种或更多种:
[0074]
[0075][0076]
结果
[0077]
由于羧酸和(杂)芳基碘化物是dna编码文库的普遍构建单元,因此首先通过pd催化的β-c-h芳基化研究了dna系链的芳基碘化物与游离羧酸的偶联。除了需要使化学适于水性条件之外,还提出了严峻的挑战,特别是dna对低ph值和热的有限的稳定性、干扰dna碱基反应性的可能性以及dna系链组分的高稀释度。尽管如此,还是决定围绕游离羧酸来发展这种化学。
[0078]
具有β-c(sp3)-h或γ-c(sp3)-h的一些举例说明性可用羧酸在下表中示出。
[0079][0080]
通过先前c-h芳基化工作
14
的指导,以下筛选了钯源、配体、银源、碱和共溶剂,如表1和表2中所示。
[0081]
优化的条件以78%的产率得到产物化合物1而无新戊酸的二芳基化或三芳基化(条目1,表1)。钯、银和热是强制性的(条目2至4,表1)。不需要配体(条目5,表1),但氨基酸来源的配体提高了产率,发现配体l1是最佳的。
[0082]
表1
[0083]
[0084][0085]
由于使用了过量的银盐和钯,主要的副反应原脱碘(protodeiodination)(例如,化合物s1b)总是以很小的程度存在。不包含碘化物的化合物s1b经受反应条件并完整恢复,证实了偶联发生在芳基碘化物而不是在dna标签上的某些未确定的位置(条目6,表1)。二硫代氨基甲酸盐由于其与钯的配位更强而将dna从dna-钯复合物中释放,导致了不溶性复合物。
[0086]
在每次反应之后,将混合物与二乙基二硫代氨基甲酸钠三水合物一起孵育以清除钯。dna回收水平受到二硫代氨基甲酸盐清除剂负载的显著影响。
[0087]
检查图3a中所示的结果,与季碳原子相邻的多种羧酸适用于这种化学,其包括包含羟基、醚或氟的那些(化合物2至14)。然而,与仲碳或叔碳相邻的酸以《30%的产率反应(化合物15至16)。重要的是,环丙烷羧酸和环丁烷羧酸(期望作为烯烃电子等排体(isostere))是能胜任的偶联配偶体(化合物17至21)。
[0088]
众所周知,pd催化的β-c-h芳基化机制仅产生顺式立体异构体。lcms分析无法确定手性配体l1是否产生任何绝对立体感应。
[0089]
图3b中所示的结果说明芳基碘化物取代模式是灵活的(化合物22至28,39至44)。尽管先前发表的有机溶剂中的反应条件不可偶联杂芳基碘化物
24,25
,但认为忍受dna的条件(包含氮杂环的碱基)应允许杂芳基碘化物(例如,吡啶和吡唑)的偶联。确实是这样;杂芳基碘化物在相同的反应条件下成功地与羧酸反应(化合物29至38,42至44)。由于芳基碘化物和杂芳基碘化物在相同条件下反应,因此它们都可以存在于所考虑的del裂池合成中。
[0090]
如上表1的部分所示,用于图3a和3b的反应的标准反应条件是基于以与1000当量(equivalent,equiv)的包含β-c(sp3)-h或γ-c(sp3)-h的羧酸反应的10纳摩尔(nanomole,nmol)的dna连接的芳族碘化物开始。这种反应在存在以下的情况下发生:在包含以8:1:1的比例存在的水、二甲基乙酰胺和六氟-2丙醇的介质中溶解或分散的10当量pd()ac)2、120当量配体、300当量ag2co3、150当量naoac。反应在80℃的温度下持续16小时的时间。
[0091]
除非另有说明,否则那些条件被用作标准条件。对于化合物2:羧酸以500当量存在。对于化合物3至14、18、19和39至44:agtfa,300当量;羧酸300当量,36小时。对于化合物15:ag3po4,200当量;羧酸,300当量;36小时。对于化合物21:羧酸,300当量;36小时。对于化合物16:agotf,300当量;羧酸,300当量;36小时。对于化合物17:h2o/dma(6/1)。
[0092]
表2
[0093]
[0094][0095]
在没有配体的情况下对银源、碱和共溶剂的重新评价导致以69%产率提供化合物45的优化条件(条目1,表2)。钯对这种转变是必不可少的(条目2,表2)。银盐和碱不是严格需要的,但对产率有显著影响(条目3至9,表2)。出乎意料的是,发现这种反应在室温下也进行良好(条目10,表2)。
[0096]
来源于环丙烷羧酸或环丁烷羧酸和广泛的a-氨基酸的酰胺在加热和室温二者下都能顺利反应(化合物45至56),这在图4a中所示的产率中也可以看出。pd催化芳基化仅在来自酰胺的β-c-h键处进行;ac-l-val-oh的尝试偶联未得到芳基化产物化合物59,表明未发生α-芳基化。两个具有相同质量的lc峰是由于在c-h芳基化之后产生了非对映体。为了证明这一点,进行了具有代表性的off-dna反应以合成产物化合物51。正如预期的那样,观察到非对映体的混合物,但是由于反应温度不同该比例略低。
[0097]
虽然关注了来源于α-氨基酸和含有环丙基或环丁基环(期望作为烯烃电子等排体)的酰胺,但化学反应可扩展到其他烷基羧酸(化合物57和58)和β-氨基酸(化合物60)。dna系链的芳基碘化物上的不同芳烃取代模式是可忍受的(化合物61至65),如在图4b中所示的产率中看到的。
[0098]
与羧酸的β-c-h芳基化情况一样,用于酰胺芳基化的dna忍受条件也可用于偶联dna系链的杂芳基碘化物例如吡啶和吡唑(化合物66至72)。如果期望的话,产物的羧酸可被进一步修饰(化合物73),示于图4c。
[0099]
已开发出用于羧酸和酰胺的与dna相容的c(sp3)-h芳基化,注意力转向了以类似的dna相容的c(sp3)-h芳基化使用酮。酮是用于构建del的有用单体,因为它们可通过还原性胺化被一步加工。通过先前的使用氨基氧乙酸作为可去除的定向基团以募集钯来活化酮的β-c-h键的工作
16
的指导,创建并优化了这种反应的dna忍受版本。
[0100]
在表3和图5a至图5d中所示的经优化的反应以62%产率得到了芳基化产物化合物83(条目1,表3,如下)。这种反应需要钯和热(条目2和3,表3),并且受银盐的强烈影响(条目4至6,表3);配体和碱基的作用较小(条目7和8,表3)。还发现配体l8减少了dna的降解并提供更清楚的lc迹线(trace)。尽管大量过量的钯通常与dna标签的降解有关,但这种化学反应在20mm pd/l(条目1,40当量)下比在30当量(条目9,表3)下得到了更高的产率。
[0101]
表3
[0102][0103][0104]
以上条件在不同的背景中包括在非环酮衍生物上(化合物74至77、84至89)、在简单或复杂的环旁边的位置处(化合物78至82、90、91)以及在简单或复合环上(化合物83、92)影响β-c-h芳基化,如通过图5a中所示的产率看到的。待芳基化的酮允许有广泛的官能团,其包括酯、醚、缩醛和酰胺。
[0105]
带有β-季铵中心的酮衍生物也可被γ-芳基化(化合物93),如图5a中所示。图5b中所示的产率说明了dna系链的芳基碘化物接受不同的取代模式(化合物94至97)并且杂芳基碘化物可在相同条件下反应(化合物98至102)。
[0106]
将肟醚转化回酮的能力对于在del构建中实施这种化学反应至关重要。发现这些肟醚在苯胺和丙酮的存在下容易水解(化合物83至103),可能是通过苯胺的平衡转移和用丙酮捕获游离氨基氧乙酸
17
。这种反应在图5c中示出。
[0107]
这些c(sp3)-h活化反应中的每一个作为del合成的新的断开都可并入独特的结构基序。del合成中多个c(sp3)-h活化的组合可进一步增强多样性。因此,开始了由羧酸的β-c-h芳基化、酰胺形成、掩蔽酮的β-c-h芳基化和酮去保护组成的dna多步合成,以表明如何将这些c-h活化化学组合以开发多种类药性化合物的大的del。代表性的类似物合成在图5d中示出。
[0108]
因此,吡啶基碘化物化合物s18和新戊酸偶联以形成中间体化合物31,并且酰胺与对碘苄胺偶联,然后建立第二个c-h活化事件。与掩蔽环丁基酮偶联得到肟醚化合物105,其水解显示酮化合物106在4个步骤中的总产率为6%,如图5e中所示。
[0109]
以上仅是技术人员可通过与常见的dna编码文库构建步骤(例如酰胺形成或还原性胺化)组合使用顺序的多个c-h芳基化步骤进行设计的许多序列中的一个。重要的是,使用dna系链的芳基碘化物进行c-h芳基化的能力意味着可实现全功率裂池组合性合成。
[0110]
为了评价c-h活化化学与del合成的dna相容性,将选择的经化学修饰on-dna类似
物组(c-h芳基化产物1、45和83)以及其起始芳基碘化物类似物s1a与65聚体dsdna酶促连接,使得所得寡聚体的长度与3循环del构建的编码标签大致相等。所有四个连接反应均顺利进行,表明了化学对可编码性没有显著影响。为了确定在暴露于c-h活化条件之后剩余的可扩增dna的量,将来自1、45和83的连接产物通过pcr扩增并与s1a(未经处理的对照)的那些进行比较。所有三个反应都显示出满意的pcr活力(剩余60%至80%的可扩增dna)。此外,sanger测序读数还证实了它们的核碱基序列结构的完整性。
[0111]
由于纯化在裂池合成中是一个固有的困难过程,因此dna相容的反应所需的反应性必须不含会使分析复杂化的未经鉴定的副产物。在这种情况下,通过我们的反应平台产生的主要副产物仅由起始材料或其原始脱卤衍生物组成。最后,我们能够通过我们的on-dna c-h芳基化平台以中等和综合有用的产率来获得所有产物;高于在del合成中被认为可行的25%的阈值。
10f
还令人欣慰的是,我们能够从qpcr实验中获得60%至80%的dna回收,高于在这些过程实践中被认为可行的可接受的30%的阈值。
4c
总之,这些有希望的结果进一步表明了我们的del相容的c(sp3)-h活化平台的可行性,使从业者能够以模块化方式快速生成结构复杂性和多样性。
[0112]
综上所述,开发了羧酸、酰胺和酮的del相容的c(sp3)-h活化反应。配体对于在del条件下的反应性至关重要。这些方案与期望用于改进类药性性质的小环和杂环偶联配偶体的c(sp3)-h键相容。用于del合成的顺序的c(sp3)-h活化为构建包含高c(sp3)-h特征的化学多样性提供了独特的工具。
[0113]
1.一般信息
[0114]
设备和化学品
[0115]
使用模块化加热块(64孔)加热pcr管以运行dna反应。10k变速迷你离心机(bt604)购自btlab systems。使用9mm螺纹聚丙烯小瓶和螺帽将样品呈递至hplc-ms。六氟异丙醇(hexafluoroisopropanol,hfip)购自oakwood。n,n-二甲基-乙酰胺(n,n-dimethyl-acetamide,dma)获自honeywell。n,n-二甲基甲酰胺(n,n-dimethylformamide,dmf)和乙腈(ch3cn)是通过使先前脱气的溶剂通过经活化的氧化铝柱获得的。所有反应均使用去离子水。pd(oac)2购自strem chemicals,inc。ag2co3、agoac、agtfa和ag3po4获自sigma-aldrich。所有其他试剂均以最高的商业质量购买而无需进一步纯化即可使用。配体是通过先前公布的方案制备的,其中一些现在可商购获得的除外。经碘取代杂芳族酸获自pfizer。带有定向基团的羧酸、酰胺和酮是通过先前公布的方案合成的,一些也可商购获得的除外。dmtmm=4-(4,6-二甲氧基-1,3,5三嗪-2-基)-4-甲基吗啉盐酸盐。
[0116]
dna头部(headpiece)材料
[0117]
dna头部(5'-/5phos/gagtca/isp9/-iuniamm/-isp9/-tgactccc-3',如下)获自biosearch technologies,petaluma,ca。缩写的dna头部如下所示。
[0118][0119]
dna样品的分析
[0120]
dna浓度:
[0121]
假定在反应之后dna总回收率为100%,将进行hplc-ms分析的dna样品制备为在h2o中的0.1mm。
[0122]
分析:
[0123]
在60℃下在waters
ⅰ‑
class lc上对1微升的dna溶液进行分析,waters beh c18为在(a)水和(b)甲醇中的114mm hfip和14mm et3n(0.3ml/分钟,10%至26%b,10分钟内)。通过计算对应于产物峰的260nm处的uv吸光度的百分比来确定产率,忽略dna产物之间可能的uv吸收系数差异并假定100%质量回收率。峰标识是通过esi使用[m]
3-离子确定的。
[0124]
去卷积:
[0125]
使用masslynx
tm v4.1软件进行数据可视化和整合。
[0126]
产率计算:
[0127]
忽略所有dna产物的uv系数差异并假设dna总回收率为100%,dna产物的产率从uv吸收痕量(260nm)峰面积使用下式来确定:
[0128][0129]
ms去卷积:
[0130]
鉴于观察到多电荷(负)质量,在所有情况下三电荷质量被确定为基峰。观察到的m/z可计算为m/z=[m]/z-1.00794。
[0131]
2.配体结构l1至l13
[0132][0133]
配体l3、l5、l6至l13购自sigma-aldrich、nova biochem、tci和combi-blocks inc。配体l1
14b
、l2
18
、l4
19
根据先前的报道进行合成。
[0134]
3.dna缀合的芳基碘化物的制备
[0135]
3.1用于dna缀合的芳基碘化物的一般性操作1
[0136][0137]
材料
[0138]
头部:20mm,在水中
[0139]
羧酸钠:1.0m,在水中[将1mmol酸添加到1.0ml naoh(40mg)水溶液中]
[0140]
4-(4,6-二甲氧基-1,3,5三嗪-2-基)-4-甲基吗啉盐酸盐(dmtmm):1.0m,在水中(294.7mg dmtmm溶解在1ml h2o中)
[0141]
硼酸盐缓冲液:100mm,在h2o中
[0142]
一般性操作1
[0143]
1)对于头部溶液(400nmol,20,在室温下保持3小时。
[0144]
2)向混合物添加5m nacl,在-20℃下储存)。然后将混合物在冰箱中在-20℃下储存超过30分钟。
[0145]
3)在微型离心机中以10000rpm在4℃下将样品离心7分钟。弃去上清液并将沉淀(precipitate)在真空下干燥。然后将沉淀物(pellet)溶解在去离子的n,n-中,在70℃下加热12小时。
[0146]
4)冷却至室温,顺序地添加5m nacl,并将所得混合物在-20℃下储存30分钟。将混合物在4℃下以10000rpm离心7分钟,然后除去所得上清液,并将沉淀在真空下干燥。沉淀物无需进一步纯化即可用于下一研究。
[0147]
5)hplc-[0148]
(10mm),
[0149]
以制备浓度在0.1mm的测试样品。
[0150]
3.2 s1至s23的结构
[0151][0152]
经碘取代芳族酸s1至s13购自sigma-aldrich、oakwood、tci和combi-blocks inc。杂芳族酸s14至s23获自pfizer。
[0153]
3.3 s1至s23的lc痕量和质量表征
[0154]
s1a的lc痕量和质量
[0155][0156]
遵循一般性操作1。
[0157]
产率:85%
[0158]
精确质量:5178.8211
[0159]
三电荷质量[m]/3-1.00794,计算值1725.2658;观测值1725.2783。
[0160][0161]
遵循一般性操作1。
[0162]
产率:83%
[0163]
精确质量:5052.9244
[0164]
三电荷质量[m]/3-1.00794,计算值1683.3002;观测值1683.3007。
[0165][0166]
遵循一般性操作1。
[0167]
产率:83%
[0168]
精确质量:5178.8211
[0169]
三电荷质量[m]/3-1.00794,计算值1725.2658;观测值1725.2783。
[0170][0171]
遵循一般性操作1。
[0172]
产率:78%
[0173]
精确质量:5192.8367
[0174]
三电荷质量[m]/3-1.00794,计算值1729.9376;观测值1729.9423。
[0175][0176]
遵循一般性操作1。
[0177]
产率:74%
[0178]
精确质量:5164.8054
[0179]
三电荷质量[m]/3-1.00794,计算值1720.5939;观测值1720.6038。
[0180][0181]
遵循一般性操作1。
[0182]
产率:69%
[0183]
精确质量:5178.8211
[0184]
三电荷质量[m]/3-1.00794,计算值1725.2658;观测值1725.2783。
[0185][0186]
遵循一般性操作1。
[0187]
产率:67%
[0188]
精确质量:5198.7664
[0189]
三电荷质量[m]/3-1.00794,计算值1731.9142;观测值1731.9187。
[0190][0191]
遵循一般性操作1。
[0192]
产率:83%
[0193]
精确质量:5164.8054
[0194]
三电荷质量[m]/3-1.00794,计算值1720.5939;观测值1720.6038。
[0195][0196]
遵循一般性操作1。
[0197]
产率:76%
[0198]
精确质量:5178.8211
[0199]
三电荷质量[m]/3-1.00794,计算值1725.2658;观测值1725.2783。
[0200][0201]
遵循一般性操作1。
[0202]
产率:71%
[0203]
精确质量:5198.7664
[0204]
三电荷质量[m]/3-1.00794,计算值1731.9142;观测值1731.9187。
[0205][0206]
遵循一般性操作1。
[0207]
产率:85%
[0208]
精确质量:5164.8054
[0209]
三电荷质量[m]/3-1.00794,计算值1720.5939;观测值1720.6038。
[0210][0211]
遵循一般性操作1。
[0212]
产率:75%
[0213]
精确质量:5178.8211
[0214]
三电荷质量[m]/3-1.00794,计算值1725.2658;观测值1725.2783。
[0215][0216]
遵循一般性操作1。
[0217]
产率:71%
[0218]
精确质量:5182.7960
[0219]
三电荷质量[m]/3-1.00794,计算值1726.5907;观测值1726.6053。
[0220][0221]
遵循一般性操作1。
[0222]
产率:55%
[0223]
精确质量:5182.7960
[0224]
三电荷质量[m]/3-1.00794,计算值1726.5907;观测值1726.6053。
[0225][0226]
遵循一般性操作1。
[0227]
产率:57%
[0228]
精确质量:5165.8007
[0229]
三电荷质量[m]/3-1.00794,计算值1720.9256;观测值1720.9265。
[0230][0231]
遵循一般性操作1。
[0232]
产率:65%
[0233]
精确质量:5165.8007
[0234]
三电荷质量[m]/3-1.00794,计算值1720.9256;观测值1720.9265。
[0235][0236]
遵循一般性操作1。
[0237]
产率:79%
[0238]
精确质量:5165.8007
[0239]
三电荷质量[m]/3-1.00794,计算值1720.9256;观测值1720.9265。
[0240][0241]
遵循一般性操作1。
[0242]
产率:59%
[0243]
精确质量:5209.8269
[0244]
三电荷质量[m]/3-1.00794,计算值1735.6010;观测值1735.6018。
[0245][0246]
遵循一般性操作1。
[0247]
产率:56%
[0248]
精确质量:5165.8007
[0249]
三电荷质量[m]/3-1.00794,计算值1720.9256;观测值1720.9265。
[0250][0251]
遵循一般性操作1。
[0252]
产率:77%
[0253]
精确质量:5168.8116
[0254]
三电荷质量[m]/3-1.00794,计算值1721.9293;观测值1721.9290。
[0255]
[0256]
遵循一般性操作1。
[0257]
产率:76%
[0258]
精确质量:5168.8116
[0259]
三电荷质量[m]/3-1.00794,计算值1721.9293;观测值1721.9459。
[0260][0261]
遵循一般性操作1。
[0262]
产率:69%
[0263]
精确质量:5168.8116
[0264]
三电荷质量[m]/3-1.00794,计算值1721.9293;观测值1721.9290。
[0265][0266]
遵循一般性操作1。
[0267]
产率:67%
[0268]
精确质量:5154.7847
[0269]
三电荷质量[m]/3-1.00794,计算值1717.2536;观测值1717.2589。
[0270][0271]
遵循一般性操作1。
[0272]
产率:69%
[0273]
精确质量:5170.7618
[0274]
三电荷质量[m]/3-1.00794,计算值1722.5793;观测值1722.5918。
[0275]
4.用于游离羧酸的on-dna c-h芳基化的实验部分
[0276]
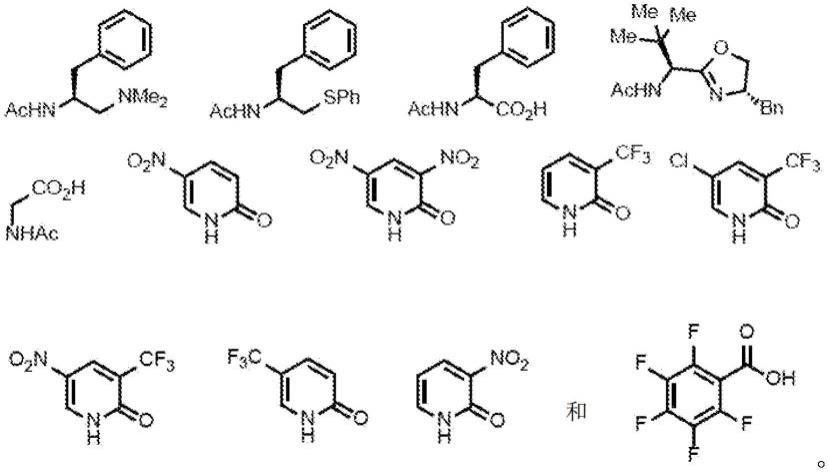
4.1游离羧酸a1至a38的底物结构
[0277][0278]
羧酸获自商业来源或遵循文献操作合成。
14b,20
[0279]
4.2条件优化
[0280]
表4.a1浓度的评价
[0281]
[0282][0283]
表5.碱基的评价
[0284][0285][0286]
表6.pd/l浓度的评价
[0287]
[0288][0289]
表7.标准条件的评价
[0290][0291][0292]a仅s1b完全回收。
[0293]
4.3 dna回收研究
[0294]
表8.dna回收的评价
[0295][0296][0297]a总dna回收率是以s1a作为标准计算的。
[0298]
4.4用于游离羧酸的on-dna c-h芳基化的一般性操作2
[0299]
条件a
[0300][0301]
材料
[0302]
dna缀合的芳基碘化物s:10mm,在h2o中
[0303]
羧酸a:3m,在dma中(注意:高浓度可提高总体积)
[0304]
l1:200mm,在六氟异丙醇(hfip)中(4.4mg,在pd(oac)2中
[0305]
naoac:1.5m,在h2o中)
[0306]
二乙基二硫代氨基甲酸钠三水合物(清除剂):1m,在h2o中(225.3mg,在1.0ml h2o中)
[0307]
操作
[0308]
1)向制备的agtfa(300当量,0.66mg)添加pd(oac)
2-干燥,羧酸a dna缀合的芳基碘化物s(10nmol,1naoac
[0309]
d。最后,l1溶液(20
[0310]
并将反应混合物在80℃下加热36小时。
[0311]
2)将反应混合物冷却至室温
[0312]
将所得混合物在80℃下再加热30分钟。
[0313]
3)将反应混合物冷却至室温,并添加5m nacl溶液(按体积计10%。将混合物在冰箱-20℃下储存超过30分钟。
[0314]
4)将样品在微型离心机中以10000rpm离心7分钟。弃去上清液并将沉淀在真空下干燥。将所得dna沉淀物再溶解在h2在微型离心机中以10000rpm 2分钟。an-ms。
[0315]
条件b:
[0316][0317]
材料
[0318]
s1a:10mm,在h2o中
[0319]
环丙烷甲酸(a22):3m,在h2o中
[0320]
l1:200mm,在hfip中
[0321]
pd(oac)2:100mm,在hfip中
[0322]
naoac:1.5m,在h2o中)
[0323]
二乙基二硫代氨基甲酸钠三水合物(清除剂):1m,在h2o中
[0324]
操作
[0325]
添加pd(oac)2,l1溶液(20
[0326]-干燥,添加ag2co3(300当量,0.63mg),然后a22(1000当量,3.3
[0327]
s1a(10nmol,1naoac水性溶液(150
[0328]
涡旋。将反应混合物在80℃下加热16小时。
[0329]
2)将反应混合物冷却至室温,9
[0330]
将所得混合物在80℃下再加热30分钟。
[0331]
3)将反应混合物冷却至室温,并添加5m nacl溶液(按体积计10%。将混合物在冰箱中在-20℃下储存超过30分钟。
[0332]
4)将样品在微型离心机中以10000rpm离心约7分钟。弃去上清液并将沉淀在真空下干燥。将所得dna沉淀物再次溶解在h2在微型离心机中以10000rpm 2分钟。an-ms。
[0333]
4.5游离羧酸的范围和限制
[0334]
表9.游离羧酸的范围和限制
[0335]
[0336]
[0337]
[0338]
[0339]
[0340][0341]a使用a2(500mm);b遵循条件b;c使用a26(1000mm),16小时。n.d.=未检测到。
[0342]
4.6 1至51的lc痕量和质量表征
[0343]
1的lc痕量和质量
[0344][0345]
使用a1(1000mm)遵循一般性操作2(条件a),不同之处在于使用ag2co3代替agtfa。
[0346]
产率:-[0347]
比率(产物/脱碘/芳基碘化物):66/2/4
[0348]
精确质量:5152.9766
[0349]
三电荷质量[m]/3-1.00794,计算值1716.6509;观测值1716.6649。
[0350]
2的lc痕量和质量
[0351][0352]
使用a2(500mm)遵循一般性操作2(条件a),不同之处在于使用ag2co3代替agtfa。
[0353]
产率:-[0354]
比率(产物/脱碘/芳基碘化物):53/6/24
[0355]
精确质量:5166.9927
[0356]
三电荷质量[m]/3-1.00794,计算值1721.3230;观测值1721.3342。
[0357]
3的lc痕量和质量
[0358][0359]
使用a3遵循一般性操作2(条件a)。
[0360]
产率:-[0361]
比率(产物/脱碘/芳基碘化物):61/3/4
[0362]
精确质量:5181.0081
[0363]
三电荷质量[m]/3-1.00794,计算值1725.9948;观测值1725.9928。
[0364]
4的lc痕量和质量
[0365][0366]
使用a4遵循一般性操作2(条件a)。
[0367]
产率:-[0368]
比率(产物/脱碘/芳基碘化物):48/5/6
[0369]
精确质量:5195.0238
[0370]
三电荷质量[m]/3-1.00794,计算值1730.6667;观测值1730.6748。
[0371]
5的lc痕量和质量
[0372][0373]
使用a5遵循一般性操作2(条件a)。
[0374]
产率:-[0375]
比率(产物/脱碘/芳基碘化物):41/10/18
[0376]
精确质量:5195.0238
[0377]
三电荷质量[m]/3-1.00794,计算值1730.6667;观测值1730.6748。
[0378]
6的lc痕量和质量
[0379][0380]
使用a6遵循一般性操作2(条件a)。
[0381]
产率:-[0382]
比率(产物/脱碘/芳基碘化物):27/12/10
[0383]
精确质量:5214.9925
[0384]
三电荷质量[m]/3-1.00794,计算值1737.3229;观测值1737.3254。
[0385]
7的lc痕量和质量
[0386][0387]
使用a7遵循一般性操作2(条件a)。
[0388]
产率:-[0389]
比率(产物/脱碘/芳基碘化物):16/4/5
[0390]
精确质量:5168.9718
[0391]
三电荷质量[m]/3-1.00794,计算值1721.9827;观测值1721.9800。
[0392]
8的lc痕量和质量
[0393][0394]
使用a8遵循一般性操作2(条件a)。
[0395]
产率:-[0396]
比率(产物/脱碘/芳基碘化物):28/3/11
[0397]
精确质量:5193.0081
[0398]
三电荷质量[m]/3-1.00794,计算值1729.9948;观测值1729.9934。
[0399]
7的lc痕量和质量
[0400][0401]
使用a9遵循一般性操作2(条件a)。
[0402]
产率:-[0403]
比率(产物/脱碘/芳基碘化物):39/4/6
[0431]
比率(产物/脱碘/芳基碘化物):52/4/5
[0432]
精确质量:5211.0187
[0433]
三电荷质量[m]/3-1.00794,计算值1735.9983;观测值1736.0114。
[0434]
12的lc痕量和质量
[0435][0436]
使用a14遵循一般性操作2(条件a)。
[0437]
产率:-[0438]
比率(产物/脱碘/芳基碘化物):54/2/10
[0439]
精确质量:5213.0144
[0440]
三电荷质量[m]/3-1.00794,计算值1736.6635;观测值1736.6769。
[0441]
13的lc痕量和质量
[0442][0443]
使用a15遵循一般性操作2(条件a)。
[0444]
产率:-[0445]
比率(产物/脱碘/芳基碘化物):42/5/6
[0446]
精确质量:5263.0112
[0447]
三电荷质量[m]/3-1.00794,计算值1753.3291;观测值1753.3391。
[0448]
14的lc痕量和质量
[0449][0450]
使用a16遵循一般性操作2(条件a)。
[0451]
产率:-[0452]
比率(产物/脱碘/芳基碘化物):52/3/12
[0453]
精确质量:5193.0081
[0454]
三电荷质量[m]/3-1.00794,计算值1729.9948;观测值1730.0104。
[0455]
15的lc痕量和质量
[0456][0457]
使用a17遵循一般性操作2(条件a),不同之处在于使用ag3po4代替agtfa。
[0458]
产率:-[0459]
比率(产物/脱碘/芳基碘化物):24/7/5
[0460]
精确质量:5124.9455
[0461]
三电荷质量[m]/3-1.00794,计算值1707.3072;观测值1707.3116。
[0462]
lc痕量和质量
[0463][0464]
使用a18遵循一般性操作2(条件a),不同之处在于使用ag2co3代替agtfa。
[0465]
产率:-[0466]
比率(产物/脱碘/芳基碘化物):24/6/6
[0467]
精确质量:5138.9612
[0468]
三电荷质量[m]/3-1.00794,计算值1711.9791;观测值1711.9851。
[0469]
lc痕量和质量
[0470][0471]
使用a19遵循一般性操作2(条件a),不同之处在于使用agoac代替agtfa。
[0472]
产率:-[0473]
比率(产物/脱碘/芳基碘化物):24/17/3
[0474]
精确质量:5152.9768
[0475]
三电荷质量[m]/3-1.00791,计算值1716.6510;观测值1716.6649。
[0476]
lc痕量和质量
[0477][0478]
使用a20遵循一般性操作2(条件a),不同之处在于使用agoac代替agtfa。
[0479]
产率:-[0480]
比率(产物/脱碘/芳基碘化物):20/16/17
[0481]
精确质量:5166.9925
[0482]
三电荷质量[m]/3-1.00794,计算值1721.3229;观测值1721.3342。
[0483]
16的lc痕量和质量
[0484][0485]
使用a21遵循一般性操作2(条件a),不同之处在于使用agotf代替agtfa。
[0486]
产率:-[0487]
比率(产物/脱碘/芳基碘化物):22/27/14
[0488]
精确质量:5206.9486
[0489]
三电荷质量[m]/3-1.00794,计算值1734.6416;观测值1734.6637。
[0490]
17的lc痕量和质量
[0491][0492]
使用a22遵循一般性操作2(条件b)。
[0493]
产率:-[0494]
比率(产物/脱碘/芳基碘化物):35/9/7
[0495]
精确质量:5136.9455
[0496]
三电荷质量[m]/3-1.00794,计算值1711.3072;观测值1711.3074。
[0497]
18的lc痕量和质量
[0498][0499]
使用a23遵循一般性操作2(条件a)。
[0500]
产率:-[0501]
比率(产物/脱碘/芳基碘化物):40/3/21
[0502]
精确质量:5193.0081
[0503]
三电荷质量[m]/3-1.00794,计算值1729.9948;观测值1729.9934。
[0504]
19的lc痕量和质量
[0505][0506]
使用a24遵循一般性操作2(条件a)。
[0507]
产率:-[0508]
比率(产物/脱碘/芳基碘化物):34/0/29
[0509]
精确质量:5255.0238
[0510]
三电荷质量[m]/3-1.00794,计算值1750.6667;观测值1750.6652。
[0511]
lc痕量和质量
[0512][0513]
使用a25遵循一般性操作2(条件a),不同之处在于使用ag2co3代替agtfa。
[0514]
产率:-[0515]
比率(产物/脱碘/芳基碘化物):18/15/6
[0516]
精确质量:5164.9768
[0517]
三电荷质量[m]/3-1.00794,计算值1720.6510;观测值1720.6547。
[0518]
20的lc痕量和质量
[0519][0520]
使用a26(1000mm)遵循一般性操作2(条件a),不同之处在于使用ag2co3代替agtfa。
[0521]
产率:-[0522]
比率(产物/脱碘/芳基碘化物):33/23/5
[0523]
精确质量:5150.9612
[0524]
三电荷质量[m]/3-1.00794,计算值1715.9791;观测值1715.9694。
[0525]
21的lc痕量和质量
[0526][0527]
使用a27遵循一般性操作2(条件a),不同之处在于使用ag2co3代替agtfa。
[0528]
产率:-[0529]
比率(产物/脱碘/芳基碘化物):34/15/18
[0530]
精确质量:5178.9925
[0531]
三电荷质量[m]/3-1.00794,计算值1725.3229;观测值1725.3293。
[0532]
22的lc痕量和质量
[0533][0534]
使用s2和a1(1000mm)遵循一般性操作2(条件a),不同之处在于使用ag2co3代替agtfa。
[0535]
产率:-[0536]
比率(产物/脱碘/芳基碘化物):46/31/4
[0537]
精确质量:5152.9768
[0538]
三电荷质量[m]/3-1.00794,计算值1716.6510;观测值1716.6649。
[0539]
lc痕量和质量
[0540][0541]
使用s3和a1(1000mm)遵循一般性操作2(条件a),不同之处在于使用ag2co3代替
agtfa。
[0542]
产率:-[0543]
比率(产物/脱碘/芳基碘化物):57/3/15
[0544]
精确质量:5166.9925
[0545]
三电荷质量[m]/3-1.00794,计算值1721.3229;观测值1721.3342。
[0546]
lc痕量和质量
[0547][0548]
使用s10和a1(1000mm)遵循一般性操作2(条件a),不同之处在于使用ag2co3代替agtfa。
[0549]
产率:-[0550]
比率(产物/脱碘/芳基碘化物):57/8/23
[0551]
精确质量:5138.9612
[0552]
三电荷质量[m]/3-1.00794,计算值1711.9791;观测值1711.9851。
[0553]
25的lc痕量和质量
[0554][0555]
使用s4和a1(1000mm)遵循一般性操作2(条件a),不同之处在于使用ag2co3代替agtfa。
[0556]
产率:-[0557]
比率(产物/脱碘/芳基碘化物):35/24/3
[0558]
精确质量:5138.9612
[0559]
三电荷质量[m]/3-1.00794,计算值1711.9791;观测值1711.9851。
[0560]
26的lc痕量和质量
[0561][0562]
使用s6和a1(1000mm)遵循一般性操作2(条件a),不同之处在于使用ag2co3代替agtfa。
[0563]
产率:-[0564]
比率(产物/脱碘/芳基碘化物):35/22/3
[0565]
精确质量:5172.9222
[0566]
三电荷质量[m]/3-1.00794,计算值1723.2995;观测值1723.3057。
[0567]
27的lc痕量和质量
[0568][0569]
使用s7和a1(1000mm)遵循一般性操作2(条件a),不同之处在于使用ag2co3代替agtfa。
[0570]
产率:-[0571]
比率(产物/脱碘/芳基碘化物):50/5/22
[0572]
精确质量:5138.9612
[0573]
三电荷质量[m]/3-1.00794,计算值1711.9791;观测值1711.9851。
[0574]
28的lc痕量和质量
[0575][0576]
使用s9和a1(1000mm)遵循一般性操作2(条件a),不同之处在于使用ag2co3代替agtfa。
[0577]
产率:-[0578]
比率(产物/脱碘/芳基碘化物):41/11/18
[0579]
精确质量:5172.9222
[0580]
三电荷质量[m]/3-1.00794,计算值1723.2995;观测值1723.3057。
[0581]
29的lc痕量和质量
[0582][0583]
使用s14和a1(1000mm)遵循一般性操作2(条件a),不同之处在于使用ag2co3代替agtfa。
[0584]
产率:-[0585]
比率(产物/脱碘/芳基碘化物):42/10/2
[0586]
精确质量:5139.9564
[0587]
三电荷质量[m]/3-1.00794,计算值1712.3109;观测值1712.3240。
[0588]
30的lc痕量和质量
[0589][0590]
使用s15和a1(1000mm)遵循一般性操作2(条件a),不同之处在于使用ag2co3代替
agtfa。
[0591]
产率:-[0592]
比率(产物/脱碘/芳基碘化物):53/7/4
[0593]
精确质量:5139.9564
[0594]
三电荷质量[m]/3-1.00794,计算值1712.3109;观测值1712.3240。
[0595]
31的lc痕量和质量
[0596][0597]
使用s18和a1(1000mm)遵循一般性操作2(条件a),不同之处在于使用ag2co3代替agtfa。
[0598]
产率:-[0599]
比率(产物/脱碘/芳基碘化物):41/7/2
[0600]
精确质量:5139.9564
[0601]
三电荷质量[m]/3-1.00794,计算值1712.3109;观测值1712.3070。
[0602]
32的lc痕量和质量
[0603][0604]
使用s16和a1(1000mm)遵循一般性操作2(条件a),不同之处在于使用ag2co3代替agtfa。
[0605]
产率:-[0606]
比率(产物/脱碘/芳基碘化物):30/18/28
[0607]
精确质量:5139.9564
[0608]
三电荷质量[m]/3-1.00794,计算值1712.3109;观测值1712.3240。
[0609]
33的lc痕量和质量
[0610][0611]
使用s17和a1(1000mm)遵循一般性操作2(条件a),不同之处在于使用ag2co3代替agtfa。
[0612]
产率:-[0613]
比率(产物/脱碘/芳基碘化物):35/13/11
[0614]
精确质量:5183.9827
[0615]
三电荷质量[m]/3-1.00794,计算值1726.9863;观测值1726.9968。
[0616]
34的lc痕量和质量
[0617][0618]
使用s19和a1(1000mm)遵循一般性操作2(条件a),不同之处在于使用ag2co3代替agtfa。
[0619]
产率:-[0620]
比率(产物/脱碘/芳基碘化物):35/24/17
[0621]
精确质量:5142.9673
[0622]
三电荷质量[m]/3-1.00794,计算值1713.3145;观测值1713.3240。
[0623]
35的lc痕量和质量
[0624][0625]
使用s20和a1(1000mm)遵循一般性操作2(条件a),不同之处在于使用ag2co3代替agtfa。
[0626]
产率:-[0627]
比率(产物/脱碘/芳基碘化物):22/43/3
[0628]
精确质量:5142.9673
[0629]
三电荷质量[m]/3-1.00794,计算值1713.3145;观测值1713.3240。
[0630]
36的lc痕量和质量
[0631][0632]
使用s21和a1(1000mm)遵循一般性操作2(条件a),不同之处在于使用ag2co3代替agtfa。
[0633]
产率:-[0634]
比率(产物/脱碘/芳基碘化物):23/19/30
[0635]
精确质量:5142.9673
[0636]
三电荷质量[m]/3-1.00794,计算值1713.3145;观测值1713.3240。
[0637]
37的lc痕量和质量
[0638]
[0639]
使用s22和a1(1000mm)遵循一般性操作2(条件a),不同之处在于使用ag2co3代替agtfa。
[0640]
产率:-[0641]
比率(产物/脱碘/芳基碘化物):51/7/0
[0642]
精确质量:5128.9405
[0643]
三电荷质量[m]/3-1.00794,计算值1708.6389;观测值1708.6487。
[0644]
38的lc痕量和质量
[0645][0646]
使用s23和a1(1000mm)遵循一般性操作2(条件a),不同之处在于使用ag2co3代替agtfa。
[0647]
产率:-[0648]
比率(产物/脱碘/芳基碘化物):46/12/0
[0649]
精确质量:5144.9176
[0650]
三电荷质量[m]/3-1.00794,计算值1713.9646;观测值1713.9681。
[0651]
39的lc痕量和质量
[0652][0653]
使用s2和a23遵循一般性操作2(条件a)。
[0654]
产率:-[0655]
比率(产物/脱碘/芳基碘化物):38/3/14
[0656]
精确质量:5193.0081
[0657]
三电荷质量[m]/3-1.00794,计算值1729.9948;观测值1729.9934。
[0658]
40的lc痕量和质量
[0659][0660]
使用s5和a23遵循一般性操作2(条件a)。
[0661]
产率:-[0662]
比率(产物/脱碘/芳基碘化物):24/16/3
[0663]
精确质量:5193.0081
[0664]
三电荷质量[m]/3-1.00794,计算值1729.9948;观测值1729.9934。
[0665]
41的lc痕量和质量
[0666][0667]
使用s7和a23遵循一般性操作2(条件a)。
[0668]
产率:-[0669]
比率(产物/脱碘/芳基碘化物):33/3/12
[0670]
精确质量:5178.9925
[0671]
三电荷质量[m]/3-1.00794,计算值1725.3229;观测值1725.3293。
[0672]
42的lc痕量和质量
[0673][0674]
使用s16和a23遵循一般性操作2(条件a)。
[0675]
产率:-[0676]
比率(产物/脱碘/芳基碘化物):21/3/25
[0677]
精确质量:5179.9877
[0678]
三电荷质量[m]/3-1.00794,计算值1725.6546;观测值1725.6526。
[0679]
43的lc痕量和质量
[0680][0681]
使用s20和a23遵循一般性操作2(条件a)。
[0682]
产率:-[0683]
比率(产物/脱碘/芳基碘化物):21/17/0
[0684]
精确质量:5182.9986
[0685]
三电荷质量[m]/3-1.00794,计算值1726.6583;观测值1726.6564。
[0686]
44的lc痕量和质量
[0687][0688]
使用s21和a23遵循一般性操作2(条件a)。
[0689]
产率:-[0690]
比率(产物/脱碘/芳基碘化物):20/12/11
[0691]
精确质量:5182.9986
[0692]
三电荷质量[m]/3-1.00794,计算值1726.6583;观测值1726.6564。
[0693]
lc痕量和质量
[0694][0695]
使用s22和a23遵循一般性操作2(条件a)。
[0696]
产率:-[0697]
比率(产物/脱碘/芳基碘化物):18/7/0
[0698]
精确质量:5168.9718
[0699]
三电荷质量[m]/3-1.00794,计算值1721.9827;观测值1721.9800。
[0700]
5.酰胺的on-dna c-h芳基化的实验部分
[0701]
5.1酰胺b1至b16的底物结构
[0702][0703]
酰胺获自商业来源或遵循文献操作合成。
21
[0704]
5.2条件优化
[0705]
表10.ag盐的评价
[0706]
[0707]
条目ag盐(300mm)产率(%)1agoac462agno2123agtfa464ag2co3425agots35
[0708]
表11.碱基的评价
[0709][0710]
条目碱基(150mm)产率(%)1naoac462na2co3553k2co3414k3po4315k2hpo4·
3h2o186li2co3697cs2co341
[0711]
表12.标准条件的评价
[0712][0713]
条目与上述的偏差产率(%)1无692无pd(oac)203无agoac244li2co3355室温 代替80℃60
[0714]
5.3用于酰胺的on-dna c-h芳基化的一般性操作3
[0715][0716]
材料
[0717]
dna缀合的芳基碘化物s:10mm,在h2o中
[0718]
酰胺b:2m,在dma中
[0719]
pd(oac)2:200mm,在hfip中
[0720]
二乙基二硫代氨基甲酸钠三水合物(清除剂):1m,在h2o中
[0721]
操作
[0722]
添加pd(oac)
2-干燥,
[0723]
agoac(300当量,0.5mg),酰胺b
[0724]
dna缀合的芳基碘化物s(10nmol,1l)li2co3[0725]
)被添加。将混合物涡旋。将反应混合物在80℃下加热20小时。
[0726]
添加清除剂,并将混合物在80℃下再加热30分钟。
[0727]
3)冷却至室温,5m nacl
[0728]
so
[0729]
在冰箱中在-20℃下储存超过30分钟。
[0730]
4)将样品在微型离心机中以10000rpm离心约10分钟。弃去上述上清液并将沉淀在真空下干燥。将dna沉淀物重新溶解在h2[0731]
在微型离心机中以10000rpm。一个al
[0732]
获得并通过hplc-ms进行分析。
[0733]
5.4用于二肽合成的一般性操作4
[0734][0735]
材料
[0736]
68:约5mm,在h2o中
[0737]
甘氨酸甲酯盐酸盐:1m,在h2o中
[0738]
dmtmm:1m,在h2o中
[0739]
ph 5.5磷酸盐缓冲液:0.2m nah2po4,在h2o中
[0740]
操作
[0741]
将68溶液添加22
[0742]
5.5磷酸盐缓冲液,甘氨酸甲酯
[0743]
温度过夜(16至18小时)。
[0744]
2)添加5m nacl溶液(按体积计10%)和冷乙醇(按体积计2.5倍,在-20℃下储存的乙醇)。将混合物在冰箱中在-20℃下储存1小时。
[0745]
3)将样品在微型离心机中以10000rpm离心约10分钟。弃去上述上清液并将沉淀在真空下干燥。将dna沉淀物重新溶解在h2[0746]
在微型离心机中以10000rpm。等分试样(50通过hplc-ms进行分析。
[0747]
5.5 52至80的lc痕量和质量表征
[0748]
45的lg痕量和质量
[0749][0750]
使用b1遵循一般性操作3。
[0751]
产率:-[0752]
比率(产物/脱碘/芳基碘化物):59/0/3
[0753]
精确质量:5221.9983
[0754]
三电荷质量[m]/3-1.00794,计算值1739.6582;观测值1739.6648。
[0755]
使用b1遵循一般性操作3,不同之处在于在室温下进行反应并用清除剂淬灭。
[0756]
产率:-[0757]
比率(产物/脱碘/芳基碘化物):51/4/5
[0758]
精确质量:5221.9983
[0759]
三电荷质量[m]/3-1.00794,计算值1739.6582;观测值1739.6648。
[0760]
46的lc痕量和质量
[0761][0762]
使用b2遵循一般性操作3。
[0763]
产率:-[0764]
比率(产物/脱碘/芳基碘化物):56/3/0
[0765]
精确质量:5236.0140
[0766]
三电荷质量[m]/3-1.00794,计算值1744.3301;观测值1744.3309。
[0767]
使用b2遵循一般性操作3,不同之处在于在室温下进行反应并用清除剂淬灭。
[0768]
产率:-[0769]
比率(产物/脱碘/芳基碘化物):71/1/10
[0770]
精确质量:5236.0140
[0771]
三电荷质量[m]/3-1.00794,计算值1744.3301;观测值1744.3309。
[0772]
47的lc痕量和质量
[0773][0774]
使用b3遵循一般性操作3。
[0775]
产率:-[0776]
比率(产物/脱碘/芳基碘化物):72/2/6
[0777]
精确质量:5262.0296
[0778]
三电荷质量[m]/3-1.00794,计算值1753.0019;观测值1752.9962。
[0779]
使用b3遵循一般性操作3,不同之处在于在室温下进行反应并用清除剂淬灭。
[0780]
产率:-[0781]
比率(产物/脱碘/芳基碘化物):55/6/28
[0782]
精确质量:5262.0296
[0783]
三电荷质量[m]/3-1.00794,计算值1753.0019;观测值1752.9962。
[0784]
48的lc痕量和质量
[0785][0786]
使用b4遵循一般性操作3。
[0787]
产率:-[0788]
比率(产物/脱碘/芳基碘化物):29/10/0
[0789]
精确质量:5219.9827
[0790]
三电荷质量[m]/3-1.00794,计算值1738.9863;观测值1738.9816。
[0791]
使用b4遵循一般性操作3,不同之处在于在室温下进行反应并用清除剂淬灭。
[0792]
产率:-[0793]
比率(产物/脱碘/芳基碘化物):46/4/10
[0794]
精确质量:5219.9827
[0795]
三电荷质量[m]/3-1.00794,计算值1738.9863;观测值1738.9816。
[0796]
49的lc痕量和质量
[0797][0798]
使用b5遵循一般性操作3。
[0799]
产率:-[0800]
比率(产物/脱碘/芳基碘化物):56/3/4
[0801]
精确质量:5248.0140
[0802]
三电荷质量[m]/3-1.00794,计算值1748.3301;观测值1748.3356。
[0803]
使用b5遵循一般性操作3,不同之处在于在室温下进行反应并用清除剂淬灭。
[0804]
产率:-[0805]
比率(产物/脱碘/芳基碘化物):35/9/41
[0806]
精确质量:5248.0140
[0807]
三电荷质量[m]/3-1.00794,计算值1748.3301;观测值1748.3356。
[0808]
50的lc痕量和质量
[0809][0810]
使用b6遵循一般性操作3。
[0811]
产率:-[0812]
比率(产物/脱碘/芳基碘化物):48/6/5
[0813]
精确质量:5193.9670
[0814]
三电荷质量[m]/3-1.00794,计算值1730.3144;观测值1730.3170。
[0815]
使用b6遵循一般性操作3,不同之处在于在室温下进行反应并用清除剂淬灭。
[0816]
产率:-[0817]
比率(产物/脱碘/芳基碘化物):51/1/29
[0818]
精确质量:5193.9670
[0819]
三电荷质量[m]/3-1.00794,计算值1730.3144;观测值1730.3170。
[0820]
51的lc痕量和质量
[0821][0822]
使用b7遵循一般性操作3。
[0823]
产率:-[0824]
比率(产物/脱碘/芳基碘化物):63/3/0
[0825]
精确质量:5236.0140
[0826]
三电荷质量[m]/3-1.00794,计算值1744.3301;观测值1744.3309。
[0827]
使用b7遵循一般性操作3,不同之处在于在室温下进行反应并用清除剂淬灭。
[0828]
产率:-[0829]
比率(产物/脱碘/芳基碘化物):66/2/13
[0830]
精确质量:5236.0140
[0831]
三电荷质量[m]/3-1.00794,计算值1744.3301;观测值1744.3309。
[0832]
52的lc痕量和质量
[0833][0834]
使用b8遵循一般性操作3。
[0835]
产率:-[0836]
比率(产物/脱碘/芳基碘化物):72/0/0
[0837]
精确质量:5207.9827
[0838]
三电荷质量[m]/3-1.00794,计算值1734.9863;观测值1734.9877。
[0839]
使用b8遵循一般性操作3,不同之处在于在室温下进行反应并用清除剂淬灭。
[0840]
产率:-[0841]
比率(产物/脱碘/芳基碘化物):70/0/16
[0842]
精确质量:5207.9827
[0843]
三电荷质量[m]/3-1.00794,计算值1734.9863;观测值1734.9877。
[0844]
53的lc痕量和质量
[0845][0846]
使用b9遵循一般性操作3。
[0847]
产率:-[0848]
比率(产物/脱碘/芳基碘化物):62/2/0
[0849]
精确质量:5236.0140
[0850]
三电荷质量[m]/3-1.00794,计算值1744.3301;观测值1744.3309。
[0851]
使用b9遵循一般性操作3,不同之处在于在室温下进行反应并用清除剂淬灭。
[0852]
产率:-[0853]
比率(产物/脱碘/芳基碘化物):70/5/9
[0854]
精确质量:5236.0140
[0855]
三电荷质量[m]/3-1.00794,计算值1744.3301;观测值1744.3309。
[0856]
54的lc痕量和质量
[0857][0858]
使用b10遵循一般性操作3。
[0859]
产率:-[0860]
比率(产物/脱碘/芳基碘化物):72/2/3
[0861]
精确质量:5250.0296
[0862]
三电荷质量[m]/3-1.00794,计算值1749.0019;观测值1749.0034。
[0863]
使用b10遵循一般性操作3,不同之处在于在室温下进行反应并用清除剂淬灭。
[0864]
产率:-[0865]
比率(产物/脱碘/芳基碘化物):19/2/55
[0866]
精确质量:5250.0296
[0867]
三电荷质量[m]/3-1.00794,计算值1749.0019;观测值1749.0034
[0868]
55的lc痕量和质量
[0869][0870]
使用b11遵循一般性操作3。
[0871]
产率:-[0872]
比率(产物/脱碘/芳基碘化物):44/4/5
[0873]
精确质量:5248.0140
[0874]
三电荷质量[m]/3-1.00794,计算值1748.3301;观测值1748.3356。
[0875]
使用b11遵循一般性操作3,不同之处在于在室温下进行反应并用清除剂淬灭。
[0876]
产率:-[0877]
比率(产物/脱碘/芳基碘化物):40/9/10
[0878]
精确质量:5218.0140
[0879]
三电荷质量[m]/3-1.00794,计算值1748.3301;观测值1748.3356。
[0880]
56的lc痕量和质量
[0881][0882]
使用b12遵循一般性操作3。
[0883]
产率:-[0884]
比率(产物/脱碘/芳基碘化物):63/3/2
[0885]
精确质量:5248.0140
[0886]
三电荷质量[m]/3-1.00794,计算值1748.3301;观测值1748.3356。
[0887]
使用b12遵循一般性操作3,不同之处在于在室温下进行反应并用清除剂淬灭。
[0888]
产率:-[0889]
比率(产物/脱碘/芳基碘化物):68/6/8
[0890]
精确质量:5248.0140
[0891]
三电荷质量[m]/3-1.00794,计算值1748.3301;观测值1748.3356。
[0892]
57的lc痕量和质量
[0893][0894]
使用b13遵循一般性操作3。
[0895]
产率:-[0896]
比率(产物/脱碘/芳基碘化物):43/6/22
[0897]
精确质量:5272.0140
[0898]
三电荷质量[m]/3-1.00794,计算值1756.3301;观测值1756.33413。
[0899]
58的lc痕量和质量
[0900][0901]
使用b14遵循一般性操作3。
[0902]
产率:-[0903]
比率(产物/脱碘/芳基碘化物):30/2/43
[0934]
比率(产物/脱碘/芳基碘化物):55/5/0
[0935]
精确质量:5295.9906
[0936]
三电荷质量[m]/3-1.00794,计算值1764.3223;观测值1764.3309。
[0937]
63的lc痕量和质量
[0938][0939]
使用s13和b3遵循一般性操作3。
[0940]
产率:-[0941]
比率(产物/脱碘/芳基碘化物):51/3/0
[0942]
精确质量:5280.0202
[0943]
三电荷质量[m]/3
–
1.00794,计算值1758.9988;观测值1759.0026。
[0944]
64的lc痕量和质量
[0945][0946]
使用s12和b3遵循一般性操作3。
[0947]
产率:-[0948]
比率(产物/脱碘/芳基碘化物):52/6/1
[0949]
精确质量:5280.0202
[0950]
三电荷质量[m]/3-1.00794,计算值1758.9988;观测值1759.0026。
[0951]
65的lc痕量和质量
[0952][0953]
使用s3和b3遵循一般性操作3。
[0954]
产率:-[0955]
比率(产物/脱碘/芳基碘化物):50/1/0
[0956]
精确质量:5290.0609
[0957]
三电荷质量[m]/3-1.00794,计算值1762.3457;观测值1762.3534。
[0958]
66的lc痕量和质量
[0959]
[0960]
使用s18和b3遵循一般性操作3。
[0961]
产率:-[0962]
比率(产物/脱碘/芳基碘化物):45/2/0
[0963]
精确质量:5263.0249
[0964]
三电荷质量[m]/3-1.00794,计算值1753.3337;观测值1753.3391。
[0965]
67的lc痕量和质量
[0966][0967]
使用s15和b3遵循一般性操作3。
[0968]
产率:-[0969]
比率(产物/脱碘/芳基碘化物):42/1/3
[0970]
精确质量:5263.0249
[0971]
三电荷质量[m]/3-1.00794,计算值1753.3337;观测值1753.3391。
[0972]
68的lc痕量和质量
[0973][0974]
使用s16和b3遵循一般性操作3。
[0975]
产率:-[0976]
比率(产物/脱碘/芳基碘化物):53/2/3
[0977]
精确质量:5263.0249
[0978]
三电荷质量[m]/3-1.00794,计算值1753.3337;观测值1753.3391。
[0979]
69的lc痕量和质量
[0980][0981]
使用s17和b3遵循一般性操作3。
[0982]
产率:-[0983]
比率(产物/脱碘/芳基碘化物):56/9/0
[0984]
精确质量:5307.0511
[0985]
三电荷质量[m]/3-1.00794,计算值1768.0091;观测值1768.0140。
[0986]
70的lc痕量和质量
[0987][0988]
使用s21和b3遵循一般性操作3。
[0989]
产率:-[0990]
比率(产物/脱碘/芳基碘化物):33/16/5
[0991]
精确质量:5266.0358
[0992]
三电荷质量[m]/3-1.00794,计算值1754.3373;观测值1754.3339。
[0993]
71的lc痕量和质量
[0994][0995]
使用s22和b3遵循一般性操作3。
[0996]
产率:-[0997]
比率(产物/脱碘/芳基碘化物):39/3/0
[0998]
精确质量:5252.0089
[0999]
三电荷质量[m]/3-1.00794,计算值1749.6617;观测值1749.6714。
[1000]
72的lc痕量和质量
[1001][1002]
使用s23和b3遵循一般性操作3。
[1003]
产率:-[1004]
比率(产物/脱碘/芳基碘化物):52/3/0
[1005]
精确质量:5267.9860
[1006]
三电荷质量[m]/3-1.00794,计算值1754.9874;观测值1754.9857。
[1007]
73的lc痕量和质量
[1008][1009]
使用68遵循一般性操作4。
[1010]
产率:-[1011]
精确质量:5334.0620
[1012]
三电荷质量[m]/3-1.00794,计算值1777.0127;观测值1777.0140。
[1013]
6.用于酮的on-dna c-h芳基化的实验部分
[1014]
6.1包含定向基团(dg)的酮c1-c30的底物结构
[1015][1016]
包含定向基团的酮c1-c30如先前所报道的来合成。
16a
[1017]
6.2条件优化
[1018]
表13.配体优化
[1019]
[1020][1021]
表14.共溶剂优化
[1022][1023]
条目h2o/共溶剂(x/y)产率(%)1h2o/dma(1/1)282h2o/dma(2/1)393h2o/dmf(2/1)354h2o/dmso(2/1)26
[1024]
表15.pd/l8浓度优化
[1025][1026]
条目pd/l8(x/y)产率(%)120/1033220/1548320/2048
[1027]
表16.溶剂比率优化
[1028][1029]
条目h2o/dma(x/y)产率(%)14/15129/162
[1030]
表17.标准条件的评价
[1031][1032]
[1033]a仅s1b完全回收。
[1034]
6.3用于酮的on-dna c-h芳基化的一般性操作5
[1035][1036]
材料
[1037]
dna缀合的芳基碘化物s:10mm,在h2o中
[1038]
酮c:3m,在dma中(注意:高浓度可提高总体积)
[1039]
l8
[1040]
pd(oac)2[1041]
naoac:1.5m,在h2o中)
[1042]
二乙基二硫代氨基甲酸钠三水合物(清除剂):1m,在h2o中
[1043]
操作
[1044]
1)向制备的agtfa(500当量,1.1mg)添加pd(oac)2,-干燥,酮c dna缀合的芳基碘化物s(10nmol,1l8(40),naoac
[1045]
将混合物涡旋。将反应混合物在80℃下加热20小时。
[1046]
添加清除剂并将混合物在80℃再加热30分钟。
[1047]
3)冷却至室温,5m nacl
[1048]
在冰箱中在-20℃下储存超过30分钟。
[1049]
4)将样品在微型离心机中以10000rpm离心约7分钟。弃去上清液并将沉淀在真空下干燥。将dna沉淀物重新溶解在h2)中并在离心约2分钟
[1050]
获得并通过hplc-ms进行分析。
[1051]
6.4酮的限制
[1052][1053]
6.5用于去除dg的一般性操作6
[1054][1055]
dna系链的底物83的溶液(约10
[1056]
随后将反应混合物在50℃下加热24小时。
[1057]
2)冷却至室温,将5m nacl混合物在冰箱中在-20℃下储存超过30分钟。
[1058]
3)将样品在微型离心机中以10000rpm离心约7分钟。弃去上清液并将沉淀在真空下干燥。将dna沉淀物重新溶解在h2[1059]
获得并通过hplc-ms进行分析。
[1060]
6.6 89至119的lc痕量和质量表征
[1061]
74的lc痕量和质量
[1062][1063]
使用c1遵循一般性操作5。
[1064]
产率:-[1065]
比率(产物/脱碘/芳基碘化物):31/1/12
[1066]
精确质量:5252.0453
[1067]
三电荷质量[m]/3-1.00794,计算值1749.6738;观测值1749.6714。
[1068]
75的lc痕量和质量
[1069][1070]
使用c2遵循一般性操作5。
[1071]
产率:-[1072]
比率(产物/脱碘/芳基碘化物):55/1/12
[1073]
精确质量:5238.0296
[1074]
三电荷质量[m]/3-1.00794,计算值1745.0019;观测值1745.0151。
[1075]
76的lc痕量和质量
[1076][1077]
使用c3遵循一般性操作5。
[1078]
产率:-[1079]
比率(产物/脱碘/芳基碘化物):38/1/25
[1080]
精确质量:5252.0453
[1081]
三电荷质量[m]/3-1.00794,计算值1749.6738;观测值1749.6886。
[1082]
77的lc痕量和质量
[1083][1084]
使用c4遵循一般性操作5。
[1085]
产率:-[1086]
比率(产物/脱碘/芳基碘化物):47/3/0
[1087]
精确质量:5224.0140
[1088]
三电荷质量[m]/3-1.00794,计算值1740.3301;观测值1740.3309。
[1089]
78的lc痕量和质量
[1090][1091]
使用c5遵循一般性操作5。
[1092]
产率:-[1093]
比率(产物/脱碘/芳基碘化物):34/1/22
[1094]
精确质量:5264.0453
[1095]
三电荷质量[m]/3-1.00794,计算值1753.6738;观测值1753.6821。
[1096]
79的lc痕量和质量
[1097][1098]
使用c6遵循一般性操作5。
[1099]
产率:-[1100]
比率(产物/脱碘/芳基碘化物):17/7/39
[1101]
精确质量:5336.0664
[1102]
三电荷质量[m]/3-1.00794,计算值1777.6809;观测值1777.6874。
[1103]
80的lc痕量和质量
[1104][1105]
使用c7遵循一般性操作5。
[1106]
产率:-[1107]
比率(产物/脱碘/芳基碘化物):34/2/41
[1108]
精确质量:5266.0245
[1109]
三电荷质量[m]/3-1.00794,计算值1754.3336;观测值1754.3339。
[1110]
81的lc痕量和质量
[1111][1112]
使用c8遵循一般性操作5。
[1113]
产率:-[1114]
比率(产物/脱碘/芳基碘化物):29/2/8
[1115]
精确质量:5321.0667
[1116]
三电荷质量[m]/3-1.00794,计算值1772.6810;观测值1772.6836。
[1117]
82的lc痕量和质量
[1118][1119]
使用c9遵循一般性操作5。
[1120]
产率:-[1121]
比率(产物/脱碘/芳基碘化物):36/2/26
[1122]
精确质量:5322.0507
[1123]
三电荷质量[m]/3-1.00794,计算值1773.0090;观测值1773.0112。
[1124]
83的lc痕量和质量
[1125][1126]
使用c10遵循一般性操作5。
[1127]
产率:-[1128]
比率(产物/脱碘/芳基碘化物):53/2/5
[1129]
精确质量:5250.0296
[1130]
三电荷质量[m]/3-1.00794,计算值1749.0019;观测值1749.0034。
[1131]
lc痕量和质量
[1132][1133]
使用c11遵循一般性操作5。
[1134]
产率:-[1135]
比率(产物/脱碘/芳基碘化物):17/9/32
[1136]
精确质量:5278.0609
[1137]
三电荷质量[m]/3-1.00794,计算值1758.3457;观测值1758.3500。
[1138]
lc痕量和质量
[1139][1140]
使用c12遵循一般性操作5。
[1141]
产率:-[1142]
比率(产物/脱碘/芳基碘化物):17/4/33
[1143]
精确质量:5308.0715
[1144]
三电荷质量[m]/3-1.00794,计算值1768.3492;观测值1768.3584。
[1145]
84的lc痕量和质量
[1146][1147]
使用c13遵循一般性操作5。
[1148]
产率:-[1149]
比率(产物/脱碘/芳基碘化物):36/2/13
[1150]
精确质量:5224.0140
[1151]
三电荷质量[m]/3-1.00794,计算值1740.3301;观测值1740.3309。
[1152]
lc痕量和质量
[1153][1154]
使用c14遵循一般性操作5。
[1155]
产率:-[1156]
比率(产物/脱碘/芳基碘化物):18/2/28
[1157]
精确质量:5296.0351
[1158]
三电荷质量[m]/3-1.00794,计算值1764.3371;观测值1764.3481。
[1159]
85的lc痕量和质量
[1160][1161]
使用c15遵循一般性操作5。
[1162]
产率:-[1163]
比率(产物/脱碘/芳基碘化物):33/1/9
[1164]
精确质量:5312.0453
[1165]
三电荷质量[m]/3-1.00794,计算值1769.6738;观测值1769.6847。
[1166]
86的lc痕量和质量
[1167][1168]
使用c16遵循一般性操作5。
[1169]
产率:-[1170]
比率(产物/脱碘/芳基碘化物):38/0/6
[1171]
精确质量:5238.0296
[1172]
三电荷质量[m]/3-1.00794,计算值1745.0019;观测值1744.9980。
[1173]
87的lc痕量和质量
[1174][1175]
使用c17遵循一般性操作5。
[1176]
产率:-[1177]
比率(产物/脱碘/芳基碘化物):32/1/21
[1178]
精确质量:5286.0296
[1179]
三电荷质量[m]/3-1.00794,计算值1761.0019;观测值1761.0127。
[1180]
lc痕量和质量
[1181][1182]
使用c18遵循一般性操作5。
[1183]
产率:-[1184]
比率(产物/脱碘/芳基碘化物):17/6/14
[1185]
精确质量:5282.0194
[1186]
三电荷质量[m]/3-1.00794,计算值1759.6652;观测值1759.6725。
[1187]
88的lc痕量和质量
[1188][1189]
使用c19遵循一般性操作5。
[1190]
产率:-[1191]
比率(产物/脱碘/芳基碘化物):37/1/24
[1192]
精确质量:5372.1028
[1193]
三电荷质量[m]/3-1.00794,计算值1789.6930;观测值1789.6906。
[1194]
89的lc痕量和质量
[1195][1196]
使用d20遵循一般性操作5,不同之处在于使用在h2o/dma(2/1)中的pd(oac)2(15mm)和l8(15mm)。
[1197]
产率:-[1198]
比率(产物/脱碘/芳基碘化物):29/2/10
[1199]
精确质量:5328.0766
[1200]
三电荷质量[m]/3-1.00794,计算值1775.0176;观测值1775.0293。
[1201]
90的lc痕量和质量
[1202][1203]
使用c21遵循一般性操作5,不同之处在于使用在h2o/dma(2/1)中的pd(oac)2(15mm)和l8(15mm)。
[1204]
产率:-[1205]
比率(产物/脱碘/芳基碘化物):58/1/14
[1206]
精确质量:5264.0453
[1207]
三电荷质量[m]/3-1.00794,计算值1753.6738;观测值1753.6821。
[1208]
91的lc痕量和质量
[1209][1210]
使用c22遵循一般性操作5。
[1211]
产率:-[1212]
比率(产物/脱碘/芳基碘化物):34/4/25
[1213]
精确质量:5276.0453
[1214]
三电荷质量[m]/3-1.00794,计算值1757.6738;观测值1757.6803。
[1215]
92的lc痕量和质量
[1216][1217]
使用c23遵循一般性操作5。
[1218]
产率:-[1219]
比率(产物/脱碘/芳基碘化物):29/1/19
[1220]
精确质量:5302.0609
[1221]
三电荷质量[m]/3-1.00794,计算值1766.3457;观测值1766.3441。
[1222]
lc痕量和质量
[1223][1224]
使用c24遵循一般性操作5。
[1225]
产率:-[1226]
比率(产物/脱碘/芳基碘化物):13/2/41
[1227]
精确质量:5266.0609
[1228]
三电荷质量[m]/3-1.00794,计算值1754.3457;观测值1754.3511。
[1229]
lc痕量和质量
[1230][1231]
使用c25遵循一般性操作5。
[1232]
产率:-[1233]
比率(产物/脱碘/芳基碘化物):8/2/52
[1234]
精确质量:5252.0453
[1235]
三电荷质量[m]/3-1.00794,计算值1749.6738;观测值1749.6886。
[1236]
93的lc痕量和质量
[1237][1238]
使用c26遵循一般性操作5。
[1239]
产率:-[1240]
比率(产物/脱碘/芳基碘化物):19/2/30
[1241]
精确质量:5306.0922
[1242]
三电荷质量[m]/3-1.00794,计算值1767.6895;观测值1767.6869。
[1243]
lc痕量和质量
[1244]
[1245]
使用s4和c10遵循一般性操作5。
[1246]
产率:-[1247]
比率(产物/脱碘/芳基碘化物):23/6/2
[1248]
精确质量:5236.0140
[1249]
三电荷质量[m]/3-1.00794,计算值1744.3301;观测值1744.3309。
[1250]
lc痕量和质量
[1251][1252]
使用s5和c10遵循一般性操作5。
[1253]
产率:-[1254]
比率(产物/脱碘/芳基碘化物):22/10/4
[1255]
精确质量:5250.0296
[1256]
三电荷质量[m]/3-1.00794,计算值1749.0019;观测值1749.0034。
[1257]
94的lc痕量和质量
[1258][1259]
使用s7和c10遵循一般性操作5。
[1260]
产率:-[1261]
比率(产物/脱碘/芳基碘化物):51/1/9
[1262]
精确质量:5236.0140
[1263]
三电荷质量[m]/3-1.00794,计算值1744.3301;观测值1744.3309。
[1264]
95的lc痕量和质量
[1265][1266]
使用s9和c10遵循一般性操作5。
[1267]
产率:-[1268]
比率(产物/脱碘/芳基碘化物):26/3/16
[1269]
精确质量:5269.9750
[1270]
三电荷质量[m]/3-1.00794,计算值1755.6504;观测值1755.6549。
[1271]
96的lc痕量和质量
[1272][1273]
使用s10和c10遵循一般性操作5。
[1274]
产率:-[1275]
比率(产物/脱碘/芳基碘化物):29/1/4
[1276]
精确质量:5236.0140
[1277]
三电荷质量[m]/3-1.00794,计算值1744.3301;观测值1744.3309。
[1278]
97的lc痕量和质量
[1279][1280]
使用s3和c10遵循一般性操作5。
[1281]
产率:-[1282]
比率(产物/脱碘/芳基碘化物):43/1/4
[1283]
精确质量:5264.0454
[1284]
三电荷质量[m]/3-1.00794,计算值1753.6739;观测值1753.6821。
[1285]
98的lc痕量和质量
[1286][1287]
使用s14和c10遵循一般性操作5。
[1288]
产率:-[1289]
比率(产物/脱碘/芳基碘化物):36/5/1
[1290]
精确质量:5237.0092
[1291]
三电荷质量[m]/3-1.00794,计算值1744.6618;观测值1744.6731。
[1292]
99的lc痕量和质量
[1293][1294]
遵循使用s15和c10的一般性操作5。
[1295]
产率:-[1296]
比率(产物/脱碘/芳基碘化物):38/3/0
[1297]
精确质量:5237.0092
[1298]
三电荷质量[m]/3-1.00794,计算值1744.6618;观测值1744.6731。
[1299]
100的lc痕量和质量
[1300][1301]
使用s18和c10遵循一般性操作5。
[1302]
产率:-[1303]
比率(产物/脱碘/芳基碘化物):29/6/2
[1304]
精确质量:5237.0092
[1305]
三电荷质量[m]/3-1.00794,计算值1744.6618;观测值1744.6731。
[1306]
101的lc痕量和质量
[1307][1308]
使用s16和c10遵循一般性操作5。
[1309]
产率:-[1310]
比率(产物/脱碘/芳基碘化物):29/6/26
[1311]
精确质量:5237.0092
[1312]
三电荷质量[m]/3-1.00794,计算值1744.6618;观测值1744.6731。
[1313]
lc痕量和质量
[1314][1315]
使用s19和c10遵循一般性操作5,不同之处在于使用h2o/dma(2/1)。
[1316]
产率:-[1317]
比率(产物/脱碘/芳基碘化物):13/10/29
[1318]
精确质量:5240.0201
[1319]
三电荷质量[m]/3-1.00794,计算值1745.6654;观测值1745.6653,
[1320]
102的lc痕量和质量
[1321][1322]
使用s23和c10遵循一般性操作5,
[1323]
产率:-[1324]
比率(产物/脱碘/芳基碘化物):28/3/14
[1325]
精确质量:5241.9704
[1326]
三电荷质量[m]/3-1.00794,计算值1746.3155;观测值1746.3156。
[1327]
103的lc痕量和质量
[1328][1329]
使用83遵循一般性操作6。
[1330]
产率:-[1331]
精确质量:5148.9819
[1332]
三电荷质量[m]/3-1.00794,计算值1715.3194;观测值1715.3248。
[1333]
7.化合物106的代表性合成
[1334]
步骤1:第一次c(sp3)-h活化
[1335]
[1336]
31的lc痕量和质量,参见上述。
[1337]
步骤2:酰胺化
[1338][1339]
104的lc痕量和质量
[1340]
使用化合物31和4-碘苄胺遵循一般性操作4。
[1341]
产率:-[1342]
精确质量:5354.9160
[1343]
三电荷质量[m]/3-1.00794,计算值1783.9641;观测值1783.9607。
[1344]
步骤3:第2次c(sp3)-h活化
[1345]
105的lc痕量和质量
[1346]
使用104和c10遵循一般性操作5。
[1347]
产率:-[1348]
精确质量:5426.1246
[1349]
三电荷质量[m]/3-1.00794,计算值1807.7003;观测值1807.7014。
[1350]
步骤4:去除dg
[1351][1352]
106的lc痕量和质量
[1353]
使用105遵循一般性操作6。
[1354]
产率:-[1355]
精确质量:5325.0769
[1356]
三电荷质量[m]/3-1.00794,计算值1774.0177;观测值1774.0288。
[1357]
引用:
[1358]
1.brenner&lerner,proc.natl.acad.sci.u.s.a.89,5381-5383(1992).
[1359]
2.(a)goodnow,
″
a brief history of the development of combinatorial chemistry and the emerging need for dna-encoded chemistry
″
.in a handbook for dna-encoded chemistry,wiley-blackwell,2014,pp 19-43;(b)franzini et al.,acc.chem.res.,2014,47,1247;(c)zimmermann&neri,drug discov.today,2016,21,1828;(d)lerner&brenner,angew.chem.,int.ed.,2017,56,1164;(e)neri,chembiochem,2017,18,827;(f)shi et al.,bioorg.med.chem.lett.,2017,27,361;(g)satz,acs med.chem.lett.,2018,9,408;(h)zhao et al.,expert opin.drug discov.,2019,14,735.
[1360]
3.(a)zhao et al.,angew.chem.,int.ed.,2014,53,10056;(b)ding et al.,acs med.chem.lett.,2015,6,888;(c)arico-muendel,med.chem.commun.,2016,7,1898;(d)belyanskaya et al.,chembiochem,2017,18,837;(e)neri&lerner,annu.rev.biochem.,
2018,87,479;(f)yuen et al.,j.am.chem.soc.,2019,141,5169;(g)cai et al.,j.am.chem.soc.,2019,141,17057.
[1361]
4.(a)satz et al.,bioconjug.chem.26,1623-1632(2015);(b)franzini&randolph,j.med.chem.,2016,59,6629;(c)malone&paegel,acs comb.sci.,2016,18,182.
[1362]
5.(a)ding&.clark,acs comb.sci.,2015,17,1;(b)ding et al.,bioconjug.chem.,2016,27,2597;(c)lu et al.,bioconjug.chem.,2017,28,1625,
[1363]
6.(a)lu et al.,bioconjug.chem.28,1625-1629(2017);b)ruff&berst,med.chem.commun.,2018,9,1188.
[1364]
7.wang et al.,iscience,2019,15,307.
[1365]
8.(a)probst et al.,chem.eur.j.,2018,24,1795;(b)liu al.,angew.chem.,int.ed.,2019,58,8029;(c)flood et al.,angew.chem.,int.ed.,2020,59,7377.
[1366]
9.(a)li et al.,org.lett.,2018,20,7186;(b)gerry et 1.,org.lett.,2019,21,1325;(c)maet al.,angew.chem.,int.ed.,2019,58,9254;(d)j.am.chem.soc.,2019,141,10546;(e)potowski et al.,chem.sci.,2019,10,10481.
[1367]
10.(a)et al.,chem.med.chem.,2018,13,2159;(b)wang et al.,proc.natl.acad.sci.u.s.a.,2018,115,e6404;(c)flood et al.,j.am.chem.soc.,2019,141,9998;(d)phelan et al.,j.am.chem.soc.,2019,141,3723;(e)badir et al.,org.lett.,2020,22,1046;(f)ruff et al.,acs comb.sci.,2020,22,120.
[1368]
11.(a)he et al.,chem.rev.,2017,117,8754;(b)zhuang&yu,nature,2020,577,656.
[1369]
12.gerry et al.,j.am.chem.soc.,2019,141,10225.
[1370]
13.wang et al.,org.lett.,2018,20,4764.
[1371]
14.(a)chen et al.,angew.chem.,int.ed.,2017,56,1506;(b)shen et al.,j.am.chem.soc.,2018,140,6545-6549.
[1372]
15.(a)gong et al.,j.am.chem.soc.,2014,136,16940;(b)liu et al.,angew.chem.,int.ed.,2017,56,10924
[1373]
16.(a)zhu et al.,j.am.chem.soc.,2017,139,16080;(b)zhu et al.,j.am.chem.soc.,2018,140,3564.
[1374]
17.&kool,chem.rev.,2017,117,10358.
[1375]
18.zhuang et al.,j.am.chem.soc.2018 140,10363-10367.
[1376]
19.wu et al.,.science 2017 355,499-503.
[1377]
20.park et al.,acs catal.2018 8,9292-9297.
[1378]
21.dydio et al.,j.am.chem.soc.2011 133,17176-17179.
[1379]
本文引用的每篇专利、专利申请和文章均通过引用并入。本文所使用的没有数量词修饰的名词是指一个/种或多于一个/种(即,至少一个/种)的语法对象。例如,“要素”是指一个要素或多于一个要素。
[1380]
前述描述和实施例旨在作为举例说明性的而不应作为限制性的。而且在本发明的精神和范围内的其他变化是可能的并且将容易地将它们自身呈现给本领域技术人员。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1