三环双内酯化合物、其生产方法及用途与流程
1.涉及一种新的三环双内酯化合物、生产其的菌株、其生产方法及其用途。
背景技术:
2.阿尔茨海默氏病(alzheimer's disease:ad)是最常见的一种神经退行性疾病,但目前还没有可以停止或逆转病理进展的药物。聚集的淀粉样蛋白-β(amyloid-beta:aβ)是阿尔茨海默氏病的关键生物标记物蛋白。单体(monomeric)aβ在病理生理学上无害,但已知aβ的异常聚集形式诱导与阿尔茨海默氏病患者的认知障碍密切相关的神经细胞凋亡、神经炎症以及脑萎缩。由于aβ在大脑中的积聚在症状出现前10年或更早地开始,因此从大脑中去除aβ的机制被广泛用于阿尔茨海默氏病的治疗。
3.虽然仍在进行针对阿尔茨海默氏病治疗的研究,但目前只能通过抑制β-淀粉样蛋白聚集和tau蛋白聚集来减缓阿尔茨海默氏病的进展。另外,自2003年的“namenda”(成分名:美金刚(memantine))之后,尚无获得美国食品药品监督管理局批准的药物。近年来,正研发减少淀粉样蛋白形成或促进淀粉样蛋白分解的物质,但是研发药物通过临床试验并实现商业化还需进行许多研究(例如,韩国专利公报第10-2101258b1、韩国专利公报第10-2106821b1)。
4.因此,需要探索对包括阿尔茨海默氏病在内的神经退行性疾病具有优异治疗效果的天然产物衍生的新的化合物。
技术实现要素:
技术问题
5.提供一种三环双内酯化合物、其衍生物、立体异构体、溶剂化物,或药学上可接受的盐。
6.提供一种细菌,其生产三环双内酯化合物、其衍生物、立体异构体、溶剂化物,或药学上可接受的盐。
7.提供一种生产三环双内酯化合物、其衍生物、立体异构体、溶剂化物,或药学上可接受的盐的方法。
8.提供一种用于预防或治疗退行性脑病的药物组合物以及用于预防或改善神经退行性脑病或认知障碍的保健功能食品,所述药物组合物与所述保健功能食品包括三环双内酯化合物、其衍生物、立体异构体、溶剂化物,或药学上可接受的盐。
9.提供一种预防或治疗神经退行性脑病的方法以及预防或改善神经退行性脑病或认知障碍的方法,其利用三环双内酯化合物、其衍生物、立体异构体、溶剂化物,或药学上可接受的盐。技术方案
10.一方面提供一种由化学式1表示的化合物、其衍生物、立体异构体、溶剂化物,或药学上可接受的盐。
11.[化学式1]
[0012][0013]
在所述化学式1中,r
x
可以是不饱和环基中的一个或多个取代基。ry可以是内酯化合物中的一个或多个取代基。rz可以是内酯化合物中的一个或多个取代基。
[0014]rx
、ry以及rz可以彼此独立地为氢、羟基、卤素原子、胺基、羰基、氰基、取代或未取代的c1至c
20
的烷基、取代或未取代的c1至c
20
的烷氧基、取代或未取代的c2至c
20
的烯基、取代或未取代的c2至c
20
的炔基、-c(=o)ra、-c(=o)ora、-oco(ora)、-c=n(ra)、-sra、-s(=o)ra、-s(=o)2ra、-pra、c2至c
20
的环氧烷烃基、取代或未取代的c6至c
30
的芳基、取代或未取代的c6至c
30
的芳氧基、取代或未取代的c6至c
30
的杂芳基、取代或未取代的碳原子数3至30的环基、取代或未取代的碳原子数3至20的杂环基,或者选自其组合中的一个或多个取代基。其中,ra可以是氢、c1至c
10
的烷基或c6至c
20
的芳基的取代基。
[0015]
在所述化学式1中,所述m和n可以彼此独立地是1至5的整数。m可以是3。n可以是2。
[0016]
所述化合物为三环双内酯化合物(tricyclic dilactone)。术语“三环(tricyclic)”是指分子中含有3个彼此连接的环基的化合物。术语“内酯(lactone)”是指分子中具有-(c=o)-o-键的杂环状羧酸酯(carboxylic ester)化合物。所述内酯可以是γ-丁内酯(γ-butyrolactone)、δ-戊内酯(δ-valerolactone)或己内酯(caprolactone)。所述双内酯(dilactone)是指分子中含有两个内酯基的化合物。所述三环双内酯是指分子中含有三个彼此连接的环基和两个内酯基的化合物。
[0017]
所述由化学式1表示的化合物可以是由化学式2表示的化合物。。
[0018]
[化学式2]
[0019][0020]
在所述化学式2中,r1、r2、r3以及r4可以彼此独立地为氢、羟基、卤素原子、胺基、羰基、氰基、取代或未取代的c1至c
20
的烷基、取代或未取代的c1至c
20
的烷氧基、取代或未取代的c2至c
20
的烯基、取代或未取代的c2至c
20
的炔基、-c(=o)ra、-c(=o)ora、-oco(ora)、-c=n(ra)、-sra、-s(=o)ra、-s(=o)2r
aa
、-pra、c2至c
20
的环氧烷烃基、取代或未取代的c6至c
30
的芳基、取代或未取代的c6至c
30
的芳氧基、取代或未取代的c6至c
30
的杂芳基、取代或未取代的碳原子数3至30的环基、取代或未取代的碳原子数3至20的杂环基,或者选自其组合中的一个或多个取代基。其中,ra可以是氢、c1至c
10
的烷基或c6至c
20
的芳基的取代基。
[0021]
r1、r3以及r4可以彼此独立地为取代或未取代的c1至c
10
的烷基。。
至c
20
的烯基可以是c2至c
15
、c2至c
10
或c2至c5的烯基。例如,所述烯基为乙烯基、烯丙基、丁烯基、异丙烯基或异丁烯基。
[0038]
术语“炔基(alkynyl)”是指具有至少一个碳-碳三键的支链或非支链烃。所述c2至c
20
的炔基可以是c2至c
15
、c2至c
10
或c2至c5的炔基。例如,所述炔基为乙炔基、丁炔基、异丁炔基或异丙炔基。
[0039]
术语“环氧烷烃(alkylene oxide)”是指由一个氧原子和两个或更多个碳原子所组成的环基。
[0040]
术语“芳基(aryl)”是指被单独或组合使用从而包括一个或多个环的芳族体系,其包括一个芳环稠合到一个或多个碳环的基团。所述c6至c
30
的芳基可以是c6至c
15
或c6至c
10
的芳基。例如,所述芳基为苯基、萘基或四氢萘基。
[0041]
术语“芳氧基(aryloxy)”是指与氧原子单键键合的芳基。
[0042]
术语“杂芳基(heteroaryl)”是指,包括选自由n、o、p以及s所组成的组中的一个或多个杂原子且其余环原子为碳的单环或双环有机化合物。所述杂芳基可以包括1至5个杂原子,可以包括5至10环员(ring member)。所述s和n可以氧化后具有各种氧化态。
[0043]
术语“环(cyclic)”基或“碳环”基是指饱和或部分不饱和的非芳族(non-aromatic)单环、双环或三环烃基。环基可以含有3至30个、5至20个碳原子,例如,5至10个。单环基可以是例如,环戊基、环戊烯基、环己基或环己烯基。双环基可以是例如,冰片基、十氢萘基、双环[2.1.1]己基、双环[2.2.1]庚基、双环[2.2.1]庚烯基或双环[2.2.2]辛基。三环基可以是例如,金刚烷基(adamantyl)。
[0044]
术语“杂环(heterocyclic)”基或“杂环”基是指包括至少一个杂原子的环状烃。杂环基可以含有3至30个、3至20个、3至10个、3至6个或3至5个原子(member)。除了环中的碳原子以外,杂环基团在环中还可以含有一个或多个其它杂原子。所述杂原子可以是选自由硫、氮、氧和硼所组成的组中的任意一种或多种。例如,所述杂环基是环氧乙烷基或四氢呋喃基。
[0045]
术语“衍生物(derivative)”是指通过其它原子或原子团取代所述化合物的部分结构来获得的化合物。
[0046]
术语“立体异构体”中的术语“异构体(isomer)”是指分子式相同但分子中构成原子的连接方式或空间排列不同的化合物。异构体包括例如,结构异构体(structural isomers)和立体异构体(stereoisomer stereoisomer)。所述立体异构体可以是非对映异构体(diasteromer)或对映异构体(enantiomer)。对映异构体是指,犹如左右手的关系般镜像不重叠的异构体,其也被称作旋光异构体(optical isomer)。当手性中心碳的四个或更多取代基彼此不同时,对映异构体分为r(rectus:顺时针)和s(sinister:逆时针)。非对映异构体是指非镜像关系的立体异构体,其为由原子的不同空间排列而成的异构体。所述非对映异构体可分为顺(cis)反(trans)异构体和构象异构体(conformationalisomer或conformer)。
[0047]
术语“溶剂化物(solvate)”是指在有机或无机溶剂中溶剂化的化合物。所述溶剂化物例如,是水合物。
[0048]
术语“盐(salt)”是指化合物的无机酸和有机酸加成盐。所述药学上可接受的盐可以是不会给施用化合物的有机体带来严重刺激,并且不损伤化合物的生物活性和物性的
盐。所述无机酸盐可以是盐酸盐、溴酸盐、磷酸盐、硫酸盐或二硫酸盐。所述有机酸盐可以是甲酸盐、乙酸盐、丙酸盐、乳酸盐、草酸盐、锡酸盐、苹果酸盐、马来酸盐、柠檬酸盐、富马酸盐、苯磺酸盐、樟脑磺酸盐、乙二磺酸盐、三氯乙酸盐、三氟乙酸盐、苯甲酸盐、葡萄糖酸盐、甲磺酸盐、乙醇酸盐、琥珀酸盐、4-甲苯磺酸盐、半乳糖醛酸盐、恩波酸盐、谷氨酸盐、乙磺酸盐、苯磺酸盐、对甲苯磺酸盐或天冬氨酸盐。所述金属盐可以是钙盐、钠盐、镁盐、锶盐或钾盐。
[0049]
另一方面提供一种链霉菌属won17菌株(保藏编号:kctc14217bp),所述菌株生产根据一方面的化合物、其衍生物、立体异构体、溶剂化物,或药学上可接受的盐。
[0050]
所述菌株可以生产根据一方面的由化学式1表示的化合物、立体异构体、溶剂化物或药学上可接受的盐。
[0051]
所述菌株包括其变体。变体可以是例如,由自然突变或人工突变所引起的变体。人工突变可通过紫外线等物理诱变剂或碱化合物等化学诱变剂而产生。
[0052]
所述菌株包括菌株的孢子、菌体或其培养物。
[0053]
另一方面提供一种生产根据一方面的由化学式1表示的化合物、其衍生物、立体异构体、溶剂化物或药学上可接受的盐的方法,所述方法包括
[0054]
培养链霉菌属won17菌株(保藏编号:kctc14217bp);以及
[0055]
从所述培养物中分离根据一方面的由化学式1表示的化合物、其衍生物、立体异构体、溶剂化物或药学上可接受的盐。
[0056]
链霉菌属won17菌株、由化学式1表示的化合物、立体异构体、溶剂化物或药学上可接受的盐如上所述。
[0057]
所述方法包括培养链霉菌属won17菌株(保藏编号:kctc14217bp)。培养步骤可以是在液体培养基或固体培养基中培养菌株。培养基可以包括作为碳源的例如,葡萄糖、淀粉糖浆、糊精、淀粉、糖蜜、动物油或植物油。培养基可以包括作为氮源的,例如,麸皮、豆粕、小麦、麦芽、棉籽粕、鱼饼、玉米浆、肉汁、酵母提取物、麦芽提取物、硫酸铵、硝酸钠或尿素。
[0058]
培养可以在需氧条件下通过振荡或静置培养。培养温度可以是例如,约20℃至约40℃、约25℃至约37℃、约28℃至约35℃或约30℃。培养时间可以是例如,约1天至约4个月、约1天至约2个月、约1天至约6周、约1天至约1个月、约1天至约2周或约1天至约1周。
[0059]
所述方法包括从培养液中分离由化学式1表示的化合物、其衍生物、立体异构体、溶剂化物或药学上可接受的盐。
[0060]
分离步骤可以包括对培养液进行浓缩、离心、过滤或色谱法。根据固定相的形式,色谱法可以是例如,柱色谱法、平面色谱法(planar chromatography)、纸色谱法或薄层色谱法。根据流动相的物理特性,色谱法可以是例如,气相色谱法、液相色谱法或亲和色谱法。液相色谱法可以是例如,高效液相色谱法(hplc)。根据分离方法,色谱法可以是例如,离子交换色谱法或尺寸排阻色谱法。色谱法可以是例如,正相色谱法或反相色谱法。
[0061]
另一方面提供一种用于预防或治疗神经退行性脑病的药物组合物,其包括根据一方面的由化学式1表示的化合物、其衍生物、立体异构体、溶剂化物或药学上可接受的盐。
[0062]
由化学式1表示的化合物、立体异构体、溶剂化物以及药学上可接受的盐如上所述。
[0063]
术语“神经退行性脑病(neurodegenerative brain disease)”是指与大脑的退行
性变化相关的所有疾病,特别地是指由于选自大脑和/或脑神经细胞中β-淀粉样蛋白的聚集、tau蛋白的聚集以及tau蛋白的过度磷酸化中的一种或多种而诱发的所有疾病(脑病)。
[0064]
所述神经退行性脑病可以选自由阿尔茨海默氏病(alzheimer's disease)、帕金森病(parkinson's disease)、亨廷顿病(huntington's disease)、轻度认知障碍(mild cognitive impairment)、淀粉贮积病(amyloidosis)、多系统萎缩症(multiple system atrophy)、多发性硬化(multiple sclerosis)、tau蛋白病(tauopathies)、皮克病(pick's disease)、老年性痴呆、肌萎缩侧索硬化(amyotrophic lateral sclerosis)、小脑萎缩症(spinocerebellaratrophy)、抽动秽语综合征(tourette's syndrome)、弗里德里希共济失调症(friedrich's ataxia)、马查多-约瑟夫病(machado-joseph's disease)、路易体痴呆(lewy body dementia)、肌张力障碍(dystonia)、核上性麻痹综合征(progressive supranuclear palsy)以及额颞痴呆(frontotemporaldementia)所组成的组。所述淀粉贮积病可以是原发性淀粉贮积病、继发性淀粉贮积病、遗传性淀粉贮积病或局限性淀粉贮积病。
[0065]
由所述化学式1表示的化合物可以具有抑制β-淀粉样蛋白聚集体形成的活性、抑制诱发β-淀粉样蛋白的细胞凋亡的活性、抑制诱发β-淀粉样蛋白的细胞炎症的活性以及抑制tau聚集体的活性。
[0066]
人β-淀粉样蛋白(amyloid-beta:aβ)可以是包括约36个至约43个氨基酸的肽分子。已知β-淀粉样蛋白是阿尔茨海默氏病患者大脑中表达的淀粉样蛋白斑的主要成分,并且与阿尔茨海默氏病的发病有关。所述β-淀粉样蛋白可以通过使用β分泌酶(beta secretase)和γ分泌酶(gamma secretase)切割淀粉样前体蛋白(amyloid precursor protein:app,uniprotkb p05067)来获得。β-淀粉样蛋白可以通过聚集来形成神经毒性低聚物,从而诱发神经退行性脑病。
[0067]
所述tau蛋白可由n端突起、脯氨酸(proline)聚集域、微细胞器结合域以及c端四部分组成(mandelkow等人,acta.neuropathol.,103,26-35,1996)。已知tau在中枢神经系统的神经细胞中异常过度磷酸化或修饰时,tau蛋白会诱发tau蛋白病(tauopathy)等神经退行性脑病。
[0068]
术语“预防”是指,通过施用组合物来抑制疾病或延迟发病的所有行为。术语“治疗”是指,通过施用组合物来改善或有益地改变疾病症状的所有行为。
[0069]
所述药物组合物可施用于存在下列情况的个体:β-淀粉样蛋白聚集水平高于正常水平或有更高的风险,或者tau蛋白聚集水平高于正常水平或有更高的风险,或者tau蛋白的磷酸化水平高于正常水平或有更高的风险,或者其组合。所述β-淀粉样蛋白或tau蛋白的聚集水平可以意指β-淀粉样蛋白聚集体或tau蛋白聚集体的量(浓度),或者β-淀粉样蛋白聚集体或tau蛋白聚集体对总β-淀粉样蛋白或总tau蛋白的比例。所述tau蛋白的磷酸化水平可以意指磷酸化的tau蛋白的(浓度)或磷酸化的tau蛋白对总tau蛋白的比例。所述“正常”可以意指在所述药物组合物的适用对象(患者)与同种异体个体中不具有先前定义的“神经退行性脑病”的个体或从所述个体分离和/或培养的脑组织或脑细胞(脑神经细胞)。
[0070]
所述药物组合物包括作为活性成分的由化学式1表示的化合物、其衍生物、立体异构体、溶剂化物或药学上可接受的盐。“活性成分”是指用于实现药理学活性(例如,神经退行性脑病)的生理活性物质。
[0071]
所述药物组合物可以进一步包括已知具有预防、治疗或改善神经退行性脑病活性的活性成分。已知具有预防、治疗或改善神经退行性脑病活性的活性成分可以是乙酰胆碱酯酶(cetylcholinesterase)抑制剂或nmda受体拮抗剂(n-methyl-d-aspartate receptor antagonist)。乙酰胆碱酯酶抑制剂可以是他克林(tacrine)、利凡斯的明(rivastigmine)、加兰他敏(galantamine)以及多奈哌齐(donepezil)。nmda受体拮抗剂可以是美金刚(memantine)。由所述化学式1表示的化合物、其衍生物、立体异构体、溶剂化物或药学上可接受的盐以及所述已知活性成分可以是用于同时或依次施用的单一组合物或个别组合物。
[0072]
所述药物组合物可以进一步包括载体、赋形剂或稀释剂。载体、赋形剂以及稀释剂可以包括例如,乳糖、右旋糖、蔗糖、山梨醇、甘露醇、木糖醇、赤藓糖醇、麦芽糖醇、淀粉、阿拉伯树胶、海藻酸钠、明胶、磷酸钙、硅酸钙、纤维素、甲基纤维素、微晶纤维素、聚乙烯吡咯烷酮、水、羟基苯甲酸甲酯、羟基苯甲酸丙酯、滑石、硬脂酸镁或矿物油。
[0073]
所述药物组合物可以分别根据常规方法以散剂、颗粒剂、片剂、胶囊剂、混悬剂、乳剂、糖浆、气雾剂等口服剂型,外用剂、栓剂或灭菌注射液等形式制剂化。在制剂化时,可使用常用的填充剂、增量剂、粘合剂、润湿剂、崩解剂、表面活性剂等稀释剂或赋形剂来制备。
[0074]
在所述药物组合物中,用于口服施用的固体剂型可以是片剂、丸剂、散剂、颗粒剂或胶囊剂。所述固体剂型可以进一步包括赋形剂。赋形剂可以是例如,淀粉、碳酸钙(calcium carbonate)、蔗糖(sucrose)、乳糖(lactose)或明胶。另外,所述固体剂型可以进一步包括硬脂酸镁或诸如滑石等润滑剂。在所述药物组合物中,用于口服施用的液体剂型可以是悬浮剂、口服溶液剂、乳剂或糖浆剂。所述液体剂型可以包括水或液体石蜡。所述液体剂型可以包括赋形剂,例如,润湿剂、甜味剂、芳香剂或保护剂。在所述药物组合物中,用于肠胃外施用的制剂可以是灭菌水溶液剂、非水溶液剂、悬浮剂、乳剂、冻干剂或/和栓剂。非水溶液剂或悬浮剂可以包括植物油或酯。植物油可以是例如,丙二醇(propyleneglycol)、聚乙二醇或橄榄油。酯可以是例如,油酸乙酯。栓剂的基质可以是合成脂肪酸酯(witepsol)、聚乙二醇、吐温(tween)61、可可脂、月桂脂肪或甘油明胶。
[0075]
所述药物组合物可以包括有效量的由化学式1表示的化合物、其衍生物、立体异构体、溶剂化物或药学上可接受的盐。术语“有效量”是指,在施用于需要预防或治疗的个体时,足以显示出预防或治疗效果的量。所属领域的技术人员可以根据被选细胞或个体,适当选择所述有效量。所述药物组合物的优选施用量根据个体的状态和体重、患病程度、药物形式、施用途径和时间而不同,但是可由所属领域的技术人员适当选择。但是,所述化合物、其衍生物、立体异构体、溶剂化物或药学上可接受的盐能够以例如,将约0.0001
㎎
/
㎏
至约100
㎎
/
㎏
、或约0.001
㎎
/
㎏
至约100
㎎
/
㎏
的量每天分1次至24次,2天至1周内分1次至7次,或者1个月至12个月内分1次至24次施用。在所述药物组合物中,化合物、其衍生物、立体异构体、溶剂化物或药学上可接受的盐能够以基于全部组合物总重量的约0.0001重量%至约10重量%,或者约0.001重量%至约1重量%来包括。
[0076]
施用方法可以是口服施用或肠胃外施用。施用方法可以是例如,口服、经皮、皮下、直肠、静脉内、动脉内、腹腔内、肌肉内、胸骨内、局部、鼻内(intranasal)、气管内(intratracheal)或皮内途径。所述组合物可以全身或局部施用,并且可以单独或与另外的药物活性化合物一同施用。
[0077]
另一方面提供一种用于预防或改善神经退行性脑病或认知障碍的保健功能食品,
其包括根据一方面的由化学式1表示的化合物、其衍生物、立体异构体、溶剂化物或盐。
[0078]
所述由化学式1表示的化合物、立体异构体、溶剂化物、盐、神经退行性脑病以及预防如上所述。
[0079]
术语“认知障碍”中的“认知”是指通过思考、经验以及感觉获得知识和领悟的精神活动或过程。其中可以包括知识、主义、记忆和工作记忆、判断和评价、推理和计算、问题的解决和决策,以及对语言的理解和生成等过程。所述认知障碍属于主要影响学习、记忆、感知和问题解决的精神健康障碍范畴,其可以包括失忆症、痴呆症和谵妄。
[0080]
术语“改善”包括使病情好转或有助于病情的所有行为。
[0081]
保健功能食品是指使用日常膳食中容易缺乏的营养素或具有对人体有益功能的原料或成分(以下称为“功能性原料”)制造,并且有助于保持健康或者预防和/或改善预定疾病或症状的食品。
[0082]
可以通过将由化学式1表示的化合物、其衍生物、立体异构体、溶剂化物或盐配制成胶囊、粉剂或悬浮液等,将所述保健功能食品用作功能食品或添加到各种食品。所述食品可以是例如,肉类、香肠、面包、巧克力、糖果类、零食类、饼干类、比萨饼、方便面、其它面条类、口香糖类、包括冰淇淋类在内的乳制品、各种汤、饮料、茶、功能饮料、酒精饮料、维生素复合物、功能性食品以及保健食品。
[0083]
另一方面提供一种预防或治疗神经退行性脑病的方法,其包括将用于预防或治疗神经退行性脑病的药物组合物施用于个体,所述药物组合物包括根据一方面的由化学式1表示的化合物、其衍生物、立体异构体、溶剂化物或药学上可接受的盐。
[0084]
所述由化学式1表示的化合物、立体异构体、溶剂化物、药学上可接受的盐、神经退行性脑病、预防、治疗以及药物组合物如上所述。
[0085]
所述个体可以是哺乳动物,例如,人、小鼠、大鼠、牛、马、猪、狗、猴、羊、山羊或猫。所述个体可能患有与神经退行性脑病相关的疾病或者患病可能性高。
[0086]
所述方法可以进一步包括向所述个体施用针对神经退行性脑病的已知活性成分。所述已知活性成分可以与由化学式1表示的化合物、其衍生物、立体异构体、溶剂化物或药学上可接受的盐同时、分别或依次施用于所述个体。
[0087]
施用方法可以是口服施用或肠胃外施用。施用方法可以是例如,口服、经皮、皮下、直肠、静脉内、动脉内、腹腔内、肌肉内、胸骨内、局部、鼻内(intranasal)、气管内(intratracheal)或皮内途径。所述药物组合物可以全身或局部施用,并且可以单独或与另外的药物活性化合物一同施用。
[0088]
所述药物组合物的优选施用量根据患者的状态和体重、患病程度、药物形式、施用途径和时间而不同,但是可由所属领域的技术人员适当选择。所述施用量可以是例如,以成人为准,约0.001mg/kg至约100mg/kg、约0.01mg/kg至约10mg/kg或约0.1mg/kg至约1mg/kg的范围。所述施用可以是1天1次、1天多次,或者1周1次、2周1次、3周1次,或者4周1次至1年1次。
[0089]
另一方面提供一种预防或改善神经退行性脑病或认知障碍的方法,其包括将保健功能食品施用于个体,所述保健功能食品包括根据一方面的由化学式1表示的化合物、其衍生物、立体异构体、溶剂化物或盐。
[0090]
所述由化学式1表示的化合物、立体异构体、溶剂化物、盐、保健功能食品、神经退
行性脑病、认知障碍、预防以及改善如上所述。有益效果
[0091]
三环双内酯化合物、其衍生物、立体异构体、溶剂化物或药学上可接受的盐抑制β-淀粉样蛋白聚集和tau蛋白聚集并具有抑制细胞凋亡活性和抗炎活性,且可用于预防、治疗或改善包括阿尔茨海默氏病在内的各种神经退行性脑病和认知障碍。
附图说明
[0092]
图1是示出培养链霉菌属(streptomyces sp.)won17菌株的培养基的图。
[0093]
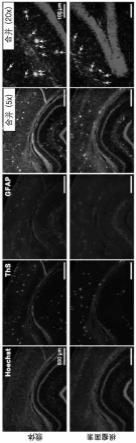
图2a是为了确认根瘤菌素对β-淀粉样蛋白聚集体形成的抑制活性的实验的示意性视图,图2b是用硫黄素s对脑组织中的β-淀粉样蛋白聚集体进行染色的图,图2c是在海马中对斑块进行定量的图表(veh:载体、rhi:根瘤菌素、*:p《0.05),图2d是示出脑组织中的gfap以及用硫黄素s染色的β-淀粉样蛋白的图与合并图(ths:硫黄素s、merged:合并)。
[0094]
图3a是示出当存在根瘤菌素时抑制β-淀粉样蛋白聚集体形成的图表,图3b是示出当存在根瘤菌素时形成的β-淀粉样蛋白聚集体分解的图表(y轴:相对荧光强度(%)、rhi:根瘤菌素、*:p《0.05、***:p《0.001)。
[0095]
图4是示出当存在根瘤菌素时经β-淀粉样蛋白处理的ht-22小鼠海马神经细胞株细胞活力(%)的图表(nt:阴性对照组、rhi:根瘤菌素、*:p《0.05、**:p《0.01)。
[0096]
图5a是确认在经β-淀粉样蛋白聚集体和根瘤菌素处理的ht-22和bv2中被切割的caspase-3和bcl-2(b-cell lymphoma 2)表达的免疫印迹图,图5b是示出通过夹心elisa法检测白细胞介素-1β量的图表(rhi:根瘤菌素、*:p《0.05、***:p《0.01)。
[0097]
图6a是示出当存在根瘤菌素时抑制tau蛋白聚集体形成的图表,图6b是示出当存在根瘤菌素时形成的tau蛋白聚集体分解的图表(y轴:相对荧光强度(%)、rhi:根瘤菌素、*:p《0.01、***:p《0.001)。
具体实施方式
[0098]
通过以下实施例进一步详细描述本发明。但是,这些实施例仅用于示例性描述,本发明的范围并不限于此。
[0099]
实施例1.分离根瘤菌素和确认其结构
[0100]
1-1.分离根瘤菌素生产菌株
[0101]
从种植人参(panax ginseng)的土壤中分离出作为根瘤菌素(rhizolutin)生产菌株的链霉菌属(streptomyces sp.)wom17菌株。从固体培养基(每1l无菌水2g的酪蛋白酸钠(sodium caseinate)、0.1g的天冬酰胺、4g的丙酸钠(sodium propionate)、0.5g的磷酸氢二钾(dipotassium phosphate)、0.1g的硫酸镁(magnesium sulfate)、0.001g的硫酸亚铁(ferrous sulfate)以及15g的琼脂粉末)中分离won17菌株。根据16s rdna碱基序列分析结果,该菌株被鉴定为链霉菌属。将该菌株命名为链霉菌属won17菌株,并于2020年6月17日将所述菌株保藏至韩国典型培养物保藏中心(kctc)(保藏编号:kctc14217bp)。
[0102]
1-2.培养链霉菌属won17菌株
[0103]
将链霉菌属won17菌株涂抹于yeme固体培养基(每1l蒸馏水4g的酵母菌提取物、10g的麦芽提取物、4g的葡萄糖以及18g的琼脂)后,在约30℃下培养约4周。
[0104]
将培养后的won17菌株的孢子接种至50ml体积的yeme液体培养基(每1l蒸馏水4g的酵母菌提取物、10g的麦芽提取物以及4g的葡萄糖)后,以200rpm振荡并在30℃下培养约5天。将10ml的培养液接种至200ml体积的改良(modified)yeme液体培养基(每1l蒸馏水4g的酵母菌提取物、10g的麦芽提取物、4g的葡萄糖、10ml的橄榄油以及11g的干燥人参粉末)后,在170rpm和30℃条件下培养约5天。
[0105]
1-3.分离和纯化根瘤菌素
[0106]
得到通过实施例1-2培养的won17菌株的培养物。
[0107]
在放置于支架的分液漏斗中,放入1l培养终止的won17菌株培养液和约1.5l体积的乙酸乙酯(et0ac,daejung chemical&metals co.,ltd.)后,用盖子封住并上下左右摇晃3分钟,从而进行1次提取。然后将分液漏斗重新放置于支架,待水层和et0ac层完全分离后,打开分液漏斗的阀去除水层。在水层中添加新的et0ac后,利用相同的方式进行重复提取。将et0ac层另外保存至干净的烧瓶中,添加无水硫酸钠(anhydrous sodium sulfate)(daejung chemical&metalsco.,ltd.)以去除培养物中剩余的水,然后使其通过数层干净的纱布以去除杂质。使用20%(v/v)甲醇水溶液和己烷(体积比1:1)水溶液,以去除橄榄油。在20%(v/v)甲醇水溶液中确认到99%的收率,将最终处理后的etoac转移到3l体积的圆烧瓶,并使用真空干燥器进行减压干燥。共培养700l的菌株,提取后得到约210mg的粗(crude)提取物。
[0108]
利用制备型高效液相色谱(preparative high-performance-liquid-chromatography)进行纯化过程,以从won17菌株的粗提取物中纯化根瘤菌素。用31%(v/v)的甲醇/69%(v/v)的h2o稳定填充有c
18
树脂的封闭柱,然后在约40分钟的浓度梯度条件下进行分离直至50%(v/v)的甲醇浓度。在约31分钟左右与萘霉素等其它物质一同检测出根瘤菌素物质。
[0109]
利用半制备高效液相色谱以40%(v/v)的乙腈/60%(v/v)的h2o等浓度条件分离物质,以从减压干燥的30分钟峰中获得纯根瘤菌素。具体的高效液相色谱条件如下。
[0110]
(1)使用反相柱(c
18
(2)phenomenex luna、5μm 250
×
21.2mm)并以31%(v/v)至50%(v/v)的甲醇/水溶液的浓度梯度条件(流速:10ml/分钟、检测:uv 254nm)分离约40分钟。在约31分钟的流份中确认到根瘤菌素。
[0111]
(2)使用反相柱(c
18 phenomenex 250
×
4.6mm)并以添加0.1%(v/v)甲酸的40%(v/v)乙腈/水溶液等浓度条件(流速:1ml/分钟、检测:uv 254nm)下分离减压干燥后的约31分钟流份。在约28分钟的流份中确认到根瘤菌素。
[0112]
通过重复该过程,从约5g的粗提取物中获得约100mg的根瘤菌素。
[0113]
1-4.确认根瘤菌素的化学结构
[0114]
基于1d和2d核磁共振(nuclear magnetic resonance:nmr)光谱确认根瘤菌素的结构。核磁共振光谱(1h nmr,
13
c nmr)使用bruker公司的500mhz nmr,溶剂使用丙酮-d6。
[0115]
将通过核磁共振光谱确认的根瘤菌素的结构定位示于表1。
[0116]
【根瘤菌素】
[0117]
(1)分子式:c
21h28
o5[0118]
(2)分子量:360
[0119]
(3)颜色:白色粉末
[0120]
(4)1h-nmr(吡啶(pyridine)-d
5、、
600mhz):参考表1
[0121]
(5)
13
c-nmr(吡啶(pyridine)-d5、150mhz):参考表1
[0122]
[表1][表1]
[0123]
经1d和2d核磁共振(nmr)光谱结果分析的根瘤菌素的化学结构式如下。
[0124]
【根瘤菌素】
[0125][0126]
实施例2.确认根瘤菌素的活性
[0127]
2-1.根瘤菌素对β-淀粉样蛋白聚集体形成的抑制活性
[0128]
确认根瘤菌素是否能够溶解β-淀粉样蛋白聚集体。
[0129]
首先,准备已注入阿尔茨海默氏病患者基因的app/ps1转基因小鼠(7.5月龄、雄性、杰克逊实验室、9至10只/组)。app/ps1转基因小鼠表达高水平的人β-淀粉样蛋白并在大脑中形成β-淀粉样蛋白类似斑块。
[0130]
向准备好的小鼠以8mg/体重kg/天的剂量每天腹腔内施用根瘤菌素,共施用3周。对于阴性对照组,仅腹腔内施用载体。
[0131]
之后取出小鼠的大脑,检测脑组织中作为阿尔茨海默氏病生物标记物的β-淀粉样蛋白聚集体(oligomer,fibril)的变化。
[0132]
将利用硫黄素s(thioflavin s,sigma-aldrich)对脑组织中的β-淀粉样蛋白聚集体进行染色的图像示于图2b,将量化海马中斑块的图表示于图2c(利用未配对样本t检验,平均
±
sem)。如图2b和图2c所示,施用根瘤菌素的组相比于阴性对照组,大脑海马中的β-淀粉样蛋白斑块的数量减少。
[0133]
将作为星形细胞增多症(astrocytosis)生物标记物的胶质纤维酸性蛋白(glial fibrillary acidic protein:gfap)以及用硫黄素s染色的β-淀粉样蛋白聚集体的图像示于图2d。如图2d所示,可通过硫黄素s染色来确认的β-淀粉样蛋白聚集体数量因施用根瘤菌素而减少,并且作为神经炎症标记物的gfap也同样减少,因而斑块周围的星形细胞增多症水平也显著减少。
[0134]
2-2.对β-淀粉样蛋白聚集的抑制和分解活性
[0135]
将人aβ
1~42
单体(uniprot kb-p05067,a.a.672至713)溶于dms0至浓度为10mm,以准备β-淀粉样蛋白溶液。之后,用蒸馏水稀释β-淀粉样蛋白溶液以准备100μm浓度的溶液。
[0136]
另一方面,硫黄素t(sigma-aldrich)溶于50mm的甘氨酸缓冲液(ph8.5)至浓度为5mm。然后,使用50mm甘氨酸缓冲液(ph8.5)将其稀释至5μm,并以避光状态贮存在暗室中。
[0137]
为了验证根瘤菌素对β-淀粉样蛋白聚集的抑制活性,将β-淀粉样蛋白溶液分别放入1.5ml的微管中至25μm,以1mm的浓度加入根瘤菌素后在37℃下孵育120小时。
[0138]
将反应终止的反应液以每孔25μl的量放入96-孔板中,然后以每孔75μl的量放入备好的硫黄素t溶液。在常温下以暗室状态反应5分钟后,使用多功能微孔读板机(multi-mode microplate reader)检测450nm激发(excitation)波长和485nm发射(emission)波长下的荧光值。
[0139]
以处理β-淀粉样蛋白后聚集120小时的组(对照组)的荧光强度为准,计算每个组
的荧光强度(%)并将其结果示于图3a(进行单因素方差分析后利用邦弗朗尼事后检定/检验法,平均
±
sem,***:p《0.001)。
[0140]
另外,为了验证根瘤菌素对β-淀粉样蛋白聚集的分解活性,将β-淀粉样蛋白溶液分别放入1.5ml的微管中至25μm后,在37℃下孵育72小时。之后,在每个微管中加入1mm的根瘤菌素后,在37℃下孵育72小时。为了比较活性,将已知有效溶解β-淀粉样蛋白聚集的化合物4-(2-羟乙基)-1-哌嗪丙磺酸(4-(2-hydroxyethyl)-1-piperazinepropanesulphonic acid:epps,cas编号:16052-06-5)以20mm的浓度在相同条件下进行孵育。
[0141]
将反应终止的反应液以每孔25μl的量放入96-孔板中,然后以每孔75μl的量放入备好的硫黄素t溶液。使用多功能微孔读板机检测450nm激发波长和485nm发射波长下的荧光值。
[0142]
以仅处理β-淀粉样蛋白后聚集72小时的组(对照组)的荧光强度为准,计算每个组的荧光强度(%)并将其结果示于图3b(平均
±
sem、*:p《0.05、***:p《0.001)。
[0143]
如图3a和图3b所示,确认到根瘤菌素很好地抑制β-淀粉样蛋白聚集体(oligomer,fibril)的形成且很好地溶解β-淀粉样蛋白聚集体,并且其溶解效果比现有报告中已知作为β-淀粉样蛋白聚集溶解物质的epps更优异。
[0144]
2-3.确认根瘤菌素的细胞凋亡抑制活性
[0145]
确认根瘤菌素是否能够抑制被β-淀粉样蛋白聚集体神经毒性暴露的神经细胞的细胞凋亡。
[0146]
为检测根瘤菌素的细胞毒性,将ht-22小鼠海马神经细胞株以一定数量接种到板中。将如实施例2-2所述准备好的β-淀粉样蛋白溶液以10μm的最终浓度加入到ht-22细胞株中,然后在37℃下孵育72小时。之后,在每个微管中加入20μm的根瘤菌素后,在37℃下孵育24小时。将不存在β-淀粉样蛋白和根瘤菌素的载体用作阴性对照组。
[0147]
利用mtt(3-(4,5-二甲基噻唑-2-基)-2,二苯基溴化四唑)(3-(4,5-dimethylthiazol-2-yl)-2,5-diphenyltetrazolium bromide)分析法检测ht-22细胞株的存活率。以未加入β-淀粉样蛋白的ht-22细胞株(阴性对照组)的活力(%)为准,计算每个组的细胞活力(%)并将其结果示于图4,(进行单因素方差分析后利用邦弗朗尼事后检定/检验法,平均
±
sem,nt:阴性对照组,*:p《0.05,**:p《0.01)。
[0148]
如图4所示,确认到暴露于β-淀粉样蛋白聚集体神经毒性的神经细胞的细胞凋亡因根瘤菌素而受到抑制。因此,证实根瘤菌素具有抑制β-淀粉样蛋白聚集体引起的神经细胞凋亡的活性。
[0149]
2-4.验证根瘤菌素的细胞凋亡抑制活性
[0150]
为验证根瘤菌素对β-淀粉样蛋白聚集体神经毒性的抑制活性,将神经细胞暴露于β-淀粉样蛋白聚集体的神经毒性后确认细胞凋亡(apoptosis)相关生物标记物的变化。将作为细胞凋亡诱导因子的经切割的caspase-3和抑制细胞凋亡的bcl-2用作生物标记物。
[0151]
将ht-22小鼠海马神经细胞株和bv2小神经胶质细胞(microglial cell)以一定数量接种到板中。将如实施例2-2所述备好的β-淀粉样蛋白溶液以1mm分别加入到ht-22和bv2细胞株中,然后在37℃下孵育24小时。之后,将20μm的根瘤菌素加入到每个微管后,与最终浓度为20μm的β-淀粉样蛋白一同在37℃下孵育24小时。将不存在根瘤菌素和β-淀粉样蛋白的组用作阴性对照组。
[0152]
通过免疫印迹确认作为细胞凋亡相关生物标记物的被切割的caspase-3和bcl-2(b-cell lymphoma 2),并将其图像示于图5a。如图5a所示,确认到β-淀粉样蛋白聚集体使bcl-2表达降低并且使被切割的caspase-3表达增加,因而β-淀粉样蛋白聚集体诱导神经细胞的细胞凋亡。另外,当同时处理β-淀粉样蛋白聚集体和根瘤菌素时bcl-2的表达增加,并且被切割的caspase-3的表达降低。因此,证实细胞的β-淀粉样蛋白诱发的细胞凋亡因根瘤菌素的处理而受到抑制。
[0153]
另一方面,通过夹心elisa法(利用未配对样本t检验)检测经β-淀粉样蛋白聚集体和根瘤菌素处理的ht-22和bv2细胞中作为炎症生物标记物的白介素-1β(interleukin-1β:il-1β)的量。将显示il-1β根据β-淀粉样蛋白聚集体和根瘤菌素处理时间的量示于图5b(平均
±
sem,*:p《0.05,**:p《0.01)。如图5b所示,确认到细胞的β-淀粉样蛋白诱发的神经炎症因根瘤菌素的处理而受到抑制。
[0154]
2-5.根瘤菌素的tau聚集体形成抑制活性
[0155]
确认根瘤菌素是否能够抑制作为另一致病蛋白的tau蛋白聚集。
[0156]
准备1mg/ml浓度的tau蛋白,然后如实施例2-3所示将tau蛋白分别放入1.5ml的微管至0.5mg/ml,分别加入1mm的根瘤菌素和20mm的epps,然后在37℃下孵育120小时。
[0157]
另一方面,将tau蛋白分别放入1.5ml的微管至0.5mg/ml并在37℃下孵育48小时后,加入1mm的根瘤菌素后在37℃下孵育72小时。加入20mm的epps后以相同条件进行孵育,以对功效进行比较。
[0158]
在反应物中加入硫黄素t并检测450nm激发波长和485nm发射波长下的荧光强度。将不存在tau蛋白和根瘤菌素的载体用作阴性对照组。
[0159]
以tau蛋白单独处理组(阳性对照组)的荧光强度为准,计算每个组的荧光强度(%)并将其结果示于图6a和图6b(平均
±
sem、**:p《0.01、***:p《0.001)。
[0160]
如图6a和图6b所示,当处理根瘤菌素时,tau蛋白聚集体形成受到抑制(图6a),同时原本生成的tau聚集体被溶解(图6b)。在将已知有效溶解β-淀粉样蛋白聚集的epps用作比较组时,确认到根瘤菌素对tau聚集体形成的抑制以及聚集体的溶解效果更优异。
[0161]
因此,证实根瘤菌素具有对β-淀粉样蛋白聚集体的抑制活性、对β-淀粉样蛋白诱发细胞凋亡的抑制活性、对β-淀粉样蛋白诱发细胞炎症的抑制活性以及对tau聚集体的抑制活性,由此可用于治疗阿尔茨海默氏病。
[0162]
【保藏编号】
[0163]
保藏机构:韩国典型培养物保藏中心(kctc)
[0164]
保藏编号:kctc14217bp
[0165]
保藏日期:20200617。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1