一种β-咔啉杂合咪唑类化合物及其制备方法、应用
一种
β
‑
咔啉杂合咪唑类化合物及其制备方法、应用
技术领域
1.本发明属于医药化学领域,具体涉及一种β
‑
咔啉杂合咪唑类化合物及其制备方法、应用。
背景技术:
2.β
‑
咔啉衍生物是一类生物碱,广泛存在于自然界中。β
‑
咔啉衍生物具有广泛的生物活性,如抗肿瘤、抗病毒、抗菌、抗包虫及抗血栓等作用。β
‑
咔啉衍生物具有潜在的应用价值。近些年来,通过人工合成得到了大量的β
‑
咔啉衍生物,其中发现β
‑
咔啉c3
‑
位烷胺基可增强抗肿瘤活性,n2
‑
位修饰可以同时增强细胞毒性和急性毒性。
3.咪唑并吡啶衍生物是一类重要的含氮杂环化合物,具有抗病毒、抗细菌、抗微生物活性和抗疲劳、抗焦虑,治疗肿瘤、高血压、胃溃疡、精神病的功效,受到药物化学研究者的广泛关注。目前已经有多种含该片段的药物进入药品市场,例如minodronic acid,alpidem,olprinone,zolpidem,zolimidine等。
[0004][0005]
有鉴于此,本发明提出一种新的化合物—β
‑
咔啉杂合咪唑类化合物,对发现具有潜在应用前景的药物具有重要意义。
技术实现要素:
[0006]
本发明的目的在于提供一种β
‑
咔啉杂合咪唑类化合物,该类化合物为新结构类型化合物,在其外部通过稠合咪唑环,使β
‑
咔啉环2,3
‑
位同时具有取代基。
[0007]
为了实现上述目的,所采用的技术方案为:
[0008]
一种β
‑
咔啉杂合咪唑类化合物,所述的β
‑
咔啉杂合咪唑类化合物的化学结构通式为:
[0009][0010]
进一步地,所述的β
‑
咔啉杂合咪唑类化合物的化学结构通式中,r选自环烷基、芳基和取代芳基、萘基中的一种;
[0011]
r9选自氢、c1
‑
c4直链或支链烷基、芳烷基、取代芳烷基、芳基中的一种。
[0012]
进一步地,所述的β
‑
咔啉杂合咪唑类化合物,为下列任一化合物:
[0013]2‑
苯基
‑
6h
‑
咪唑并[1',2':1,6]吡啶并[3,4
‑
b]吲哚,
[0014]2‑
(4
‑
三氟甲基)苯基
‑
6h
‑
咪唑并[1',2':1,6]吡啶并[3,4
‑
b]吲哚,
[0015]2‑
(4
‑
甲氧基)苯基
‑
6h
‑
咪唑并[1',2':1,6]吡啶并[3,4
‑
b]吲哚,
[0016]6‑
甲基
‑2‑
苯基
‑
6h
‑
咪唑并[1',2':1,6]吡啶并[3,4
‑
b]吲哚,
[0017]6‑
甲基
‑2‑
(4
‑
氟苯基)
‑
6h
‑
咪唑并[1',2':1,6]吡啶并[3,4
‑
b]吲哚,
[0018]6‑
甲基
‑2‑
(4
‑
三氟甲基)苯基
‑
6h
‑
咪唑并[1',2':1,6]吡啶并[3,4
‑
b]吲哚,
[0019]6‑
甲基
‑2‑
(4
‑
甲氧基)苯基
‑
6h
‑
咪唑并[1',2':1,6]吡啶并[3,4
‑
b]吲哚,
[0020]6‑
甲基
‑2‑
环丙基
‑
6h
‑
咪唑并[1',2':1,6]吡啶并[3,4
‑
b]吲哚,
[0021]6‑
丁基
‑2‑
苯基
‑
6h
‑
咪唑并[1',2':1,6]吡啶并[3,4
‑
b]吲哚,
[0022]6‑
丁基
‑2‑
(4
‑
氟苯基)
‑
6h
‑
咪唑并[1',2':1,6]吡啶并[3,4
‑
b]吲哚,
[0023]6‑
丁基
‑2‑
(4
‑
三氟甲基)苯基
‑
6h
‑
咪唑并[1',2':1,6]吡啶并[3,4
‑
b]吲哚,
[0024]6‑
丁基
‑2‑
(4
‑
甲氧基)苯基
‑
6h
‑
咪唑并[1',2':1,6]吡啶并[3,4
‑
b]吲哚,
[0025]6‑
丁基
‑2‑
环丙基
‑
6h
‑
咪唑并[1',2':1,6]吡啶并[3,4
‑
b]吲哚,
[0026]6‑
苄基
‑2‑
苯基
‑
6h
‑
咪唑并[1',2':1,6]吡啶并[3,4
‑
b]吲哚,
[0027]6‑
苄基
‑2‑
(4
‑
三氟甲基)苯基
‑
6h
‑
咪唑并[1',2':1,6]吡啶并[3,4
‑
b]吲哚,
[0028]6‑
苄基
‑2‑
(4
‑
氟苯基)
‑
6h
‑
咪唑并[1',2':1,6]吡啶并[3,4
‑
b]吲哚,
[0029]6‑
丁基
‑2‑
环丙基
‑
6h
‑
咪唑并[1',2':1,6]吡啶并[3,4
‑
b]吲哚,
[0030]6‑
苄基
‑2‑
(4
‑
甲氧基)苯基
‑
6h
‑
咪唑并[1',2':1,6]吡啶并[3,4
‑
b]吲哚,
[0031]6‑
(4
‑
氟苄基)
‑2‑
苯基
‑
6h
‑
咪唑并[1',2':1,6]吡啶并[3,4
‑
b]吲哚,
[0032]6‑
(4
‑
氟苄基)
‑2‑
(4
‑
氟苯基)
‑
6h
‑
咪唑并[1',2':1,6]吡啶并[3,4
‑
b]吲哚,
[0033]6‑
(4
‑
氟苄基)
‑2‑
(4
‑
甲氧基)苯基
‑
6h
‑
咪唑并[1',2':1,6]吡啶并[3,4
‑
b]吲哚,
[0034]6‑
(4
‑
氟苄基)
‑2‑
(4
‑
三氟甲基)苯基
‑
6h
‑
咪唑并[1',2':1,6]吡啶并[3,4
‑
b]吲哚,
[0035]6‑
(4
‑
氟苄基)
‑2‑
环丙基
‑
6h
‑
咪唑并[1',2':1,6]吡啶并[3,4
‑
b]吲哚。
[0036]
本发明的另一个目的在于提供上述β
‑
咔啉杂合咪唑类化合物在制备抗肿瘤药物中的应用。
[0037]
本发明还有一个目的在于提供上述β
‑
咔啉杂合咪唑类化合物的制备方法,借鉴β
‑
咔啉环含有吡啶环的结构特点,在其外部通过稠合咪唑环,使β
‑
咔啉环2,3
‑
位同时具有取代基,获得β
‑
咔啉杂合咪唑类化合物。且该制备方法具有较好的收率。
[0038]
为了实现上述目的,所采用的技术方案为:
[0039]
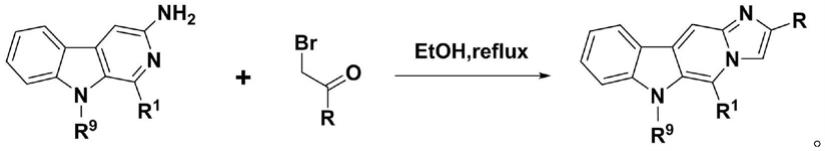
上述的β
‑
咔啉杂合咪唑类化合物的制备方法,所述的制备方法的化学反应式为:
[0040][0041]
进一步地,向相应的3
‑
氨基
‑
β
‑
咔啉、2
‑
溴苯乙酮加入无水乙醇并加热搅拌,至原料完全溶解后,加热回流;回流过程中有大量固体析出,至固体不再析出后停止加热,将反应液冷却、过滤,得析出的黄色粉末状的固体;将所述的固体用无水乙醇重结晶,得所述的咪唑并[1',2':1,6]吡啶并[3,4
‑
b]吲哚类化合物。
[0042]
再进一步地,所述的相应的3
‑
氨基
‑
β
‑
咔啉与2
‑
溴苯乙酮的摩尔比为1:2。
[0043]
再进一步地,所述的相应的3
‑
氨基
‑
β
‑
咔啉与无水乙醇的比例为1mmol:15ml。
[0044]
与现有技术相比,本发明的有益效果在于:
[0045]
1、本发明在借鉴β
‑
咔啉环含有吡啶环的结构特点,在其外部通过稠合咪唑环,使β
‑
咔啉环2,3
‑
位同时具有取代基,获得β
‑
咔啉杂合咪唑类化合物。
[0046]
2、本发明的β
‑
咔啉杂合咪唑类化合物,结合了已有技术方案的β
‑
咔啉c3‑
位烷胺基可增强抗肿瘤活性,n2‑
位修饰可以同时增强细胞毒性和急性毒性(其修饰位置如下所示)。
[0047][0048]
3、本发明的β
‑
咔啉杂合咪唑类化合物为一种新的化合物,具有较好的抗肿瘤活性,可应用于抗肿瘤药物中。
具体实施方式
[0049]
为了进一步阐述本发明一种β
‑
咔啉杂合咪唑类化合物及其制备方法、应用,达到预期发明目的,以下结合较佳实施例,对依据本发明提出的一种β
‑
咔啉杂合咪唑类化合物及其制备方法、应用,其具体实施方式、结构、特征及其功效,详细说明如后。在下述说明中,不同的“一实施例”或“实施例”指的不一定是同一实施例。此外,一或多个实施例中的特定特征、结构或特点可由任何合适形式组合。
[0050]
下面将结合具体的实施例,对本发明一种β
‑
咔啉杂合咪唑类化合物及其制备方法、应用做进一步的详细介绍:
[0051]
实施例1.
[0052]
β
‑
咔啉杂合咪唑类化合物的制备方法采用以下反应式:
calcd for c
20
h
16
n3o
+
[m+h]
+
314.12879,found 314.12891.
[0065]
实施例5.
[0066]
实施例5的操作步骤与实施例1相同,其中,r为苯基,r9为甲基,得到的产物为6
‑
甲基
‑2‑
苯基
‑
6h
‑
咪唑并[1',2':1,6]吡啶并[3,4
‑
b]吲哚。
[0067]6‑
甲基
‑2‑
苯基
‑
6h
‑
咪唑并[1',2':1,6]吡啶并[3,4
‑
b]吲哚(d):黄色固体,收率:89.2%。1h nmr(400mhz,dmso
‑
d6)δ9.30(s,1h),8.83(s,1h),8.58(s,1h),8.50(d,j=8.0hz,1h),8.03(d,j=8.0hz,2h),7.69(t,j=7.6hz,1h),7.65
–
7.60(m,3h),7.58
–
7.53(m,1h),7.33
–
7.28(m,1h),3.89(s,3h).
13
c nmr(100mhz,dmso
‑
d6)δ145.76,136.53,135.97,134.68,131.47,131.24,130.73,129.88,127.15,126.71,123.85,120.40,119.84,110.64,110.17,109.51,100.49,30.29.hrms(esi)m/z calcd for c
20
h
16
n
3+
[m+h]
+
298.13387,found298.13382.
[0068]
实施例6.
[0069]
实施例6的操作步骤与实施例1相同,其中,r为4
‑
氟苯基,r9为甲基,得到的产物为6
‑
甲基
‑2‑
(4
‑
氟苯基)
‑
6h
‑
咪唑并[1',2':1,6]吡啶并[3,4
‑
b]吲哚。
[0070]6‑
甲基
‑2‑
(4
‑
氟苯基)
‑
6h
‑
咪唑并[1',2':1,6]吡啶并[3,4
‑
b]吲哚(e):黄色固体,收率:91.3%。1h nmr(400mhz,dmso
‑
d6)δ9.31(d,j=1.2hz,1h),8.81(s,1h),8.59(s,1h),8.51(d,j=7.6hz,1h),8.12
–
8.05(m,2h),7.73
–
7.68(m,1h),7.64(d,j=8.4hz,1h),7.52
–
7.45(m,2h),7.34
–
7.29(m,1h),3.90(s,3h).
13
c nmr(100mhz,dmso
‑
d6)δ162.28(d,j=246.8hz),145.79,136.54,135.21,134.72,131.50,131.26,129.23(d,j=8.6hz),123.87,123.83,120.43,119.87,117.12(d,j=22.1hz),110.58,110.20,109.55,100.56,30.30.hrms(esi)m/z calcd for c
20
h
15
fn
3+
[m+h]
+
316.12445,found316.12473.
[0071]
实施例7.
[0072]
实施例7的操作步骤与实施例1相同,其中,r为4
‑
三氟甲基苯基,r9为甲基,得到的产物为6
‑
甲基
‑2‑
(4
‑
三氟甲基)苯基
‑
6h
‑
咪唑并[1',2':1,6]吡啶并[3,4
‑
b]吲哚。
[0073]6‑
甲基
‑2‑
(4
‑
三氟甲基)苯基
‑
6h
‑
咪唑并[1',2':1,6]吡啶并[3,4
‑
b]吲哚(f):黄色固体,收率:93.4%。1h nmr(400mhz,dmso
‑
d6)δ9.31(s,1h),8.97(s,1h),8.60(s,1h),8.51(d,j=8.0hz,1h),8.23(d,j=8.0hz,2h),7.98(d,j=8.0hz,2h),7.70(t,j=7.6hz,1h),7.62(d,j=8.0hz,1h),7.31(t,j=7.6hz,1h),3.89(s,3h).
13
c nmr(100mhz,dmso
‑
d6)δ145.94,137.14,134.82,131.66,131.53,130.18(q,j=31.7hz),126.80(q,j=4.1hz),123.97,123.07(q,j=270.6hz),120.47,119.91,112.10,110.24,109.58,100.90,30.32.hrms(esi)m/z calcd for c
21
h
15
f3n
3+
[m+h]
+
366.12126,found 366.12143.
[0074]
实施例8.
[0075]
实施例8的操作步骤与实施例1相同,其中,r为4
‑
甲氧基苯基,r9为甲基,得到的产物为6
‑
甲基
‑2‑
(4
‑
甲氧基)苯基
‑
6h
‑
咪唑并[1',2':1,6]吡啶并[3,4
‑
b]吲哚。
[0076]6‑
甲基
‑2‑
(4
‑
甲氧基)苯基
‑
6h
‑
咪唑并[1',2':1,6]吡啶并[3,4
‑
b]吲哚(g):浅黄色固体,收率:87.8%。1h nmr(400mhz,dmso
‑
d6)δ8.81(s,1h),8.43(s,1h),8.31(s,1h),8.21(d,j=7.6hz,1h),7.96(d,j=8.4hz,2h),7.52(t,j=7.6hz,1h),7.45(d,j=8.4hz,1h),7.16(t,j=7.2hz,1h),7.03(d,j=8.4hz,2h),3.81(s,3h),3.74(s,3h).
13
c nmr(100mhz,dmso
‑
d6)δ159.44,145.14,142.90,142.88,133.70,129.03,127.37,127.25,
126.43,122.11,121.61,119.18,114.59,109.03,107.92,105.72,105.23,55.62,29.91.hrms(esi)m/z calcd for c
21
h
18
n3o
+
[m+h]
+
328.14444,found 328.14481.
[0077]
实施例9.
[0078]
实施例9的操作步骤与实施例1相同,其中,r为环丙基,r9为甲基,得到的产物为6
‑
甲基
‑2‑
环丙基
‑
6h
‑
咪唑并[1',2':1,6]吡啶并[3,4
‑
b]吲哚。
[0079]6‑
甲基
‑2‑
环丙基
‑
6h
‑
咪唑并[1',2':1,6]吡啶并[3,4
‑
b]吲哚(h):黄色固体,收率:82.5%。1h nmr(400mhz,dmso
‑
d6)δ9.23(d,j=1.2hz,1h),8.51(s,1h),8.47(d,j=7.6hz,1h),8.16(s,1h),7.73
–
7.68(m,1h),7.64(d,j=8.0hz,1h),7.34
–
7.28(m,1h),3.87(s,3h),2.30(tt,j=8.4,5.2hz,1h),1.23
–
1.16(m,2h),1.07
–
1.00(m,2h).
13
c nmr(100mhz,dmso
‑
d6)δ145.59,140.63,135.51,134.46,131.24,130.49,123.71,120.32,119.93,110.13,110.04,109.17,100.20,30.24,9.02,7.12.hrms(esi)m/z calcd for c
17
h
16
n
3+
[m+h]
+
262.13387,found 262.13388.
[0080]
实施例10.
[0081]
实施例10的操作步骤与实施例1相同,其中,r为苯基,r9为丁基,得到的产物为6
‑
丁基
‑2‑
苯基
‑
6h
‑
咪唑并[1',2':1,6]吡啶并[3,4
‑
b]吲哚。
[0082]6‑
丁基
‑2‑
苯基
‑
6h
‑
咪唑并[1',2':1,6]吡啶并[3,4
‑
b]吲哚(i):黄色固体,收率:79.4%。1h nmr(400mhz,dmso
‑
d6)δ9.44(s,1h),8.83(s,1h),8.62(s,1h),8.53(d,j=8.0hz,1h),8.03(d,j=8.4hz,2h),7.71
–
7.61(m,4h),7.58
–
7.54(m,1h),7.34
–
7.29(m,1h),4.41(t,j=7.2hz,2h),1.85
–
1.77(m,2h),1.43
–
1.33(m,2h),0.93(t,j=7.2hz,3h).
13
c nmr(100mhz,dmso
‑
d6)δ145.28,136.52,135.91,133.90,131.49,131.36,130.74,129.90,127.13,126.72,123.98,120.40,119.92,110.60,110.36,109.73,100.56,43.42,30.38,20.24,14.22.hrms(esi)m/z calcd for c
23
h
22
n
3+
[m+h]
+
340.18082,found 340.18091.
[0083]
实施例11.
[0084]
实施例11的操作步骤与实施例1相同,其中,r为4
‑
氟苯基,r9为丁基,得到的产物为6
‑
丁基
‑2‑
(4
‑
氟苯基)
‑
6h
‑
咪唑并[1',2':1,6]吡啶并[3,4
‑
b]吲哚。
[0085]6‑
丁基
‑2‑
(4
‑
氟苯基)
‑
6h
‑
咪唑并[1',2':1,6]吡啶并[3,4
‑
b]吲哚(j):黄色固体,收率:85.6%。1h nmr(400mhz,dmso
‑
d6)δ9.43(d,j=0.8hz,1h),8.80(s,1h),8.66(d,j=6.8hz,1h),8.58
–
8.54(m,1h),8.12
–
8.07(m,2h),7.76
–
7.70(m,2h),7.55
–
7.49(m,2h),7.37
–
7.31(m,1h),4.43(t,j=7.2hz,2h),1.86
–
1.78(m,2h),1.42
–
1.32(m,2h),0.92(t,j=7.2hz,3h).
13
c nmr(100mhz,dmso
‑
d6)δ162.31(d,j=247.0hz),145.33,136.60,135.19,133.99(d,j=3.6hz),131.56,131.44,129.28(d,j=8.7hz),124.04,123.88,120.46,119.98,117.18(d,j=21.9hz),110.60,110.44,109.78,100.68,43.42,30.40,20.24,14.22.hrms(esi)m/z calcd for c
23
h
21
fn
3+
[m+h]
+
358.17140,found 358.17169.
[0086]
实施例12.
[0087]
实施例12的操作步骤与实施例1相同,其中,r为4
‑
三氟甲基苯基,r9为丁基,得到的产物为6
‑
丁基
‑2‑
(4
‑
三氟甲基)苯基
‑
6h
‑
咪唑并[1',2':1,6]吡啶并[3,4
‑
b]吲哚。
[0088]6‑
丁基
‑2‑
(4
‑
三氟甲基)苯基
‑
6h
‑
咪唑并[1',2':1,6]吡啶并[3,4
‑
b]吲哚(k):黄色固体,收率:87.2%。1h nmr(400mhz,dmso
‑
d6)δ9.43(d,j=1.2hz,1h),8.97(s,1h),8.69
(s,1h),8.57(d,j=7.6hz,1h),8.26(d,j=8.0hz,2h),8.03(d,j=8.0hz,2h),7.76
–
7.70(m,2h),7.37
–
7.32(m,1h),4.44(t,j=7.2hz,2h),1.86
–
1.78(m,2h),1.42
–
1.32(m,2h),0.92(t,j=7.2hz,3h).
13
c nmr(100mhz,dmso
‑
d6)δ145.47,137.12,134.71,134.08,131.84,131.70,131.51,130.55(q,j=32.1hz),127.46,126.85(q,j=3.8hz),124.42(q,j=270.6hz),124.12,120.50,120.00,112.10,110.47,109.82,100.97,43.42,30.39,20.24,14.22.hrms(esi)m/z calcd for c
24
h
21
f3n
3+
[m+h]
+
408.16821,found 408.16827.
[0089]
实施例13.
[0090]
实施例13的操作步骤与实施例1相同,其中,r为4
‑
甲氧基苯基,r9为丁基,得到的产物为6
‑
丁基
‑2‑
(4
‑
甲氧基)苯基
‑
6h
‑
咪唑并[1',2':1,6]吡啶并[3,4
‑
b]吲哚。
[0091]6‑
丁基
‑2‑
(4
‑
甲氧基)苯基
‑
6h
‑
咪唑并[1',2':1,6]吡啶并[3,4
‑
b]吲哚(l):黄色固体,收率:88.3%。1h nmr(400mhz,dmso
‑
d6)δ9.38(s,1h),8.68(s,1h),8.56(d,j=3.6hz,1h),8.50(dd,j=7.6,2.4hz,1h),7.94(dd,j=8.4,2.0hz,2h),7.71
–
7.63(m,2h),7.33
–
7.28(m,1h),7.17
–
7.13(m,2h),4.40(t,j=7.2hz,2h),3.84(s,3h),1.85
–
1.77(m,2h),1.43
–
1.32(m,2h),0.93(t,j=7.2hz,3h).
13
c nmr(100mhz,dmso
‑
d6)δ161.19,145.14,136.20,135.97,133.81,131.32,130.90,128.25,123.86,120.34,119.94,119.31,115.27,110.30,109.55,109.35,100.35,55.91,43.39,30.39,20.24,14.21.
[0092]
实施例14.
[0093]
实施例14的操作步骤与实施例1相同,其中,r为环丙基,r9为丁基,得到的产物为6
‑
丁基
‑2‑
环丙基
‑
6h
‑
咪唑并[1',2':1,6]吡啶并[3,4
‑
b]吲哚。
[0094]6‑
丁基
‑2‑
环丙基
‑
6h
‑
咪唑并[1',2':1,6]吡啶并[3,4
‑
b]吲哚(m):黄色固体,收率:83.2%。1h nmr(400mhz,dmso
‑
d6)δ9.35(d,j=1.2hz,1h),8.54(s,1h),8.49(d,j=8.0hz,1h),8.16(s,1h),7.7365(m,2h),7.33
–
7.28(m,1h),4.38(t,j=7.2hz,2h),2.28(tt,j=8.4,5.2hz,1h),1.85
–
1.73(m,2h),1.40
–
1.30(m,2h),1.25
–
1.16(m,2h),1.07
–
1.01(m,2h),0.91(t,j=7.2hz,3h).
13
c nmr(100mhz,dmso
‑
d6)δ145.06,140.58,135.47,133.63,131.22,130.54,123.80,120.28,119.98,110.29,109.98,109.34,100.23,43.37,30.35,20.21,14.19,9.00,7.10.hrms(esi)m/z calcd for c
20
h
22
n
3+
[m+h]
+
304.18082,found 304.18069.
[0095]
实施例15.
[0096]
实施例15的操作步骤与实施例1相同,其中,r为苯基,r9为苄基,得到的产物为6
‑
苄基
‑2‑
苯基
‑
6h
‑
咪唑并[1',2':1,6]吡啶并[3,4
‑
b]吲哚。
[0097]6‑
苄基
‑2‑
苯基
‑
6h
‑
咪唑并[1',2':1,6]吡啶并[3,4
‑
b]吲哚(n):黄色固体,收率:90.7%。1h nmr(400mhz,dmso
‑
d6)δ9.40(d,j=1.1hz,1h),8.86(s,1h),8.72(s,1h),8.61(d,j=7.6hz,1h),8.04
–
8.01(m,2h),7.75
–
7.71(m,2h),7.67
–
7.62(m,2h),7.58(d,j=7.2hz,1h),7.40
–
7.35(m,1h),7.33
–
7.27(m,5h),5.73(s,2h).
13
c nmr(100mhz,dmso
‑
d6)δ145.41,136.92,136.14,134.35,131.74,131.63,130.82,129.97,129.25,129.20,128.15,127.40,127.35,126.76,124.16,120.88,120.27,110.93,110.73,109.89,101.04,46.79.hrms(esi)m/z calcd for c
26
h
20
n
3+
[m+h]
+
374.16517,found 374.16525.
[0098]
实施例16.
[0099]
实施例16的操作步骤与实施例1相同,其中,r为4
‑
三氟甲基苯基,r9为苄基,得到
的产物为6
‑
苄基
‑2‑
(4
‑
三氟甲基)苯基
‑
6h
‑
咪唑并[1',2':1,6]吡啶并[3,4
‑
b]吲哚。
[0100]6‑
苄基
‑2‑
(4
‑
三氟甲基)苯基
‑
6h
‑
咪唑并[1',2':1,6]吡啶并[3,4
‑
b]吲哚(o):黄色固体,收率:89.5%。1h nmr(400mhz,dmso
‑
d6)δ9.41(d,j=1.2hz,1h),9.00(s,1h),8.73(s,1h),8.60(d,j=8.0hz,1h),8.25(d,j=8.0hz,2h),8.02(d,j=8.0hz,2h),7.75
–
7.67(m,3h),7.39
–
7.34(m,1h),7.33
–
7.28(m,5h),5.73(s,2h).
13
c nmr(100mhz,dmso
‑
d6)δ145.48,136.92,134.39,131.89,131.80,130.53(q,j=31.6hz),129.25,129.20,128.15,127.44,127.41,127.34,126.90(q,j=4.0hz),124.43(q,j=270.8hz),124.18,120.88,120.30,112.29,110.71,109.86,101.40,46.78.hrms(esi)m/z calcd for c
27
h
19
f3n
3+
[m+h]
+
442.15256,found 442.15277.
[0101]
实施例17.
[0102]
实施例17的操作步骤与实施例1相同,其中,r为4
‑
氟苯基,r9为苄基,得到的产物为6
‑
苄基
‑2‑
(4
‑
氟苯基)
‑
6h
‑
咪唑并[1',2':1,6]吡啶并[3,4
‑
b]吲哚。
[0103]6‑
苄基
‑2‑
(4
‑
氟苯基)
‑
6h
‑
咪唑并[1',2':1,6]吡啶并[3,4
‑
b]吲哚(p):黄色固体,收率:88.2%。1h nmr(400mhz,dmso
‑
d6)δ9.35(s,1h),8.79(s,1h),8.67(s,1h),8.55(d,j=8.0hz,1h),8.08(dd,j=8.4,5.2hz,2h),7.72
–
7.63(m,2h),7.48(t,j=8.4hz,2h),7.36
–
7.25(m,6h),5.71(s,2h).
13
c nmr(100mhz,dmso
‑
d6)δ162.10(d,j=246.0hz),145.27,137.94,137.03,134.13,131.30,130.78,129.23,129.06(d,j=8.7hz),128.10,127.39,123.83,120.65,120.53,117.02(d,j=22.0hz),110.50,109.25,101.87,46.72.hrms(esi)m/z calcd for c
26
h
19
fn
3+
[m+h]
+
392.15575,found 392.15594.
[0104]
实施例18.
[0105]
实施例18的操作步骤与实施例1相同,其中,r为环丙基,r9为丁基,得到的产物为6
‑
丁基
‑2‑
环丙基
‑
6h
‑
咪唑并[1',2':1,6]吡啶并[3,4
‑
b]吲哚。
[0106]6‑
丁基
‑2‑
环丙基
‑
6h
‑
咪唑并[1',2':1,6]吡啶并[3,4
‑
b]吲哚(q):灰白色固体,收率:82.6%。1h nmr(400mhz,dmso
‑
d6)δ9.30(s,1h),8.60(s,1h),8.53(d,j=8.0hz,1h),8.15(s,1h),7.74
–
7.68(m,2h),7.33
–
7.26(m,6h),5.68(s,2h),2.25(tt,j=8.4,5.2hz,1h),1.19
–
1.15(m,2h),1.03
–
0.98(m,2h).
13
c nmr(100mhz,dmso
‑
d6)δ145.12,140.74,136.90,135.72,133.98,131.40,130.73,129.21,128.11,127.38,123.93,120.72,120.27,110.59,110.14,109.46,100.60,46.74,8.97,7.07.hrms(esi)m/z calcd for c
23
h
20
n
3+
[m+h]
+
338.16517,found 338.16534.
[0107]
实施例19.
[0108]
实施例19的操作步骤与实施例1相同,其中,r为4
‑
甲氧基苯基,r9为苄基,得到的产物为6
‑
苄基
‑2‑
(4
‑
甲氧基)苯基
‑
6h
‑
咪唑并[1',2':1,6]吡啶并[3,4
‑
b]吲哚。
[0109]6‑
苄基
‑2‑
(4
‑
甲氧基)苯基
‑
6h
‑
咪唑并[1',2':1,6]吡啶并[3,4
‑
b]吲哚(r):黄色固体,收率:94.5%。1h nmr(400mhz,dmso
‑
d6)δ9.35(s,1h),8.73(s,1h),8.67(s,1h),8.58(d,j=7.6hz,1h),7.96(d,j=8.4hz,2h),7.75
–
7.68(m,2h),7.39
–
7.25(m,6h),7.20(d,j=8.4hz,2h),5.72(s,2h),3.87(s,3h).
13
c nmr(100mhz,dmso
‑
d6)δ161.27,145.29,136.95,136.82,131.54,131.10,129.25,128.34,128.14,127.39,124.02,120.81,120.36,115.40,110.67,109.71,109.65,101.00,55.97,46.77.hrms(esi)m/z calcd for c
27
h
22
n3o
+
[m+h]
+
404.17574,found 404.17593.
[0110]
实施例20.
[0111]
实施例20的操作步骤与实施例1相同,其中,r为苯基,r9为4
‑
氟苄基,得到的产物为6
‑
(4
‑
氟苄基)
‑2‑
苯基
‑
6h
‑
咪唑并[1',2':1,6]吡啶并[3,4
‑
b]吲哚。
[0112]6‑
(4
‑
氟苄基)
‑2‑
苯基
‑
6h
‑
咪唑并[1',2':1,6]吡啶并[3,4
‑
b]吲哚(s):灰色固体,收率:81.1%。1h nmr(400mhz,dmso
‑
d6)δ9.42(d,j=1.2hz,1h),8.86(s,1h),8.71(s,1h),8.60(d,j=8.0hz,1h),8.05
–
8.02(m,2h),7.78
–
7.69(m,2h),7.67
–
7.62(m,2h),7.59
–
7.54(m,1h),7.39
–
7.34(m,3h),7.19
–
7.13(m,2h),5.72(s,2h).
13
c nmr(100mhz,dmso
‑
d6)δ161.6(d,j=241.9hz),145.25,136.96,136.24,134.21,133.15(d,j=3hz),131.71,131.58,130.79,129.95,129.62(d,j=8.2hz),127.28,126.76,124.15,120.91,120.32,116.16(d,j=21.3hz),110.90,110.67,109.88,101.10,46.09.hrms(esi)m/z calcd for c
26
h
19
fn
3+
[m+h]
+
392.15575,found 392.15585.
[0113]
实施例21.
[0114]
实施例21的操作步骤与实施例1相同,其中,r为4
‑
氟苯基,r9为4
‑
氟苄基,得到的产物为6
‑
(4
‑
氟苄基)
‑2‑
(4
‑
氟苯基)
‑
6h
‑
咪唑并[1',2':1,6]吡啶并[3,4
‑
b]吲哚。
[0115]6‑
(4
‑
氟苄基)
‑2‑
(4
‑
氟苯基)
‑
6h
‑
咪唑并[1',2':1,6]吡啶并[3,4
‑
b]吲哚(t):黄色固体,收率:83.2%。1h nmr(400mhz,dmso
‑
d6)δ9.43(d,j=1.2hz,1h),8.83(s,1h),8.70(s,1h),8.59(d,j=8.0hz,1h),8.13
–
8.05(m,2h),7.77
–
7.68(m,2h),7.55
–
7.47(m,2h),7.39
–
7.34(m,3h),7.20
–
7.13(m,2h),5.72(s,2h).
13
c nmr(100mhz,dmso
‑
d6)δ162.31(d,j=246.7hz),160.85(d,j=241.9hz),145.23,136.92,135.42,134.21,133.15(d,j=3.0hz),131.70,131.55,129.62(d,j=8.2hz),129.28(d,j=8.7hz),124.14,123.97(d,j=3.3hz),120.90,120.31,117.18(d,j=22.1hz),116.15(d,j=21.3hz),115.94,110.81,110.66,109.88,101.10,46.08.hrms(esi)m/z calcd for c
26
h
18
f2n
3+
[m+h]
+
410.14633,found 410.14645.
[0116]
实施例22.
[0117]
实施例22的操作步骤与实施例1相同,其中,r为4
‑
甲氧基苯基,r9为4
‑
氟苄基,得到的产物为6
‑
(4
‑
氟苄基)
‑2‑
(4
‑
甲氧基)苯基
‑
6h
‑
咪唑并[1',2':1,6]吡啶并[3,4
‑
b]吲哚。
[0118]6‑
(4
‑
氟苄基)
‑2‑
(4
‑
甲氧基)苯基
‑
6h
‑
咪唑并[1',2':1,6]吡啶并[3,4
‑
b]吲哚(u):黄色固体,收率:85.7%。1h nmr(400mhz,dmso
‑
d6)δ9.36(d,j=0.8hz,1h),8.73(s,1h),8.67(s,1h),8.58(d,j=7.6hz,1h),7.99
–
7.94(m,2h),7.77
–
7.69(m,2h),7.39
–
7.33(m,3h),7.22
–
7.13(m,4h),5.71(s,2h),3.87(s,3h).
13
c nmr(100mhz,dmso
‑
d6)δ162.06(d,j=241.9hz),161.29,145.16,136.78,134.17,133.16(d,j=3.0hz),131.58,131.16,129.55(d,j=8.2hz),128.36,124.05,120.87,120.39,116.05(d,j=21.4hz),115.41,110.65,109.73,101.00,55.98,46.06.hrms(esi)m/z calcd for c
27
h
21
fn3o
+
[m+h]
+
422.16632,found 422.16647.
[0119]
实施例23.
[0120]
实施例23的操作步骤与实施例1相同,其中,r为4
‑
三氟甲基苯基,r9为4
‑
氟苄基,得到的产物为6
‑
(4
‑
氟苄基)
‑2‑
(4
‑
三氟甲基)苯基
‑
6h
‑
咪唑并[1',2':1,6]吡啶并[3,4
‑
b]吲哚。
[0121]6‑
(4
‑
氟苄基)
‑2‑
(4
‑
三氟甲基)苯基
‑
6h
‑
咪唑并[1',2':1,6]吡啶并[3,4
‑
b]吲哚(v):黄色固体,收率:81.5%。1h nmr(400mhz,dmso
‑
d6)δ9.42(s,1h),8.99(s,1h),8.73(s,1h),8.60(d,j=7.6hz,1h),8.26(d,j=8.4hz,2h),8.03(d,j=8.4hz,2h),7.77
–
7.70(m,2h),7.40
–
7.33(m,3h),7.19
–
7.13(m,2h),5.72(s,2h).
13
c nmr(100mhz,dmso
‑
d6)δ162.06(d,j=242.1hz),145.34,137.55,134.28,133.15(d,j=3.2hz),131.88,131.80,131.74,130.20(q,j=31.9hz),129.53(d,j=8.2hz),127.44,124.43(q,j=270.8hz),124.19,120.92,120.35,116.06(d,j=21.4hz),112.30,110.68,109.87,101.47,46.08.hrms(esi)m/z calcd for c
27
h
18
f4n
3+
[m+h]
+
460.14314,found460.14334.
[0122]
实施例24.
[0123]
实施例24的操作步骤与实施例1相同,其中,r为环丙基,r9为4
‑
氟苄基,得到的产物为6
‑
(4
‑
氟苄基)
‑2‑
环丙基
‑
6h
‑
咪唑并[1',2':1,6]吡啶并[3,4
‑
b]吲哚。
[0124]6‑
(4
‑
氟苄基)
‑2‑
环丙基
‑
6h
‑
咪唑并[1',2':1,6]吡啶并[3,4
‑
b]吲哚(w):黄色固体,收率:87.2%。1h nmr(400mhz,dmso
‑
d6)δ9.33(d,j=1.2hz,1h),8.60(s,1h),8.54(d,j=7.6hz,1h),8.16(s,1h),7.76
–
7.66(m,2h),7.37
–
7.31(m,3h),7.18
–
7.10(m,2h),5.67(s,2h),2.26(tt,j=8.4,5.2hz,1h),1.22
–
1.15(m,2h),1.04
–
0.97(m,2h).
13
c nmr(100mhz,dmso
‑
d6)δ163.24(d,j=242.0hz),145.00,140.76,135.75,133.88,133.13(d,j=3.0hz),131.43,130.78,129.59(d,j=8.1hz),123.96,120.79,120.32,116.12(d,j=21.3hz),110.58,110.16,109.49,100.63,46.04,8.97,7.06.hrms(esi)m/z calcd for c
23
h
19
fn
3+
[m+h]
+
356.15575,found 356.15582.
[0125]
实施例2
‑
24制备的产物的化学结构式具体见表1。
[0126]
表1
[0127]
[0128][0129]
实施例25.
[0130]
抗肿瘤活性研究
[0131]
以a549(肺癌细胞),bgc
‑
823(胃癌细胞),ct
‑
26(结肠癌细胞),bel
‑
7402(肝癌细胞)和mcf
‑
7(乳腺癌细胞)为对象,采用mtt法测试了目标化合物3a
‑
3x对肿瘤细胞株的抑制活性。分别将生长状态良好、处于对数生长期的细胞株以1
×
104个
·
ml
‑1的浓度接种于96孔板,置于37℃的co2培养箱中培养24h,弃旧液,换新鲜培养液,加入灭菌处理的待测化合物,继续培养48h后,弃去培养液,每孔加20μl含5mg
·
ml
‑1mtt的rpmi1640培养液,继续培养4h,小心除去上清后,每孔加入100μl的dmso,振荡约10min溶解沉淀,随后用酶标仪检测od值,波长490nm,按作图法求出每个样品的ic
50
值。具体结果见表2。
[0132]
表2目标化合物的体外抗肿瘤活性
[0133]
[0134][0135]
由表2可知,本发明的β
‑
咔啉杂合咪唑类化合物,具有较好的抗肿瘤活性,可应用于抗肿瘤药物中
[0136]
以上所述,仅是本发明实施例的较佳实施例而已,并非对本发明实施例作任何形式上的限制,依据本发明实施例的技术实质对以上实施例所作的任何简单修改、等同变化与修饰,均仍属于本发明实施例技术方案的范围内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1