一种牛膝多糖、其制备工艺和用途
1.本发明属于多糖技术领域,具体涉及一种牛膝多糖、其制备工艺及在制备抗肝纤维化药物中的用途。
背景技术:
2.肝纤维化是指由各种致病因子诱发肝内结缔组织异常增生,导致肝内弥漫性细胞外基质过度沉淀的病理过程。其发病机制为当肝脏遭到各种致病因子侵袭后,诱发肝脏损伤与炎症反应,肝组织免疫系统被激活,进行组织修复,当这种组织修复过程过度及失控时,肝组织内细胞外基质过度增生与异常沉淀就会导致肝脏结构和肝功能异常改变。它不是一种独立的疾病,是大多数慢性肝病的共同过程及主要病因之一,也是进一步向肝硬化、肝癌等疾病发展所经历的病理阶段。因此,找到一种可有效治疗肝纤维化的药物具有重要的临床意义。
3.肝纤维化是由多种细胞因子和分子途径参与的复杂病理过程。所以,多糖因其具有多环节、多途径、多层次、多靶点的作用特点以及能够整体调节器官组织病理过程的优点,在临床抗肝纤维化的治疗方面具有非常突出的优势,应用前景广阔。
4.牛膝,中药名。又名百倍、鸡胶骨,为苋科牛膝achyranthes bidentata bl.的干燥根,是我国传统中药,归肝、肾经,具有逐瘀通经、补肝肾、强筋骨、利尿通淋等功效。目前对于牛膝的化学成分研究,主要集中在牛膝苷等小分子化合物。牛膝多糖的药理活性集中在免疫及骨形成方向,而鲜有对于牛膝多糖用于肝纤维化治疗药物方面的研究。
技术实现要素:
5.本发明的一个方面提供一种牛膝多糖,所述牛膝多糖的平均分子量为1000-20000da。
6.在所述牛膝多糖中,含有果糖与葡萄糖的摩尔比为5~10:1。
7.在所述牛膝多糖中,连接方式包括α-d-glcp-(1
→
、β-d-fruf-(2
→
、
→
1,6)-β-d-fruf-(2
→
、
→
1)-β-d-fruf-(2
→
和
→
2)-β-d-fruf-(6
→
。
8.本发明的另一个方面提供所述牛膝多糖的制备方法,所述方法包括:以干燥的牛膝根为原料,经沸水提取、浓缩、透析、醇沉得粗多糖后,进一步过离子交换柱层析得到牛膝多糖。
9.特别地,所述牛膝多糖的制备方法包括:
10.(1)干燥的牛膝根茎粉碎成粉末,经沸水提取、浓缩提取液并透析、乙醇沉淀多糖、收集沉淀物、冷冻干燥得到粗多糖;
11.(2)粗多糖在deae-sepharose快流柱上进一步分离纯化,依次用蒸馏水、0.05、0.1、0.2、0.4m nacl溶液逐步洗脱,收集0.2m nacl洗脱组分得纯化得到牛膝多糖。
12.特别地,上述步骤(1)如下进行:干燥的牛膝根茎粉碎成粉末,经沸水提取2h、浓缩提取液并透析3天、乙醇沉淀多糖、离心收集沉淀物、冷冻干燥得到粗多糖。
13.特别地,上述步骤(2)如下进行:取粗多糖,水溶解,离心,上清液通过deae-sepharose快流柱上进一步分离纯化,依次用蒸馏水、0.05、0.1、0.2、0.4m nacl溶液逐步洗脱,硫酸-苯酚检测,收取合并0.2m nacl洗脱液,浓缩,透析,冷冻干燥得牛膝多糖。
14.特别地,透析时透析袋的截留分子量为3500da。
15.本发明的又一方面提供所述牛膝多糖在制备用于治疗肝纤维化的药物中的用途。
16.其中所述多糖是通过抑制肝星状细胞激活、抑制细胞外基质的生成,从而起到抑制肝纤维化的功效。
17.因此,本发明的又一方面提供所述牛膝多糖在制备用于抑制肝星状细胞激活和/或抑制细胞外基质的生成的药物中的用途。
18.本发明通过以下附图和实施例作进一步阐述,但并不限制本发明的内容。
附图说明
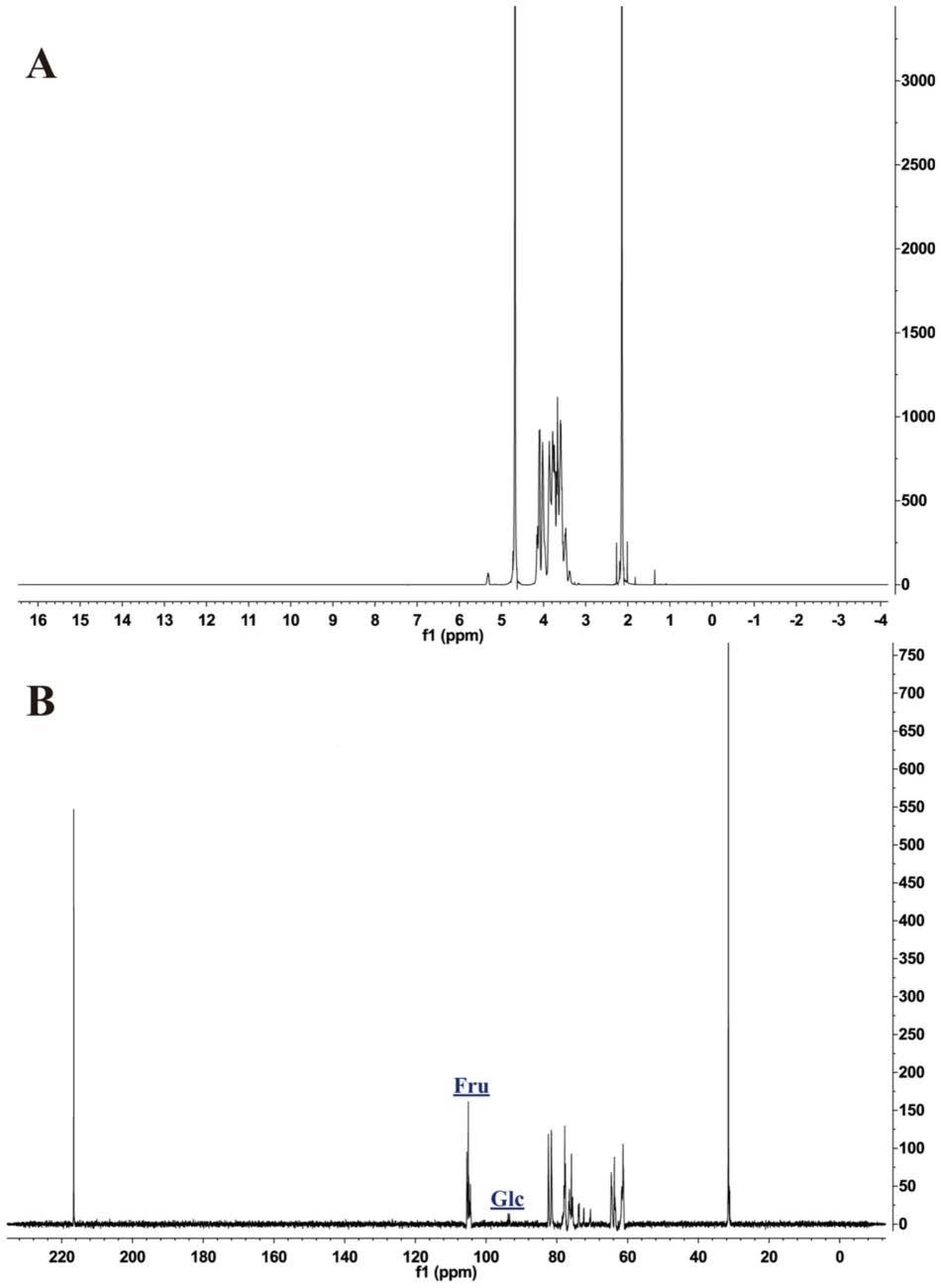
19.图1为实施例1制备的牛膝多糖abww的1h nmr谱图(a)和
13
c nmr谱图(b)。
20.图2显示实施例1制备的牛膝多糖abww在细胞水平上抑制肝星状细胞激活的作用;其中,a.abww浓度依赖的抑制肝星状细胞fibronectin、α-sma、col1a1的蛋白表达量。b-d.abww浓度依赖的抑制肝星状细胞fibronectin、α-sma、col1a1的mrna表达量。
21.图3显示实施例1制备的牛膝多糖abww在动物水平上改善四氯化碳诱导的肝纤维化作用;其中a.天狼星红染色结果提示abww抑制肝组织中胶原沉积;b.马松三色染色结果提示abww抑制肝组织中胶原沉积;c.western blot结果提示abww抑制肝脏中tgf-β1、α-sma蛋白表达量。
具体实施方式
22.实施例1:牛膝多糖abww的制备
23.a.牛膝粗多糖提取:
24.干燥的牛膝根茎粉碎成粉末。然后将粉末(5.0kg)浸入100l水中并用沸水提取2h。浓缩提取液并使用透析膜(mwco 3500da)在自来水中透析3天。加入乙醇(95%)沉淀多糖(乙醇:浓溶液=3:1)。通过离心收集沉淀物(rcf=14430g,10min)。沉淀经冷冻干燥得到粗多糖(264.2g,收率5.3%)。
25.b.多糖纯化:
26.上述粗多糖在deae-sepharose快流柱(5cm
×
50cm)上进一步分离。具体而言,将牛膝粗多糖(7.7g)溶解于100ml蒸馏水中,搅拌并离心。将上清液应用于deae-sepharose快速流动柱,并用蒸馏水、0.05、0.1、0.2、0.4m nacl溶液逐步洗脱。根据苯酚-硫酸法的洗脱曲线汇集洗脱液。收取合并0.2m nacl洗脱液,浓缩,透析,冷冻干燥得abww多糖866mg。
27.c.多糖结构鉴定:
28.1.采用高效凝胶渗透色谱法(hpgpc)测定分子质量
29.abww多糖的分子量和纯度采用hpgpc方法测定。具体而言,样品以流动相配制成1~2mg/ml的多糖溶液。采用两根多糖凝胶色谱柱串联,waters ultra hydrogel tm 500(排阻极限1
×
104~4
×
105da,7.8mm
×
300mm)和ultra hydrogelt m 2000(排阻极限5
×
104~10
×
106da,7.8mm
×
300mm),流速为0.5ml/min。配有g1362a示差检测器,g1314紫外检测器,
在线脱气装置等。以0.1m nano3为流动相,样品进样体积为20μl,紫外吸收波长为280nm,柱温40℃。示差和紫外检测器记录信号。在色谱柱分子量范围内,样品洗脱曲线出现了单一对称峰,则该多糖为均一组分。通过安捷伦工作站,配套色谱gpc软件计算abww多糖的相对平均分子量约为3000da。
30.2.采用hpaec-pad测定单糖组成
31.abww(5mg)在密封管中在120℃下用2m三氟乙酸(tfa,2ml)水解6小时。用甲醇共蒸馏法将多余的酸完全除去。然后将水解产物(1mg)溶解于纯水(1ml)中。采用高效阴离子交换色谱-脉冲安培检测法(hpaec-pad)对单糖进行鉴定。以7种单糖(葡萄糖、木糖、果糖、半乳糖、鼠李糖、甘露糖和阿拉伯糖)为标准。稀释样品通过0.45μm过滤器,并通过hpaec-pad系统(dionex-5500,dionex公司,加拿大)进行分析。用水和200mm naoh的混合物以92:8的体积比洗脱。
32.单糖组成分析结果显示,abww含有果糖与葡萄糖的摩尔比为5~10:1。
33.3.核磁测定:
34.对于nmr分析,30mg样品与d2o通过冷冻干燥共蒸发两次,然后溶解于0.5ml d2o中。在25℃下以丙酮为内标(δc=31.5,δh=2.29)测量1h nmr和
13
c nmr。在bruker avance iii核磁共振谱仪上记录了核磁共振谱。
35.实施例2:牛膝多糖abww抑制肝星状细胞激活活性
36.纤维化是细胞外基质(ecm),如i型和iii型胶原,沉积在disse空间。细胞外基质的沉积程度是肝纤维化中的重要评判标准,也是肝脏硬度增高的主要原因。肝星状细胞(hsc)激活是细胞外基质增多的主要原因之一。肝脏星状细胞占肝脏固有细胞总数的15%左右,占非实质细胞的30%左右。hsc存在于disse腔中,呈梭形或多边形,胞浆内有富含维生素a脂滴。在正常肝脏中,hsc处于静止状态,不表达α平滑肌肌动蛋白(α-sma),增殖活性低,合成胶原能力低,其主要功能是贮存视黄醛类。当肝脏受到炎症等损伤时,hsc被激活,其表型由静止型转变为活化型,肝星状细胞大量增殖与活化,逐渐失去维生素a脂滴,分化为肌成纤维细胞,大量分泌胶原、基质金属蛋白酶,进而发生修复反应,此时,因细胞外基质合成降解与沉积不平衡,导致以胶原为主的细胞外基质在肝内过度沉积。
37.人肝星状细胞(lx2),取自正常人体肝脏组织,具有典型的肝星状细胞生物学特征,是理想的肝纤维化体外细胞学实验模型。由于tgf-β1是参与肝星状细胞活化和胶原蛋白产生的主要刺激因子之一,采用tgf-β1体外激活hsc细胞模型,诱发α-sma蛋白表达,产生大量的细胞外基质(ecm)的沉积包含(fibronectin,collagen-α1),模拟细胞外基质在肝脏内的异常沉积等一系列反应。
38.处理lx2细胞,胰酶消化,离心(1000rpm,5min),重悬。根据实验要求接种6孔板。待细胞贴壁后,用无血清dmem高糖培养基对细胞进行饥饿处理24h。在无血清dmem高糖培养基中加入tgf-β1(终浓度10ng/ml),用此培养基稀释牛膝多糖至相应浓度。吸走饥饿细胞用的培养基,再将稀释好的化合物放入孔内。24h后,用pbs洗一次,加100μl1x loading收蛋白样品。用qpcr及western blot方法检测fibronectin、α-sma、col1a1,gapdh作为内参对照。
39.实验结果见图2的a-d。由图2可以看出,abww可以在100,300,600ug/ml中呈浓度依赖降低fibronectin、α-sma、col1a1的mrna及蛋白表达,即提示abww在细胞水平上可以抑制肝星状细胞的激活和细胞外基质的生成。
40.实施例3:牛膝多糖abww抑制四氯化碳诱导小鼠肝纤维化活性
41.实验采用雄性c57bl/6j小鼠,腹腔注射ccl4造模(10%ccl4的橄榄油(olive oil)溶液,2ml/kg,i.p,每周三次),9只同批次小鼠仅腹腔注射橄榄油作为正常对照组。实验在上海药物所实验动物中心进行,specific pathogen free(spf)条件下饲养,自由饮食,实验遵照中国科学院上海药物研究所实验动物使用与管理委员会规定进行。
42.小鼠随机分成四组,分别为正常对照组(vehicle control)、模型对照组(ccl4 model)、abww 100mg/kg组(ccl4+abww(100mg/kg))、abww 200mg/kg组(ccl4+abww(200mg/kg)),其中模型对照组及abww组均为给与腹腔注射10%ccl4,一周三次,共四周,诱导肝损伤,正常对照组给与腹腔注射同体积橄榄油作为对照,每周监测动物体重。给药结束后,安乐死小鼠,收集肝脏组织,一份于4%的多聚甲醛固定,另一份于-80℃保存肝组织。实验结束后对肝脏组织α-sma等蛋白水平的表达量以及肝脏组织病理切片进行检测。
43.ccl4诱导的肝纤维化模型实验中,经masson染色和天狼星红染色的结果见图3的a-b。由a可见,ccl4诱导小鼠肝损伤模型的肝脏细胞周围纤维化,胶原的沉积显著增加。由b可见,给予牛膝多糖abww(100mg/kg,200mg/kg)后明显降低ccl4诱导的肝脏中胶原沉积。肝组织western blot结果见图3的c。由c可见,abww(100mg/kg,200mg/kg)给药组均能显著降低α-sma及tgf-β1的蛋白表达。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1