一种含硒咪唑类化合物及其在制备抗菌药物中的应用
1.本发明涉及一种含硒的咪唑类化合物及其在制备抗菌药物中的应用。
背景技术:
2.硒是氧族元素中的一种人体必需微量元素,因其在适合的条件下可以以硒负离子、硒正离子和硒自由基三种形态来参与反应,形成硒
‑
卤键、硒
‑
碳键、硒
‑
氧键等,也可以催化(介导)氮
‑
碳键、氧
‑
碳键等的构建,在现代有机合成中具有重要的作用。它是各种具有免疫调节功能营养素中唯一可以直接抗病毒的元素,含有硒键的有机化合物已显示出了在抗炎症、抗溃疡、抗氧化性和抗癌等方面作用。咪唑用作医药原料,用于支气管哮喘治疗药、抗真菌药、抗霉剂、人造血浆、滴虫治疗药、低血糖治疗药、防斑疹剂等的制造。咪唑类和咪唑衍生物的大量开发合成已经证明了其对各种菌有不同的效应。(a)mokale等人以咪唑基取代的氯苯乙酮合成制备了一系列具有抗菌活性的咪唑衍生物,对白色念珠菌、黄曲霉和烟曲霉均具有良好的抗真菌活性。(b)xu等人通过硒分子取代硫原子制备了新的硒代苯并二氢吡喃
‑4‑
酮和2,3
‑
二氢
‑
4h
‑1‑
苯并硒啉
‑4‑
酮衍生物。结果表明硒原子的引入可以使抗白色念珠菌等真菌活性明显增强,这些结果对于寻找更好的含硒抗菌剂具有重要的指导意义。
3.[0004][0005]
咪唑是一种重要的精细化工原料,主要用于医药和农药的合成以及环氧树脂的固化剂。在医药中用于咪唑类抗真菌药物,是双氯苯咪唑,益康唑,酮康唑,克霉唑等药物的主要原料之一,还广泛地用于水果的防腐剂。硒也是一种具有潜在生物活性的元素,本发明在咪唑类化合物中引入有机硒基团,制备了一类新型的含硒咪唑化合物,经测试对金黄色葡萄球菌、大肠杆菌、芽孢杆菌和酵母菌具有良好的抗菌效果,是一种新型的含硒抗菌剂。
技术实现要素:
[0006]
本发明开发了一种新型含硒的咪唑类化合物的合成方法,该方法具有简便、产率高、相对绿色等优点。本发明在咪唑类化合物中引入有机硒基团,制备了一类新型的含硒咪唑化合物,经测试对金黄色葡萄球菌、大肠杆菌、芽孢杆菌和酵母菌具有良好的抗菌效果,是一种新型的含硒抗菌剂。
[0007]
为实现上述目的,本发明采用如下技术方案:
[0008]
本发明提供了式(ii)所示的含硒咪唑类化合物,
[0009][0010]
其中,r1为c
1~8
烷基、苯基、苄基或被c
1~4
烷基、c
1~4
烷氧基或氨基取代的苯基。
[0011]
优选地,r1为c
1~4
烷基、苯基、苄基或被甲基、甲氧基或氨基取代的苯基。
[0012]
本发明还提供一种上述式(ii)所示的含硒咪唑类化合物在制备抗菌药物中的应用。
[0013]
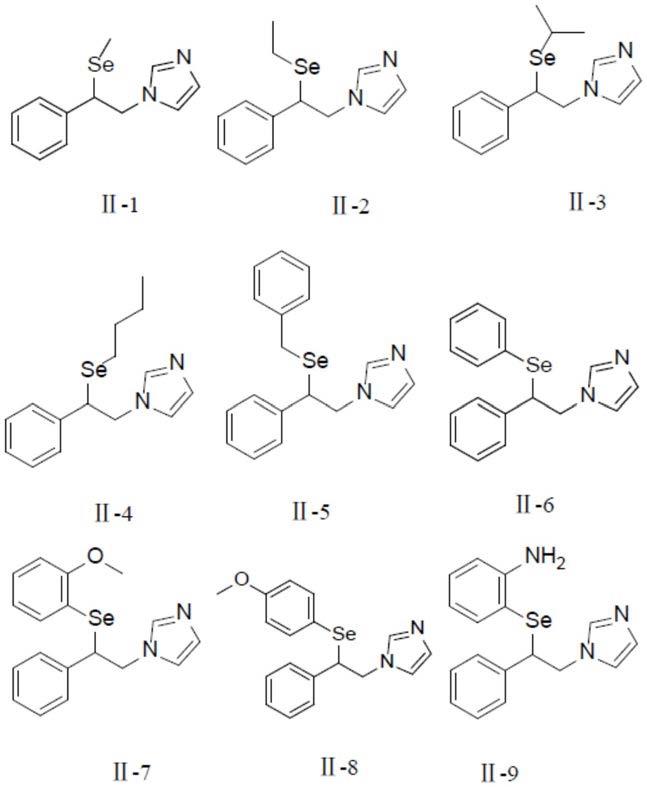
进一步优选地,所述式(ii)所示的含硒咪唑类化合物为下列之一:
[0014][0015]
进一步,所述菌为细菌或真菌,优选为酵母菌、金黄色葡萄球菌、大肠杆菌或芽孢杆菌;尤其是对真菌如酵母菌的抑制效果特别好。
[0016]
所述菌为细菌时,本发明尤其推荐所述式(ii)所示的含硒咪唑类化合物为化合物
ⅱ‑
1、
ⅱ‑
3或
ⅱ‑
6。所述菌为真菌时,尤其推荐化合物
ⅱ‑
5、
ⅱ‑
7、
ⅱ‑
9或
ⅱ‑
10。
[0017]
具体地,上述化合物按如下方法制备:
[0018]
(1)将咪唑溶在dmf中,待完全溶解后,再将化合物a缓慢加入,随后往反应液中加入水和甲苯的混合液,并在冰浴下搅拌反应。反应结束后,对反应液进行抽滤,用甲苯对滤饼进行重结晶,得到白色目标化合物b;
[0019]
(2)在冰浴条件下将nabh4缓慢加入到化合物b的乙醇溶液中,保持反应液温度不高于室温,混合物在室温下搅拌12小时至反应结束,然后向混合物中加入适量的冰水,通过过滤和乙醇重结晶获得白色化合物c;
[0020]
(3)将化合物c加入二氯亚砜溶液中。将混合物在室温下搅拌17小时,反应结束后将溶液加入适量的冰水混合物,并用氢氧化钾将混合物的ph值调整为中性。最后通过过滤和etoh重结晶获得白色固体d;
[0021]
(4)将白色固体d与化合物(i)溶于乙醇中,再将nabh4缓慢加入,放出气体后再反应4
‑
5h。将反应液过滤,利用柱层析进行分纯处理得到式(ⅱ)所示产物。
[0022]
所述咪唑的用量为化合物a物质的量的100%~1000%,优选500%;所述nabh4的
用量为化合物b物质的量的100%~500%,优选300%;所述二氯亚砜的用量为化合物c物质的量的100%~800%,优选500%;所述对称二硒醚的用量为化合物d物质的量的50%~200%,优选60%;所述的nabh4用量为化合物d物质的量的100%~500%,优选200%;
[0023][0024]
式(ⅰ)、(ⅱ)中,r1为c
1~4
的烷基、苯基、苄基、2
‑
苯甲醚基、4
‑
苯甲醚基、2
‑
苯氨基、2
‑
甲苯基;
[0025]
优选地,所述式(i)所示化合物为下列之一:
[0026][0027][0028]
进一步,步骤(1)中所述dmf体积用量以所示化合物a的物质的量计为0.25ml/mmol;
[0029]
进一步,步骤(1)中所述水体积用量以所示化合物a的物质的量计为2.5ml/mmol;
[0030]
进一步,步骤(1)中所述甲苯体积用量以所示化合物a的物质的量计为0.5ml/mmol;
[0031]
进一步,步骤(2)中所述乙醇体积用量以所示化合物b的物质的量计为1000ml/
mmol;
[0032]
进一步,步骤(4)中所述乙醇体积用量以所示化合物d的物质的量计为1ml/mmol。
[0033]
本发明的反应进程可采用常规方法进行监测,例如用tlc监测原料来判断反应结束时间点;反应时间通常在1~4h。
[0034]
与现有技术相比,本发明的有益效果在于:本发明在咪唑类化合物中引入有机硒基团,制备了一类新的含硒咪唑化合物,经测试对金黄色葡萄球菌、大肠杆菌、芽孢杆菌和酵母菌具有良好的抗菌效果,是一种新型的含硒抗菌剂。
附图说明
[0035]
图1~3分别为化合物
ⅱ‑
1的1h谱图、
13
c谱图和ms图;
[0036]
图4~6分别为化合物
ⅱ‑
2的1h谱图、
13
c谱图和ms图;
[0037]
图7~9分别为化合物
ⅱ‑
3的1h谱图、
13
c谱图和ms图;
[0038]
图10~12分别为化合物
ⅱ‑
4的1h谱图、
13
c谱图和ms图;
[0039]
图13~15分别为化合物
ⅱ‑
5的1h谱图、
13
c谱图和ms图;
[0040]
图16~18分别为化合物
ⅱ‑
6的1h谱图、
13
c谱图和ms图;
[0041]
图19、20分别为化合物
ⅱ‑
7的1h谱图和
13
c谱图;
[0042]
图21~23分别为化合物
ⅱ‑
8的1h谱图、
13
c谱图和ms图;
[0043]
图24、25分别为化合物
ⅱ‑
9的1h谱图和
13
c谱图;
[0044]
图26、27分别为化合物
ⅱ‑
9的1h谱图和
13
c谱图;
[0045]
图28为化合物d的质谱图。
具体实施方式
[0046]
下面结合具体实施例对本发明进行进一步描述,但本发明的保护范围并不仅限于此。
[0047]
本发明中,克霉唑(clotrimazole,cas:23593
‑
75
‑
1)和氨苄西林(ampicillin,cas:69
‑
53
‑
4)购于萨恩化学技术(上海)有限公司;金黄色葡萄球菌、大肠杆菌、芽孢杆菌和酵母菌均来自于浙江工业大学生物工程学院。
[0048]
本发明中化合物d按照文献xu h,su x,guo m b,et al.design,synthesis,and biological evaluation of novel miconazole analogues containing selenium as potent antifungal agents[j].european journal of medicinal chemistry,2020,198:112360.中方法合成,区别仅在于用苯替代卤代苯,质谱验证获得化合物d,质谱见图28。
[0049]
实施例1:含硒的咪唑化合物ii
‑
1的制备
[0050][0051]
在氮气气氛下将207mg化合物d(1.0mmol)用1.0ml无水乙醇溶解,备用。向反应瓶中加入二甲基二硒醚(
ⅰ‑
1)113mg(0.6mmol)和1.0ml无水乙醇,室温下开搅拌,再称取硼氢
化钠76mg(2mmol)加入反应瓶中,并于60℃条件下反应0.5h,用注射器将已配好的化合物d的无水乙醇溶液加入反应中,60℃条件下继续反应3.0h,反应结束后,过滤,滤饼用2.0ml二氯甲烷洗涤,合并滤液,归一法gc
‑
ms检测收率96%,滤液用旋转蒸发仪除去有机溶剂后,残余物通过柱层析进一步分离提纯,洗脱剂为乙酸乙酯:石油醚=3:1,收集含目标产物的洗脱液,蒸去洗脱液,得到化合物ii
‑
1 233mg,分离产率88%,gc
‑
ms检测纯度98.2%。化合物式ii
‑
1的结构表征如下:
[0052]1h nmr(500mhz,cdcl3)δ7.32
‑
7.28(m,3h),7.26
‑
7.19(m,3h),6.95(s,1h),6.75(s,1h),4.42(d,j=7.6hz,2h),4.14(t,j=7.5hz,1h),1.83(s,3h);
13
c nmr(126mhz,cdcl3)δ139.08,137.24,129.28,128.90,127.90,127.69,118.97,52.43,44.63,5.03;gc
‑
ms(ei):m/z 266.0[m
+
].
[0053]
实施例2:含硒的咪唑化合物ii
‑
2的制备
[0054][0055]
在氮气气氛下将207mg化合物d(1.0mmol)用1.0ml无水乙醇溶解,备用。向反应瓶中加入二乙基二硒醚(
ⅰ‑
2)130mg(0.6mmol)和1.0ml无水乙醇,室温下开搅拌,再称取硼氢化钠76mg(2mmol)加入反应瓶中,并于60℃条件下反应0.5h,用注射器将已配好的化合物d的无水乙醇溶液加入反应中,60℃条件下继续反应3.0h,反应结束后,过滤,滤饼用2.0ml二氯甲烷洗涤,合并滤液,归一法gc
‑
ms检测收率92%,滤液用旋转蒸发仪除去有机溶剂后,残余物通过柱层析进一步分离提纯,洗脱剂为乙酸乙酯:石油醚=3:1,收集含目标产物的洗脱液,蒸去洗脱液,得到化合物ii
‑
2 232mg,分离产率83%,gc
‑
ms检测纯度97.4%。化合物式ii
‑
2的结构表征如下:
[0056]1h nmr(500mhz,cdcl3)δ7.42
‑
7.34(m,5h),7.15(s,1h),6.95(d,j=1.1hz,1h),6.73(dd,j=3.0,1.8hz,1h),4.42(d,j=7.6hz,2h),4.23(t,j=7.6hz,1h),2.41(qd,j=7.5,1.9hz,2h),1.30(t,j=7.5hz,3h);
13
c nmr(126mhz,cdcl3)δ139.48,134.39,128.91,128.04,127.74,126.16,118.91,52.85,43.41,18.66,15.40;gc
‑
ms(ei):m/z 280.0[m
+
].
[0057]
实施例3:含硒的咪唑化合物ii
‑
3的制备
[0058][0059]
在氮气气氛下将207mg化合物d(1.0mmol)用1.0ml无水乙醇溶解,备用。向反应瓶中加入二异丙基二硒醚
ⅰ‑
3 146mg(0.6mmol)和1.0ml无水乙醇,室温下开搅拌,再称取硼氢化钠76mg(2mmol)加入反应瓶中,并于60℃条件下反应0.5h,用注射器将已配好的化合物d的无水乙醇溶液加入反应中,60℃条件下继续反应3.0h,反应结束后,过滤,滤饼用2.0ml二
氯甲烷洗涤,合并滤液,归一法gc
‑
ms检测收率97%,滤液用旋转蒸发仪除去有机溶剂后,残余物通过柱层析进一步分离提纯,洗脱剂为乙酸乙酯:石油醚=3:1,收集含目标产物的洗脱液,蒸去洗脱液,得到化合物ii
‑
3 255mg,分离产率87%,gc
‑
ms检测纯度98.5%。化合物式ii
‑
3的结构表征如下:
[0060]1h nmr(500mhz,cdcl3)δ7.24
‑
7.14(m,6h),6.87(s,1h),6.66(s,1h),4.39
‑
4.26(m,2h),4.17(dd,j=8.4,6.6hz,1h),2.78(p,j=6.8hz,1h),1.28(d,j=6.8hz,3h),1.24(d,j=6.9hz,3h);
13
c nmr(126mhz,cdcl3)δ139.89,129.06,128.86,128.82,127.73,127.70,126.13,53.05,43.40,30.94,24.52,24.19;gc
‑
ms(ei):m/z 294.1[m
+
]
[0061]
实施例4:含硒的咪唑化合物ii
‑
4的制备
[0062][0063]
在氮气气氛下将207mg化合物d(1.0mmol)用1.0ml无水乙醇溶解,备用。向反应瓶中加入二丁基二硒醚
ⅰ‑
4 163mg(0.6mmol)和1.0ml无水乙醇,室温下开搅拌,再称取硼氢化钠76mg(2mmol)加入反应瓶中,并于60℃条件下反应0.5h,用注射器将已配好的化合物d的无水乙醇溶液加入反应中,60℃条件下继续反应3.0h,反应结束后,过滤,滤饼用2.0ml二氯甲烷洗涤,合并滤液,归一法gc
‑
ms检测收率96%,滤液用旋转蒸发仪除去有机溶剂后,残余物通过柱层析进一步分离提纯,洗脱剂为乙酸乙酯:石油醚=3:1,收集含目标产物的洗脱液,蒸去洗脱液,得到化合物ii
‑
4 267mg,分离产率87%,gc
‑
ms检测纯度98.0%。化合物式ii
‑
4的结构表征如下:
[0064]1h nmr(500mhz,cdcl3)δ7.24
‑
7.13(m,6h),6.88(s,1h),6.67(s,1h),4.34(d,j=7.5hz,2h),4.14(t,j=7.5hz,1h),2.33(t,j=7.5hz,2h),1.46(p,j=7.3hz,2h),1.24(qd,j=7.3,1.8hz,2h),0.77(t,j=7.4hz,3h);
13
c nmr(126mhz,cdcl3)δ139.54,137.18,129.06,128.78,127.72,127.70,118.96,52.71,43.54,32.18,24.80,22.83,13.47;gc
‑
ms(ei):m/z 308.1[m
+
].
[0065]
实施例5:含硒的咪唑化合物ii
‑
5的制备
[0066][0067]
在氮气气氛下将207mg化合物d(1.0mmol)用1.0ml无水乙醇溶解,备用。向反应瓶中加入二苄基二硒醚
ⅰ‑
5 204mg(0.6mmol)和1.0ml无水乙醇,室温下开搅拌,再称取硼氢化
钠76mg(2mmol)加入反应瓶中,并于60℃条件下反应0.5h,用注射器将已配好的化合物d的无水乙醇溶液加入反应中,60℃条件下继续反应3.0h,反应结束后,过滤,滤饼用2.0ml二氯甲烷洗涤,合并滤液,归一法gc
‑
ms检测收率93%,滤液用旋转蒸发仪除去有机溶剂后,残余物通过柱层析进一步分离提纯,洗脱剂为乙酸乙酯:石油醚=3:1,收集含目标产物的洗脱液,蒸去洗脱液,得到化合物ii
‑
5 290mg,分离产率85%,gc
‑
ms检测纯度97.7%。
[0068]1h nmr(500mhz,cdcl3)δ7.30(d,j=8.5hz,4h),7.23(dd,j=12.6,7.2hz,4h),7.17
‑
7.11(m,3h),6.91(s,1h),6.59(s,1h),4.33(dd,j=14.2,9.0hz,1h),4.24(dd,j=14.2,6.1hz,1h),3.99(dd,j=9.1,6.1hz,1h),3.65(s,2h);
13
c nmr(126mhz,cdcl3)δ139.25,138.23,137.17,129.03,128.95,128.76,128.66,127.92,127.78,127.15,118.99,52.64,43.87,28.69;gc
‑
ms(ei):m/z 342.1[m
+
].
[0069]
实施例6:含硒的咪唑化合物ii
‑
6的制备
[0070][0071]
在氮气气氛下将207mg化合物d(1.0mmol)用1.0ml无水乙醇溶解,备用。向反应瓶中加入二苯基二硒醚
ⅰ‑
6 187mg(0.6mmol)和1.0ml无水乙醇,室温下开搅拌,再称取硼氢化钠76mg(2mmol)加入反应瓶中,并于60℃条件下反应0.5h,用注射器将已配好的化合物d的无水乙醇溶液加入反应中,60℃条件下继续反应3.0h,反应结束后,过滤,滤饼用2.0ml二氯甲烷洗涤,合并滤液,归一法gc
‑
ms检测收率82%,滤液用旋转蒸发仪除去有机溶剂后,残余物通过柱层析进一步分离提纯,洗脱剂为乙酸乙酯:石油醚=3:1,收集含目标产物的洗脱液,蒸去洗脱液,得到化合物ii
‑
6 242mg,分离产率74%,gc
‑
ms检测纯度97.0%。化合物式ii
‑
6的结构表征如下:
[0072]1h nmr(500mhz,cdcl3)δ7.47
‑
7.40(m,2h),7.26
‑
7.05(m,9h),6.84(s,1h),6.54(s,1h),4.42
‑
4.34(m,2h),4.29(td,j=11.0,8.5hz,1h);
13
c nmr(126mhz,cdcl3)δ138.55,137.14,135.25,129.33,129.02,128.84,128.51,128.43,127.99,127.69,118.91,52.02,47.99;gc
‑
ms(ei):m/z 328.0[m
+
].
[0073]
实施例7:含硒的咪唑化合物ii
‑
7的制备
[0074][0075]
在氮气气氛下将207mg化合物d(1.0mmol)用1.0ml无水乙醇溶解,备用。向反应瓶中加入二(邻甲氧基苯基)二硒醚
ⅰ‑
7 223mg(0.6mmol)和1.0ml无水乙醇,室温下开搅拌,再称取硼氢化钠76mg(2mmol)加入反应瓶中,并于60℃条件下反应0.5h,用注射器将已配好的
化合物d的无水乙醇溶液加入反应中,60℃条件下继续反应3.0h,反应结束后,过滤,滤饼用2.0ml二氯甲烷洗涤,合并滤液,归一法gc
‑
ms检测收率89%,滤液用旋转蒸发仪除去有机溶剂后,残余物通过柱层析进一步分离提纯,洗脱剂为乙酸乙酯:石油醚=3:1,收集含目标产物的洗脱液,蒸去洗脱液,得到化合物ii
‑
7 286mg,分离产率80%,gc
‑
ms检测纯度98.0%。
[0076]1h nmr(500mhz,cdcl3)δ7.46(dd,j=7.5,1.7hz,1h),7.31(ddd,j=8.3,7.3,1.7hz,1h),7.28
‑
7.19(m,5h),7.16(s,1h),6.93
‑
6.85(m,3h),6.58(s,1h),4.65(dd,j=9.7,4.9hz,1h),4.46(dd,j=14.2,9.7hz,1h),4.36(dd,j=14.2,5.0hz,1h),3.89(d,j=0.8hz,3h);
13
c nmr(126mhz,cdcl3)δ159.01,138.57,137.12,135.45,130.03,129.00,128.83,127.96,127.75,121.50,118.89,117.70,111.03,55.90,52.39,45.66;gc
‑
ms(ei):m/z 358.1[m
+
].
[0077]
实施例8:含硒的咪唑化合物ii
‑
8的制备
[0078][0079]
在氮气气氛下将207mg化合物d(1.0mmol)用1.0ml无水乙醇溶解,备用。向反应瓶中加入二(对甲氧基苯基)二硒醚
ⅰ‑
8 223mg(0.6mmol)和1.0ml无水乙醇,室温下开搅拌,再称取硼氢化钠76mg(2mmol)加入反应瓶中,并于60℃条件下反应0.5h,用注射器将已配好的化合物d的无水乙醇溶液加入反应中,60℃条件下继续反应3.0h,反应结束后,过滤,滤饼用2.0ml二氯甲烷洗涤,合并滤液,归一法gc
‑
ms检测收率90%,滤液用旋转蒸发仪除去有机溶剂后,残余物通过柱层析进一步分离提纯,洗脱剂为乙酸乙酯:石油醚=3:1,收集含目标产物的洗脱液,蒸去洗脱液,得到化合物ii
‑
8 297mg,分离产率83%,gc
‑
ms检测纯度98.5%。化合物式ii
‑
8的结构表征如下:
[0080]1h nmr(500mhz,cdcl3)δ7.45
‑
7.37(m,2h),7.28
‑
7.21(m,3h),7.17(s,1h),7.13
‑
7.09(m,2h),6.88(s,1h),6.85
‑
6.78(m,2h),6.60(d,j=1.3hz,1h),4.45(dd,j=14.0,9.5hz,1h),4.41
‑
4.28(m,2h),3.80(s,3h);
13
c nmr(126mhz,cdcl3)δ160.28,138.76,137.71,137.14,129.08,128.81,127.90,127.63,118.85,118.45,114.95,55.29,51.96,48.24;gc
‑
ms(ei):m/z 358.1[m
+
].
[0081]
实施例9:含硒的咪唑化合物ii
‑
9的制备
[0082][0083][0084]
在氮气气氛下将207mg化合物d(1.0mmol)用1.0ml无水乙醇溶解,备用。向反应瓶中加入二(邻氨基苯基)二硒醚
ⅰ‑
9 205mg(0.6mmol)和1.0ml无水乙醇,室温下开搅拌,再称
取硼氢化钠76mg(2mmol)加入反应瓶中,并于60℃条件下反应0.5h,用注射器将已配好的化合物d的无水乙醇溶液加入反应中,60℃条件下继续反应3.0h,反应结束后,过滤,滤饼用2.0ml二氯甲烷洗涤,合并滤液,归一法gc
‑
ms检测收率91%,滤液用旋转蒸发仪除去有机溶剂后,残余物通过柱层析进一步分离提纯,洗脱剂为乙酸乙酯:石油醚=3:1,收集含目标产物的洗脱液,蒸去洗脱液,得到化合物ii
‑
9 281mg,分离产率82%,gc
‑
ms检测纯度97.8%。化合物式ii
‑
9的结构表征如下:
[0085]1h nmr(500mhz,cdcl3)δ7.40(dd,j=7.6,1.6hz,1h),7.29
‑
7.24(m,3h),7.21
‑
7.12(m,4h),6.87(s,1h),6.76(dd,j=8.0,1.3hz,1h),6.68
‑
6.56(m,2h),4.48(dd,j=13.3,9.3hz,1h),4.42
‑
4.38(m,1h),4.34(dd,j=13.2,4.9hz,1h);
13
c nmr(126mhz,cdcl3)δ149.08,138.78,138.57,137.18,131.21,129.01,128.89,128.01,127.49,118.91,118.72,114.92,112.81,52.01,46.53;gc
‑
ms(ei):m/z 343.1[m
+
].
[0086]
实施例10:含硒的咪唑化合物ii
‑
10的制备
[0087][0088]
在氮气气氛下将207mg化合物d(1.0mmol)用1.0ml无水乙醇溶解,备用。向反应瓶中加入204mg(0.6mmol)二(邻甲基苯基)二硒醚
ⅰ‑
10和1.0ml无水乙醇,室温下开搅拌,再称取硼氢化钠76mg(2mmol)加入反应瓶中,并于60℃条件下反应0.5h,用注射器将已配好的化合物d的无水乙醇溶液加入反应中,60℃条件下继续反应3.0h,反应结束后,过滤,滤饼用2.0ml二氯甲烷洗涤,合并滤液,归一法gc
‑
ms检测收率85%,滤液用旋转蒸发仪除去有机溶剂后,残余物通过柱层析进一步分离提纯,洗脱剂为乙酸乙酯:石油醚=3:1,收集含目标产物的洗脱液,蒸去洗脱液,得到化合物ii
‑
10 266mg,分离产率78%,gc
‑
ms检测纯度96.7%。化合物式ii
‑
10的结构表征如下:
[0089]1h nmr(500mhz,cdcl3)δ7.56
‑
7.50(m,1h),7.43
‑
7.33(m,1h),7.29
‑
7.26(m,2h),7.25
‑
7.23(m,2h),7.18
‑
7.09(m,4h),6.88(s,1h),6.58(d,j=1.3hz,1h),4.48(dd,j=12.9,8.9hz,1h),4.37(ddd,j=17.7,13.3,4.7hz,2h),2.39(s,3h);
13
c nmr(126mhz,cdcl3)δ141.52,138.55,137.10,135.57,130.41,129.71,129.12,128.90,128.06,127.64,126.76,126.18,118.82,52.16,47.38,22.90;gc
‑
ms(ei):m/z 342.1[m
+
].
[0090]
实施例11:含硒的咪唑化合物的抑菌实验
[0091]
采用牛津杯法抑菌试验,检测上述合成化合物
ⅱ‑
1—
ⅱ‑
10、ampicillin、clotrimazole对金黄色葡萄球菌、大肠杆菌、芽孢杆菌和酵母菌的抗菌作用。以化合物
ⅱ‑
1为例,具体操作方法如下:(1)lb培养基的配制:准确称取胰蛋白胨0.5g、酵母提取物0.25g、nacl 0.5g并加入到50ml的去离子水内,不断搅拌至溶质完全溶解。用1mol/l的naoh溶液调节ph值至7.0
‑
7.2;ypd培养基的配制:准确称取酵母膏0.5g、蛋白胨1g,加入到45ml的去离子水内,不断搅拌至溶质完全溶解。将上述lb液体培养基和ypd液体培养基使用灭菌锅1kg压力下灭菌15min。灭菌完后将1g葡萄糖溶解到5ml去离子水内,将葡萄糖溶液加入到ypd培
养基中。(lb和ypd固体培养基需要各再称取0.75g琼脂粉)(2)菌悬液的制备:将待测的金黄色葡萄球菌、大肠杆菌、芽孢杆菌和酵母菌菌株由斜面培养基分别挑取一环接种到液体lb培养基和液体pyd培养基中(实施例11,(1)配制)中,在37℃、120r/min环境下活化12
‑
16h,分别从中吸取0.5ml活化后的培养液,并向该0.5ml的培养液内分别加入无菌水倍比稀释到105‑
106ml
‑1,备用。(3)平板培养皿的制备:将上述(实施例11,(1))灭菌后的lb液体培养基和ypd液体培养基冷却至60℃左右,缓慢倒入培养皿内,每盘约倒入培养基15ml,水平放置直至完全凝固。取0.1ml实施例11(2)中所制备的菌悬液分别均匀涂布在不同平板表面至表面无可见水滴。用镊子将灭菌后的牛津杯垂直放入培养皿内,每个培养皿内等距离放置牛津杯五个,轻轻按压牛津杯,使其与培养基接触无空隙。(4)样品的配制:取0.5mg、5mg、10mg、20mg的化合物
ⅱ‑
1并分别溶于1ml的dmso中,之后分别向其中加入lb液体培养基9ml,配制化合物
ⅱ‑
1的浓度为0.05mg/ml、0.5mg/ml、1mg/ml、2mg/ml。同时使用相同的方法制备不加样品的含有10%dmso的lb液体培养基作为空白对照即
ⅱ‑
1的浓度为0mg/ml。(酵母菌的样品只需将lb液体培养基换成ypd培养基)(5)检测:用移液枪准确量取不同浓度(0.05mg/ml、0.5mg/ml、1mg/ml、2mg/ml)的化合物
ⅱ‑
1的溶液于含不同菌的平板培养皿中的牛津杯中(实施例11(3)中制备),置37℃恒温培养箱中培养12h后,用毫米尺测量抑菌圈直径并记录实验结果。通过牛津杯抑菌圈的直径大小对化合物
ⅱ‑
1抑菌活性强弱进行评估,其中根据实验结果,一般认为,抑菌圈直径若小于6mm,说明该物质不具有抗菌性(记作
“‑”
);在6
‑
10mm之间,说明该物质具有抗菌性(记作“+”);11
‑
15mm为中度敏感(记作“++”);直径达到16mm以上则为高度敏感(记作“+++”)。
[0092]
将上述步骤(1)
‑
(5)中的化合物
ⅱ‑
1分别换为化合物
ⅱ‑
2、
ⅱ‑
3、
ⅱ‑
4、
ⅱ‑
5、
ⅱ‑
6、
ⅱ‑
7、
ⅱ‑
8、
ⅱ‑
9、
ⅱ‑
10、ampicillin、clotrimazole,其余不变,即可测定化合物
ⅱ‑
2至化合物
ⅱ‑
10、ampicillin和clotrimazole的抑菌作用。
[0093]
注:金黄色葡萄球菌、芽孢杆菌、大肠杆菌利用lb培养基;酵母菌利用ypd培养基。
[0094]
抑菌实验结果如下:
[0095][0096]
[0097]
a=0.05mg/ml,b=0.5mg/ml,c=1mg/ml,d=2mg/ml,bg=0mg/ml
[0098]
由上表可知,当给药浓度为0.05mg/ml时,化合物
ⅱ‑
9对黄色葡萄球菌具有抗菌性;化合物
ⅱ‑
1到
ⅱ‑
10对芽孢杆菌没有抗菌性;化合物
ⅱ‑
1、
ⅱ‑
3、
ⅱ‑
6对大肠杆菌具有抗菌性;化合物
ⅱ‑
1到
ⅱ‑
10对酵母菌都具有抗菌性,其中化合物
ⅱ‑
5到
ⅱ‑
10对酵母菌都具有高度敏感抗菌性。
[0099]
当给药浓度为0.5mg/ml时,化合物
ⅱ‑
2、
ⅱ‑
3、
ⅱ‑
4、
ⅱ‑
5、
ⅱ‑
6、
ⅱ‑
8、
ⅱ‑
9、
ⅱ‑
10对黄色葡萄球菌具有抗菌性,其中化合物
ⅱ‑
4、
ⅱ‑
6、
ⅱ‑
8、
ⅱ‑
9、
ⅱ‑
10具有高度敏感抗菌性,优于氨苄西林;化合物
ⅱ‑
2、
ⅱ‑
3、
ⅱ‑
4、
ⅱ‑
5、
ⅱ‑
6、
ⅱ‑
7、
ⅱ‑
8、
ⅱ‑
9、
ⅱ‑
10对芽孢杆菌具有抗菌性,其中化合物
ⅱ‑
6具有高度敏感抗菌性,优于氨苄西林;化合物
ⅱ‑
1到
ⅱ‑
10对大肠杆菌都具有抗菌性,其中化合物
ⅱ‑
2、
ⅱ‑
3、
ⅱ‑
4、
ⅱ‑
5、
ⅱ‑
6、
ⅱ‑
8、
ⅱ‑
9具有高度敏感抗菌性;化合物
ⅱ‑
1到
ⅱ‑
10对酵母菌都具有抗菌性,其中化合物
ⅱ‑
5到
ⅱ‑
10对酵母菌都具有高度敏感抗菌性。
[0100]
当给药浓度为1mg/ml时,化合物
ⅱ‑
1到
ⅱ‑
10对黄色葡萄球菌都具有抗菌性,其中化合物
ⅱ‑
2、
ⅱ‑
3、
ⅱ‑
4、
ⅱ‑
5、
ⅱ‑
6、
ⅱ‑
8、
ⅱ‑
9、
ⅱ‑
10具有高度敏感抗菌性;化合物
ⅱ‑
1到
ⅱ‑
10对芽孢杆菌都具有抗菌性,其中化合物
ⅱ‑
4、
ⅱ‑
5、
ⅱ‑
6具有高度敏感抗菌性;化合物
ⅱ‑
1到
ⅱ‑
10对大肠杆菌都具有抗菌性,其中化合物
ⅱ‑
2、
ⅱ‑
3、
ⅱ‑
4、
ⅱ‑
5、
ⅱ‑
6、
ⅱ‑
8、
ⅱ‑
9、
ⅱ‑
10具有高度敏感抗菌性;化合物
ⅱ‑
1到
ⅱ‑
10对酵母菌都具有高度敏感抗菌性。
[0101]
当给药浓度为2mg/ml时,化合物
ⅱ‑
1到
ⅱ‑
10对黄色葡萄球菌都具有抗菌性,其中化合物
ⅱ‑
2到
ⅱ‑
10具有高度敏感抗菌性;化合物
ⅱ‑
1到
ⅱ‑
10对芽孢杆菌都具有抗菌性,其中化合物
ⅱ‑
1到
ⅱ‑
7、
ⅱ‑
9、
ⅱ‑
10具有高度敏感抗菌性;化合物
ⅱ‑
1到
ⅱ‑
10对大肠杆菌和酵母菌都具有高度敏感抗菌性。
[0102]
实施例12:含硒的咪唑化合物的抑酵母菌实验
[0103]
采用牛津杯法抑菌试验,检测上述合成化合物
ⅱ‑
1—
ⅱ‑
10、clotrimazole对酵母菌的抗菌作用。以化合物
ⅱ‑
1为例,具体操作方法如下:(1)ypd培养基的配制:准确称取酵母膏0.5g、蛋白胨1g,加入到45ml的去离子水内,不断搅拌至溶质完全溶解。将上述ypd液体培养基使用灭菌锅1kg压力下灭菌15min。灭菌完后将1g葡萄糖溶解到5ml去离子水内,将葡萄糖溶液加入到ypd培养基中。(ypd固体培养基需要再称取0.75g琼脂粉)(2)菌悬液的制备:将待测的酵母菌菌株由斜面培养基分别挑取一环接种到液体pyd培养基中(实施例12,(1)配制)中,在37℃、120r/min环境下活化12
‑
16h,分别从中吸取0.5ml活化后的培养液,并向该0.5ml的培养液内分别加入无菌水倍比稀释到105‑
106ml
‑1,备用。(3)平板培养皿的制备:将上述(实施例12,(1))灭菌后的ypd液体培养基冷却至60℃左右,缓慢倒入培养皿内,每盘约倒入培养基15ml,水平放置直至完全凝固。取0.1ml实施例12(2)中所制备的菌悬液分别均匀涂布在不同平板表面至表面无可见水滴。用镊子将灭菌后的牛津杯垂直放入培养皿内,每个培养皿内等距离放置牛津杯五个,轻轻按压牛津杯,使其与培养基接触无空隙。(4)样品的配制:取0.05mg、0.1mg、0.25mg的化合物
ⅱ‑
1并分别溶于1ml的dmso中,之后分别向其中加入ypd液体培养基9ml,配制化合物
ⅱ‑
1的浓度为5ug/ml、10ug/ml、25ug/ml。同时使用相同的方法制备不加样品的含有10%dmso的ypd液体培养基作为空白对照即
ⅱ‑
1的浓度为0mg/ml。(5)检测:用移液枪准确量取不同浓度(5ug/ml、10ug/ml、25ug/ml)的化合物
ⅱ‑
1的溶液于含酵母菌的平板培养皿中的牛津杯中(实施例12(3)中制备),置37℃恒温培
养箱中培养12h后,用毫米尺测量抑菌圈直径并记录实验结果。通过牛津杯抑菌圈的直径大小对化合物
ⅱ‑
1抑菌活性强弱进行评估,其中根据实验结果,一般认为,抑菌圈直径若小于6mm,说明该物质不具有抗菌性(记作
“‑”
);在6
‑
10mm之间,说明该物质具有抗菌性(记作“+”);11
‑
15mm为中度敏感(记作“++”);直径达到16mm以上则为高度敏感(记作“+++”)。
[0104]
将上述步骤(1)
‑
(5)中的化合物
ⅱ‑
1分别换为化合物
ⅱ‑
2、
ⅱ‑
3、
ⅱ‑
4、
ⅱ‑
5、
ⅱ‑
6、
ⅱ‑
7、
ⅱ‑
8、
ⅱ‑
9、
ⅱ‑
10、clotrimazole,其余不变,即可测定化合物
ⅱ‑
2至化合物
ⅱ‑
10和clotrimazole的抑菌作用。
[0105]
注:酵母菌利用ypd培养基。
[0106]
抑菌实验结果如下:
[0107][0108]
a=5ug/ml,b=10ug/ml,c=25ug/ml,bg=0ug/ml
[0109]
由上表可知,当给药浓度为5ug/ml时,化合物
ⅱ‑
1到化合物
ⅱ‑
4、化合物
ⅱ‑
6、化合物
ⅱ‑
8对酵母菌没有抗菌性;化合物
ⅱ‑
5、
ⅱ‑
7、
ⅱ‑
9和
ⅱ‑
10对酵母菌有抗菌性,其中化合物
ⅱ‑
7、
ⅱ‑
9对酵母菌中度敏感,优于克霉唑。
[0110]
当给药浓度为10ug/ml时,化合物
ⅱ‑
1到化合物
ⅱ‑
4对酵母菌没有抗菌性;化合物
ⅱ‑
5、
ⅱ‑
6、
ⅱ‑
7、
ⅱ‑
8、
ⅱ‑
10对酵母菌有抗菌性,其中化合物
ⅱ‑
5、
ⅱ‑
7、
ⅱ‑
10对酵母菌中度敏感;化合物
ⅱ‑
9对酵母菌具有感度敏感抗菌性,优于克霉唑。
[0111]
当给药浓度为25ug/ml时,化合物
ⅱ‑
2和
ⅱ‑
4对酵母菌没有抗菌性;化合物
ⅱ‑
1、
ⅱ‑
3、
ⅱ‑
8对酵母菌具有抗菌性;化合物
ⅱ‑
5、
ⅱ‑
6、
ⅱ‑
10对酵母菌具有中度敏感抗菌性;化合物
ⅱ‑
7、
ⅱ‑
9对酵母菌均为高度敏感抗菌性。
[0112]
化合物
ⅱ‑
5、
ⅱ‑
10、
ⅱ‑
7、
ⅱ‑
9对酵母菌有较良好的抑制作用。其抗菌活性大小为化合物
ⅱ‑
9>化合物
ⅱ‑
7>化合物
ⅱ‑
5、
ⅱ‑
10。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1