一种连续性检测铁离子和L-Cys的荧光探针及其制备方法和应用
一种连续性检测铁离子和l-cys的荧光探针及其制备方法和应用
技术领域
1.本发明属于荧光检测领域,涉及连续性检测fe
3+
和l-cys的荧光探针及其在纸基检测上的应用,特别是指一种定量检测fe
3+
和l-cys的荧光探针及其制备方法和应用。
背景技术:
2.生物硫醇主要是指l-半胱氨酸(l-cys)、高半胱氨酸(hcy)和谷胱甘肽(gsh),在生物系统中起着至关重要的作用,如清除自由基、维持氧化还原稳态的平衡以及调节解毒和代谢。尽管这三种生物硫醇具有相似的结构和反应性,但它们在不同的生理活动中发挥的作用不同。l-cys对于机体解毒和保护细胞免受自由基和活性氧的侵害具有极其重要的作用,同时阿尔茨海默病和帕金森病与人体液中l-cys的异常表达密切相关。因此,l-cys常被用做功能性食品的主要成分,用于补充l-cys和改善人体健康。由于l-cys在医学、毒理学、某些代谢紊乱的诊断和食品营养价值测定中的实际意义,因此检测和确定各种产品中l-cys的含量具有重要的意义。
3.目前,检测l-cys的分析技术有多种,如高效液相色谱(hplc)、伏安法、毛细管区带电泳(cze)、激光解吸/电离质谱(ldi-ms)和液相色谱-质谱(lc-ms)。但这些方法大多存在操作复杂、耗时等限制。而荧光光谱法具有灵敏度高、特异性好、响应时间快等优点,荧光光谱法检测l-cys具有一定的应用前景。因此,研究人员在开发用于检测这些生物硫醇的荧光探针方面做出了相当大的努力。已经报道的方法主要基于迈克尔加成,硫醇与醛的环化,二硫醚和磺酰胺被硫醇裂解,以及金属配合物的脱金属。尽管在生物硫醇荧光检测方面的研究取得了很大进展,但许多已报道的探针仍存在合成过程繁琐、选择性低和响应时间长的问题。因此,非常需要开发一种简单、高选择性和快速响应的荧光探针,用于检测l-cys。
技术实现要素:
4.本发明提供一种合成路线简单、反应条件温和、成本较低的荧光探针;灵敏度高、选择性好,抗干扰能力强,能够在复杂体系中准确识别fe
3+
和l-cys,结构如下:
[0005][0006]
其合成路线是:
[0007][0008]
具体合成方法:将1-芘甲醛与盐酸羟胺在乙醇中均匀混合,反应60-90分钟。反应后将溶剂旋干得到固体粗产品,经柱层分析法得到探针pyr-1。其中,1-芘甲醛与盐酸的物质的量比为1:4,所述的溶剂为乙醇,柱层析法采用的硅胶200-300目,淋洗剂为:v
二氯甲烷
/v
石油醚
=6/1。
[0009]
本发明提供的的荧光探针可用于定性、定量检测fe
3+
。
[0010]
进一步地,检测fe
3+
的步骤为:将荧光探针pyr-1溶解于dmso溶剂中,配置成1
×
10-3
mol/l的探针溶液,然后取探针溶液加入待测物质中,反应后进行荧光检测。
[0011]
进一步地,采用纸基检测fe
3+
,具体步骤为:将实验用滤纸剪成滤纸纸条,浸泡在浓度为1.0
×
10-3
mol/l的pyr-1溶液中,等待干燥后滴加待测溶液,根据荧光强度的变化得到待测溶液中fe
3+
的浓度。
[0012]
本发明提供的的荧光探针可用于定性、定量的检测l-cys。
[0013]
进一步地,检测l-cys的步骤为:将荧光探针pyr-1溶解于dmso溶剂中,配置成1
×
10-3
mol/l的探针溶液,然后加入50倍于探针物质的量的fe
3+
,反应后加入待测物质,进行荧光检测。
[0014]
进一步地,采用纸基检测l-cys,具体步骤为:将实验用滤纸剪成滤纸纸条,浸泡在浓度为1.0
×
10-3
mol/l的pyr-1溶液中,等待干燥后滴加5.0
×
10-2
mol/l的fe
3+
溶液,猝灭完全后滴加待测溶液,根据荧光强度的变化得到待测溶液中l-cys的浓度。
[0015]
本发明的荧光探针作用机制如下,在探针分子中,肟基和酚羟基为fe
3+
提供了一个选择性螯合剂“口袋”,从而在溶液(1%dmso)中产生强烈的荧光猝灭(检测限:7.44
×
10-7
mol/l)。同时形成1:1化学计量比的pyr-1-fe
3+
复合物。复合物加入l-cys后,由于l-cys与fe
3+
之间的结合力大于pyr-1与fe
3+
之间的结合力,使得l-cys将fe
3+
从原先形成的pyr-1-fe
3+
复合物中置换下来,随后荧光显着增强。l-cys对于fe
3+
的置换方法引起探针本身被释放,因此检测系统显示出对l-cys的高选择性、快速响应(~50s)和低检测限(4.66
×
10-7
mol/l)。
[0016]
本发明的有益效果如下:本发明提供的荧光探针具有合成路线简单、高选择性、响应快速、低检测限、受环境干扰小的特点。
附图说明
[0017]
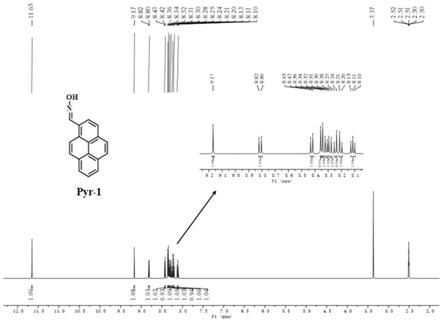
图1为本发明中探针pyr-1在氘代dmso中氢谱,横坐标为化学位移(ppm),纵坐标为强度。
[0018]
图2本发明中探针pyr-1在氘代dmso中碳谱,横坐标为化学位移(ppm),纵坐标为强度。
[0019]
图3发明中探针pyr-1的质谱,电离源为:esi
+
。
[0020]
图4本发明中探针pyr-1在1%dmso中的紫外吸收光谱。
[0021]
图5本发明探针pyr-1(1
×
10-5
mol/l),在1%dmso溶液中,室温分别与对照,na
+
,k
+
,ca
2+
,mg
2+
,al
3+
,cu
2+
,fe
3+
,ag
+
,mn
2+
,zn
2+
,ni
+
,pb
2+
,cd
2+
,cr
2+
,ba
2+
,hg
2+
以及fe
2+
反应记录的荧光光谱。激发波长为:325nm。
[0022]
图6为本发明探针pyr-1与不同浓度fe
3+
反应后的荧光强度与线性关系。
[0023]
图7为本发明探针pyr-1-fe
3+
(1
×
10-5
mol/l),在1%dmso溶液中,室温分别与对照,asp,hcy,his,met,sar,thr,gly,l-cys,gsh,val,pro,phe,arg,ala,ser,trp,tyr,glu,gln,ieu反应记录的荧光光谱。激发波长为:325nm。
[0024]
图8为本发明中pyr-1-fe
3+
与不同浓度l-cys反应的荧光强度与线性关系。
[0025]
图9为本发明中pyr-1-fe
3+
的质谱图,电离源为:esi
+
。
[0026]
图10为本发明中pyr-1-fe
3+
与l-cys反应后的质谱图,电离源为:esi
+
。
[0027]
图11为实施例中pyr-1-fe
3+
复合物检测l-cys在纸基上的应用效果图。
[0028]
图12为本发明的探针的机理。
具体实施方式
[0029]
下面结合实例和附图对本发明作进一步说明,但本发明不受下述实施例的限制。
[0030]
实施例1pyr-1荧光探针的合成
[0031]
在50ml圆底烧瓶中,加入1-芘甲醛(0.45g,2.17
×
10-3
mol),吡啶(1ml)和盐酸羟胺(0.60g,8.69
×
10-3
mol),然后倒入10ml乙醇。室温下搅拌90分钟,将反应液进行旋蒸后得到粗产物。粗产物用水和乙酸乙酯萃取3次后。收集上层有机层,然后用无水na2so4干燥。减压除溶剂后,以ch2cl2/石油醚(v/v,6:1)为洗脱剂,柱层析纯化,得到黄色探针pyr-1固体(0.36g,产率69%)。1h nmr(dmso-d6,500mhz):δ11.65(s,oh),δ9.17(s,nh),δ8.81(d,j=9.3hz,1h),δ8.42(d,j=8.1hz,1h),δ8.36(s,1h),δ8.34(s,1h),δ8.31(d,j=8.1hz,1h),δ8.29(d,j=9.3hz,1h),δ8.24(d,j=8.9hz,1h),δ8.20(d,j=8.9hz,1h),δ8.11(t,j=7.6hz,1h).
13
c nmr(dmso-d6,125mhz):δ147.91,131.85,131.35,130.71,128.79,128.49,128.44,127.83,126.67,126.67,126.29,125.98,125.57,125.47,124.62,124.29,123.81.[m+h]
+
:246.09157.
[0032]
实施例2pyr-1荧光探针对不同金属离子的选择性
[0033]
将实施例1中pyr-1荧光探针配置成1
×
10-3
mol/l的母液。
[0034]
将下列物质nacl,kcl,cacl2,mgcl2·
6h2o,alcl3,cucl2·
2h2o,fecl3·
6h2o,agno3,mncl2·
4h2o,zncl2,nicl
·
6h2o,pbcl2,cdcl2·
2.5h2o,crcl3·
6h2o,bacl2·
2h2o,fecl2·
4h2o,hgcl2配置成1
×
10-2
mol/l的母液。
[0035]
取18支试管,分别依次加入150μl上述不同的金属离子母液,对照以等量水代替干扰物质,然后加入2820μl的超纯水,最后分别加入30μl的探针母液。各溶液摇匀后进行荧光检测(ex=325nm)。以荧光强度为纵坐标,波长为横坐标作图5;由图5可以发现fe
3+
能够明显猝灭pyr-1的荧光强度,其它金属离子对其荧光强度几乎没有干扰。
[0036]
实施例3不同浓度fe
3+
下pyr-1的荧光强度
[0037]
配置浓度为1
×
10-3
mol/l的fe
3+
母液,通过改变加入试管中体积的不同来控制最
后fe
3+
的浓度,形成0-50当量fe
3+
的含量。反应后进行荧光检测(ex=325nm),检测各体系中的荧光强度。以荧光强度为纵坐标,fe
3+
的浓度为横坐标作曲线,并绘制线性关系,得到图6。由图6可知,随着fe
3+
的浓度增加探针的荧光强度逐渐降低,当fe
3+
的含量达到50当量时,探针的荧光不再降低。
[0038]
实施例4pyr-1-fe
3+
复合物对不同氨基酸的选择性
[0039]
将下列物质asp,hcy,his,met,sar,thr,gly,l-cys,gsh,val,pro,phe,arg,ala,ser,trp,tyr,glu,gln,ieu配置成1
×
10-3
mol/l的母液。
[0040]
取21支试管,分别依次加入150μ实例2中的不同金属离子母液,对照以等量水代替干扰物质,加入2790μl的超纯水,然后分别加入30μl的探针母液,反应后加入30μl的氨基酸母液。各溶液摇匀后进行荧光检测(ex=325nm)。以荧光强度为纵坐标,波长为横坐标作图7。从图7中可以看出,只有l-cys能够与pyr-1-fe
3+
复合物发生置换反应,使得探针的荧光得以恢复。
[0041]
实施例5不同浓度l-cys下pyr-1-fe
3+
复合物的荧光强度
[0042]
配置浓度为1
×
10-4
mol/l的l-cys母液。与实例3类似,通过改变加入试管中体积的不同来控制最后l-cys的浓度,形成0-1当量l-cys的含量。在试管中加入30μl的探针母液然后加入50当量的fe
3+
,使探针荧光被猝灭完全。然后加入不同体积的l-cys母液,反应后进行荧光检测(ex=325nm),检测各体系中的荧光强度。以荧光强度为纵坐标,l-cys的浓度为横坐标作曲线,并绘制线性关系。由图8可知,随着l-cys的浓度增加探针的荧光强度逐渐增加,当l-cys的含量达到1当量时,探针的荧光达到饱和。
[0043]
实施例6pyr-1荧光探针对不同水样中fe
3+
检测
[0044]
选取6种水样进行加标回收率实验(包括西湖水、食品厂废水、化工厂废水、污水处理厂废水、雨水和自来水),用这些水样配置6种fe
3+
浓度为1
×
10-3
mol/l的溶液。
[0045]
在6支试管中加入pyr-1母液30μl,分别用6种水样2970μl稀释至3ml,在ex=325nm下进行荧光检测。计算回收率以及rsd。以水样为纵坐标,fe
3+
浓度、回收率、rsd为横坐标绘制表1。回收率均在99.5%-100.5%之间,rsd均小于1。
[0046]
表1实际水样中fe
3+
回收率数据
[0047][0048]
实施例7pyr-1-fe
3+
复合物对不同功能性样品中l-cys检测
[0049]
实际样品选取了市场上具有代表性的6种功能性食品。用超纯水稀释所有功能性
食品样品(c=4
×
10-4
mol/l)。
[0050]
实际样品检测时,取30μl的pyr-1母液,加入2790μl的超纯水后加入50当量的fe
3+
,反应后,滴加30μl功能性食品样品,同样反应。各溶液摇匀后进行荧光检测(ex=325nm),计算回收率以及rsd。以实际样品为纵坐标,l-cys浓度、回收率、rsd为横坐标绘制表2。
[0051]
表2功能性食品样品中l-cys检测数据
[0052][0053]
实施例8pyr-1-fe
3+
复合物对不同稀释倍数人血清中的l-cys检测
[0054]
选取健康人的血清样本并进行稀释,分别稀释成体积分数为:1%、5%、15%的实际样本。每种稀释的人血清溶液都加入不同浓度的l-cys(0.5-8
×
10-6
mol/l),以获取真实样品溶液。进行荧光测试时,将30μl的pyr-1母液和50当量的fe
3+
溶液转移至试管中,反应后,然后利用实际样品稀释至3ml。自来水和矿泉水中l-cys的检测也是如此。计算回收率以及rsd。以实际样品为纵坐标,l-cys浓度、回收率、rsd为横坐标绘制表3。
[0055]
表3稀释人血清、水样中l-cys回收率数据
[0056][0057]
实施例9pyr-1-fe
3+
复合物检测l-cys在纸基上的应用
[0058]
将实验室用的滤纸剪成大小一致的9张条状滤纸条,将所有滤纸条浸泡在探针母液(c=1
×
10-4
mol/l)中,取出后在空气中干燥。干燥后在每张滤纸条上滴加50当量的fe
3+
溶液将探针的荧光猝灭完全,同样在空气中干燥。然后滴加不容浓度的l-cys溶液(0.01当量-1当量),对照滴加等量的水。反应后在手持紫外灯下观察荧光变化。在黑暗条件下,拍摄每张滤纸条的荧光变化,标明l-cys具体含量绘制图11。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1